Similar presentations:
Валентність хімічних елементів
1. Валентність
Хімія, 7 класУрок- презентація
Підготувала: вчитель хімії
Сосницької гімназії ім. О.П.
Довженка
Мотчана С. І.
2. Тема уроку
Валентність хімічнихелементів.
Складання формул бінарних
сполук за валентністю
3. Необхідні терміни:
РечовинаСкладна речовина
Проста речовина
Молекула
Атом
Хімічний елемент
Хімічна формула
4. Мета уроку
З'ясувати, що таке валентність елемента;Прогнозувати можливі значення
валентності елемента за його
положенням у Періодичній системі;
Вивчити алгоритм складання хімічних
формул бінарних сполук;
Навчитись складати хімічні формули
бінарних сполук.
5. Давайте поміркуємо
Чому в природі так малоокремих атомів, більшість
існує тільки у вигляді молекул?
6. Як Ви вважаєте
Атом може з'єднуватись звизначеною кількістю атомів,
чи кількість таких зв'язків
необмежена?
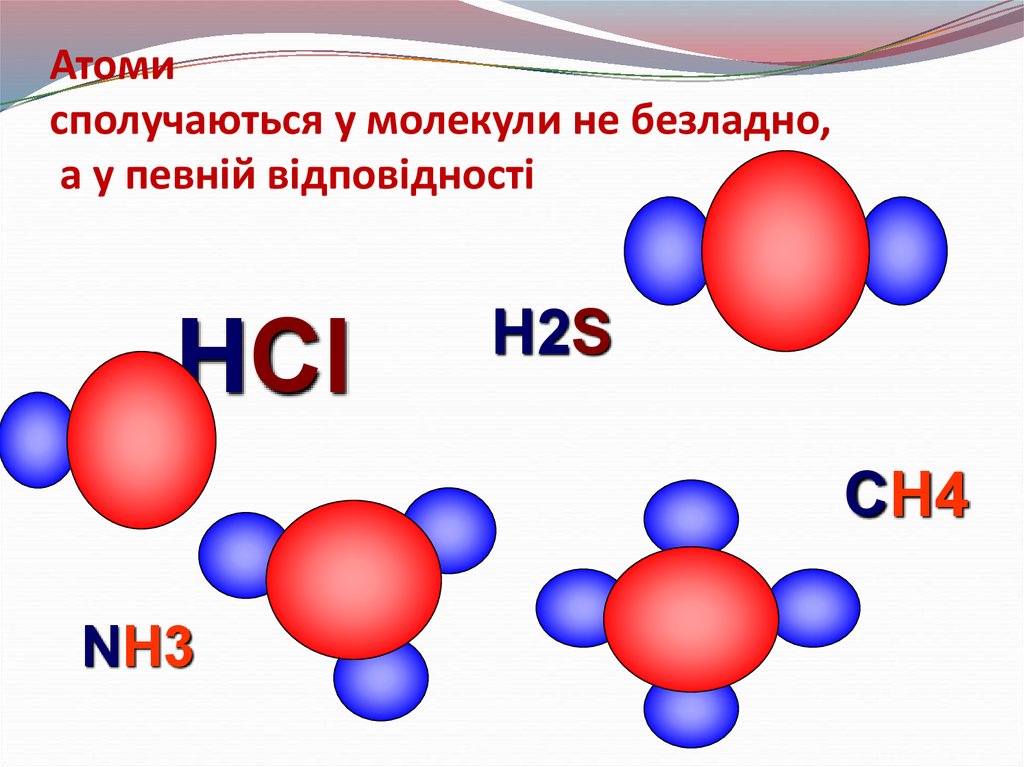
7. Атоми сполучаються у молекули не безладно, а у певній відповідності
HClH2S
CH4
NH3
8.
HСlH2O
Хлоридна
кислота
Вода
NH3
Амоніак
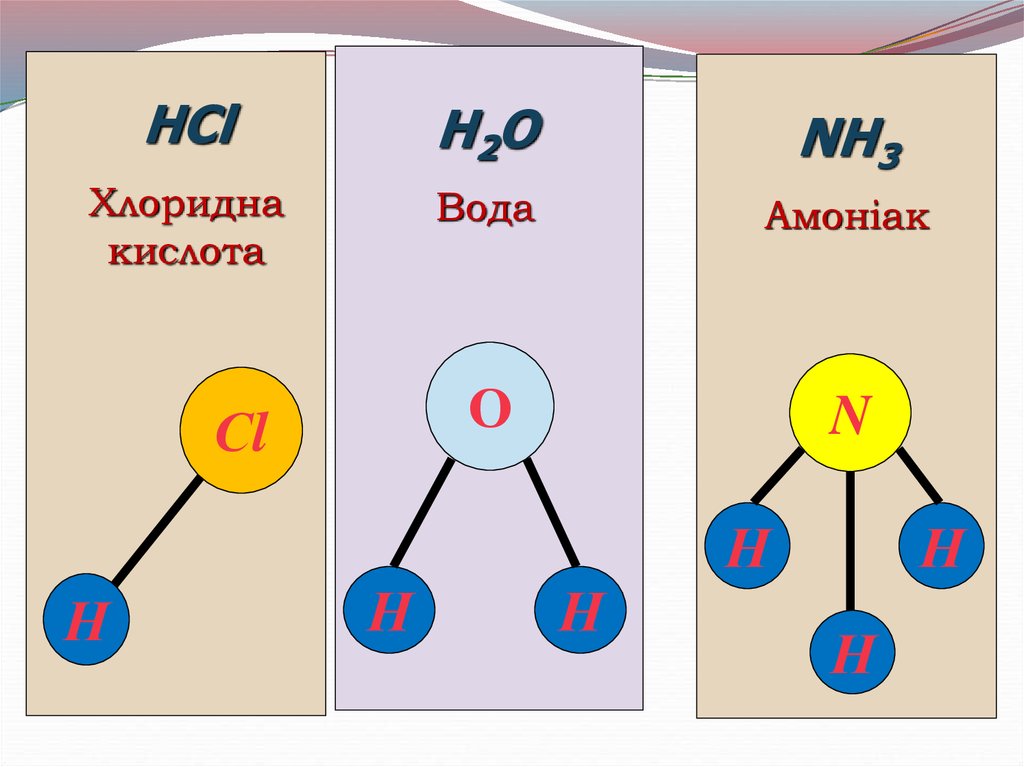
9.
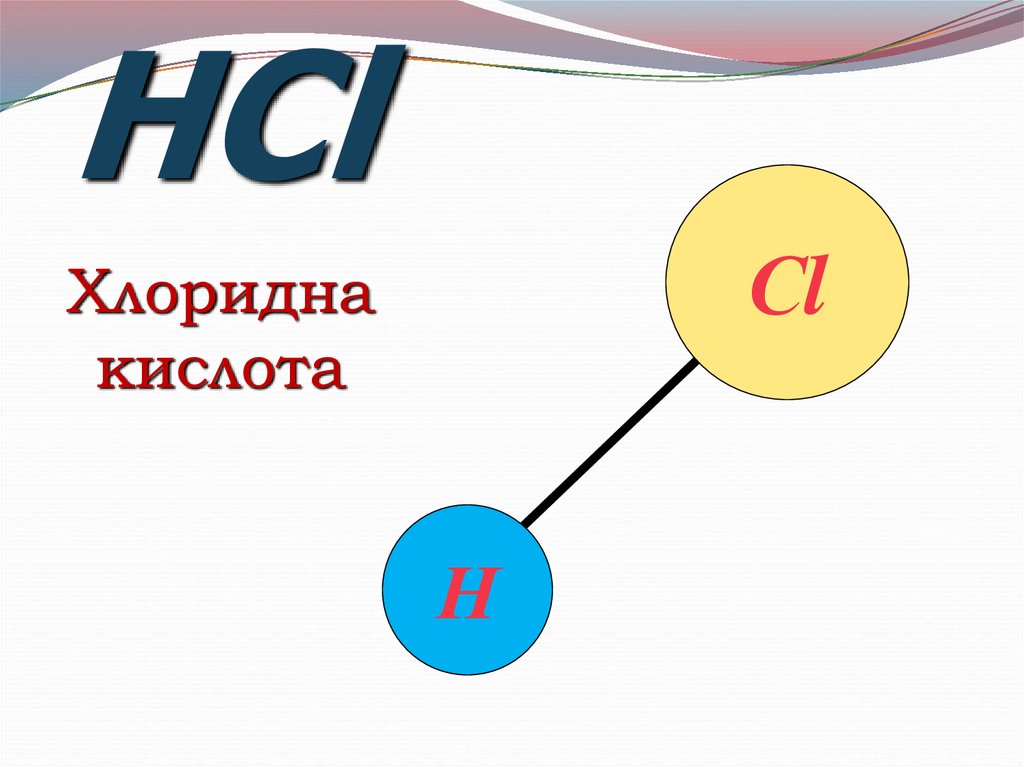
HСlСl
Хлоридна
кислота
Н
10.
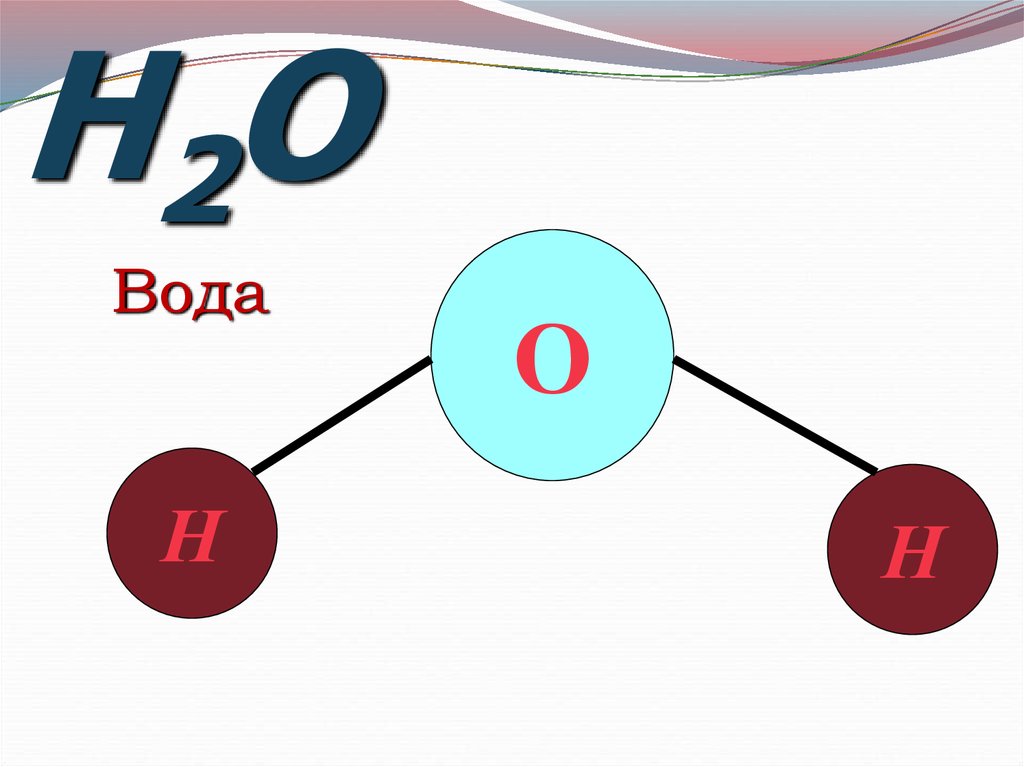
H2OВода
Н
О
Н
11.
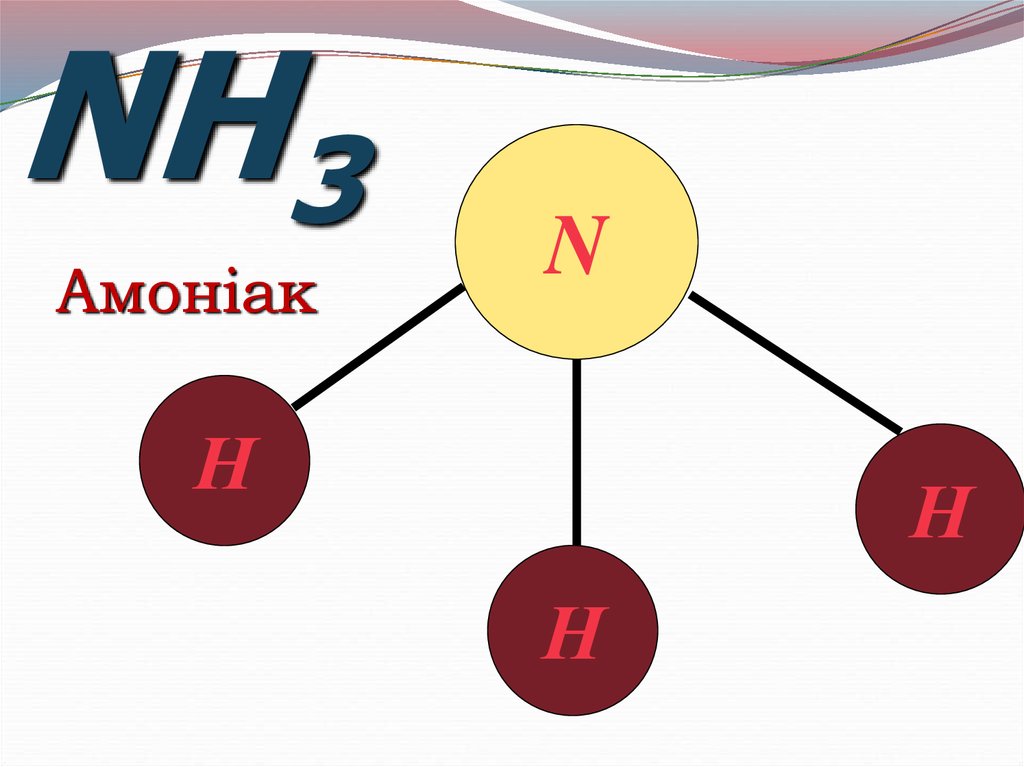
NH3Амоніак
N
Н
Н
Н
12.
HСlH2O
NH3
Хлоридна
кислота
Вода
Амоніак
О
N
Сl
Н
Н
Н
Н
Н
Н
13.
Здатність атомівутворювати певну
кількість зв'язків
називається
ВАЛЕНТНІСТЮ
14.
Атомирізних елементів
можуть
утворювати
певну
кількість зв'язків,
притаманну лише
їм
15.
Атомизі сталою валентністю
H2O
Na2O
CaO
Вода
Натрій
оксид
Кальцій
оксид
О
Н
О
О
Н
Na
Na
Са
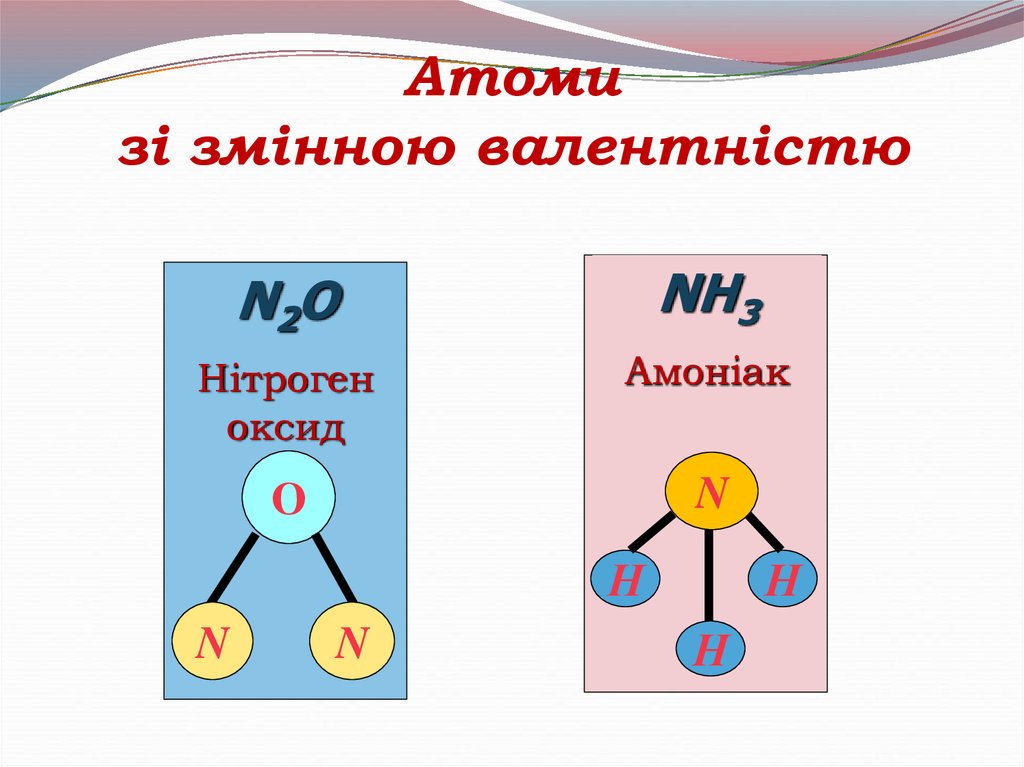
16.
Атомизі змінною валентністю
N2O
NH3
Нітроген
оксид
Амоніак
О
N
Н
N
N
Н
Н
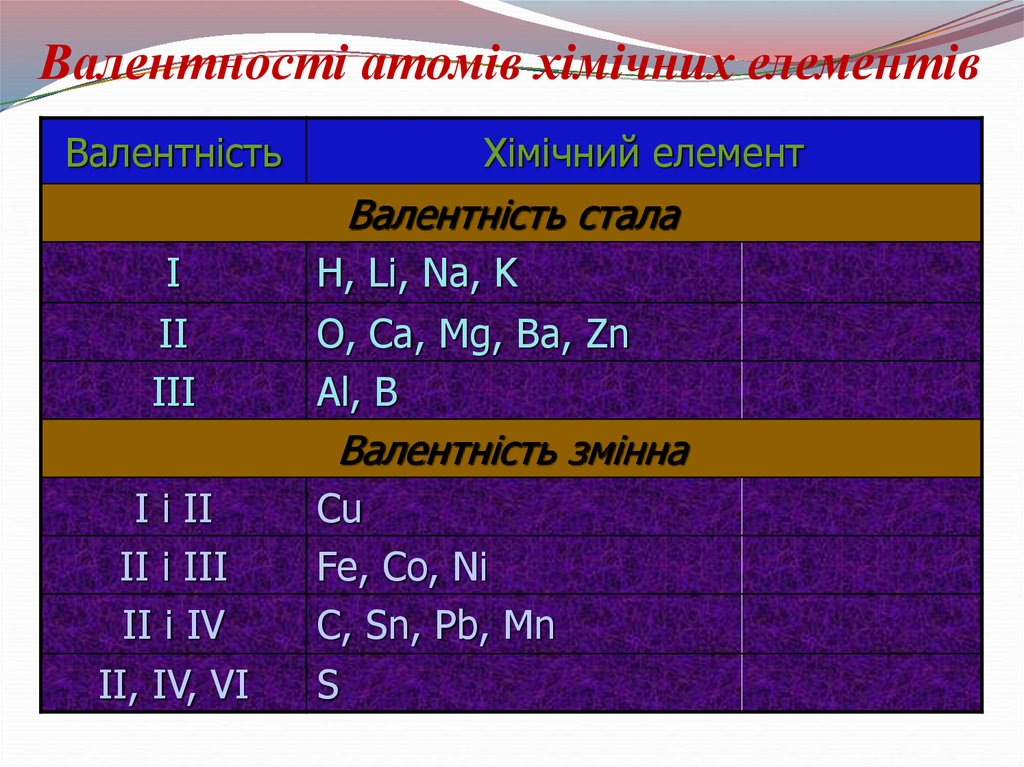
17.
Валентності атомів хімічних елементівВалентність
Хімічний елемент
Валентність стала
І
ІІ
ІІІ
H, Li, Na, K
O, Ca, Mg, Ba, Zn
Al, B
Валентність змінна
І і ІІ
II i III
II i IV
II, IV, VI
Сu
Fe, Co, Ni
C, Sn, Pb, Mn
S
18.
Яким же чином миможемо визначити
валентність елемента і
від чого вона залежить?
19.
Валентність залежить від будови атома івизначається за положенням у періодичній системі.
Валентність
Стала
Змінна
Валентність (Н) = І
Максимальна валентність = № групи.
(виключення О = ІІ, Fe = ІІ, ІІІ)
Валентність (О) = ІІ
Валентність (F) = І
Валентність елементів І,ІІ,ІІІ груп
= № групи (виключення Cu = I і ІІ)
Мінімальна валентність ( неметалів у
сполуках із металами і Н) = 8 – № групи.
Проміжні валентності = максимальна
валентність мінус числа кратні двом.
У бінарних сполуках
сумарна валентність усіх атомів одного елемента завжди
дорівнює сумарній валентності усіх атомів другого елемента
20.
Валентність атомів позначаєтьсяримськими цифрами, які
розташовуються над елементом
IV
II
С О2
III
II
Al2 О3
21.
Правила складання хімічних формул:1. Об'єднуватись у молекули можуть:
Метал + неметал
Метал + Оксиген
Неметал + Оксиген
Гідроген + Неметал
2. Всі валентності мають бути зайняті
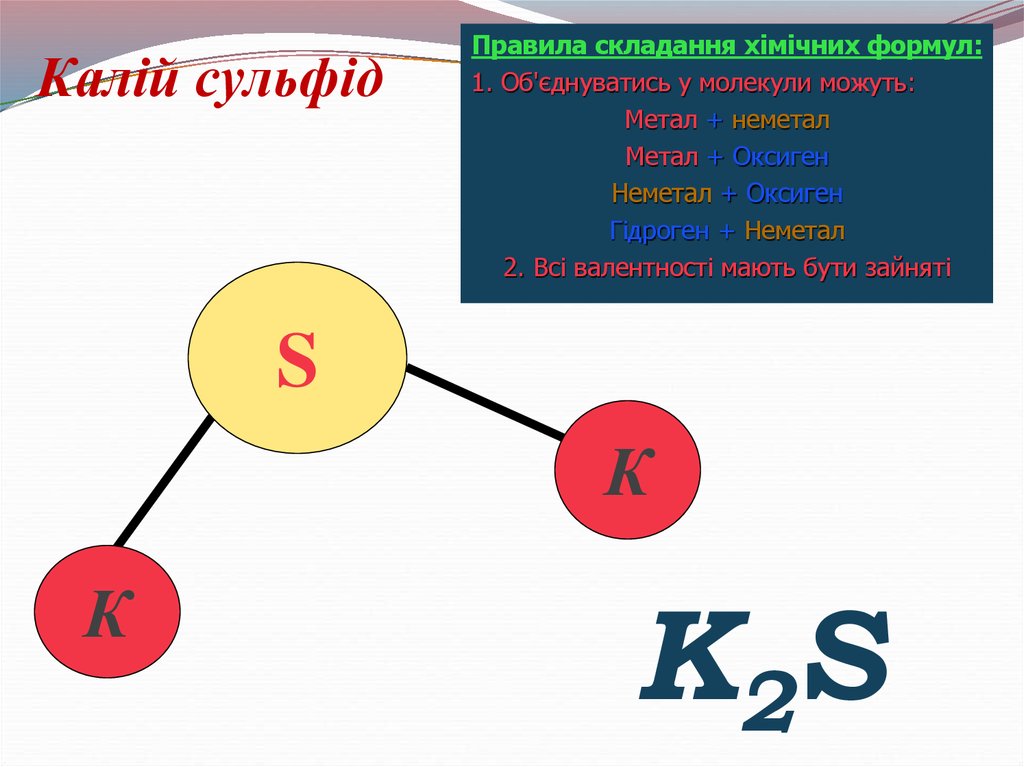
22.
Калій сульфідПравила складання хімічних формул:
1. Об'єднуватись у молекули можуть:
Метал + неметал
Метал + Оксиген
Неметал + Оксиген
Гідроген + Неметал
2. Всі валентності мають бути зайняті
S
К
К
K2S
23.
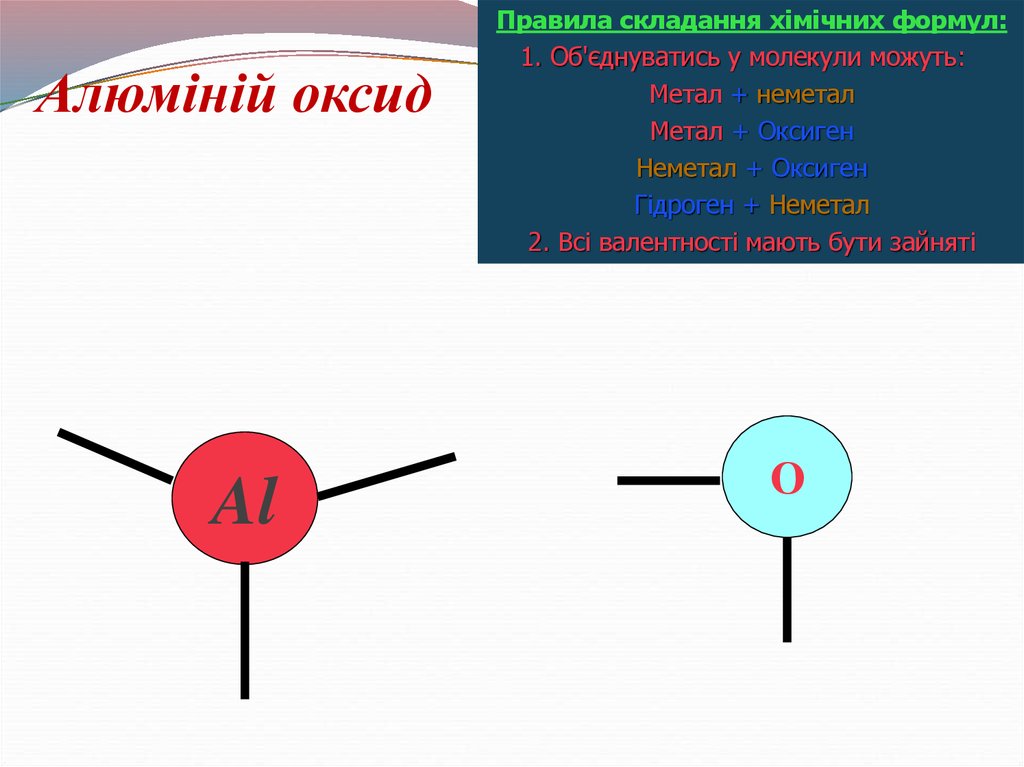
Алюміній оксидAl
Правила складання хімічних формул:
1. Об'єднуватись у молекули можуть:
Метал + неметал
Метал + Оксиген
Неметал + Оксиген
Гідроген + Неметал
2. Всі валентності мають бути зайняті
О
24.
Правила складання хімічних формул:1. Об'єднуватись у молекули можуть:
Метал + неметал
Метал + Оксиген
Неметал + Оксиген
Гідроген + Неметал
2. Всі валентності мають бути зайняті
Алюміній оксид
Al – ІІІ
6
О - ІІ
Al
Al2O3
Al
О
О
О
25.
Правила складання хімічних формул:1. Об'єднуватись у молекули можуть:
Метал + неметал
Метал + Оксиген
Неметал + Оксиген
Гідроген + Неметал
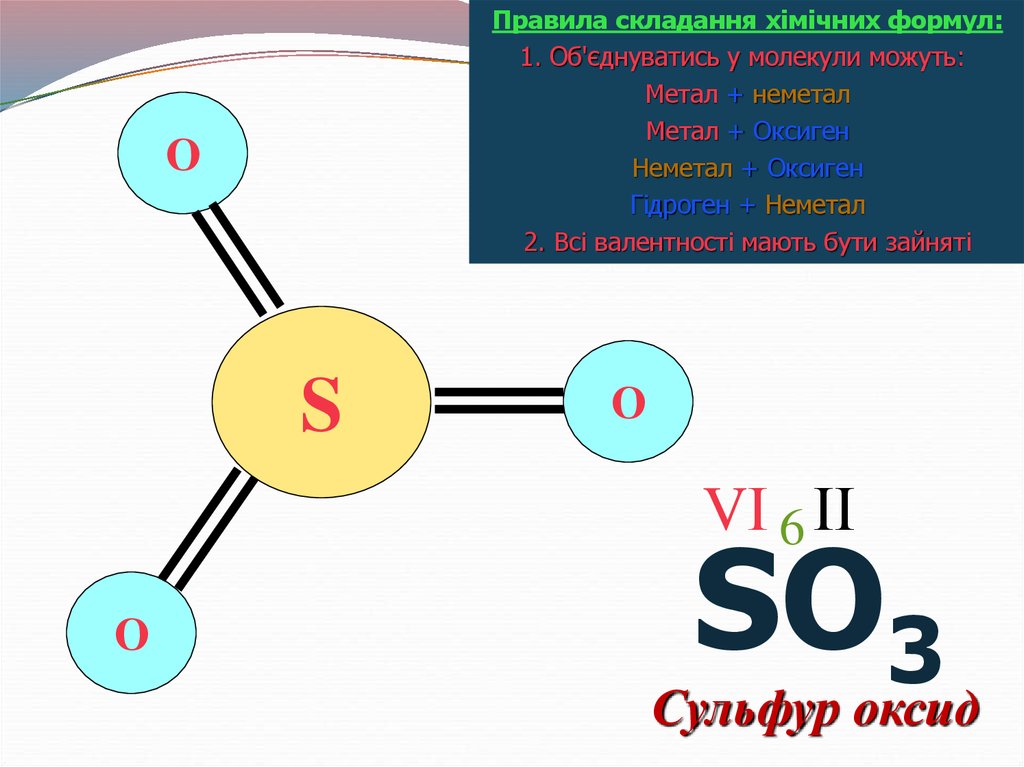
2. Всі валентності мають бути зайняті
О
S
О
VІ 6 ІІ
О
SO3
Сульфур оксид
26. Застосуємо набуті знання на практиці
Складіть формули сполук за їхвалентністю:
KO, CaCl, AlCl, NaS, CuO, MgS
Складіть формули бінарних сполук з
Оксигеном:
Натрію; Карбону (ІІ); Феруму (ІІІ);
Нітрогену (V).
27.
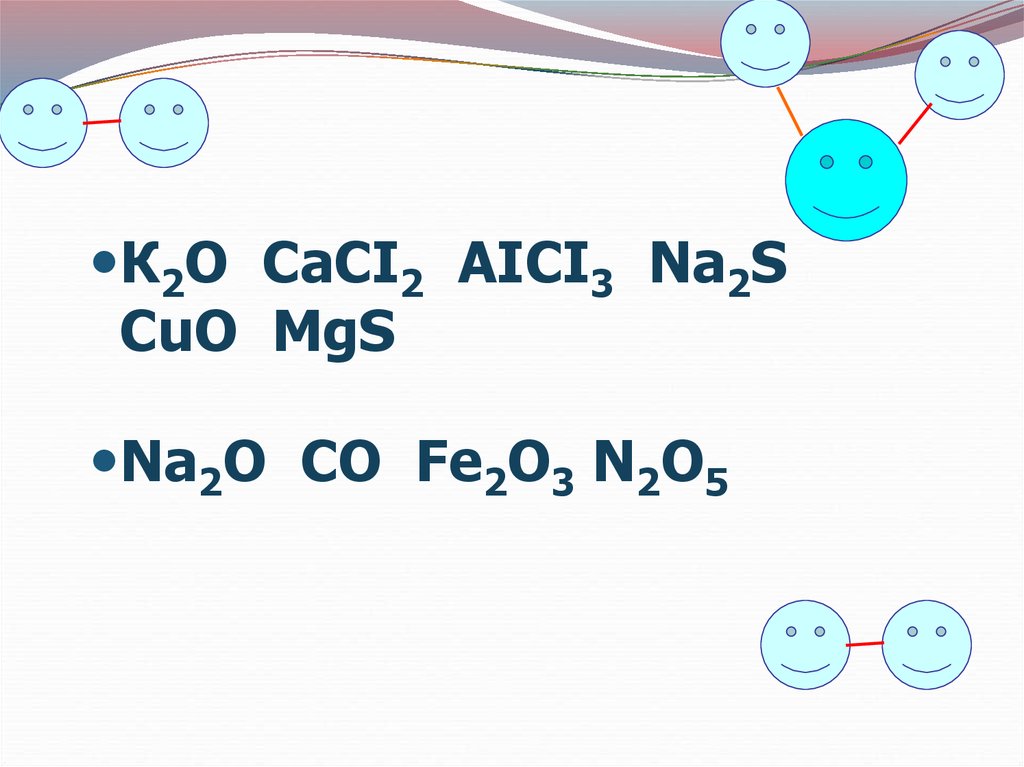
К2О CaCI2 AICI3 Na2SCuO MgS
Na2O CO Fe2O3 N2O5
28.
Визначення валентностей хімічних елементів заформулами речовин
1. Записати формулу речовини
2. Позначити відомі валентності
3. Записати загальну кількість валентностей відомого елемента
(число валентностей х кількість атомів відповідного елемента)
ЗКВ (О) = 2 х 3 = 6
4. Визначити і записати найменше спільне
кратне валентностей для двох елементів
ІІ
VІ
6
5. Розрахувати валентність невідомого елемента
6
(Найменше спільне кратне /
кількість атомів елемента
з невідомою валентністю)
В(S) = 6 / 1 = 6
SO3
Сульфур оксид
29.
Визначення валентностей хімічних елементів заформулами речовин
1. Записати формулу речовини
2. Позначити відомі валентності
3. Записати загальну кількість валентностей відомого елемента (число
валентностей х кількість атомів відповідного елемента)
4. Визначити і записати найменше спільне кратне валентностей для двох
елементів
5. Розрахувати валентність невідомого елемента (Спільне кратне
валентностей / кількість атомів елемента з невідомою валентністю)
V
10
ІІ
Р2О5
10
Фосфор оксид
30.
Визначити валентності хімічних елементівза формулами речовин
ІІ
І
ІІI
ІІ
ІІI
HgO B2O3 MgCl2 PH3 ZnS
ІV
VII
ІV
ІІI
І
SiO2 Cl2O7 SO2 Fe2O3 N2O
Визначення валентностей хімічних елементів за формулами речовин
1. Записати формулу речовини
2. Позначити відомі валентності
3. Записати загальну кількість валентностей відомого елемента (число валентностей х
кількість атомів відповідного елемента)
4. Визначити і записати найменше спільне кратне валентностей для двох елементів
5. Розрахувати валентність невідомого елемента (найменше спільне кратне / кількість
атомів елемента з невідомою валентністю)
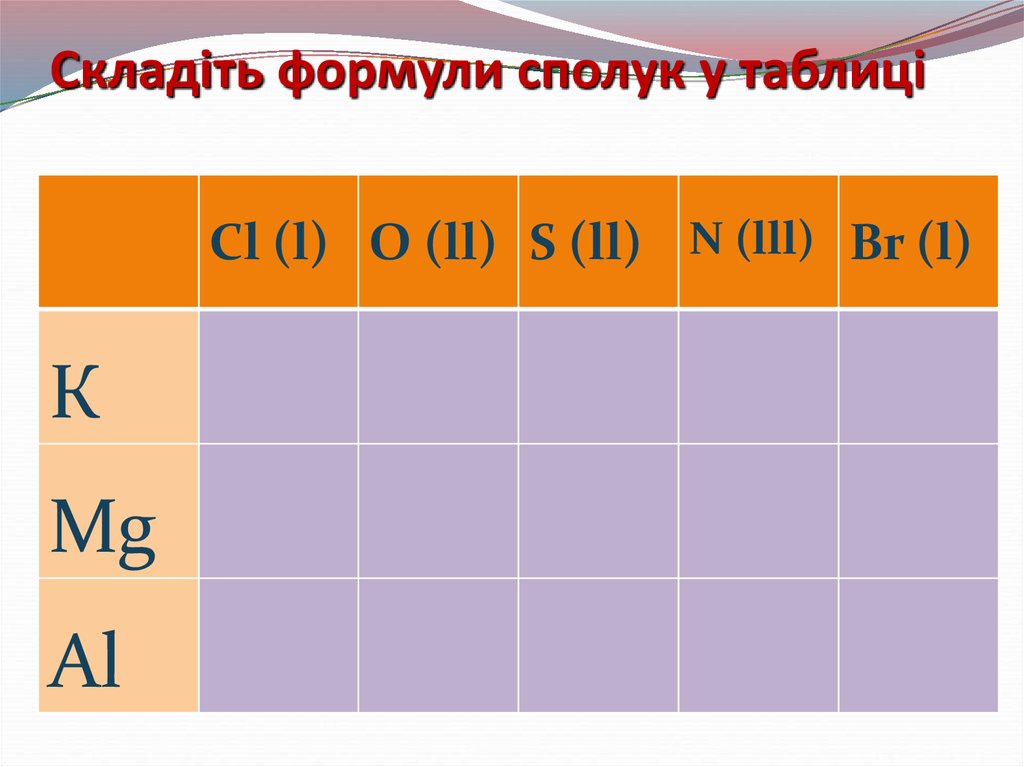
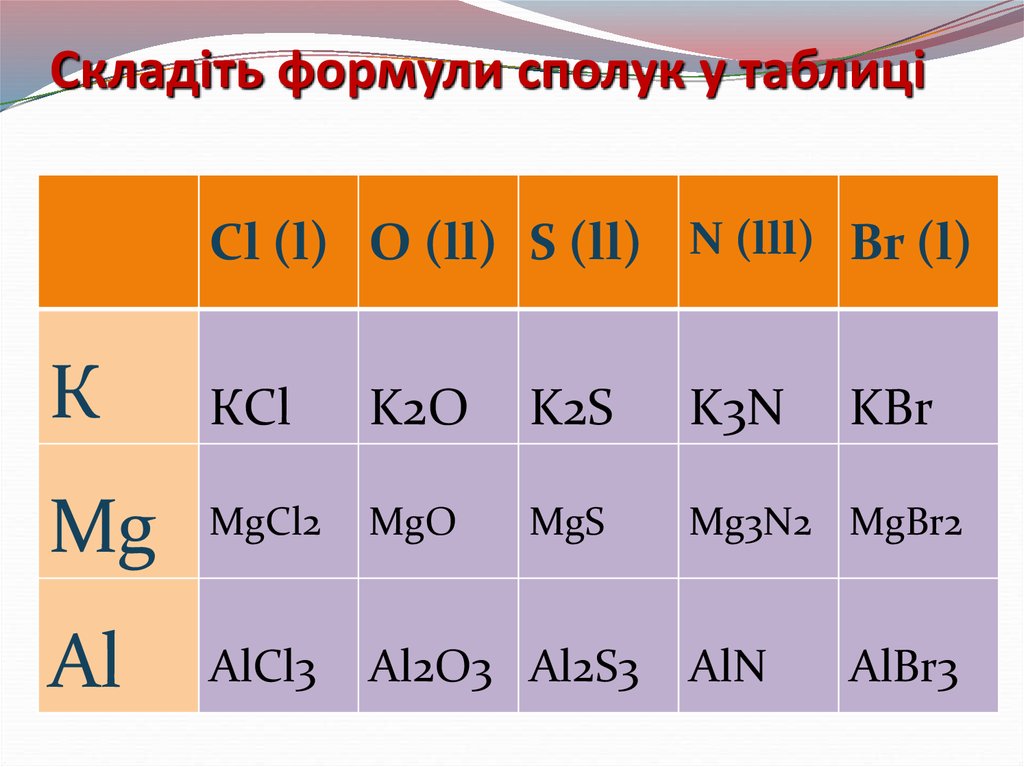
31. Складіть формули сполук у таблиці
Cl (l) O (ll) S (ll) N (lll) Br (l)К
Mg
Al
32. Складіть формули сполук у таблиці
Cl (l) O (ll) S (ll) N (lll) Br (l)К
КCl
K2O
K2S
K3N
Mg
MgCl2
MgO
MgS
Mg3N2 MgBr2
Al
AlCl3
Al2O3 Al2S3
AlN
KBr
AlBr3
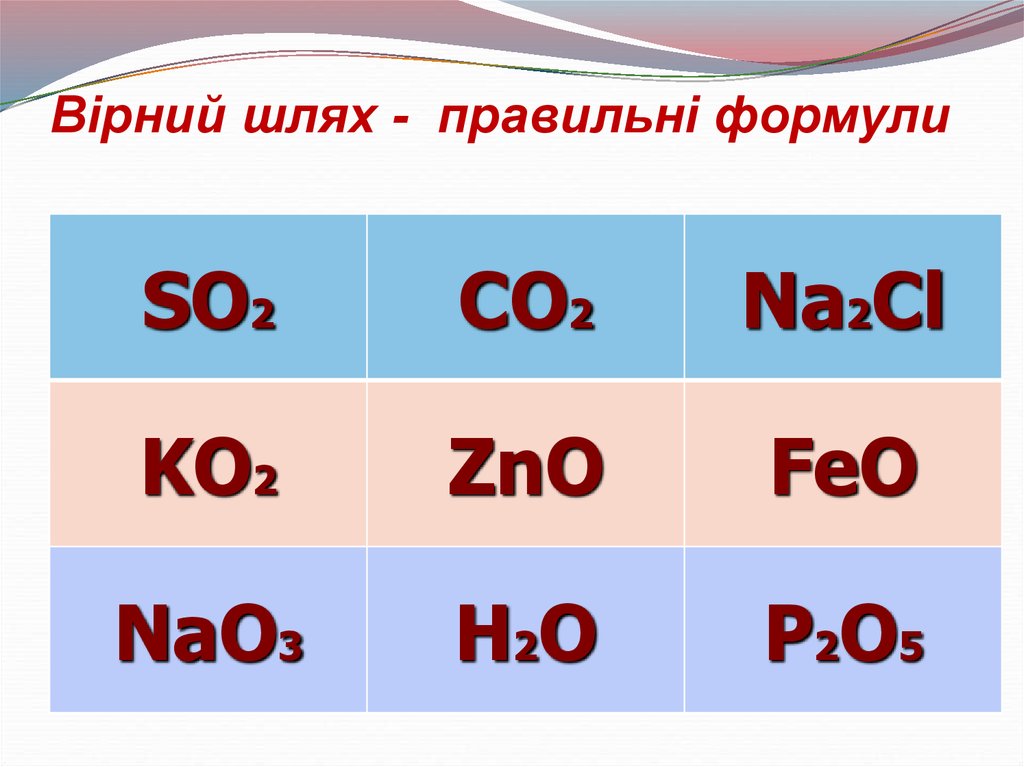
33. Вірний шлях - правильні формули
SO2СО2
Na2Cl
KO2
ZnO
FeO
NaO3
H2O
P2O5
34. Підведемо підсумки уроку
З якою метою ми вивчали валентністьхімічних елементів?
Чи досягли ми мети?
Чи навчилися визначати валентність за
формулами?
Чи навчилися складати хімічні формули
сполук?
Що необхідно знати для складання формул?
Що є “підказкою”?
Оцініть результати своєї діяльності
35.
Домашнє завдання:• прочитати § 10,
• вивчити визначення та алгоритми,
• письмово у зошиті виконати
Вправи 78,79,80 стор. 70





















 chemistry
chemistry








