Similar presentations:
Бензол
1.
2.
1825 год.Майкл Фарадей
выделил бензол из
светильного газа.
3.
1833 годФридрих Вёлер и
Юстус Либих
выделили бензойную
кислоту из бензойной смолы.
4.
1833 годЭйльхард Мичерлих
получил бензол из
бензойной кислоты
5.
1865 годФридрих-Август Кекуле
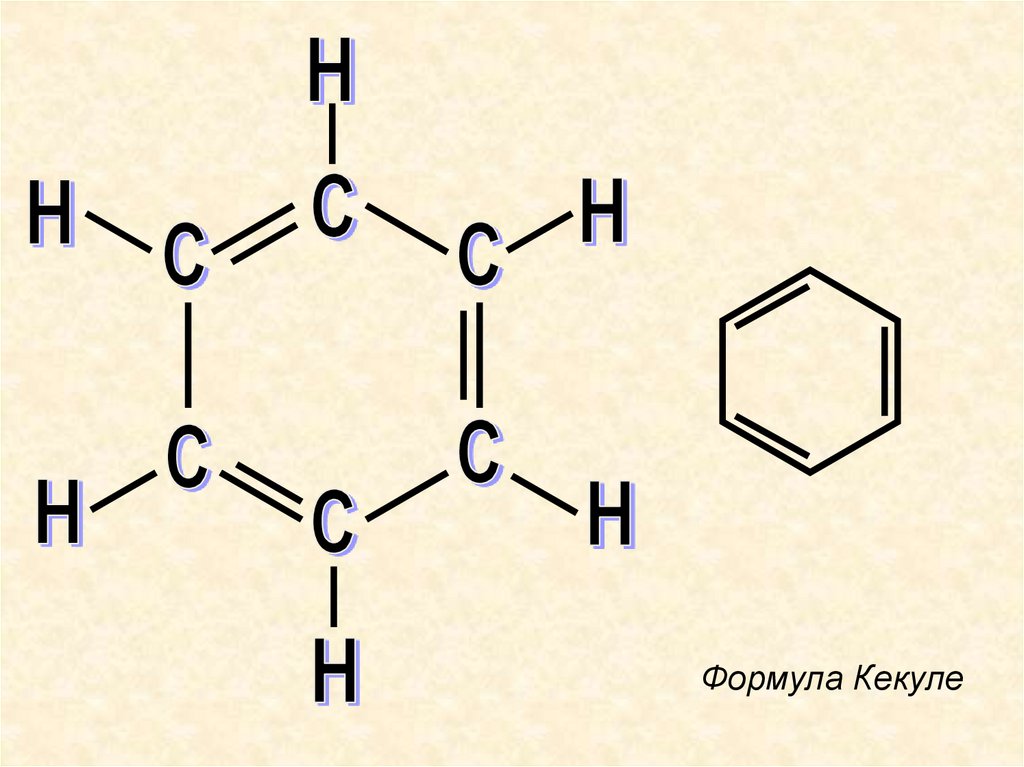
открыл структуру бензола
6.
Формула Кекуле7.
RR
R
R
8.
1892 год9.
В 1899 г. профессор Мюнхенскогоуниверситета Фридрих-Карл-Иоганнес Тиле
он выдвинул гипотезу, согласно которой
атомы углерода в бензольном кольце
связаны «полуторными» связями,
уступающими в активности двойным или
даже одинарным.
10.
С*p
2s
sp2
+
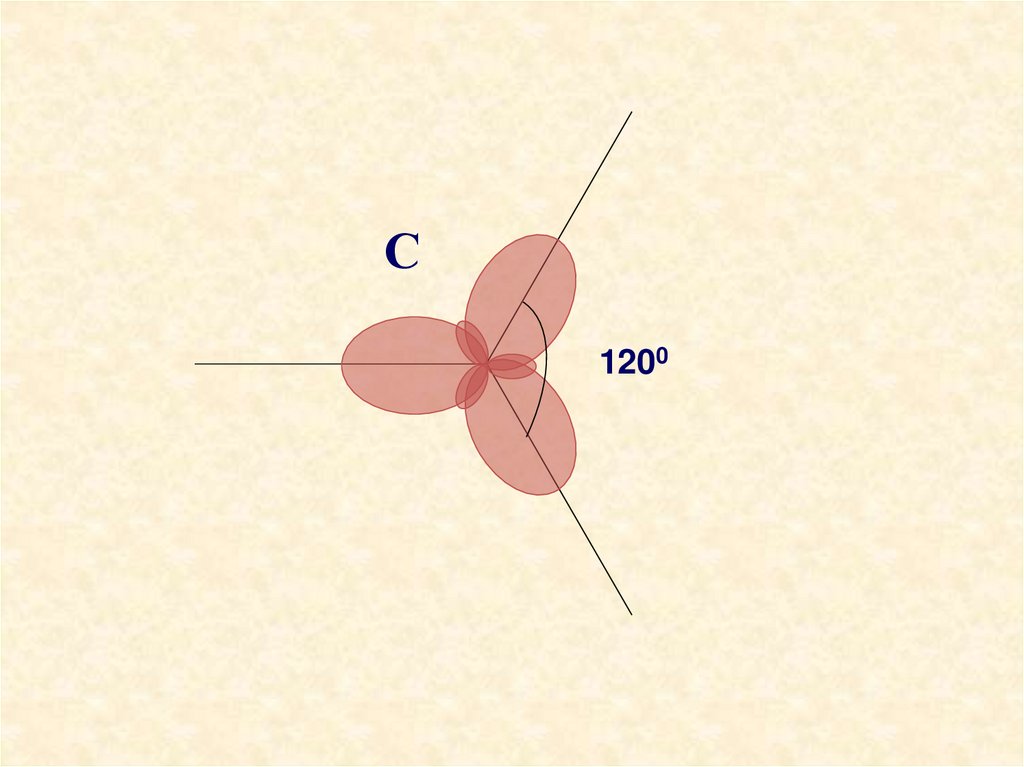
11.
С1200
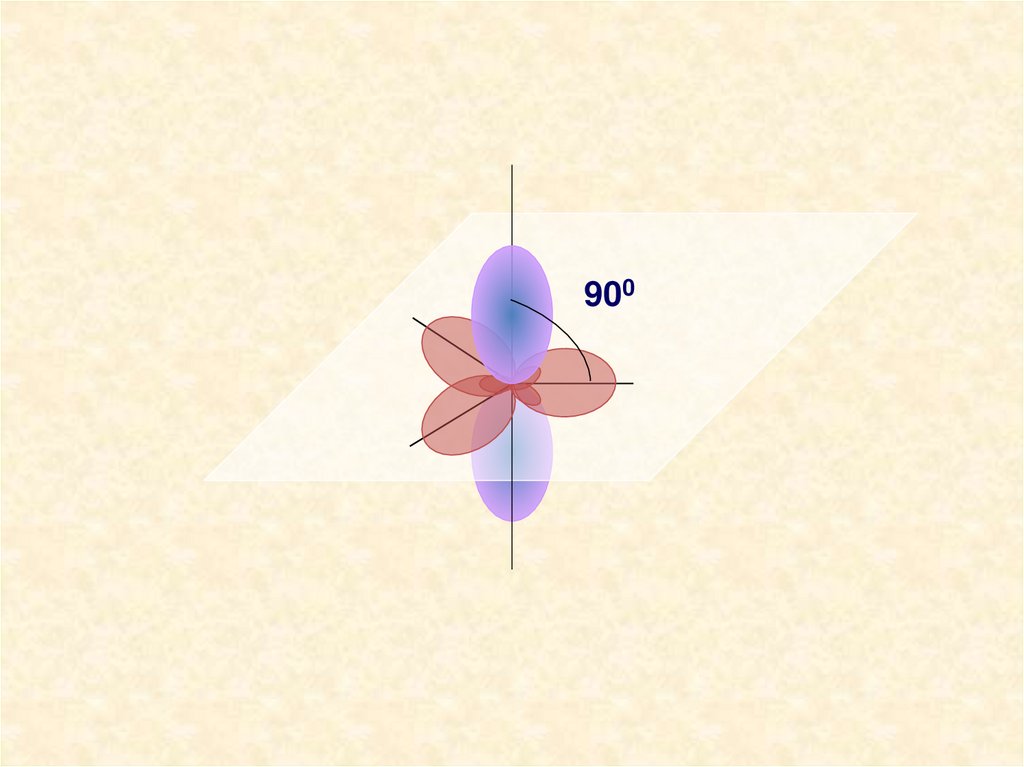
12.
90013.
НН
σ
С
С
σ
С
С
Н
Н
С
Н
С
Н
14.
15.
НН
С
Н
С
С
С
С
Н
С
Н
Н
16.
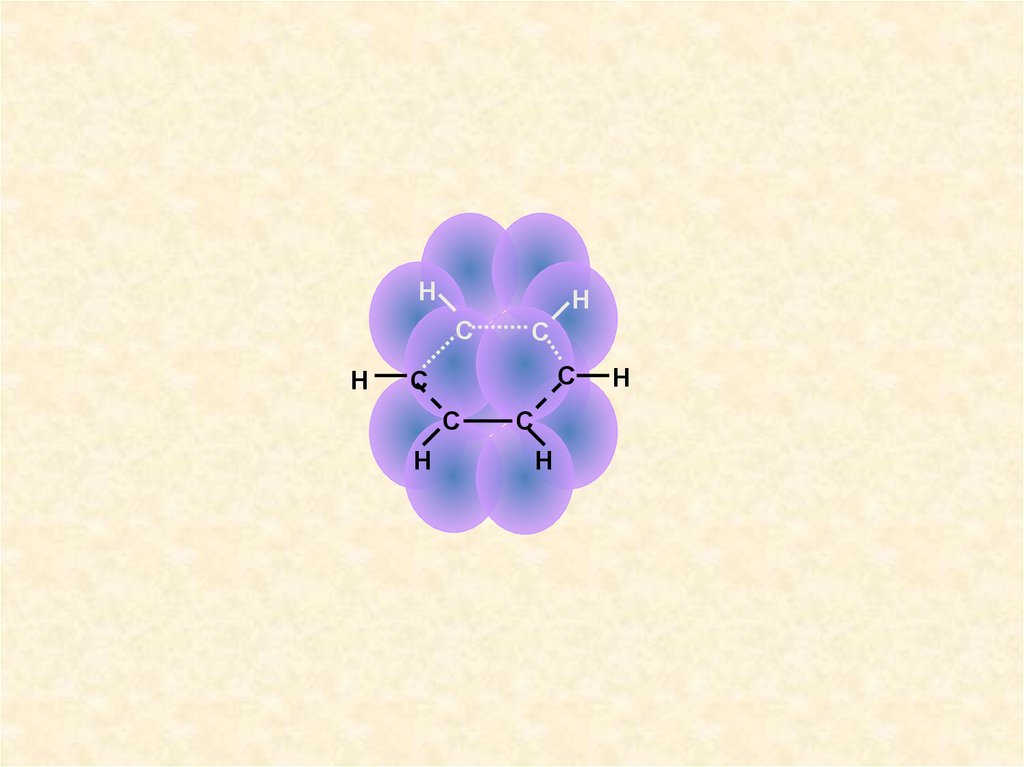
Нр-орбитали
Н
С
Н
Н
С
С
0,140нм
(вид сверху)
С
С
0,108нм
-связи
С
1200
Н
Н
17.
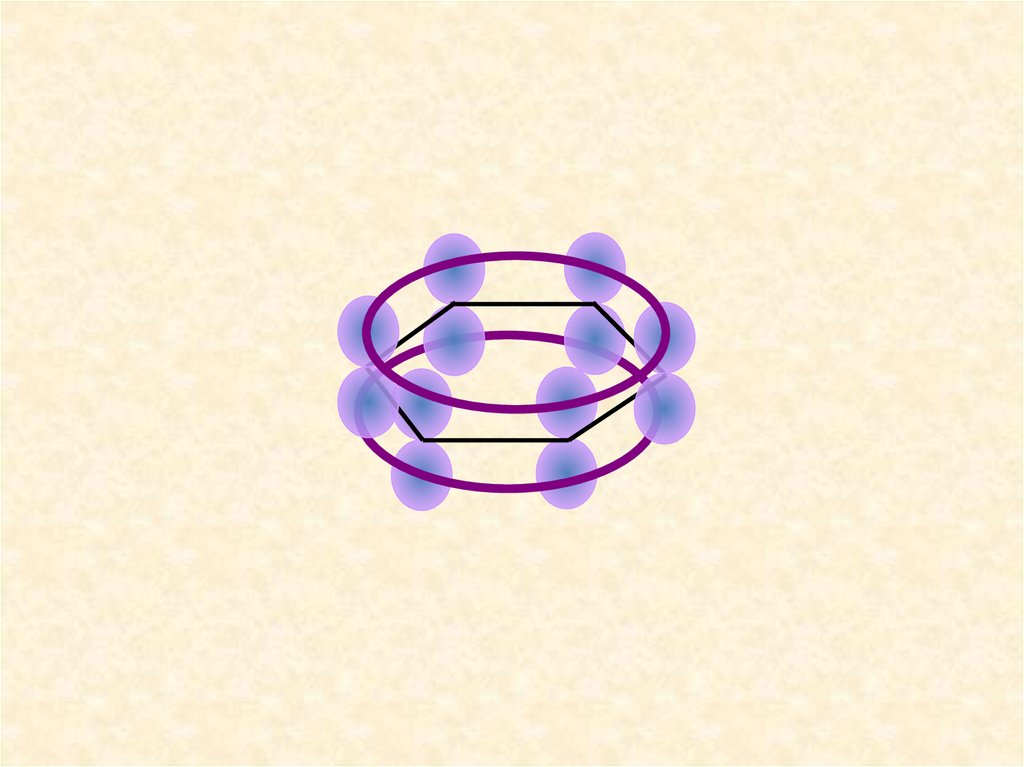
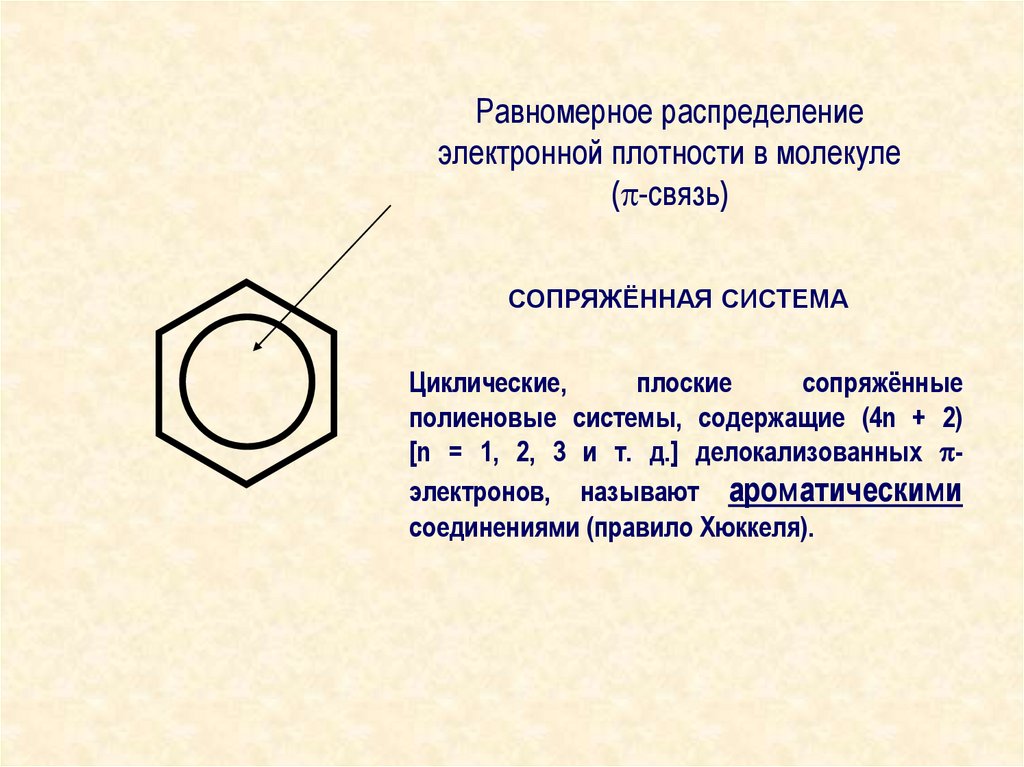
Равномерное распределениеэлектронной плотности в молекуле
( -связь)
СОПРЯЖЁННАЯ СИСТЕМА
Циклические,
плоские
сопряжённые
полиеновые системы, содержащие (4n + 2)
[n = 1, 2, 3 и т. д.] делокализованных электронов, называют ароматическими
соединениями (правило Хюккеля).
18.
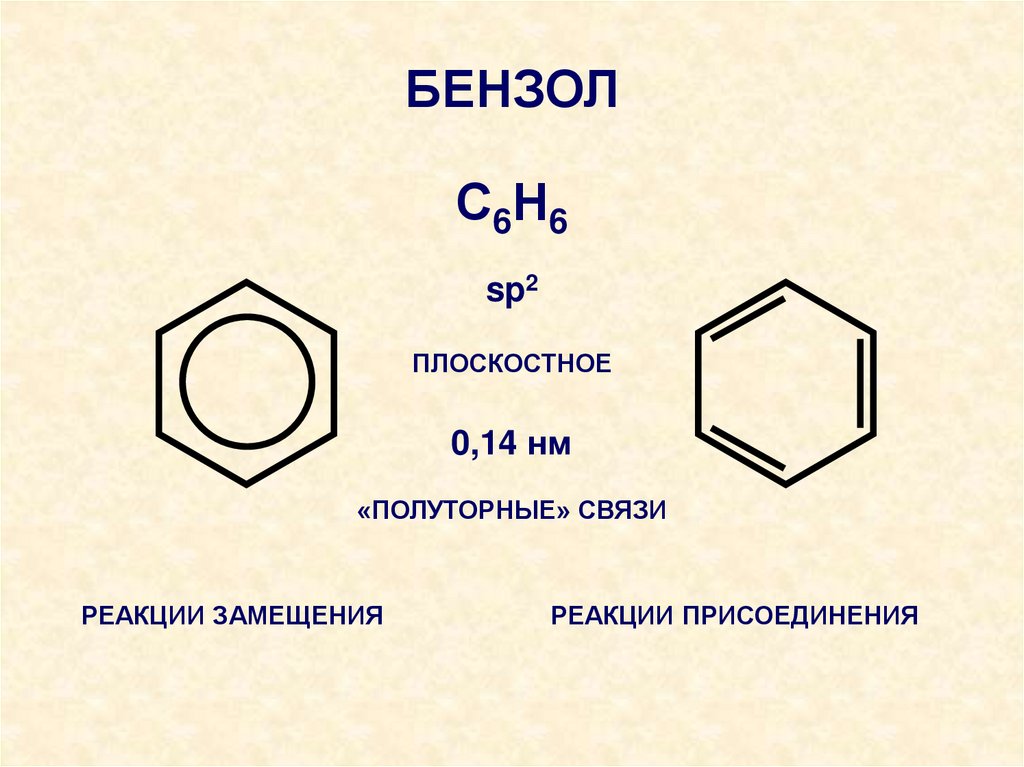
БЕНЗОЛС6Н6
sp2
ПЛОСКОСТНОЕ
0,14 нм
«ПОЛУТОРНЫЕ» СВЯЗИ
РЕАКЦИИ ЗАМЕЩЕНИЯ
РЕАКЦИИ ПРИСОЕДИНЕНИЯ
19.
БЕНЗОЛ – бесцветная жидкостьсо своеобразным запахом, не
растворяется в воде, хорошо
смешивается с неполярными
органическими растворителями
ρ = 0,88 г/см3
20.
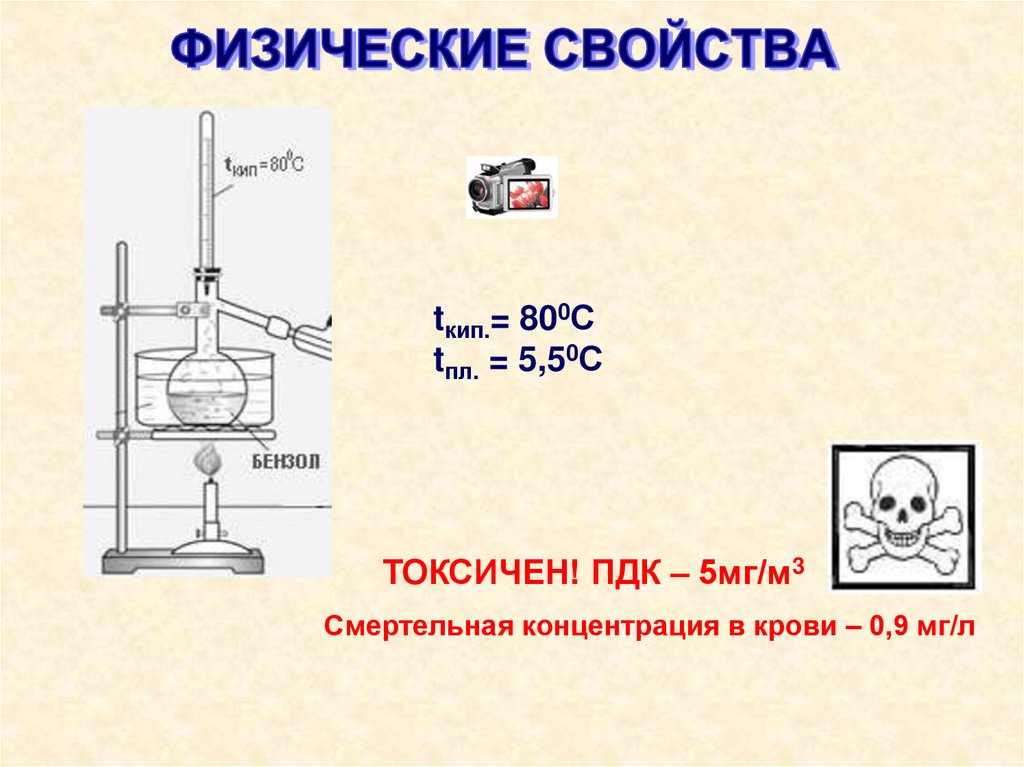
tкип.= 800Сtпл. = 5,50С
ТОКСИЧЕН! ПДК – 5мг/м3
Смертельная концентрация в крови – 0,9 мг/л
21.
ГорениеБензол не обесцвечивает бромную воду
Бензол не окисляется сильными окислителями
22.
I. Реакция замещенияа) галогенирование
СН
СН
+ BrBr
СН
НС
НС
СН
23.
I. Реакция замещенияа) галогенирование
СН
СН
СН
FeBr3 НС
+ BrBr
СН
НС
НС
НС
СН
СBr
+ HBr
СН
СН
бромбензол
FeBr3
C6H6 + Br2 C6H5Br + HBr
24.
I. Реакция замещенияб) нитрование
СН
СН
НС
СН
НС
СН
+ HONO2
HNO3
25.
I. Реакция замещенияб) нитрование
СН
СН
СН
НС
СН
НС
СН
+ HONO2
HNO3
СNO2
+ H2O
СН
H2SO4конц НС
НС
СН
нитробензол
H2SO4конц
C6H6 + HNO3 C6H5NO2 + H2O
26.
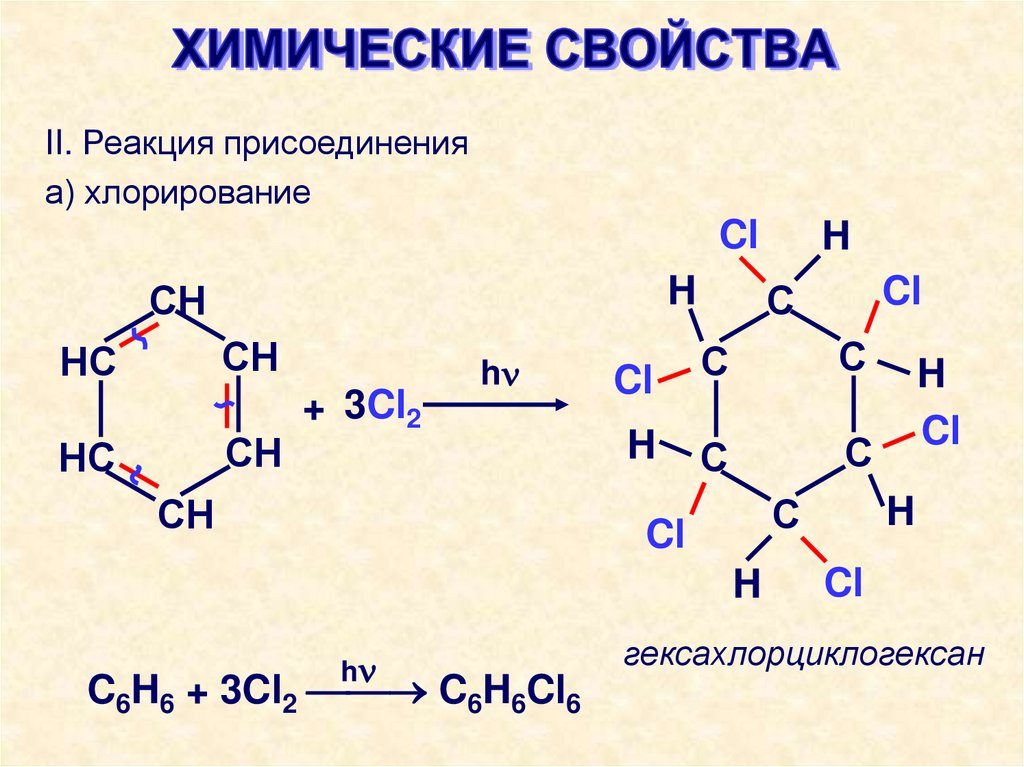
II. Реакция присоединенияа) хлорирование
Cl
H
СН
СН
НС
СН
НС
+ 3Cl2
h
СН
Cl
С
С
H
С
С
С
H
C6H6 + 3Cl2 C6H6Cl6
Cl
С
Cl
h
H
H
Cl
H
Cl
гексахлорциклогексан
27.
II. Реакция присоединенияб) гидрирование
Н
H
СН
СН
НС
СН
НС
+ 3Н2
t0, Ni
СН
Н
С
С
H
С
С
С
H
C6H6 + 3Н2 C6H12
Н
С
Н
t0, Ni
H
H
Н
H
Н
циклогексан
28.
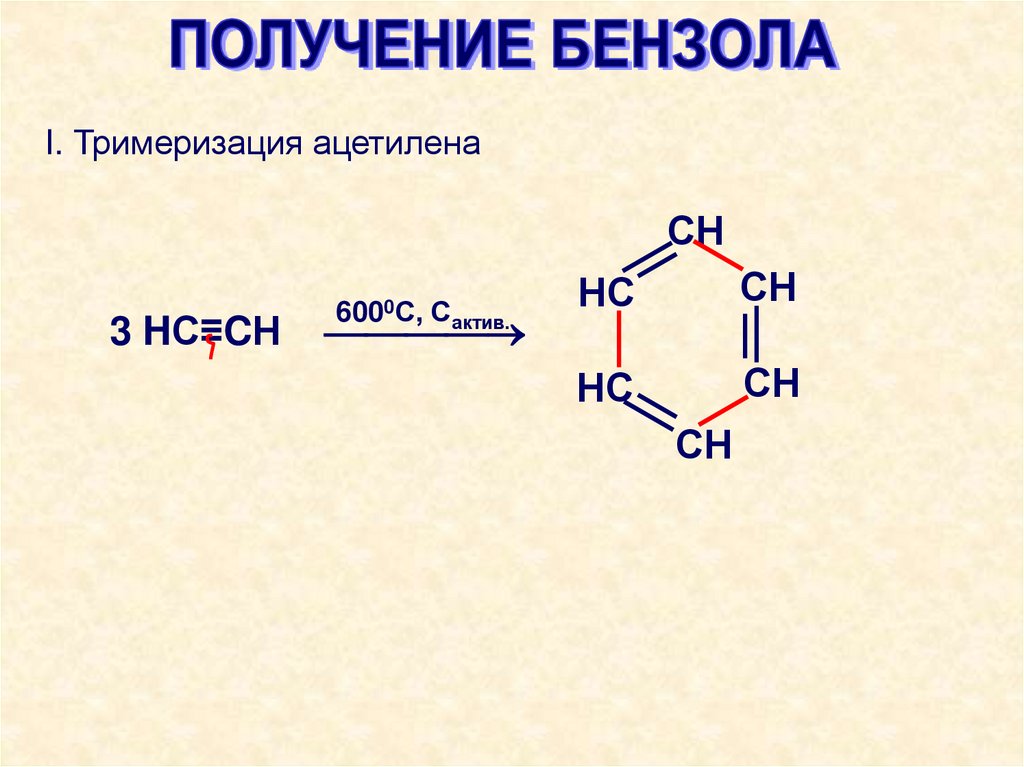
I. Тримеризация ацетиленаСН
3 HС≡CН
6000С, Сактив.
НС
СН
НС
СН
СН
29.
II. Дегидрирование циклогексанаН
H
H
Н
Н
С
H
С
С
С
С
С
Н
СН
H
Н
Н
H
H
3000, Pt
СН
НС
+ 3H2
СН
НС
СН
30.
III. Каталитическая дегидроциклизация гексанаН
Н
H
С
H
С
Н
С
Н
Н
H
С
С
С
Н
СН
H
Н
Н
H
H
t0, kat
СН
НС
+ 4H2
СН
НС
СН
31.
ФЕНОЛФОРМАЛЬДЕГИДНАЯ СМОЛАИНСЕКТИЦИДЫ
КРАСИТЕЛИ
ФЕНОЛ
С6Н5-ОН
ГЕКСАХЛОРАН
С6Н6Сl6
АНИЛИН
С6Н5-NН2
КУМОЛ
С6Н5-СН(СН3)2
БЕНЗОЛ
С 6Н 6
НИТРОБЕНЗОЛ
С6Н5-NO2
ПОЛИСТИРОЛ
АЦЕТОН
СН3СОСН3
ЭТИЛБЕНЗОЛ
С6Н5-С2Н5
СТИРОЛ
С6Н5-СН=СН2
ЛЕКАРСТВЕННЫЕ ПРЕПАРАТЫ
КАПРОН





















 chemistry
chemistry








