Similar presentations:
Физико-химические свойства и биологическая активность новых антрахиноновых производных
1.
МИНИСТЕРСТВО ОБРАЗОВАНИЯ РЕСПУБЛИКИ БЕЛАРУСЬУчреждение образования
«Международный государственный экологический институт
имени А.Д. Сахарова»
Белорусского государственного университета
ФАКУЛЬТЕТ ЭКОЛОГИЧЕСКОЙ МЕДИЦИНЫ
КАФЕДРА ЭКОЛОГИЧЕСКОЙ ХИМИИ И БИОХИМИИ
ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА И БИОЛОГИЧЕСКАЯ АКТИВНОСТЬ НОВЫХ
АНТРАХИНОНОВЫХ ПРОИЗВОДНЫХ
Дипломная работа студента IV курса
Исполнитель:
Студент 4 курса А81МЕД2 группы
дневной формы обучения
Сырыцкий Илья Александрович
Научный руководитель:
канд.хим.наук., доцент, профессор Российской
Академии Естествознания
Шахаб Сиямак Насер
2. Цель работы - изучение физико-химических и антиоксидантных свойств новых антрахиноновых производных.
Задачи:1.
Предварительное и полное квантово-химическое моделирование
антрахиноновых производных полуэмперическим методом PM6 и
неэмпирическим методом теории функционала плотности B3LYP с
базисом 6-31+G*.
2.
Изучение физико-химических свойств.
3.
Исследование антиоксидантной активности.
2
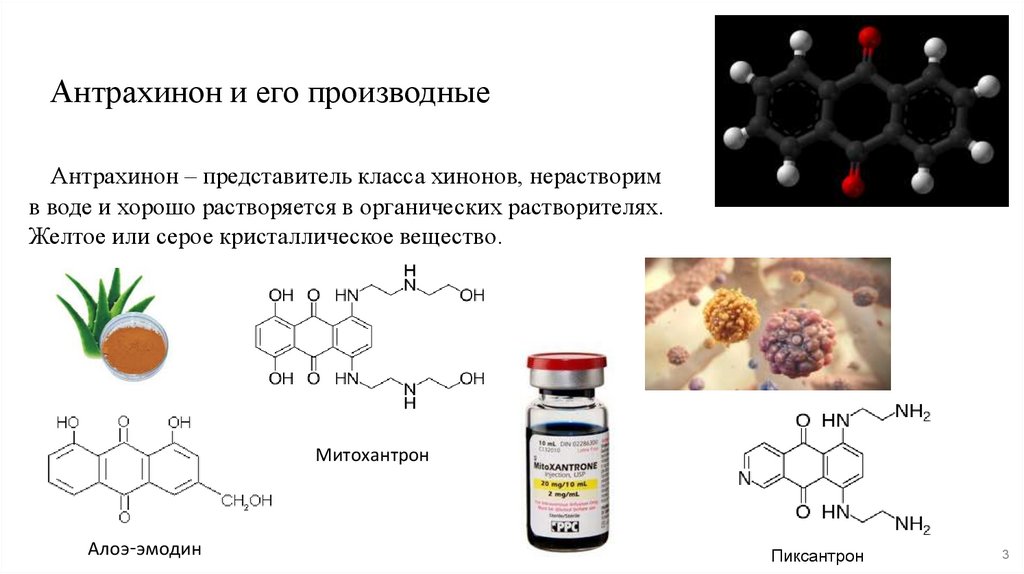
3. Антрахинон и его производные
Антрахинон – представитель класса хинонов, нерастворимв воде и хорошо растворяется в органических растворителях.
Желтое или серое кристаллическое вещество.
Митохантрон
Алоэ-эмодин
Пиксантрон
3
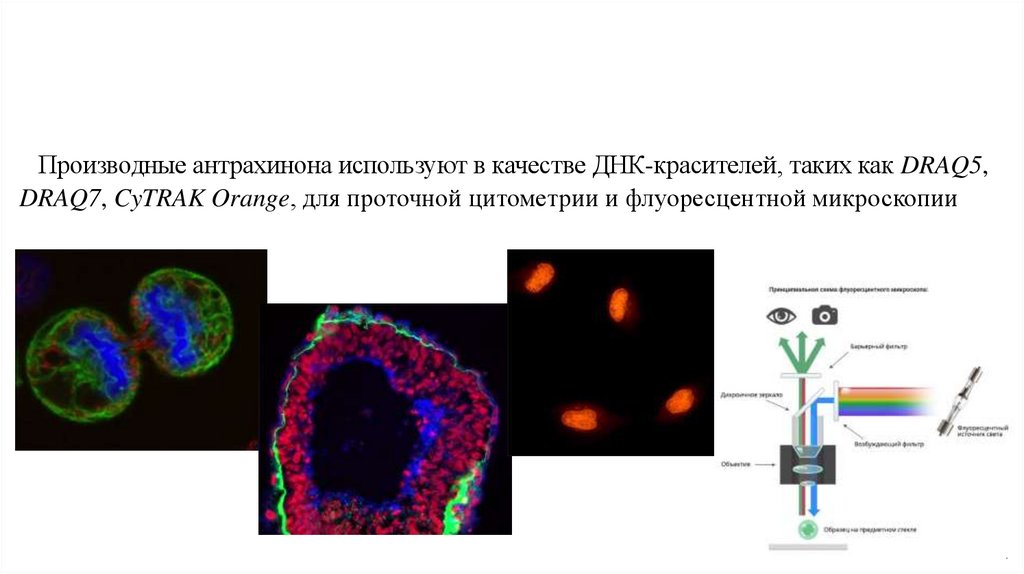
4.
Производные антрахинона используют в качестве ДНК-красителей, таких как DRAQ5,DRAQ7, CyTRAK Orange, для проточной цитометрии и флуоресцентной микроскопии
4
5. Материалы и методы расчетов
Для квантово-химических вычислений применен химический пакет Gaussian09W. Оптимизация структур проводилась в водной среде полуэмпирическим
методом PM6 до достижения глобального минимума полной энергии изучаемых
систем.
Для визуализации результатов использованы ChemOffice2016 и
GaussView06.
Для расчета УФ спектров и антиоксидантной активности использован
метод B3LYP/6-31+G* с усредненным масштабирующим коэффициентом
0,99 в среде растворителя (вода).
5
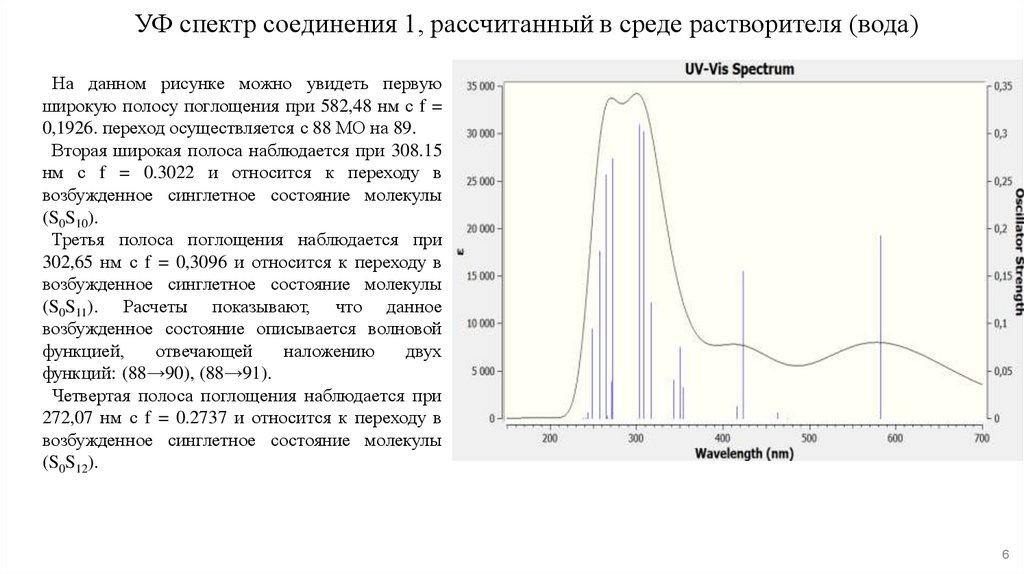
6. УФ спектр соединения 1, рассчитанный в среде растворителя (вода)
На данном рисунке можно увидеть первуюширокую полосу поглощения при 582,48 нм с f =
0,1926. переход осуществляется с 88 МО на 89.
Вторая широкая полоса наблюдается при 308.15
нм с f = 0.3022 и относится к переходу в
возбужденное синглетное состояние молекулы
(S0S10).
Третья полоса поглощения наблюдается при
302,65 нм с f = 0,3096 и относится к переходу в
возбужденное синглетное состояние молекулы
(S0S11). Расчеты показывают, что данное
возбужденное состояние описывается волновой
функцией,
отвечающей
наложению
двух
функций: (88→90), (88→91).
Четвертая полоса поглощения наблюдается при
272,07 нм с f = 0.2737 и относится к переходу в
возбужденное синглетное состояние молекулы
(S0S12).
6
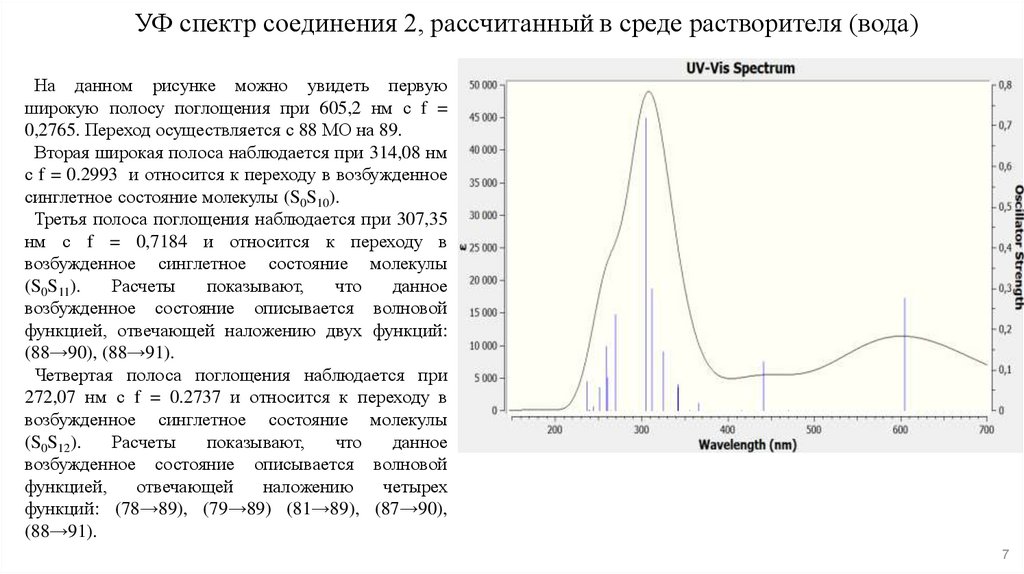
7. УФ спектр соединения 2, рассчитанный в среде растворителя (вода)
На данном рисунке можно увидеть первуюширокую полосу поглощения при 605,2 нм с f =
0,2765. Переход осуществляется с 88 МО на 89.
Вторая широкая полоса наблюдается при 314,08 нм
с f = 0.2993 и относится к переходу в возбужденное
синглетное состояние молекулы (S0S10).
Третья полоса поглощения наблюдается при 307,35
нм с f = 0,7184 и относится к переходу в
возбужденное синглетное состояние молекулы
(S0S11).
Расчеты
показывают,
что
данное
возбужденное состояние описывается волновой
функцией, отвечающей наложению двух функций:
(88→90), (88→91).
Четвертая полоса поглощения наблюдается при
272,07 нм с f = 0.2737 и относится к переходу в
возбужденное синглетное состояние молекулы
(S0S12).
Расчеты
показывают,
что
данное
возбужденное состояние описывается волновой
функцией,
отвечающей
наложению
четырех
функций: (78→89), (79→89) (81→89), (87→90),
(88→91).
7
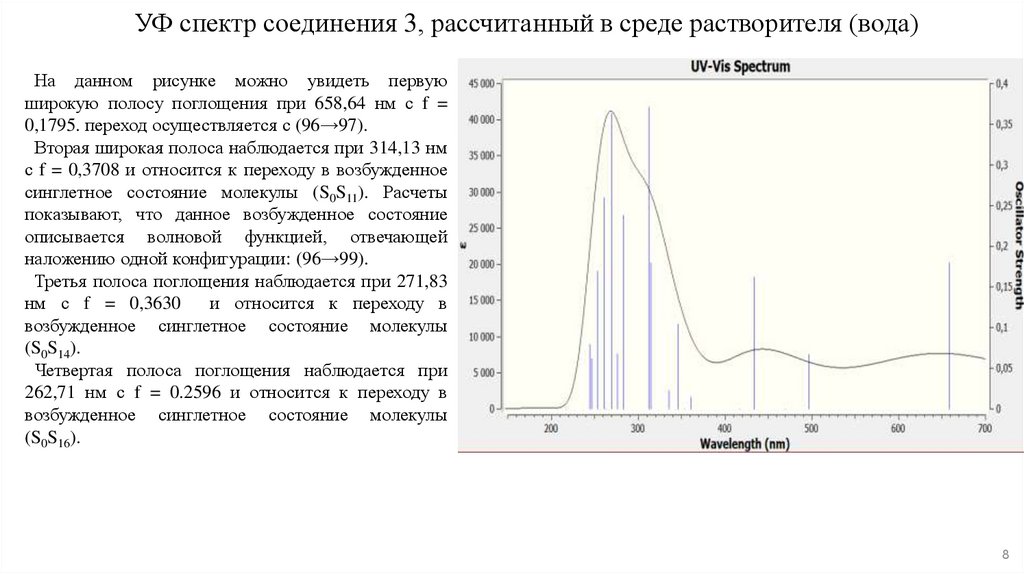
8. УФ спектр соединения 3, рассчитанный в среде растворителя (вода)
На данном рисунке можно увидеть первуюширокую полосу поглощения при 658,64 нм с f =
0,1795. переход осуществляется с (96→97).
Вторая широкая полоса наблюдается при 314,13 нм
с f = 0,3708 и относится к переходу в возбужденное
синглетное состояние молекулы (S0S11). Расчеты
показывают, что данное возбужденное состояние
описывается волновой функцией, отвечающей
наложению одной конфигурации: (96→99).
Третья полоса поглощения наблюдается при 271,83
нм с f = 0,3630
и относится к переходу в
возбужденное синглетное состояние молекулы
(S0S14).
Четвертая полоса поглощения наблюдается при
262,71 нм с f = 0.2596 и относится к переходу в
возбужденное синглетное состояние молекулы
(S0S16).
8
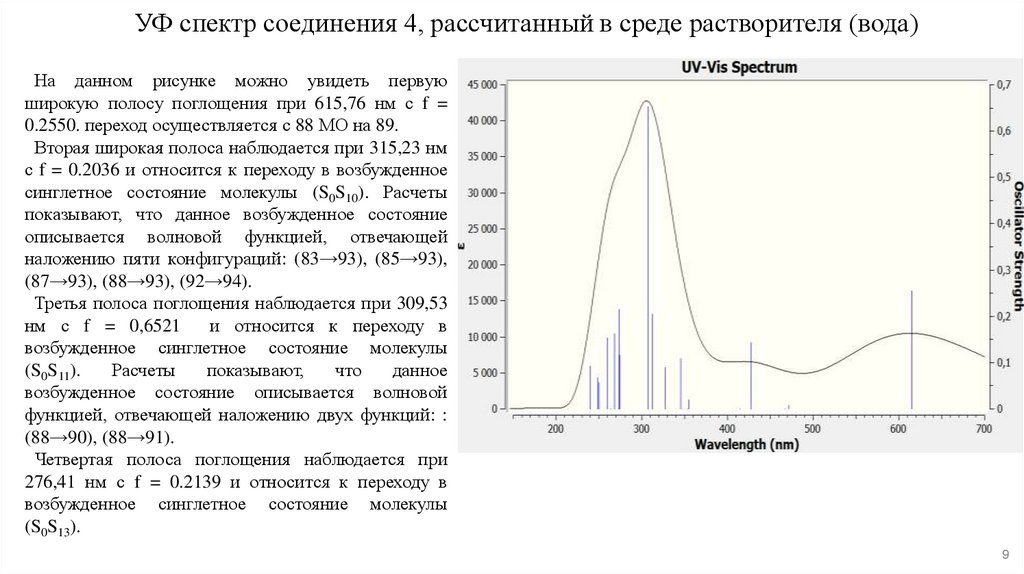
9. УФ спектр соединения 4, рассчитанный в среде растворителя (вода)
На данном рисунке можно увидеть первуюширокую полосу поглощения при 615,76 нм с f =
0.2550. переход осуществляется с 88 МО на 89.
Вторая широкая полоса наблюдается при 315,23 нм
с f = 0.2036 и относится к переходу в возбужденное
синглетное состояние молекулы (S0S10). Расчеты
показывают, что данное возбужденное состояние
описывается волновой функцией, отвечающей
наложению пяти конфигураций: (83→93), (85→93),
(87→93), (88→93), (92→94).
Третья полоса поглощения наблюдается при 309,53
нм с f = 0,6521
и относится к переходу в
возбужденное синглетное состояние молекулы
(S0S11).
Расчеты
показывают,
что
данное
возбужденное состояние описывается волновой
функцией, отвечающей наложению двух функций: :
(88→90), (88→91).
Четвертая полоса поглощения наблюдается при
276,41 нм с f = 0.2139 и относится к переходу в
возбужденное синглетное состояние молекулы
(S0S13).
9
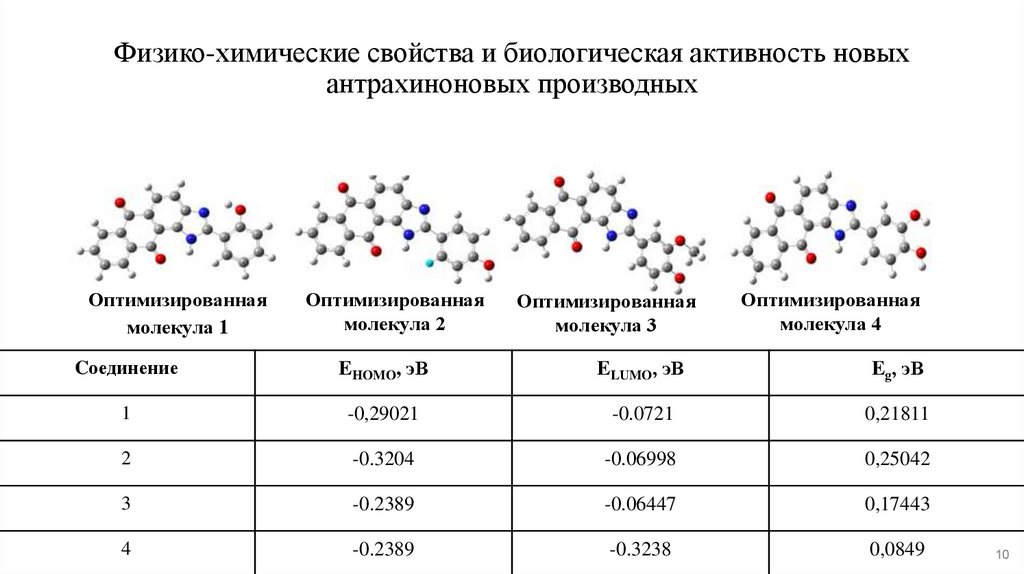
10. Физико-химические свойства и биологическая активность новых антрахиноновых производных
Оптимизированнаямолекула 1
Оптимизированная
молекула 2
Оптимизированная
молекула 3
Оптимизированная
молекула 4
Cоединение
EHOMO, эВ
ELUMO, эВ
Eg, эВ
1
-0,29021
-0.0721
0,21811
2
-0.3204
-0.06998
0,25042
3
-0.2389
-0.06447
0,17443
4
-0.2389
-0.3238
0,0849
10
11.
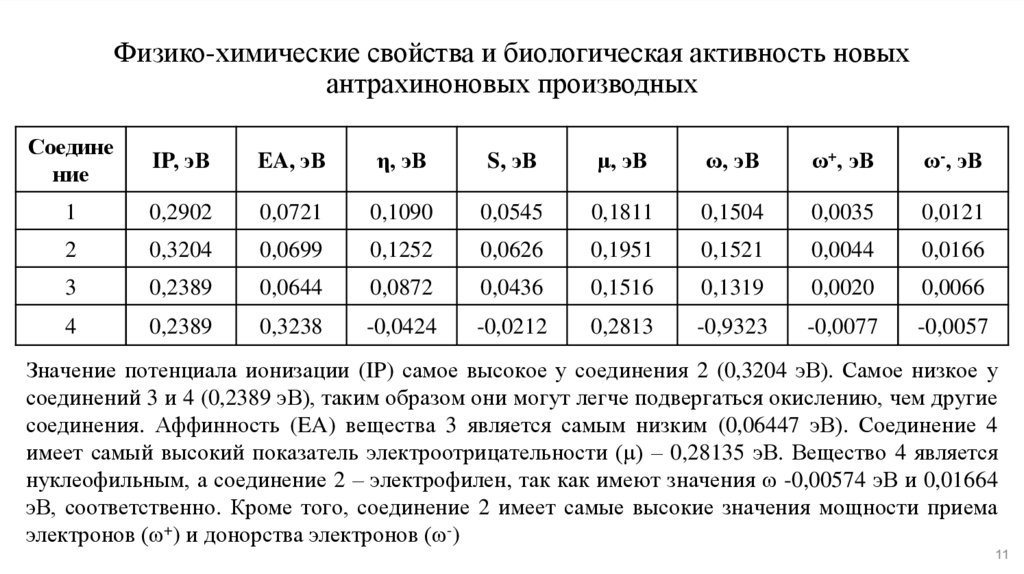
Физико-химические свойства и биологическая активность новыхантрахиноновых производных
Соедине
ние
IP, эВ
EA, эВ
η, эВ
S, эВ
μ, эВ
ω, эВ
ω+, эВ
ω-, эВ
1
0,2902
0,0721
0,1090
0,0545
0,1811
0,1504
0,0035
0,0121
2
0,3204
0,0699
0,1252
0,0626
0,1951
0,1521
0,0044
0,0166
3
0,2389
0,0644
0,0872
0,0436
0,1516
0,1319
0,0020
0,0066
4
0,2389
0,3238
-0,0424
-0,0212
0,2813
-0,9323
-0,0077
-0,0057
Значение потенциала ионизации (IP) самое высокое у соединения 2 (0,3204 эВ). Самое низкое у
соединений 3 и 4 (0,2389 эВ), таким образом они могут легче подвергаться окислению, чем другие
соединения. Аффинность (EA) вещества 3 является самым низким (0,06447 эВ). Соединение 4
имеет самый высокий показатель электроотрицательности (μ) – 0,28135 эВ. Вещество 4 является
нуклеофильным, а соединение 2 – электрофилен, так как имеют значения ω -0,00574 эВ и 0,01664
эВ, соответственно. Кроме того, соединение 2 имеет самые высокие значения мощности приема
электронов (ω+) и донорства электронов (ω-)
11
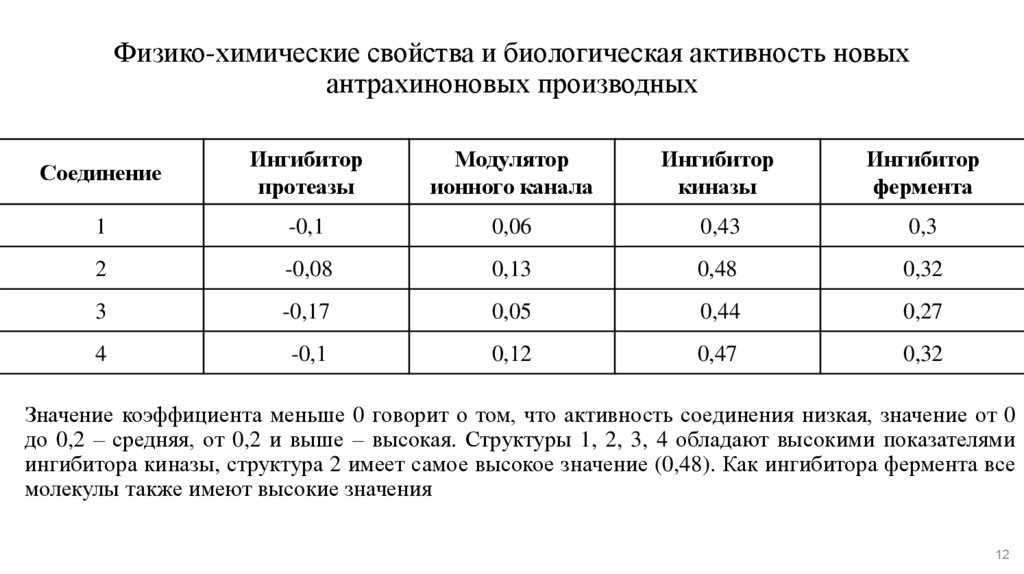
12.
Физико-химические свойства и биологическая активность новыхантрахиноновых производных
Соединение
Ингибитор
протеазы
Модулятор
ионного канала
Ингибитор
киназы
Ингибитор
фермента
1
-0,1
0,06
0,43
0,3
2
-0,08
0,13
0,48
0,32
3
-0,17
0,05
0,44
0,27
4
-0,1
0,12
0,47
0,32
Значение коэффициента меньше 0 говорит о том, что активность соединения низкая, значение от 0
до 0,2 – средняя, от 0,2 и выше – высокая. Структуры 1, 2, 3, 4 обладают высокими показателями
ингибитора киназы, структура 2 имеет самое высокое значение (0,48). Как ингибитора фермента все
молекулы также имеют высокие значения
12
13. Выводы
1.Полуэмпирическим методом PM6 проведено предварительное квантовохимическое моделирование 2-(2-гидроксифенил)-1Н-антра[1,2-d] имидазол-6,11-диона,
2-(4-гидроксифенил)-1Н-антра[1,2-d]имидазол-6,11-диона,
2-(4-гидрокси-3метоксифенил)-1Н-антра-[1,2-d] имидазол-6,11-диона, 2-(3,4-дигидроксифенил)-1Нантра[1,2-d]имидазол-6,11-диона. Неэмпирическим методом теории функционала
плотности (DFT) B3LYP с базисом 6-31+G* проведено полное квантово-химическое
моделирование веществ и найдены энергии HOMO и LUMO. Ширина запрещенной
зоны (Eg) для соединений 1, 2, 3 и 4 составляет 0,21811, 0,25042, 0,17443, 0,08490 эВ,
соответственно.
2.
Для структур 1, 2, 3 и 4 найдены энергия Гиббса: 358,96, 358,96, 252,75, 204,34
кДж/моль, соответственно – и константа диссоциации: 7,691, 8,934, 8,590, 7,744.
Рассчитаны электронные спектры молекул в среде растворителя (вода). Установлено,
что самые интенсивные пики для соединений 1, 2, 3 и 4 наблюдаются при 302,65,
307,35, 314,13 и 309,52 нм соответственно.
13
14. Выводы
3.Изучены биологическая активность и антиоксидантные свойства веществ.
Соединения 3 и 4 имеют самый низкий показатель потенциала ионизации (0,2389 эВ),
следовательно, могут легче подвергаться окислению, в отличие от других изученных
структур. Аффинность (EA) молекул 1, 2, 3 и 4 составляет 0,07210, 0,06998, 0,06447 и
0,32380 эВ, соответственно. Вещество 3 имеет самый низкий показатель EA (0,06447
эВ), следовательно, ему требуется меньше энергии для присоединения электрона.
Соединение 4 является нуклеофильным, а структура 2 – электрофилен, так как имеют
значения ω -0,00574 эВ и 0,01664 эВ, соответственно. Кроме того, соединение 2 имеет
самые высокие значения ω+ (0,00440 эВ) и ω- (0,01664 эВ). Все вещества также могут
выступить ингибитором фермента (0,30, 0,32, 0,27, 0,32) и киназы (0,43, 0,48, 0,44, 0,47).
14
15. Список собственных публикаций, выполненных по теме курсовой работы
Syrytskii I., Shahab S., Linnik V., Pyrko A., Filippovich L. Molecular docking of 5-(2hydroxybenzylidene)pyrimidine-2,4,6(1h,3h,5h)-trione with a crystal structure of the
protein complex 7d2s // 11-ая Международная научная конференция молодых ученых,
студентов, магистрантов и аспирантов “Актуальные экологические проблемы”:
Материалы междунар. конф., Минск, 2021. – С. 136 – 137.
Syrytskii I., Shahab S., Pyrko A., Filippovich L. Antioxidant activities of the 5-(2hydroxybenzylidene)pyrimidine-2,4,6(1h,3h,5h)-trione // 11-ая Международная научная
конференция молодых ученых, студентов, магистрантов и аспирантов “Актуальные
экологические проблемы”: Материалы междунар. конф., Минск, 2021. – С. 137 – 138.
Syrytskii I., Shahab S., Linnik V., Pyrko A., Filippovich L. Antioxidant activity (z)-4-(2hydroxybenzilidene)-3-methylisoxazol-5 (4h)–one // 11-ая Международная научная
конференция молодых ученых, студентов, магистрантов и аспирантов “Актуальные
экологические проблемы”: Материалы междунар. конф., Минск, 2021. – С. 138 – 139.
15
16. Список собственных публикаций, выполненных по теме курсовой работы
• Сырыцкий И.А. Квантово-химическое моделирование и антиоксидантная активностьновых антрахиноновых производных для фармацевтических применений // 1-ая
Международная научно-практическая конференция “Медико-биологические и
нутрициологические аспекты здоровьесберегающих технологий”: Материалы
междунар. конф., Кемерово, 2020. – С. 113 – 116.
• Шахаб С.Н., Сырыцкий И.А., Казаков Р.В., Пырко А.Н. Молекулярный докинг
производного декагидроакридиндиона с кристаллической структурой протеазы
дикого типа ВИЧ-1 5COK // 4-ая Международная научно-практическая конференция
“Организм и среда жизни”: Материалы международн. конф., Кемерово, 2021. – С.
360 – 366.
• Казаков Р.В., Кашаева А.А., Сиротина К.А, Кравченко В.С., Сологуб Е.В.,
Сырыцкий И.А. Физическая сорбция между молекулой сульфорафана и нанотрубкой
B-N (15-15-8) // 1-ая Международная научно-практическая конференция “Медикобиологические и нутрициологические аспекты здоровьесберегающих технологий”:
16
Материалы междунар. конф., Кемерово, 2020. –С.48–52.