Similar presentations:
Фотобиологические процессы
1.
Фотобиологическиепроцессы
Демакин В.А. и Самычева М.С.
2.
Классификация фотобиологическихпроцессов
Свет выполняет две важных функции в живых системах:
Энергетическую – обеспечение живых систем энергией от Солнца, и
информационную – обеспечение взаимодействия живых систем с
окружающей средой.
3.
С энергетической точки зренияПо характеру использования энергии света все процессы делятся на
эндэргонические – при которых энергия света превращается в энергию
химических связей с высоким запасом свободной энергии, и экзэргонические –
при которых большая часть энергии рассеивается в тепло, а часть энергии
используется для преодоления активационного барьера.
4.
С биологической точки зренияПо значению процессы делятся на: физиологические – аккумуляция энергии,
реакции синтеза, активного транспорта, фотоинформационные и
фоторегуляционные процессы;
деструктивно-модификационные – повреждение и модификация молекул
биологического объекта.
5.
ВСЕ ФОТОБИОЛОГИЧЕСКИЕ ПРОЦЕССЫПРОТЕКАЮТ ПО ОБЩЕЙ СХЕМЕ:
1. Поглощение света молекулой
Не все молекулы поглощают свет, поглощается свет не любой длины волны и не
всеми атомными группами молекулы. Атомные группы, поглощающие свет
определённой длины волны – хромофорные группы. Наиболее хорошо
поглощают свет группы с делокализованными π-электронами в длинных цепях
сопряжения. Эти электроны могут легко переходить на более высокие
энергетические уровни. Процесс релаксации делокализованных электронов
наиболее долгий. После поглощения кванта света хромофорная группа
переходит на более высокое энергетическое состояние.
6.
2. Деактивация возбужденного состояния·
Внутримолекулярная инверсия. Молекула может вернуться
на более низкий энергетический уровень с излучением теплоты или теплоты и
флуоресценции.
·
Фотохимическая реакция. Уровень энергии возбуждённого
состояния превышает энергетический барьер разрыва химических связей, это
приводит к протеканию химической реакции.
·
Миграция энергии и Конформационные превращения. При
этом может происходить миграция энергии к другим атомным группам или
молекулам, что сопровождается изменениями конформации.
7.
3. Проявление специфическогофотобиологического процесса
Например, перенос протона, регуляторный акт,
изменение проницаемости мембран,
биосинтез.
8.
Воздействие света разных длин волнвызывает разные фотобиологические
эффекты:
Ультрафиолет - эритема, загар и рак кожи
Видимый свет - зрение, фототропизм, фототаксис, фотопериодизм
Инфракрасное излучение - тепловое излучение, терапевтические
эффекты красного света
9.
ЭНЕРГЕТИЧЕСКИЕ УРОВНИ АТОМОВ ИМОЛЕКУЛ
СИНГЛЕТНЫЕ УРОВНИ S(электроны спаренные)
S1 и S2 - возбужденные синглетные уровни
So –основной синглетный уровень
СИНГЛЕТНЫЕ S и ТРИПЛЕТНЫЕ(электроны не спаренные)
УРОВНИ Т
10.
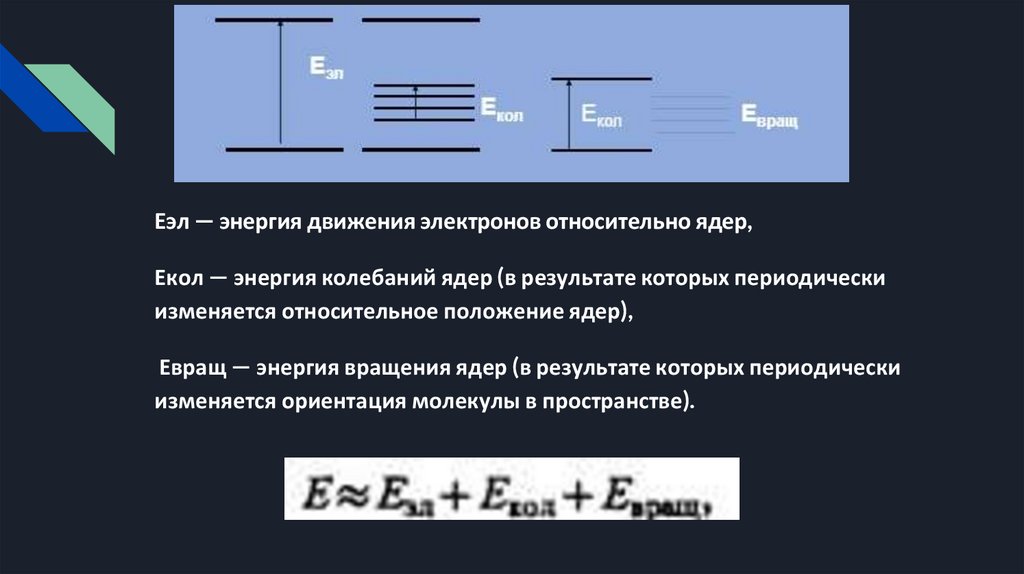
Еэл — энергия движения электронов относительно ядер,Екол — энергия колебаний ядер (в результате которых периодически
изменяется относительное положение ядер),
Евращ — энергия вращения ядер (в результате которых периодически
изменяется ориентация молекулы в пространстве).
11.
Спектры поглощения биомакромолекулСпектры макромолекул, в том числе биомолекул, не проанализированы
детально, ввиду сложности их электронной структуры. Однако это не
мешает с успехом использовать оптическую спектроскопию во многих
научных дисциплинах.
12.
Многие биологически важные соединения, имеющие двойные сопряженныесвязи, поглощают в ближнем ультрафиолетовом и видимом диапазонах,
причем, чем больше в молекуле число сопряженных двойных связей, тем
больше длина волны максимума поглощения данного вещества.
Характеристики спектров поглощения биомолекул позволяют качественно и
количественно идентифицировать вещества, исследовать механизмы
биохимических реакций, особенности взаимодействия белков с лигандами,
получать информацию об особенностях строения хромофорных групп,
активности простетических центров белковых молекул.
13.
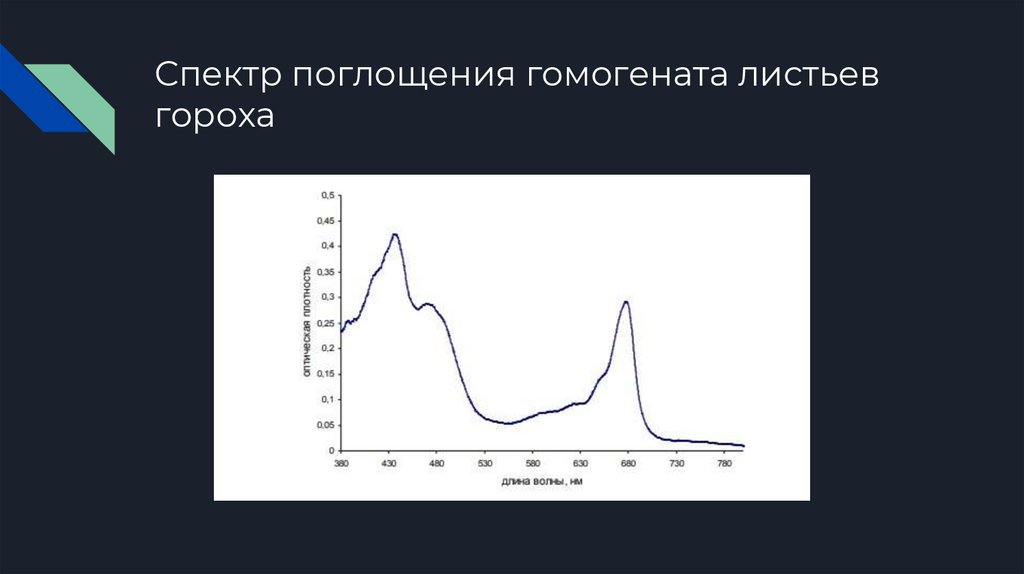
Спектр поглощения гомогената листьевгороха
14.
На рисунке приведены спектральные характеристики хлорофилла всоставе гомогената листьев гороха, молекулы которого обладают
обширной делокализованной π-электронной системой (система
сопряженных связей). Спектр представляет собой сложную систему
полос и плеч и является суперпозицией спектров поглощения
хлорофиллов а и b.
15.
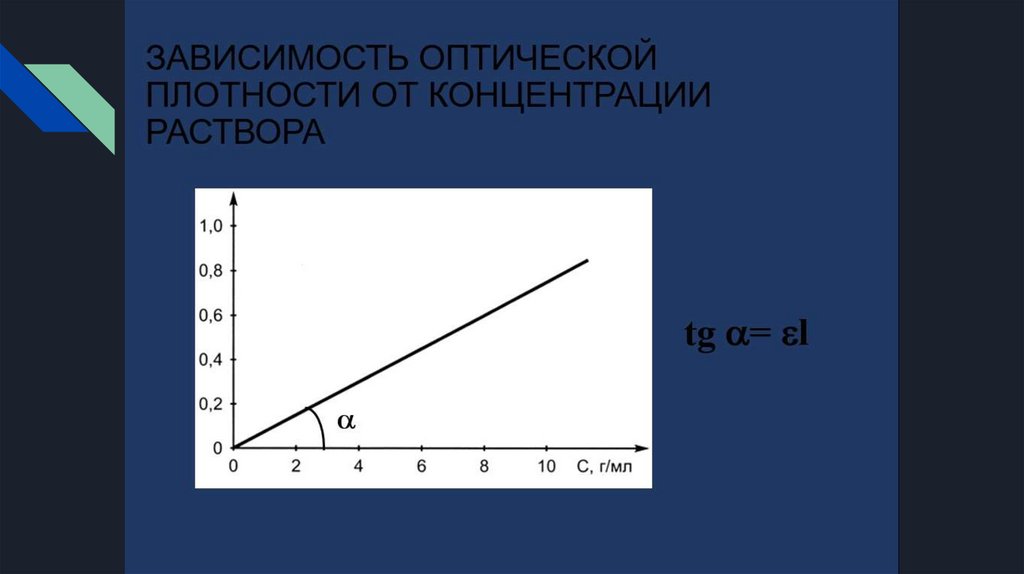
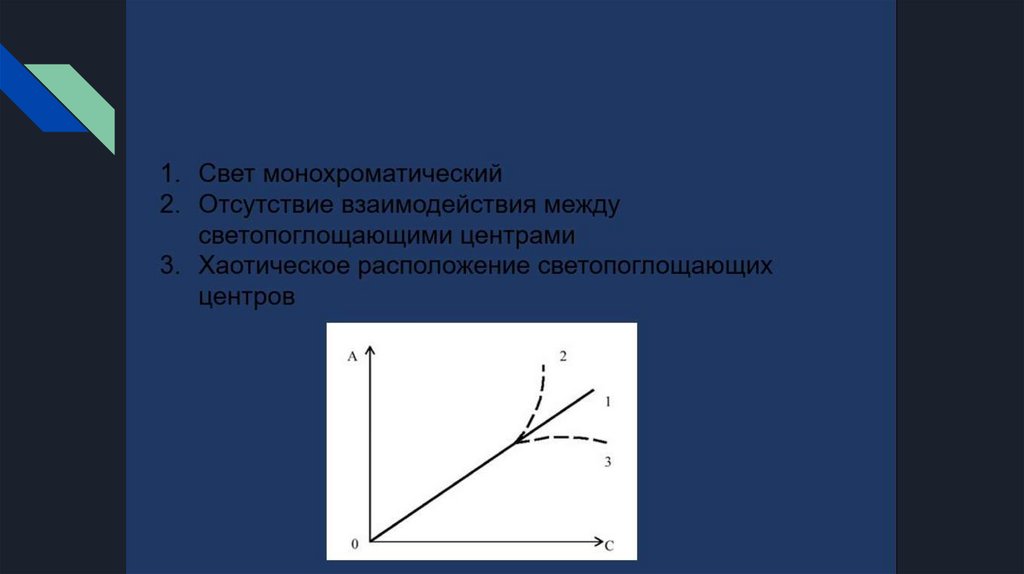
ЗАКОН БУГЕРА – ЛАМБЕРТА – БЕРА 16.
17.
18.
19.
20.
21.
22.
23.
Поглощение белковДля рассмотрения поглощения белков возьмем в
пример гемоглобин
24.
25.
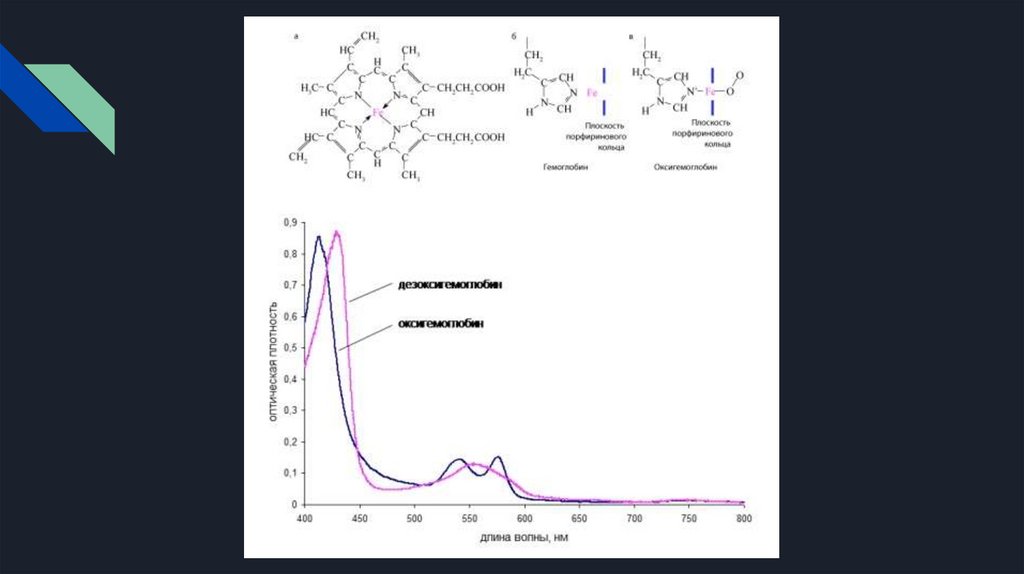
На рисунке представлена структурная формула хромофорной группы белкагемоглобина (гема) и спектры поглощения гемоглобина и оксигемоглобина. Из
рисунка видно, что связывание Fe(II) с молекулой кислорода (связь
нековалентная) приводит к характерным изменениям спектра поглощения:
коротковолновый максимум смещается в еще более коротковолновую
область, а в длинноволновой области видимого диапазона вместо одного
максимума (555 нм) появляется два (540 и 576 нм). Характерные особенности
спектров поглощения гемоглобина и оксигемоглобина широко используются
для количественной оценки степени насыщения гемоглобина кислородом.
26.
ПОГЛОЩЕНИЕ АМИНОКИСЛОТНЫХОСТАТКОВ
Для боковых групп многих аминокислот (Asp, Glu, Asn, Gln, Arg и His)
зарегистрировать электронные переходы в белках или полипептидах
практически нельзя.
ПРИЧИНЫ
Эти электронные переходы маскируются интенсивным поглощением
пептидной группы.
Они уступают по интенсивности электронному переходу пептидной
группы
Число соответствующих боковых радикалов обычно меньше, чем число
пептидных групп.














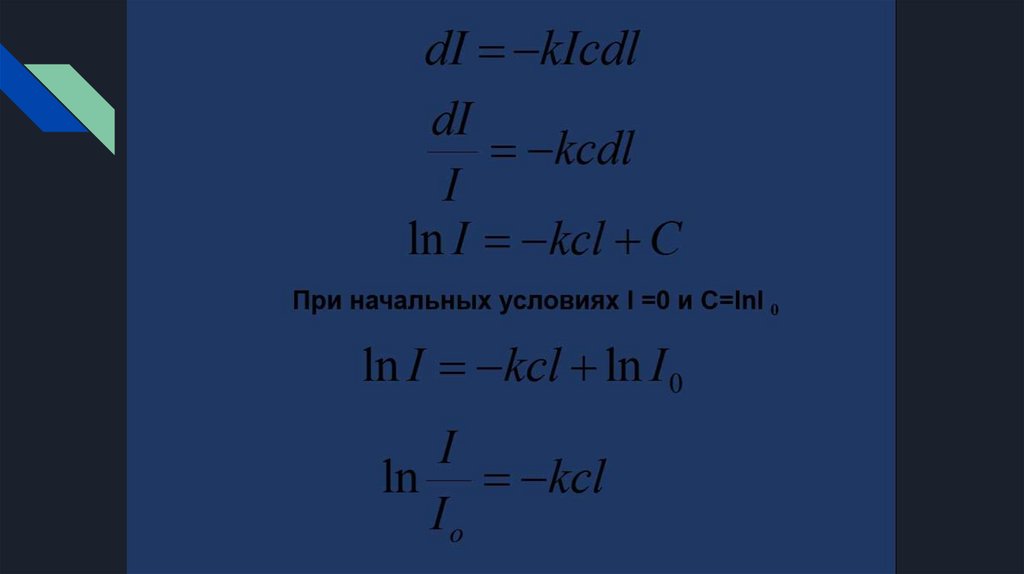






 physics
physics








