Similar presentations:
Общая характеристика генома человека
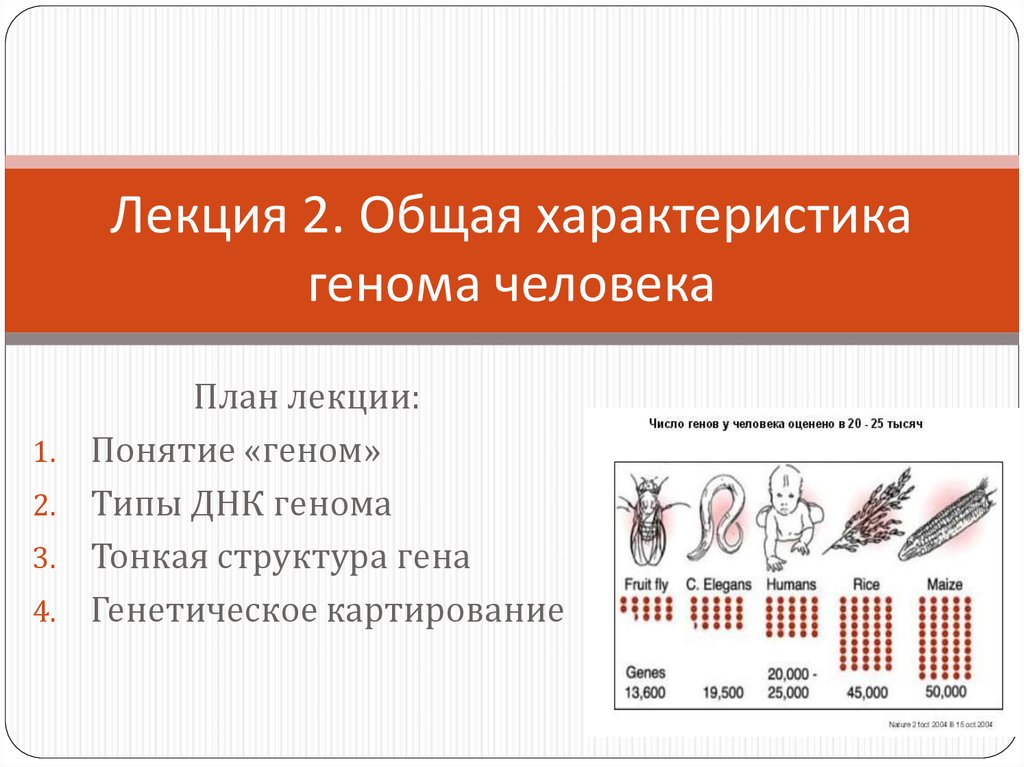
1. Лекция 2. Общая характеристика генома человека
1.2.
3.
4.
План лекции:
Понятие «геном»
Типы ДНК генома
Тонкая структура гена
Генетическое картирование
2. Задание на практические занятия
Классификации генов вгенотипе человека
конспект:
«Классификации
генов в генотипе»
Устные ответы:
1) Структурные гены,
особенности
строения и роль
2) Функциональные
гены – особенности
строения и роль
Взаимодействие генов
Конспект: «Виды
взаимодействия
генов, примеры у
человека»
Устные ответы:
1) взаимодействие
аллельных генов
2) взаимодействие
неаллельных генов
3. Терминология
1920 г. - Г. Винклер – термин «геном»(совокупность генов в гаплоидном наборе –
характеристика целого вида организмов)
“ГЕНОМ” – СОВОКУПНОСТЬ СБАЛАНСИРОВАННЫХ по БАЗОВОЙ
БИОИНФОРМАЦИИ ГЕНОВ, ОПРЕДЕЛЯЮЩИХ во
ВЗАИМОДЕЙСТВИИ ВИДОСПЕЦИФИЧНЫЕ ТИПЫ ОБМЕНА
ВЕЩЕСТВ и ОНТОГЕНЕЗА
«ГЕНОТИП» – ОПРЕДЕЛЯЕТ ИНДИВИДУАЛЬНОЕ
(ВНУТРИВИДОВОЕ) РАЗНООБРАЗИЕ ОСОБЕЙ по СОДЕРЖАНИЮ и
ДОЗАМ ОТДЕЛЬНЫХ “КВАНТОВ” БИОИНФОРМАЦИИ,
ИНСТРУМЕНТ СОЗДАНИЯ РЕЗЕРВА НАСЛЕДСТВЕННОЙ
ИЗМЕНЧИВОСТИ;
“КАРИОТИП” ОТРАЖАЕТ СПОСОБ СТРУКТУРНОГО ОФОРМЛЕНИЯ
ГЕНОМОВ и ГЕНОТИПОВ у ЭУКАРИОТ;
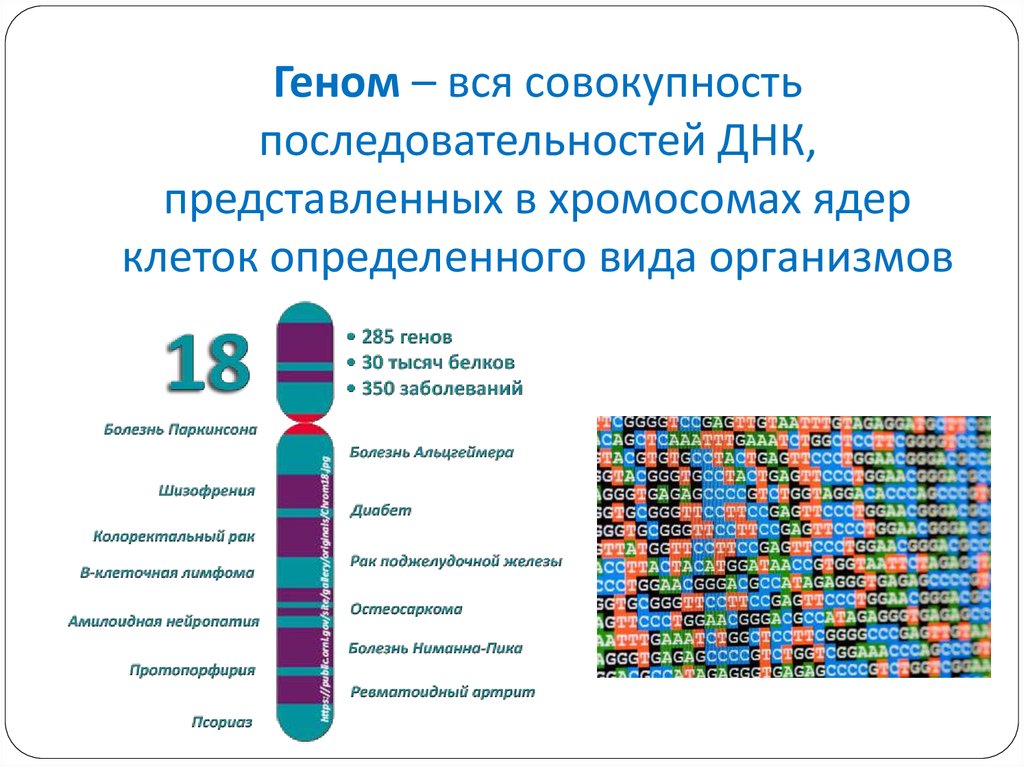
4. Геном – вся совокупность последовательностей ДНК, представленных в хромосомах ядер клеток определенного вида организмов
5. ГЕНОМЫ ЧЕЛОВЕКА и ДРУГИХ ВИДОВ ЖИВОТНЫХ (СРАВНИТЕЛЬНО-ЭВОЛЮЦИОННЫЙ АСПЕКТ)
В ГЕНОМЕ ЧЕЛОВЕКА есть ГЕНЫ:= ОБЩИЕ для ПРО- и ЭУКАРИОТ – 21%;
= ОБЩИЕ для ЖИВОТНЫХ и др. ЭУКАРИОТ – 32%;
= ОБЩИЕ для ПОЗВОНОЧНЫХ и др. ЖИВОТНЫХ – 24%;
= ОБЩИЕ для ПОЗВОНОЧНЫХ – 22%;
= ОБЩИЕ для ПРИМАТОВ – 90-99%;
В ГЕНОМЕ ЧЕЛОВЕКА есть ДНК от:
= РЕТРОТРАНСПОЗОНОВ (РНК ВИРУСОВ) – 8%;
= ДНК ТРАНСПОЗОНОВ (БАКТЕРИАЛЬНЫХ) – 3%;
= еще 220 ГЕНОВ от БАКТЕРИЙ-СИМБИОНТОВ, ВКЛЮЧАЯ ГЕН МАО;
ГИПОТЕЗА – эти ГЕНЫ ИНТРОДУЦИРОВАНЫ в ГЕНОМ ГОМИНИДА
ПРИШЕЛЬЦАМИ из КОСМОСА для ПРЕВРАЩЕНИЯ в РАБОЧУЮ СИЛУ; от
ЧЕЛОВЕКА – ГЕНЫ ДОСТАЛИСЬ БАКТЕРИЯМ-СИМБИОНТАМ;
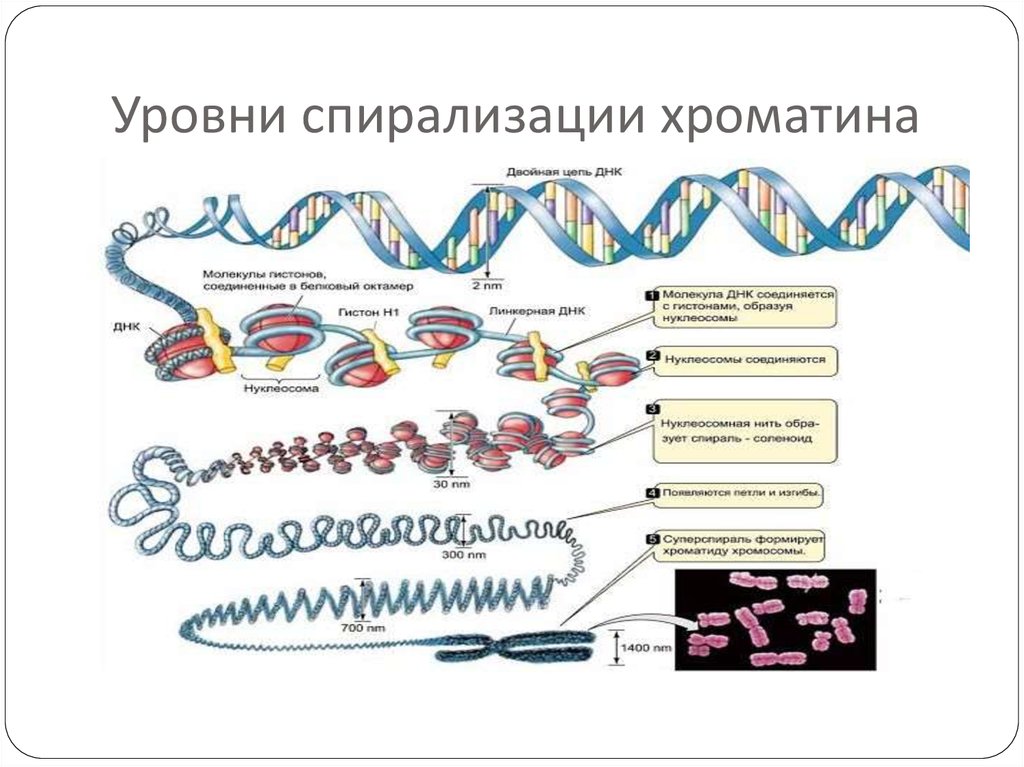
6. Уровни спирализации хроматина
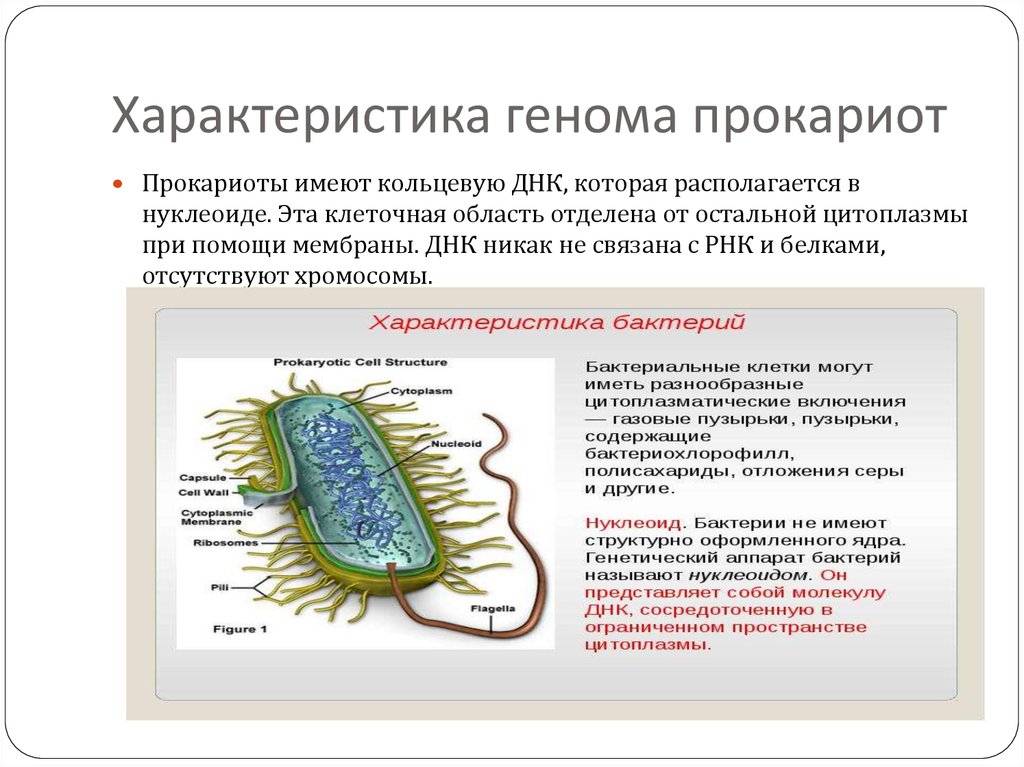
7. Характеристика генома прокариот
Прокариоты имеют кольцевую ДНК, которая располагается внуклеоиде. Эта клеточная область отделена от остальной цитоплазмы
при помощи мембраны. ДНК никак не связана с РНК и белками,
отсутствуют хромосомы.
8. Геном вируса
9. В-2. ДНК-уровень
Ядерная ДНК (95%)73% однокопийные
гены
Интроны, молчащие
гены,
последовательности
между генами
2% структурные
гены
Кодируют структуру
белков
25% повторяющиеся
последовательности
Входят в состав
кодирующих
областей генов
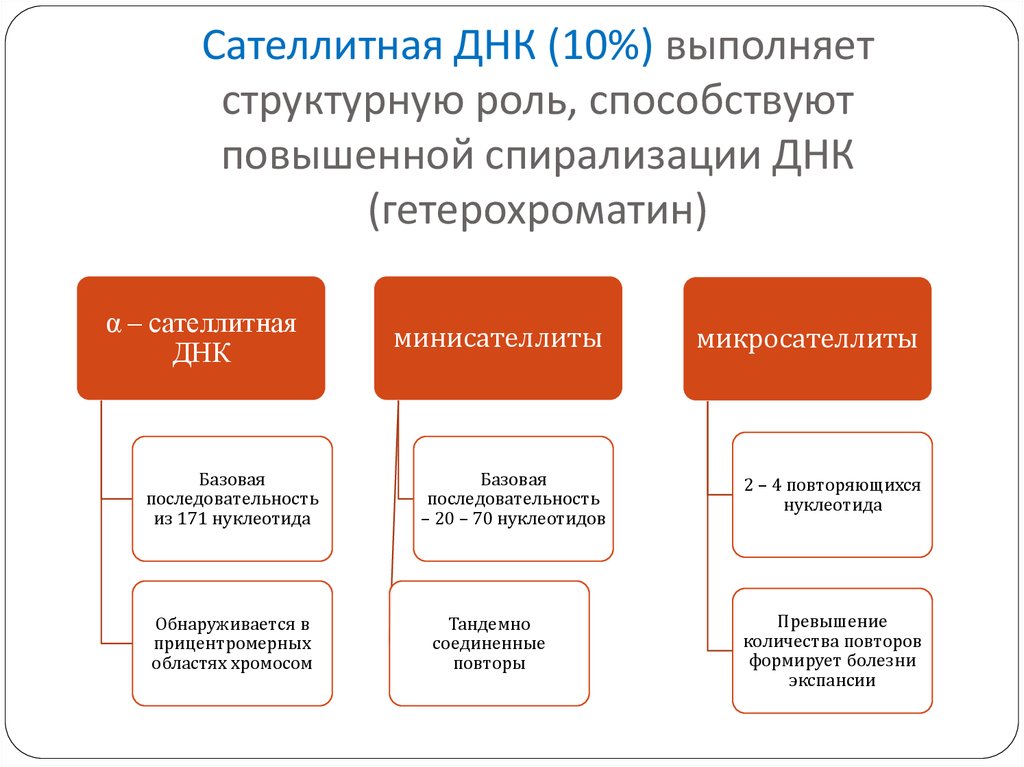
10. Сателлитная ДНК (10%) выполняет структурную роль, способствуют повышенной спирализации ДНК (гетерохроматин)
α – сателлитнаяДНК
Базовая
последовательность
из 171 нуклеотида
Обнаруживается в
прицентромерных
областях хромосом
минисателлиты
микросателлиты
Базовая
последовательность
– 20 – 70 нуклеотидов
2 – 4 повторяющихся
нуклеотида
Тандемно
соединенные
повторы
Превышение
количества повторов
формирует болезни
экспансии
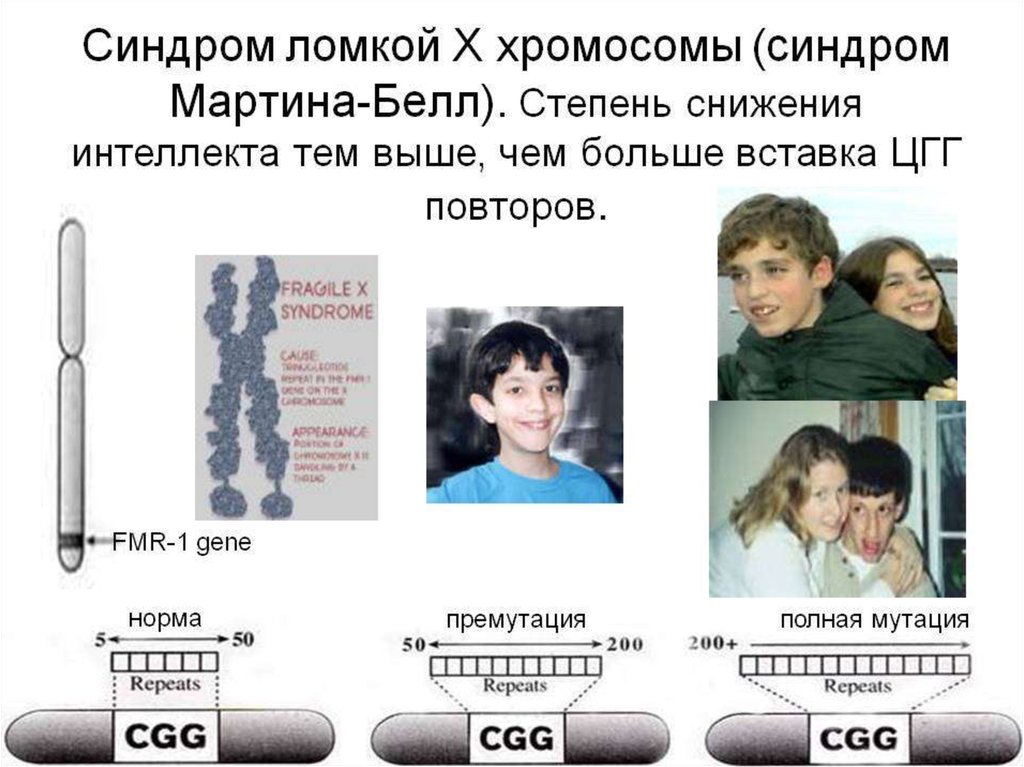
11. Болезни экспансии
К болезням экспансииотносятся наследственные
заболевания, обусловленные
динамическими мутациями. В
основе динамических мутаций
лежит нестабильность микрои минисателлитных повторов
ДНК, локализованных в
значимых областях генов. При
болезнях экспансии
наблюдается превышение
(экспансия) определенного
порогового уровня числа
повторяющихся элементов в
месте локализации
динамической мутации.
Подобные экспансии
сопровождаются нарушениями
работы гена.
В настоящее время
насчитывается более 20
болезней экспансии,
подавляющее большинство из
них связаны с экспансией
тринуклеотидных повторов.
Это синдром Мартина-Белл
(синдром фрагильной или
ломкой Х-хромосомы),
миотоническая дистрофия,
атаксия Фридрейха, целая
серия спиноцеребеллярных
атаксий, хорея Гентингтона и
ряд других. Болезни экспансии
могут быть аутосомными или
Х-сцепленными в зависимости
от локализации мутантного
гена.
12.
13. Болезни экспансии
У некоторых больныхУ некоторых больных
синдромом Ушера
(Ашера)
идентифицирована
инсерция Aluповторов в 9 экзоне
гена рецептора 2-го
фибробластного
фактора роста.
миодистрофией
Дюшенна удалось
проследить
присутствие Aluповторов в точке
разрыва,
образованного
делецией гена DMD.
14. Синдром Ашера (Ушера)
Синдром Ашера - это сочетаниеврожденной нейросенсорной
тугоухости, медленно
прогрессирующей пигментной
дегенерации сетчатки (начало на
первом или втором десятилетии
жизни) и вестибулярных
расстройств. Также наблюдаются
глаукома, катаракта, нистагм,
задержка умственного развития,
психозы. Встречается у 1 из 6000
детей. Выделяют три типа синдрома:
I тип – врожденные глубокая
тугоухость и нарушение
вестибулярных функций, раннее
начало пигментного ретинита;
II тип – позднее начало пигментной
дегенерации сетчатки и сохранность
вестибулярных функций;
III тип – доброкачественный,
встречается редко и характеризуется
медленным усугублением
нарушений зрения и слуха.
15.
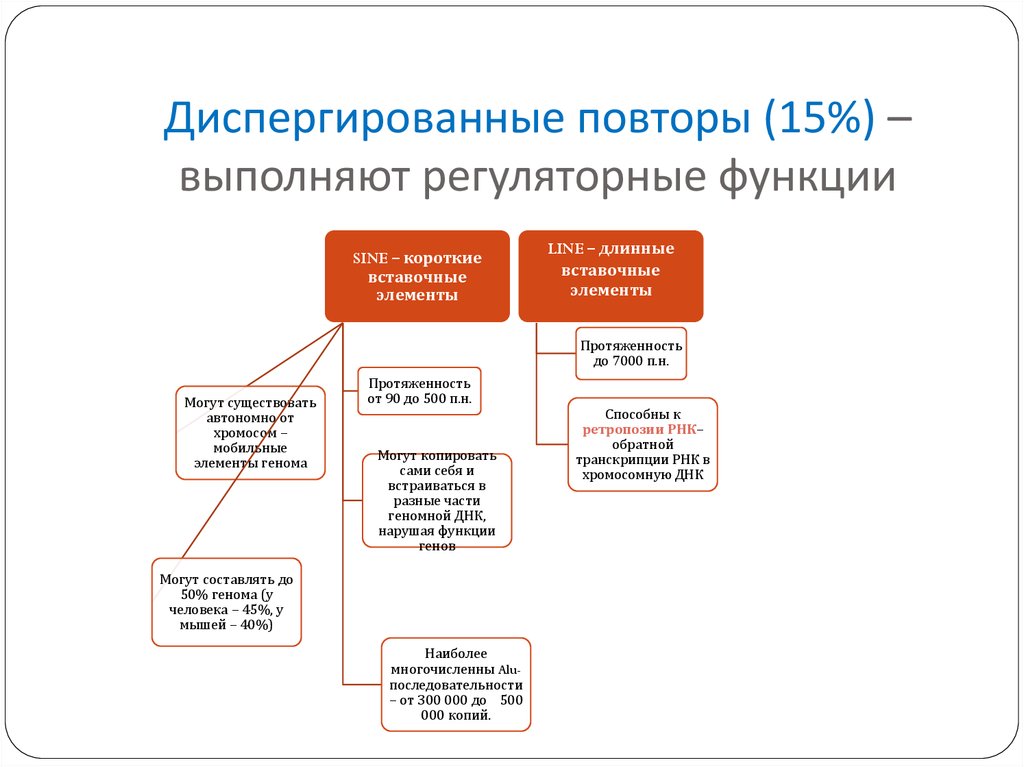
16. Диспергированные повторы (15%) – выполняют регуляторные функции
SINE – короткиевставочные
элементы
LINE – длинные
вставочные
элементы
Протяженность
до 7000 п.н.
Могут существовать
автономно от
хромосом –
мобильные
элементы генома
Протяженность
от 90 до 500 п.н.
Могут копировать
сами себя и
встраиваться в
разные части
геномной ДНК,
нарушая функции
генов
Могут составлять до
50% генома (у
человека – 45%, у
мышей – 40%)
Наиболее
многочисленны Aluпоследовательности
– от 300 000 до 500
000 копий.
Способны к
ретропозии РНК–
обратной
транскрипции РНК в
хромосомную ДНК
17. Гипотезы о роли интронов
1.2.
3.
Внутри интронных областей одних генов могут
располагаться экзоны других генов,
«прочитывающихся» в противоположном
направлении;
В интронных областях есть «дополнительные»
промоторы, которые способны запускать синтез РНК с
разных точек гена (альтернативная транскрипция);
Альтернативный сплайсинг – вырезание разных
интронов из одной и той же молекулы гяРНК – в
результате образуются разные мРНК
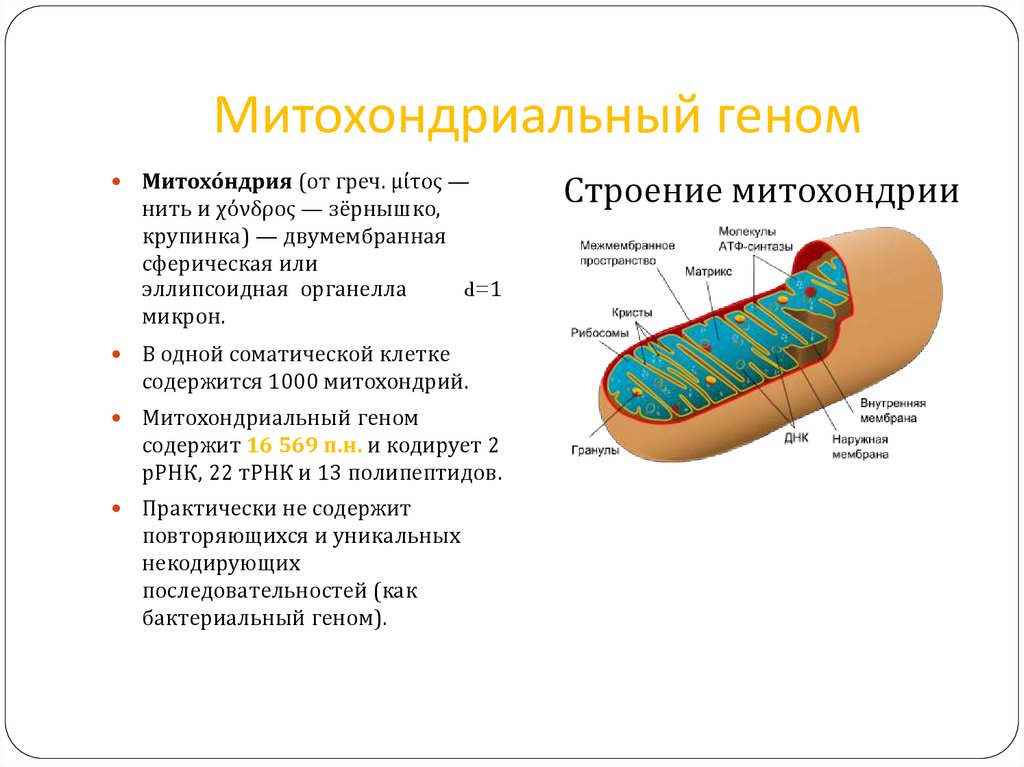
18. Митохондриальный геном
Митохо́ ндрия (от греч. μίτος —нить и χόνδρος — зёрнышко,
крупинка) — двумембранная
сферическая или
эллипсоидная органелла
d=1
микрон.
В одной соматической клетке
содержится 1000 митохондрий.
Митохондриальный геном
содержит 16 569 п.н. и кодирует 2
рРНК, 22 тРНК и 13 полипептидов.
Практически не содержит
повторяющихся и уникальных
некодирующих
последовательностей (как
бактериальный геном).
Строение митохондрии
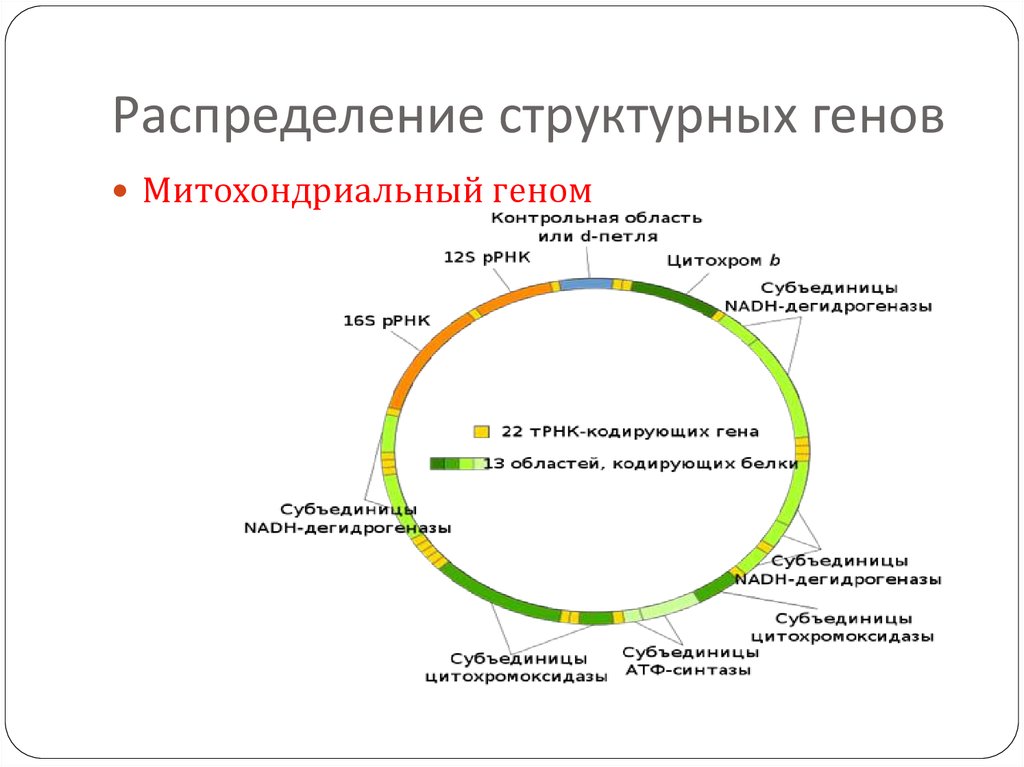
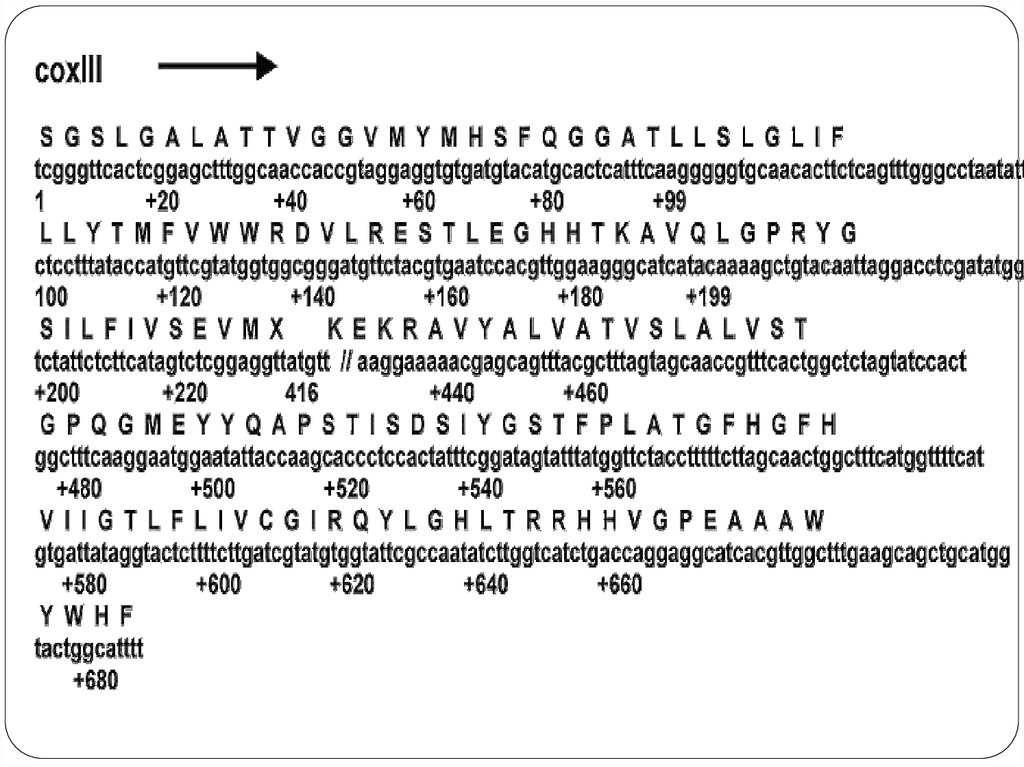
19. Распределение структурных генов
Митохондриальный геном20. Особенности митохондриального генома
1) мтДНК наследуется по материнскому типу (доля отцовскихмитохондрий в зиготе – от 0 до 4, материнских – до 2500 после
оплодотворения репликация отцовских митохондрий блокируется);
2) комбинативная изменчивость (мейоз) отсутствует (мтДНК меняется
только в результате мутаций);
3) митохондриальный геном непрерывен, он практически не содержит
интронов (известен один интрон - -около 1000 нукеотидов);
4) в мтДНК нет гистонов и отсутствует система репарации ДНК
(высокая скорость мутирования);
5) внутри одной клетки могут функционировать митохондрии с
разными типами мтДНК – гетероплазмия;
6) в мтДНК транскрибируются обе цепи, причем код мтДНК несколько
отличается от ядерного;
7) мутации мтДНК лежат в основе митохондриальных болезней,
отличающихся от моногенных болезней не только особенностями
передачи из поколения в поколения по материнской линии. Но и
общими признаками клинической картины.
21. Митохондриальные болезни
Описаны различные сочетания следующихклинических признаков:
1)
повторные коматозные состояния,
сопровождающиеся ацидозом крови и
увеличением концентрации кетоновых
тел;
2)
задержка физического развития, нанизм;
3)
дисфункция щитовидной железы;
4)
симптомы поражения различных отделов
нервной системы (судороги, атаксия,
полинейропатия, изменение мышечного
тонуса и др.);
5)
миопатии и кардиомиопатии;
6)
витамин-D-резистентный рахит;
7)
диарея, целиакие-подобный синдром;
8)
печеночная недостаточность;
9)
атрофия зрительных нервов;
10) панцитопения, анемия.
Митохондриальные заболевания передаются только по
женской линии к детям обоих полов.
Патологические нарушения клеточного
энергетического обмена могут проявляться в виде
дефектов различных звеньев в цикле Кребса,
дыхательной цепи, в процессах окисления.
Не все ферменты и другие регуляторы, необходимые для
эффективного функционирования митохондрий,
кодируются митохондриальной ДНК. Большая часть
митохондриальных функций контролируется
ядерной ДНК.
Можно выделить две группы митохондриальных
заболеваний:
Ярко выраженные наследственные синдромы,
обусловленные мутациями генов, ответственных за
митохондриальные белки (синдром Барта, синдром
Кернса -Сейра и другие).
Вторичные митохондриальные заболевания,
включающие нарушение клеточного энергообмена
как важное звено формирования
патогенеза (болезни соединительной ткани,
синдром хронической усталости, кардиомиопатия,
мигрень, печеночная недостаточность и другие).
22. Геном как единое целое
Несмотря на дискретное генетическое определение отдельныхпризнаков, в индивидуальном развитии воссоздается единый
сбалансированный комплекс признаков и свойств,
соответствующий типу морфофункциональной организации
конкретного биологического вида.
Генные взаимодействия происходят на нескольких уровнях: 1.
непосредственно в генетическом материале клеток, 2. между
иРНК и образующимися полипептидами в процессе
биосинтеза белка, 3. между белками-ферментами одного
метаболического цикла.
Типы взаимодействия аллельных и неаллельных генов.
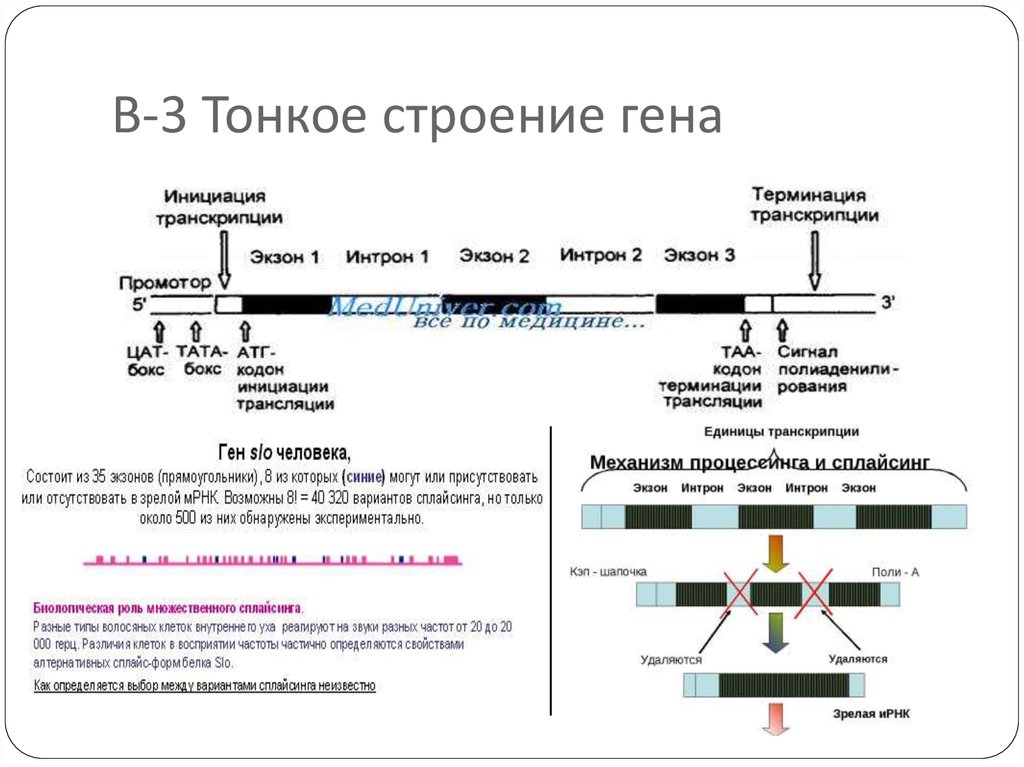
23. В-3 Тонкое строение гена
24.
25.
26.
27.
28. Регуляторные зоны
Регуляторные зоны - это участки ДНК на которых непроисходит синтез РНК, но которые служат местом
связывания различных белков (или РНК). Эти
последовательности часто
называют регуляторными зонами ( или
регуляторные области, элементы, структуры,
участки и др.).
Большинство учёных приходит к мнению, что
наименьшей функциональной областью в ДНК
является совокупность нуклеотидов, состоящая из
структурного гена, регуляторных зон и
регуляторных генов.
29. Регуляторные участки гена содержат:
А. Стартовый кодон – сайт (место) начала транскрипции(распознает фермент).
Б. Промотор (прикрепляется фермент)
В. Контролирующие зоны располагаются вблизи от
обслуживаемого гена (лидерную последовательность,
трейлерную последовательность).
Г. Модуляторы (энхансеры, сайленсеры) – располагаются
вдали от гена.
Д. Терминатор – сайт окончания транскрипции.
Промотор - лидер - кодирующая
последовательность – трейлер - терминатор
30.
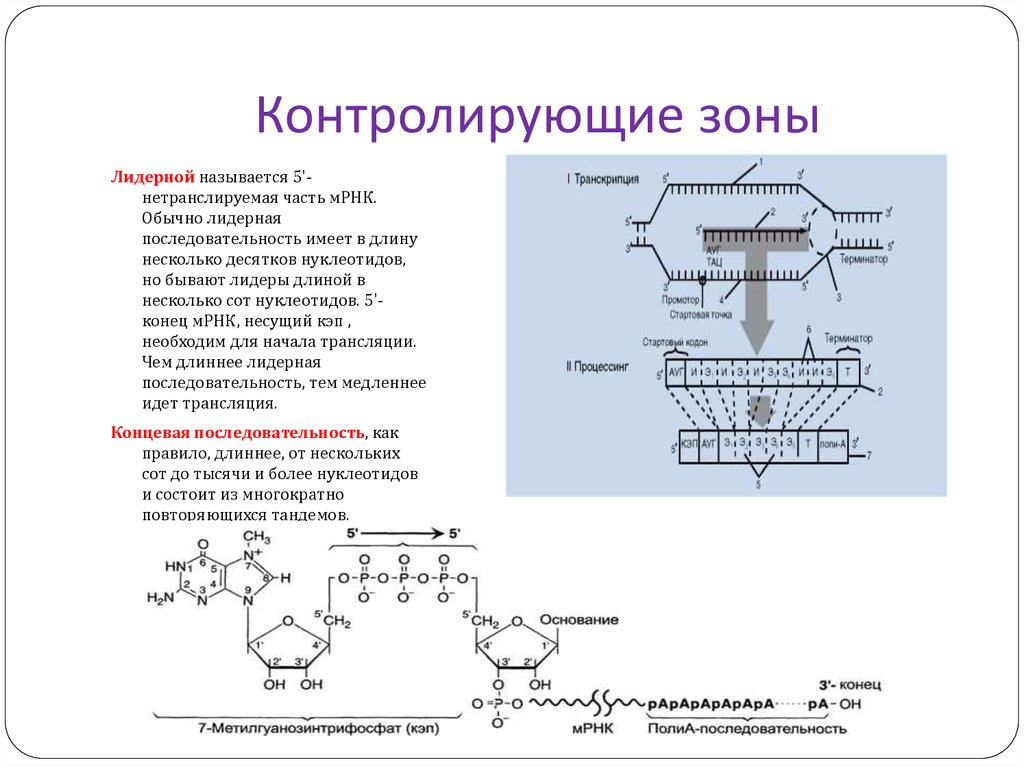
31. Контролирующие зоны
Лидерной называется 5'нетранслируемая часть мРНК.Обычно лидерная
последовательность имеет в длину
несколько десятков нуклеотидов,
но бывают лидеры длиной в
несколько сот нуклеотидов. 5'конец мРНК, несущий кэп ,
необходим для начала трансляции.
Чем длиннее лидерная
последовательность, тем медленнее
идет трансляция.
Концевая последовательность, как
правило, длиннее, от нескольких
сот до тысячи и более нуклеотидов
и состоит из многократно
повторяющихся тандемов.
32. Функции контролирующих зон
Лидерная последовательностьтранскрибируется, но не
транслируется, и может
регулировать возможность
самого процесса транскрипции.
В случае необходимости
«выключения» транскрипции
мРНК в области лидерной
последовательности образуется
«шпилька» и процесс
транскрипции не идет.
Трейлерная
последовательность
транскрибируется и служит
сигналом
формирования
поли-(А) –
хвостика при
созревании
мРНК.
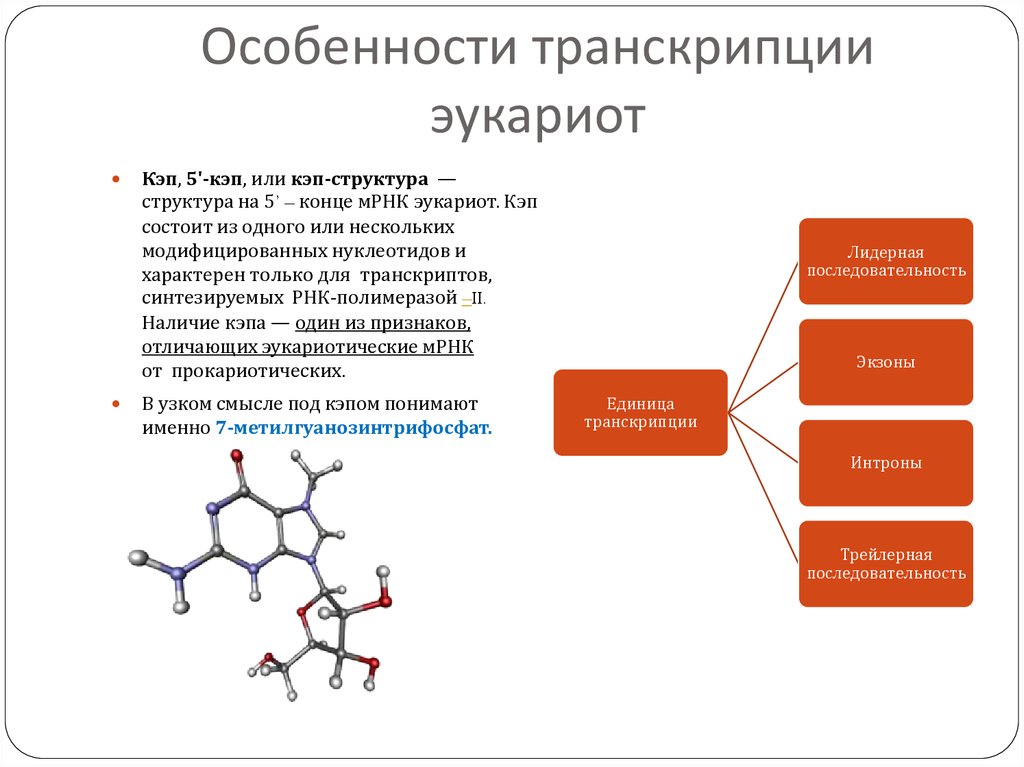
33. Особенности транскрипции эукариот
Кэп, 5'-кэп, или кэп-структура —структура на 5’ – конце мРНК эукариот. Кэп
состоит из одного или нескольких
модифицированных нуклеотидов и
характерен только для транскриптов,
синтезируемых РНК-полимеразой –II.
Наличие кэпа — один из признаков,
отличающих эукариотические мРНК
от прокариотических.
В узком смысле под кэпом понимают
именно 7-метилгуанозинтрифосфат.
Лидерная
последовательность
Экзоны
Единица
транскрипции
Интроны
Трейлерная
последовательность
34. Роль хвоста поли-(А)
Хвост поли-(А ) -полиаденильный хвост,
некодируемая поли (А) последовательность
эукариотических мРНК длиной
100-200 нуклеотидов,
присоединяемая в процессе
полиаденилирования.
Предполагается, что
полиаденильный хвост (наряду с
расположенным с 5’-конца кэпом
- белком-активатором
катаболитных оперонов)
обеспечивает более высокую
стабильность мРНК и ее защиту
от действия экзонуклеаз.
Полиаденилирование происходит
непосредственно после
терминации транскрипции.
Специальный фермент - poly(A)полимераза присоединяет к 3'концу каждого РНК-транскрипта,
от 100 до 200 остатков адениловой
кислоты (poly(A)), что завершает
процесс образования первичного
РНК-транскрипта.
Конкретные функции poly(A)
неизвестны, но считается, что
такой "хвост" способствует
последующему процессингу РНК и
экспорту зрелых молекул мРНК из
ядра.
35. ТАТА-бокс
TATA-бокс (бокс Хогнесса, TATA-box): у эукариот последовательность ДНК,богатая А – Т парами (ТAТA(A/Т)A(A/Т)), содержащая обычно 7 или 8
нуклеотидов, и расположенная приблизительно за 25 пар оснований перед
сайтом начала транскрипции.
Положение TATA-бокса строго определяет сайт инициации транскрипции , т.е. 5'конец транскрипта . При повреждении или удалении TATA-бокса образуется
набор молекул РНК с разными 5'-концами. Отдельные нуклеотидные замены в
TATA-бокса могут приводить к резкому снижению эффективности
транскрипции.
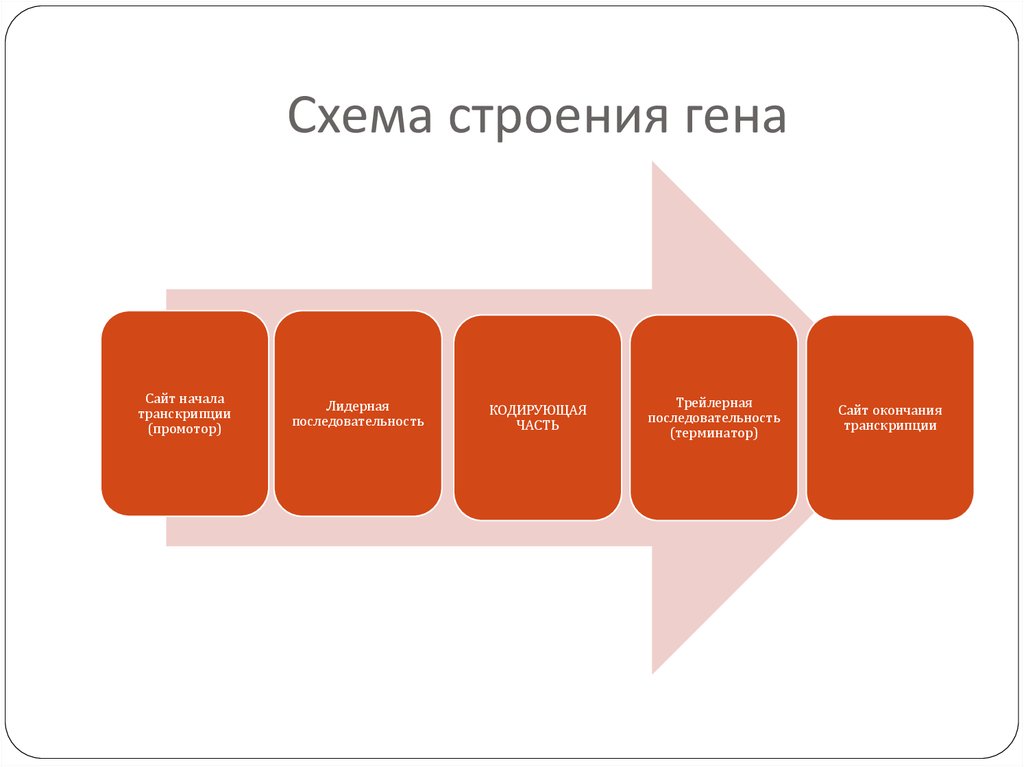
36. Схема строения гена
Сайт началатранскрипции
(промотор)
Лидерная
последовательность
КОДИРУЮЩАЯ
ЧАСТЬ
Трейлерная
последовательность
(терминатор)
Сайт окончания
транскрипции
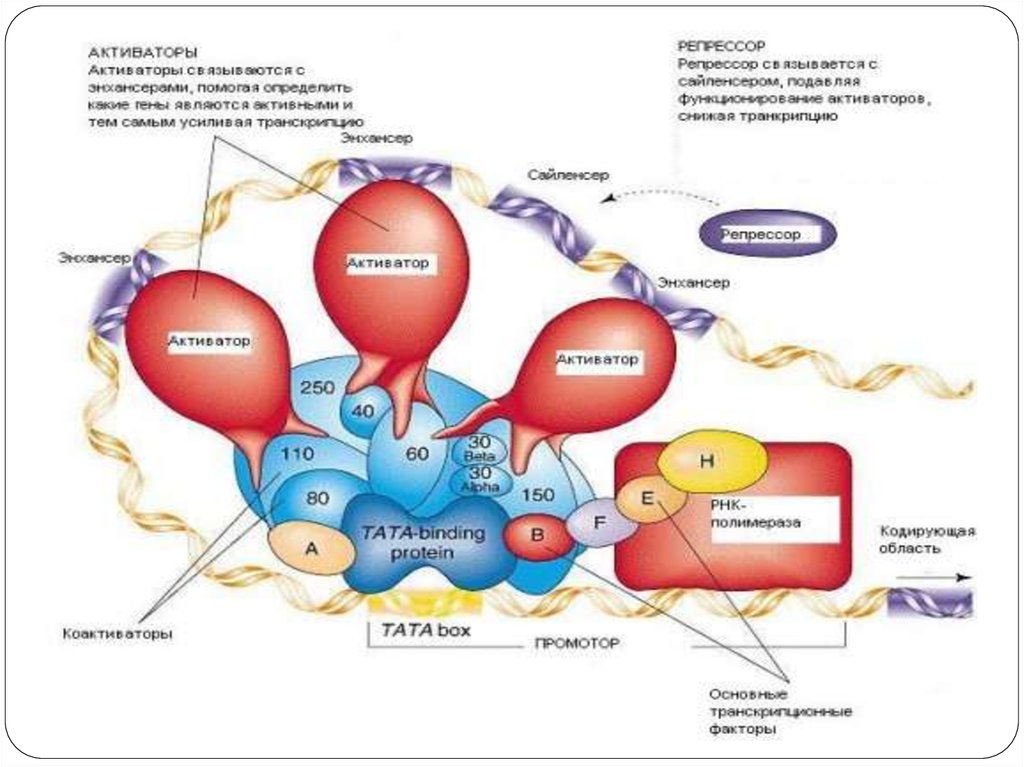
37. Виды регуляторных последовательностей
Образование комплекса транскрипции и его активность в свою очередь контролируютещё два типа белков-регуляторов. Первый тип белков осаждается на регуляторные
(зоны) последовательности ДНК, которые располагаются, как правило, рядом с
промотором. Эти белки ускоряют или тормозят образование транскрипционного
комплекса. Регуляторные последовательности имеют различные названия. Чаще всего их
объединяют термином – контролирующие зоны или цис-регуляторные элементы. К
этой зоне относится лидерная последовательность, промотор и регуляторные зоны,
располагающиеся рядом с промотором - рядом расположенные области. К
контролирующим зонам присоединяются различные регуляторные белки, которые
влияют на начальное связывание РНК-полимеразы с промотором. Эти белки носят
специальное название –факторы транскрипции.
Второй тип регуляторных последовательностей усиливает или тормозит движение
транскрипционного комплекса по гену. У эукариот эти участки часто расположены
далеко от контролируемого ими гена: - впереди от 5’- конца кодирующей области, но за
несколько тысяч пар нуклеотидов от кодирующего участка, в самой кодирующей области
или позади неё. В некоторых случаях их выявляют на других хромосомах. Как правило, на
этих областях, также как и на контролирующих зонах, осаждаются регуляторные белки
усиливающие или замедляющие транскрипцию. Эти регуляторные последовательности
настолько разнообразны по строению, положению и функциям, что для большинства из
них пока не найдено название. В последнее время некоторые учёные называют
их модуляторы или транс-регуляторные элементы.
К модуляторам относят энхансеры (усиливают транскрипцию с некоторых
эукариотических промоторов) и сайленсеры (обладают противоположным действием по
отношению к энхансерам), оказывающие дистанционное влияние на инициацию
транскрипции независимо от своей ориентации относительно кодирующей области.
38. Факторы транскрипции
РНК-полимераза эукариот не может самостоятельноинициировать транскрипцию. Для ее активации
необходимо большое количество белков, называемых
общими факторами транскрипции.
Для РНК-полимеразы-II выделено 6 факторов
транскрипции: TFIIA, TFIIB, TFIID, TFIIE, TFIIF, TFIIH.
В составе TFIID содеражатся белки TBP (TATA-box binding
protein).
В состав транскрипционного комплекса TFIIF входит 14
полипептидов, которые помогают РНК-полимеразе
разрушать нуклеосомы и декомпактизировать молекулу
ДНК.
39. Виды РНК-полимераз
• Считывает гены 18 S, 28 S, 5,8 Sрибосомных РНК
PHK I
PHK II
PHK III
• Считывает основную часть генов,
кодирующих полипептиды, и гены малых
РНК
• Считывает гены 5 S рибосомальных РНК,
гены транспортных РНК и малых РНК
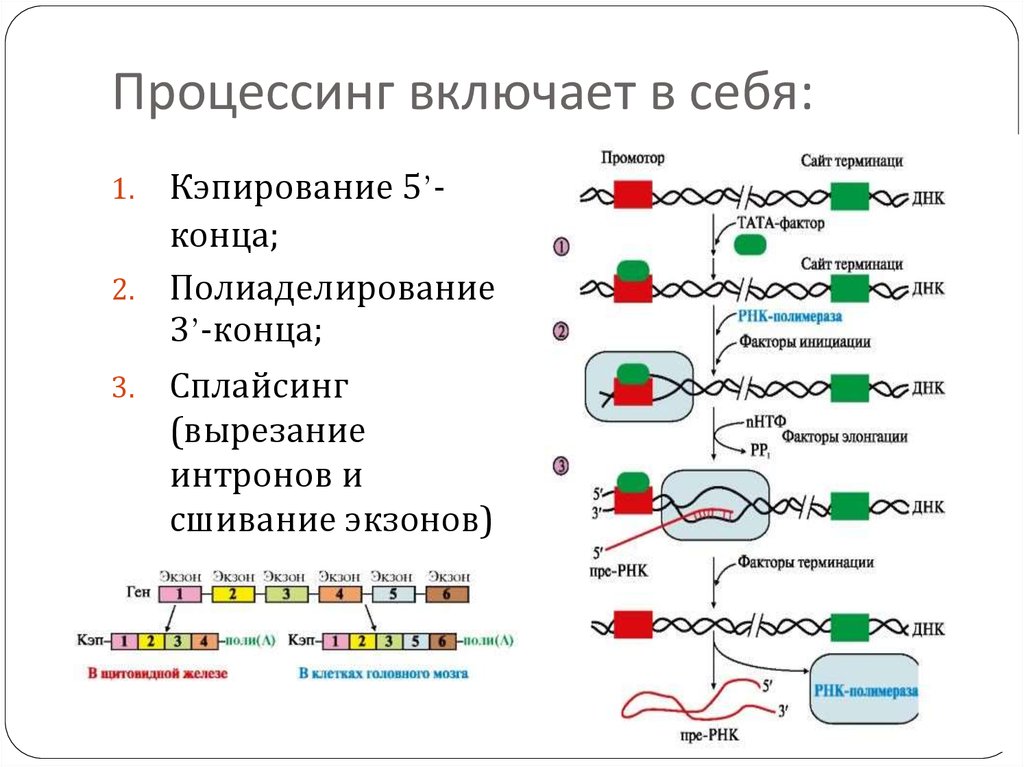
40. Процессинг включает в себя:
Кэпирование 5’конца;2. Полиаделирование
3’-конца;
1.
3.
Сплайсинг
(вырезание
интронов и
сшивание экзонов)
41.
42.
43. Экзон-интронная структура гена
Экзоны – от 100 до 600 п.н.,их несколько десятков в
гене.
Термины «экзон» и
«интрон» были введены У.
Гилбертом в 1978 г.
Интроны – имеют
длину от нескольких
десятков п.н. до
нескольких тысяч.
Составляют до 80%
материала ДНК.
Отделяются от
экзонов парой ГТ на
5’-конце и парой АГ
на 3’-конце.
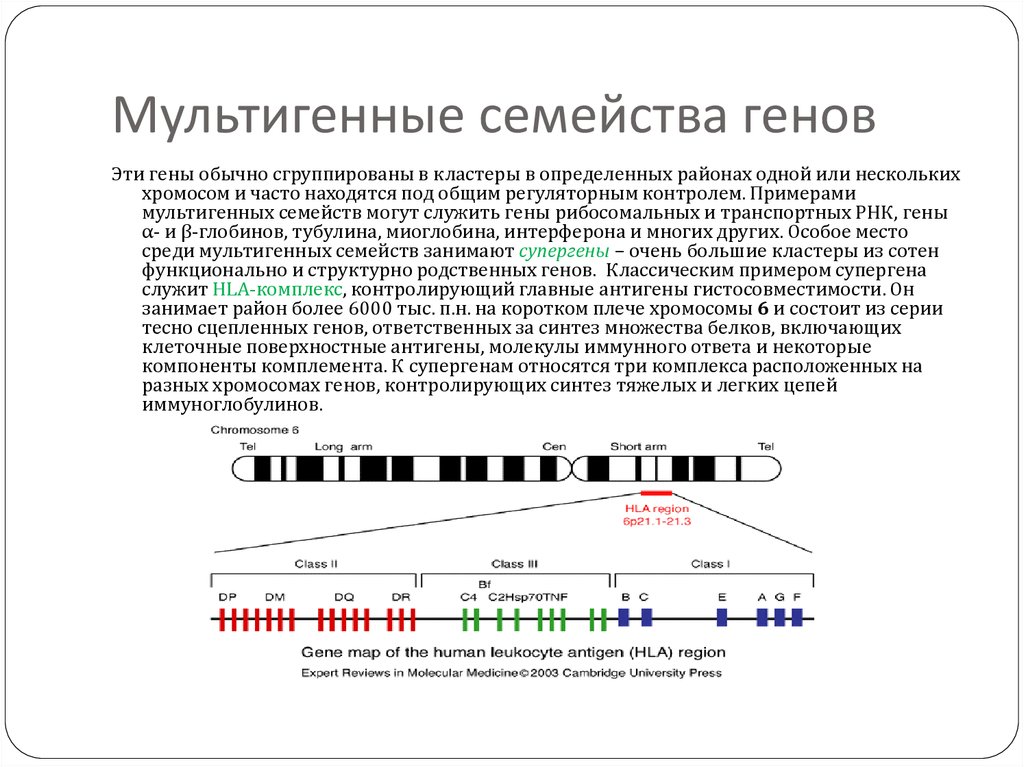
44. Мультигенные семейства генов
Эти гены обычно сгруппированы в кластеры в определенных районах одной или несколькиххромосом и часто находятся под общим регуляторным контролем. Примерами
мультигенных семейств могут служить гены рибосомальных и транспортных РНК, гены
α- и β-глобинов, тубулина, миоглобина, интерферона и многих других. Особое место
среди мультигенных семейств занимают супергены – очень большие кластеры из сотен
функционально и структурно родственных генов. Классическим примером супергена
служит HLA-комплекс, контролирующий главные антигены гистосовместимости. Он
занимает район более 6000 тыс. п.н. на коротком плече хромосомы 6 и состоит из серии
тесно сцепленных генов, ответственных за синтез множества белков, включающих
клеточные поверхностные антигены, молекулы иммунного ответа и некоторые
компоненты комплемента. К супергенам относятся три комплекса расположенных на
разных хромосомах генов, контролирующих синтез тяжелых и легких цепей
иммуноглобулинов.
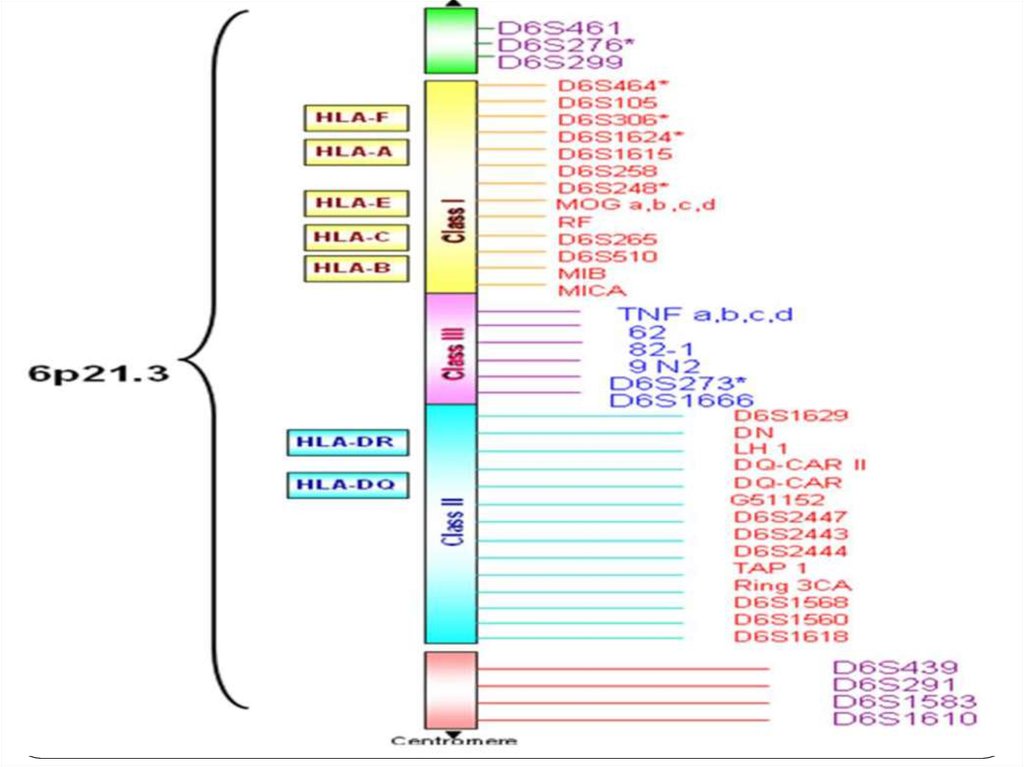
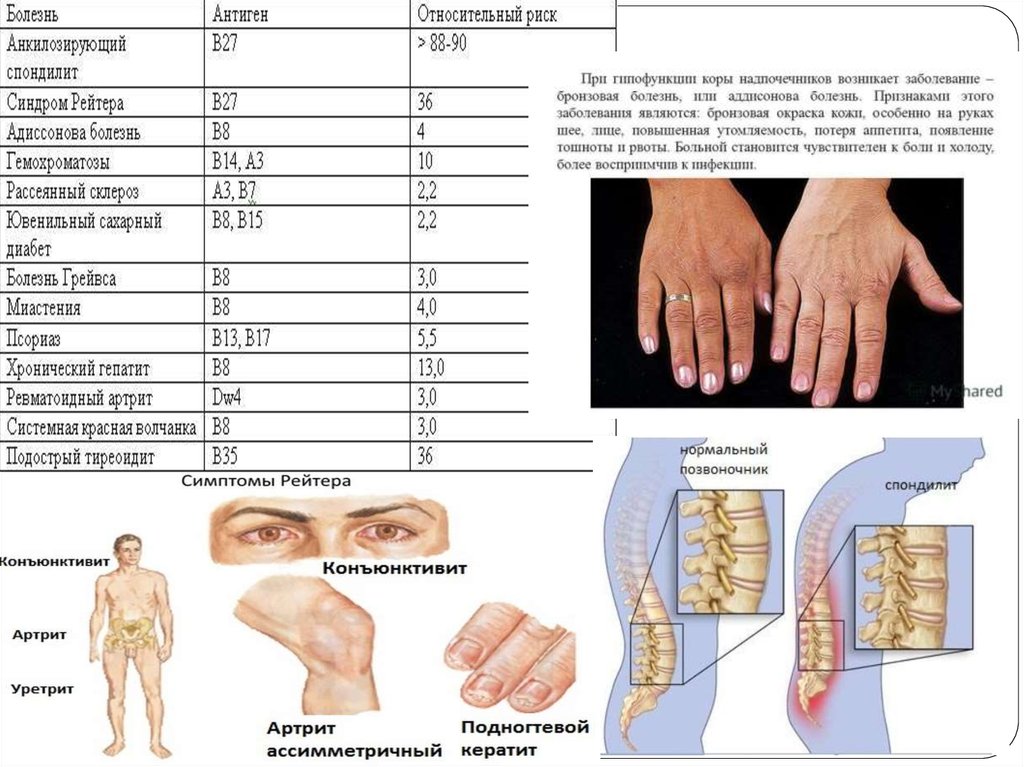
45. Человеческие лейкоцитарные антигены
Система генов тканевой совместимостичеловека ( HLA, Human Leucocyte Antigens) — группа
антигенов гистосовместимости у людей.
Представлены более, чем 150 антигенами. Локус,
расположенный на в коротком плече 6
хромосомы, содержит большое количество генов,
связанных с иммунной системой человека. Этими
генами кодируются в том числе и
антигенпредставляющие белки, расположенные на
поверхности клетки.
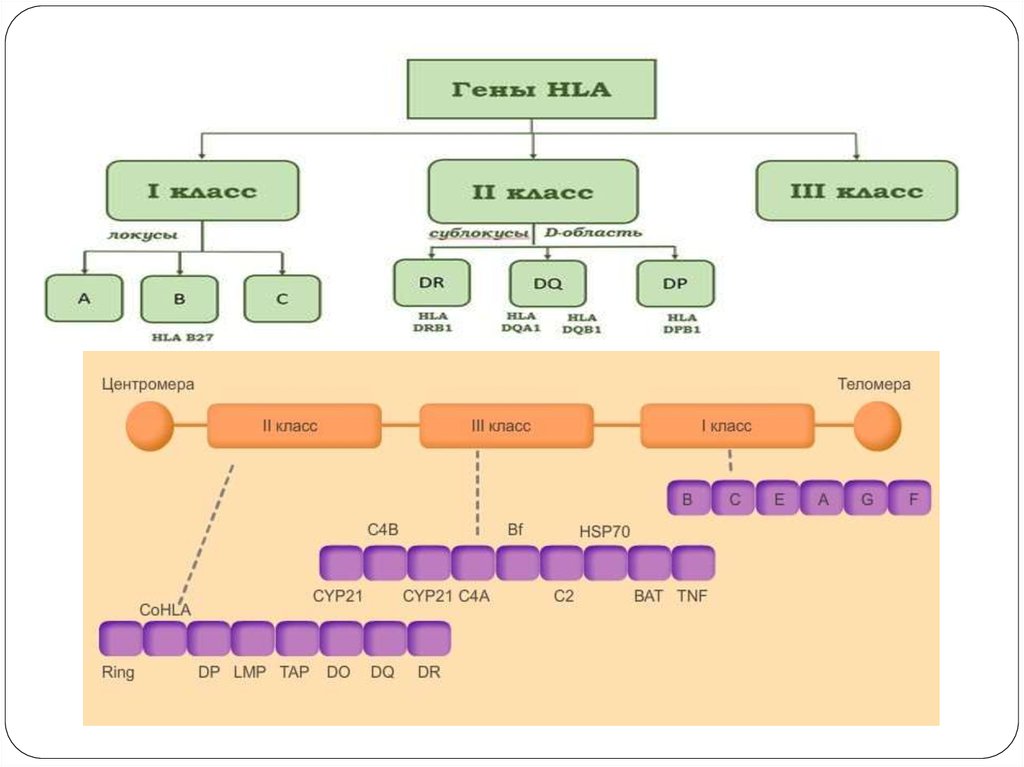
46. Система HLA
представляет собой индивидуальный набор различного типабелковых молекул, находящихся на поверхности клеток. Набор
антигенов (HLA-статус) уникален для каждого человека.
К первому классу МНС относятся молекулы типов HLA-A, -B и -C.
Антигены первого класса системы HLA находятся на поверхности
ЛЮБЫХ клеток. Для гена HLA-А известны около 60 вариантов, для
HLA-B — 136, а для гена HLA-С — 38 разновидностей.
Представителями МНС второго класса являются HLA-DQ, -DP и DR. Антигены второго класса системы HLA находятся на
поверхности только некоторых клеток ИМУННОЙ системы (в
основном это лимфоциты и макрофаги). Для транплантации
ключевое значение имеет полная совместимость по HLA-DR (по
другим HLA-антигенам отсутствие совместимости менее значимо).
47.
48.
49. HLA-типирование – определение HLA-варианта
HLA-типирование –определение HLA-варианта
Типирование на HLA-B27 является, пожалуй, самым известным из всех. Этот антиген
относится к MHC-I (молекулам главного комплекса гистосовместимости 1-го класса), то
есть находится на поверхности всех клеток.
У здоровых европейцев антиген HLA-B27 встречается всего в 8% случаев. Однако его
наличие резко увеличивает (до 20-30%) шансы заболеть ассиметричным
олигоартритом (воспаление нескольких суставов) и (или) получить
поражение крестцово-подвздошного сочленения (воспаление соединения между
крестцом и тазовыми костями).
Установлено, что HLA-B27 встречается:
у страдающих болезнью Бехтерева в 90-95% случаев (это воспаление межпозвонковых
суставов с последующим сращением позвонков),
при реактивных (вторичных) артритах в 36-100% (аутоиммунно-аллергическое
воспаление суставов после некоторых мочеполовых и кишечных инфекций),
при болезни (синдроме) Рейтера в 70-85% (артрит + воспаление мочевыводящего канала
+ воспаление слизистой оболочки глаз),
при псориатическом артрите в 54%,
при энтеропатических артритах в 50% (артриты, связанные с поражением кишечника).
50. HLA-типирование для оценки риска сахарного диабета
Ученые пришли к выводу, что некоторые аллели (варианты одного гена)могут обладать провоцирующим или защитным действием при
сахарном диабете. Например, наличие B8 или B15 в генотипе по
отдельности увеличивает риск диабета в 2-3 раза, а совместно — в 10 раз.
Присутствие определенных разновидностей генов может
увеличивать риск заболевания сахарным диабетом 1 типа с 0,4% до 68%.
Счастливые носители B7 болеют диабетом в 14,5 раз реже тех людей, у
которых B7 отсутствует. «Защитные» аллели в генотипе также
способствуют более мягкому течению болезни в случае, если диабет всетаки разовьется.
HLA-типирование позволяет установить риск развития сахарного диабета
1 типа. Наиболее информативны антигены HLA II класса: DR3/DR4 и DQ. У
50% больных СД I типа обнаружены HLA-антигены DR4,
DQB*0302 и/или DR3, DQB*0201. При этом риск развития болезни
возрастает многократно.
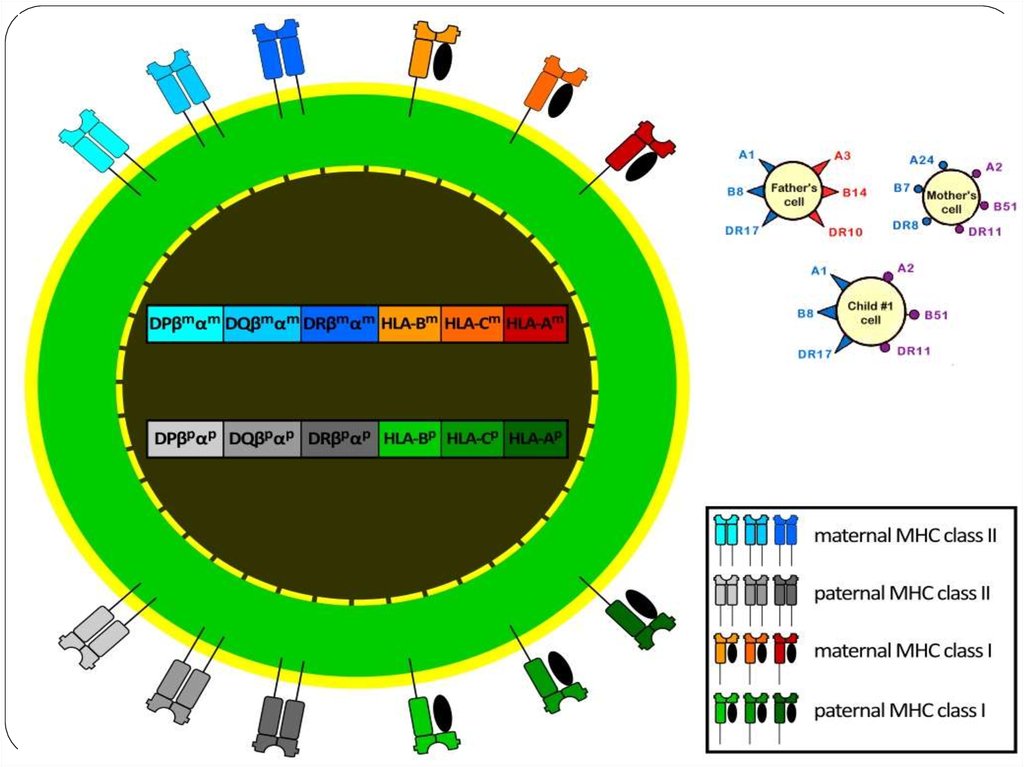
51. HLA-антигены и невынашивание беременности
Одним из иммунологических факторов невынашивания беременности являетсясовпадение по 3 и более общим антигенам HLA II класса. Антигены HLA II класса
находятся преимущественно на клетках иммунной системы. Ребенок получает половину
генов от отца и половину от матери. Для иммунной системы любые белки, кодируемые
генами, являются антигенами и потенциально способны вызывать иммунный ответ. В
начале беременности (первый триместр) чужеродные для организма матери отцовские
антигены плода вызывают у матери выработку защитных (блокирующих) антител.
Эти защитные антитела связываются с отцовскими HLA-антигенами плода, защищая их
от клеток иммунной системы матери (натуральных киллеров) и способствуя
нормальному протеканию беременности.
Если же у родителей совпадает 4 и более антигена HLA II класса, то образование
защитных антител резко снижается или не происходит. В этом случае развивающийся
плод остается беззащитным от материнской иммунной системы, которая без защитных
антител расценивает клетки эмбриона как скопление опухолевых клеток и старается
их уничтожить (это естественный процесс, потому что в любом организме ежесуточно
образуются опухолевые клетки, которые ликвидируются иммунной системой). В итоге
наступает отторжение эмбриона и происходит выкидыш. Таким образом, для для
нормального протекания беременности нужно, чтобы супруги отличались HLAантигенами II класса. Также существует статистика, какие аллели (варианты) HLA-генов
женщин и мужчин приводят к выкидышам чаще или реже.
52.
53.
54.
55. Сроки развития наследственных болезней
во многом зависят от функций вовлеченного в патологиюгена:
- гены, кодирующие транскриптационные факторы,
могут проявиться во внутриутробном периоде (30%
врожденных пороков развития);
- гены, кодирующие ферменты (47% проявляется на
первом году жизни;
- гены, кодирующие модуляторы белковой индукции, в
периоде до 50 лет.
Количественное распределение генов, участвующих в
основных процессах типичной клетки: синтез РНК и
белков – 22%, клеточное деление – 12 %, клеточные
сигналы – 12%, защита клетки – 12%, метаболизм – 17%,
клеточные структуры – 8%, неизвестная функция – 17%.
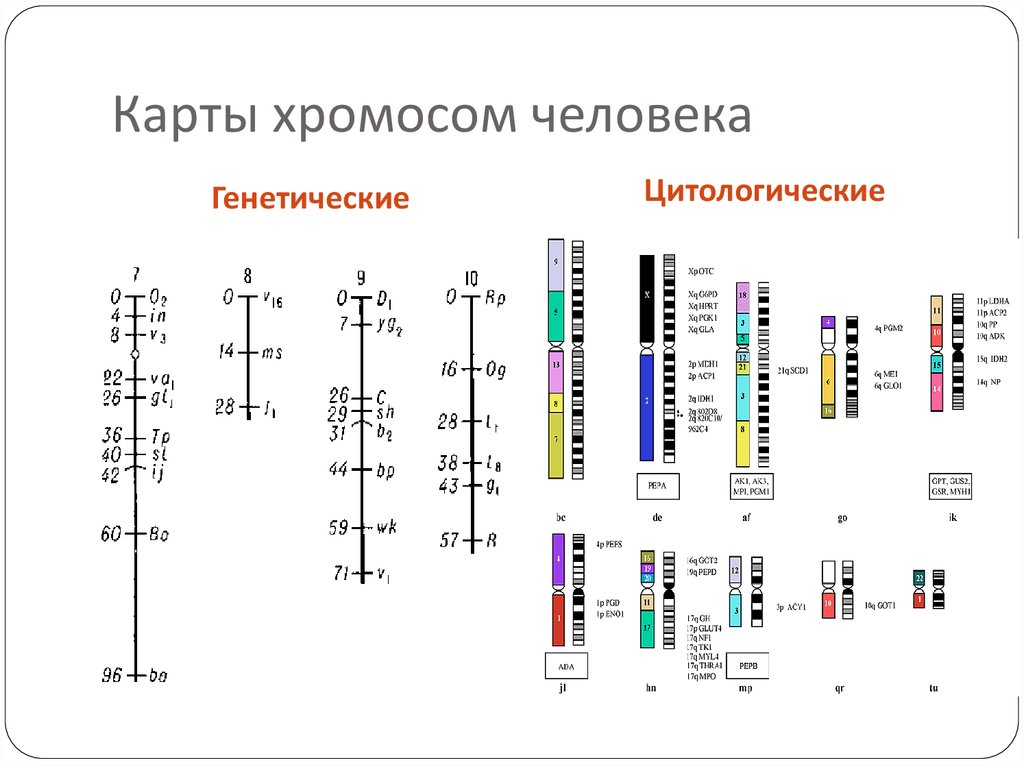
56. Карты хромосом
Генети́ ческая ка́ рта — схема взаимного расположения структурных генов,регуляторных элементов и генетических маркеров, а также относительных
расстояний между ними на хромосоме. Метод построения генетических карт
называется генетическим картированием.
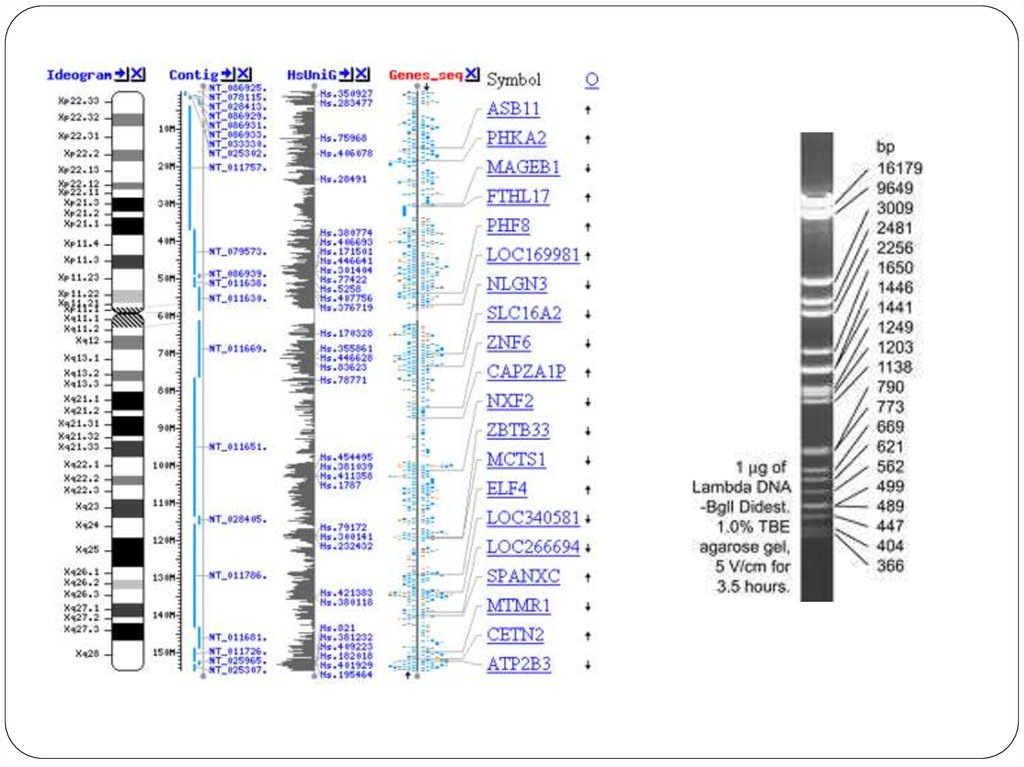
Цитологическая карта — пространственное представление порядка
взаимного расположения структурных элементов хромосом (например, их
дифференциально окрашенных участков).
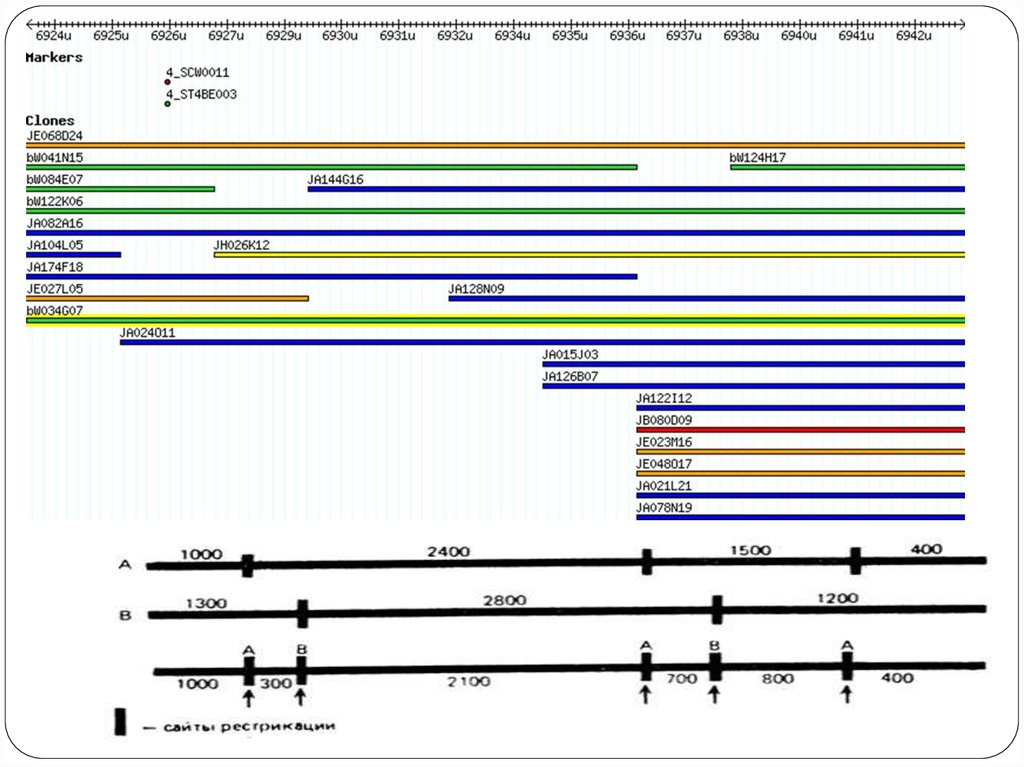
Физическая карта — представление порядка следования физических
маркеров (фрагментов молекулы ДНК), расстояние между которыми
определяется в парах нуклеотидов (п. н.).
Рестрикционная карта — вид физической карты, на которой указан порядок
следования и расстояния между сайтами расщепления ДНКрестриктазами (обычно участок узнавания рестриктазы размером 4—6 п. н.).
Маркерами этой карты являются рестрикционные фрагменты.
Секвенсовые карты – вид карт, на которых указана последовательность
нуклеотидов в ДНК.
Конечной целью изучения генома определенного организма является
интеграция его генетических, цитогенетических и физических карт , а также
их привязка к полной геномной последовательности.
57. Карты хромосом человека
ГенетическиеЦитологические




































 biology
biology