Similar presentations:
Строение и свойства неорганических веществ. Кислоты и основания
1.
Строение и свойстванеорганических веществ. Кислоты
и основания
Выполнила учитель естествознания
Середа Анастасия Сергеевна
2.
ВеществаПРОСТЫЕ
Состоят из атомов одного
химического элемента:
H2, O2, Cl2, Al
СЛОЖНЫЕ
Состоят из двух и более
химических элементов:
H2O, CO2, HCl, NaOH, NaCl
3.
ВеществаОРГАНИЧЕСКИЕ
- Только сложные
вещества
- Обязательно содержат
углерод
СН4, С2Н5ОН, NH2CH2COOH
НЕОРГАНИЧЕСКИЕ
- И простые, и сложные
вещества:
H2O, CO2, C, Br2, Na….
4.
Простые неорганические веществаПрочитайте параграф, выпишите:
1. Физические свойства металлов
2. Примеры металлов
3. Физические свойства неметаллов
4. Примеры неметаллов
5.
Сложные неорганические вещества6.
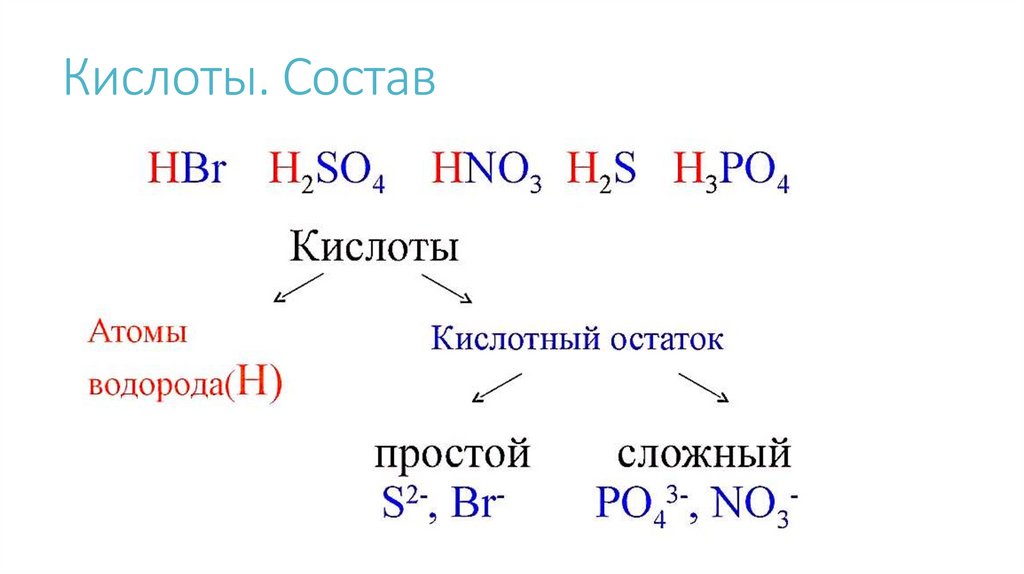
Кислоты. Состав7.
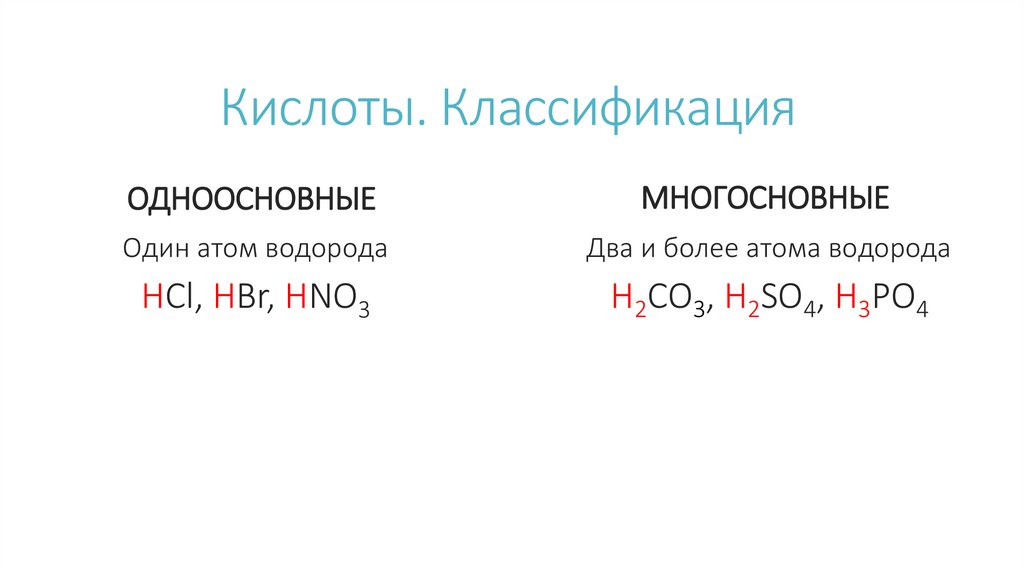
Кислоты. КлассификацияОДНООСНОВНЫЕ
МНОГОСНОВНЫЕ
Один атом водорода
Два и более атома водорода
HCl, HBr, HNO3
H2CO3, H2SO4, H3PO4
8.
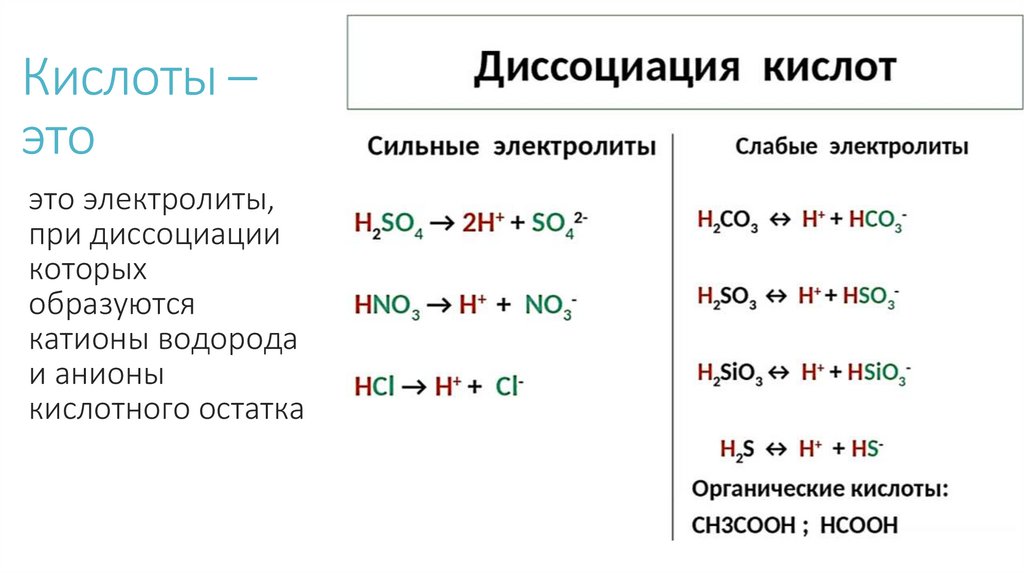
Кислоты –это
это электролиты,
при диссоциации
которых
образуются
катионы водорода
и анионы
кислотного остатка
9.
Основания этоОснования – это
электролиты, при
диссоциации
которых
образуются
катионы металла и
в качестве анионов
гидроксид-ионы
10.
Среда раствораРазличают три основных
типа сред водных
растворов:
•Нейтральная среда (вода)
•Кислая среда (растворы
кислот)
•Щелочная среда
(растворы щелочей)
11.
рН – водородный показательПредставляет собой отрицательный десятичный логарифм
концентрации ионов водорода
12.
Нейтральная среда (рН = 7)Концентрация ионов Н+ и ОН– одинаковая
Примеры:
Вода, растворы солей
13.
Кислотная среда (рН < 7)Концентрация ионов Н+ выше
Примеры:
Растворы кислот
14.
Кислотная среда (рН > 7)Концентрация ионов OН- выше
Примеры:
Растворы щелочей
15.
Индикатор(лат. indicator — показатель,
указатель) — это вещество,
обратимо изменяющее цвет
в зависимости от среды
раствора
16.
Индикаторы – твердые вещества.Видео
Лакмус
Метилоранж
Фенолфталеин
17.
Разнообразие индикаторовПомимо специально
полученных для исследования
среды индикаторов,
существуют так же и
природные индикаторы,
многие из которых можно
найти на любой кухне:
Краснокочанная капуста, чай,
свекла
! Питьевая сода – не щелочь,
но образует щелочной раствор
в воде
Питьевая
сода
Вода
Уксус
18.
19.
20.
Химические свойства кислот иоснований
Сильные кислоты и щелочи очень химически активны. Могут
разрушать многие материалы. Соприкосновение с кожей могут
вызывать ожоги.
Видео

















 chemistry
chemistry








