Similar presentations:
Изготовление индикаторов растительного происхождения
1.
«Изготовление индикатороврастительного происхождения»
Практическая работа № 3
2.
Цели работы:1. Ознакомиться с понятием «индикатор», классификацией индикаторов и
предъявляемым к ним требованиям.
2. Ознакомиться с методикой изготовления индикаторов из природного
сырья.
3. Ознакомиться с результатами исследований индикаторов растительного
происхождения.
4. Приготовить индикатор растительного происхождения в домашних
условиях и провести определение среды растворов моющих средств для
посуды (согласно примера).
5. Результаты выполнения практической работы и проведения домашнего
эксперимента оформить в тетради.
3.
Индикаторы – вещества, изменяющие свою окраску взависимости от реакции среды. Название «индикаторы»
происходит от латинского слова indicator, что означает
«указатель».
В химической лаборатории или на заводе индикаторы в
наглядной форме расскажут о том, прошла ли до конца
химическая реакция или нет, достаточно добавлено одного
реактива к другому или нужно еще добавлять.
4.
Из истории индикаторовИстория индикаторов начинается в XVII веке. Еще в 1640 году ботаники описали
гелиотроп – душистое растение с темно-лиловыми цветками (см. рисунок), из
которого было выделено красящее вещество. Этот краситель, наряду с соком фиалок,
стал широко применяться химиками в качестве индикатора. Об этом можно прочитать
в трудах знаменитого физика и химика XVII века Роберта Бойля.
В 1663 году был открыт лакмус – водный настой лишайника, растущего на скалах
Шотландии. Роберт Бойль приготовил водный настой лакмусового лишайника для
своих опытов. Склянка, в которой он хранил настой, понадобилась для соляной
кислоты. Вылив настой, Бойль наполнил склянку кислотой и с удивлением обнаружил,
что кислота покраснела. Заинтересовавшись этим, Бойль на пробу добавил несколько
капель настоя лакмуса к водному раствору гидроксида натрия и обнаружил, что в
щелочной среде лакмус синеет. Так был открыт первый индикатор для обнаружения
кислот и оснований, названный по имени лишайника лакмусом.
Фенолфталеин, который применяется в виде спиртового раствора, приобретает в
щелочной среде малиновый цвет, а в нейтральной и кислой он бесцветен. Синтез
фенолфталеина впервые осуществил в 1871 году немецкий химик Адольф фон Байер,
будущий лауреат Нобелевской премии.
Что касается индикатора метилового оранжевого, открытого в 1887 году, он
действительно оранжевый в нейтральной среде. В кислотах его окраска становится
розово-малиновой, а в щелочах – желтой.
5.
Классификация индикаторовОдни из самых распространенных – кислотно-основные индикаторы, которые изменяют цвет в зависимости от кислотности раствора. Происходит
это потому, что в кислой и щелочной среде молекулы индикаторов имеют разное строение. Примером может служить общеизвестный индикатор
фенолфталеин. В кислой среде это соединение находится в виде недиссоциированных молекул и раствор бесцветен, а в щелочной среде – в виде
ионов и раствор имеет малиновый цвет.
Помимо кислотно-основных применяют и другие типы индикаторов.
Окислительно-восстановительные индикаторы изменяют свой цвет в зависимости от того, что присутствует в растворе окислитель или
восстановитель. Такими индикаторами служат вещества, которые сами подвергаются окислению или восстановлению, причем окисленная и
восстановленная формы имеют разные окраски. Например, окисленная форма дифениламина имеет фиолетовую окраску, а восстановленная –
бесцветную.
Широкое распространение получили комплексонометрические индикаторы – вещества, образующие с ионами металлов окрашенные
комплексные соединения.
Некоторые вещества, адсорбируются на поверхности осадка, изменяя его окраску; такие индикаторы называются адсорбционными.
При определении среды мутных или окрашенных растворов, в которых практически невозможно заметить изменение окраски обычных кислотноосновных индикаторов, используют флуоресцентные индикаторы. Они светятся (флуоресцируют) разным цветом в зависимости от рН раствора.
При этом важно, что свечение индикатора не зависит от прозрачности и собственной окраски раствора.
Нередко используются универсальные индикаторы – смесь нескольких индивидуальных индикаторов, подобранных так, что их раствор
поочередно меняет окраску, проходя все цвета радуги при изменении кислотности раствора в широком диапазоне рН (например, от 1 до 11).
Раствором универсального индикатора часто пропитывают полоски бумаги, которые позволяют быстро (хотя и с не очень высокой точностью)
определить рН анализируемого раствора, сравнивая окраску полоски, смоченной раствором с эталонной цветовой шкалой.
6.
Природные индикаторыЕсли нет настоящих химических индикаторов, то для определения среды растворов можно успешно применять индикаторы, выделенные из
природного сырья.
Исходным сырьем могут служить цветы герани, лепестки пиона или мальвы, ирис, темные тюльпаны или анютины глазки, а также ягоды малины,
черники, черноплодной рябины, соки вишни, смородины, винограда, плоды крушины и черемухи.
Эти природные индикаторы содержат окрашенные вещества (пигменты), способные менять свой цвет в ответ на то или иное воздействие и,
попадая в кислую или щелочную среду, они наглядным образом сигнализируют об этом.
Такими пигментами являются, прежде всего, антоцианы: в нейтральной среде приобретают пурпурную окраску, в кислой среде – красный цвет, в
щелочной среде – зелено-желтый цвет.
Именно антоцианы придают разнообразные оттенки розового, красного, голубого и лилового многим цветам, плодам и осенним листьям. Эта
окраска часто зависит от рН клеточного содержимого, и потому может меняться при созревании плодов, отцветании цветков и увядании листьев
Антоцианы - неустойчивые соединения, в клетках растений обычно содержится несколько различных антоцианов , и проявление их связано с
химическим составом почвы и возрастом растения.
Обычный чай – тоже индикатор. Если в стакан с крепким чаем капнуть лимонный сок или растворить несколько кристалликов лимонной кислоты,
то чай сразу станет светлее. Если же растворить в чае питьевую соду, раствор потемнеет (пить такой чай, конечно, не следует). Чай же из цветков
каркаде дает намного более яркие цвета. Индикатором являются и обычные чернила, которые под влиянием кислоты изменяют окраску с
фиолетовой на зеленую, и вновь приобретают фиолетовую окраску при нейтрализации кислоты щелочью.
7.
Биохимическая роль индикаторовПоступая в организм человека с фруктами и овощами, антоцианы проявляют действие, схожее с
витамином Р, они поддерживают нормальное состояние кровяного давления и сосудов,
предупреждая внутренние кровоизлияния. Антоцианы требуются клеткам головного мозга,
улучшают память.
Антоцианы – мощные антиоксиданты, которые сильнее в 50 раз витамина С. Многие исследования
подтвердили пользу антоцианов для зрения. Наибольшая концентрация антоцианов содержится в
чернике. Поэтому препараты, содержащие чернику, наиболее востребованы в медицине.
8.
Требования к индикаторамЧтобы какое-либо вещество могло служить индикатором, оно должно удовлетворять следующим
необходимым условиям:
1) должно быть слабой кислотой или слабым основанием;
2) его молекулы и ионы должны иметь разную окраску;
3) окраска их должна быть чрезвычайно интенсивной, чтобы быть заметной при добавке к
испытуемому раствору малого количества индикатора.
У природных индикаторов есть серьезный недостаток: их отвары довольно быстро портятся –
скисают или плесневеют (более устойчивы спиртовые растворы). Другой недостаток – слишком
широкий интервал изменения цвета. При этом трудно или невозможно отличить, например,
нейтральную среду от слабокислой или слабощелочную от сильнощелочной.
9.
Методика приготовления индикатороврастительного происхождения
Получение индикатора из краснокочанной капусты.
Измельчаем лист краснокочанной капусты и растираем его в ступке с небольшим объёмом спиртоводной смеси (1:1). Вытяжка приобретает фиолетовый цвет, поскольку из капустной ткани
экстрагируется рубробрассицин. Это и есть кислотно-щелочной индикатор растительной природы.
Приготовим 4 пробирки: первая – с раствором уксусной кислоты, капустный индикатор в этой
пробирке ярко-красный цвет; вторая – просто с водой – цвет фиолетовый; третья – со слабым
раствором гидрокарбоната натрия (соды пищевой) – цвет синий; четвёртая – с раствором щёлочи
(едкий натр и др.), приобретает зелёный цвет.
10.
Методика приготовления индикатороврастительного происхождения
Получение индикатора из сока сахарной свёклы.
Очистим свёклу от кожуры, отрежем кусочек весом 5-10 грамм. Данный кусочек прокипятим в 100
мл воды в течение 5-10 минут. Протрём кусок свёклы на терке, измельчим в ступке и отфильтруем
полученный настой. Фильтрат приобретает бордовый цвет. Приготовим 2 пробирки с растворами
кислоты и щёлочи, добавим к содержимому пробирок по несколько капель полученного
индикатора. В растворе кислоты свекольный индикатор приобретает малиновую окраску, а в
растворе щёлочи становится жёлто-коричневым.
11.
Методика приготовления индикатороврастительного происхождения
Получение индикатора из чёрного винограда.
С ягод чёрного винограда осторожно снимаем кожицу и измельчаем её в ступке с пестиком,
добавляем несколько миллилитров спирта. Необходимым условием является экстракция пигмента
(краски) данным растворителем. После этого экстракт нейтрализуем мелом, так как сок винограда
содержит природные кислоты. Профильтруем полученную смесь через марлевый фильтр. Вытяжка
приобретает бордово-красный цвет. Приготовим пробирки с растворами уксусной кислоты и
питьевой соды и добавим в каждую по несколько капель виноградного индикатора. В растворе с
кислотой индикатор приобретает красную окраску, а в растворе со щёлочью – жёлто-зелёную.
12.
Методика приготовления индикатороврастительного происхождения
Получение индикатора из цветков домашней фиалки.
Сорвём несколько цветков с комнатного растения – фиалка. Измельчим цветки в ступке с
небольшим количеством чистого речного песка и добавим несколько миллилитров спирто-водной
смеси (1:1). Полученную смесь отфильтруем в стакан. Вытяжка приобретает сиреневый цвет.
Приготовим пробирки с растворами уксусной кислоты и гидроксида натрия (соды пищевой),
добавим в каждую пробирку по несколько капель фиалкового индикатора. В растворе с кислотой
индикатор приобретает розовый цвет, а в растворе со щёлочью – зелёный.
13.
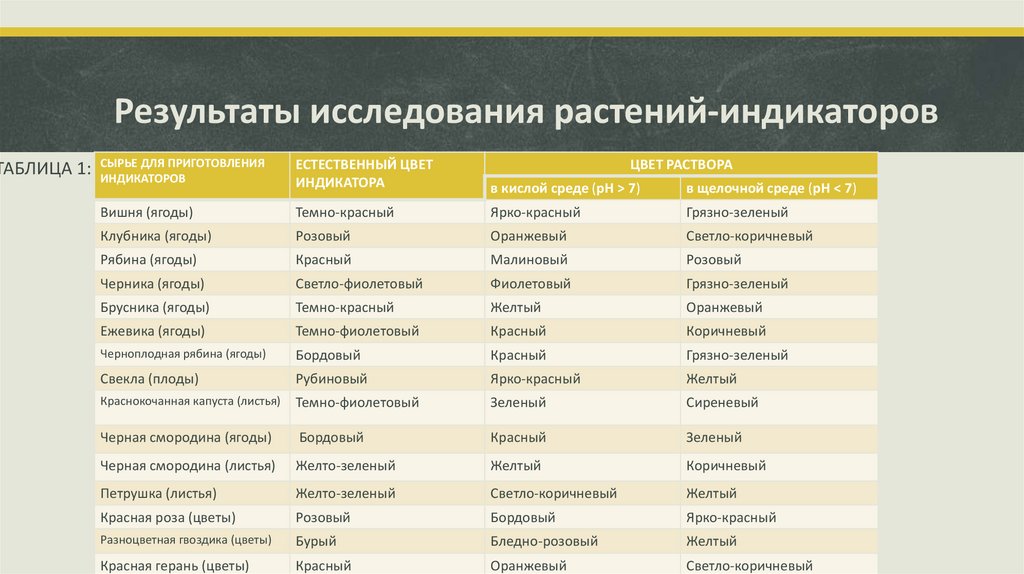
ТАБЛИЦА 1:Результаты исследования растений-индикаторов
СЫРЬЕ ДЛЯ ПРИГОТОВЛЕНИЯ
ИНДИКАТОРОВ
ЕСТЕСТВЕННЫЙ ЦВЕТ
ИНДИКАТОРА
в кислой среде (рН > 7)
в щелочной среде (рН < 7)
Вишня (ягоды)
Темно-красный
Ярко-красный
Грязно-зеленый
Клубника (ягоды)
Розовый
Оранжевый
Светло-коричневый
Рябина (ягоды)
Красный
Малиновый
Розовый
Черника (ягоды)
Светло-фиолетовый
Фиолетовый
Грязно-зеленый
Брусника (ягоды)
Темно-красный
Желтый
Оранжевый
Ежевика (ягоды)
Темно-фиолетовый
Красный
Коричневый
Черноплодная рябина (ягоды)
Бордовый
Красный
Грязно-зеленый
Свекла (плоды)
Рубиновый
Ярко-красный
Желтый
Краснокочанная капуста (листья)
Темно-фиолетовый
Зеленый
Сиреневый
Черная смородина (ягоды)
Бордовый
Красный
Зеленый
Черная смородина (листья)
Желто-зеленый
Желтый
Коричневый
Петрушка (листья)
Желто-зеленый
Светло-коричневый
Желтый
Красная роза (цветы)
Розовый
Бордовый
Ярко-красный
Разноцветная гвоздика (цветы)
Бурый
Бледно-розовый
Желтый
Красная герань (цветы)
Красный
Оранжевый
Светло-коричневый
ЦВЕТ РАСТВОРА
14.
Реакция среды растворов моющих средств для посудыТАБЛИЦА 2:
№
Моющее средство для посуды
1
«Миф»
Отвар краснокочанной капусты
Бледно-зеленая
Слабощелочная
2
«Fairy»
Отвар краснокочанной капусты
Зеленая
Щелочная
3
«AOS»
Отвар клубники
Бледно-желтая
Слабощелочная
4
«Pril»
Отвар ягод черноплодной рябины
Бледно-розовая
Слабокислая
Растительный индикатор
Окраска индикатора
Среда раствора












 chemistry
chemistry








