Similar presentations:
Химические реакции
1.
2.
?Что называют химической
реакцией?
3.
?Перечислите условия
протекания химических
реакций.
4.
?Перечислите внешние
признаки протекания
химических реакций.
5.
?Что называют уравнением
химической реакции?
6.
?На основании какого закона
составляют уравнения
химических реакций?
7.
?Перечислите признаки
классификации химических
реакций.
8.
?Как классифицируют
химические реакции по числу
и составу исходных веществ и
продуктов реакции?
9.
?Как классифицируют
химические реакции по
тепловому эффекту?
10.
?Как классифицируют
химические реакции по
изменению степеней
окисления атомов ХЭ?
11.
?Можно ли управлять
ходом химической
реакции?
12.
Тема урока:Скорость химических
реакций
13.
Что мы узнаем:• Что такое скорость химических реакций.
• Как можно измерить скорость реакции.
• От чего зависит скорость реакции.
14.
Химические реакции в природепротекают с разными скоростями.
Очень быстро протекают реакции в
водных растворах, взрывы.
15.
Быстро, но не мгновенно горитсера, цинк растворяется в
соляной кислоте.
Медленно образуется ржавчина
на железных предметах, гниет
листва, разрушаются зубы.
16.
?Что называют скоростью
в физике?
17.
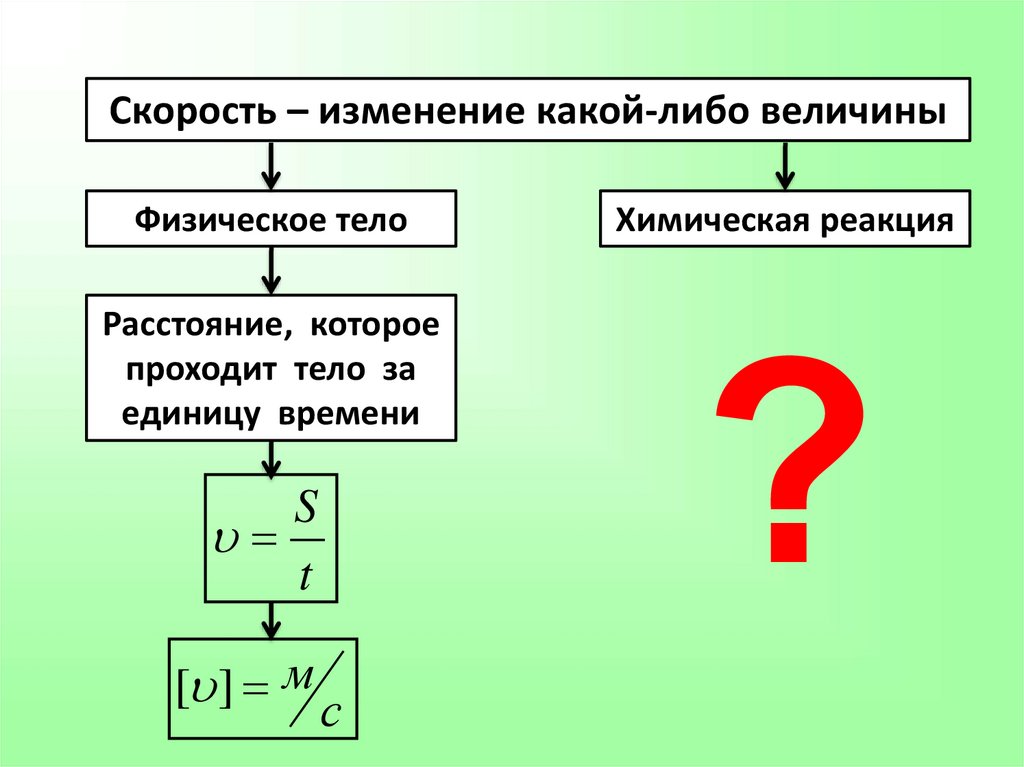
Скорость – изменение какой-либо величиныФизическое тело
Расстояние, которое
проходит тело за
единицу времени
S
t
[ ] м
с
Химическая реакция
?
18.
?Как можно применить
понятие «скорость»
к химическим реакциям?
19.
?Как можно измерить скорость
химической реакции?
S + O2 = SO2
При взаимодействии 1 моль серы с 1 моль
кислорода образуется 1 моль оксида серы(IV)
?
Что изменяется в ходе
протекания химической
реакции?
20.
Выведем формулу для расчетаскорости химической реакции:
!
=
+
–
n2 – n1
( t2 – t1 ) V
=
+
–
=
+
–
C2 – C1
=
t2 – t1
C
t
график
21.
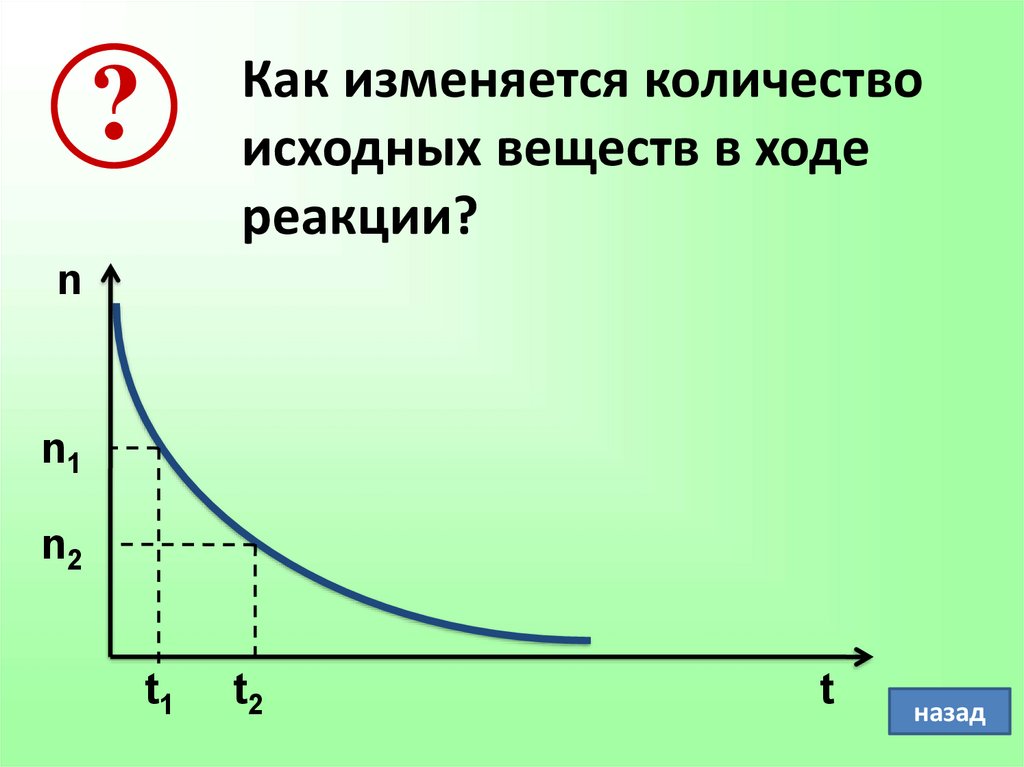
Как изменяется количествоисходных веществ в ходе
реакции?
?
n
n1
n2
t1
t2
t
назад
22.
Скорость химическойреакции – изменение
концентрации одного из веществ
в единицу времени.
23.
?В каких единицах измеряют
скорость химической
реакции?
C
t
моль
[ ]
л с
24.
Демонстрационный опытОпыт 1.
Опыт 2.
Взаимодействие
двух веществ,
взятых в твердом
виде.
Взаимодействие
двух веществ,
взятых в виде
растворов.
?
В каком случае реакция протекает
быстрее?
25.
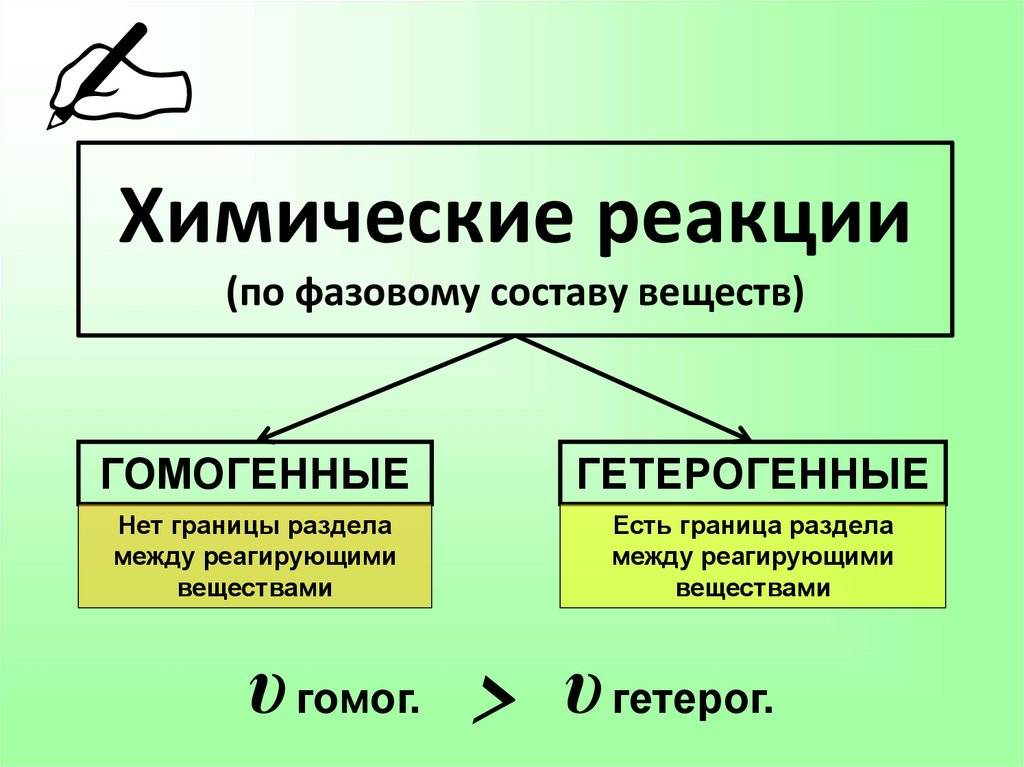
Химические реакции(по фазовому составу веществ)
ГОМОГЕННЫЕ
ГЕТЕРОГЕННЫЕ
Нет границы раздела
между реагирующими
веществами
Есть граница раздела
между реагирующими
веществами
υ гомог. > υ гетерог.
26.
?Выберите гетерогенные
системы:
кислород – водород
цинк – соляная кислота
цинк – сера
вода – спирт
углекислый газ – вода
кислород – железо
вода – масло
27.
?От каких факторов зависит
скорость химических
реакций?
28.
Скорость химическихреакций зависит от:
1. температуры;
2. концентрации исходных веществ
(давления – для газов);
3. площади соприкосновения
исходных веществ;
4. природы реагирующих веществ;
5. наличия катализатора.
29.
ФакторПримеры
реакций
Действие
Наблюдения
фактора
30.
Демонстрационный опыт«Природа реагирующих веществ»
1) Mg + 2HCl = MgCl2 + H2↑
2) Zn + 2HCl = ZnCl2 + H2↑
3) Fe + 2 HCl = FeCl2 + H2↑
1 > 2 > 3
31.
Демонстрационный опыт«Концентрация веществ»
1) Zn + 2HCl(20%) = ZnCl2 + H2↑
2) Zn + 2HCl(10%) = ZnCl2 + H2↑
1 > 2
32.
Закон действующих массaA + bB = dD + fF
k C ( A) C ( B)
a
b
C – концентрации исходных веществ
k – константа скорости реакции
33.
Демонстрационный опыт«Температура»
1) Zn + 2HCl = ZnCl2 + H2↑
t
2) Zn + 2HCl = ZnCl2 + H2↑
2 > 1
34.
Правило Вант-Гоффа2 1
t 2 t1
10
- температурный
коэффициент
скорости
При увеличении
температуры на
каждые 10о скорость
химических реакций
увеличивается в 2-4
раза.
35.
Якоб Хендрик Вант-ГоффаГолландский химик. Один из
основателей физической
химии. Исследовал кинетику
реакций, растворы, строение
органических веществ.
Член ряда академий наук и
научных обществ.
Нобелевская премия (1901 г.).
30.08.1852 - 1.03.1911
36.
Демонстрационный опыт«Площадь соприкосновения
реагирующих веществ»
1) Zn(гранула) + 2HCl = ZnCl2 + H2↑
2) Zn(порошок) + 2HCl = ZnCl2 + H2↑
2 > 1
37.
Домашнее задание:Учебник: § 29, 30, упр. 1, 2, 5, 6.
Записать определения в словарь.

































 chemistry
chemistry








