Similar presentations:
Степень окисления
1.
Центр дистанционного образованиядетей-инвалидов
при ОГАОУ
«Белгородский инженерный юношеский лицей-интернат»
СТЕПЕНЬ ОКИСЛЕНИЯ
Составила: Быкова О.С., учитель химии
2.
Степень окисления элемента – этоусловный заряд его атома, в
молекуле, если считать, что
молекула состоит из ионов.
3.
4.
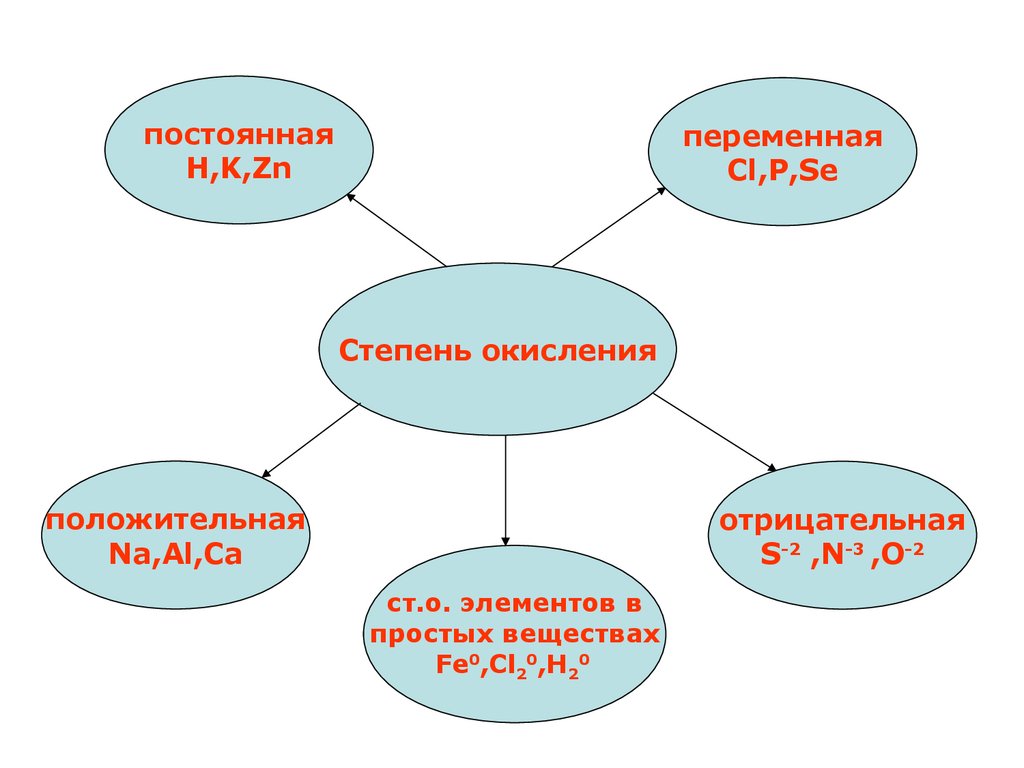
постояннаяH,K,Zn
переменная
Cl,P,Se
Степень окисления
положительная
Na,Al,Ca
отрицательная
S-2 ,N-3 ,O-2
ст.о. элементов в
простых веществах
Fe0,Cl20,H20
5.
Положительная степень окисления – равначислу электронов, отданных данным атомам.
Атом может отдать все валентные электроны
(для главных групп это электроны внешнего
уровня) соответствующее номеру группы, в
котором находится элемент, проявляя при
этом высшую степень окисления (исключение
ОF2).Например: высшая степень окисления
главной подгруппы II группы равна +2
( Zn+2)Положительную степень проявляют
как металлы и неметаллы, кроме F, He,
Ne.Например: С+4 ,Na+1 , Al+3
6.
Отрицательная степень окисления равна числуэлектронов, принятых данным атомом, ее
проявляют только неметаллы. Атомы
неметаллов присоединяют столько электронов,
сколько их не хватает до завершения внешнего
уровня, проявляя при этом отрицательную
степень.
У элементов главных подгрупп IV-VII групп
минимальная степень окисления численно равна
Номер группы -8 = «минимальная отрицательная
степень окисления»
7.
Для определения степени окисления атома в соединении следуетучитывать ряд положений:
1. Степень окисления F во всех соединениях равна « -1». Na+1 F-1,
H+1 F-1
2. Степень окисления кислорода в большинстве соединений равна
(-2) исключение: ОF2, где степень окисления О+2F-1
3. Водород в большинстве соединений имеет степень окисления
+1, кроме соединения с активными металлами, где степень
окисления (-1) :Na+1H-1
4.Степень окисления металлов главных подгрупп I, II, III групп во
всех соединениях равна +1,+2,+3.
8.
Составление химическихформул по степени
окисления
АЛГОРИТМ:
1. Записать химические знаки элементов
2. Определить ст.о. элементов по таблице
Al S
Д.И. Менделеева.
3. Найти НОК и определить индексы.
Al+3S-2
6
НОК=6
Al+3S-2
Al2S3
алгебраическая сумма степеней окисления элементов равна нулю.
9.
Алгоритм составления формулы в соединениях:1 способ
1. На первом месте пишется элемент с меньшей
электроотрицательностью, на втором с большей
электроотрицательностью.
2. Элемент, написанный на первом месте имеет положительный
заряд «+», а на втором с отрицательным зарядом «-».
3. Указать для каждого элемента степень окисления.
4. Найти общее кратное значение степеней окисления.
5. Разделить наименьшее общее кратное на значение степеней
окисления и полученные индексы приписать внизу справа после
символа соответствующего элемента.
10.
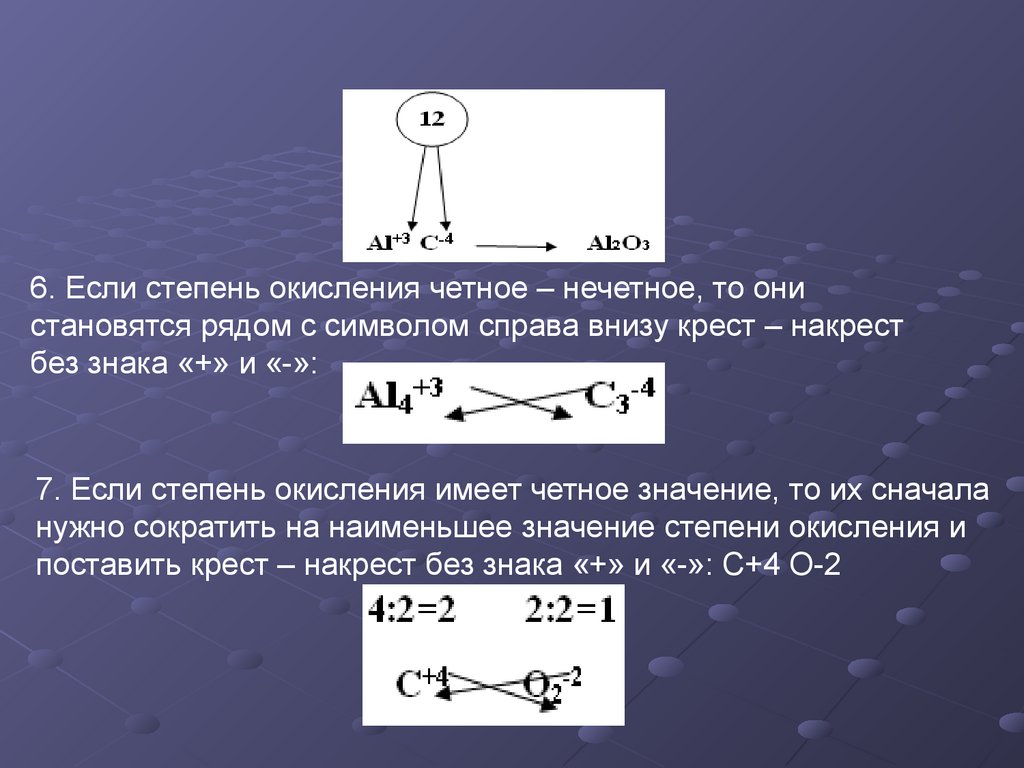
6. Если степень окисления четное – нечетное, то онистановятся рядом с символом справа внизу крест – накрест
без знака «+» и «-»:
7. Если степень окисления имеет четное значение, то их сначала
нужно сократить на наименьшее значение степени окисления и
поставить крест – накрест без знака «+» и «-»: С+4 О-2
11.
2 способ1. Обозначим степень окисления N через Х, указать
степень окисления О: N2x O3-2
2. Определить сумму отрицательных зарядов, для этого
степень окисления кислорода умножаем на индекс
кислорода: 3· (-2)= -6
3.Чтобы молекула была электронейтральной нужно
определить сумму положительных зарядов: Х2 = 2Х
4.Составить алгебраическое уравнение:
2Х+ (-6)=0
2Х =6
Х=6:2
Х=3










 chemistry
chemistry








