Similar presentations:
Изопреноиды. Терпены. Терпеноиды. Стероиды
1.
Кафедра ФАРМАЦИИТема лекции:
Изопреноиды. Терпены. Терпеноиды.
Стероиды.
1
2.
НИЗКОМОЛЕКУЛЯРНЫЕ БИОРЕГУЛЯТОРЫНеомыляемые липиды представляют собой
группу нейтральных веществ, которую можно
разделить, сообразуясь с особенностями структуры, на
терпеноиды и стероиды.
присутствуют одинаковые пятиуглеродные
изопреновые фрагменты
3.
Значительная часть низкомолекулярныхбиорегуляторов является изопреноидами.
2- метилбутадиен-1,3
Состав молекул изопреноидов по углероду равен (С5)n, где n –
целое число, число структурных звеньев изопрена.
4.
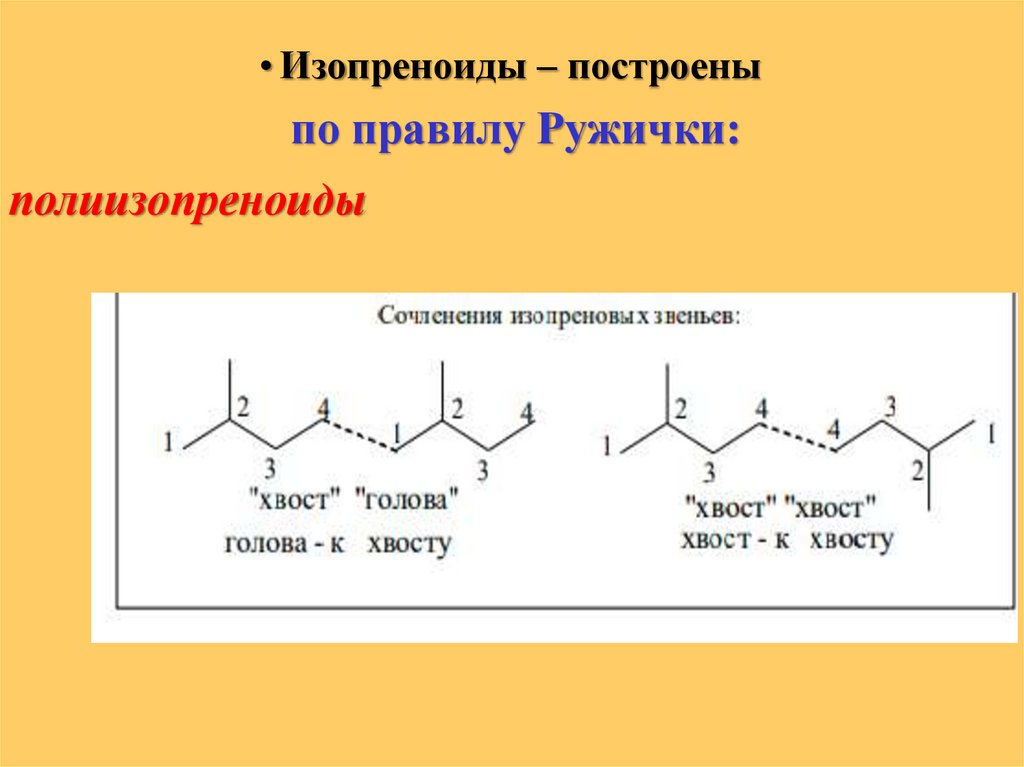
• Изопреноиды – построеныпо правилу Ружички:
полиизопреноиды
"голова" одного звена к "хвосту" следующего
C
CH2
C
C
CH2 CH2
C
CH3 H
CH3 H
CH3 H
CH3 H
H
C
CH2 CH2
C
C
CH2 CH2
C
CH3
C
CH2 CH2
C
CH2
n
5.
• Изопреноиды – построеныпо правилу Ружички:
полиизопреноиды
6.
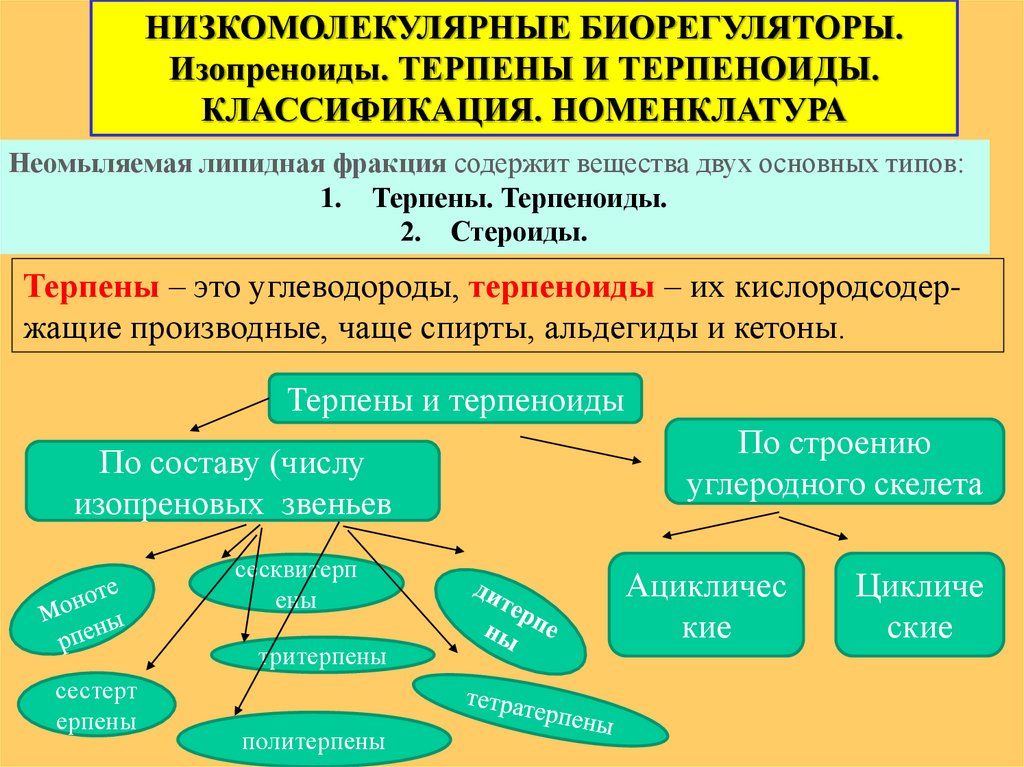
НИЗКОМОЛЕКУЛЯРНЫЕ БИОРЕГУЛЯТОРЫ.Изопреноиды. ТЕРПЕНЫ И ТЕРПЕНОИДЫ.
КЛАССИФИКАЦИЯ. НОМЕНКЛАТУРА
Неомыляемая липидная фракция содержит вещества двух основных типов:
1. Терпены. Терпеноиды.
2. Стероиды.
Терпены – это углеводороды, терпеноиды – их кислородсодержащие производные, чаще спирты, альдегиды и кетоны.
Терпены и терпеноиды
По составу (числу
изопреновых звеньев
сесквитерп
ены
тритерпены
сестерт
ерпены
политерпены
По строению
углеродного скелета
Ацикличес
кие
Цикличе
ские
7.
ТерпеныСами углеводороды, скелет которых построен из 2,
3 или более звеньев изопрена, называют
терпеновыми углеводородами, или терпенами.
К терпеноидам относят разнообразные
кислородсодержащие функциональные
производные изопреноидов.
8.
Полиизопреноиды.n
каучук гевеи
гуттаперча
n
n = 1000 - 5000
общая формула полипренолов
В листьях, коре и в
корнях содержится гутта
(в коре корней – до 30%)
m
n
m=3-5;n=3-6;p=0-4
Основной липидный компонент черного
p = 0 - полипренолы
вещества(вчеловеческого
растениях) мозга (14% по массе).
Мощная
гепатопротекторная
активность,
обычно m+n
= 7-14
применяются
при
лечении нейродегеративных
заболеваниях (болезнь Альцгеймера).
Функция: переносят глюкозу и другие сахара
(гидрофильные молекулы) через биологичес-
OH
p
p > 0 - долихолы
(в животных)
обычно m+n+p = 14-21
Каучука в млечном соке
– 40–50%.
9.
Общая формула терпеновых углеводородов(С5Н8)n
Терпеноиды могут иметь ациклическое и
циклическое строение.
10.
Монотерпеновые ациклические соединения.голова-к-хвосту
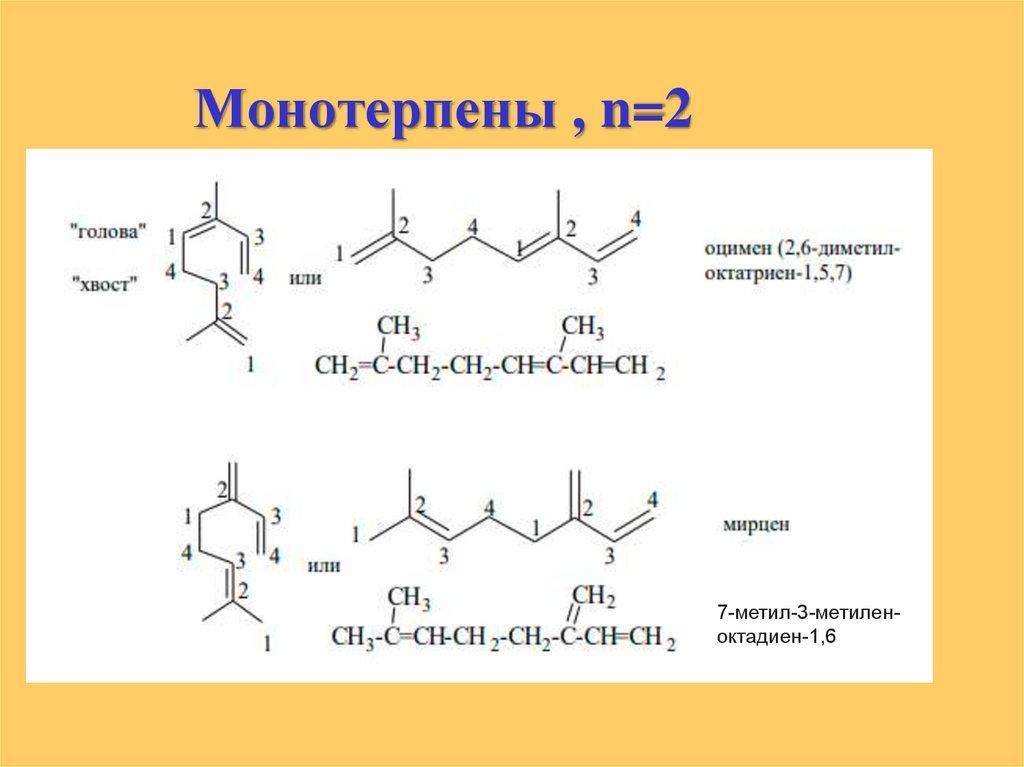
мирцен
2,6-диметилоктан
лавандулан
артемизан
«голова-к-п
«голова-к-плавнику»
аллооцимен
оцимен
лавр, ландыш, вербена, хмель
OH
OH
HO
HO
линалоол
лаванда, роза
иланг-иланг
цитронеллол
нерол
гераниол
герань, роза,
лаванда, роза
в секреции аллигаторов
шиповник
бергамотовое масло,
померанцевое масло
O
H
H
O
цитронеллаль
гераниаль
цитрусовые,
H
нераль
O
11.
Среди терпенов наиболее распространенымоно- и бициклические соединения.
12.
Монотерпены , n=27-метил-3-метиленоктадиен-1,6
13.
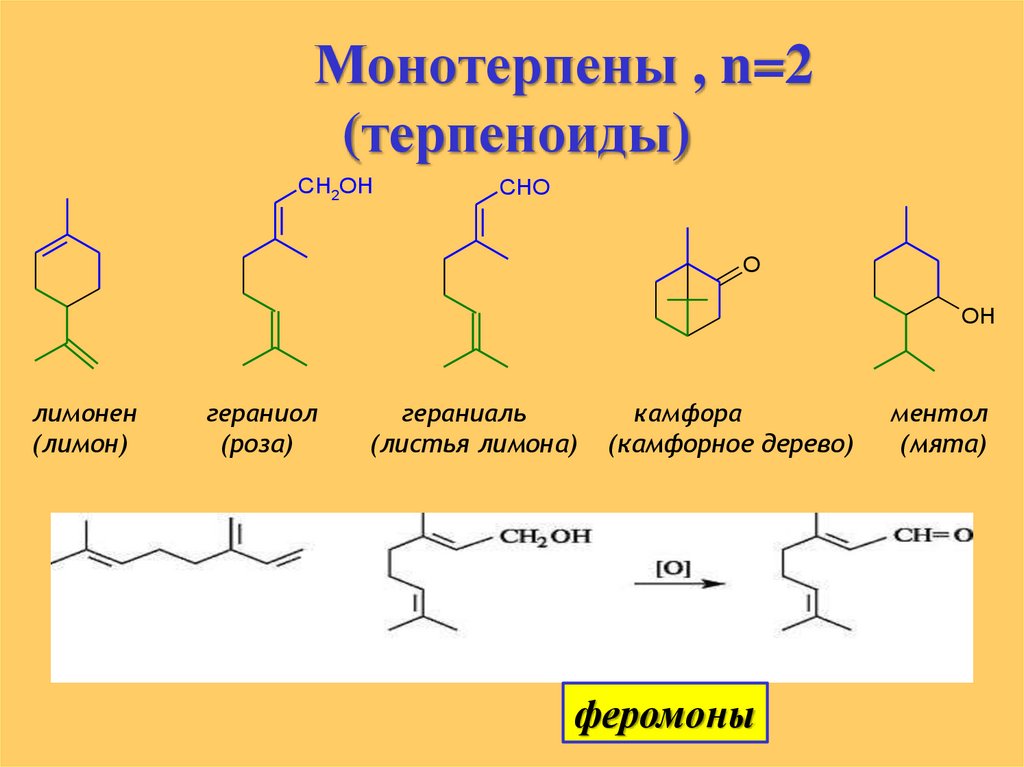
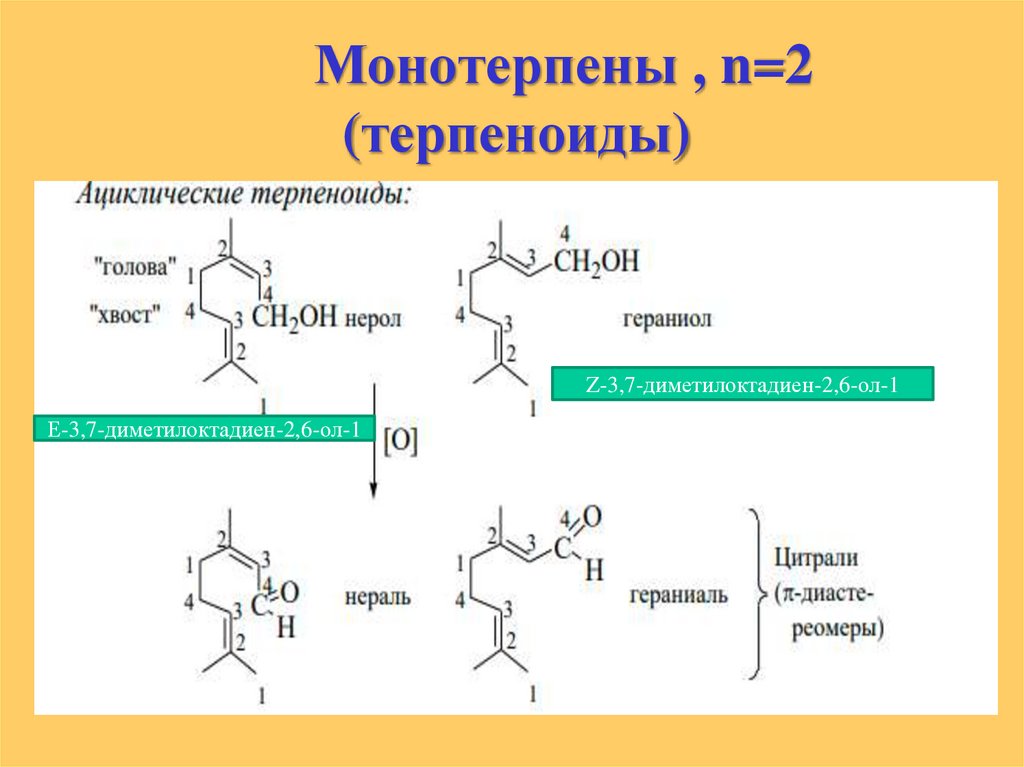
Монотерпены , n=2(терпеноиды)
CH2OH
CHO
O
OH
лимонен
(лимон)
гераниол
(роза)
гераниаль
(листья лимона)
камфора
(камфорное дерево)
феромоны
ментол
(мята)
14.
Монотерпены , n=2(терпеноиды)
Z-3,7-диметилоктадиен-2,6-ол-1
Е-3,7-диметилоктадиен-2,6-ол-1
15.
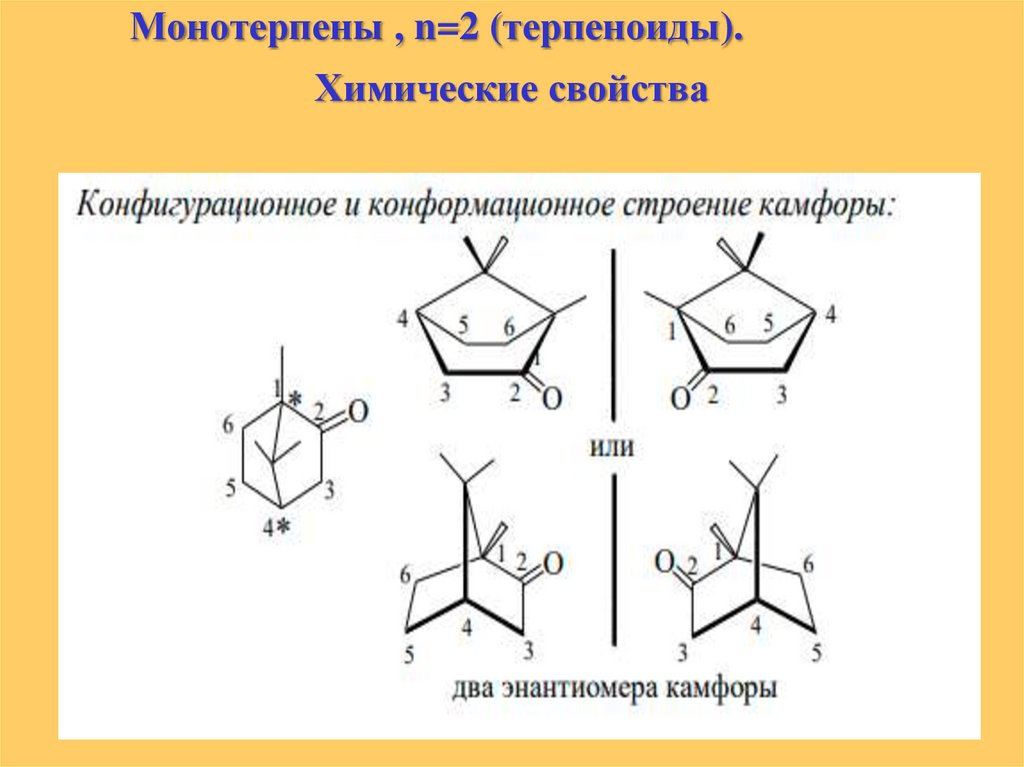
Монотерпены , n=2 (терпеноиды).Химические свойства
Главные типы реакций оцимена и мирцена обусловлены
сопряженными и изолированной двойными связями, нерол
и гераниол показывают реакции и первичных одноатомных
спиртов, цитрали – альдегидов.
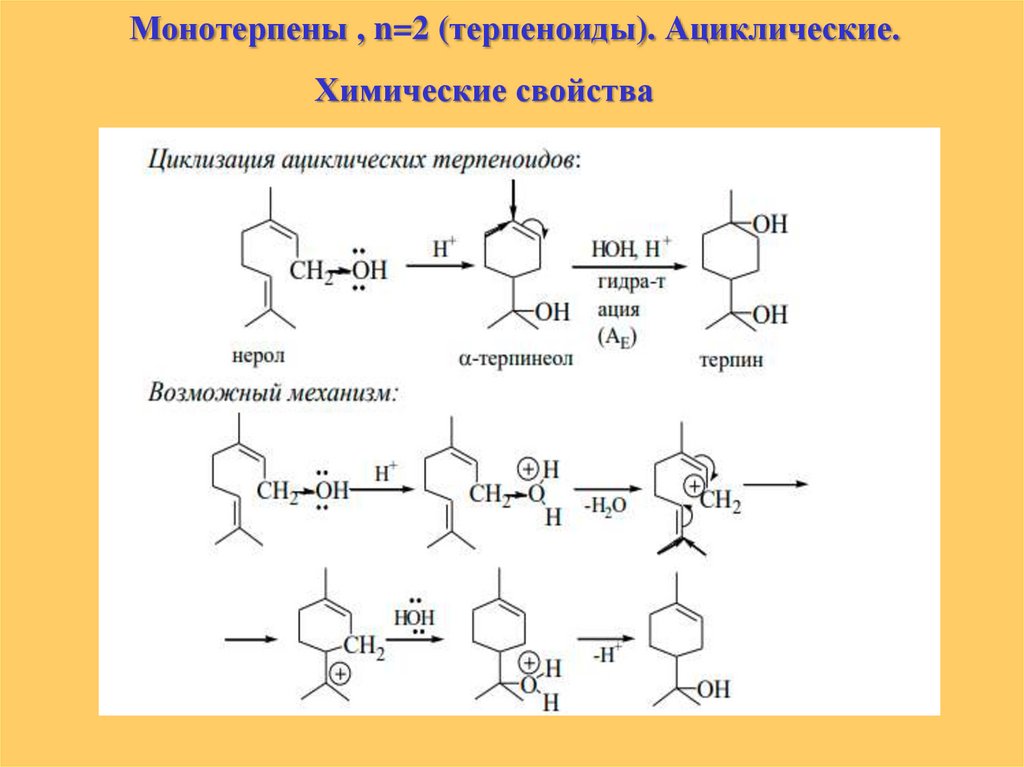
Особенностью реакционной способности ациклических
монотерпеноидов является их склонность к циклизации в
присутствии кислот.
16.
Монотерпены , n=2 (терпеноиды). Ациклические.Химические свойства
17.
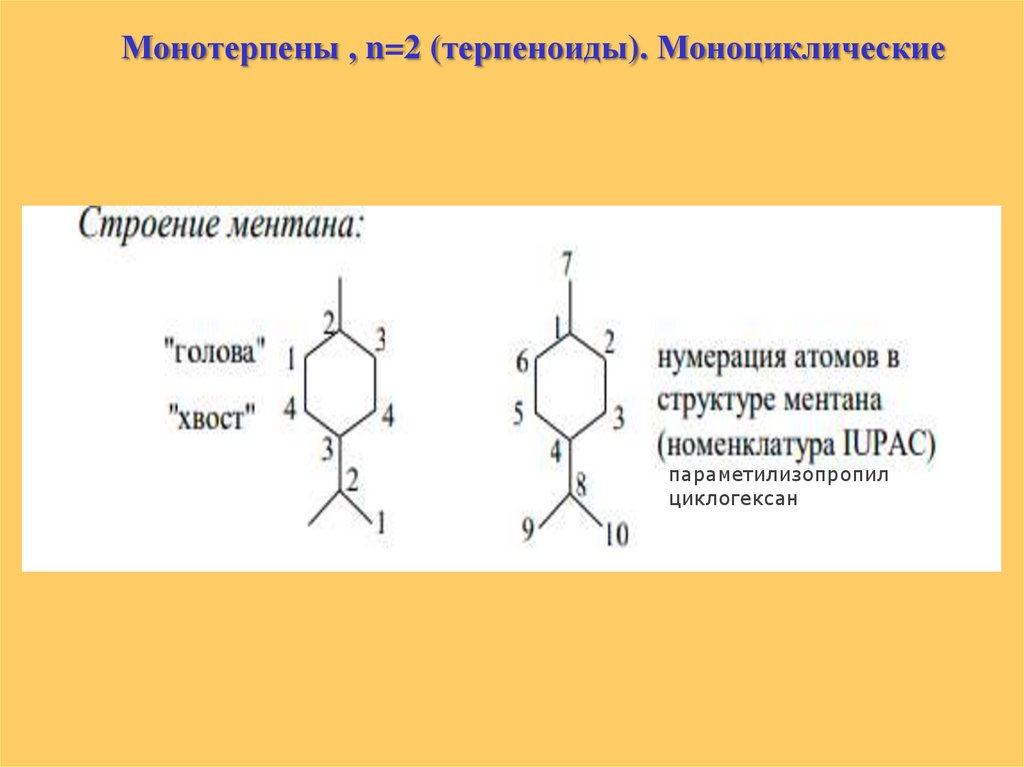
Монотерпены , n=2 (терпеноиды). Моноциклическиепараметилизопропил
циклогексан
18.
Монотерпены , n=2 (терпеноиды). Моноциклические19.
Монотерпены , n=2 (терпеноиды).Моноциклические
Химические свойства
Лимонен (1-метил4-изопропенилциклогексен-1)
20.
Моноциклические терпены(-)-Лимонен
содержится в лимонном масле и
скипидаре. (+)-Лимонен входит в состав
масла тмина.
Рацемическая форма лимонена (дипентен) может быть
получена из изопрена.
21.
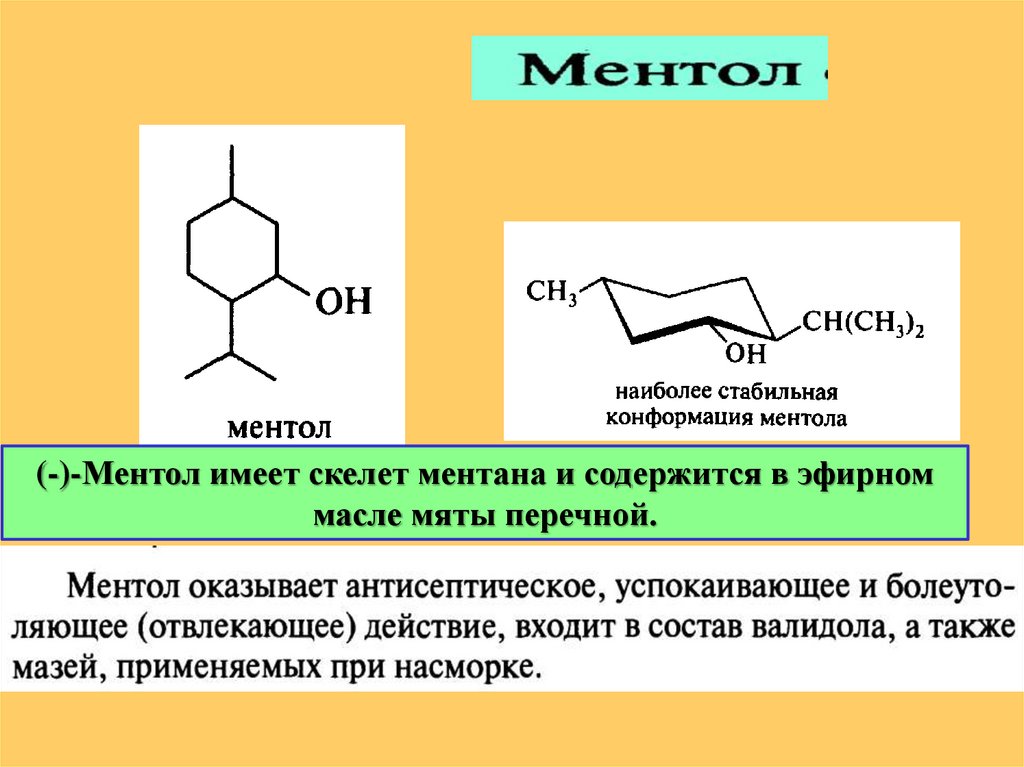
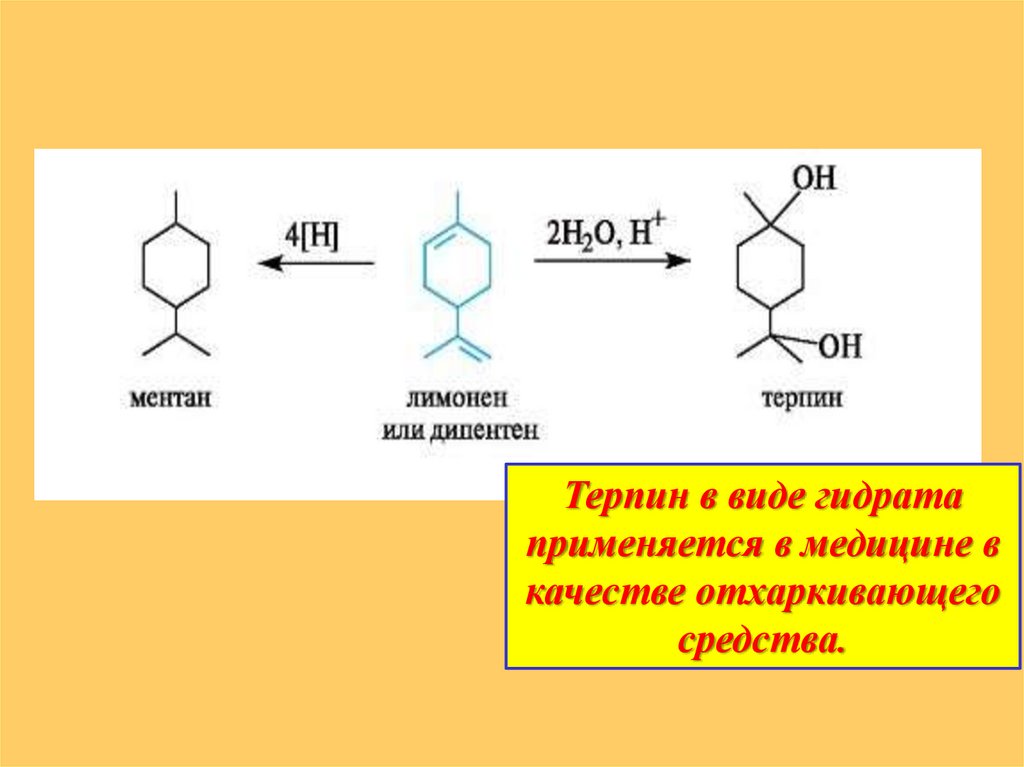
(-)-Ментол имеет скелет ментана и содержится в эфирноммасле мяты перечной.
22.
Терпин в виде гидратаприменяется в медицине в
качестве отхаркивающего
средства.
23.
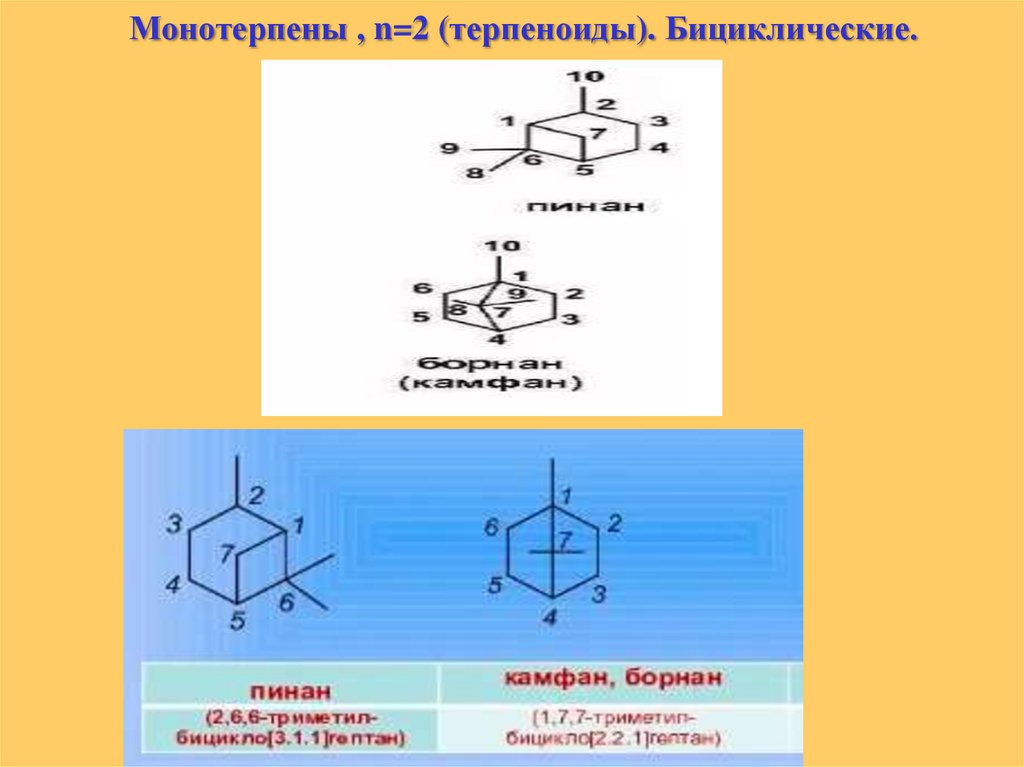
Монотерпены , n=2 (терпеноиды). Бициклические.24.
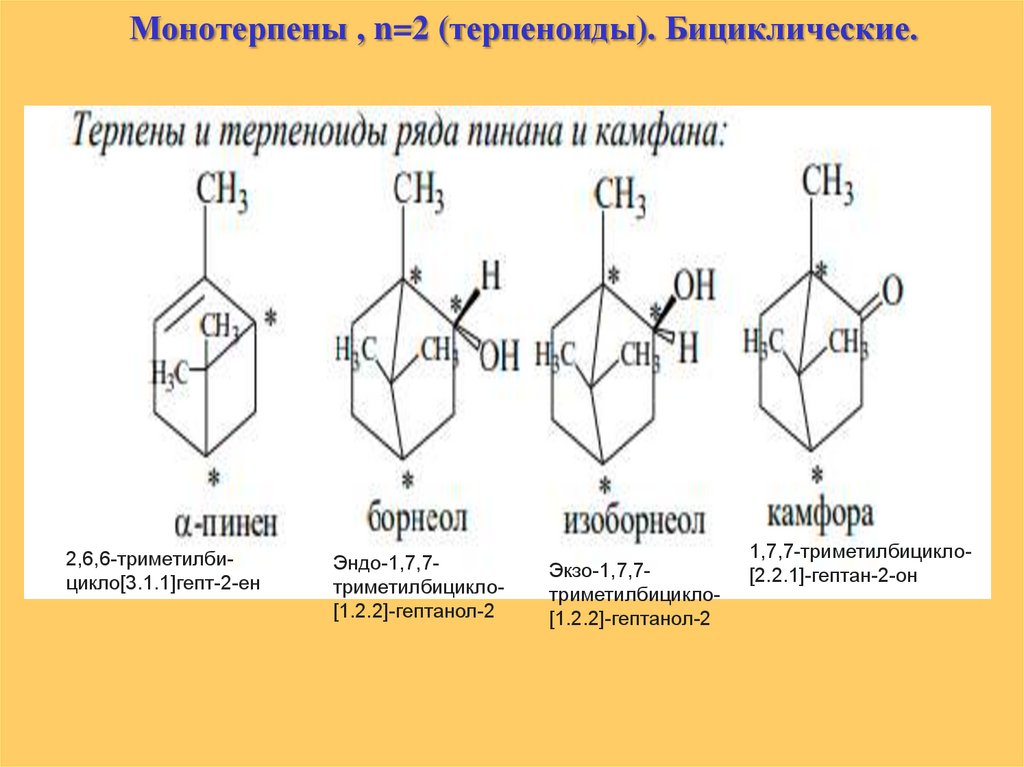
Монотерпены , n=2 (терпеноиды). Бициклические.2,6,6-триметилбицикло[3.1.1]гепт-2-ен
Эндо-1,7,7триметилбицикло[1.2.2]-гептанол-2
Экзо-1,7,7триметилбицикло[1.2.2]-гептанол-2
1,7,7-триметилбицикло[2.2.1]-гептан-2-он
25.
бициклический монотерпен ряда пинанаCH3
C
HC
CH
H3C
C
H2C
a-пинен
C
H
CH3
CH2
26.
Монотерпены , n=2 (терпеноиды). БициклическиеХимические свойства
Стандартные
27.
Монотерпены , n=2 (терпеноиды).Химические свойства
Специфические присоединение
28.
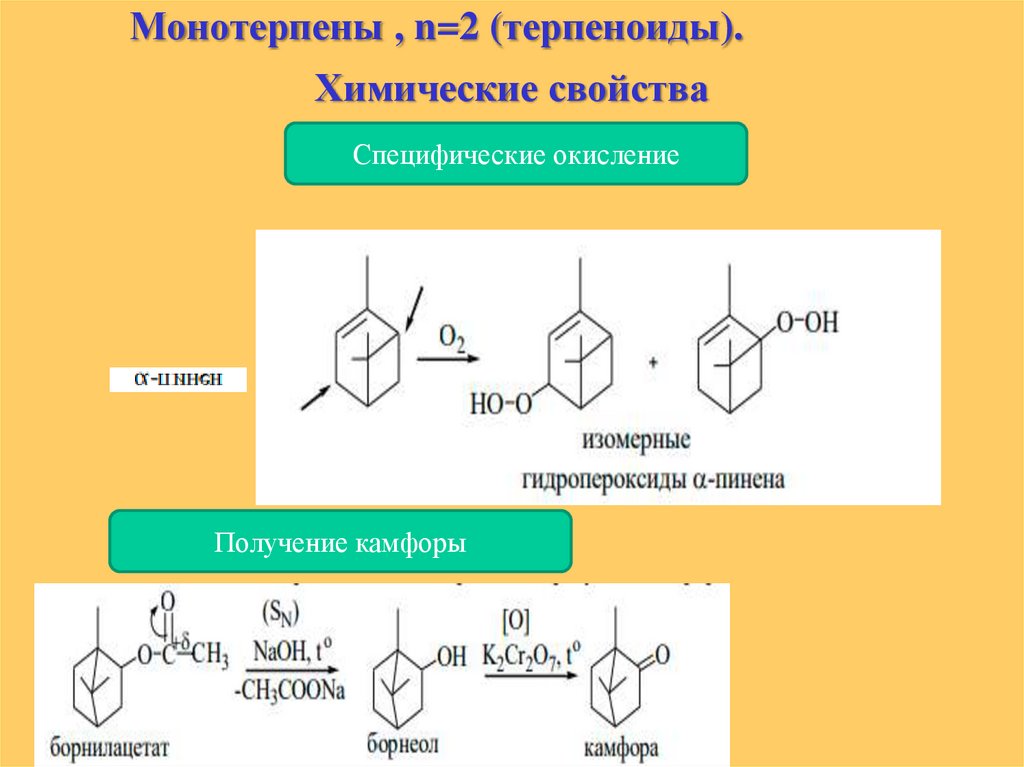
Монотерпены , n=2 (терпеноиды).Химические свойства
Специфические окисление
Получение камфоры
29.
Монотерпены , n=2 (терпеноиды).Химические свойства
30.
Монотерпены , n=2 (терпеноиды).Химические свойства
Примеры реакций камфоры как кетона:
изоборнеол
борнеол
31.
Монотерпены , n=2 (терпеноиды).Химические свойства
32.
α33.
Сесквитерпены, n=3CH2OH
Фарнезол
((2E,6E)-3,7,11-триметилдодека-2,6,10-триен-1-ол) —
спирт, производное терпеноидов.
Фарнезол — вязкая бесцветная жидкость,
сильно разбавленные растворы имеют устойчивый
запах ландышей.
34.
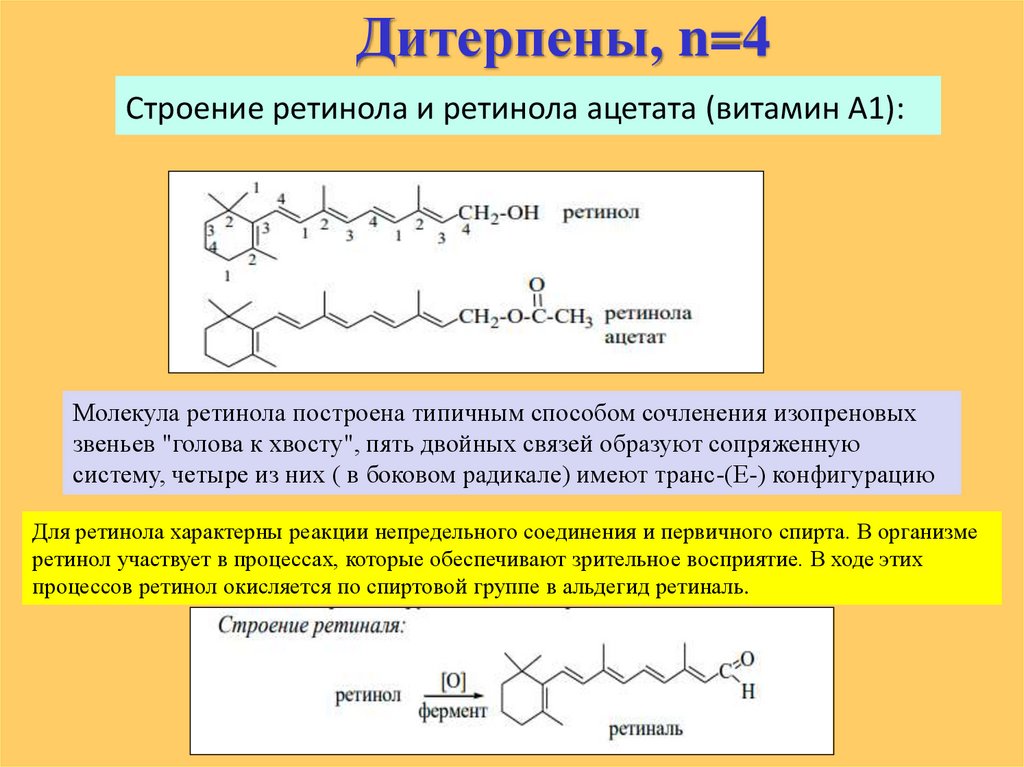
Дитерпены, n=4Строение ретинола и ретинола ацетата (витамин А1):
Молекула ретинола построена типичным способом сочленения изопреновых
звеньев "голова к хвосту", пять двойных связей образуют сопряженную
систему, четыре из них ( в боковом радикале) имеют транс-(Е-) конфигурацию
Для ретинола характерны реакции непредельного соединения и первичного спирта. В организме
ретинол участвует в процессах, которые обеспечивают зрительное восприятие. В ходе этих
процессов ретинол окисляется по спиртовой группе в альдегид ретиналь.
35.
Дитерпены, n=4CH2OH
фитол
Входит в состав хлорофилла, витамина Е, витамина К.
Служит стимулятором роста для молочнокислых бактерий
36.
Тритерпены, n=6.промежуточный продукт в биосинтезе холестерина
Сквален
Сквален является промежуточным соединением в
биологическом синтезе стероидов ,в том числе и
Холестерина,
и участвует в обмене веществ.
Амарантовое
масло (чистый
Сквален)
37.
Тритерпеновые соединения.сквален
OH
HO
HO
амбреин
(из серой амбры)
ланостерин
циклоартенол
38.
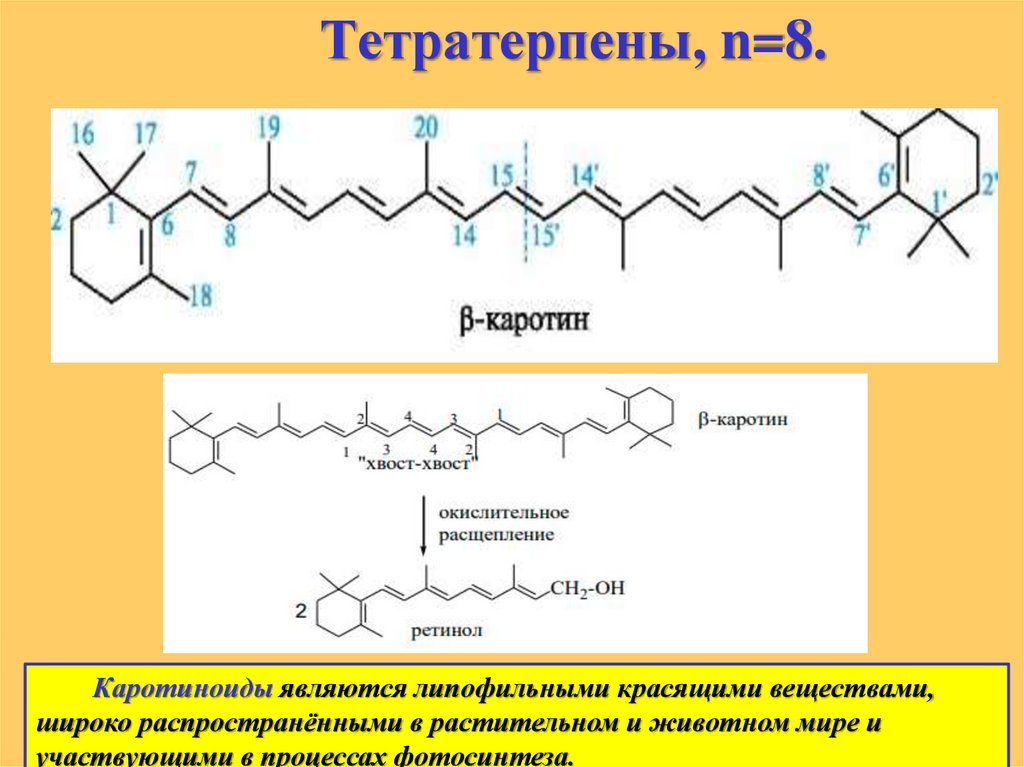
Тетратерпены, n=8.Каротиноиды являются липофильными красящими веществами,
широко распространёнными в растительном и животном мире и
участвующими в процессах фотосинтеза.
39.
Тетратерпеноиды. Каротиноиды.H3C
-каротин
H3 C
CH3
H3C
a-каротин
H3 C
CH3
H3C
-каротин
CH3
H3 C
40.
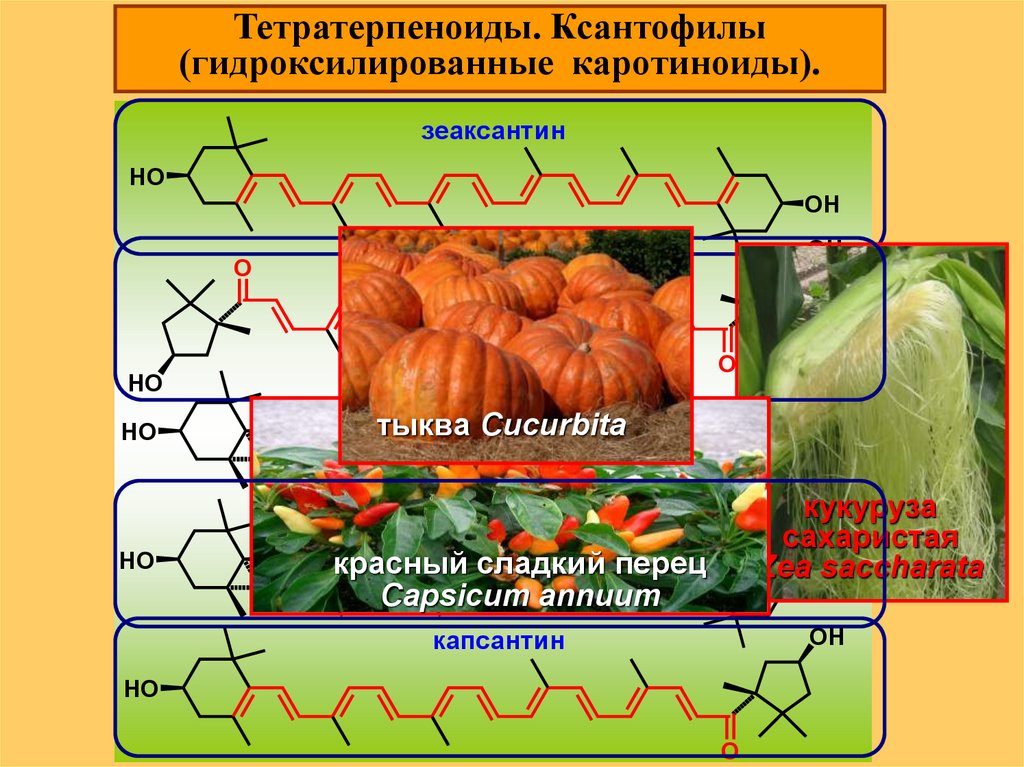
Тетратерпеноиды. Ксантофилы(гидроксилированные каротиноиды).
зеаксантин
HO
OH
OH
капсорубин
O
HO
эпоксид лютеина
HO
тыква Cucurbita
O
O
OH
кyкуруза
сахаристая
Zea saccharata
виолаксантин
HO
O
красный сладкий перецO
Capsicum annuum
OH
капсантин
OH
HO
O
41.
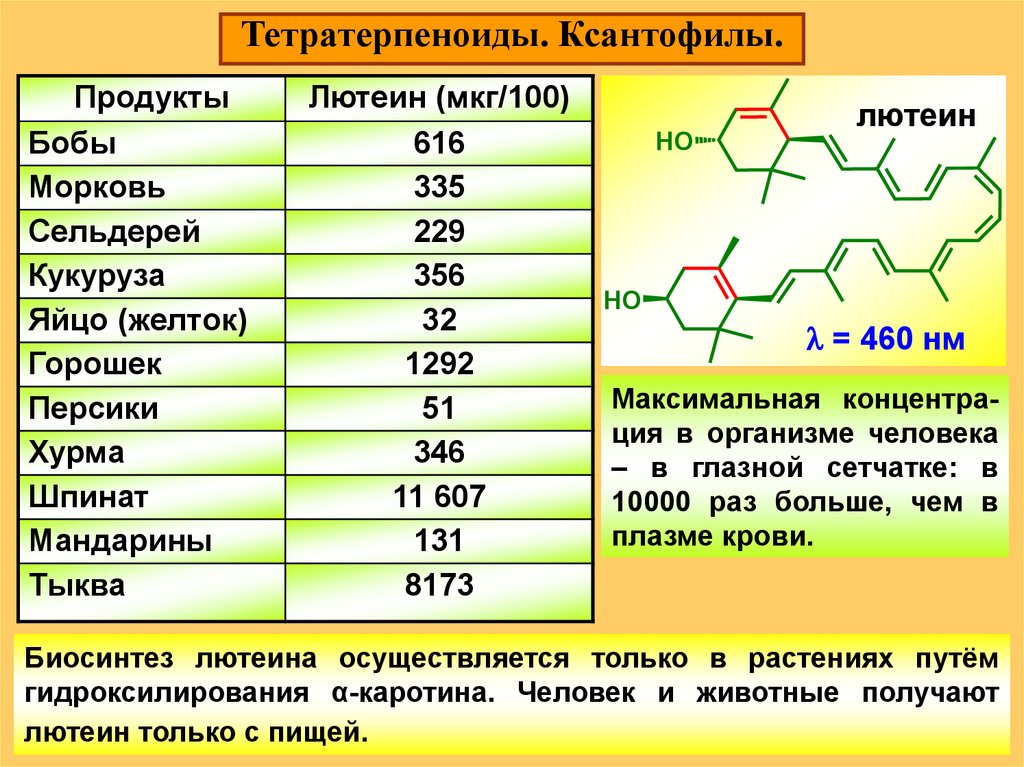
Тетратерпеноиды. Ксантофилы.Продукты
Бобы
Морковь
Сельдерей
Кукуруза
Яйцо (желток)
Горошек
Персики
Хурма
Шпинат
Мандарины
Тыква
Лютеин (мкг/100)
616
335
229
356
32
1292
51
346
11 607
131
8173
HO
лютеин
HO
= 460 нм
Максимальная концентрация в организме человека
– в глазной сетчатке: в
10000 раз больше, чем в
плазме крови.
Биосинтез лютеина осуществляется только в растениях путём
гидроксилирования α-каротина. Человек и животные получают
лютеин только с пищей.
42.
Стероиды12
11
1
2
3
10
A
4
C
9
B
5
13
R
CH
12
3 17
17
D
8 14
16
11
H3C 9
15
2
7
6
1
4
B
5
16
D
15
8 14
10
3A
X
13
C
7
6
Стеран (гонан)
общий скелет стероидов
Структура и нумерация атомов по IUPAC
(X=OH, OR )
Конформация
CH3
A
5
a
H
CH3
H
C
B
H
D
H
CH3
H
H
C
B
5
A
CH3
H
5α-стероид
5 -стероид
(транс-сочленение А/В)-более устойчива
(цис-сочленение А/В)
H
D
43.
СТЕРОИДЫCH3
CH3
C
H3C
H
H
A
Конфигурация
D
H
H
A
H
B
C
H3C
5α-стероид
H
D
H
B
H
5 -стероид
У природных стероидов
углеводородные заместители атомов
углерода С10, С13 и С17 имеют
β-конфигурацию
.
Соласодин является ценным сырьем для производства прогестерона
и кортикостероидов, а диосгенин – для промышленного синтеза кортикостероидов и андрогенов.
H
H
H3C
H3C
N
CH3
H3C
O
H3C
H
H3C
H
H
H
H
O
H3C
O
H
H
HO
HO
соласодин
диосгенин
H
CH3
44.
СТЕРОИДЫ. Классификация и номенклатура45.
АНДРОГЕНЫ. Мужские половые гормоныCH3
OH
H3C
тестостерон
O
Строение тестостерона.
46.
АНДРОГЕНЫ. Мужские половые гормоныТестостерона пропионат и Тестостерона этантат (гептилат) самые востребованные в бодибилдинге стероиды.
Предназначены для развития мышечной массы и силы
47.
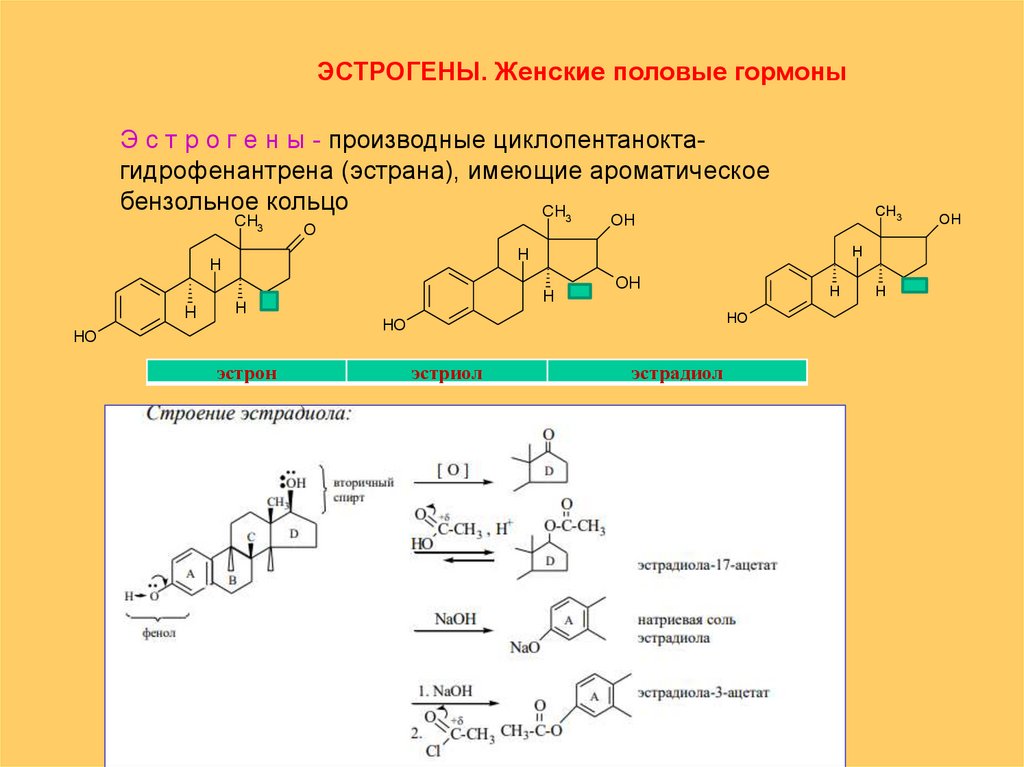
ЭСТРОГЕНЫ. Женские половые гормоныЭ с т р о г е н ы - производные циклопентаноктагидрофенантрена (эстрана), имеющие ароматическое
бензольное кольцо
CH3
CH3
H
H
H
H
CH3
OH
O
H
HO
эстрон
H
OH
H
HO
HO
эстриол
эстрадиол
H
OH
48.
Женские половые гормоныCH3
CH3
O
H
H
H
H
H
HO
H
HO
эстрон
эстрадиол
OH
49.
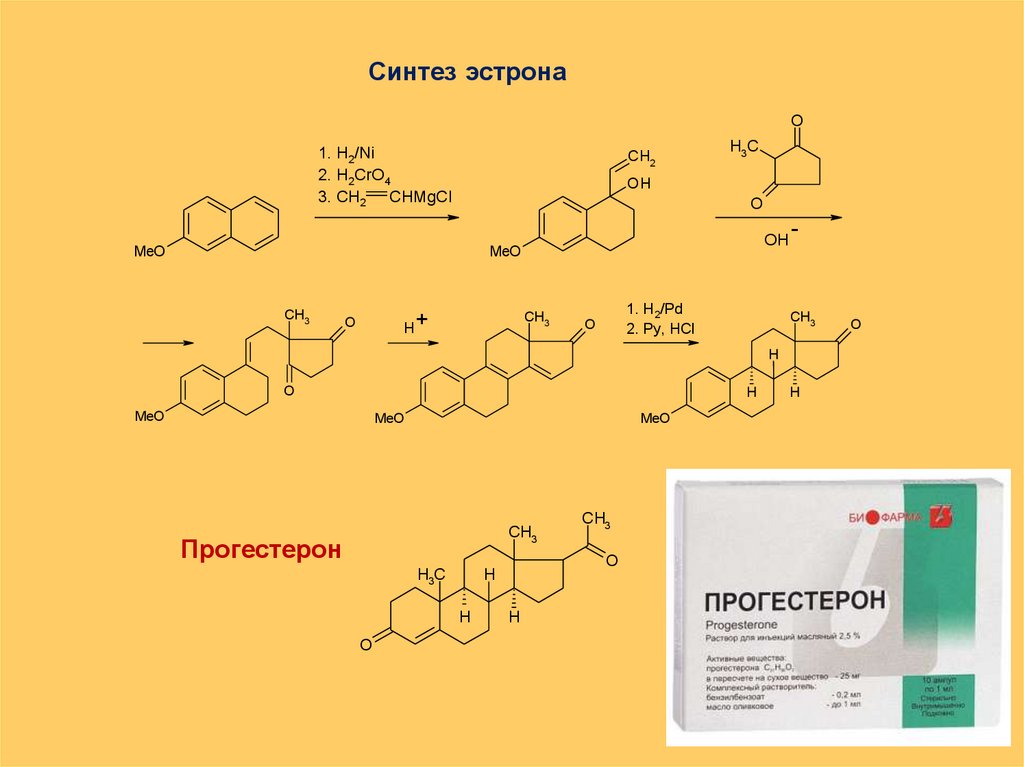
Синтез эстронаO
1. H2/Ni
2. H2CrO4
3. CH2 CHMgCl
CH2
H3C
OH
O
MeO
OH
MeO
CH3
H+
O
CH3
1. H2/Pd
2. Py, HCl
O
-
CH3
H
O
H
MeO
MeO
MeO
CH3
Прогестерон
H3C
O
O
H
H
CH3
H
H
O
50.
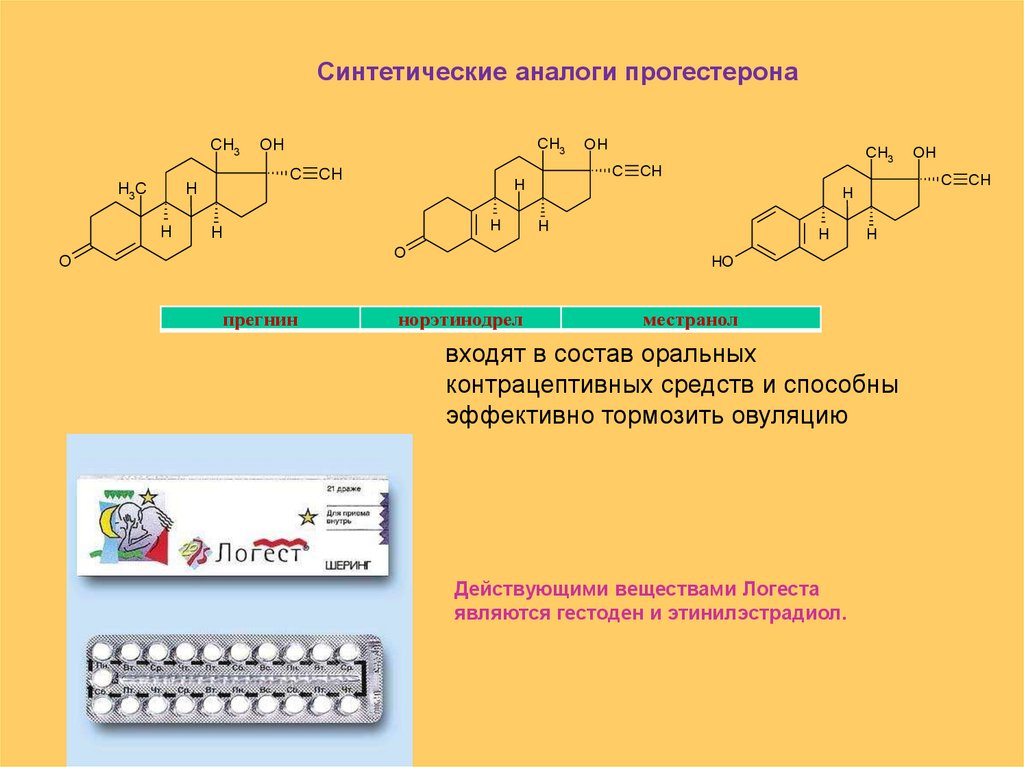
Синтетические аналоги прогестеронаCH3
H3C
C
H
H
CH3
OH
CH
H
O
O
прегнин
C
H
H
OH
CH3
CH
C
H
H
H
H
HO
норэтинодрел
местранол
входят в состав оральных
контрацептивных средств и способны
эффективно тормозить овуляцию
Действующими веществами Логеста
являются гестоден и этинилэстрадиол.
OH
CH
51.
Кортикостероиды52.
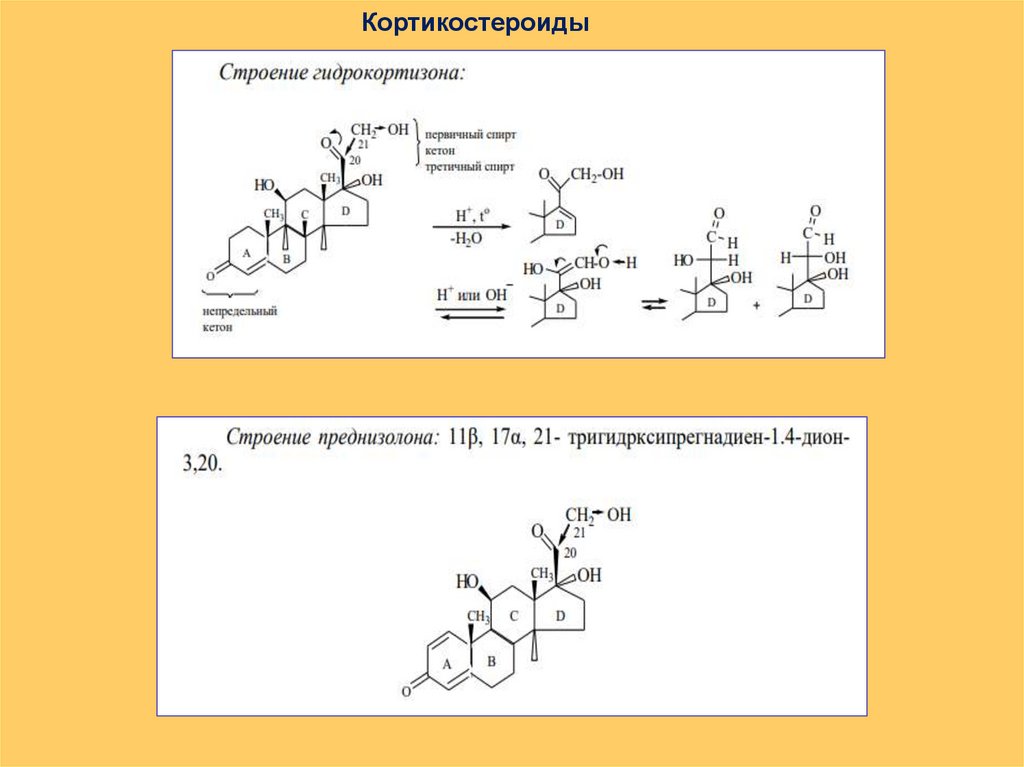
КортикостероидыO
OH
HO
H3C
O
OH
H
H
OH
O
OH
H3C
H
H
кортизол (гидрокортизон)
H3C
H
H
OH
H
O
кортизон
O
HO
H
O
O
OH
OH
H
H
O
альдостерон
53.
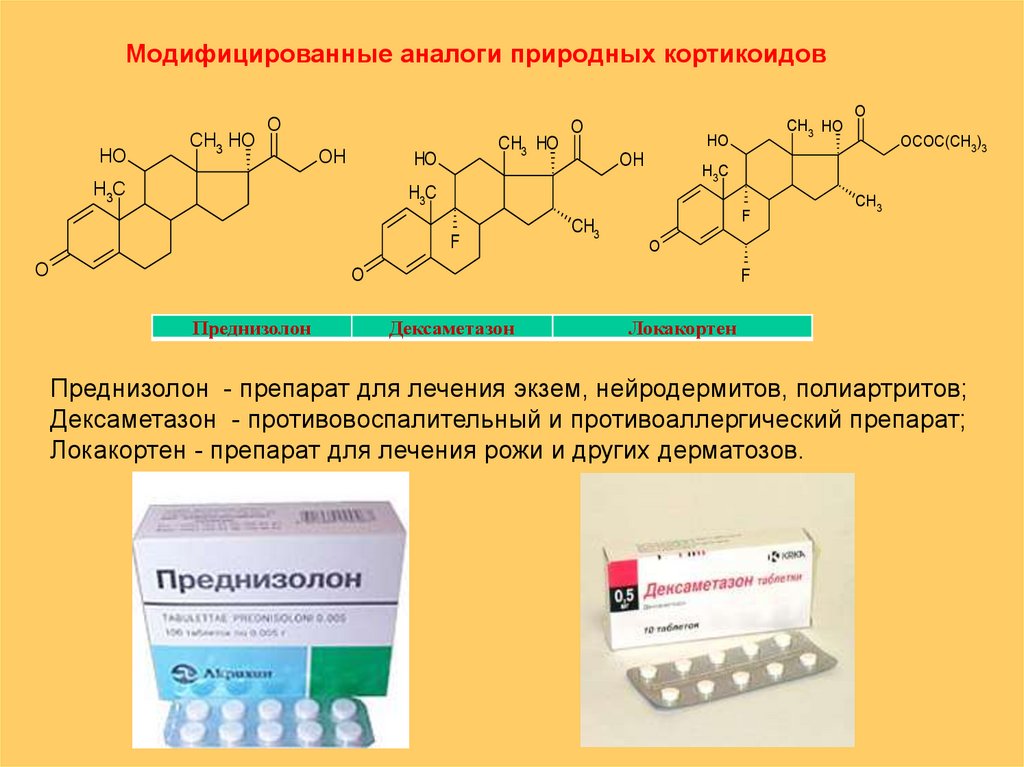
Модифицированные аналоги природных кортикоидовHO
CH3 HO
O
OH
CH3 HO
HO
H3C
O
HO
OH
O
CH3
F
OCOC(CH3)3
CH3
O
O
Преднизолон
O
H3C
H3C
F
CH3 HO
F
Дексаметазон
Локакортен
Преднизолон - препарат для лечения экзем, нейродермитов, полиартритов;
Дексаметазон - противовоспалительный и противоаллергический препарат;
Локакортен - препарат для лечения рожи и других дерматозов.
54.
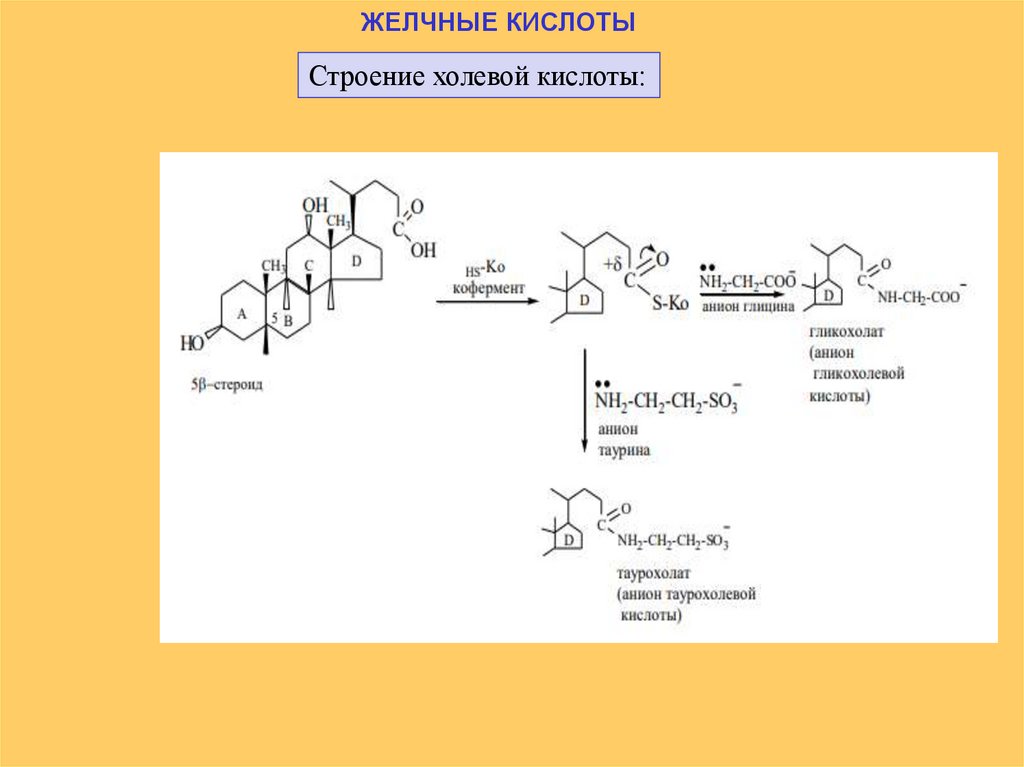
ЖЕЛЧНЫЕ КИСЛОТЫСтроение холевой кислоты:
55.
СТЕРИНЫСтроение эргостерина и витамина Д2:
56.
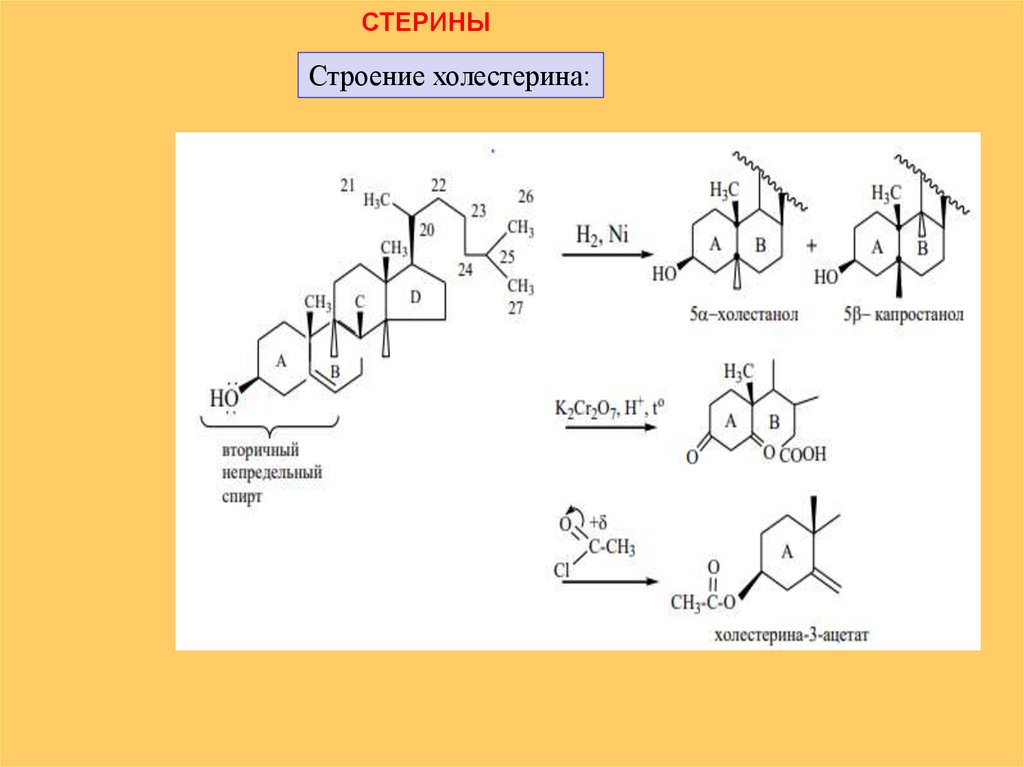
СТЕРИНЫСтроение холестерина:
57.
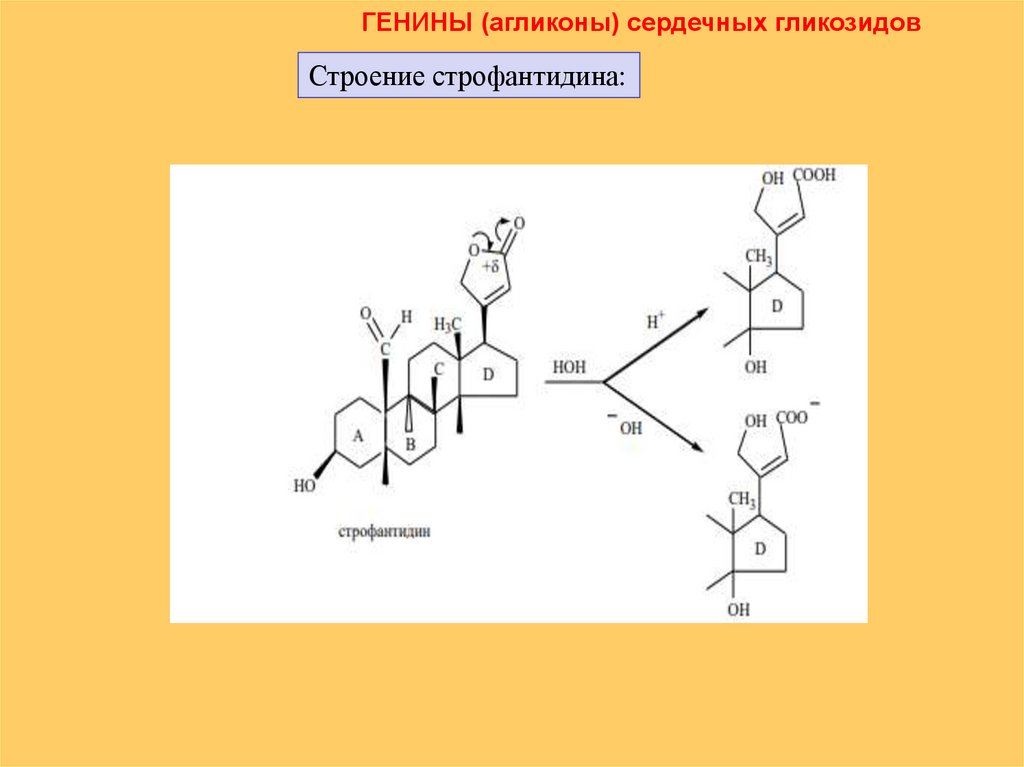
ГЕНИНЫ (агликоны) сердечных гликозидовСтроение строфантидина:
58.
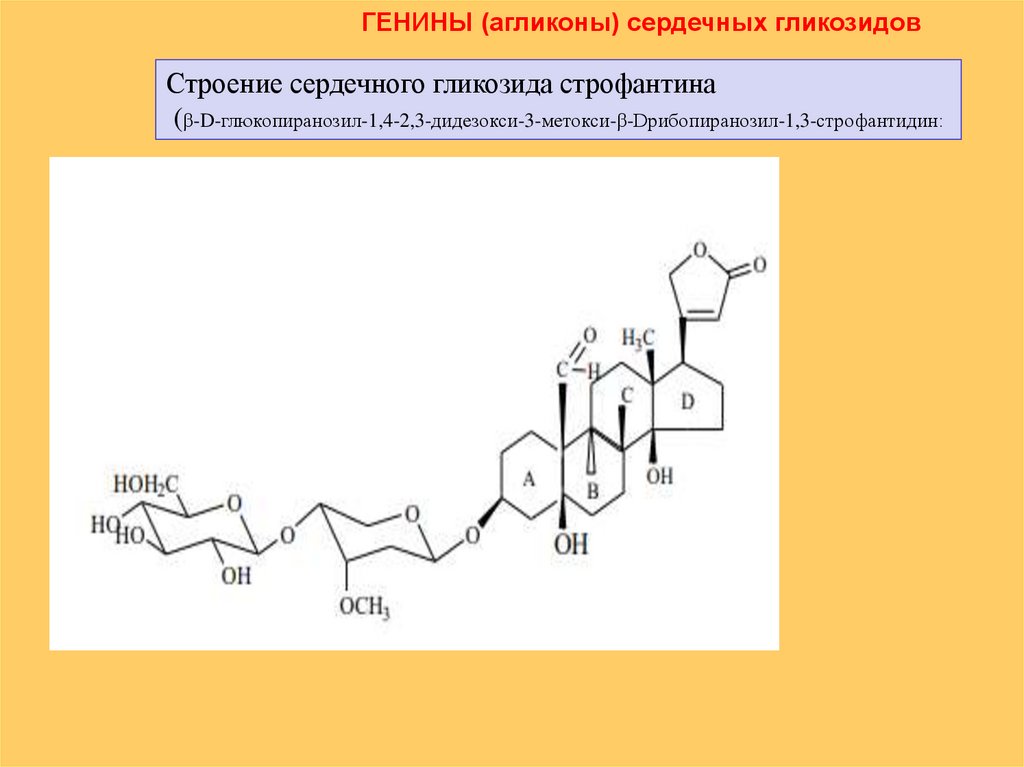
ГЕНИНЫ (агликоны) сердечных гликозидовСтроение сердечного гликозида строфантина
(β-D-глюкопиранозил-1,4-2,3-дидезокси-3-метокси-β-Dрибопиранозил-1,3-строфантидин:
59.
Л И Т Е РАТ У РАа). Использованная при подготовке текста лекции
1. Оганесян Э.Т. Органическая химия. – 2-е издание. – М.: Академия, 2011.432 с.
2. Органическая химия: учебник/Н.А. Тюкавкина и [др.]; под ред.
Н.А.Тюкавкиной. –М.: ГЭОТАР-Медиа, 2015.-640с.
3. Артеменко А.И. Органическая химия. – М.: Высшая школа, 1998.- 545 с.
4. Травень В.Ф. Органическая химия (в 3 томах) – 4-е издание.- М.: БИНОМ,
2015.
5. Иванов В.Г., Горленко В.А., Гева О.Н. Органическая химия – М: Инфра-М,
2016.560 с.
6. Дрюк В.Г., Карцев В.Г., Хиля В.П. Органическая химия. Учебное пособие
для вузов:
3-е издание. – М.: ЮРАЙТ, 2020. – 502 с.
б). Рекомендуемая обучаемым для самостоятельной работы по теме лекции
1. Оганесян Э.Т. Органическая химия. – 2-е издание. – М.: Академия, 2011.- с.
329-351
2. Белобородов В.Л., Зурабян С.Э., Лузин А.П., Тюкавкина Н.А. Органическая
химия. Специальный курс.-Т.2 - М: Дрофа, 2008.- с. 317-359
59

































 chemistry
chemistry








