Similar presentations:
Примеры решения задач. Водородоподобные атомы. Оптические спектры излучения
1. Примеры решения задач.
6.7. Примерырешения задач.
Водородоподобные
атомы.
Оптические спектры
излучения.
2.
А1. Найти радиусы rk трёх первых боровских электронных орбит в атомеводорода и скорости vk электрона на них.
Дано:
k1 = 1
k3 = 3
Решение.
Согласно теории Бора, электрон в атоме водорода может
находиться на орбитах с радиусами
Rn 4 0
rk - ?
Vk - ?
2
mZe2
n2 .
Здесь n – целое число, Z = 1.
Радиус орбиты произвольного состояния с любым номером n удобно выражать
через радиус первой боровской орбиты:
Rn R1 n 2 .
Для атома водорода (Z = 1)
R1 4 0
2
me2
n2 0,529 10 10 (м).
R2 R1 22 4 0,529 10 10 2,12 10 10 (м).
R3 R1 32 9 0,529 10 10 4, 76 10 10 (м).
3.
А1. Найти радиусы rk трёх первых боровских электронных орбит в атомеводорода и скорости vk электрона на них.
Решение (продолжение).
Скорость электрона в атоме водорода определим из второго закона Ньютона.
Ze 2
ma
,
2
4 0 R
V2
a .
R
1
где V - скорость электрона, R - радиус орбиты, Z = 1.
V2
1 e2
m
,
2
R 4 0 R
e2
Vn
.
4 0 mRn
1
R1 4 0
2
me2
R2 22 R1 2,12 10 10 (м).
n2 0,529 10 10 (м).
R3 R1 32 4, 76 10 10 (м).
4.
А1. Найти радиусы rk трёх первых боровских электронных орбит в атомеводорода и скорости vk электрона на них.
Решение (продолжение).
e2
Vn
.
4 0 mRn
1
1
2,56 10 38
6
(м/c).
V1
2,
2
10
12
31
11
4 8,85 10
9,1 10 5, 29 10
V1
e2
Vn
.
2
4 0 mR1n
n
1
V1
V2 1,1 106 (м/c).
2
V1
V3 0, 73 106 (м/c).
3
Ответ: r1 = 53 пм; r2 = 212 пм; r3 = 477 пм; v1 = 2,19·106 м/с; v2 = l,1· 106 м/c;
v3 =7,3 ·105 м/c.
5.
А2. Найти период Т обращения электрона на первой боровской орбите атомаводорода и его угловую скорость ω.
Дано:
n=1
Z=1
T-?
ω-?
Решение.
Угловую скорость электрона в атоме водорода определим из
второго закона Ньютона.
Ze 2
ma
,
2
4 0 R
1
a 2 R.
где ω - скорость электрона, R - радиус орбиты, Z = 1.
e2
m R
,
2
4 0 R
1
2
e2
.
3
4 0 mR
1
1
2,56 10 38
16
(рад/c).
4,
4
10
12
31
3
33
4 8,85 10
9,1 10 5, 29 10
6.
А2. Найти период Т обращения электрона на первой боровской орбите атомаводорода и его угловую скорость
Решение (продолжение).
Период обращения по орбите связан с угловой скоростью простым
соотношением:
T
2
.
2
6, 28
16
T
1,
43
10
(c).
16
4, 4 10
Ответ: Т =1,43·10-16 с; ω = 4,4·1016 рад/с.
7.
B2. Определить ток, соответствующий движению электрона по п-й орбите атомаводорода.
Решение .
Ток, связанный с движением электрона в атоме водорода
q
I
.
t
Δq – заряд, проходящий через поперечное сечение
проводника за время Δt.
В качестве сечения проводника рассмотрим плоскость
AB на рисунке. Её пересекает один электрон за время,
равное периоду обращения электрона вокруг ядра.
q e,
I
t T .
q e
,
t T
T
2
,
I
q e
1
e .
t T 2
Угловую скорость электрона ω в атоме водорода определим из второго закона
Ньютона.
Ze 2
ma
,
2
4 0 R
1
a 2 R.
где ω - скорость электрона, R - радиус орбиты, Z = 1.
8.
B2. Определить ток, соответствующий движению электрона по п-й орбите атомаводорода.
Решение (продолжение) .
Ze 2
ma
,
2
4 0 R
1
e2
2
m R
,
2
4 0 R
1
a 2 R.
e2
.
3
4 0 mR
1
1
1 e2
1
e
,
I
e
3
2
2
4 0 mR
Согласно теории Бора, электрон в атоме водорода может находиться на орбитах
с радиусами
2
Rn 4 0
me2
n2 ,
n – целое число.
1
1 e2
1
1 e2
m3e6
I
e
e
,
3 6 6
3
2
4 0 mR
2
4 0 m 4 0 n
9.
B2. Определить ток, соответствующий движению электрона по п-й орбите атомаводорода.
Решение (продолжение) .
1
1 e2
m3e6
I
e
3 6 6
2
4 0 m 4 0 n
1
e
2
m2e8
4 0
4
6 6
,
n
1
me5
I
.
2 3 3
2 4 0 n
1
me5
81 1018 9,1 10 31 10, 49 10 95
I
2 3 3
102
2 4 0 n
6, 28
1,16 10
7,73 104 10 108
102 1, 06 10 2 ( A).
7, 27 10
Ответ: I1 =1,06·10-2 A.
10.
B1. Фотон с энергией E = 16,5 эВ выбивает электрон из невозбуждённого атомаводорода. Какую скорость будет иметь электрон вдали от ядра?
Дано:
E = 16,5 эВ
n=1
V-?
Решение.
Энергия электрона в основном состоянии в атоме водорода
Eel E1 13,6 (эВ).
После поглощения атомом фотона энергия электрона станет
Eel E1 E ph 13, 6 16,5 2,9 (эВ).
Энергия электрона больше нуля, следовательно, он удалится от ядра атома на
сколь угодно большое расстояние. При этом его потенциальная энергия станет
равной нулю, а кинетическая
2
T
mV
Eel .
2
Скорость электрона на большом удалении от ядра
2 Eel
V
.
m
2Eel
2 2,9 1,6 10 19
6
(м/с).
V
1,0
10
31
m
9,1 10
Ответ: v =1·106 м/с.
11.
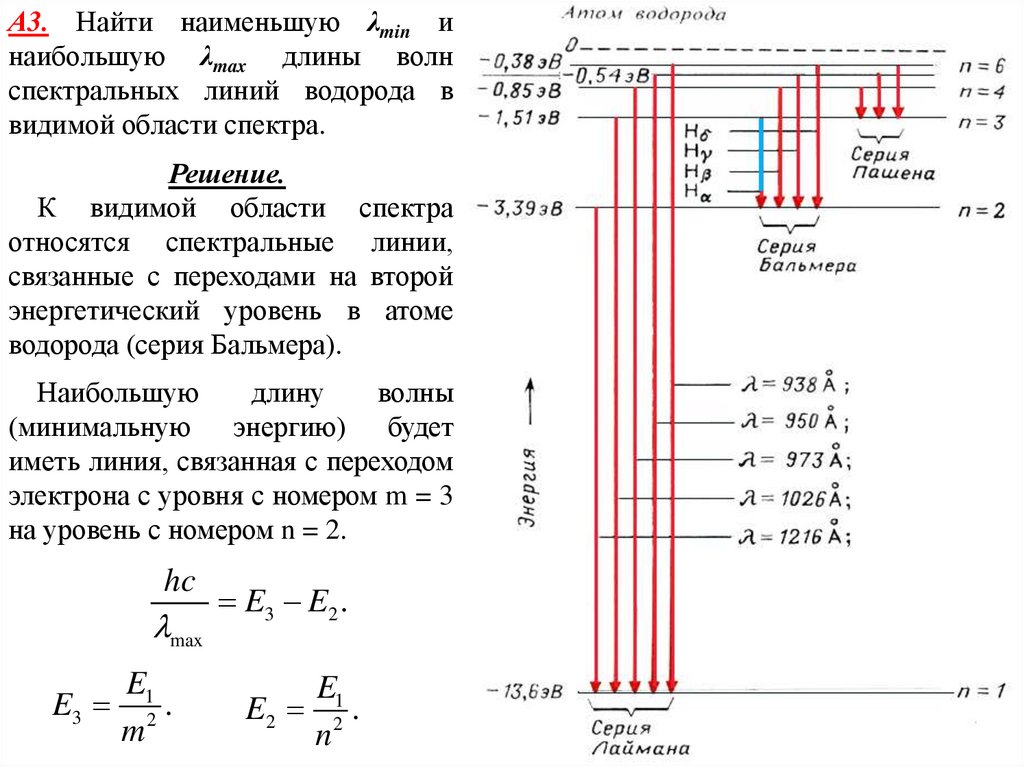
А3. Найти наименьшую λmin инаибольшую λmax длины волн
спектральных линий водорода в
видимой области спектра.
Решение.
К видимой области спектра
относятся спектральные линии,
связанные с переходами на второй
энергетический уровень в атоме
водорода (серия Бальмера).
Наибольшую
длину
волны
(минимальную энергию) будет
иметь линия, связанная с переходом
электрона с уровня с номером m = 3
на уровень с номером n = 2.
hc
max
E1
E3 2 .
m
E3 E2 .
E1
E2 2 .
n
12.
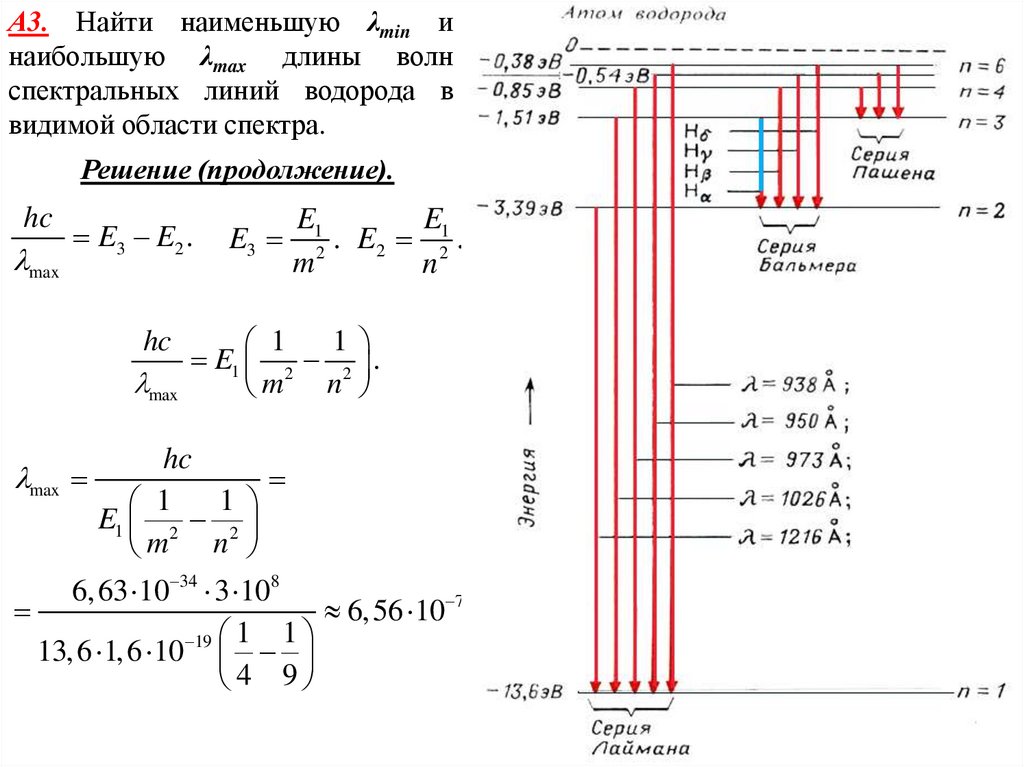
А3. Найти наименьшую λmin инаибольшую λmax длины волн
спектральных линий водорода в
видимой области спектра.
Решение (продолжение).
hc
max
E3 E2 .
hc
max
max
E3
E1
E1
.
E
.
2
2
2
m
n
1
1
E1 2 2 .
m n
hc
1
1
E1 2 2
m n
6, 63 10 34 3 108
6,56 10 7
1
19 1
13, 6 1, 6 10
(м).
4 9
13.
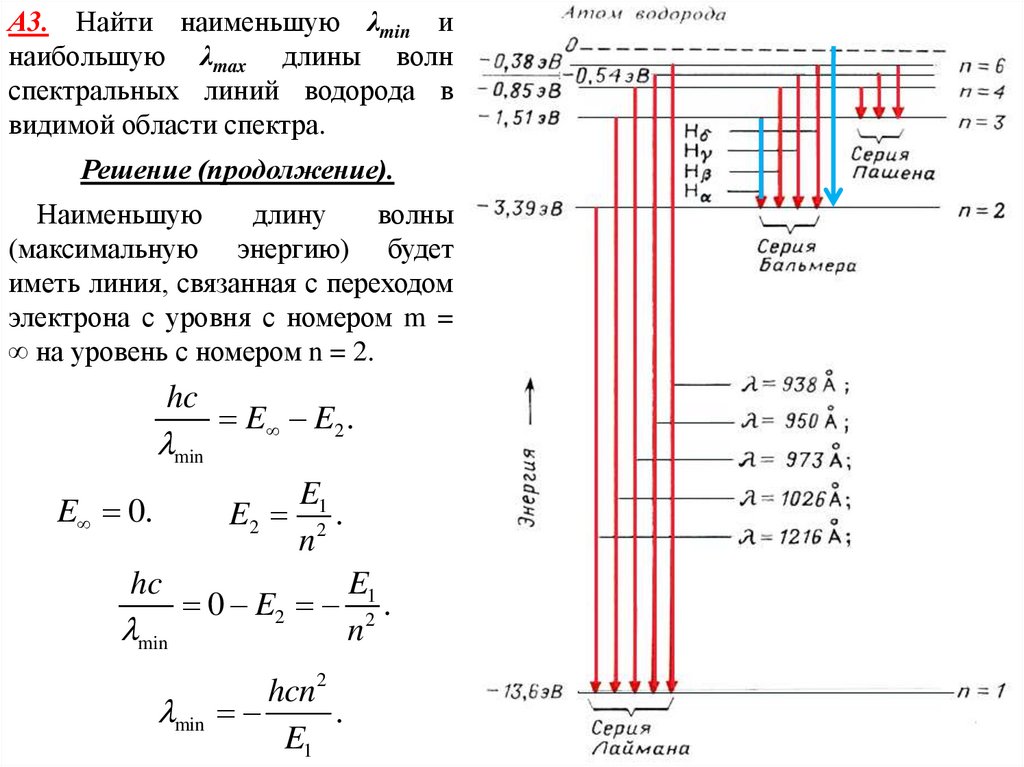
А3. Найти наименьшую λmin инаибольшую λmax длины волн
спектральных линий водорода в
видимой области спектра.
Решение (продолжение).
Наименьшую
длину
волны
(максимальную энергию) будет
иметь линия, связанная с переходом
электрона с уровня с номером m =
∞ на уровень с номером n = 2.
hc
min
E E2 .
E 0.
E1
E2 2 .
n
hc
0 E2
min
min
hcn2
.
E1
E1
.
2
n
14.
А3. Найти наименьшую λmin и наибольшую λmax длины волн спектральных линийводорода в видимой области спектра.
Решение (продолжение).
min
min
hcn2
.
E1
hcn2 6, 63 10 34 3 108 4
7
3,
65
10
(м).
19
E1
13, 6 1, 6 10
Ответ: λmin =365 нм; λmax =656 нм.
15.
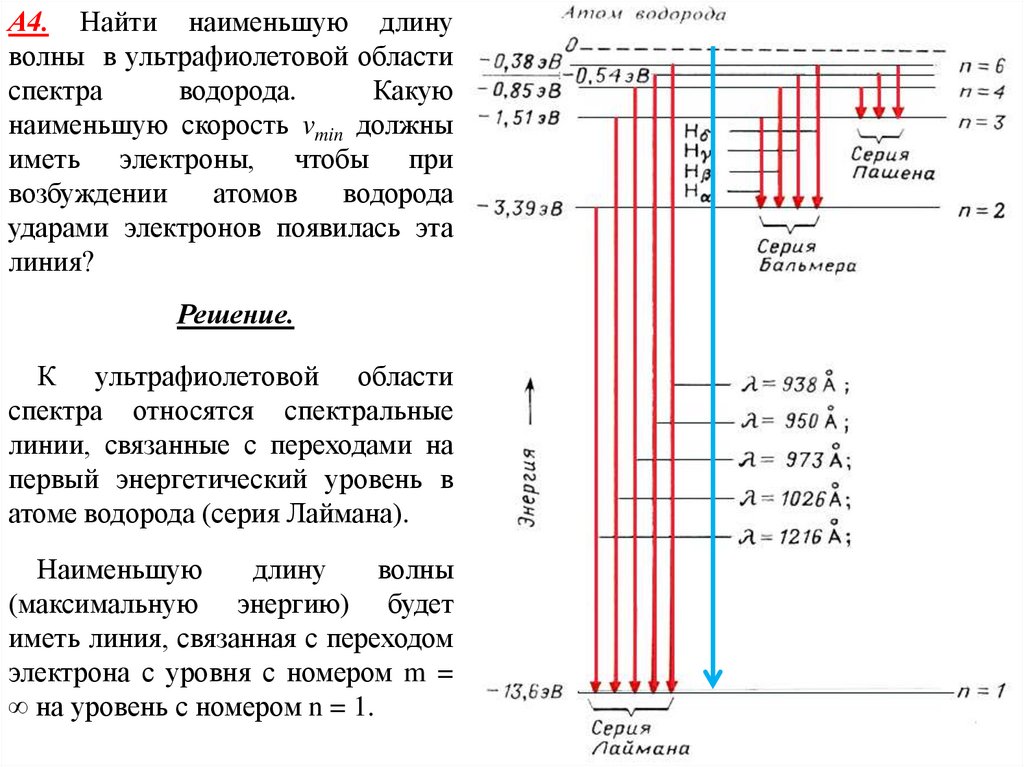
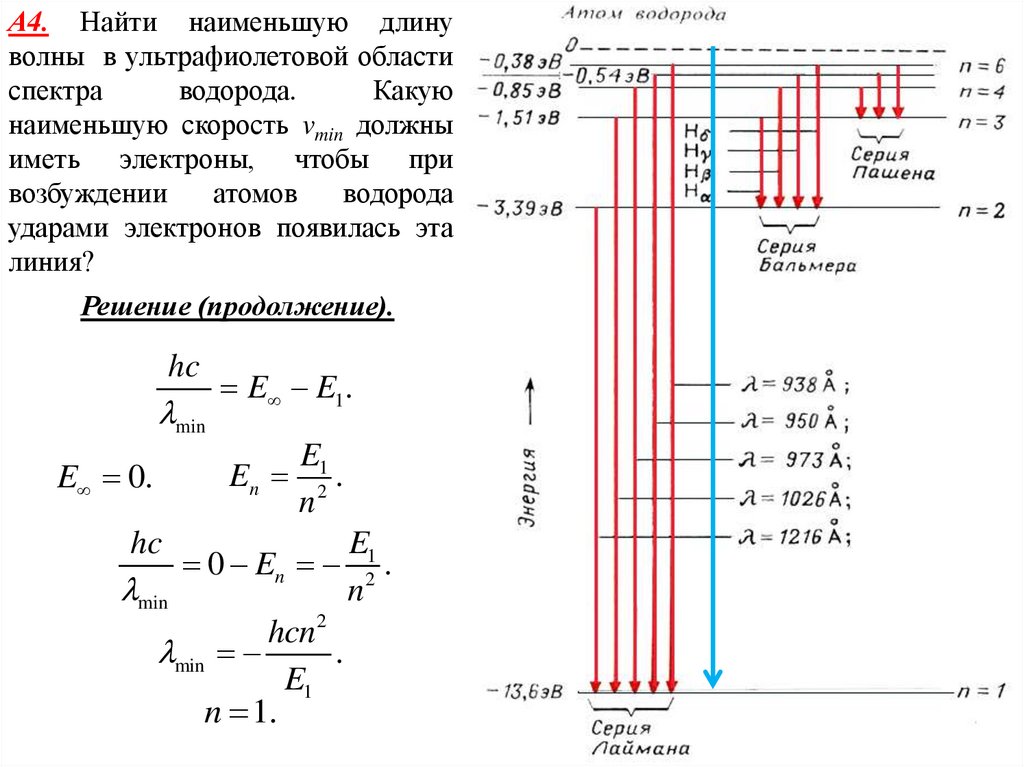
А4. Найти наименьшую длинуволны в ультрафиолетовой области
спектра
водорода.
Какую
наименьшую скорость vmin должны
иметь электроны, чтобы при
возбуждении
атомов
водорода
ударами электронов появилась эта
линия?
Решение.
К ультрафиолетовой области
спектра относятся спектральные
линии, связанные с переходами на
первый энергетический уровень в
атоме водорода (серия Лаймана).
Наименьшую
длину
волны
(максимальную энергию) будет
иметь линия, связанная с переходом
электрона с уровня с номером m =
∞ на уровень с номером n = 1.
16.
А4. Найти наименьшую длинуволны в ультрафиолетовой области
спектра
водорода.
Какую
наименьшую скорость vmin должны
иметь электроны, чтобы при
возбуждении
атомов
водорода
ударами электронов появилась эта
линия?
Решение (продолжение).
hc
min
E E1.
E 0.
E1
En 2 .
n
hc
0 En
min
hcn2
min
.
E1
n 1.
E1
.
2
n
17.
А4. Найти наименьшую длину волны в ультрафиолетовой области спектраводорода. Какую наименьшую скорость vmin должны иметь электроны, чтобы при
возбуждении атомов водорода ударами электронов появилась эта линия?
Решение (продолжение).
min
hcn 2
min
,
n 1.
E1
hcn 2 6, 63 10 34 3 108
7
0,91
10
(м).
19
E1
13, 6 1, 6 10
При возбуждении атома электронными ударами кинетическая энергия
электрона должна быть больше (или равна) энергии возбуждения.
Vmin
2
mVmin
T
E E1 E1 13, 6 (эВ).
2
2 13, 6 1, 6 10 19
2
6
(м/с).
2,
2
10
E1
31
9,1 10
m
Ответ: λ = 91,4 нм; Vmin =2,20·106 м/с.
18.
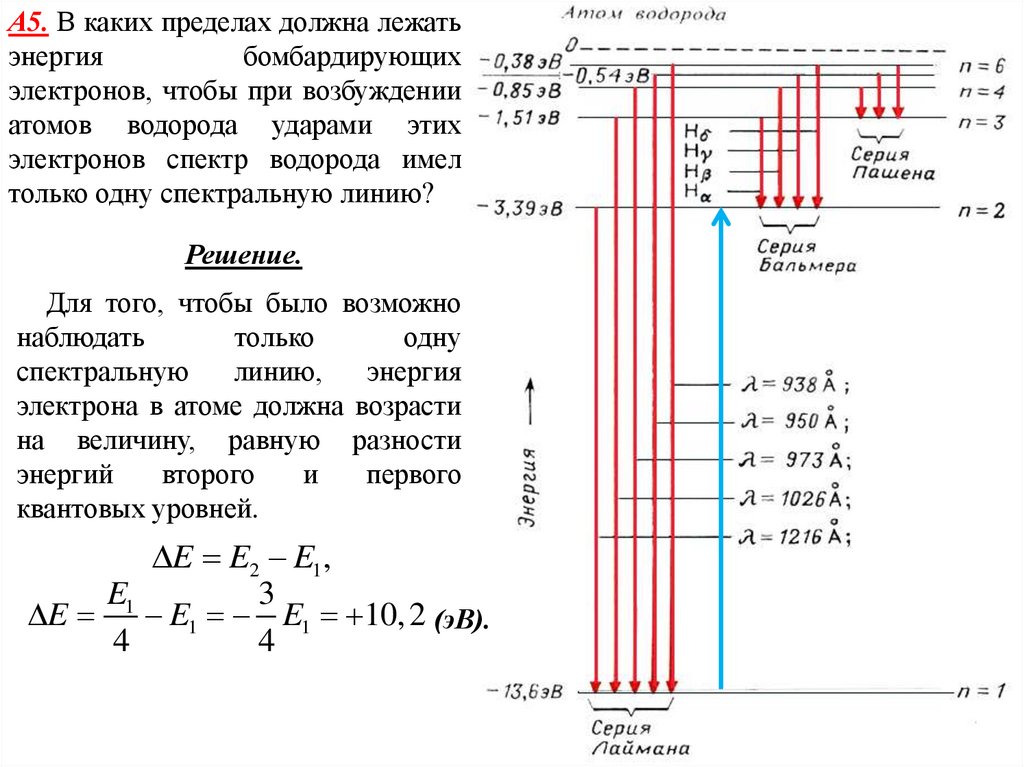
А5. В каких пределах должна лежатьэнергия
бомбардирующих
электронов, чтобы при возбуждении
атомов водорода ударами этих
электронов спектр водорода имел
только одну спектральную линию?
Решение.
Для того, чтобы было возможно
наблюдать
только
одну
спектральную
линию,
энергия
электрона в атоме должна возрасти
на величину, равную разности
энергий
второго
и
первого
квантовых уровней.
E E2 E1 ,
E
3
E 1 E1 E1 10, 2 (эВ).
4
4
19.
А5. В каких пределах должна лежатьэнергия
бомбардирующих
электронов, чтобы при возбуждении
атомов водорода ударами этих
электронов спектр водорода имел
только одну спектральную линию?
Решение (продолжение).
При столкновении бомбардирующий электрон не может передать
энергию,
большую,
чем
кинетическая
энергия
этого
электрона, поэтому.
Emin
3
E E1 10, 2 (эВ).
4
В то же время электрон атома не
должен
получить
энергию,
достаточную для перехода на
уровень номер 3.
E1
8
E E1 E1 12,1 (эВ).
9
9
20.
А5. В каких пределах должна лежать энергия бомбардирующих электронов,чтобы при возбуждении атомов водорода ударами этих электронов спектр
водорода имел только одну спектральную линию?
Решение (продолжение).
Таким образом, энергия бомбардирующего электрона должна быть меньше
энергии, достаточную для перехода электрона в атоме на уровень номер 3.
Emax
E1
8
E1 E1 12,1 (эВ).
9
9
Ответ: энергия бомбардирующих электронов должна лежать в пределах
10, 2 эВ E 12,1 эВ.
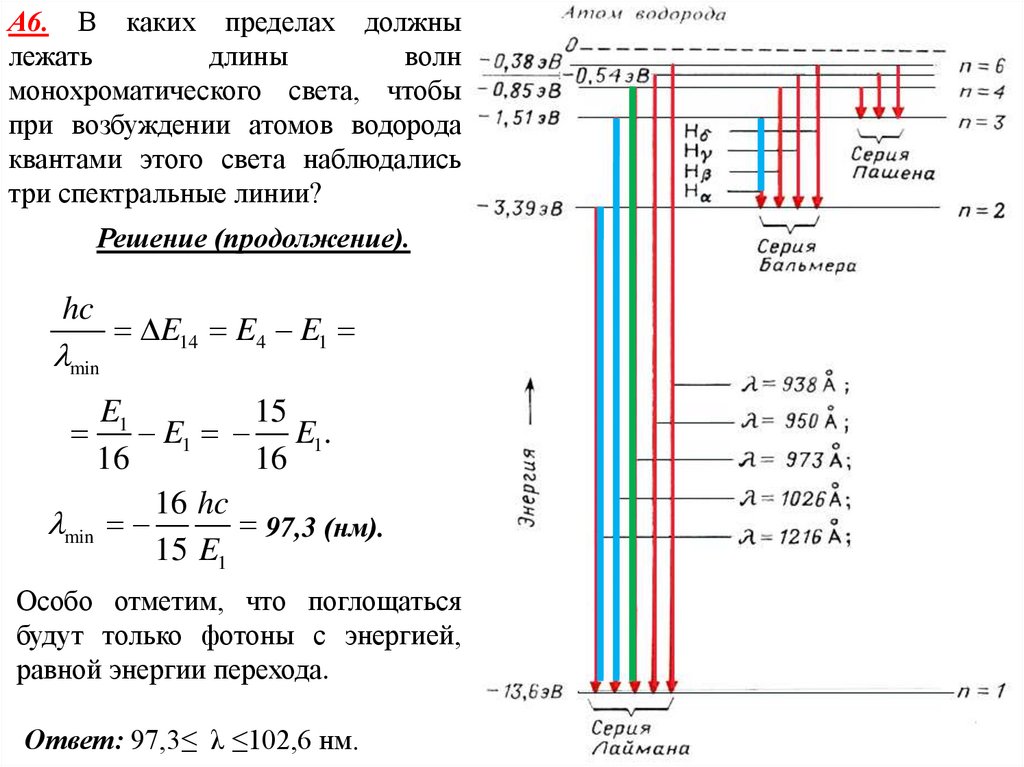
21.
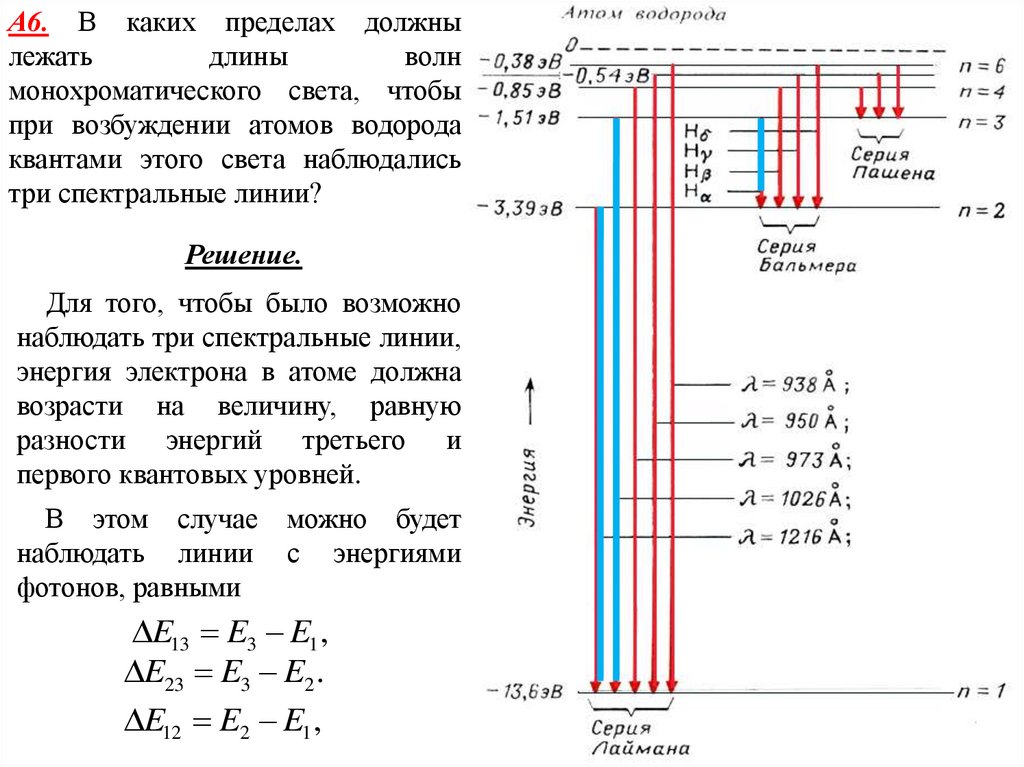
А6. В каких пределах должнылежать
длины
волн
монохроматического света, чтобы
при возбуждении атомов водорода
квантами этого света наблюдались
три спектральные линии?
Решение.
Для того, чтобы было возможно
наблюдать три спектральные линии,
энергия электрона в атоме должна
возрасти на величину, равную
разности энергий третьего и
первого квантовых уровней.
В этом случае можно будет
наблюдать линии с энергиями
фотонов, равными
E13 E3 E1 ,
E23 E3 E2 .
E12 E2 E1 ,
22.
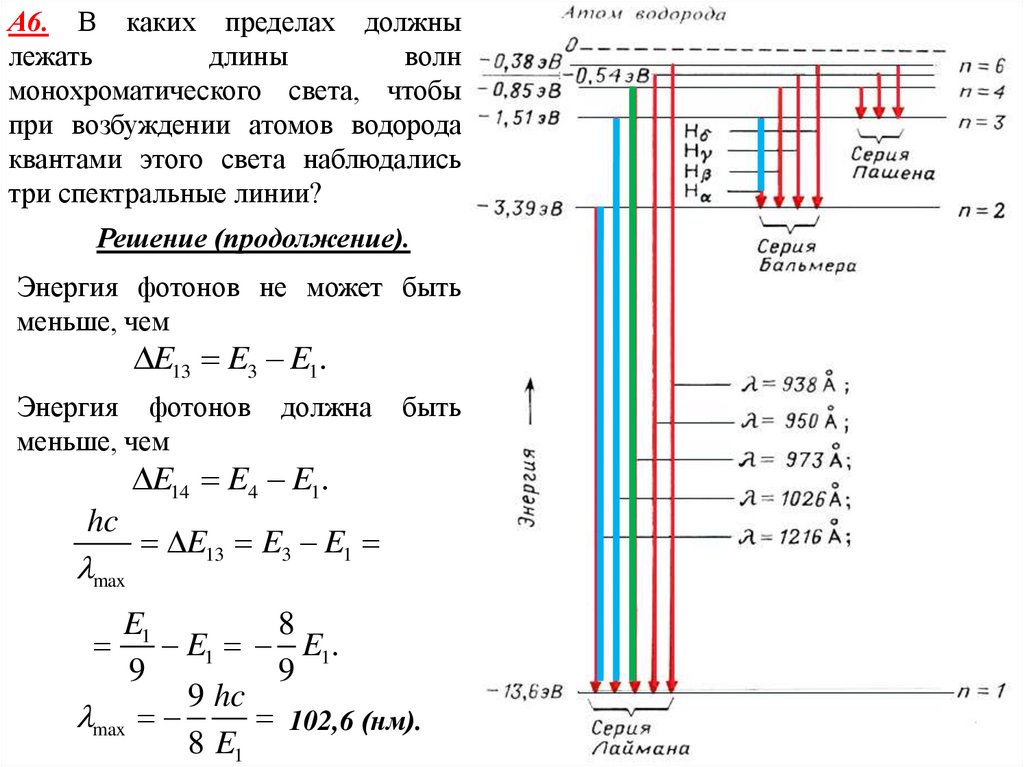
А6. В каких пределах должнылежать
длины
волн
монохроматического света, чтобы
при возбуждении атомов водорода
квантами этого света наблюдались
три спектральные линии?
Решение (продолжение).
Энергия фотонов не может быть
меньше, чем
E13 E3 E1.
Энергия фотонов
меньше, чем
должна
быть
E14 E4 E1.
hc
max
E13 E3 E1
E1
8
E1 E1.
9
9
9 hc
max
102,6 (нм).
8 E1
23.
А6. В каких пределах должнылежать
длины
волн
монохроматического света, чтобы
при возбуждении атомов водорода
квантами этого света наблюдались
три спектральные линии?
Решение (продолжение).
hc
min
E14 E4 E1
E1
15
E1 E1.
16
16
16 hc
min
97,3 (нм).
15 E1
Особо отметим, что поглощаться
будут только фотоны с энергией,
равной энергии перехода.
Ответ: 97,3≤ λ ≤102,6 нм.
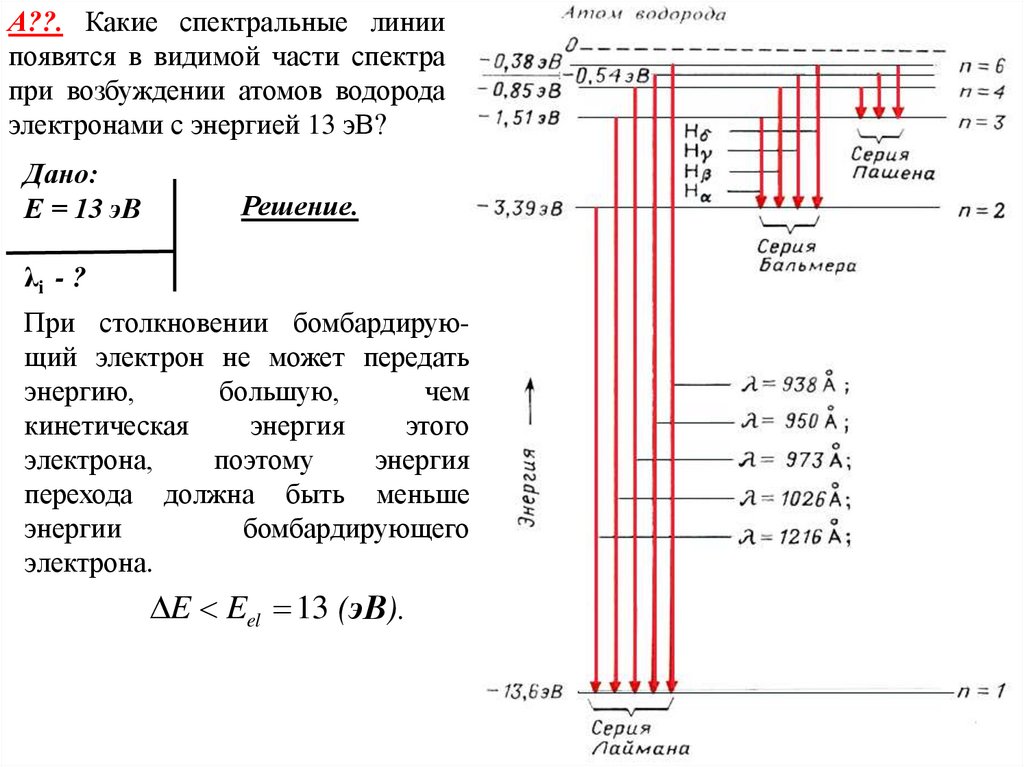
24.
А??. Какие спектральные линиипоявятся в видимой части спектра
при возбуждении атомов водорода
электронами с энергией 13 эВ?
Дано:
Е = 13 эВ
Решение.
λi - ?
При столкновении бомбардирующий электрон не может передать
энергию,
большую,
чем
кинетическая
энергия
этого
электрона,
поэтому
энергия
перехода должна быть меньше
энергии
бомбардирующего
электрона.
E Eel 13 (эВ).
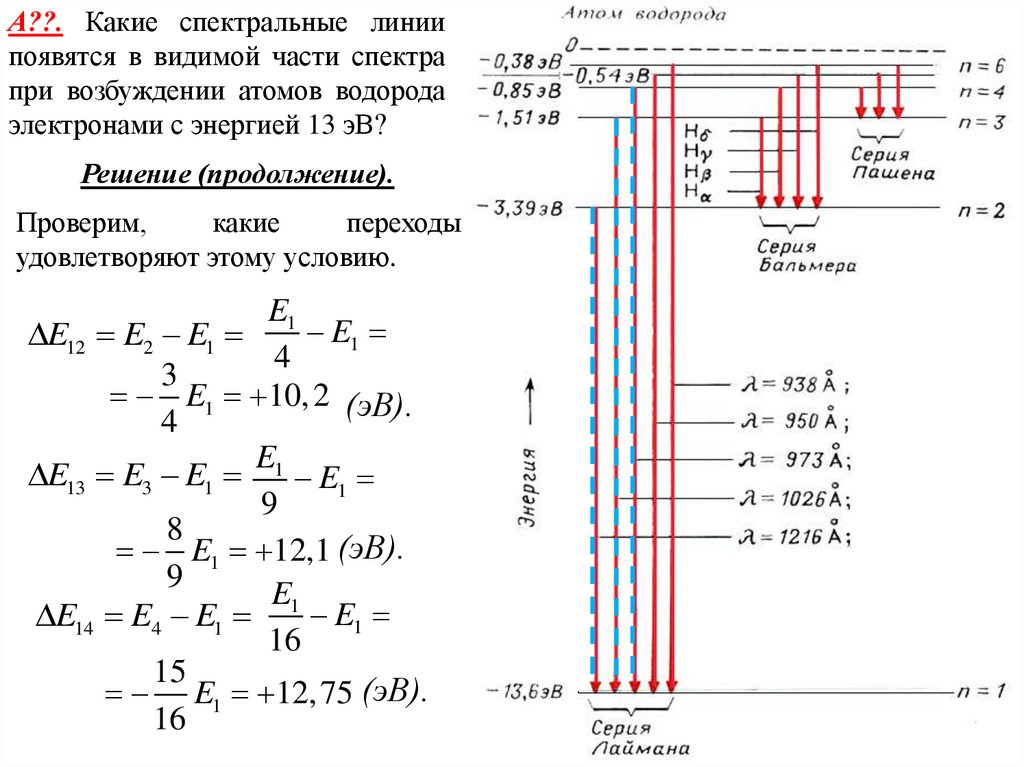
25.
А??. Какие спектральные линиипоявятся в видимой части спектра
при возбуждении атомов водорода
электронами с энергией 13 эВ?
Решение (продолжение).
Проверим,
какие
переходы
удовлетворяют этому условию.
E1
E1
E12 E2 E1
4
3
E1 10, 2 (эВ).
4
E
E13 E3 E1 1 E1
9
8
E1 12,1 (эВ).
9
E
E14 E4 E1 1 E1
16
15
E1 12, 75 (эВ).
16
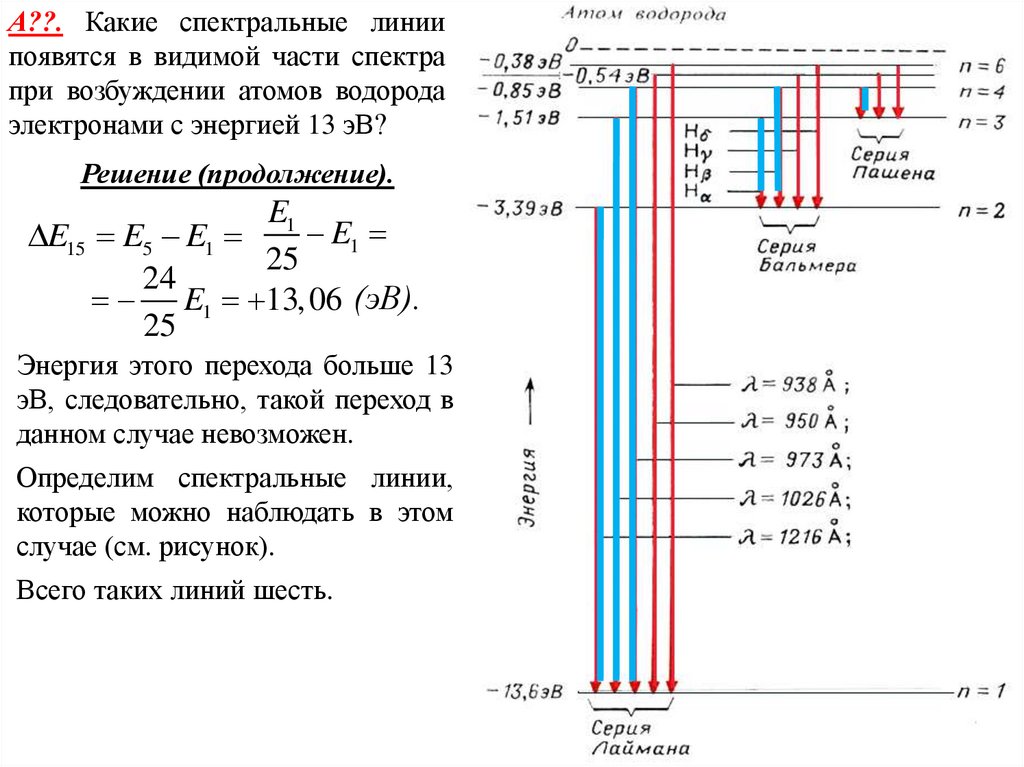
26.
А??. Какие спектральные линиипоявятся в видимой части спектра
при возбуждении атомов водорода
электронами с энергией 13 эВ?
Решение (продолжение).
E1
E1
E15 E5 E1
25
24
E1 13, 06 (эВ).
25
Энергия этого перехода больше 13
эВ, следовательно, такой переход в
данном случае невозможен.
Определим спектральные линии,
которые можно наблюдать в этом
случае (см. рисунок).
Всего таких линий шесть.














 physics
physics








