Similar presentations:
Выделение ферментных препаратов методами осаждения и высаливания
1.
ФГАОУ ВО «УрФУ имени первого Президента России Б.Н. Ельцина»Химико-технологический институт
Кафедра технологии органического синтеза
ВЫДЕЛЕНИЕ ФЕРМЕНТНЫХ
ПРЕПАРАТОВ МЕТОДАМИ
ОСАЖДЕНИЯ И ВЫСАЛИВАНИЯ
ДИСЦИПЛИНА: МЕТОДЫ ВЫДЕЛЕНИЯ
БИОТЕХНОЛОГИЧЕСКИХ ПРОДУКТОВ
Студент
Клементьева С.Ю.
группы Х-470007
Преподаватель
Берсенева В.С.
доцент, к.х.н
Екатеринбург 2020
2.
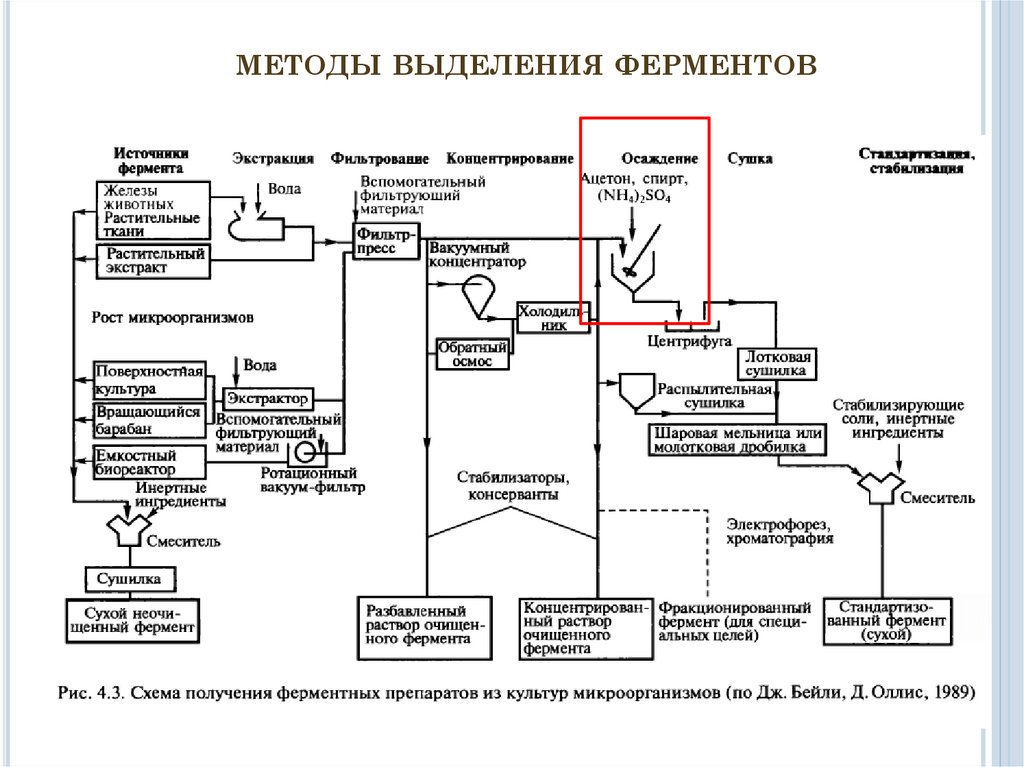
МЕТОДЫ ВЫДЕЛЕНИЯ ФЕРМЕНТОВ2
3.
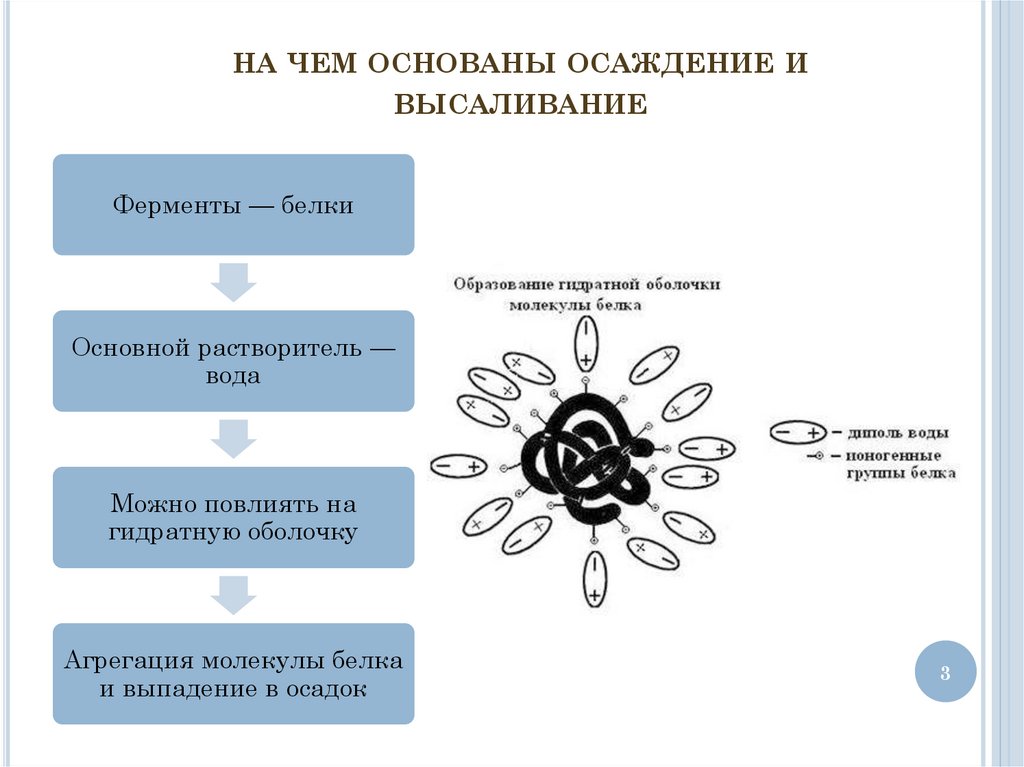
НА ЧЕМ ОСНОВАНЫ ОСАЖДЕНИЕ ИВЫСАЛИВАНИЕ
Ферменты — белки
Основной растворитель —
вода
Можно повлиять на
гидратную оболочку
Агрегация молекулы белка
и выпадение в осадок
3
4.
ОСАЖДЕНИЕ ОРГАНИЧЕКИМИРАСТВОРИТЕЛЯМИ
Растворитель должен
смешиваться с водой
Растворитель не должен
связываться с ферментом
Следует помнить о
токсичности
взрывоопасности и
возможности регенерации
Чаще — этанол,
изопропанол, ацетон,
метанол, диоксан
Реже – эфир,
диэтилкарбонил,
коллидин, некоторые
ароматические и
гетероциклические
амины
4
5.
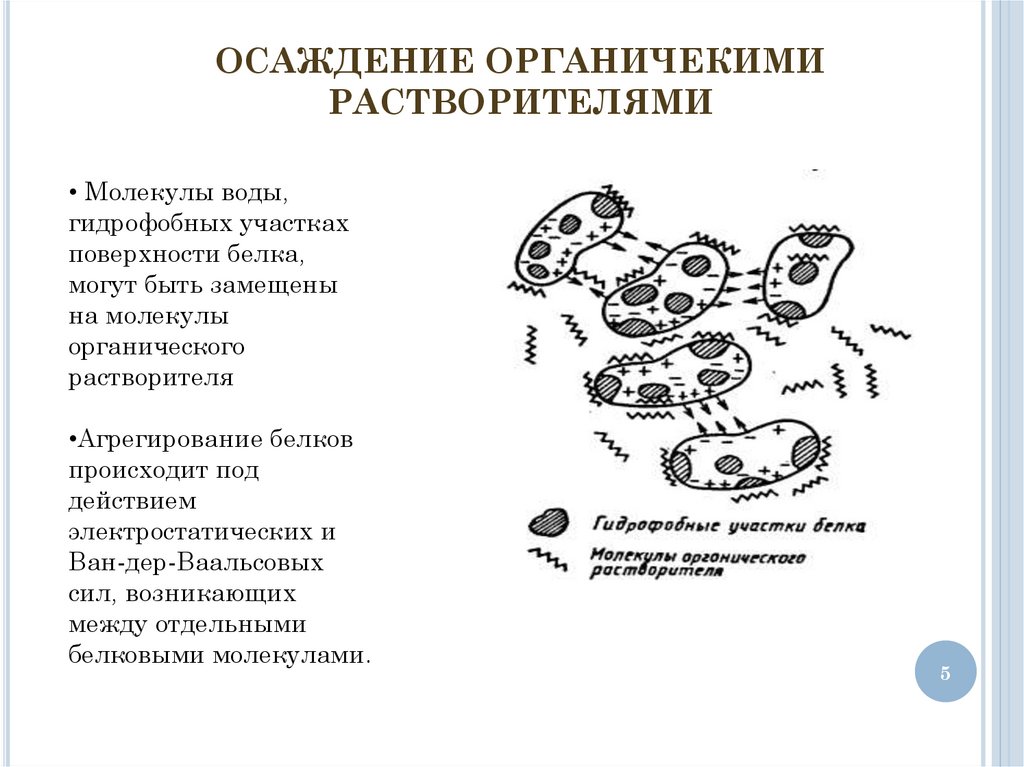
ОСАЖДЕНИЕ ОРГАНИЧЕКИМИРАСТВОРИТЕЛЯМИ
• Молекулы воды,
гидрофобных участках
поверхности белка,
могут быть замещены
на молекулы
органического
растворителя
•Агрегирование белков
происходит под
действием
электростатических и
Ван-дер-Ваальсовых
сил, возникающих
между отдельными
белковыми молекулами.
5
6.
ФАКТОРЫ, ВЛИЯЮЩИЕ НА ОСАЖДЕНИЕРазмер молекулы белка
Крупные молекулы агрегируют быстрее, чем мелкие
6
7.
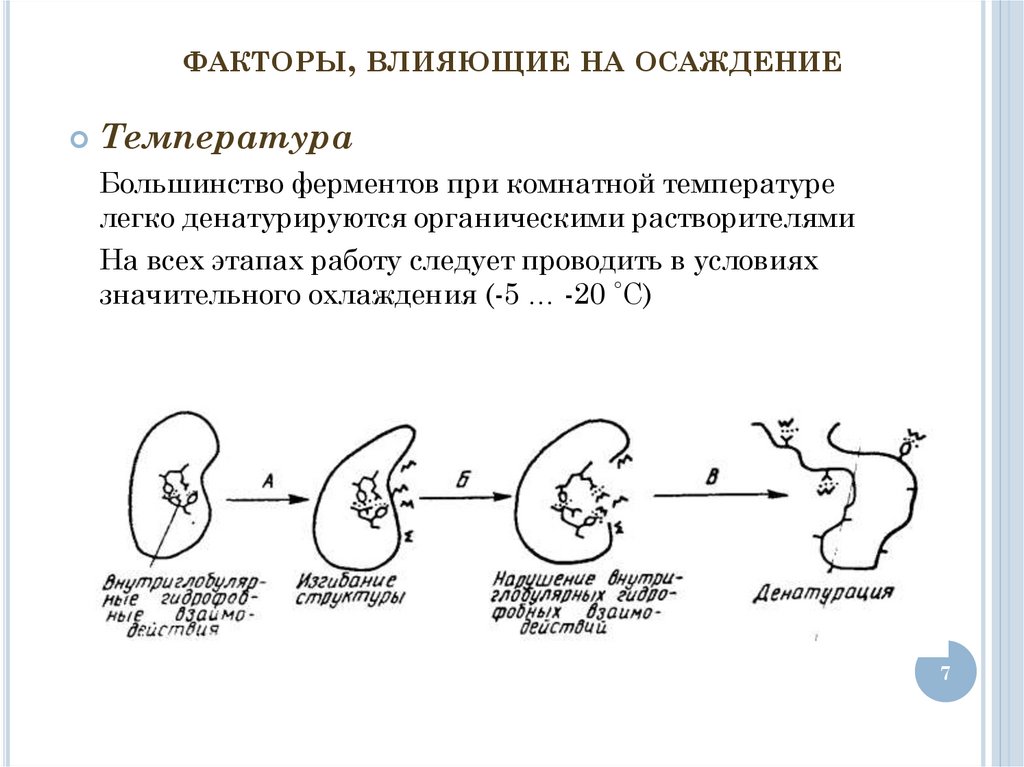
ФАКТОРЫ, ВЛИЯЮЩИЕ НА ОСАЖДЕНИЕТемпература
Большинство ферментов при комнатной температуре
легко денатурируются органическими растворителями
На всех этапах работу следует проводить в условиях
значительного охлаждения (-5 … -20 ˚С)
7
8.
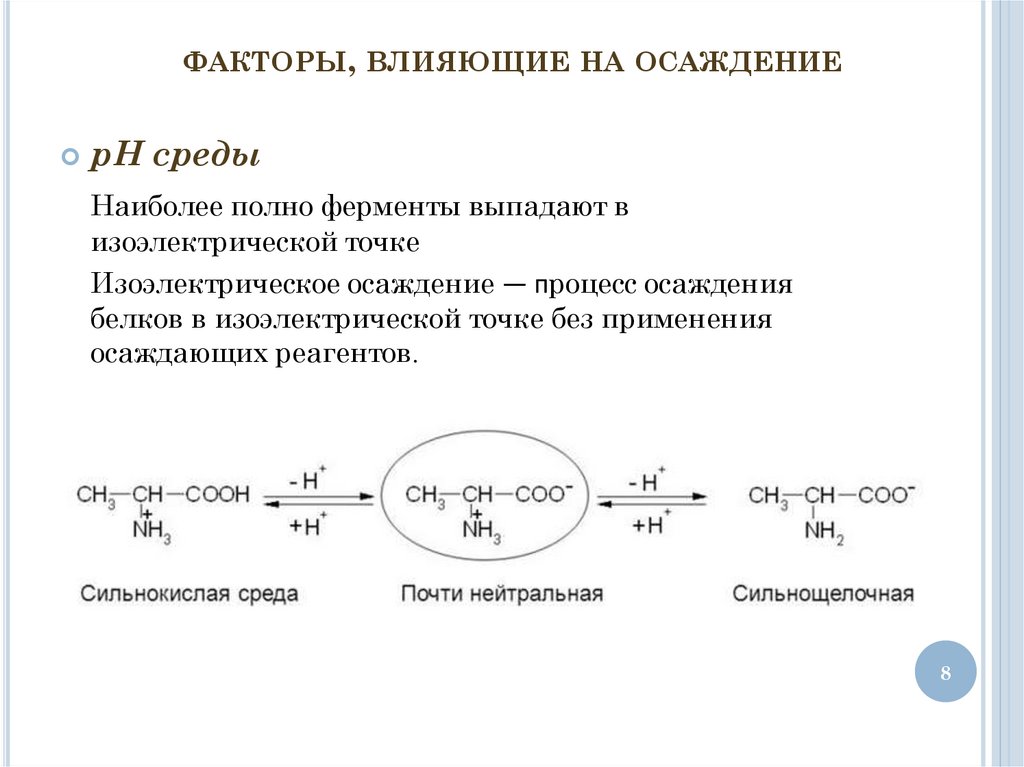
ФАКТОРЫ, ВЛИЯЮЩИЕ НА ОСАЖДЕНИЕрН среды
Наиболее полно ферменты выпадают в
изоэлектрической точке
Изоэлектрическое осаждение — процесс осаждения
белков в изоэлектрической точке без применения
осаждающих реагентов.
8
9.
УСТАНОВКА ДЛЯ НЕПРЕРЫВНОГО ОСАЖДЕНИЯФЕРМЕНТОВ
а – общая схема: 1сборник для ферментного
раствора; 2 – мерник для
спирта; 3,4 – ротаметры; 5 –
смеситель; 6 – сепаратор;
б – смеситель
непрерывного действия:
1—корпус; 2—шток; 3 –
распорные втулки; 4—
перегородки; 5 – гайка; 6 –
уплотнение.
9
10.
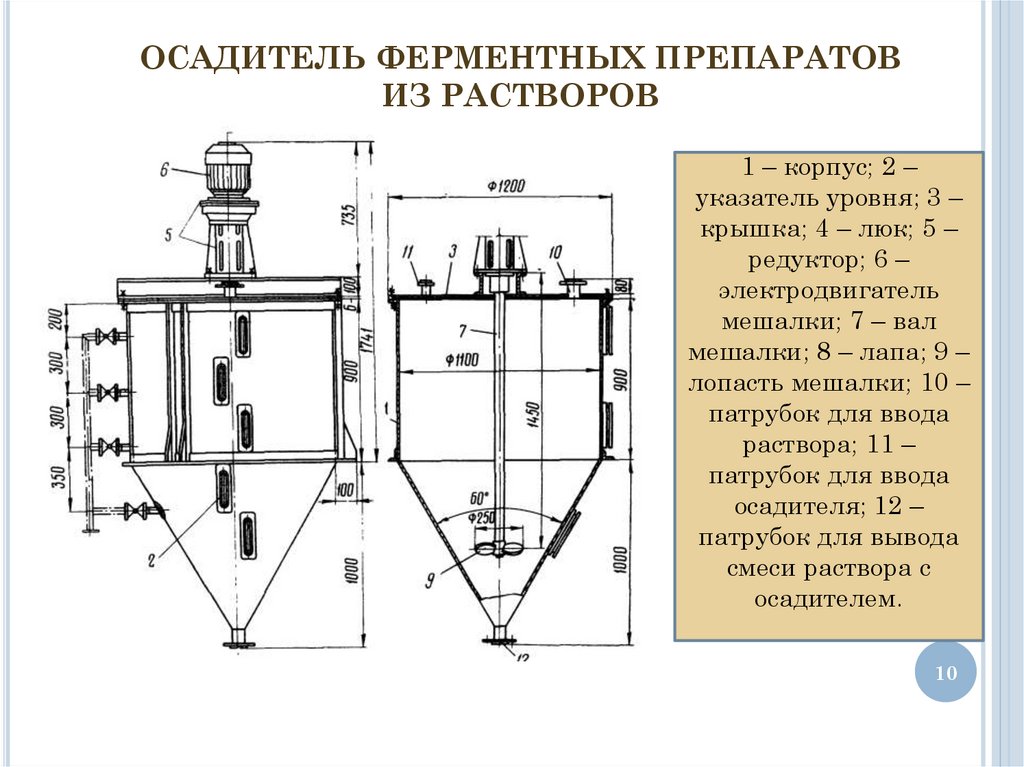
ОСАДИТЕЛЬ ФЕРМЕНТНЫХ ПРЕПАРАТОВИЗ РАСТВОРОВ
1 – корпус; 2 –
указатель уровня; 3 –
крышка; 4 – люк; 5 –
редуктор; 6 –
электродвигатель
мешалки; 7 – вал
мешалки; 8 – лапа; 9 –
лопасть мешалки; 10 –
патрубок для ввода
раствора; 11 –
патрубок для ввода
осадителя; 12 –
патрубок для вывода
смеси раствора с
осадителем.
10
11.
ПРИМЕРЫ ОСАЖДЕНИЯ ОРГАНИЧЕСКИМИРАСТВОРИТЕЛЯМИ
Гексокиназа — этанолом из
дрожжей
Ферменты мышечного экстракта
— ацетоном
Амилаза — ацетоном из слюны
Каталаза – диоксаном из бычьей
печени
11
12.
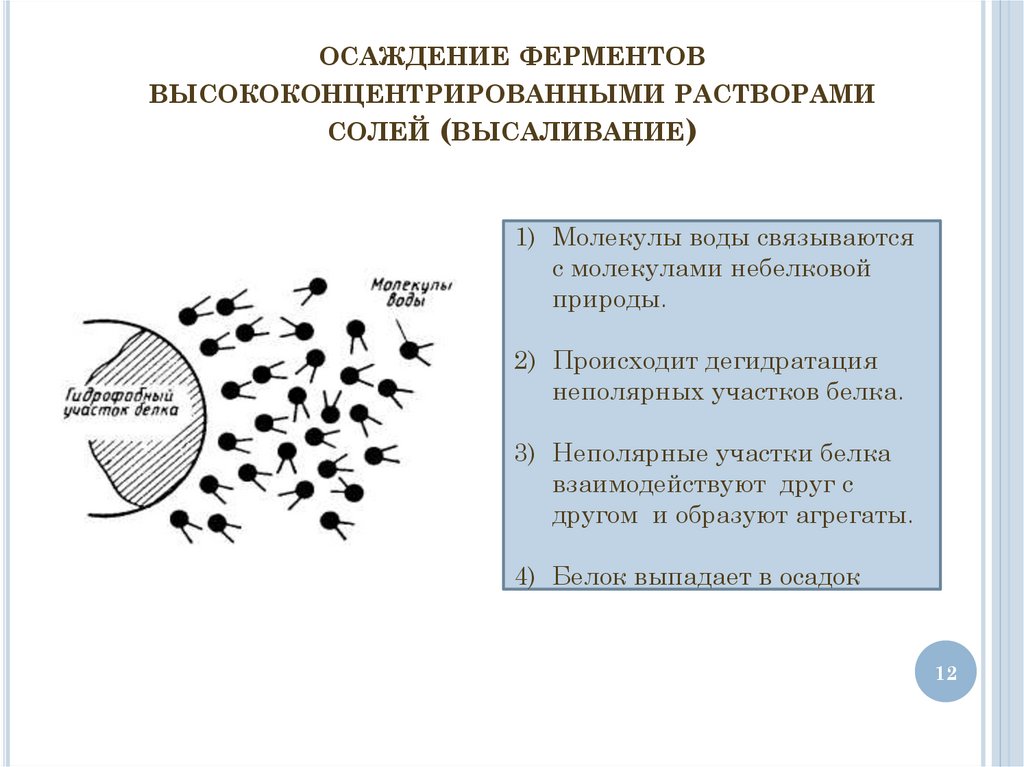
ОСАЖДЕНИЕ ФЕРМЕНТОВВЫСОКОКОНЦЕНТРИРОВАННЫМИ РАСТВОРАМИ
СОЛЕЙ (ВЫСАЛИВАНИЕ)
1) Молекулы воды связываются
с молекулами небелковой
природы.
2) Происходит дегидратация
неполярных участков белка.
3) Неполярные участки белка
взаимодействуют друг с
другом и образуют агрегаты.
4) Белок выпадает в осадок
12
13.
КАКИЕ СОЛИ ИСПОЛЬЗУЮТСЯПо силе высаливающего действия анионы натриевых
солей можно расположить в следующий ряд:
SO4 2- > CH3COO- > Cl-> NO3- > Br- > I- > CNS-
а катионы —
Li +> Na+> K+ >(NH4)+
13
Наиболее часто используют сульфат аммония
14.
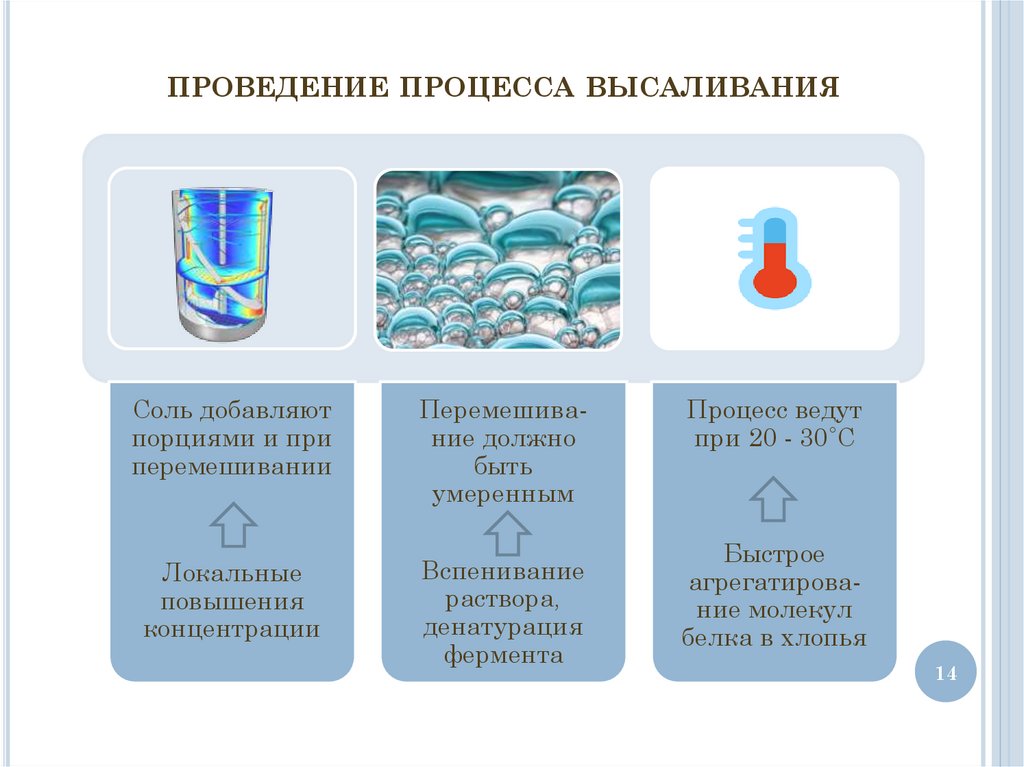
ПРОВЕДЕНИЕ ПРОЦЕССА ВЫСАЛИВАНИЯСоль добавляют
порциями и при
перемешивании
Перемешивание должно
быть
умеренным
Локальные
повышения
концентрации
Вспенивание
раствора,
денатурация
фермента
Процесс ведут
при 20 - 30˚С
Быстрое
агрегатирование молекул
белка в хлопья
14
15.
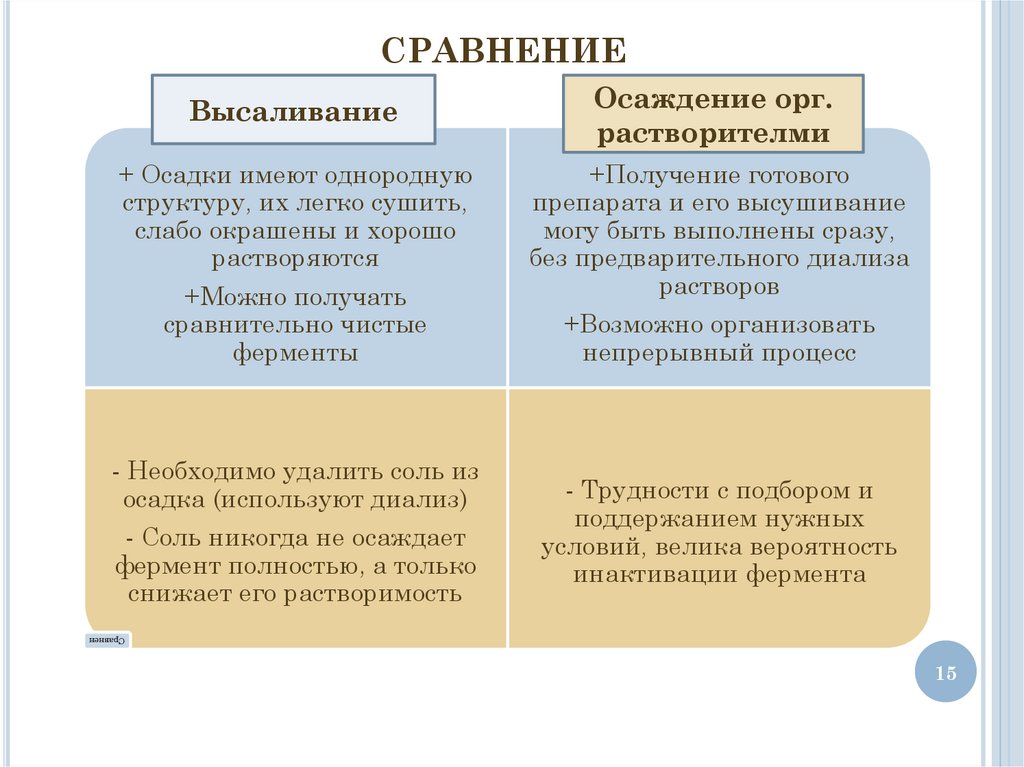
СРАВНЕНИЕВысаливание
Осаждение орг.
растворителми
+ Осадки имеют однородную
структуру, их легко сушить,
слабо окрашены и хорошо
растворяются
+Можно получать
сравнительно чистые
ферменты
+Получение готового
препарата и его высушивание
могу быть выполнены сразу,
без предварительного диализа
растворов
- Необходимо удалить соль из
осадка (используют диализ)
- Соль никогда не осаждает
фермент полностью, а только
снижает его растворимость
+Возможно организовать
непрерывный процесс
- Трудности с подбором и
поддержанием нужных
условий, велика вероятность
инактивации фермента
Сравнен
15
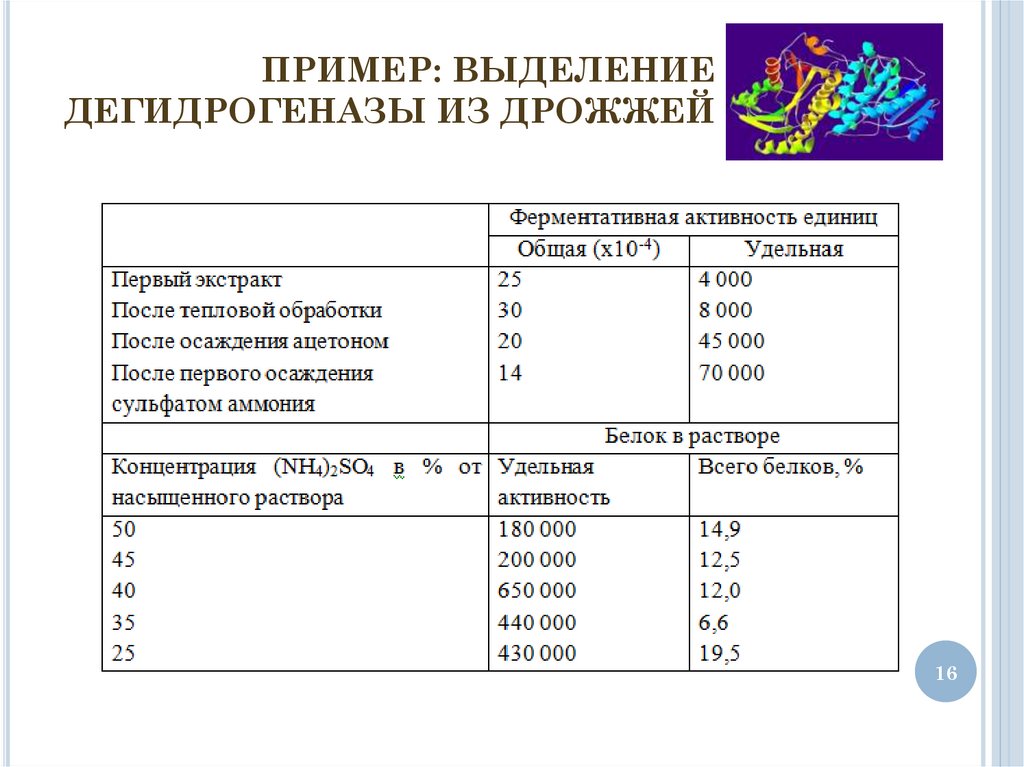
16.
ПРИМЕР: ВЫДЕЛЕНИЕДЕГИДРОГЕНАЗЫ ИЗ ДРОЖЖЕЙ
16
17.
ОСАЖДЕНИЕ ФЕРМЕНТОВОРГАНИЧЕСКИМИ ПОЛИМЕРАМИ
Чаще всего используют декстран и
полиэтиленгликоль различной степени
полимеризации.
17
18.
ОСАЖДЕНИЕ ПОЛИЭТИЛЕНГЛИКОЛЕМ(ПЭГ)
•Для осаждения используют ПЭГ двух типов: с
молекулярными массами 6 000 и 20 000.
•Механизм аналогичен осаждению органическими
растворителями
•Требуются более низкие
концентрации
•Процесс можно вести при
комнатной температуре
•Реактив сравнительно дешевый
•Не оказывает отрицательного
воздействия на белок при его
дальнейшем выделении
•Труднее удалить из
ферментной
фракции, чем соль
или органический
растворитель (но
часто не удаляют)
18
19.
ОСАЖДЕНИЕ ИОНАМИ МЕТАЛЛОВДля выделения ß-галактозидазы из разрушенных
клеток E.coli успешно используются ионы марганца.
После удаления ионов металла происходит полное
восстановление фермента и его одновременная очистка
от 30-40 % сопутствующих нуклеиновых кислот.
Отделить атомы металлов от белков можно
диализом;
снижением рН смеси;
с помощью катионообменных смол
Основной недостаток — способность металлов
19
интенсивно денатурировать белки.
Необходимо тщательно регулировать температуру и рН
20.
ИЗБИРАТЕЛЬНАЯ ДЕНАТУРАЦИЯПриемлем только для стабильных ферментов, сохраняющих
устойчивость в экстремальных условиях внешней среды.
Пример: глюкозоизомераза выдерживает температуру до 9095˚С.
Помещая такие ферменты в смеси с сопутствующими белками
в экстремальные условия, можно вызвать денатурацию
ненужных белков. Денатурированные белки можно осадить и
удалить, а в растворе остается целевой фермент.
Для проведения избирательной денатурации используют
три фактора:
— температуру;
— рН;
— воздействие органическими растворителями;
20
21.
ЗАКЛЮЧЕНИЕОсаждение ферментов можно осуществить:
1) органическими растворителями (этанол, изопропанол,
ацетон и др.);
2) высаливанием (сульфат аммония, хлористый натрий и
др.);
3) органическими полимерами (декстран, ПЭГ и др.)
4) ионами металлов (ртуть, свинец, марганец и др.)
+ избирательная денатурация (в осадок выпадают
балластные вещества)
• Рассмотренный методы связаны со сложностями подбора условий для
осаждения конкретного фермента. Возможно выпадение в осадок
балластных веществ. Поэтому осаждение и высаливание используются в
комбинации с другими методами
21
22.
СПИСОК ИСПОЛЬЗОВАННОЙЛИТЕРАТУРЫ
1.
2.
3.
4.
5.
6.
Егорова Т.А. Основы биотехнологии: учеб. пособие для
высш. пед. учеб. заведений / Т.А. Егорова, С.М.
Клунова, Е.А. Живухина. – 4-е изд., стер – М.:
Издательский центр «Академия», 2008. – 208 с.
Грачева И.М. Технология ферментных препартов /
И.М. Грачева , Кривова А.Ю. – 3 –е изд. — М.: Элевар,
2000. — 336с.
Цыперович А.С. Ферменты (основы химии и
технологии) / А.С. Цыперович – Киев: Texнiка, 1971. –
360с.
Бейли Дж. Основы биохимической инженерии / Бейли
Дж., Оллис Д. – Пер. с англ. В 2-х частях. Ч.2. — М.:
Мир, 1989.— 590 с.
Колосков С.П. Оборудование предприятий
ферментной промышленности. М.: Пищевая
промышленность, 1969. — 398 с.
Кувикова А.Ф. Технология выделения ферментов. М.:
Пищепромиздат., 1961. — 566 с.
22













 chemistry
chemistry








