Similar presentations:
Химические понятия
1.
«Первоначальныехимические понятия»
2.
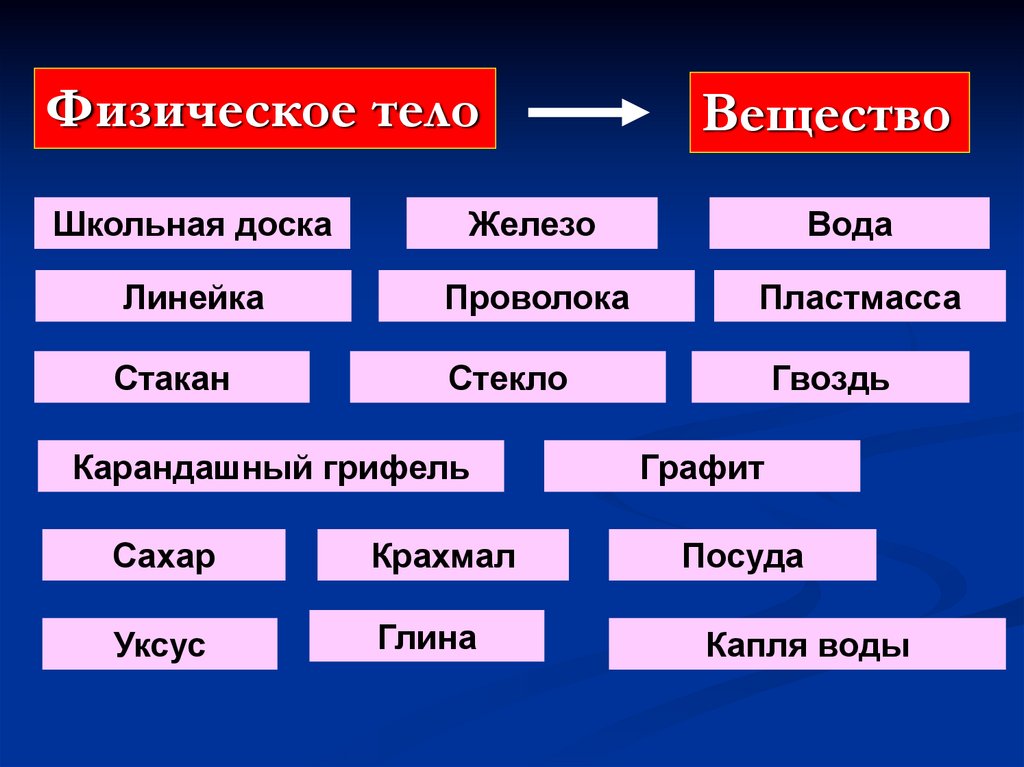
Физическое телоШкольная доска
Железо
Линейка
Проволока
Стакан
Стекло
Карандашный грифель
Сахар
Крахмал
Уксус
Глина
Вещество
Вода
Пластмасса
Гвоздь
Графит
Посуда
Капля воды
3.
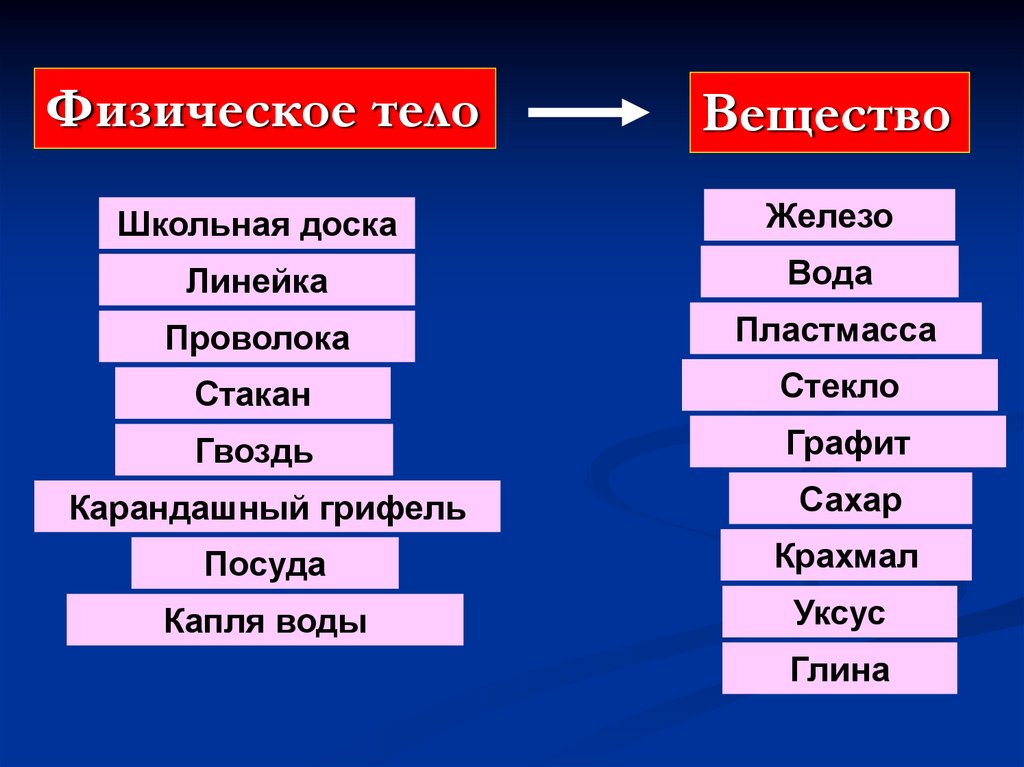
Физическое телоВещество
Школьная доска
Железо
Линейка
Вода
Проволока
Пластмасса
Стакан
Стекло
Гвоздь
Графит
Карандашный грифель
Сахар
Посуда
Крахмал
Капля воды
Уксус
Глина
4.
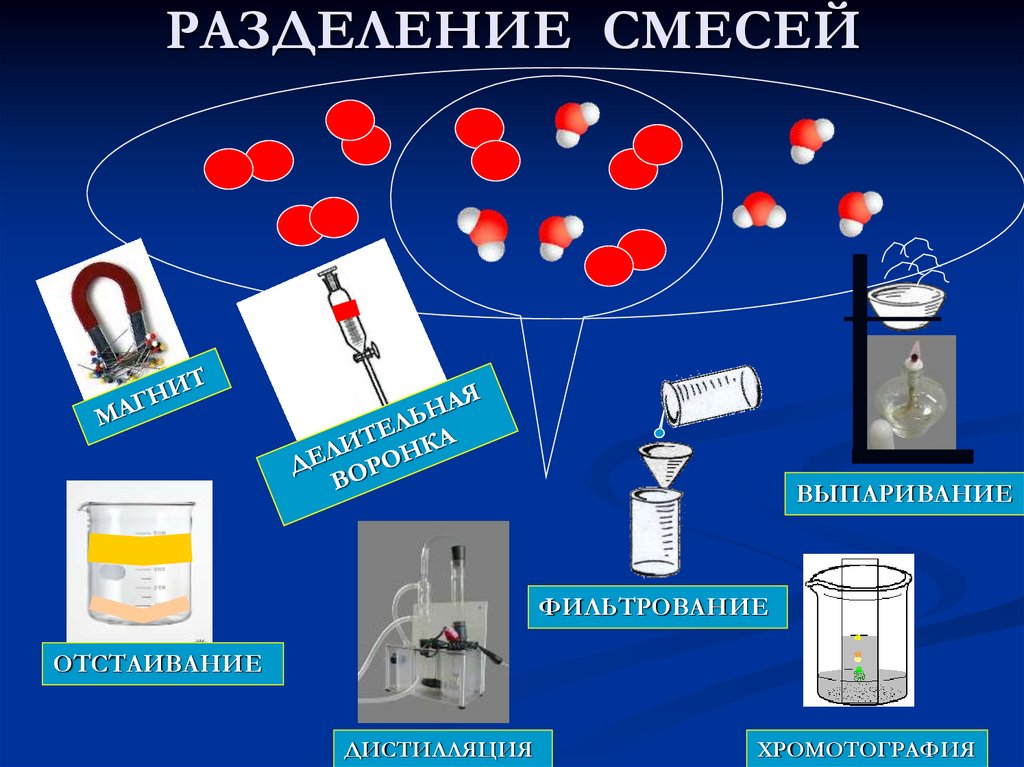
РАЗДЕЛЕНИЕ СМЕСЕЙВЫПАРИВАНИЕ
ФИЛЬТРОВАНИЕ
ОТСТАИВАНИЕ
ДИСТИЛЛЯЦИЯ
ХРОМОТОГРАФИЯ
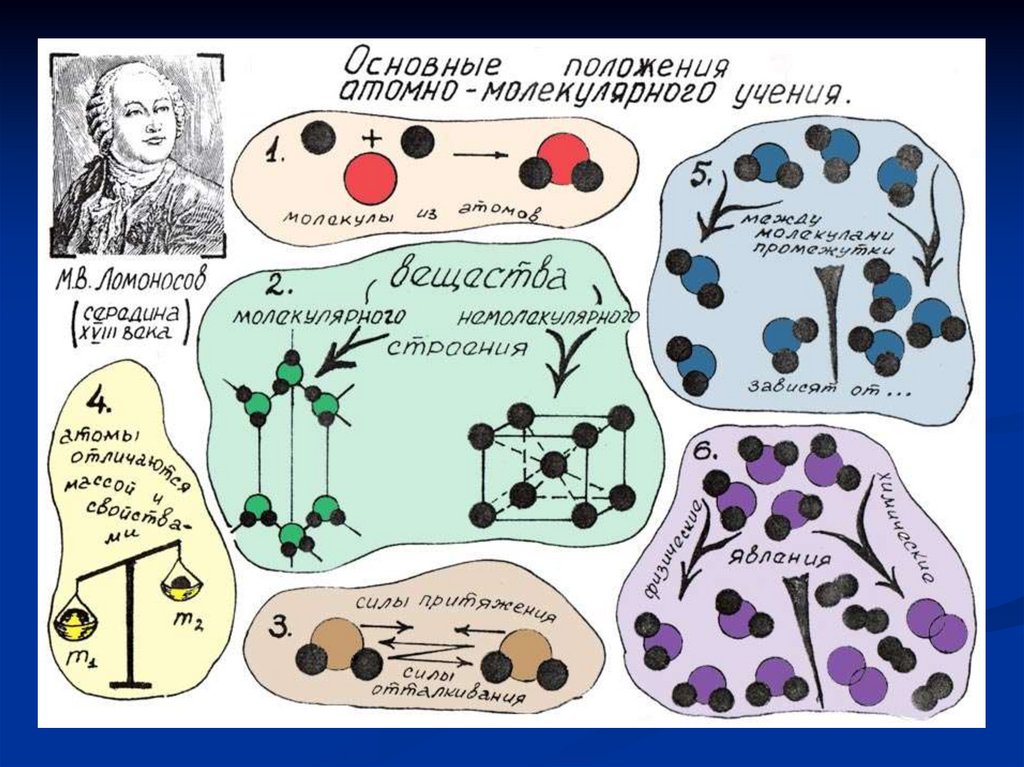
5.
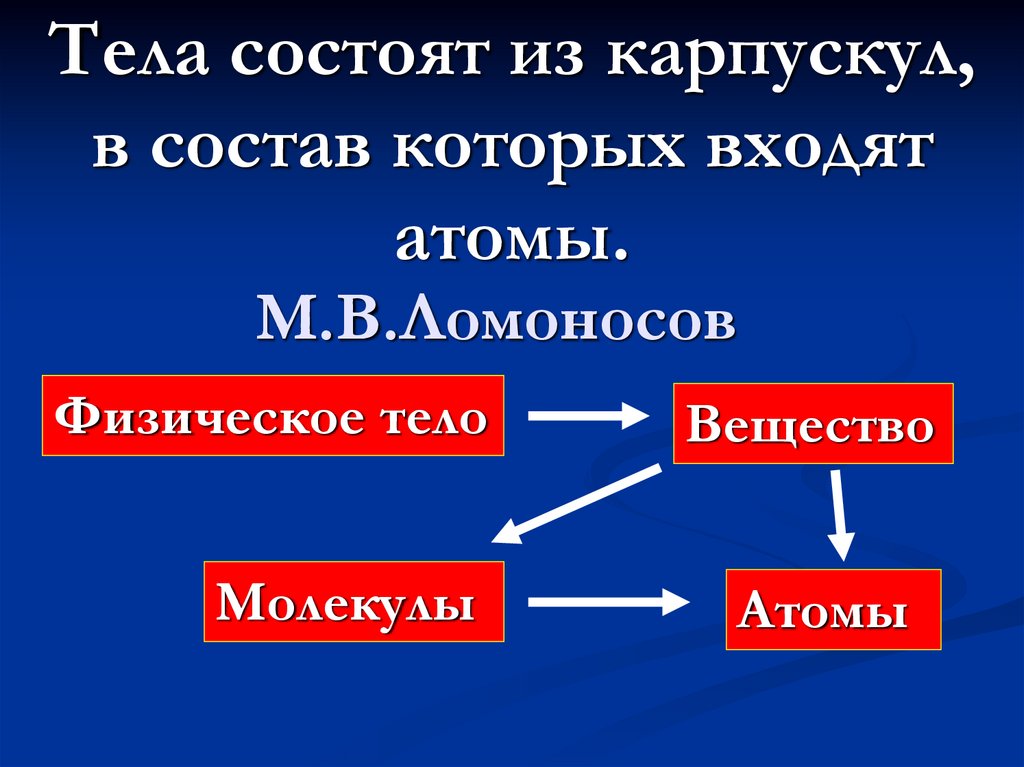
Тела состоят из карпускул,в состав которых входят
атомы.
М.В.Ломоносов
Физическое тело
Молекулы
Вещество
Атомы
6.
ЭЛЕКТРИЧЕСКИЙ ТОКВОДА
ВОДОРОД
+
КИСЛОРОД
2 атома
ВОДОРОДА
1 атом
КИСЛОРОДА
+
2 молекулы ВОДЫ
2 молекулы
ВОДОРОДА
1 молекула
КИСЛОРОДА
7.
8.
9.
ПРОСТОЕвещество
СЛОЖНОЕ
вещество
10.
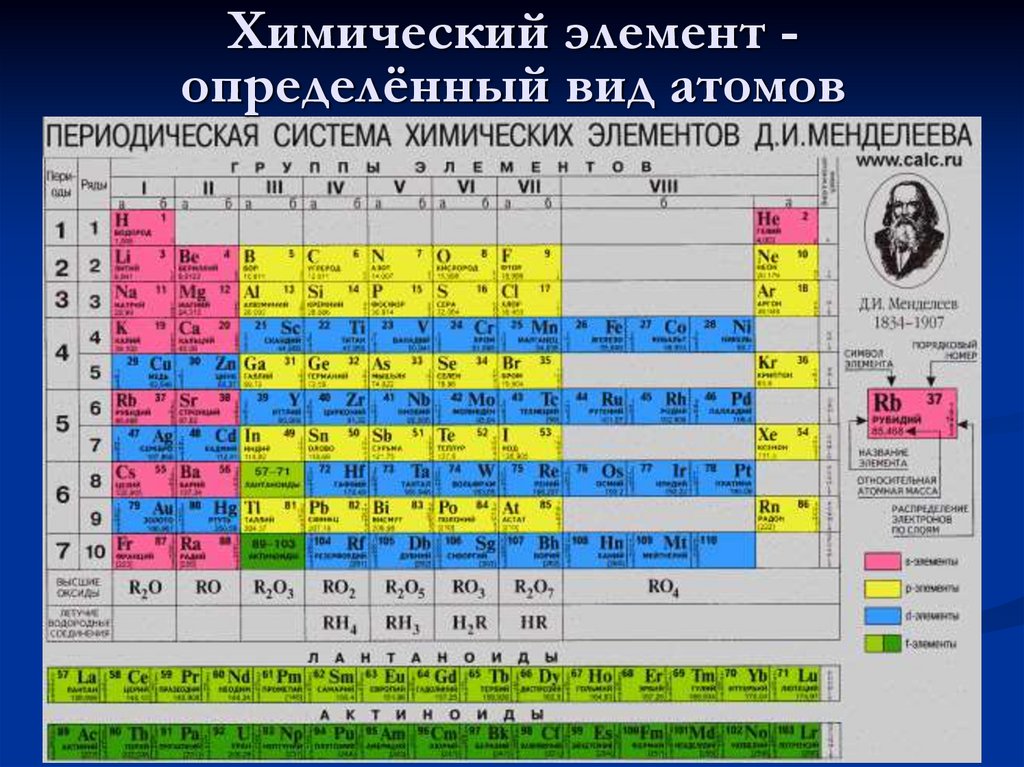
Химический элемент определённый вид атомов11.
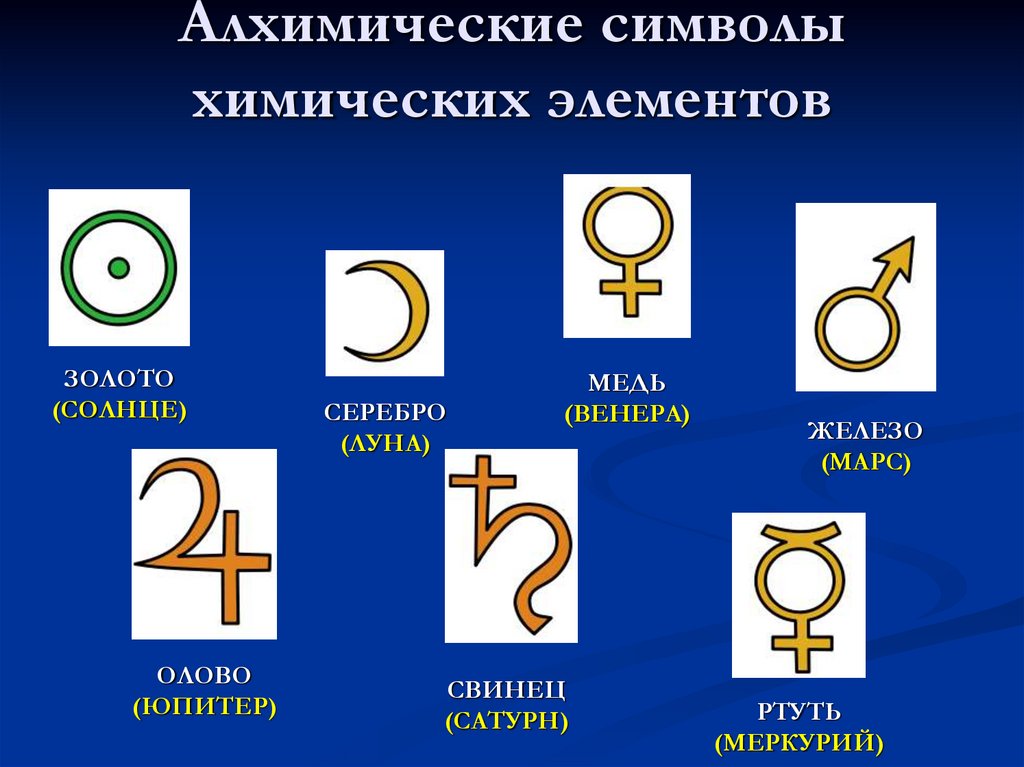
Алхимические символыхимических элементов
ЗОЛОТО
(СОЛНЦЕ)
ОЛОВО
(ЮПИТЕР)
СЕРЕБРО
(ЛУНА)
МЕДЬ
(ВЕНЕРА)
СВИНЕЦ
(САТУРН)
ЖЕЛЕЗО
(МАРС)
РТУТЬ
(МЕРКУРИЙ)
12.
Йёнс Якоб БерцелиусДля обозначения химических
элементов Берцелиус
предложил использовать
начальные буквы их
латинских названий (1814)
Русское
название
элемента
Латинское
название
элемента
Знак
хим.
элемента
Чтение знака в
формулах
Кислород
Oxygenium
O
«O»
Углерод
Медь
Водород
Ртуть
Сarboneum
Cuprum
Hydrogenium
Hydrargyrum
C
Cu
H
Hg
«Це»
«Купрум»
«Аш»
«Гидраргирум»
13.
Разгадайте химические анаграммы,переставив буквы в каждом слове надо получить
название химического элемента
Е
С
Е
Е
З
Л И К
К
О
Л
О Д
Л
И
О
Ж
Р
Н
Ь
Без него не отрежете и
куска хлеба
Без него не проживёте и
пяти минут
Помогает первому бороться
со вторым
Н
А
П
Л
И
Т
А
Дороже золота
О
Р
Р
Е
Б
Е
С
Младший брат предыдущего
Ц
И
Н
В
Е
С
Без него и рыбку не
поймаешь
14.
15.
Запишите знак химическогоэлемента и его произношение
l Вариант
O
«О»
КИСЛОРОД
K
«калий»
КАЛИЙ
N
«Эн»
АЗОТ
Hg РТУТЬ
«Гидраргирум»
SbСУРЬМА
«Стибиум»
Ag
«Аргентум»
СЕРЕБРО
Cu МЕДЬ
«Купрум»
КРЕМНИЙ
Si
«Силициум»
ll Вариант
«Це»
УГЛЕРОД
CaКАЛЬЦИЙ
«кальций»
HВОДОРОД
«Аш»
Pb СВИНЕЦ
«Плюмбум»
Au ЗОЛОТО
«Аурум»
Sn ОЛОВО
«Станум»
AsМЫШЬЯК
«Арсеникум»
FeЖЕЛЕЗО
«Феррум»
C
16.
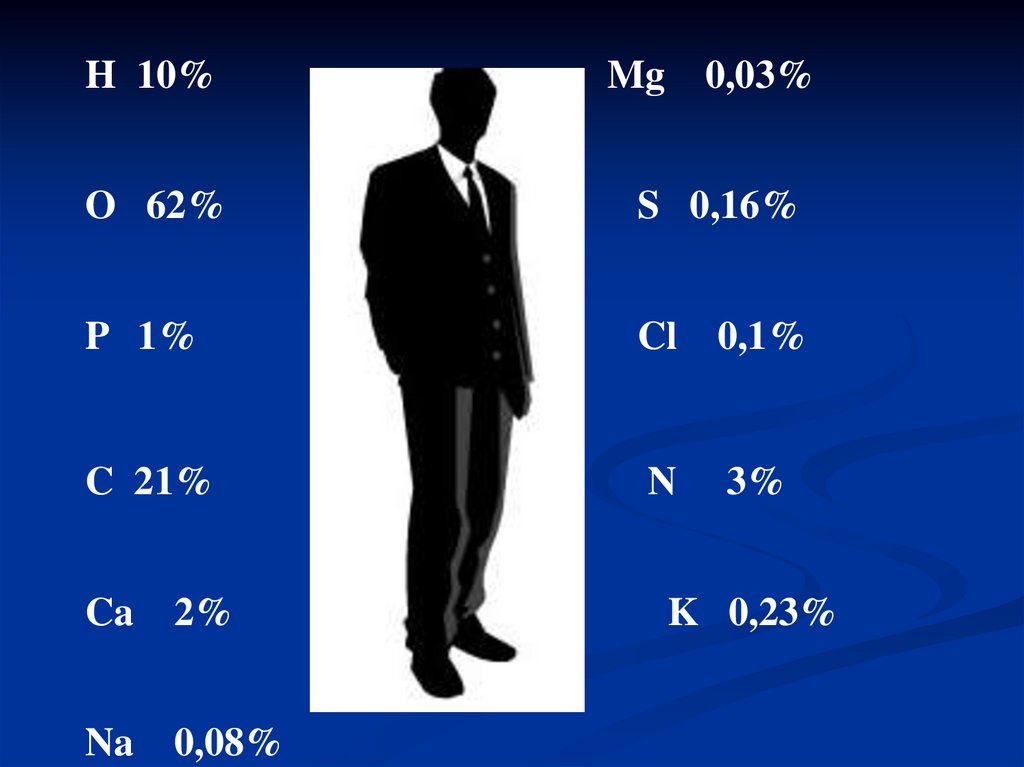
В организме человека17.
H 10%Mg 0,03%
O 62%
S 0,16%
P 1%
Cl
0,1%
C 21%
N
3%
Ca
2%
Na
0,08%
K 0,23%
18.
АТОМНАЯ ЕДИНИЦА МАССЫа.е.м.
- это 1/12
массы атома углерода, масса
-10
10 м
которого равна
12 а.е.м. *10-27кг
ma(H)=1,67375
АБСОЛЮТНАЯ
ma(C)=1,9927*10-26кг
ma 10-27 10-25кг
АБСОЛЮТНАЯ
АБСОЛЮТНАЯ
ma(O)=2,656812*10-26кг
АБСОЛЮТНАЯ
1 а.е.м.
1/12 ma(C)
C
ma(C) кг
12
1,9927*10-26 кг
12
1 а.е.м. =
=
1 а.е.м. = 1,66 * 10-27 кг
=
19.
Относительная атомная массаma(Э) Ar
кг
Ar(Э)=
безразмерная
элемента показывает
во
сколько
раз
1/12ma(C) кг
масса его
«relativ»
относительный
атома больше
1/12
массы
Её получают
атомапри
углерода
сравнении масс
атомов разных хмических
элементов с 1 а.е.м.
m(He)= 4 а.е.м.
He
Ar(He)=4
20.
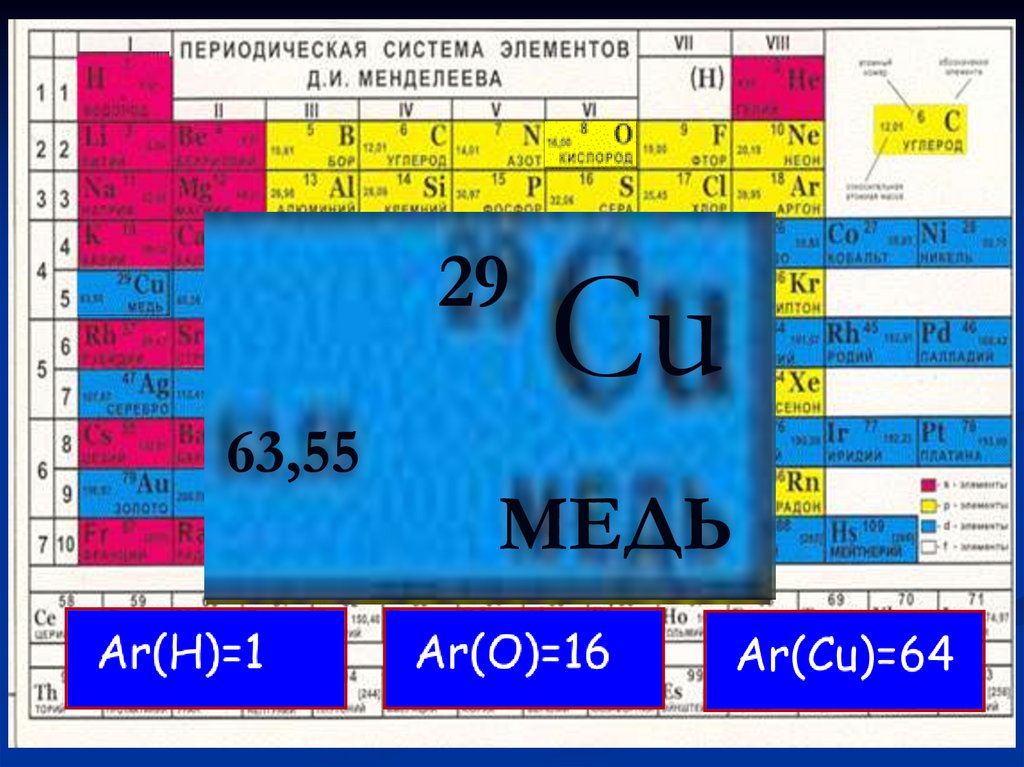
15,9963,55
0
829 Cu
КИСЛОРОД
МЕДЬ
21.
показываетобозначается
Относительная
атомная
масса
измеряется
значения
во сколько раз
масса атома х.э.
больше 1/12 массы
атома углерода
Ar
безразмерная
значения записаны в
таблице
Д.И.Менделеева
(округляем до целых чисел)
22.
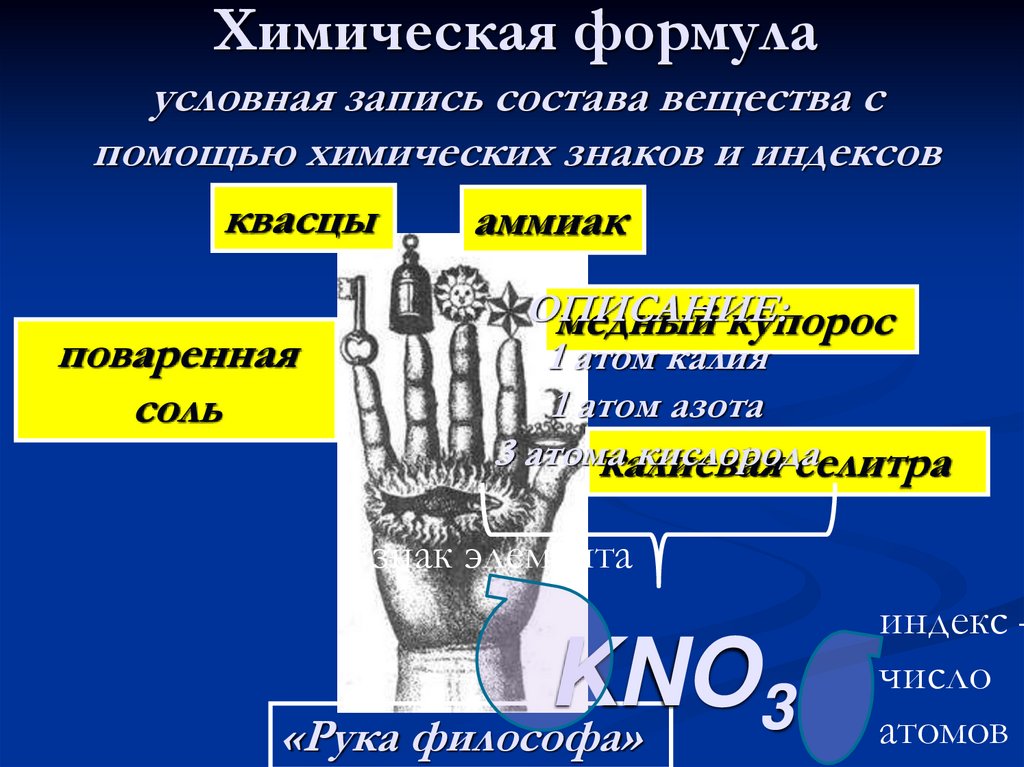
Химическая формулаусловная запись состава вещества с
помощью химических знаков и индексов
квасцы
аммиак
поваренная
соль
ОПИСАНИЕ:
медный купорос
1 атом калия
1 атом азота
3 атома
кислорода
калиевая
селитра
знак элемента
KNO
3
«Рука философа»
индекс –
число
атомов
23.
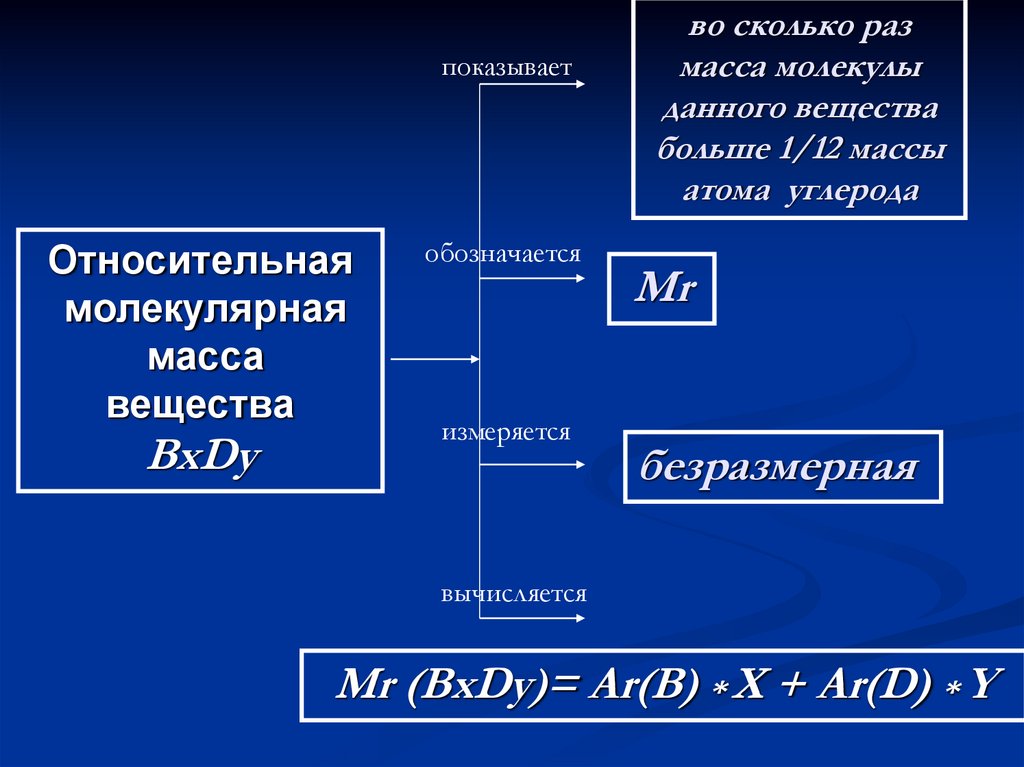
показываетОтносительная
молекулярная
масса
вещества
BxDy
обозначается
измеряется
во сколько раз
масса молекулы
данного вещества
больше 1/12 массы
атома углерода
Мr
безразмерная
вычисляется
Мr (BxDy)= Ar(B) * X + Ar(D) * Y
24.
показываетобозначается
Массовая доля
элемента в
веществе
(BxDy)
выражается
Какую долю от
общей массы
вещества
составляют атомы
данного элемента
ω (В)%
В долях единицы
или в %
вычисляется
ω (В)% =
xAr(B)
Mr(BxDy) 100%
25.
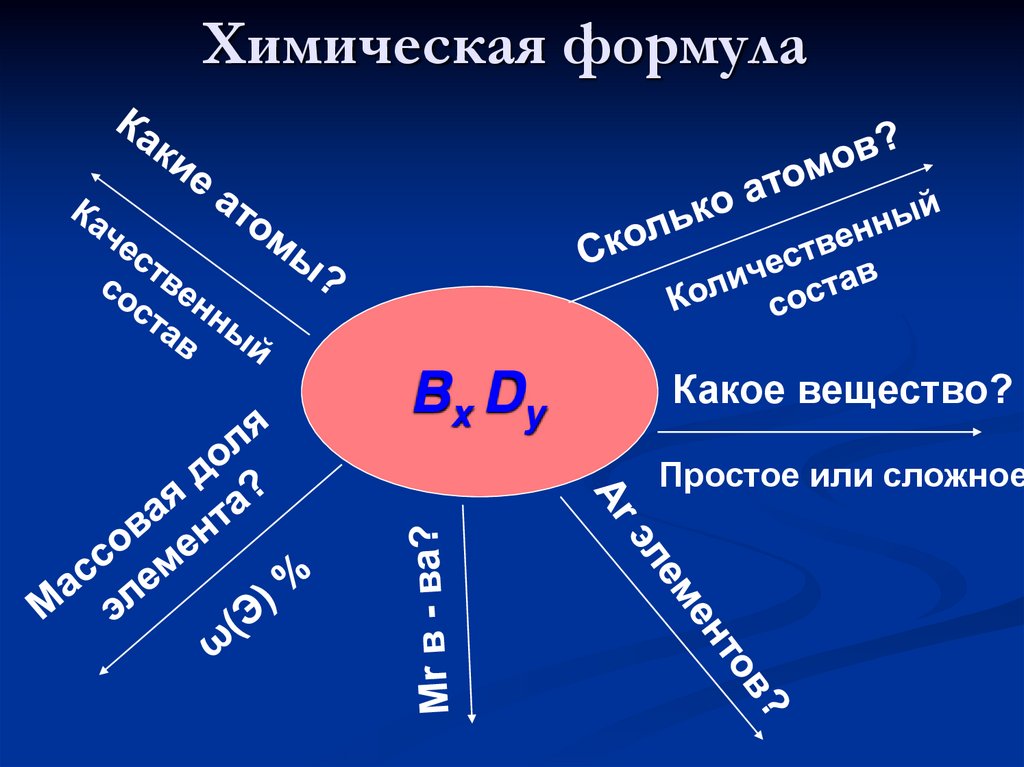
Химическая формулаBx Dy
Какое вещество?
Простое или сложное
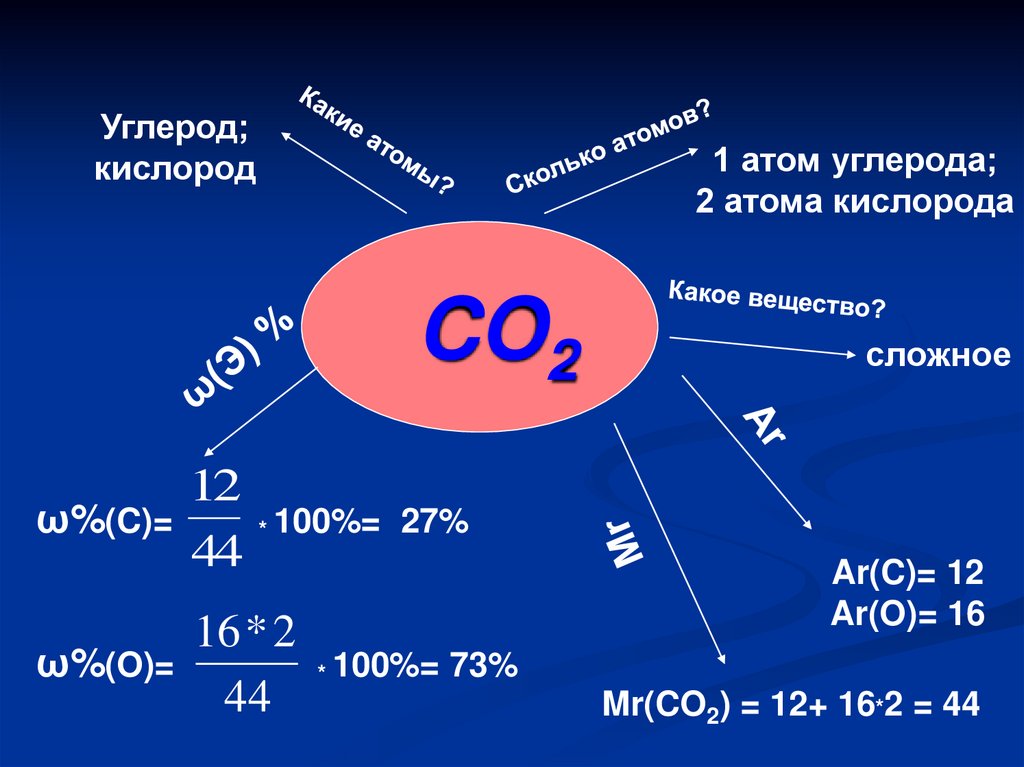
26.
Углерод;кислород
1 атом углерода;
2 атома кислорода
CO2
ω%(C)=
ω%(O)=
12
44
* 100%=
16 * 2
44
сложное
27%
Ar(C)= 12
Ar(O)= 16
* 100%=
73%
Mr(CO2) = 12+ 16*2 = 44
27.
Определить валентности элементов в оксиде серебра1. Запишите формулу вещества.
2. Обозначьте
известную
валентность
Алгоритм
элемента
определения
II
валентности по
химической
2
Оксиды - это сложныеформуле
вещества, которые
состоят из двух
вещества
элементов, один из
Ag O
которых кислород.
О – II !
28.
Определить валентности элементов в оксиде серебра3. Найдите число единиц валентности атомов
известного элемента, умножив валентность
элемента на количество его атомов
II * 1=
Ag2O 1
2
29.
Определить валентности элементов в оксиде серебра4. Поделите число единиц валентности атомов на количество
атомов другого элемента. Полученный ответ и является
искомой валентностью
2:2=I
II
Ag 2 O
30.
Обобщённая формула для нахождениявалентностей элементов
по молекулярной формуле вещества
a-? b
Am Bn
a=
Am
bn
m
b
Bn
31.
Составить химическую формулу оксида алюминия1. Запишите рядом знаки химических
элементов, которые входят в состав
Алгоритм
вещества.
составления
химической
формулы бинарного
соединения по
известным
валентностям
Al O
32.
Составить химическую формулу оксида алюминия2. Над знаками химических элементов
поставьте их валентности
III
II
Al O
33.
Составить химическую формулу оксида алюминия3. Определите НОК валентностей обоих
элементов
6
III
II
Al O
34.
Составить химическую формулу оксида алюминия4. Разделите НОК на валентность каждого
элемента. Запишите полученный индекс
6
III
II
Al O
6 : III = 2
6 : II = 3
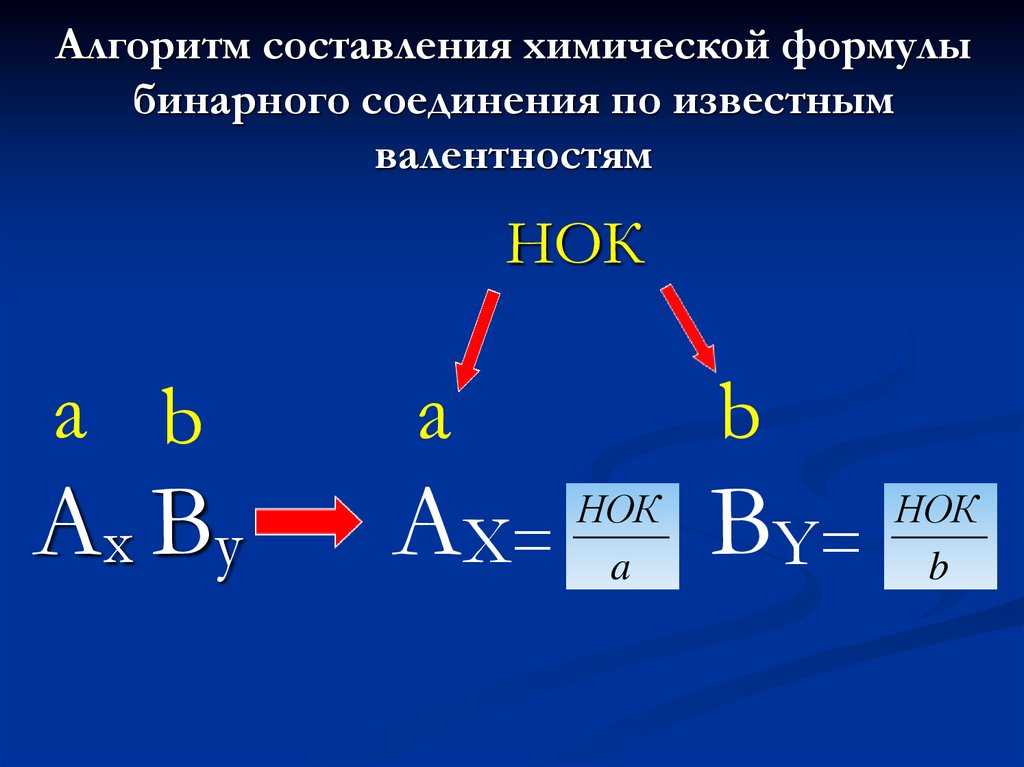
35.
Алгоритм составления химической формулыбинарного соединения по известным
валентностям
НОК
a b
Ax By
a
AX=
b
НОК
a
BY=
НОК
b
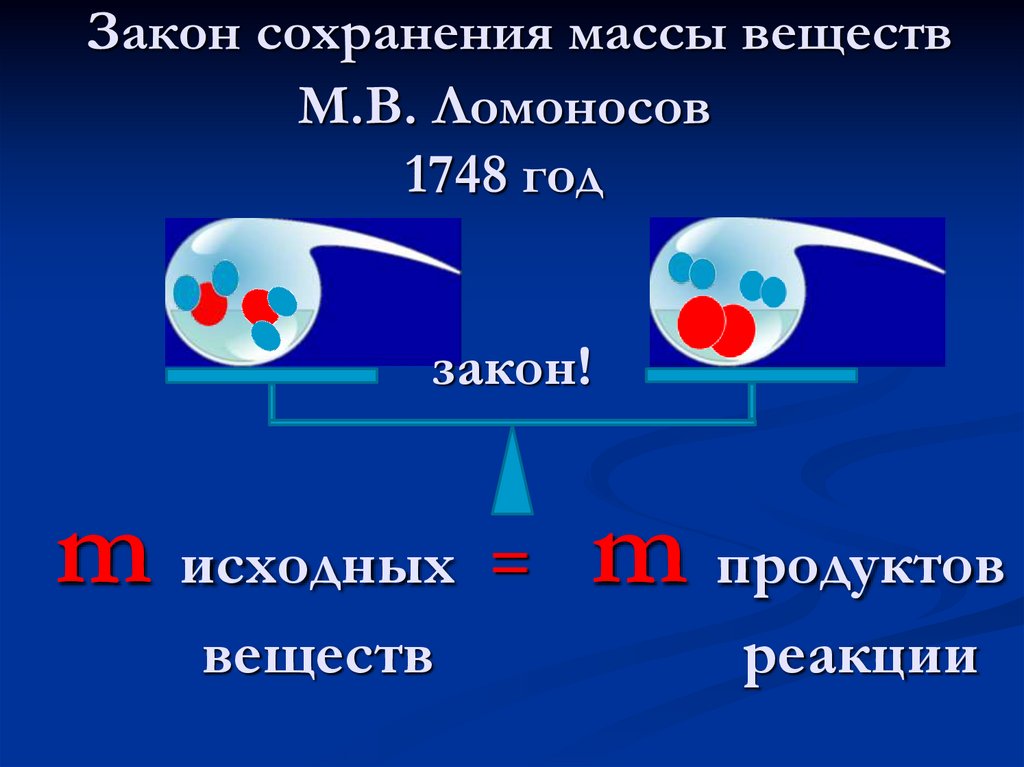
36.
закон!m исходных
веществ
m продуктов
реакции
37.
Ссылка на кинофильмhttp://video.mail.ru/mail/ninrubcov/50-60/5317.html
38.
Уравнения химических реакцийПри пропускании постоянного электрического тока
через воду образуются газы водород и кислород
ЭЛЕКТРИЧЕСКИЙ ТОК
ВОДОРОД
ВОДА
H2O
исходные в-ва
m исход. в-в
Mr(H2O)
18
18
H2
ЗАКОН!
=
=
=
=
+
КИСЛОРОД
+
O2
m продукт. р-ции
продукты р-ции
Mr(H2) + Mr(O2)
2
+
32
34
39.
Уравненияхимических
реакций
Химическим уравнением
называют условную запись
КОЭФФИЦИЕНТЫ показывают число
химической реакциичастиц
с помощью
каждого
вещества в реакции
химических знаков и формул
2 H2O
m исход. в-в
2 * Mr(H2O)
2 * 18
36
2 H2
ЗАКОН!
=
=
=
=
+
O2
m продукт. р-ции
2 * Mr(H2) + Mr(O2)
2*2
+
32
36
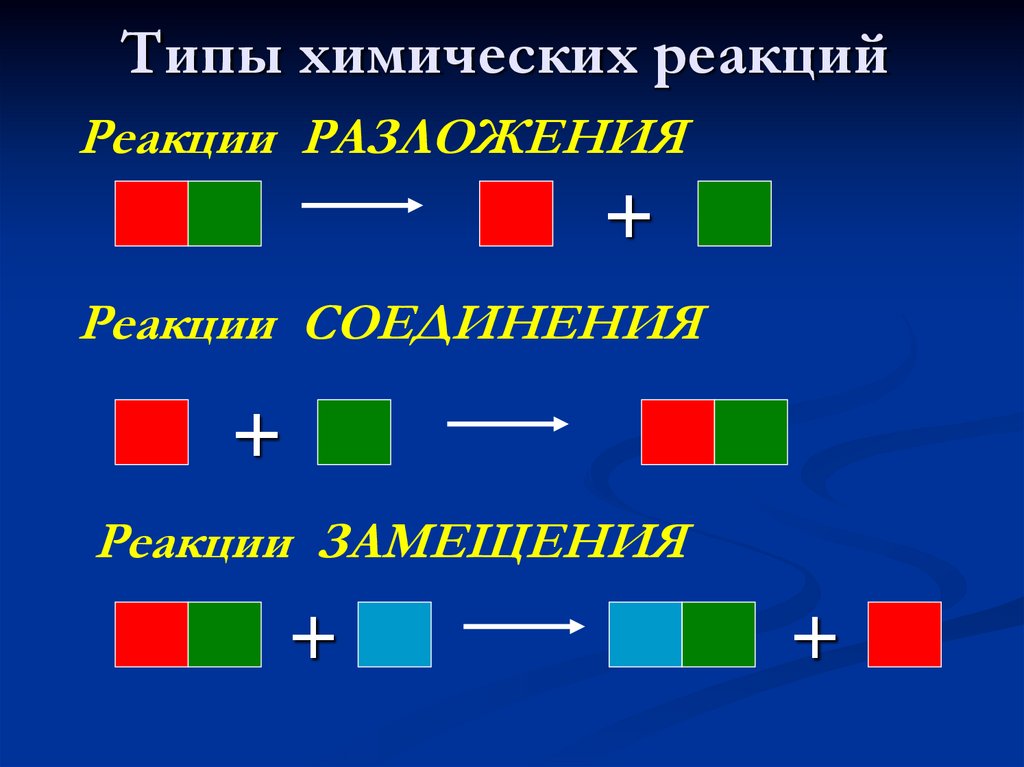
40.
Типы химических реакцийРеакции РАЗЛОЖЕНИЯ
+
Реакции СОЕДИНЕНИЯ
+
Реакции ЗАМЕЩЕНИЯ
+
+
41.
Типы химических реакцийРеакции РАЗЛОЖЕНИЯ
2 H2O2
2 KNO3
2 H2O + O2
+
2 KNO2 + O2
Реакции СОЕДИНЕНИЯ
2 Fe + 3 Cl2
2 Fe Cl3
CaO + CO2
CaCO3
+
Реакции ЗАМЕЩЕНИЯ
WO3 + 3+
H2
2 Al + 3 CuCl2
W + 3H
+2 O
2 AlCl3 + 3 Cu
42.
Количество вещества- это физическая величина,
которая означает
определенное число структурных частиц
(атомов, молекул и др.) и др.)
(«ню»)
43.
Моль вещества1 моль - это количество вещества, которое
содержит столько же частиц,сколько
содержится атомов углерода
в 12 граммах углерода
1 моль любого
вещества
NA=6.02•10²³
Постоянная Авогадро - физическая величина,
которая показывает сколько структурных частиц
содержится в одном моль вещества
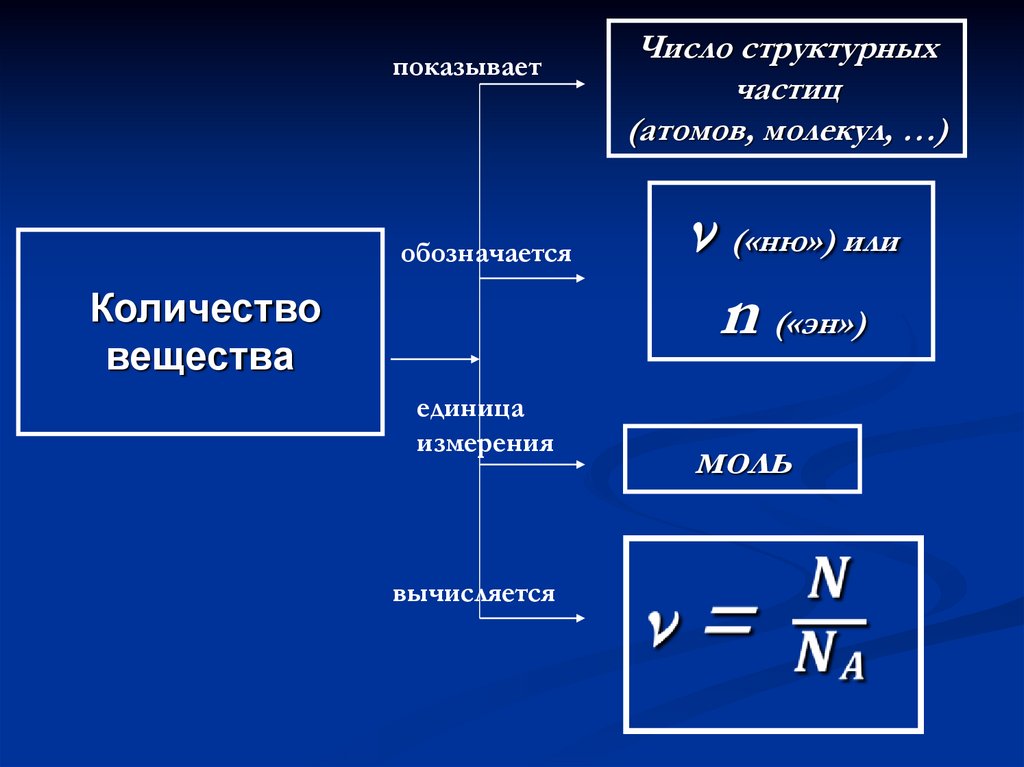
44.
показываетобозначается
Количество
вещества
единица
измерения
вычисляется
Число структурных
частиц
(атомов, молекул, …)
ν («ню») или
n («эн»)
моль
45.
показываетобозначается
Число Авогадро
(постоянная
Авогадро)
Число структурных
частиц
в 1 моль вещества
NA
единица
измерения
численное
значение
NA= 6,02 * 10 23
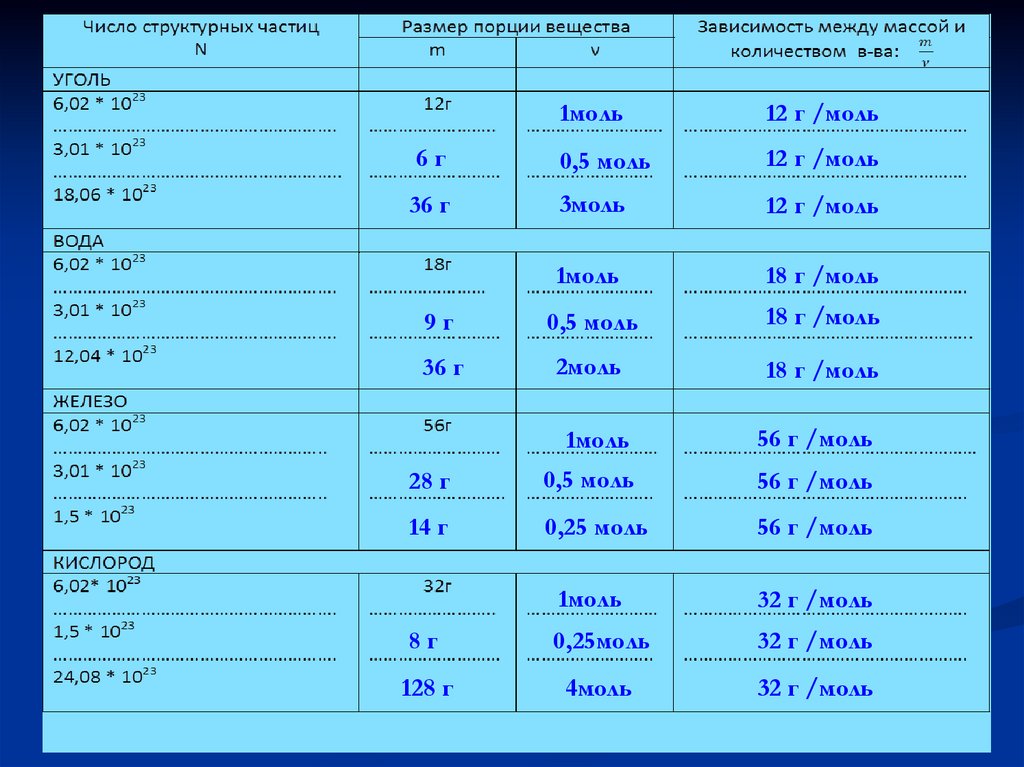
46.
Молярная масса1моль
12 г /моль
- это физическая
величина,
6г
0,5 моль
12 г /моль
1моль
18 г /моль
0,5 моль
18 г /моль
которая показывает
какова масса
3моль
36 г
12 г /моль
одного моль вещества
вещества
m
M=
9г
2моль
36 г
[кг/моль;г/моль]
28 г
18 г /моль
1моль
56 г /моль
0,5 моль
56 г /моль
{M г/моль}=Mr
14 г
0,25 моль
56 г /моль
1моль
32 г /моль
8г
0,25моль
32 г /моль
128 г
4моль
32 г /моль
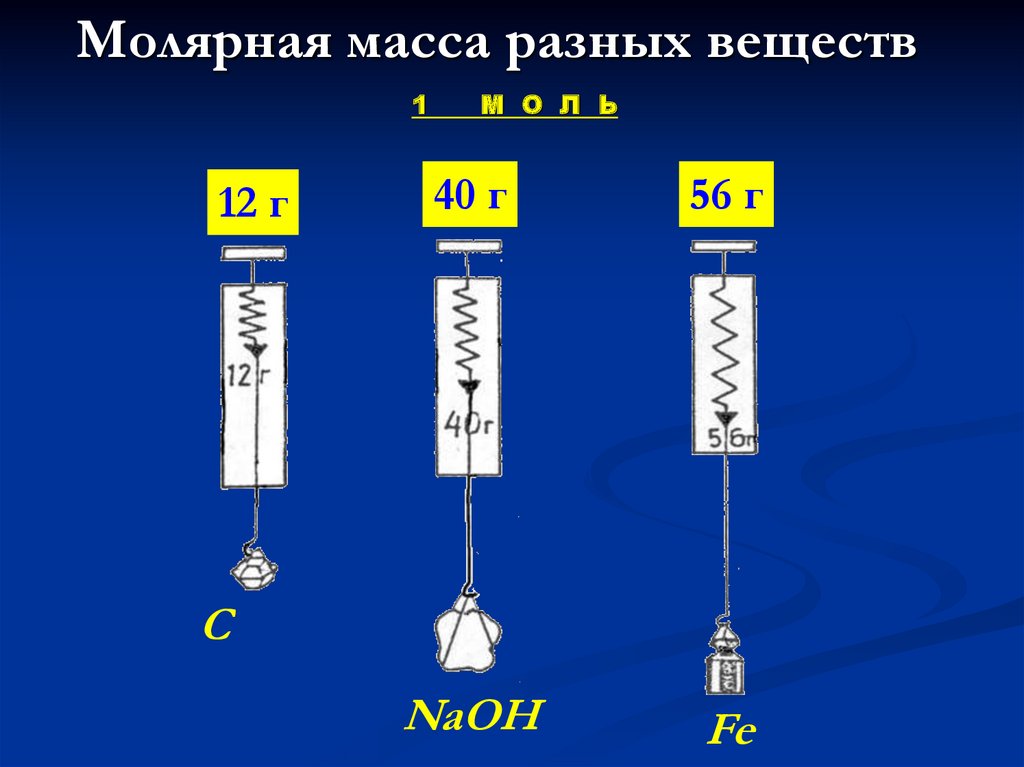
47.
Молярная масса разных веществ1
12 г
М О Л Ь
40 г
56 г
NaOH
Fe
C
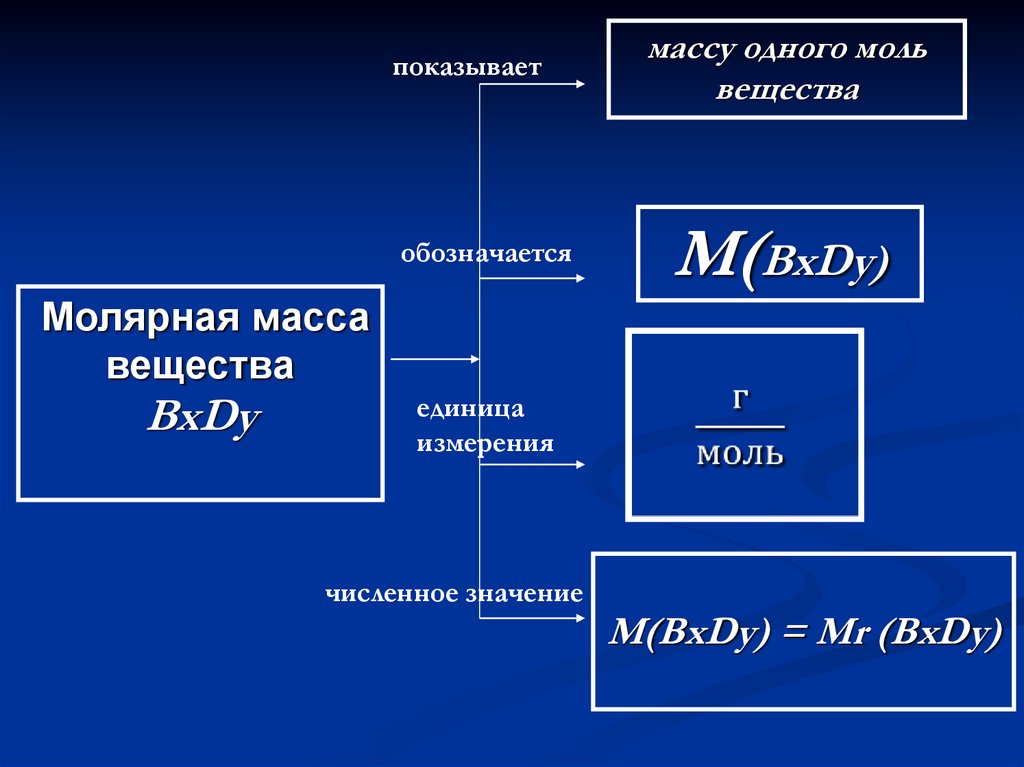
48.
показываетобозначается
массу одного моль
вещества
М(BxDy)
Молярная масса
вещества
BxDy
единица
измерения
численное значение
М(BxDy) = Мr (BxDy)
49.
Закон АвогадроВ равных объёмах различных газов
при одинаковых условиях
содержится одинаковое число
молекул
50.
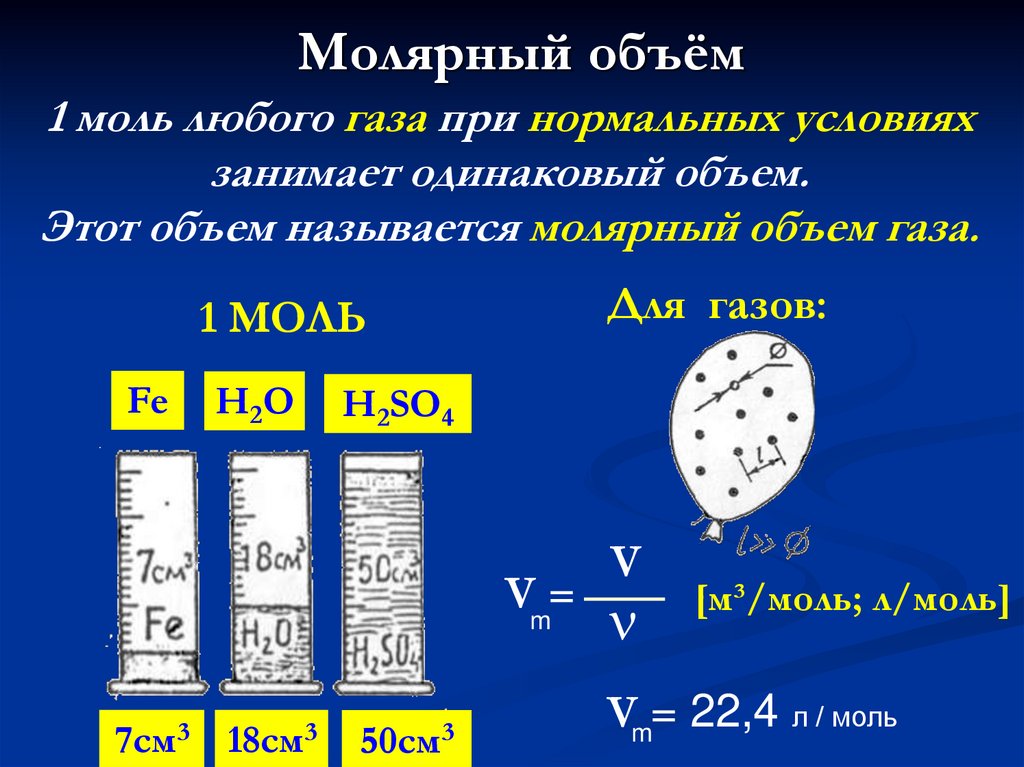
Молярный объём1 моль любого газа при нормальных условиях
занимает одинаковый объем.
Этот объем называется молярный объем газа.
Для газов:
1 МОЛЬ
Fe
H2O
H2SO4
Vm=
7см3
18см3
50см3
V
[м³/моль; л/моль]
Vm= 22,4 л / моль
51.
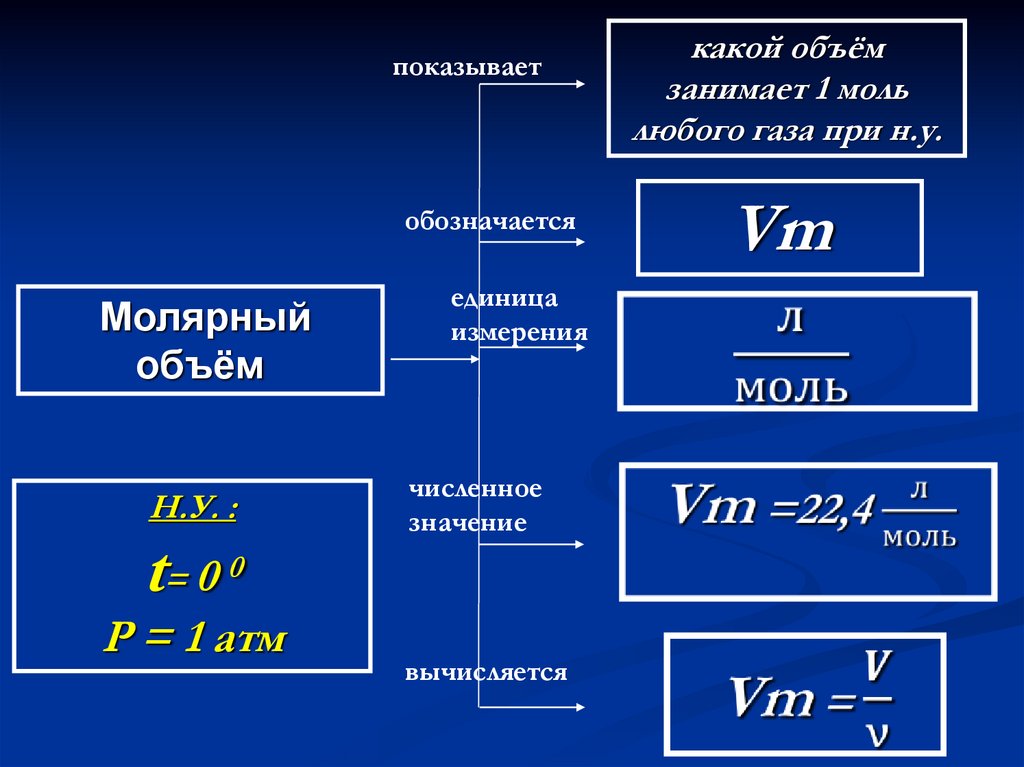
показываетобозначается
Молярный
объём
Н.У. :
t= 0 0
P = 1 атм
единица
измерения
численное
значение
вычисляется
какой объём
занимает 1 моль
любого газа при н.у.
Vm
52.
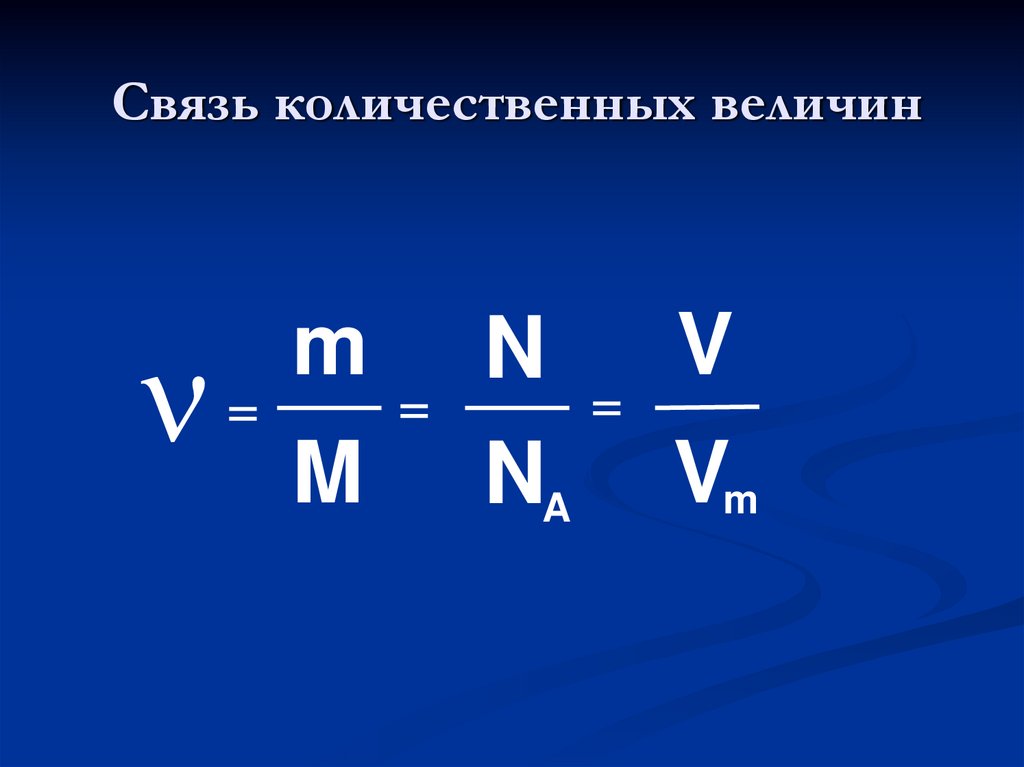
Связь количественных величин=
m
M
=
V
N
=
NA Vm
53.
Список литературы«Обобщающие опорные схемы по химии: методика
конструирования и использования, примеры схем с описанием»
И.И. Супоницкая, Н.И. Гоголевская
«Химия-8» Г.Е. Рудзитис, Ф.Г. Фельдман
рабочая тетрадь для 8 класса «Первоначальные химические
понятия» И.Н. Городничева
рабочая тетрадь для 8 класса «Химические элементы и
химические законы» И.А. Леенсон
рабочей тетради для 7 класса О.С. Габриелян, Г.А. Шипарева
«Использование алгоритмов при изучении валентности»
Супоницкая И.И.
Авторские разработки, сайт учителя
www.netschools.ru/sch518/koridor/him/site/index.htm






























 chemistry
chemistry








