Similar presentations:
Циклоалканы
1.
Циклопарафины, нафтены, цикланы,полиметилены — это всё названия
циклоалканов.
2.
Циклоалканы — это представителиуглеводородов с замкнутой
(циклической) углеродной цепью.
3.
Амбра и мускус, лимонное имятное масла издавна входили
в состав восточных благовоний.
4.
Лекарствами служили камфора,получаемая из листьев
камфорного лавра, а также
терпентинное масло из смолы
хвойного дерева.
5.
Состав и строение давноизвестных природных
веществ были определены
лишь в XIX веке.
6.
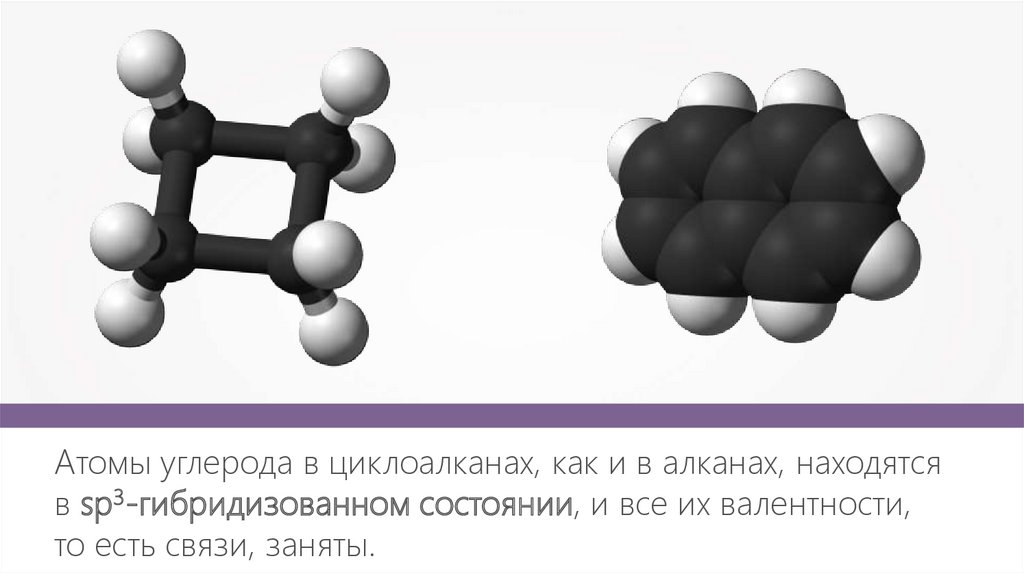
Атомы углерода в циклоалканах, как и в алканах, находятсяв sp3-гибридизованном состоянии, и все их валентности,
то есть связи, заняты.
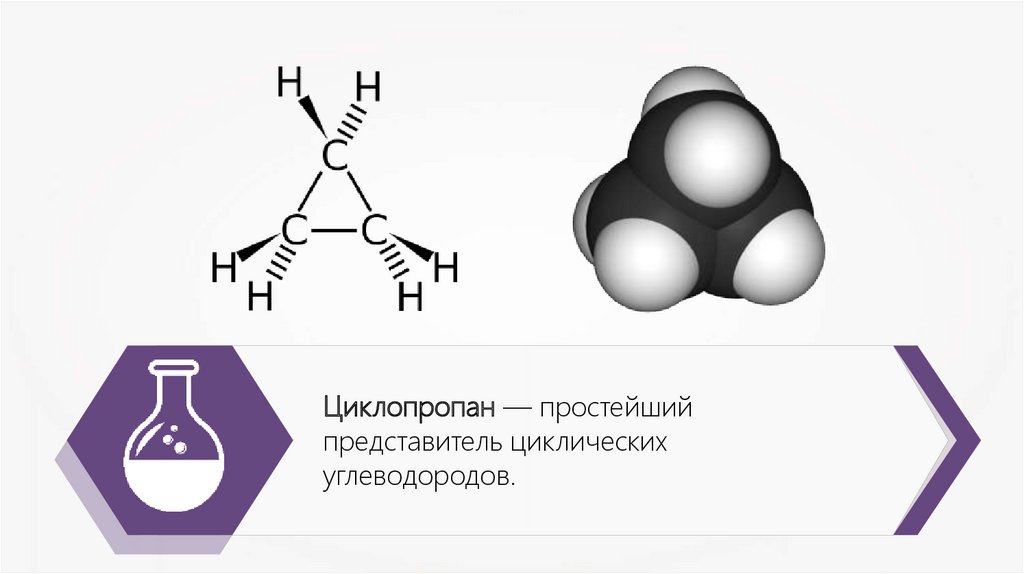
7.
Циклопропан — простейшийпредставитель циклических
углеводородов.
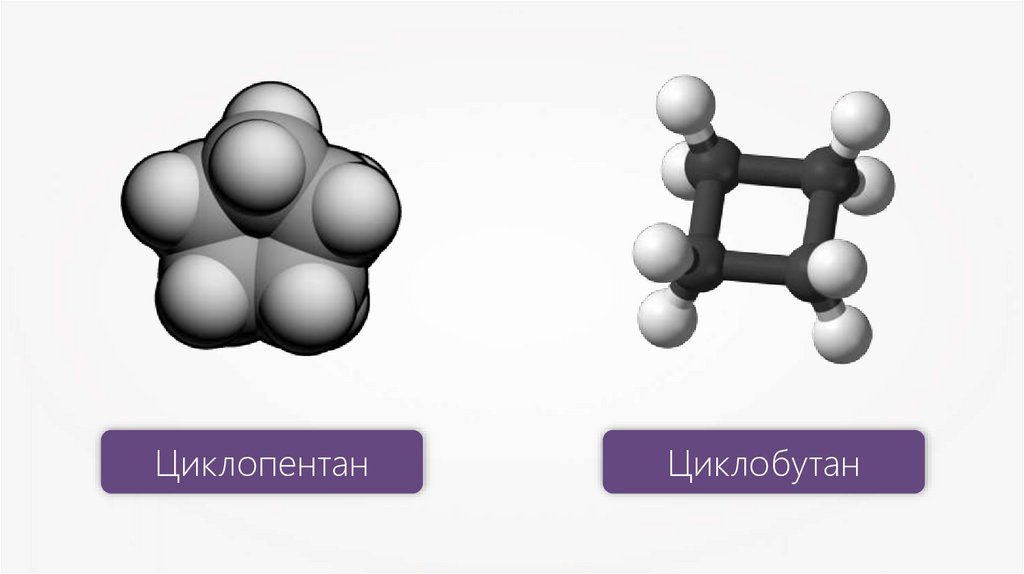
8.
ЦиклопентанЦиклобутан
9.
СnН2nОбщая формула гомологического ряда
циклоалканов. Циклоалканы изомерны
этиленовым углеводородам.
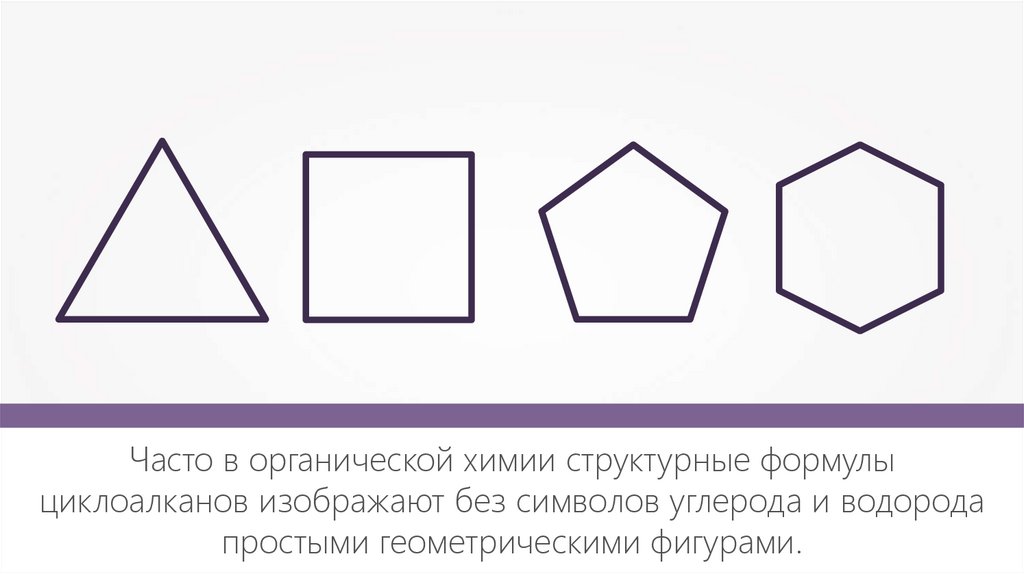
10.
Часто в органической химии структурные формулыциклоалканов изображают без символов углерода и водорода
простыми геометрическими фигурами.
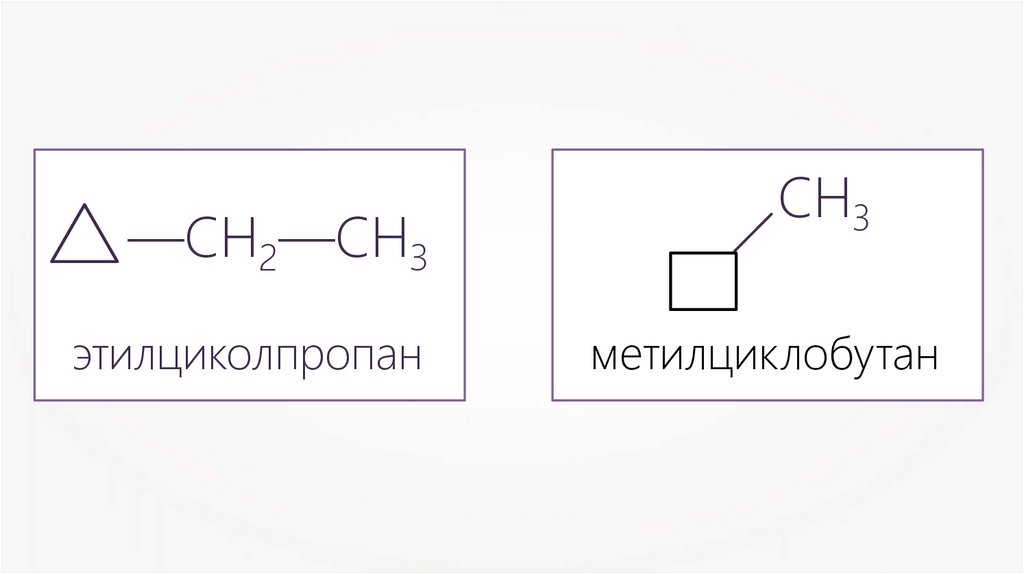
11.
—СН2—СН3этилциколпропан
СН3
метилциклобутан
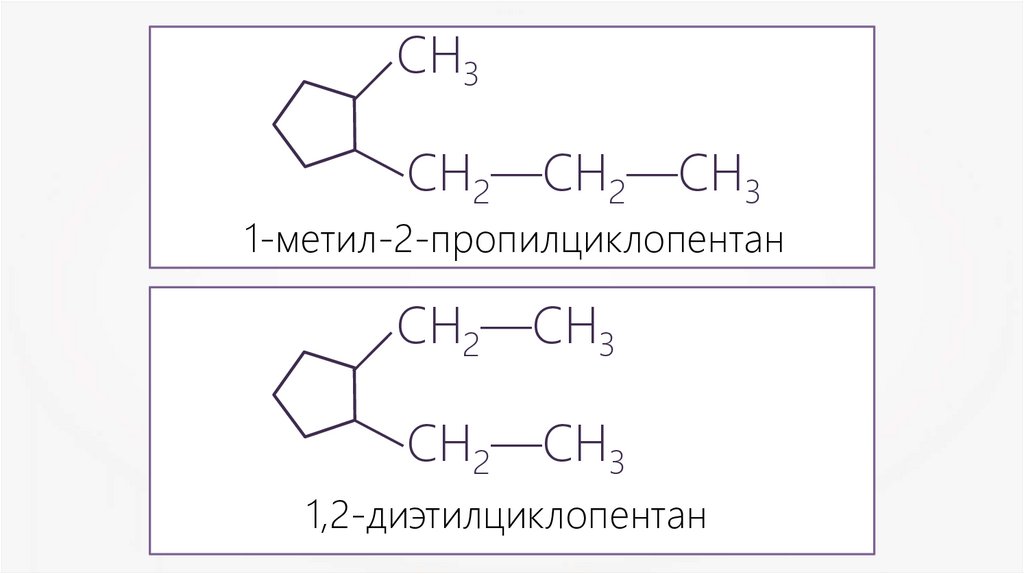
12.
СН3СН2—СН2—СН3
1-метил-2-пропилциклопентан
СН2—СН3
СН2—СН3
1,2-диэтилциклопентан
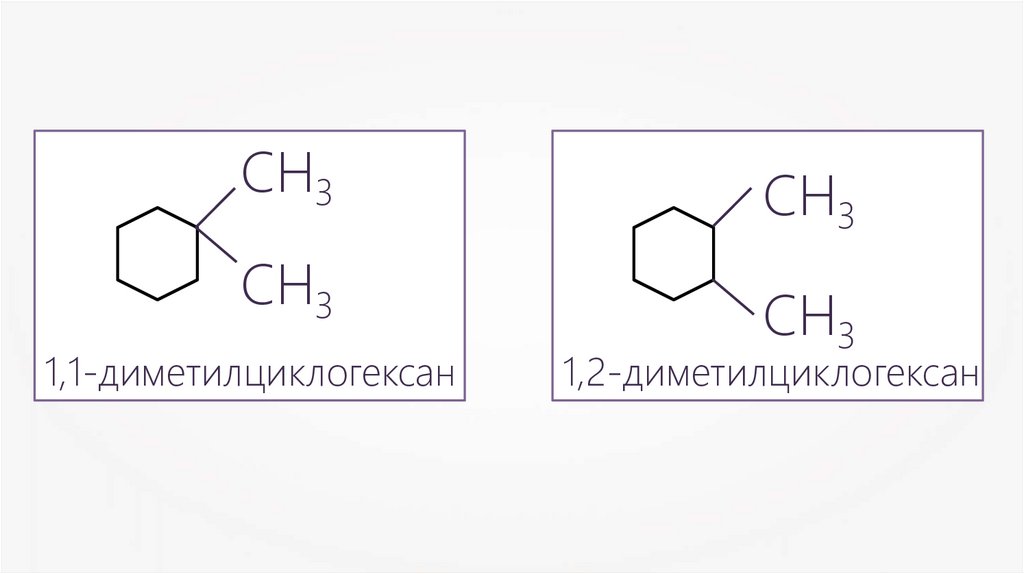
13.
СН3СН3
1,1-диметилциклогексан
СН3
СН3
1,2-диметилциклогексан
14.
Для циклоалканов характерна такжемежклассовая изомерия с алкенами.
При наличии двух заместителей
в кольце у разных углеродных атомов
возможна геометрическая
цис-транс-изомерия, начиная с C5H10 ,
и оптическая изомерия.
15.
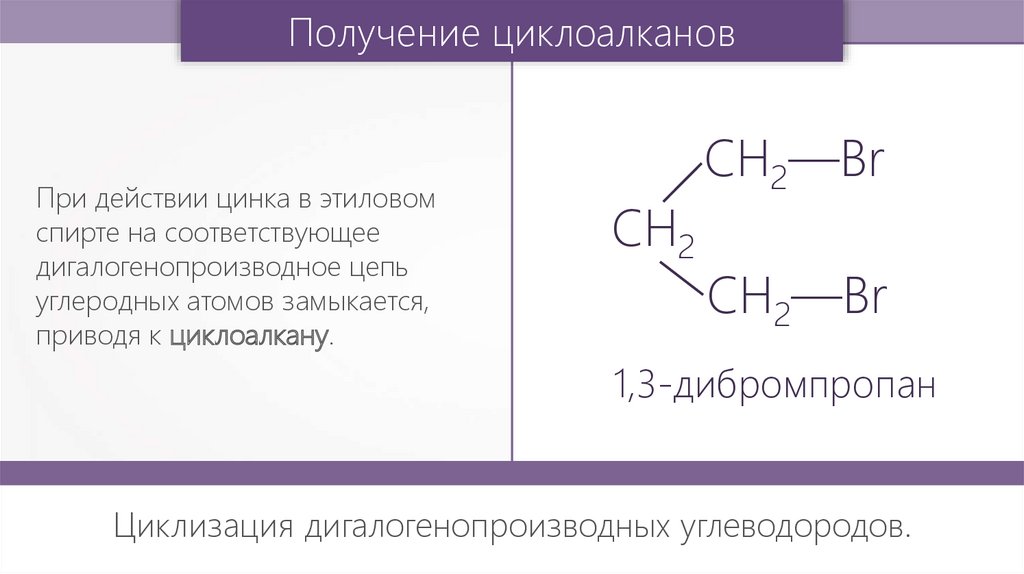
Получение циклоалкановПри действии цинка в этиловом
спирте на соответствующее
дигалогенопроизводное цепь
углеродных атомов замыкается,
приводя к циклоалкану.
СН2
СН2—Br
СН2—Br
1,3-дибромпропан
Циклизация дигалогенопроизводных углеводородов.
16.
Получение циклоалканов— —
—
—
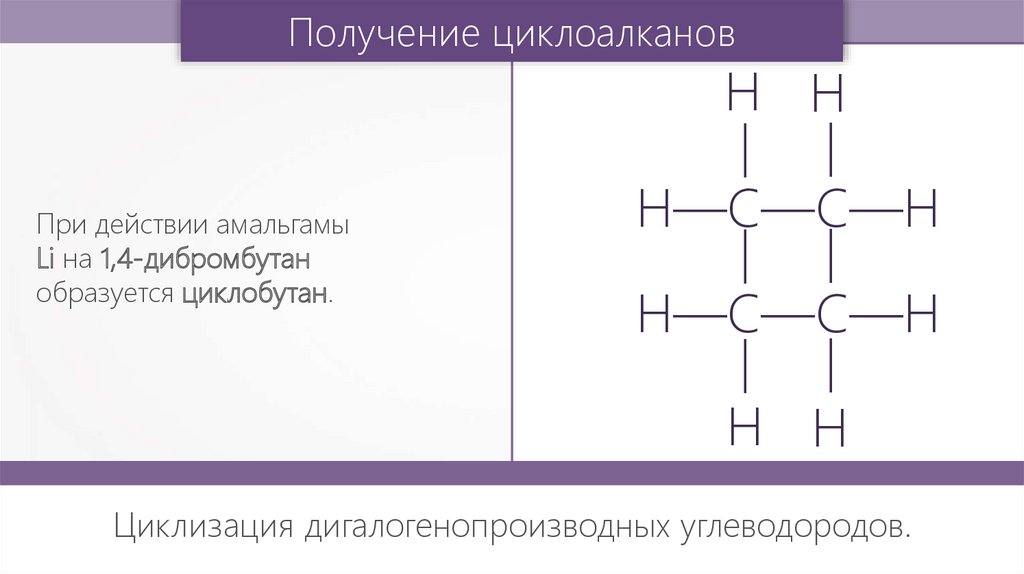
При действии амальгамы
Li на 1,4-дибромбутан
образуется циклобутан.
— —
Н Н
Н—С—С—Н
Н—С—С—Н
Н Н
Циклизация дигалогенопроизводных углеводородов.
17.
Получение циклоалканов+ 3H2 →
t, p, Ni
Гидрогенизация ароматических соединений.
18.
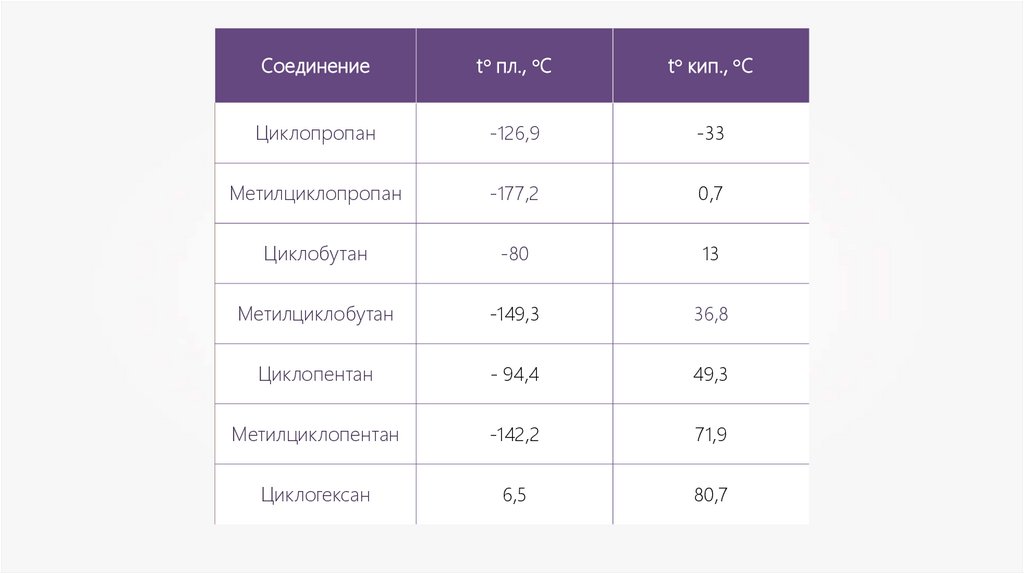
Соединениеt° пл., °С
t° кип., °С
Циклопропан
-126,9
-33
Метилциклопропан
-177,2
0,7
Циклобутан
-80
13
Метилциклобутан
-149,3
36,8
Циклопентан
- 94,4
49,3
Метилциклопентан
-142,2
71,9
Циклогексан
6,5
80,7
19.
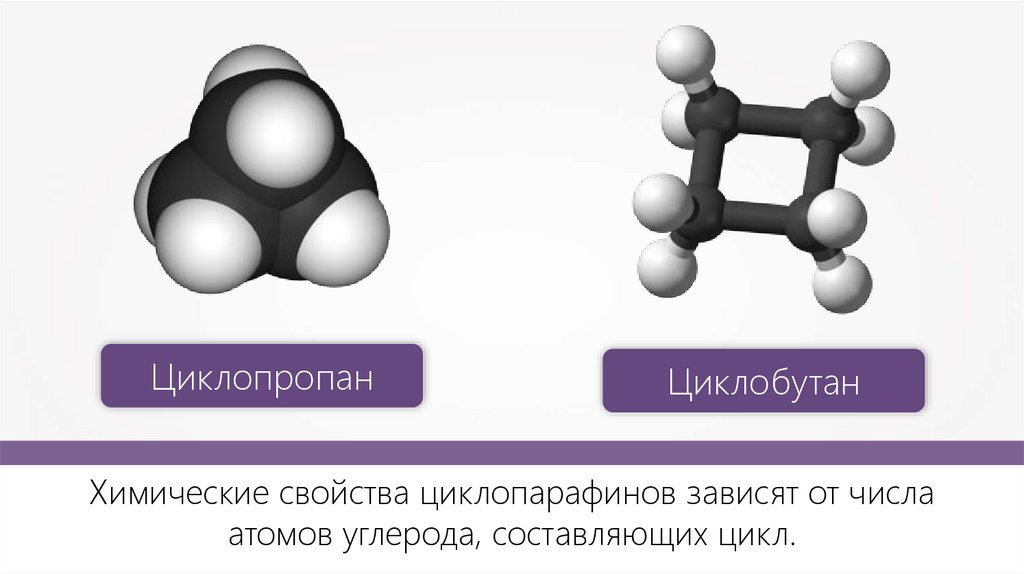
ЦиклопропанЦиклобутан
Химические свойства циклопарафинов зависят от числа
атомов углерода, составляющих цикл.
20.
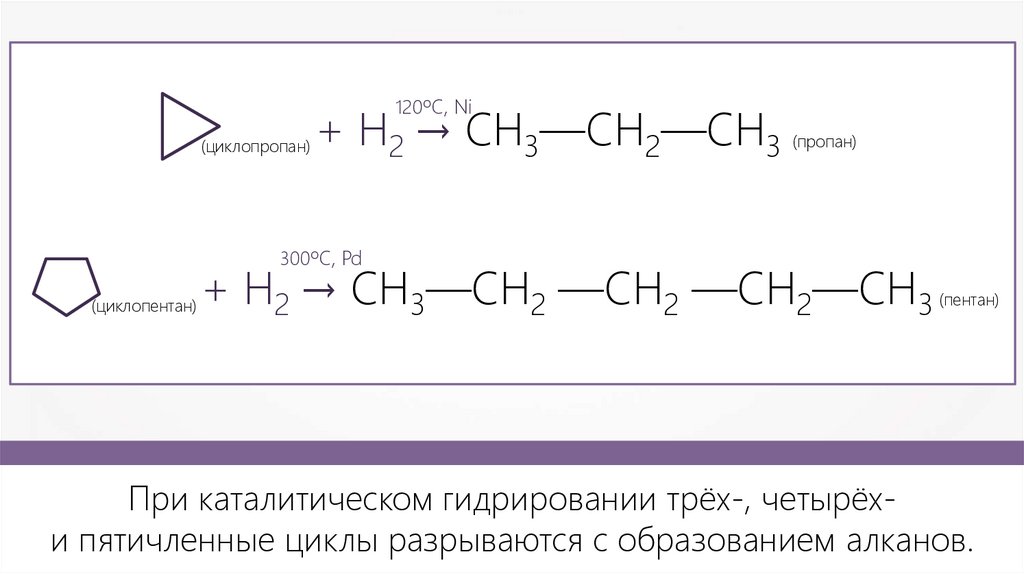
120ºC, Ni(циклопропан)
+ H2 → CH3—CH2—CH3
(пропан)
300ºC, Pd
(циклопентан)
+ H2 → CH3—CH2 —CH2 —CH2—CH3
(пентан)
При каталитическом гидрировании трёх-, четырёхи пятичленные циклы разрываются с образованием алканов.
21.
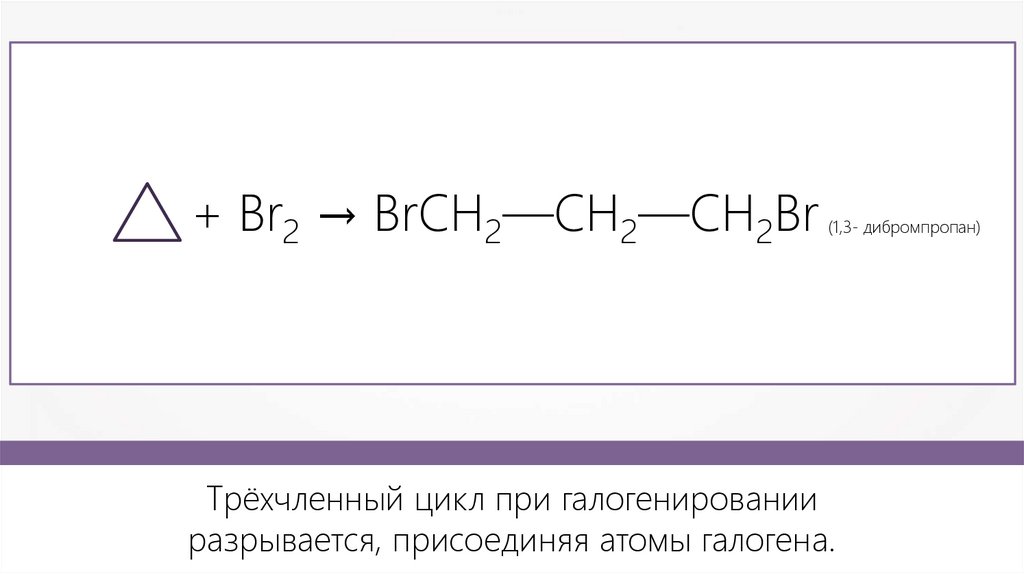
+ Br2 → BrCH2—CH2—CH2Br(1,3- дибромпропан)
Трёхчленный цикл при галогенировании
разрывается, присоединяя атомы галогена.
22.
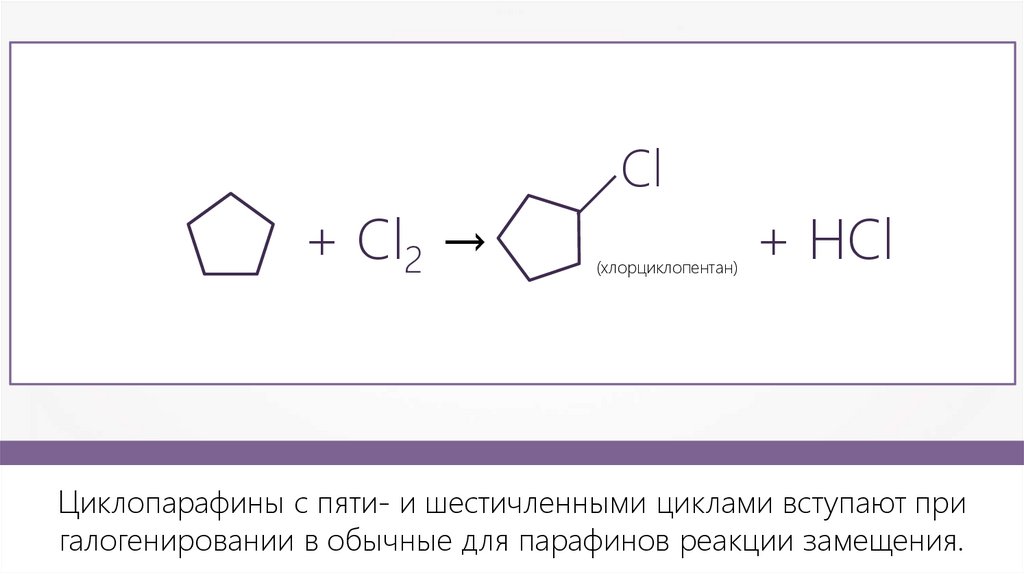
+ Cl2 →Сl
(хлорциклопентан)
+ НCl
Циклопарафины с пяти- и шестичленными циклами вступают при
галогенировании в обычные для парафинов реакции замещения.
23.
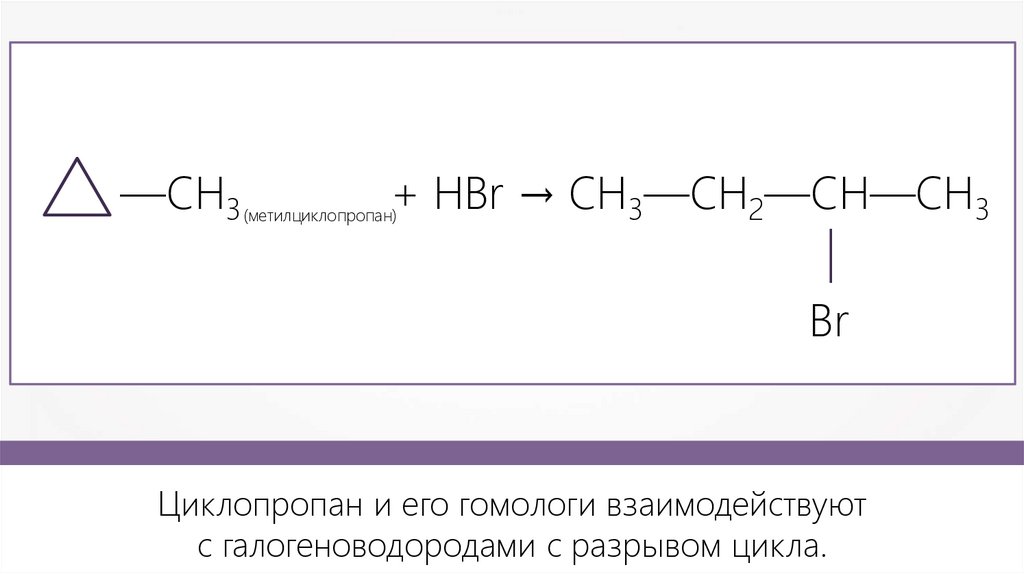
—CH3+ HBr → CH3—CH2—CH—CH3
(метилциклопропан)
—
Br
Циклопропан и его гомологи взаимодействуют
с галогеноводородами с разрывом цикла.
24.
Правило Марковникова:при присоединении галогенводорода
к алкену водород присоединяется
к более гидрогенизированному
атому.
В.В. Марковников
1837–1904 гг.
25.
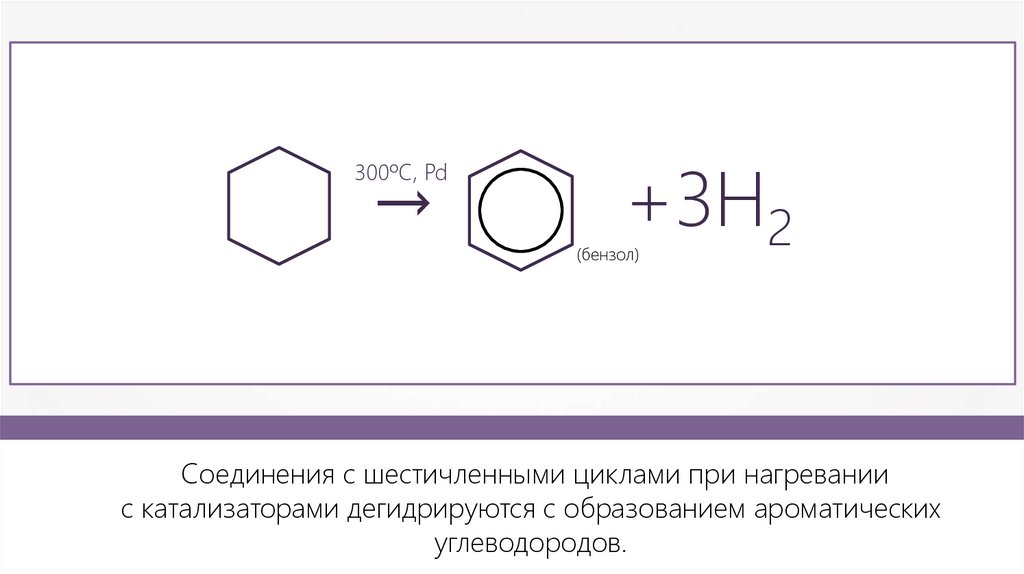
→300ºC, Pd
+3Н2
(бензол)
Соединения с шестичленными циклами при нагревании
с катализаторами дегидрируются с образованием ароматических
углеводородов.
26.
О—
[O]
—
О
НО
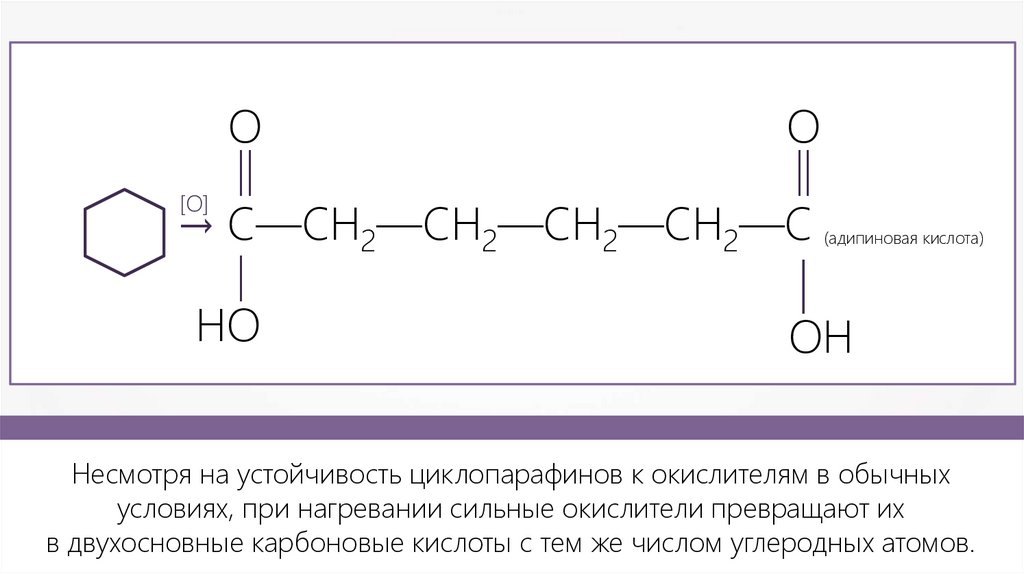
(адипиновая кислота)
—
—
→ С—CH2—CH2—CH2—CH2—С
ОН
Несмотря на устойчивость циклопарафинов к окислителям в обычных
условиях, при нагревании сильные окислители превращают их
в двухосновные карбоновые кислоты с тем же числом углеродных атомов.
27.
С4Н8 + 6О2→ 4СО2 + 4Н2ОРеакция полного сгорания циклобутана.
28.
Наибольшее практическое значениеимеют циклогексан, этилциклогексан.
Циклогексан используется
для получения циклогексанола,
циклогексанона, адипиновой кислоты,
а также в качестве растворителя.










 chemistry
chemistry