Similar presentations:
Биохимия биологических мембран
1.
БАШКИРСКИЙ ГОСУДАРСТВЕННЫЙМЕДИЦИНСКИЙ УНИВЕРСИТЕТ
БИОХИМИЯ
БИОЛОГИЧЕСКИХ
МЕМБРАН
Профессор, д.м.н. – Ш.Н. Галимов
2.
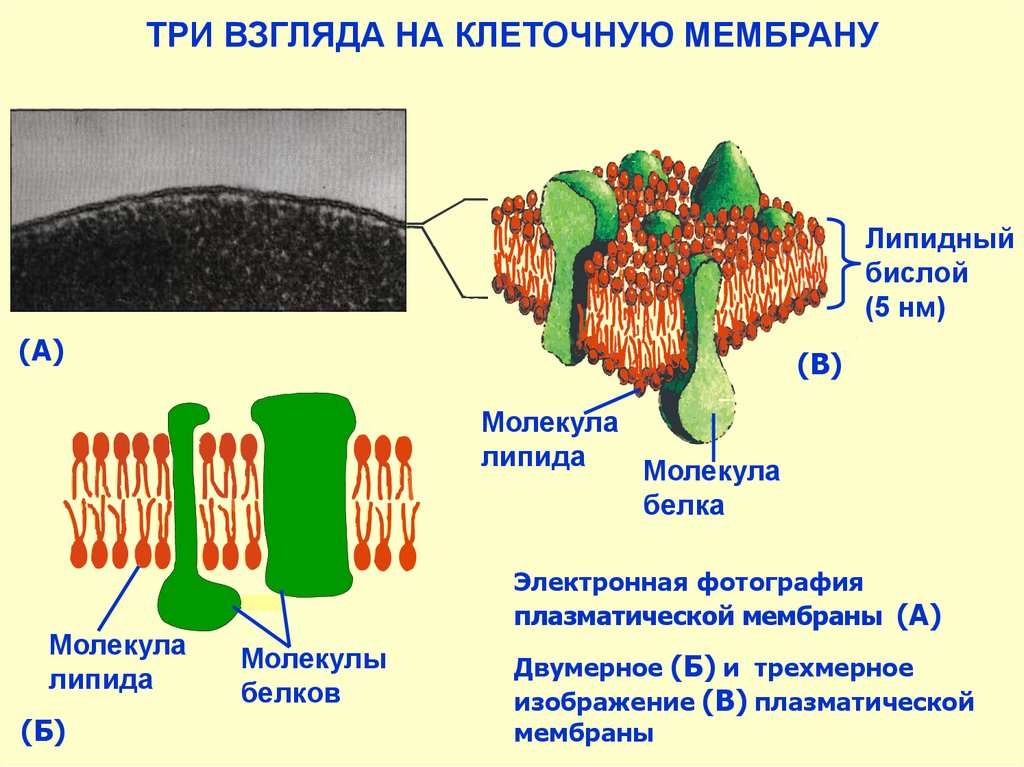
ТРИ ВЗГЛЯДА НА КЛЕТОЧНУЮ МЕМБРАНУЛипидный
бислой
(5 нм)
(А)
(В)
Молекула
липида
Молекула
липида
(Б)
Молекула
белка
Электронная фотография
плазматической мембраны (А)
Молекулы
белков
Двумерное (Б) и трехмерное
изображение (В) плазматической
мембраны
3.
ГЛИЦЕРОФОСФОЛИПИДЫ МЕМБРАНСН2―N+(CH3)3
Полярная
«головка»
CH2
O
O=P―O-
ХОЛИН
ФОСФАТ
ЖИРНАЯ КИСЛОТА
ГЛИЦЕРОЛ
Гидрофобный
«хвост»
Полярная
«головка»
O
CH2―CH―CH2
O
O
C=O
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH3
C=O
CH2
CH2
CH2
CH2
CH2 цис-двойная
CH2
связь
CH2
CH
CH
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH3
Гидрофобный
«хвост»
4.
ПОЛОЖЕНИЕ ХОЛЕСТЕРОЛА В ЛИПИДНОМ БИСЛОЕФосфолипиды
3
«Полярные
головки»
нм
2
1
0
Область
холестерола,
придающего
жесткость
мембране
Область
гидрофобного
хвоста,
обладающего
большей
жидкостностью
5.
РАСПОЛОЖЕНИЕ БЕЛКОВ В МЕМБРАНАХНаружная поверхность мембраны
Цитозольная поверхность мембраны
Интегральные (трансмембранные) белки:
1 – гликофорин А, 2 - рецептор адреналина и 3.
Поверхностные белки:
4 - белки, присоединённые к полярным «головкам» липидного слоя
(протеинкиназа С), 5 - белки, «заякоренные» в мембране с помощью
короткого гидрофобного концевого домена (цитохром Ь5) 6 - «заякоренные»
белки, ковалентно соединённые с липидом мембраны (щелочная фосфатаза),
7 и 8 - белки, связанные с интегральными белками (сукцинатдегидрогенза).
6.
РАЗЛИЧНАЯ СПОСОБНОСТЬ УПАКОВКИ МЕМБРАННЫХЛИПИДОВ В ЗАВИСИМОСТИ ОТ НАСЫЩЕННОСТИ ЖИРНЫХ
КИСЛОТ В БИСЛОЕ
Ненасыщенные
жирные кислоты
(цис-двойные связи)
Насыщенные
жирные кислоты
7.
ТИПЫ ДВИЖЕНИЙ ЛИПИДНЫХ МОЛЕКУЛ В БИСЛОЕМЕМБРАН
Латеральная диффузия
«Флип-флоп»
перескоки
происходят
очень
редко
Изгибание
Вращение
8.
АКТИВНЫЙ И ПАССИВНЫЙ ТРАНСПОРТТранспортируемые молекулы
Белковый
канал
Белкипереносчики
Концентрационный
градиент
Простая
диффузия
Облегченная диффузия
ПАССИВНЫЙ ТРАНСПОРТ
АКТИВНЫЙ ТРАНСПОРТ
9.
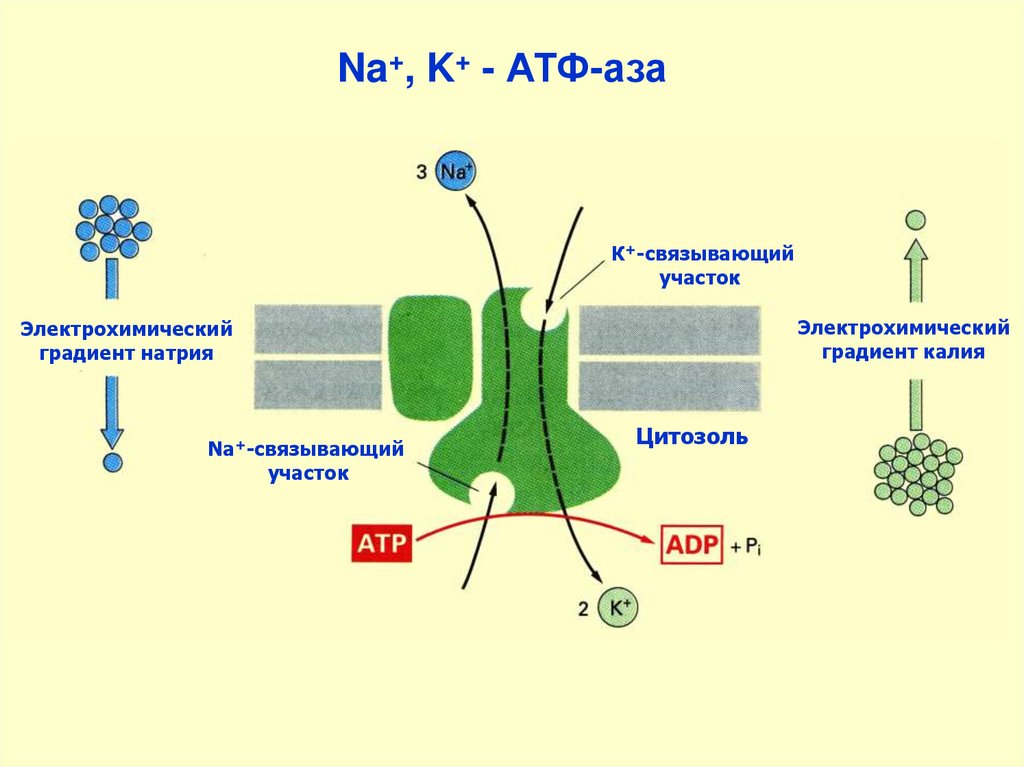
Na+, K+ - АТФ-азаК+-связывающий
участок
Электрохимический
градиент калия
Электрохимический
градиент натрия
Na+-связывающий
участок
Цитозоль
10.
Na+- ЗАВИСИМЫЙ ТРАНСПОРТ Ca2+Наружная
поверхность
мембраны
Внутренняя
поверхность
мембраны
Na+
Ca2+
3 Na+
2
K+
Na+
Na+- зависимый
переносчик
2+
Ca ионов кальция
3 Na+
2 K+
Na+, К+- АТФ-аза
АДФ+Рi
АТФ
11.
Na+- ЗАВИСИМЫЙ ТРАНСПОРТ ГЛЮКОЗЫВ ТОНКОМ КИШЕЧНИКЕ
Полость
тонкой
кишки
Цитоплазма
энтероцита
Na+
Na+
Глюкоза
3 Na+
2
K+
Глюкоза
3 Na+
2 K+
Na+, К+- АТФ-аза
АДФ+Рi
АТФ
12.
ВИДЫ ТРАНСМЕМБРАННОГО ТРАНСПОРТАС УЧАСТИЕМ ПЕРЕНОСЧИКОВ (ТРАНСЛОКАЗ)
Транспортируемая молекула
УНИПОРТ
СИМПОРТ
Ко-транспортируемое
молекула (ион)
АНТИПОРТ
13.
ПОЛОЖЕНИЕ РЕЦЕПТОРОВ ЛПНПВ ЦИТОПЛАЗМАТИЧЕСКОЙ МЕМБРАНЕ
Участок связывания
с частицей ЛПНП
Частица ЛПНП
Цитоплазма
Белок
рецептор ЛПНП
Участок связывания
с окаймленной ямкой
Дефектные белки-рецепторы
ЛПНП, не имеющие участка
связывания с окаймленной ямкой
Клатрин и другие
ассоциированные с
каймой белки
Окаймленная ямка
Плазматическая
мембрана
14.
БЕЛКИ (РЕЦЕПТОРЫ) КЛЕТОЧНОЙ АДГЕЗИИИНТЕГРИНЫ:
КАДГЕРИНЫ и СЕЛЕКТИНЫ
(более 20 разных типов)
- Рецепторы для белков
Са2+-зависимые гликопротеиды
внеклеточного матрикса
Рецепторы эпителиальных и
(коллаген, фибронектин,
эмбриональных тканей, нервных
ламинин и др.)
клеток, миокарда, хрусталика и
- Интегрины тромбоцитов
других
- Лейкоцитарные белки адгезии
© 2010, Ш.Н.Галимов
15.
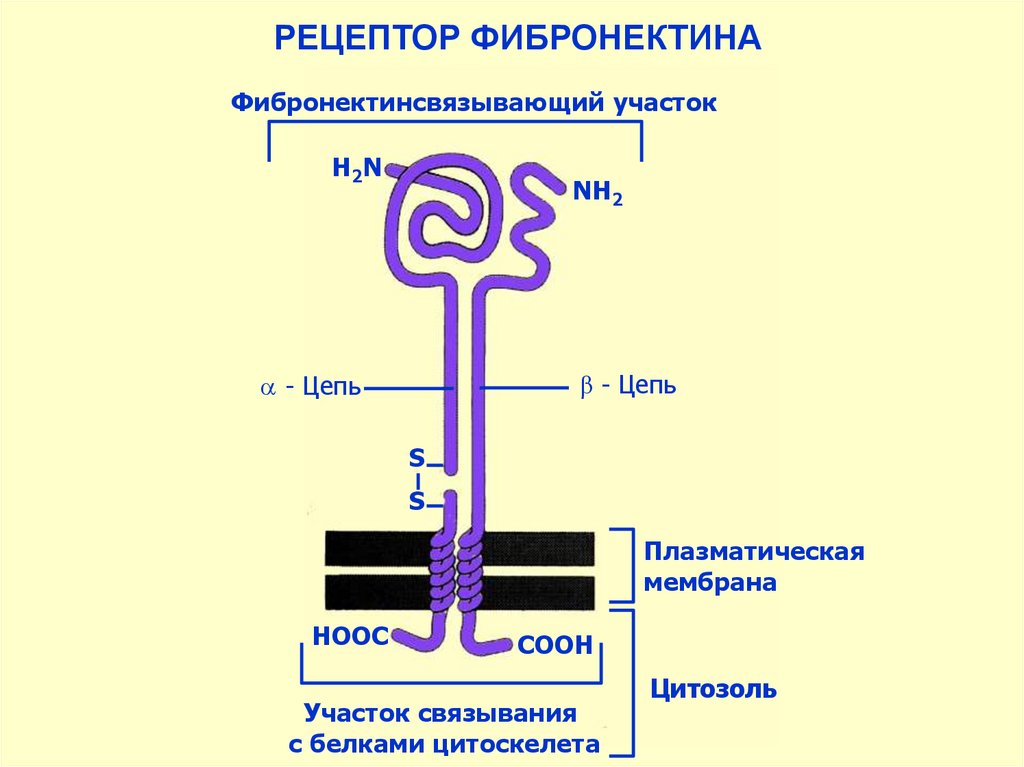
РЕЦЕПТОР ФИБРОНЕКТИНАФибронектинсвязывающий участок
Н 2N
NН2
β - Цепь
- Цепь
S
S
Плазматическая
мембрана
НООС
СООН
Участок связывания
с белками цитоскелета
Цитозоль
16.
Краткая схема перекисного окисления липидовНАДФН+Н+
Н2О2
Fe2+
О2
О2
НО2 НО
Fe3+
Н
Х
НО2
Н
ФП
Радикал ЖК
(R )
Цитохром Р450
RO
Генерация в дыхательной
цепи микросом, митохондрий
и других процессах
Н
NH2-содержащие
соединения
Fe3+
НО
ПНЖК
Гидроксильный
радикал
ROOH
O2
ПНЖК
Гидропероксид ЖК
Альдегиды и
кетоны
Основания
Шиффа
Fe2+
Пероксидный
ROO радикал
Радикал ЖК
(R )
Белки,
нуклеиновые
кислоты,
углеводы
Алкоксильный
радикал
АФК
О С
О
О С
О
О Ф
и т.д.
Радикал ЖК
(R )
17.
Факторы антиоксидантной защитыФерментативной природы:
Неферментативной природы:
- супероксиддисмутаза (СОД)
- каталаза
жирорастворимые: водорастворимые:
- токоферолы
- витамин С
- глутатионпероксидаза
- витамины А, К
- глутатион
-глутатионредуктаза
- убихинон
- цистеин
- полифенолы
- бензойная кислота
- холестерол
- мочевина
- другие
- другие
-церулоплазмин
18.
Ri + SHРадикал
инициатора
Субстрат
R iH
+
Молекулярный
продукт
S
Радикал
субстрата
Механизм действия антиоксидантов
неферментативной природы
Ri
Ri-H
S
S-H
X
Любые
радикалы
+
A-H
Антиоксидант
X-H
+
A
Стабильный радикал
антиоксиданта
Молекулярные
продукты
19.
Дисбаланс в системе «перекисное окисление липидов антиоксиданты» является важным патогенетическимзвеном следующих заболеваний:
- Атеросклероза (ИБС и др.)
- Бронхолегочных заболеваний
- Злокачественных опухолей
- Радиационных поражений
- Сахарного диабета
- Нейродегенеративных заболеваний
- Холодовой и термической травм
- Интоксикаций различного генеза
- и многих других
















 biology
biology








