Similar presentations:
Скорость химических реакций
1. Скорость химических реакций
11 класс2. Скорость химической реакции
Определяется изменениемконцентрации реагирующих или
образующихся веществ в единицу
времени
С
t
С – молярная концентрация, t - время
3. Химические реакции
гомогенныегетерогенные
4. Скорость гомогенной реакции
Определяется изменением количествавещества, вступившего в реакцию или
образовавшегося в результате реакции за
единицу времени в единице объема
С моль
v
t л с
Это реакции, в которых отсутствует поверхность
раздела между взаимодействующими веществами
5. Скорость гетерогенной реакции
Определяется изменением количествавещества, вступившего в реакцию или
образовавшегося в результате реакции за
единицу времени на единице поверхности
n моль
2
S t м с
S – площадь поверхности соприкосновения веществ
6. Факторы, влияющие на скорость химических реакций
Природа реагирующих веществПоверхность соприкосновения
Температура
Концентрация
Действие катализатора
7.
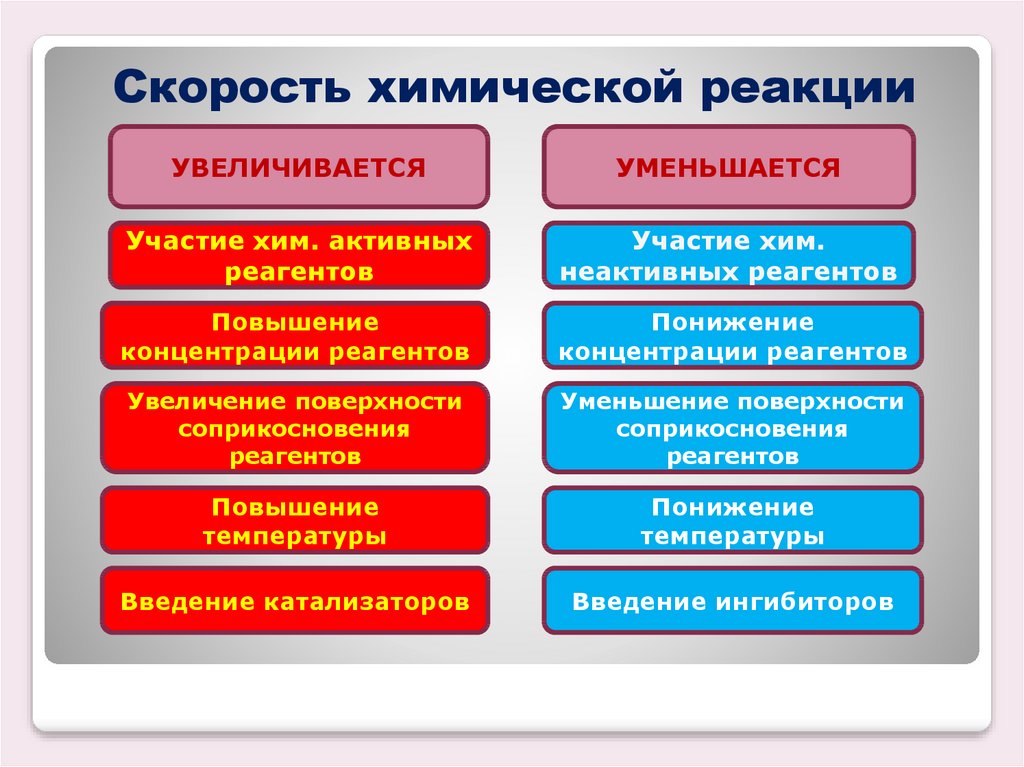
Скорость химической реакцииУВЕЛИЧИВАЕТСЯ
УМЕНЬШАЕТСЯ
Участие хим. активных
реагентов
Участие хим.
неактивных реагентов
Повышение
концентрации реагентов
Понижение
концентрации реагентов
Увеличение поверхности
соприкосновения
реагентов
Уменьшение поверхности
соприкосновения
реагентов
Повышение
температуры
Понижение
температуры
Введение катализаторов
Введение ингибиторов
8.
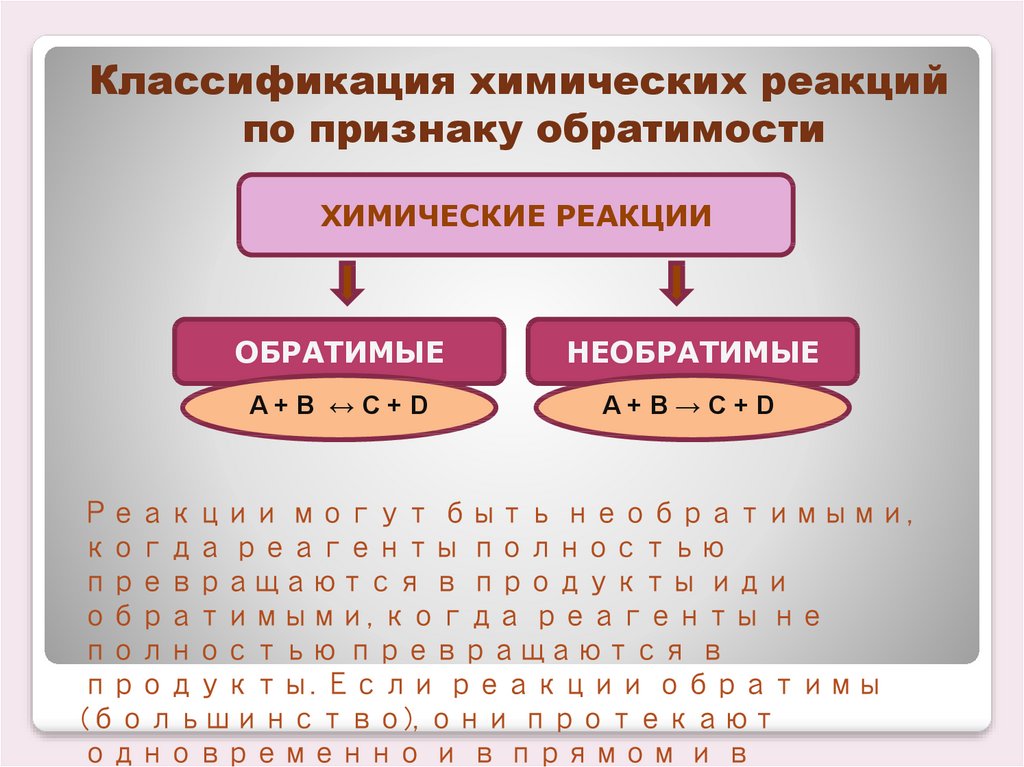
Классификация химических реакцийпо признаку обратимости
ХИМИЧЕСКИЕ РЕАКЦИИ
ОБРАТИМЫЕ
НЕОБРАТИМЫЕ
A+B ↔C+D
A+B→C+D
Реакции могут быть необратимыми,
когда реагенты полностью
превращаются в продукты иди
обратимыми, когда реагенты не
полностью превращаются в
продукты. Если реакции обратимы
(большинство), они протекают
одновременно и в прямом и в
9.
Правило Вант-Гоффа:При повышении температуры на каждые
100 C скорость большинства реакций
увеличивается в 2-4 раза.
(эту величину называют температурным
коэффициентом реакции)
2
1
t 2 t1
10
v2 ,v1 – cкорости реакций соответственно
при конечной t2 и начальной t1
температурах, а y – температурный
коэффициент реакции, показывающий во
сколько раз увеличивается скорость
реакции с повышением температуры на
каждые 10оC
10.
Лабораторный прибордля сравнения
скорости химических
реакций.
11.
Тестовое заданиеВопрос № 1
Вопрос № 3
Вопрос № 2
Вопрос № 4
12. ВЕРНО!!!
13. Попробуй еще раз…
14.
Попробуйеще раз…
15.
Попробуйеще раз…
16.
Попробуйеще раз…
17. Вопрос № 1
Какая из факторов не оказываетвлияния на скорость химической
реакции в растворах?
1) концентрация вещества
3) использование ингибитора
2) использование катализатора
4) объем реакционного сосуда
18.
Вопрос № 2Скорость химической реакции
между металлом и серой не
зависит
1) от температуры
2) от площади поверхности соприкосновения
веществ
3) от давления
4) от природы металла
19. Взаимодействие какой пары веществ будет протекать с большей скоростью, если известно, что концентрация раствора кислот во всех
Вопрос № 3Взаимодействие какой пары веществ
будет протекать с большей скоростью,
если известно, что концентрация
раствора кислот во всех случаях
одинакова
1) Pb и HCL
2) Fe и HCL
3) Zn и HCL
4) Mg и HCL
20.
Вопрос № 4Реакция, протекающая на грани
раздела двух фаз, называется
1) гетерогенной
2) окислительно-восстановительной
3) гомогенной
4) каталитической

















 chemistry
chemistry








