Similar presentations:
Изменения морфологии неопластических клеток. Лекция 6
1.
Курс «Биология опухолевой клетки»(2019 г.)
Н.Л. Лазаревич
Лекция 6
Изменения морфологии неопластических клеток,
детерминирующие «локомоторный» фенотип
2.
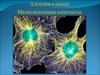
Злокачественные новообразования возникают врезультате неограниченной пролиферации клеточных
клонов, выходящих за пределы собственной ткани и
способных к росту на территориях других тканей.
Инвазивный рост,
метастазирование
Интенсивное и
неограниченное
во времени
деление клеток
Ускользание от
иммунологического
надзора
Изменения морфологии
клетки, «локомоторный»
фенотип
Модификация
микроокружения
(ангиогенез и др.)
Нестабильность генома
(мутации и эпигенетические изменения)
3.
Прогрессия эпителиальных опухолейНормальный
эпителий
Аденома
Рак in situ
Инвазивный
рак
Базальная мембрана
Макрометастаз
Выход из сосуда
(экстравазация)
микрометастазы
Проникновение в сосуд
(интравазация)
4.
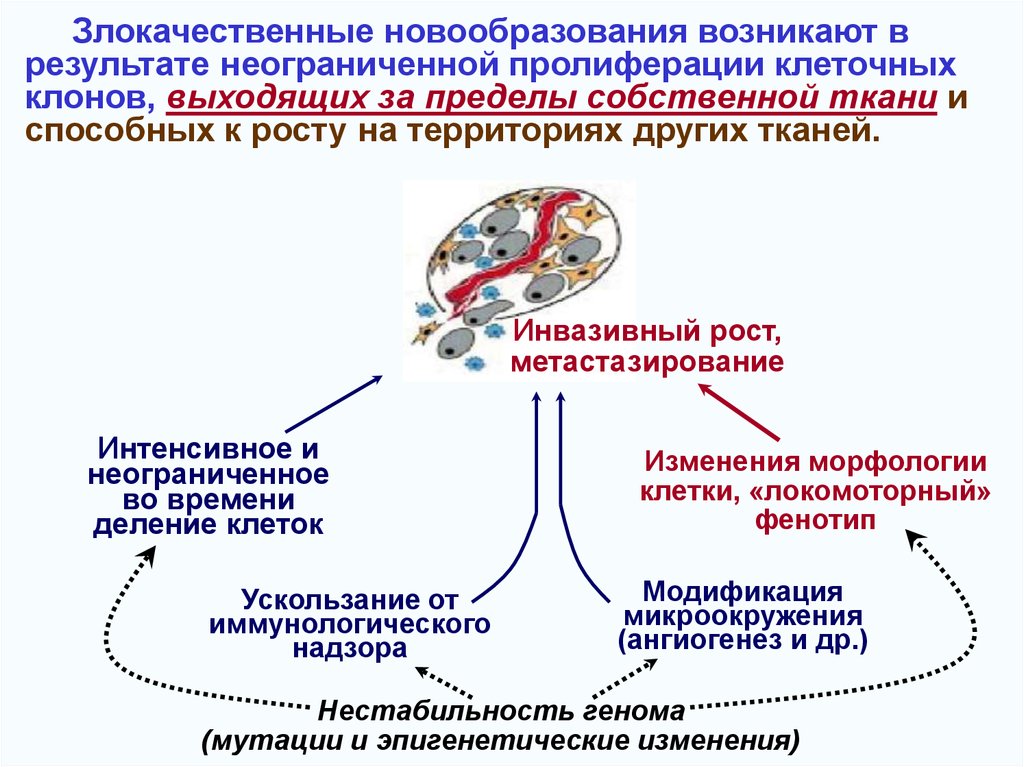
Инвазия клеток рака молочной железыНормальная ткань
молочной железы
Рак in situ
(внутрипротоковый рак)
Инвазивный рак
5.
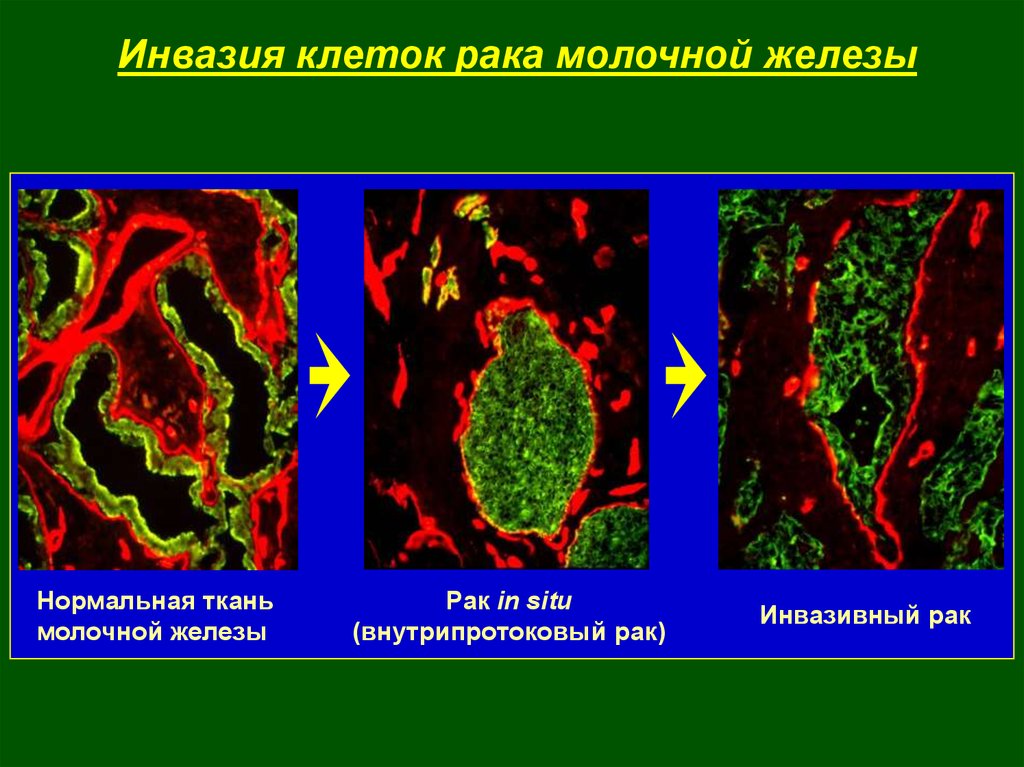
Прижизненная мультифотонная микроскопия:Внеклеточный матрикс
Кровеносный сосуд
Опухолевые клетки
Опухолевые клетки в
кровеносном сосуде
6.
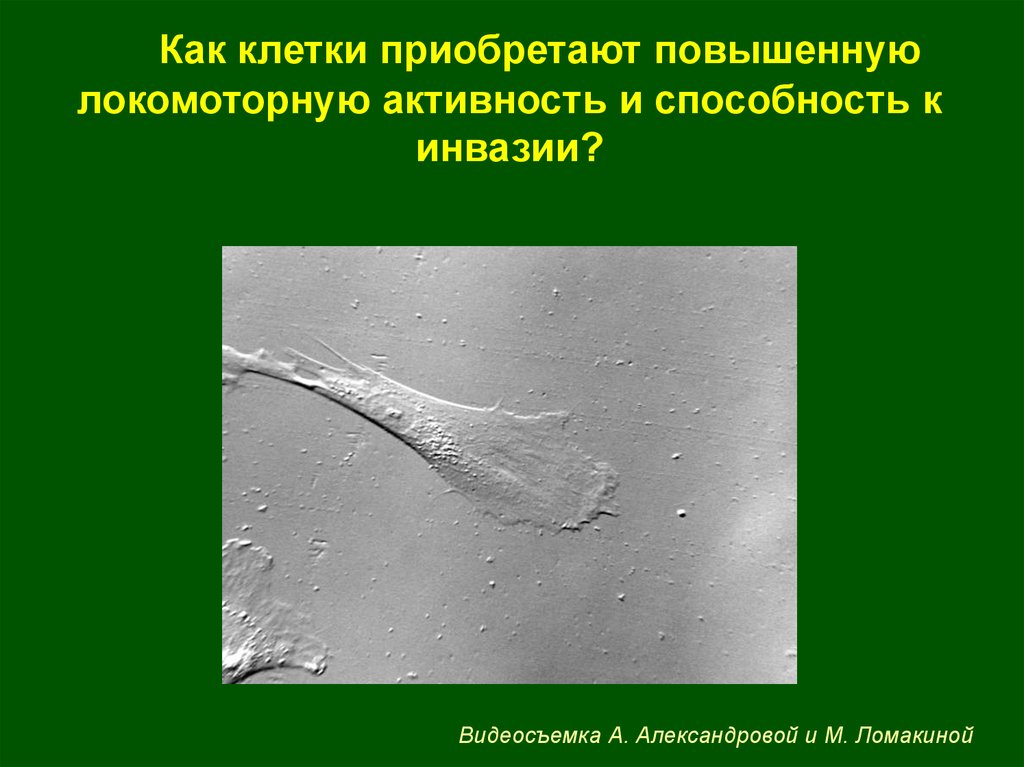
Как клетки приобретают повышеннуюлокомоторную активность и способность к
инвазии?
Видеосъемка А. Александровой и М. Ломакиной
7.
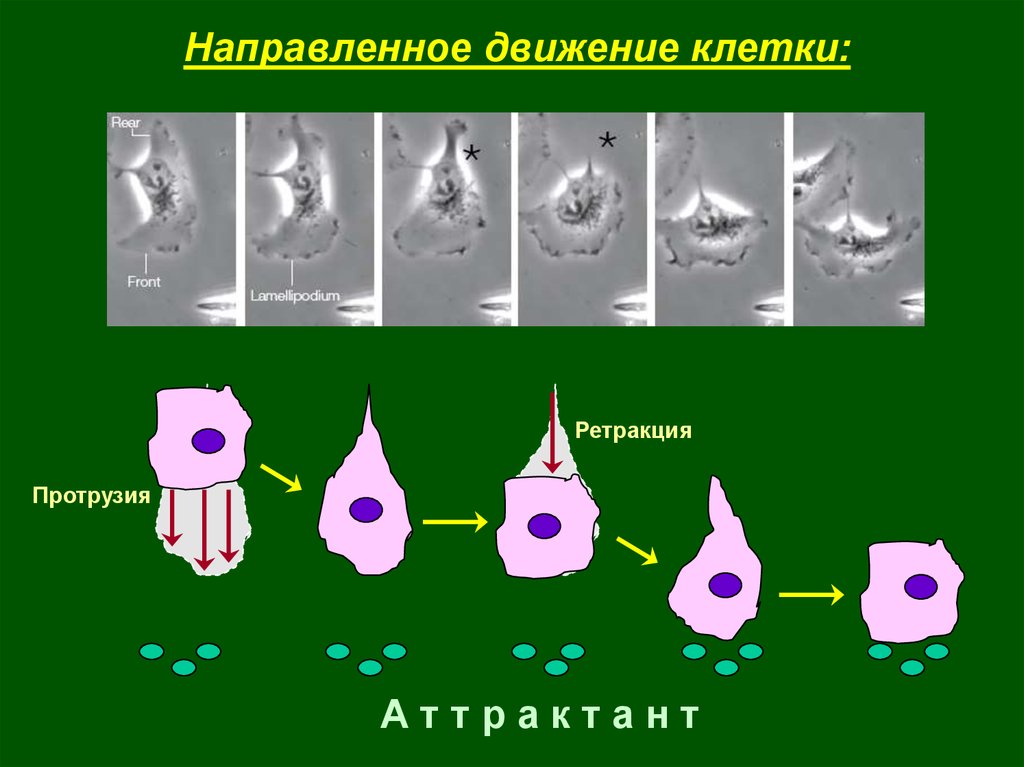
Направленное движение клетки:Ретракция
Протрузия
Аттрактант
8.
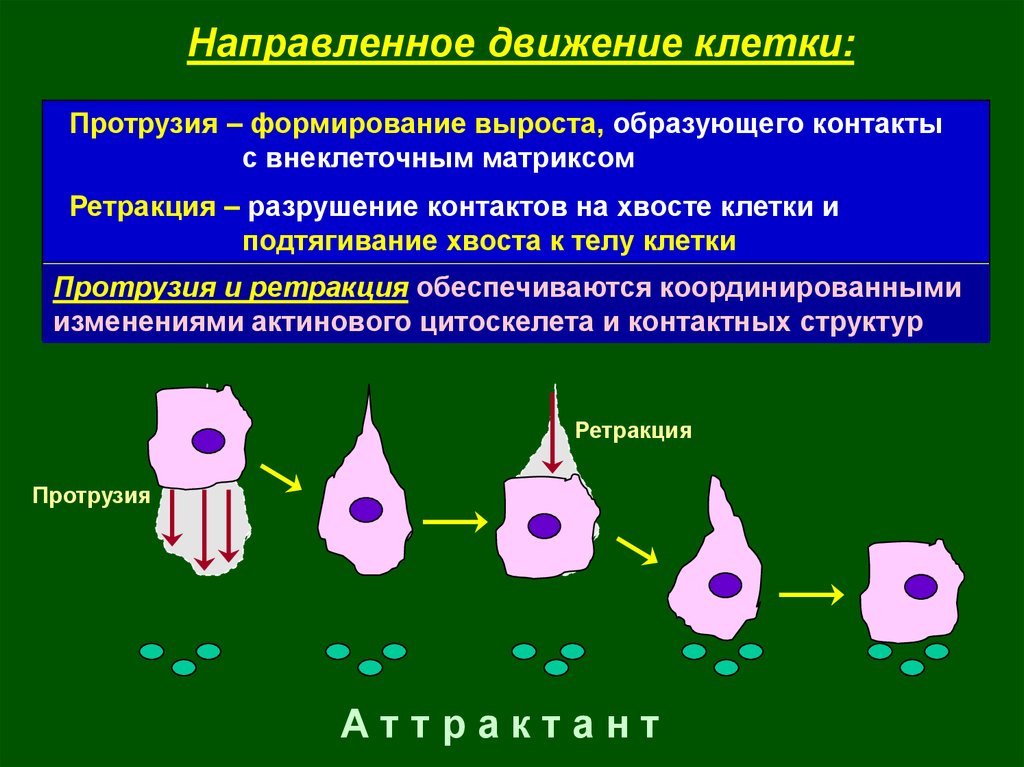
Направленное движение клетки:Протрузия – формирование выроста, образующего контакты
с внеклеточным матриксом
Ретракция – разрушение контактов на хвосте клетки и
подтягивание хвоста к телу клетки
Протрузия и ретракция обеспечиваются координированными
изменениями актинового цитоскелета и контактных структур
Ретракция
Протрузия
Аттрактант
9.
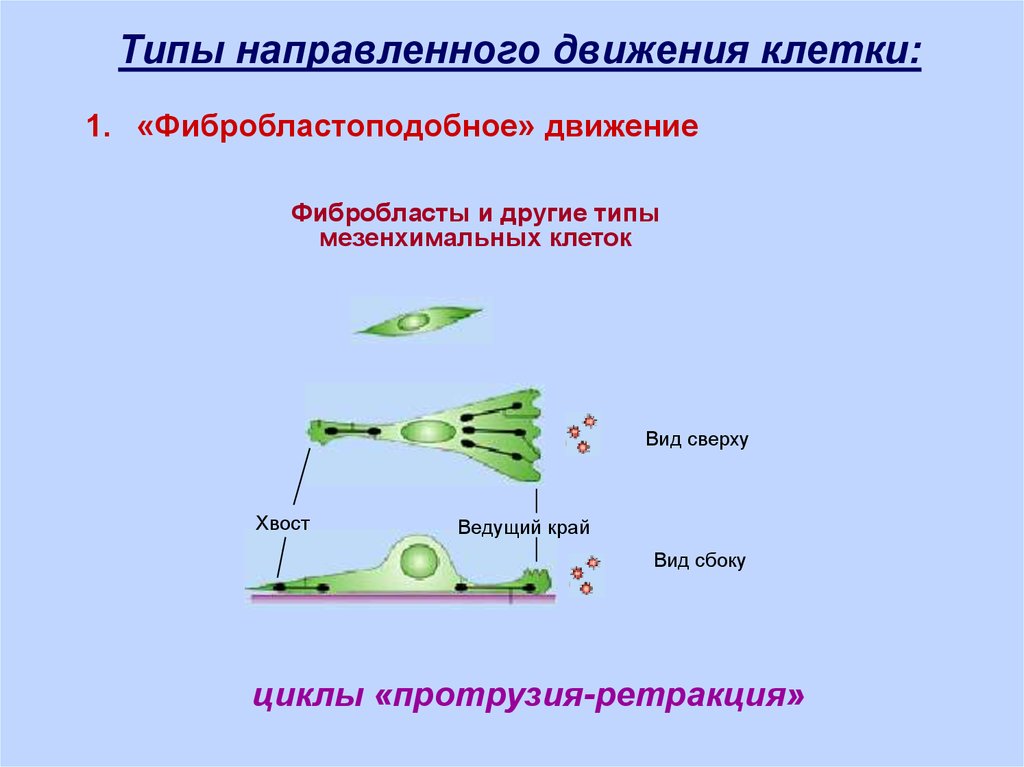
Типы направленного движения клетки:1. «Фибробластоподобное» движение
Фибробласты и другие типы
мезенхимальных клеток
Вид сверху
Хвост
Ведущий край
Вид сбоку
циклы «протрузия-ретракция»
10.
«Фибробластоподобное» движениеРецепторы
мотогенных факторов
Разрушение контактов
клеток друг с другом,
изменения контактов с
внеклеточным матриксом
Активность псевдоподий и
перестройка актинового
цитоскелета, обеспечивающая
протрузии и ретракции
Локомоция
11.
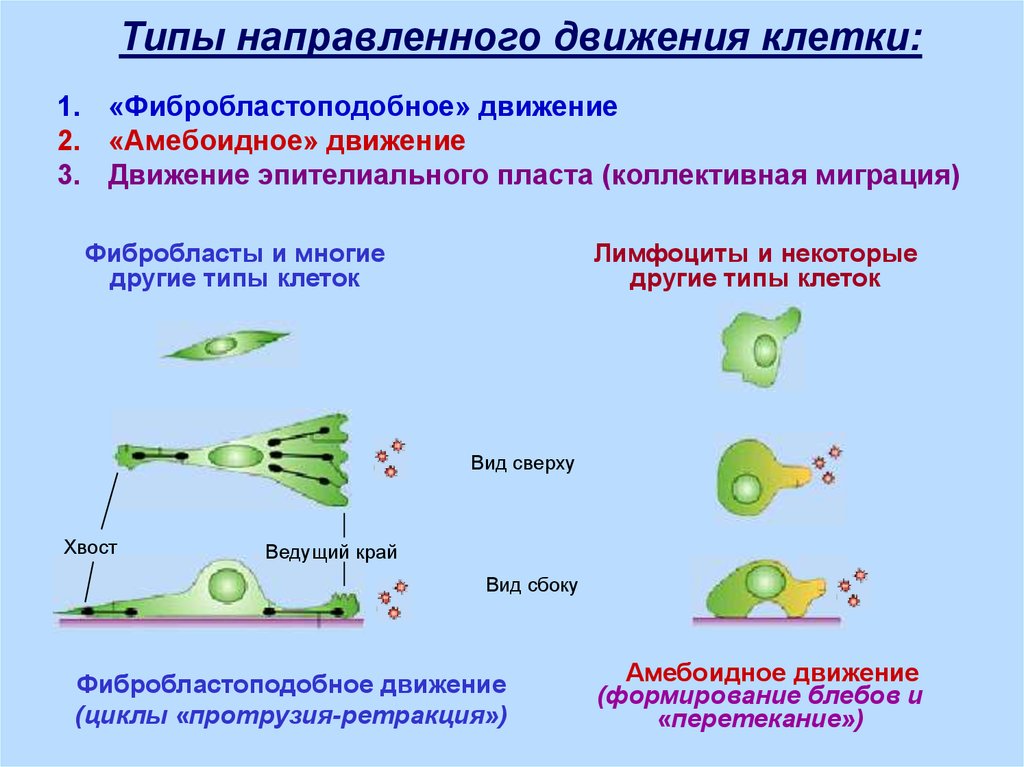
Типы направленного движения клетки:1. «Фибробластоподобное» движение
2. «Амебоидное» движение
3. Движение эпителиального пласта (коллективная миграция)
Фибробласты и многие
другие типы клеток
Лимфоциты и некоторые
другие типы клеток
Вид сверху
Хвост
Ведущий край
Вид сбоку
Фибробластоподобное движение
(циклы «протрузия-ретракция»)
Амебоидное движение
(формирование блебов и
«перетекание»)
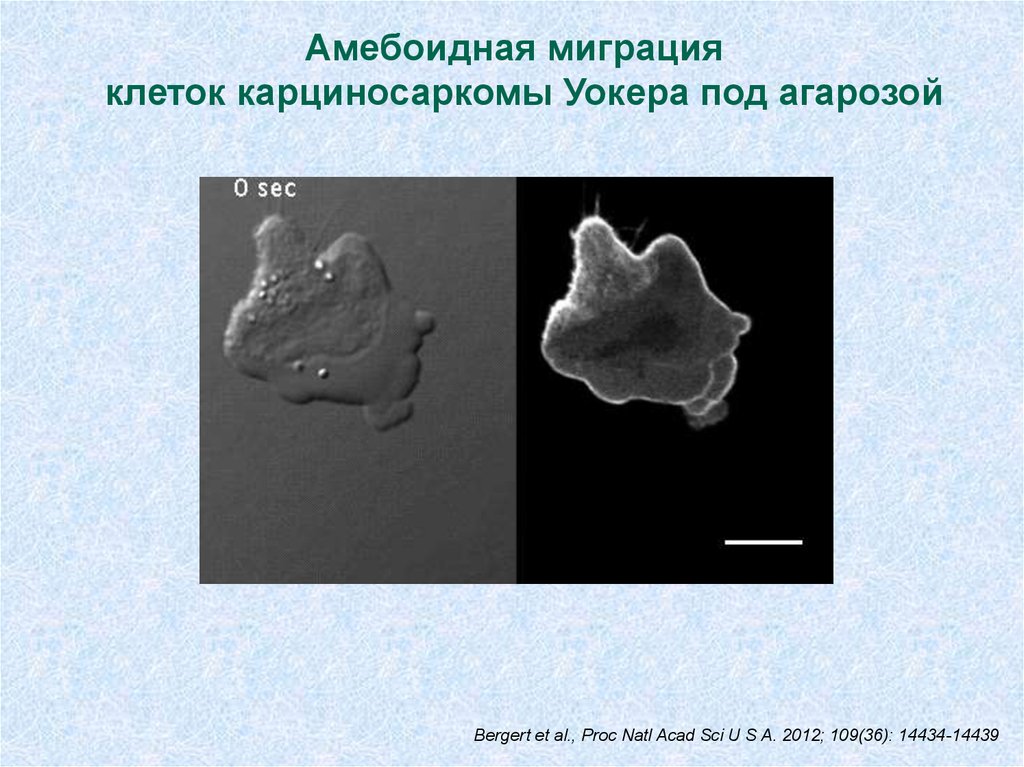
12.
Амебоидная миграцияклеток карциносаркомы Уокера под агарозой
Bergert et al., Proc Natl Acad Sci U S A. 2012; 109(36): 14434-14439.
13.
Разные типы клеток исходно обладаютразной способностью к миграции:
клетки крови, фибробласты – высокой
эпителиальные клетки - низкой
Различия в миграционной способности
разных типов клеток обусловлены разной
организацией их цитоскелета и контактных
структур
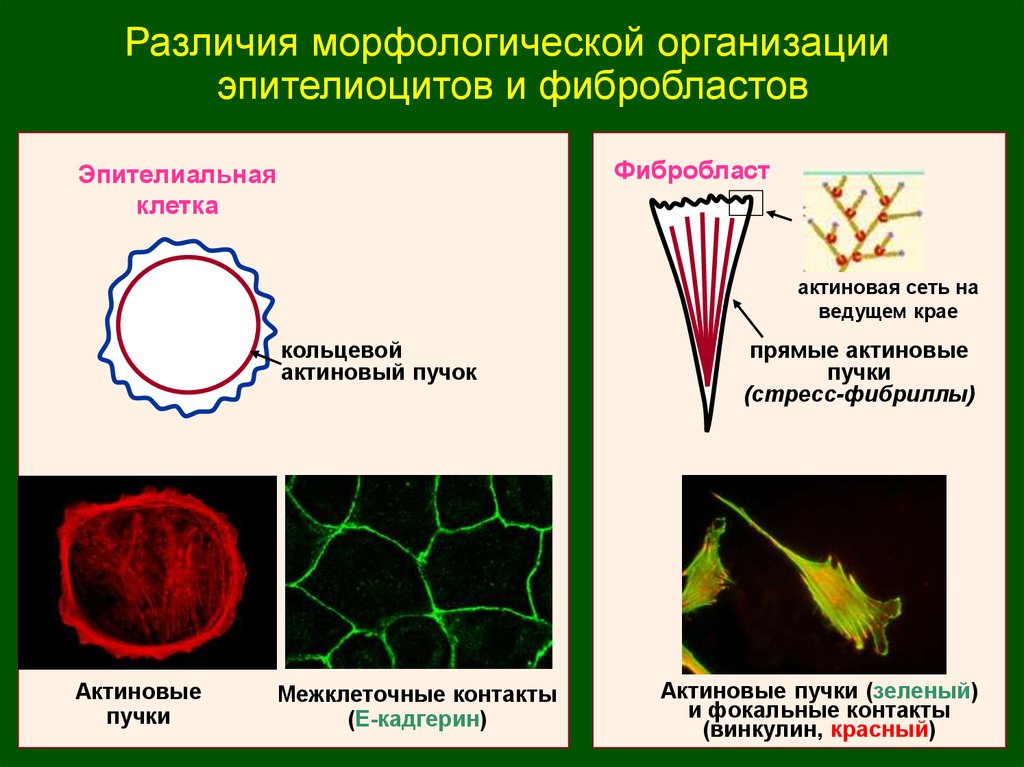
14.
Различия морфологической организацииэпителиоцитов и фибробластов
Фибробласт
Эпителиальная
клетка
актиновая сеть на
ведущем крае
кольцевой
актиновый пучок
Актиновые
пучки
Межклеточные контакты
(Е-кадгерин)
прямые актиновые
пучки
(стресс-фибриллы)
Актиновые пучки (зеленый)
и фокальные контакты
(винкулин, красный)
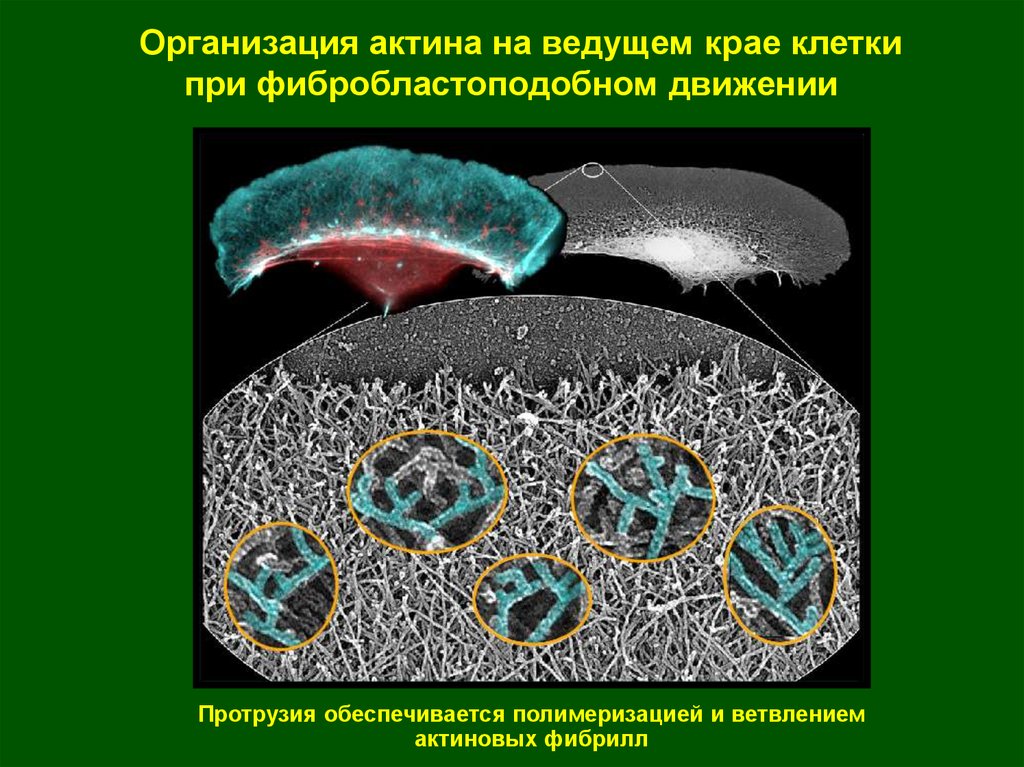
15.
Организация актина на ведущем крае клеткипри фибробластоподобном движении
Протрузия обеспечивается полимеризацией и ветвлением
актиновых фибрилл
16.
Функция Rac1 обеспечивает формирование протрузий(полимеризация актина ламеллоподии), функция Rho
ответственна за ретракции (активность стресс-фибрилл)
Rho
Rac1
Rac1
WAVE
Rho
PAK
Rho-киназа
mDia
MLC-P
Arp2/3
Филамин
Полимеризация
актина на
ведущем крае
ЛАМЕЛЛОПОДИИ
LIMK-P
кофилин-P
Полимеризация
актина
Активность
миозина
Стабилизация
полимеров актина
СТРЕСС-ФИБРИЛЛЫ
17.
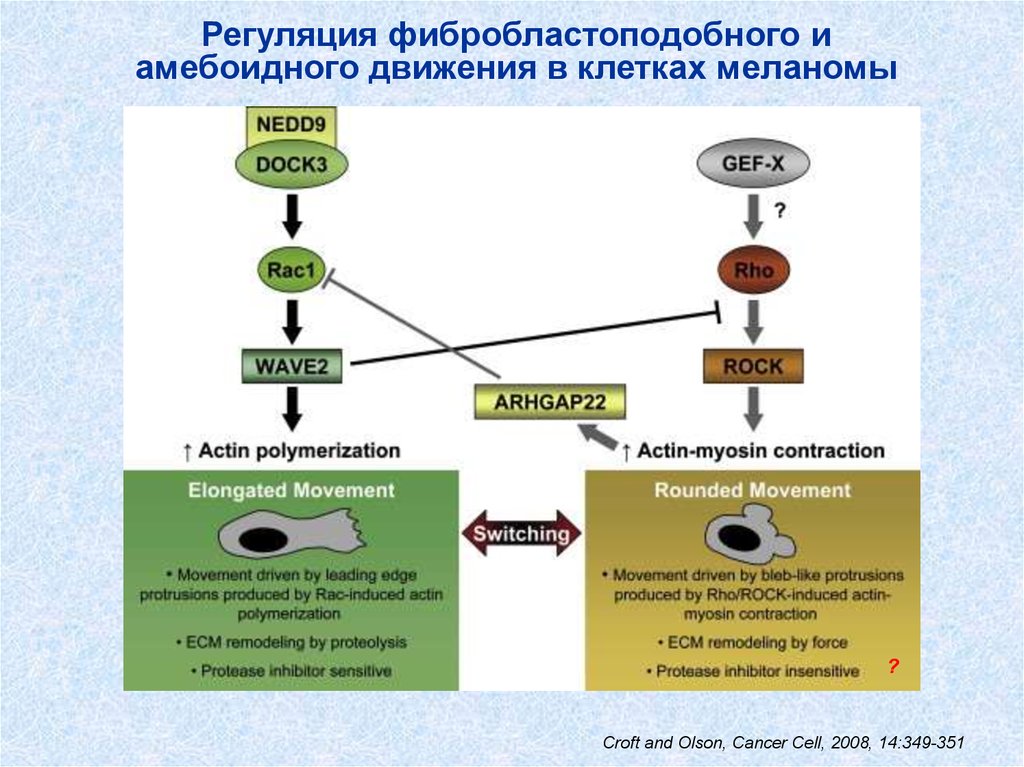
Регуляция фибробластоподобного иамебоидного движения в клетках меланомы
?
Croft and Olson, Cancer Cell, 2008, 14:349-351
18.
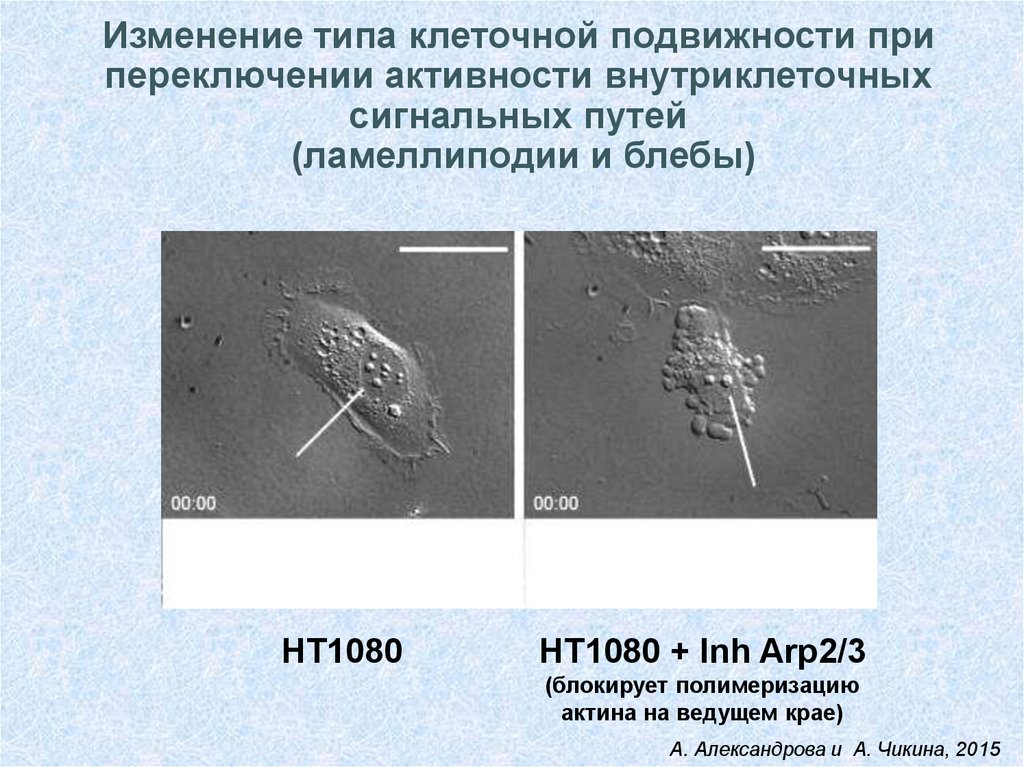
Изменение типа клеточной подвижности припереключении активности внутриклеточных
сигнальных путей
(ламеллиподии и блебы)
НТ1080
НТ1080 + Inh Arp2/3
(блокирует полимеризацию
актина на ведущем крае)
А. Александрова и А. Чикина, 2015
19.
3D cancer cell invasion. Multicellular spheroids of HT-1080 fibrosarcoma cells were embedded within3D gels of native type I collagen for 3 d. Gels were fixed in 2% glutaraldehyde/1.5% paraformaldehyde
in 0.1 M sodium cacodylate buffer, freeze-fractured, and processed for SEM. Images of infiltrating
cells and the surrounding ECM were digitally imaged using XStream imaging software.
Sabeh et al., J.Cell.Biol., 2009, 185:11-19
20.
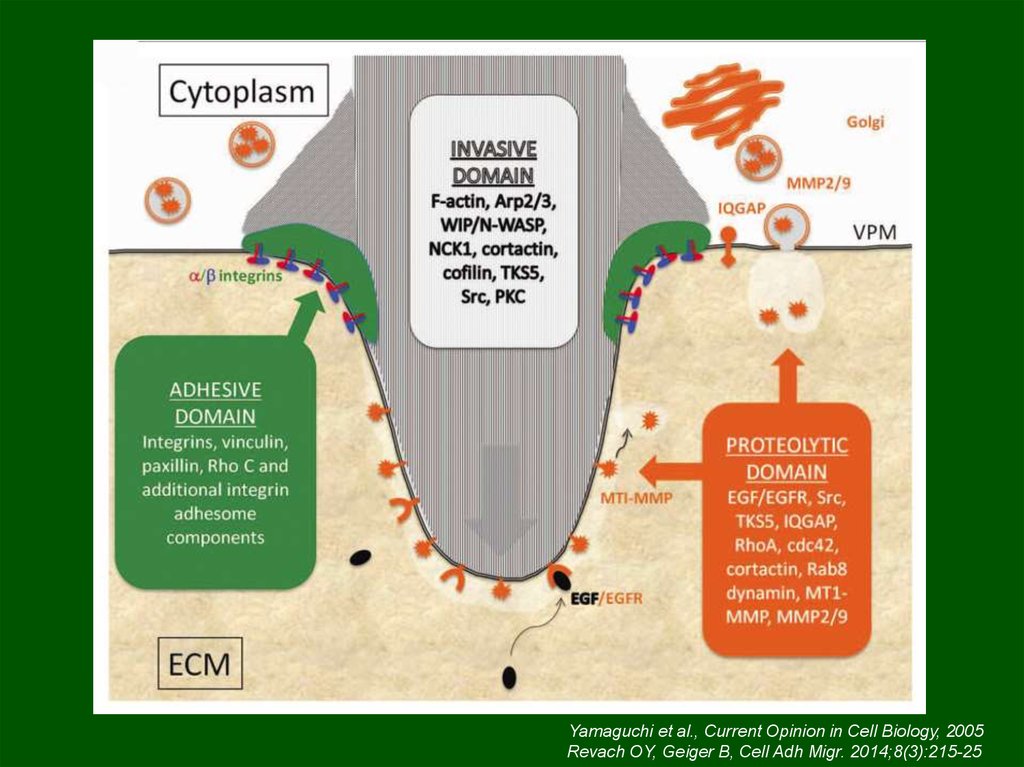
Инвадоподии (подосомы)Yamaguchi et al., Current Opinion in Cell Biology, 2005
Revach OY, Geiger B, Cell Adh Migr. 2014;8(3):215-25
21.
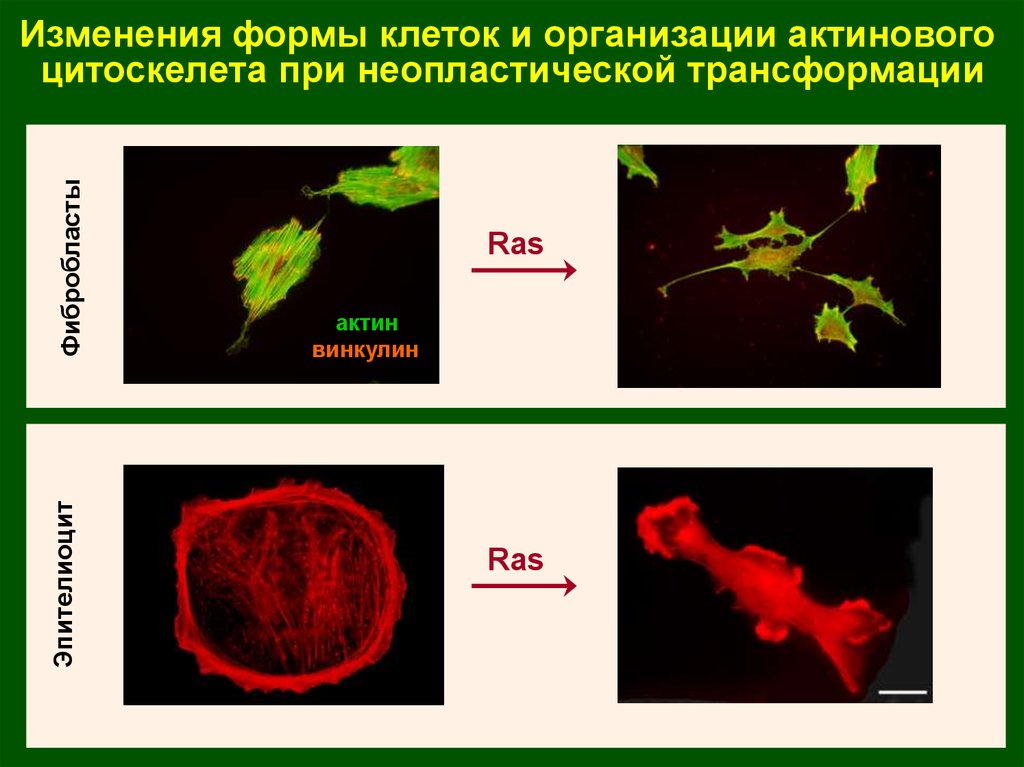
ЭпителиоцитФибробласты
Изменения формы клеток и организации актинового
цитоскелета при неопластической трансформации
Ras
актин
винкулин
Ras
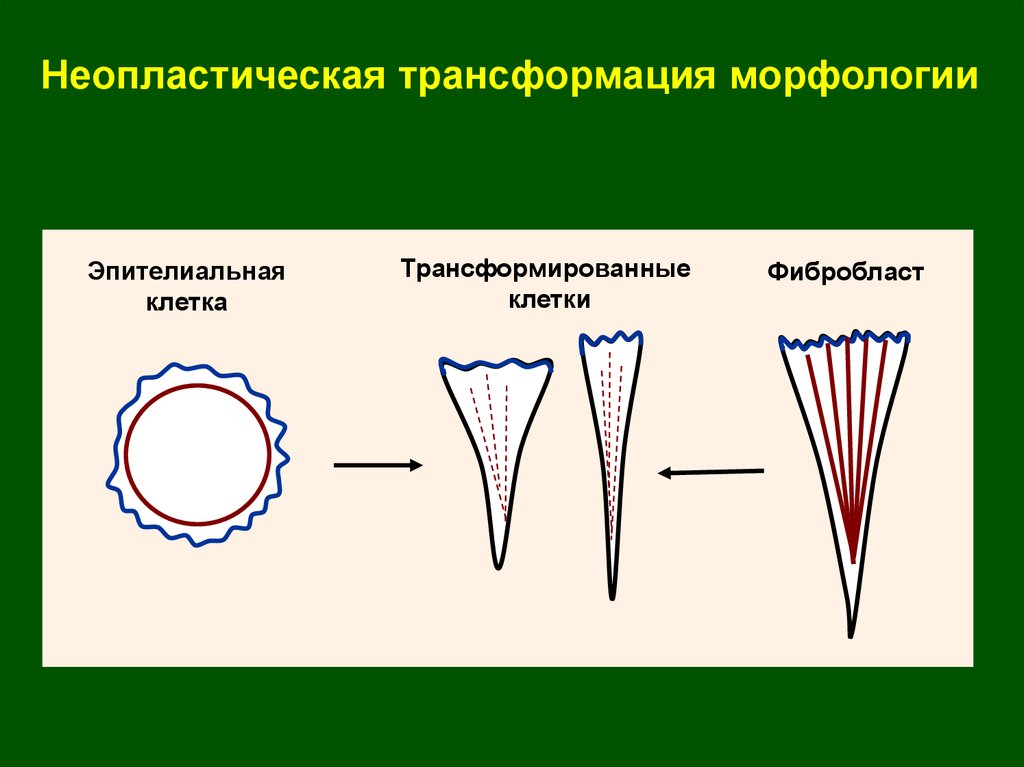
22.
Неопластическая трансформация морфологииЭпителиальная
клетка
Трансформированные
клетки
Фибробласт
23.
Ras-индуцированные изменения морфологии фибробластовсвязаны с повышением активности Rac1 и подавлением
способности Rho вызывать фосфорилирование кофилина
Ras
Клетки REF52
Rac1
N-Ras
WAVE
Rac1/GTP
Rho/GTP
Rho
Erk
LIMK
P
Arp2/3
P-cofilin
Образование
«рафлов»
кофилин
Разрушение
актиновых
фибрилл
24.
Нормальный фибробластчеловека
Фибробласт человека,
трансформированный SV40
Препараты и видеосъемка А. Александровой и М. Ломакиной
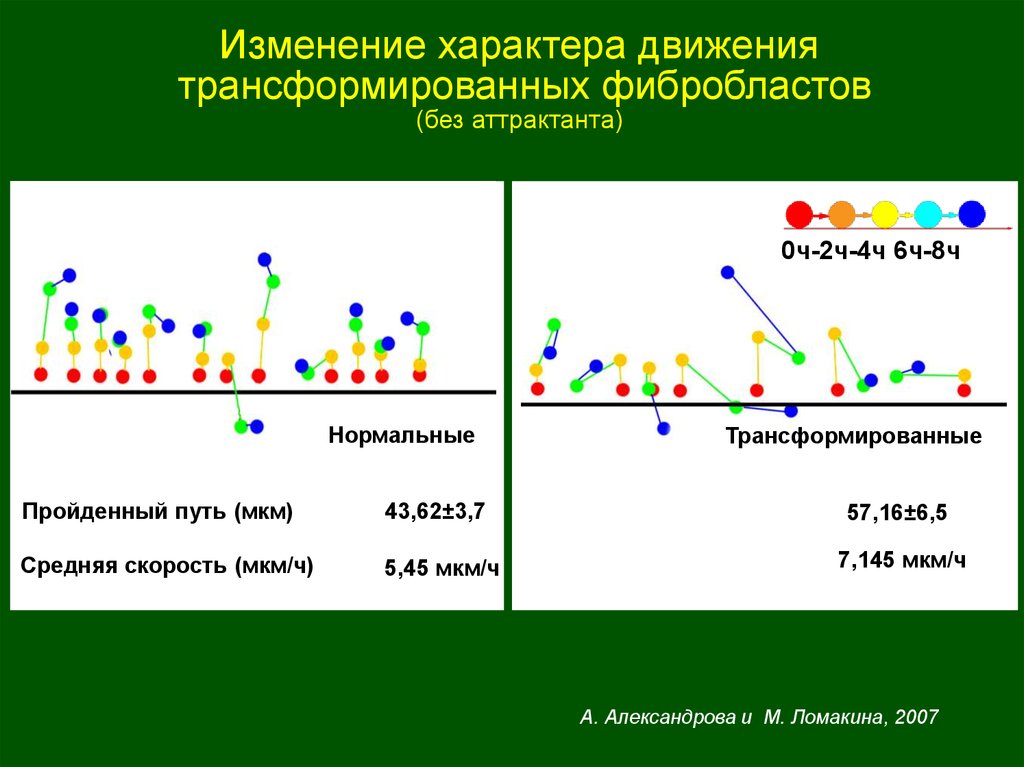
25.
Изменение характера движениятрансформированных фибробластов
(без аттрактанта)
0ч-2ч-4ч 6ч-8ч
Нормальные
Трансформированные
Пройденный путь (мкм)
43,62±3,7
57,16±6,5
Средняя скорость (мкм/ч)
5,45 мкм/ч
7,145 мкм/ч
А. Александрова и М. Ломакина, 2007
26.
Тесты на миграционную и инвазивную способность клетокin vitro: миграция через фильтры (8 μM), покрытые
матригелем, по градиенту сыворотки
Нормальные
Трансформированные
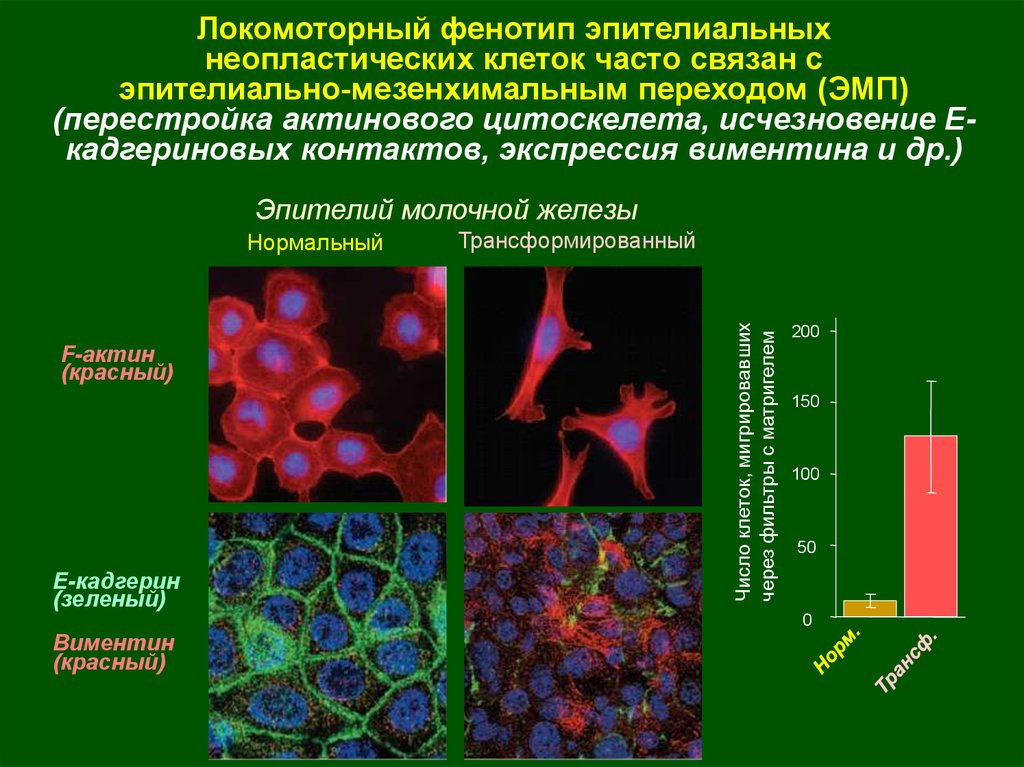
27.
Локомоторный фенотип эпителиальныхнеопластических клеток часто связан с
эпителиально-мезенхимальным переходом (ЭМП)
(перестройка актинового цитоскелета, исчезновение Екадгериновых контактов, экспрессия виментина и др.)
Эпителий молочной железы
F-актин
(красный)
Е-кадгерин
(зеленый)
Трансформированный
Число клеток, мигрировавших
через фильтры с матригелем
Нормальный
200
150
100
50
0
Виментин
(красный)
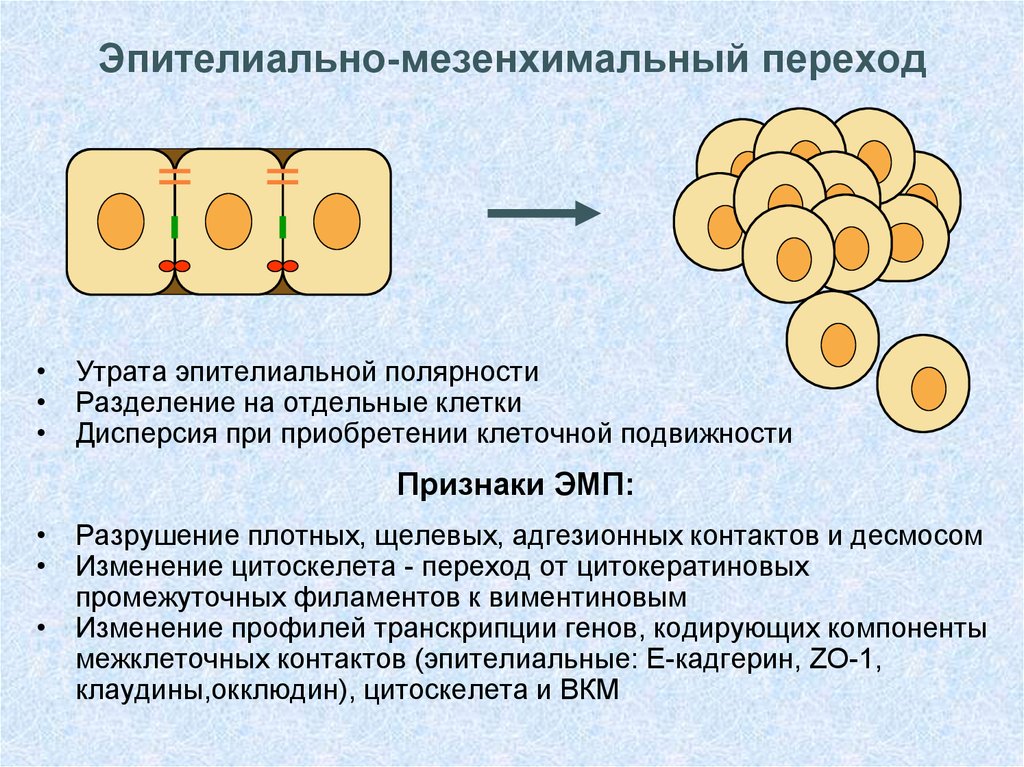
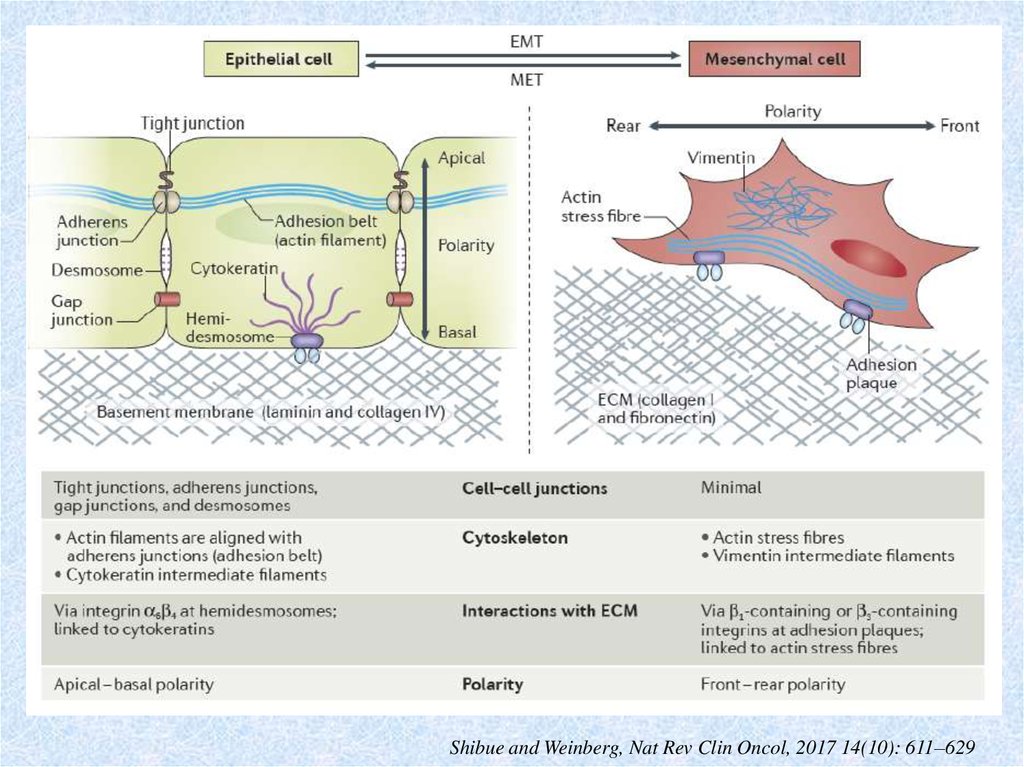
28. Эпителиально-мезенхимальный переход
• Утрата эпителиальной полярности• Разделение на отдельные клетки
• Дисперсия при приобретении клеточной подвижности
Признаки ЭМП:
• Разрушение плотных, щелевых, адгезионных контактов и десмосом
• Изменение цитоскелета - переход от цитокератиновых
промежуточных филаментов к виментиновым
• Изменение профилей транскрипции генов, кодирующих компоненты
межклеточных контактов (эпителиальные: Е-кадгерин, ZO-1,
клаудины,окклюдин), цитоскелета и ВКМ
29.
Shibue and Weinberg, Nat Rev Clin Oncol, 2017 14(10): 611–62930.
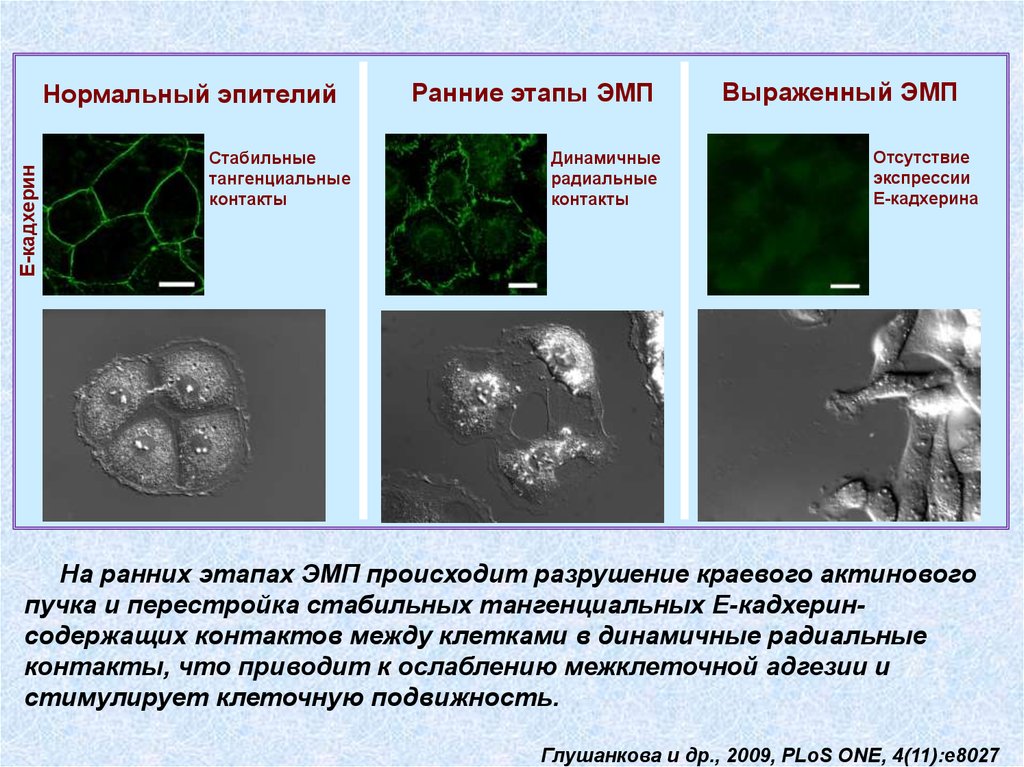
Е-кадхеринНормальный эпителий
Стабильные
тангенциальные
контакты
Ранние этапы ЭМП
Динамичные
радиальные
контакты
Выраженный ЭМП
Отсутствие
экспрессии
Е-кадхерина
На ранних этапах ЭМП происходит разрушение краевого актинового
пучка и перестройка стабильных тангенциальных Е-кадхеринсодержащих контактов между клетками в динамичные радиальные
контакты, что приводит к ослаблению межклеточной адгезии и
стимулирует клеточную подвижность.
Глушанкова и др., 2009, PLoS ONE, 4(11):e8027
31.
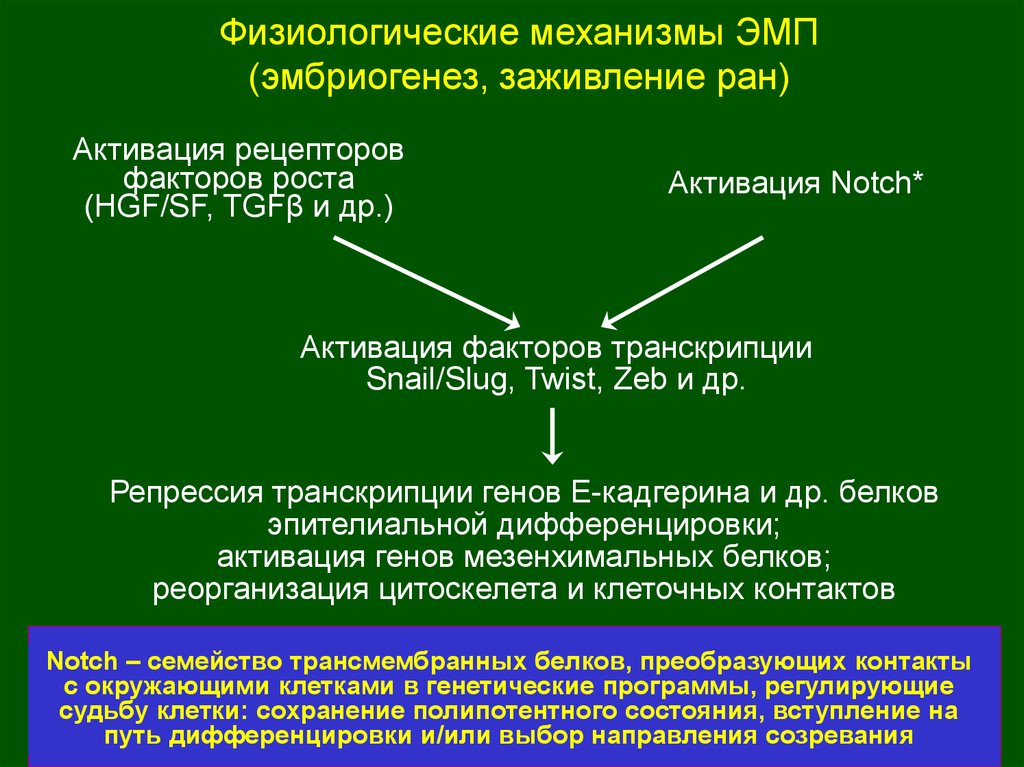
Физиологические механизмы ЭМП(эмбриогенез, заживление ран)
Активация рецепторов
факторов роста
(HGF/SF, TGFβ и др.)
Активация Notch*
Активация факторов транскрипции
Snail/Slug, Twist, Zeb и др.
Репрессия транскрипции генов Е-кадгерина и др. белков
эпителиальной дифференцировки;
активация генов мезенхимальных белков;
реорганизация цитоскелета и клеточных контактов
Notch – семейство трансмембранных белков, преобразующих контакты
с окружающими клетками в генетические программы, регулирующие
судьбу клетки: сохранение полипотентного состояния, вступление на
путь дифференцировки и/или выбор направления созревания
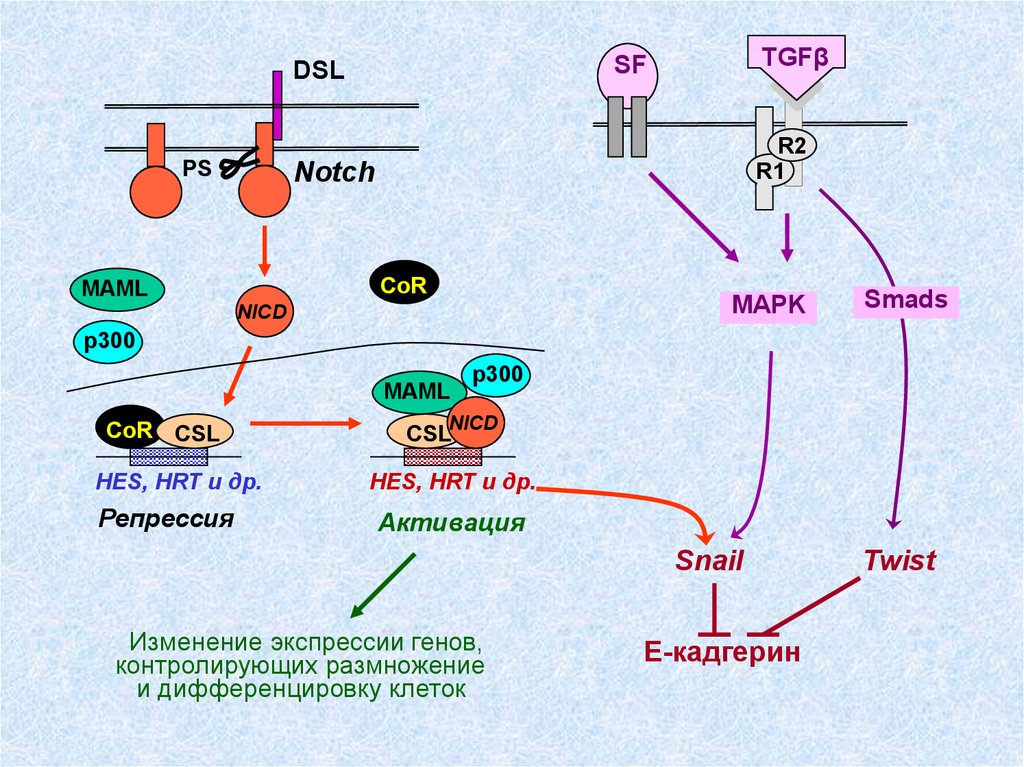
32.
PSTGFβ
SF
DSL
R2
R1
Notch
CoR
MAML
MAPK
NICD
Smads
p300
MAML
CoR CSL
HES, HRT и др.
Репрессия
p300
NICD
CSL
HES, HRT и др.
Активация
Snail
Изменение экспрессии генов,
контролирующих размножение
и дифференцировку клеток
Е-кадгерин
Twist
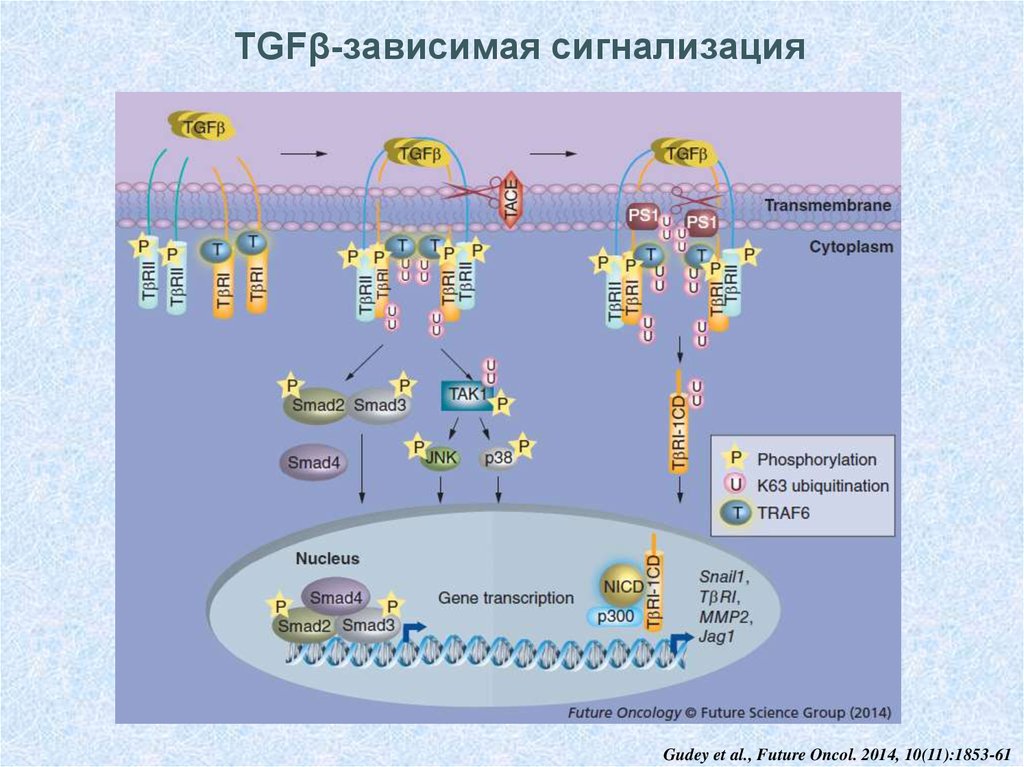
33. TGFβ-зависимая сигнализация
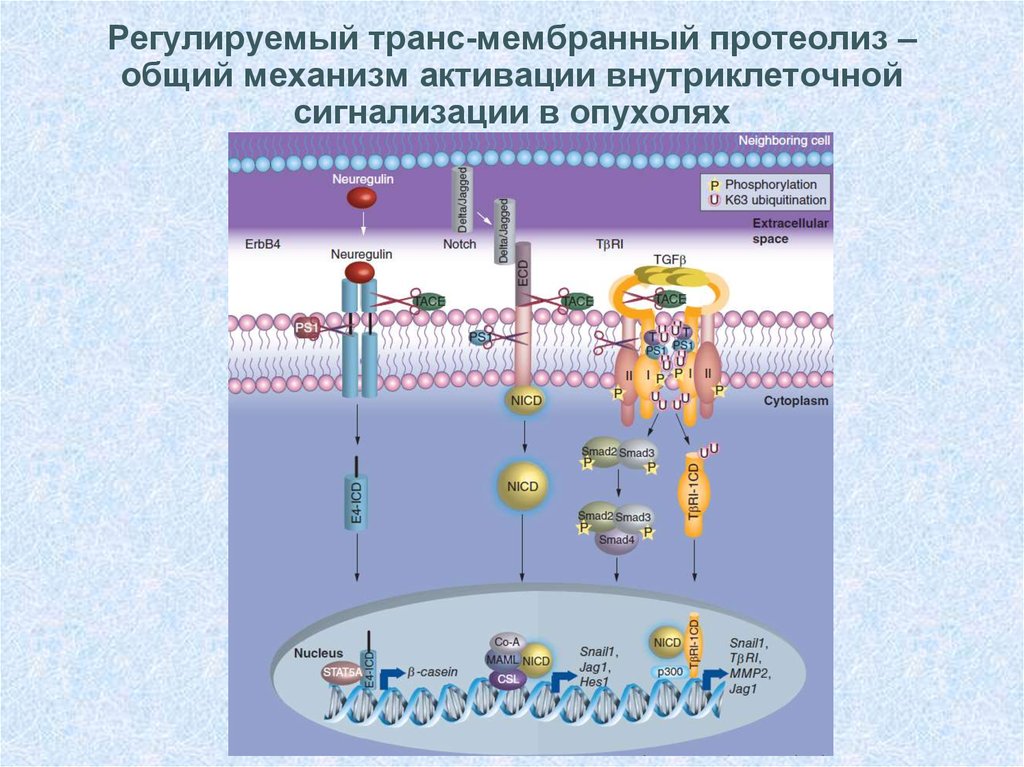
Gudey et al., Future Oncol. 2014, 10(11):1853-6134. Регулируемый транс-мембранный протеолиз – общий механизм активации внутриклеточной сигнализации в опухолях
35.
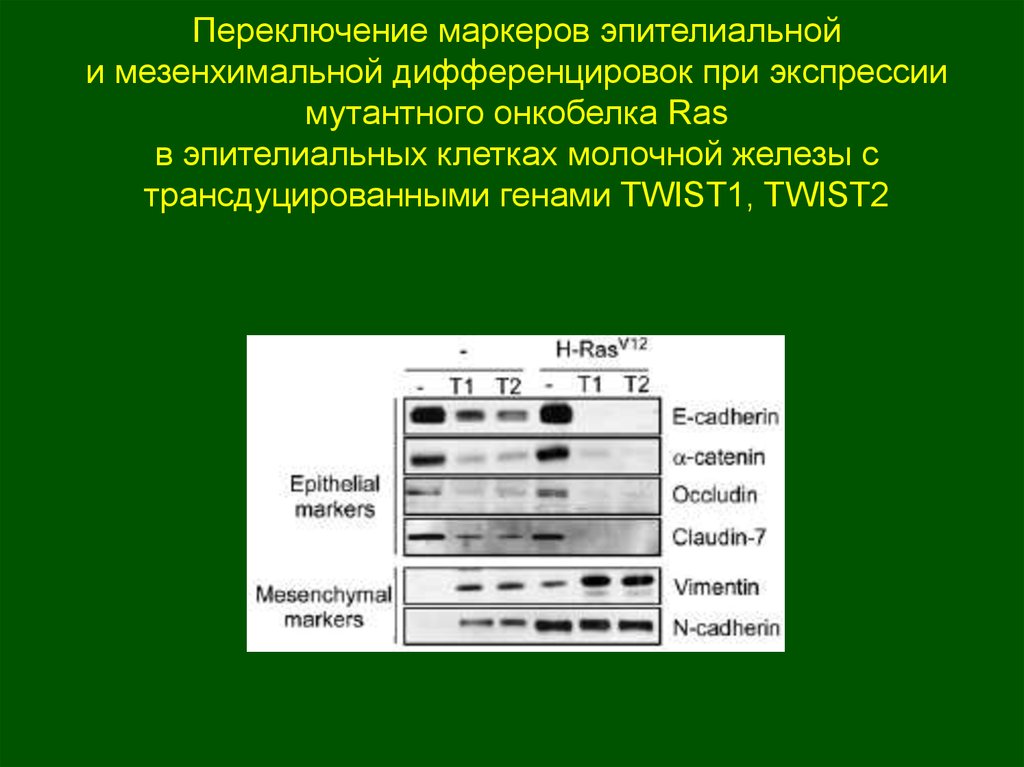
Переключение маркеров эпителиальнойи мезенхимальной дифференцировок при экспрессии
мутантного онкобелка Ras
в эпителиальных клетках молочной железы с
трансдуцированными генами TWIST1, TWIST2
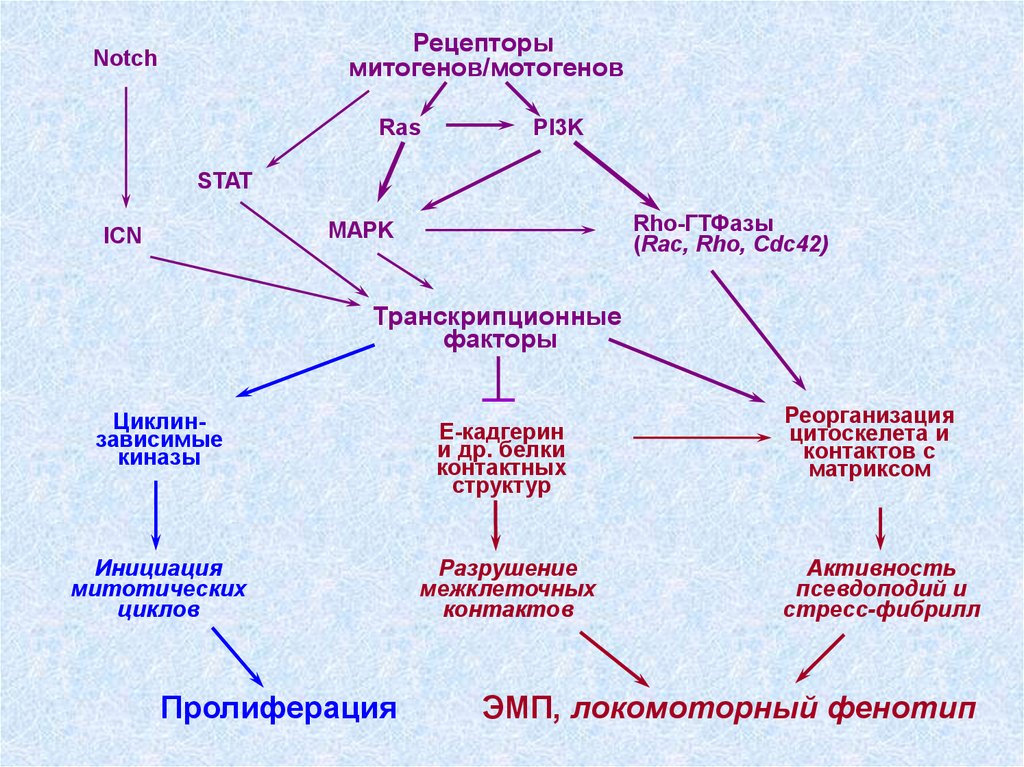
36.
Рецепторымитогенов/мотогенов
Notch
Ras
PI3K
STAT
Rho-ГТФазы
(Rac, Rho, Cdc42)
MAPK
ICN
Транскрипционные
факторы
Циклинзависимые
киназы
Е-кадгерин
и др. белки
контактных
структур
Инициация
митотических
циклов
Разрушение
межклеточных
контактов
Пролиферация
Реорганизация
цитоскелета и
контактов с
матриксом
Активность
псевдоподий и
стресс-фибрилл
ЭМП, локомоторный фенотип
37.
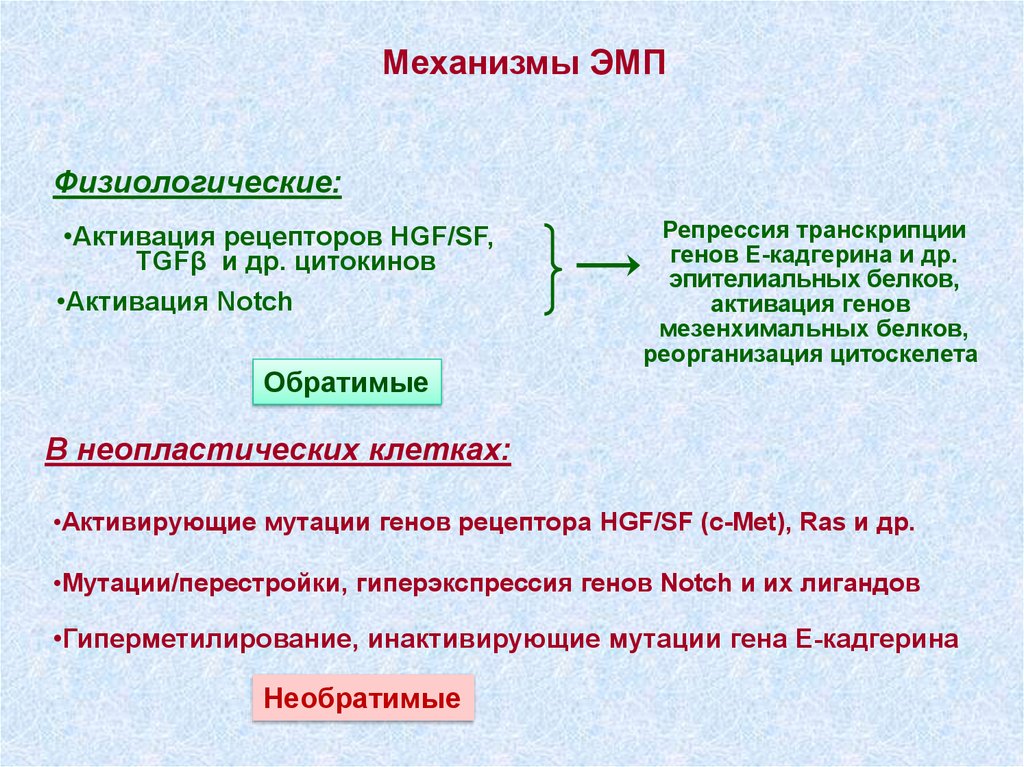
Механизмы ЭМПФизиологические:
•Активация рецепторов HGF/SF,
TGFβ и др. цитокинов
•Активация Notch
Обратимые
Репрессия транскрипции
генов Е-кадгерина и др.
эпителиальных белков,
активация генов
мезенхимальных белков,
реорганизация цитоскелета
В неопластических клетках:
•Активирующие мутации генов рецептора HGF/SF (c-Met), Ras и др.
•Мутации/перестройки, гиперэкспрессия генов Notch и их лигандов
•Гиперметилирование, инактивирующие мутации гена Е-кадгерина
Необратимые
38.
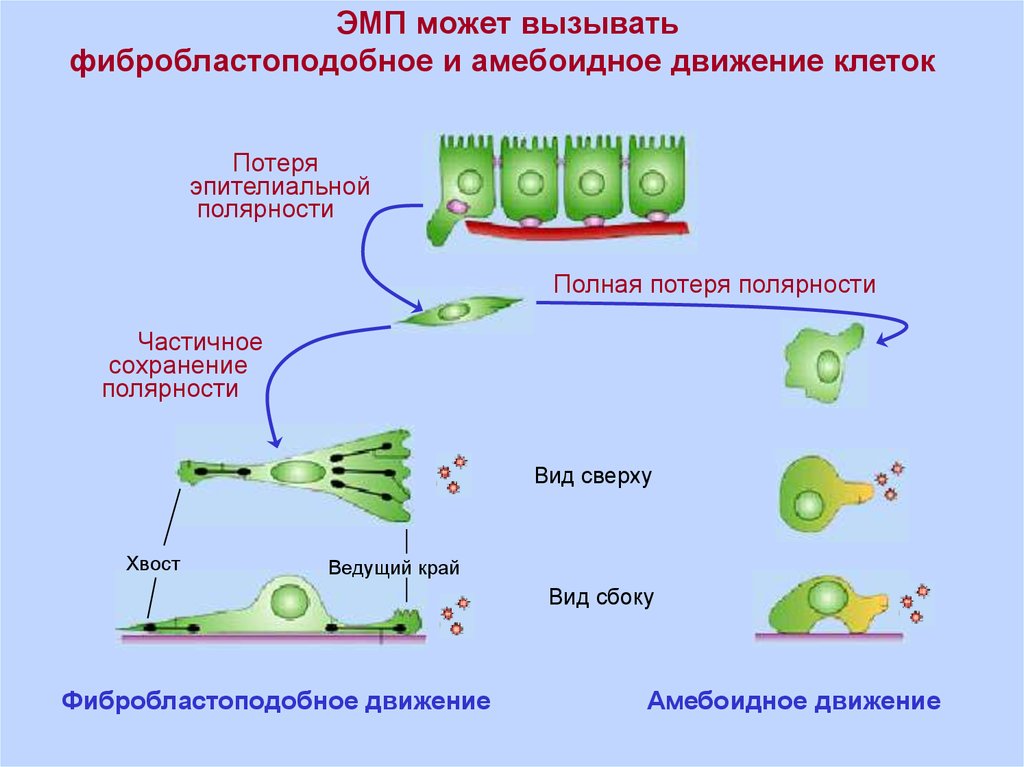
ЭМП может вызыватьфибробластоподобное и амебоидное движение клеток
Потеря
эпителиальной
полярности
Полная потеря полярности
Частичное
сохранение
полярности
Вид сверху
Хвост
Ведущий край
Вид сбоку
Фибробластоподобное движение
Амебоидное движение
39.
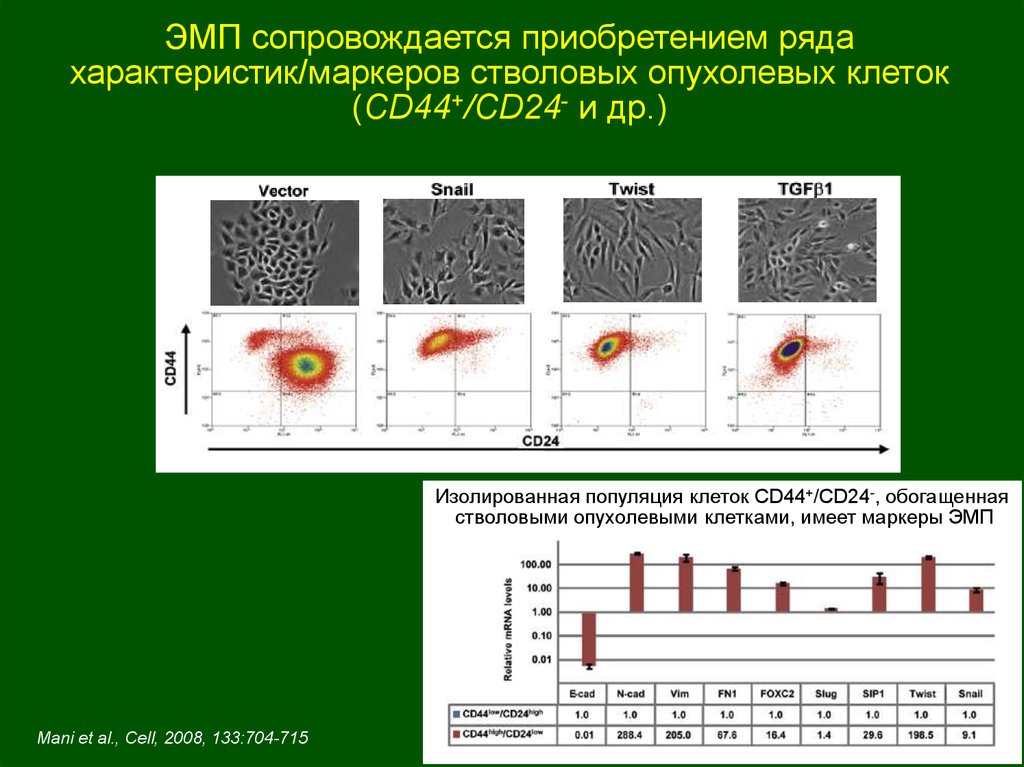
ЭМП сопровождается приобретением рядахарактеристик/маркеров стволовых опухолевых клеток
(CD44+/CD24- и др.)
Изолированная популяция клеток CD44+/CD24-, обогащенная
стволовыми опухолевыми клетками, имеет маркеры ЭМП
Mani et al., Cell, 2008, 133:704-715
40.
Рецепторымитогенов/мотогенов
ГТФ-азы сем. Rho
(Rac, Rho, Cdc42)
Транскрипционные
факторы
Протеазы
Разрушение
внеклеточного
матрикса
Подопланин
(плоскоклеточные раки,
рак молочной железы)
Е-кадгерин
и др. белки
контактных
структур
Разрушение
межклеточных
контактов
Миграция
Реорганизация
цитоскелета и
контактов с
матриксом
Активность
псевдоподий и
стрессфибрилл
41.
Экспрессия подопланина вызывает перестройкуцитоскелета и приобретение локомоторного
фенотипа, не связанные с классическим ЭМП
(коллективная миграция)
Эпителиальные клетки молочной железы
MCF7
MCF7/Podo
Актин (зеленый), подопланин (красный)
Подопланин (красный) и
Е-кадгерин (коричневый)
ко-экспрессируются на
инвазивном фронте рака
молочной железы
Wicki et al., Cancer Cell, 2006, 9:261-272
42.
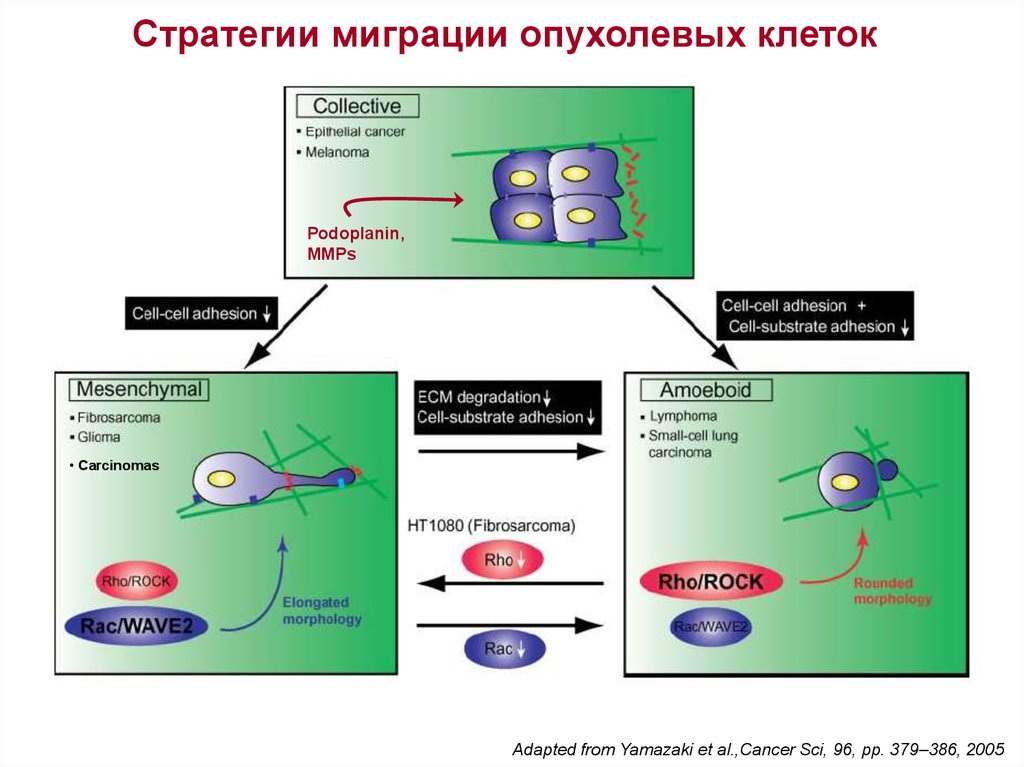
Стратегии миграции опухолевых клетокPodoplanin,
MMPs
• Carcinomas
Adapted from Yamazaki et al.,Cancer Sci, 96, pp. 379–386, 2005
43.
ЭМП и МЭП при прогрессии опухолейShibue and Weinberg, Nat Rev Clin Oncol, 2017 14(10): 611–629
44.
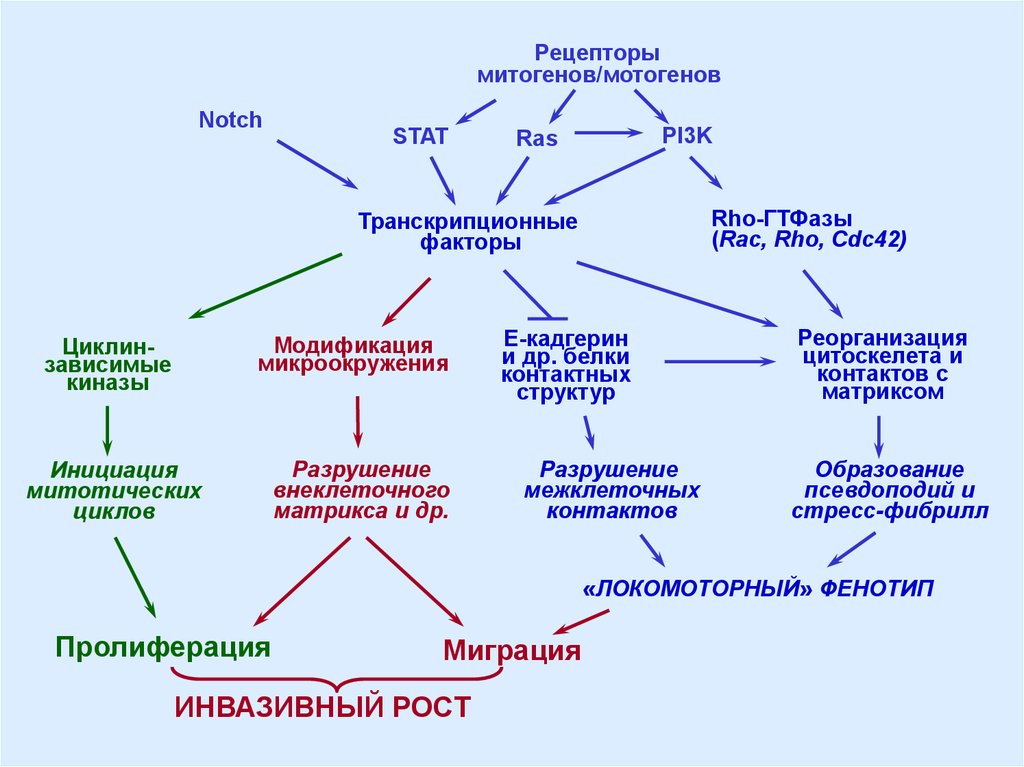
Рецепторымитогенов/мотогенов
Notch
STAT
PI3K
Ras
Транскрипционные
факторы
Модификация
микроокружения
Циклинзависимые
киназы
Инициация
митотических
циклов
Разрушение
внеклеточного
матрикса и др.
Rho-ГТФазы
(Rac, Rho, Cdc42)
Е-кадгерин
и др. белки
контактных
структур
Разрушение
межклеточных
контактов
Реорганизация
цитоскелета и
контактов с
матриксом
Образование
псевдоподий и
стресс-фибрилл
«ЛОКОМОТОРНЫЙ» ФЕНОТИП
Пролиферация
Миграция
ИНВАЗИВНЫЙ РОСТ
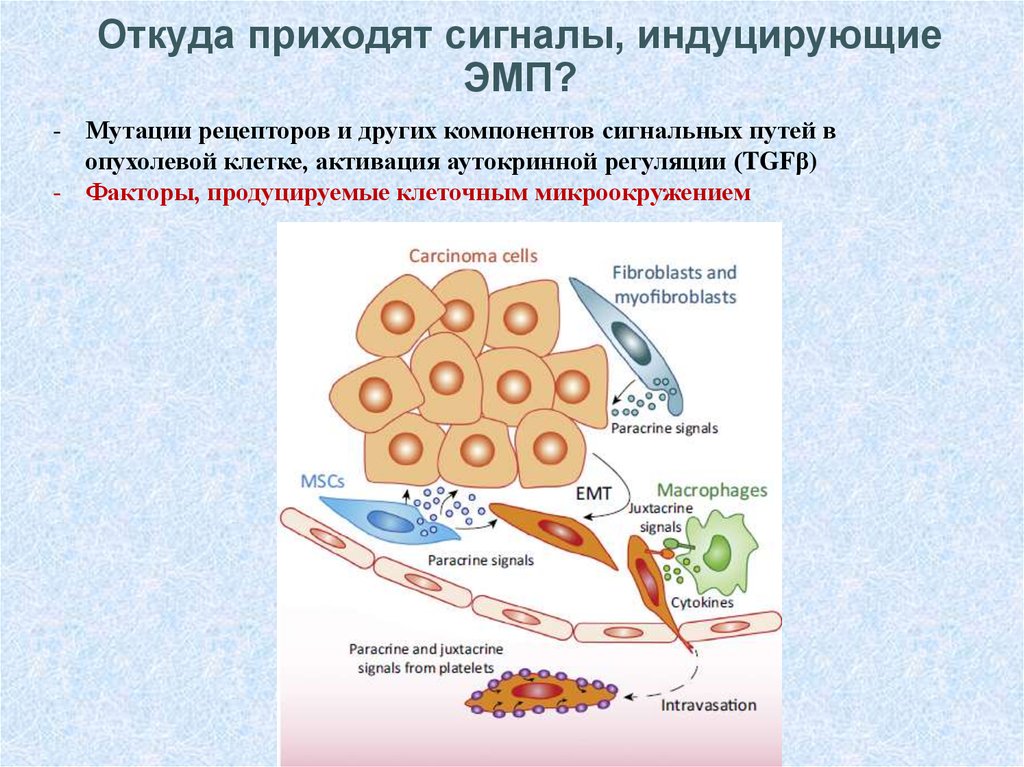
45. Откуда приходят сигналы, индуцирующие ЭМП?
- Мутации рецепторов и других компонентов сигнальных путей вопухолевой клетке, активация аутокринной регуляции (TGFβ)
- Факторы, продуцируемые клеточным микроокружением
46.
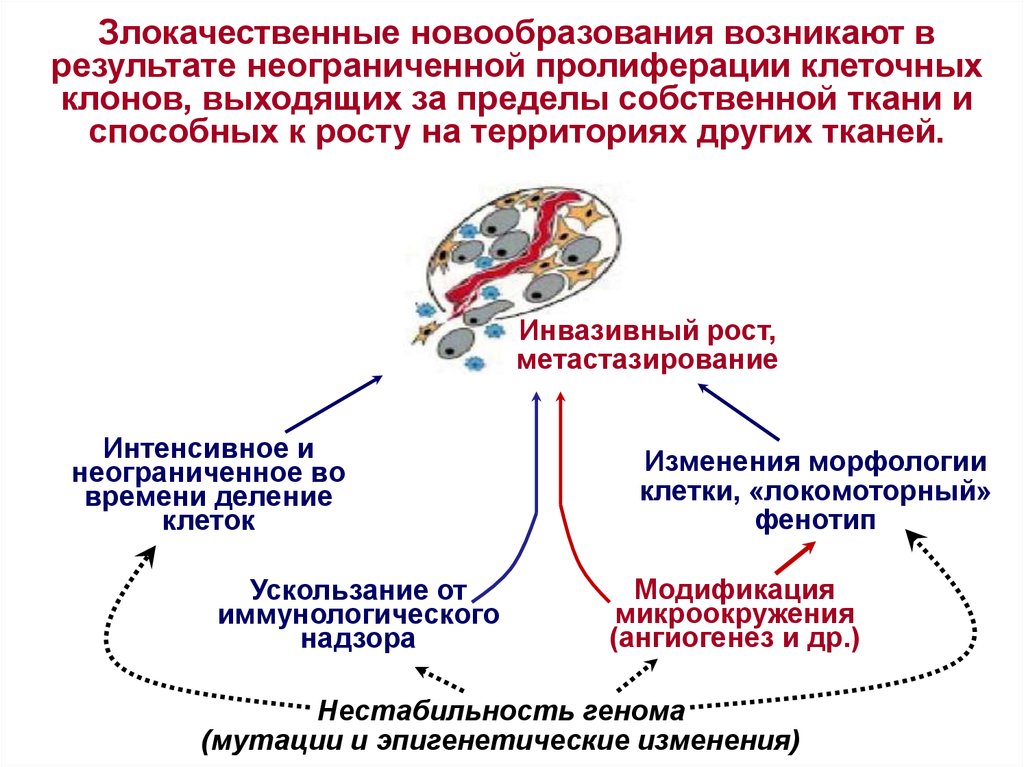
Злокачественные новообразования возникают врезультате неограниченной пролиферации клеточных
клонов, выходящих за пределы собственной ткани и
способных к росту на территориях других тканей.
Инвазивный рост,
метастазирование
Интенсивное и
неограниченное во
времени деление
клеток
Ускользание от
иммунологического
надзора
Изменения морфологии
клетки, «локомоторный»
фенотип
Модификация
микроокружения
(ангиогенез и др.)
Нестабильность генома
(мутации и эпигенетические изменения)
47.
Курс «Биология опухолевой клетки»(2019 г.)
Н.Л. Лазаревич
Лекция 7
Способность неопластических клеток
модифицировать микроокружение













 biology
biology