Similar presentations:
Антикоагулянты. Гемостаз
1. АО «МЕДИЦИНСКИЙ УНИВЕРСИТЕТ АСТАНА»
АНТИКОАГУЛЯНТЫВыполнила: Жубанова Б.М.
Проверил:
Смагулов Ж.Б.
2.
Гемостаз – процессы, направленные насохранение крови в сосудистом русле,
предотвращение кровоточивости и
восстановление кровотока в случае
окклюзии сосуда тромбом.
3. Стадии гемостатического процесса
Нарушение целостности сосудистой стенкиЛокальная вазоконстрикция
Адгезия и активация тромбоцитов
Формирование тромбоцитарного тромба
Стабилизация тромба фибрином
Растворение тромба после регенерации
поврежденной сосудистой стенки
4. Тромбообразование
Серый тромб(действующие лица)
Тромбоциты
Моноциты
Фактор фон
Виллебранда
Фибрин
Красный тромб
(действующие лица)
Фибрин –
образование
фибринового
матрикса
Эритроциты
5.
Адгезией называется процесс прилипания тромбоцитов ксубэндотелиальным структурам, являющийся первичной реакцией
на возникновение дефекта эндотелия.
Активация тромбоцитов – процесс, характеризующийся
изменением формы тромбоцитов, секрецией содержимого гранул
(выделение АДФ, серотонина, 4-го фактора тромбоцитов,
тромбоцитарного фактора роста), синтезом тромбоксана А2
(TxA2), активацией гликопротедных (GP) рецепторов.
Агрегация тромбоцитов – процесс стабилизации
тромбоцитарного тромба тромбином, фибриновыми нитями,
изменение формы тромбоцитов от дисковидной к сферической с
псевдоподиями, слипание тромбоцитов друг с другом.
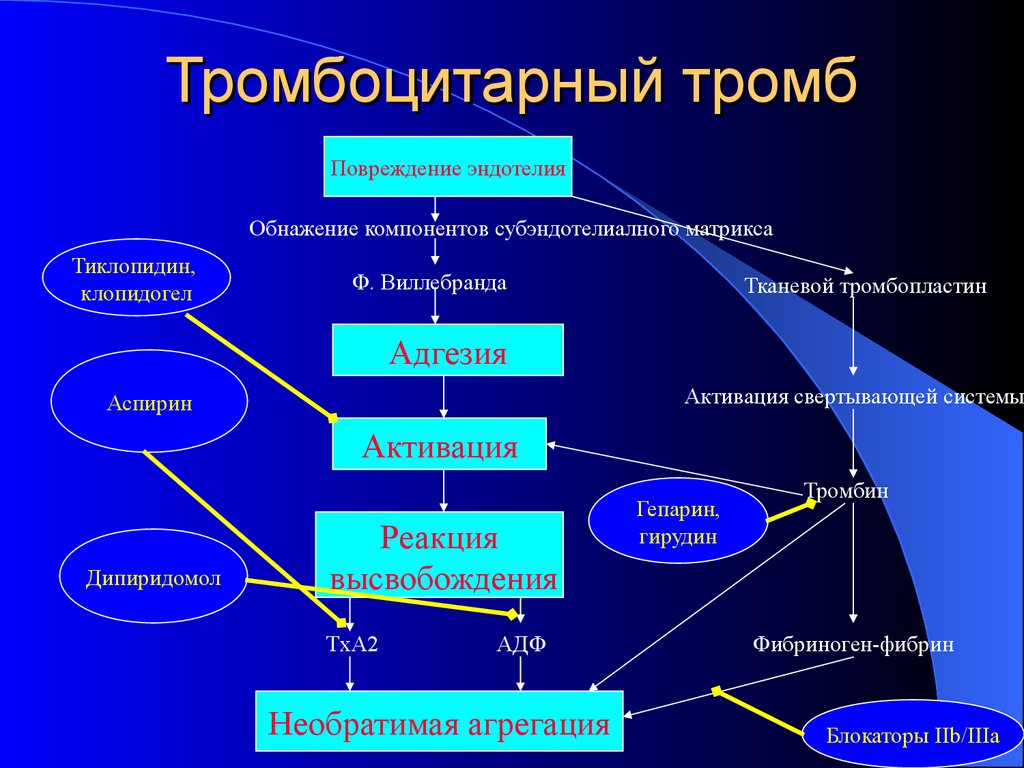
6. Тромбоцитарный тромб
Повреждение эндотелияОбнажение компонентов субэндотелиалного матрикса
Тиклопидин,
клопидогел
Ф. Виллебранда
Тканевой тромбопластин
Адгезия
Активация свертывающей системы
Аспирин
Активация
Дипиридомол
Реакция
высвобождения
TxA2
АДФ
Необратимая агрегация
Гепарин,
гирудин
Тромбин
Фибриноген-фибрин
Блокаторы IIb/IIIa
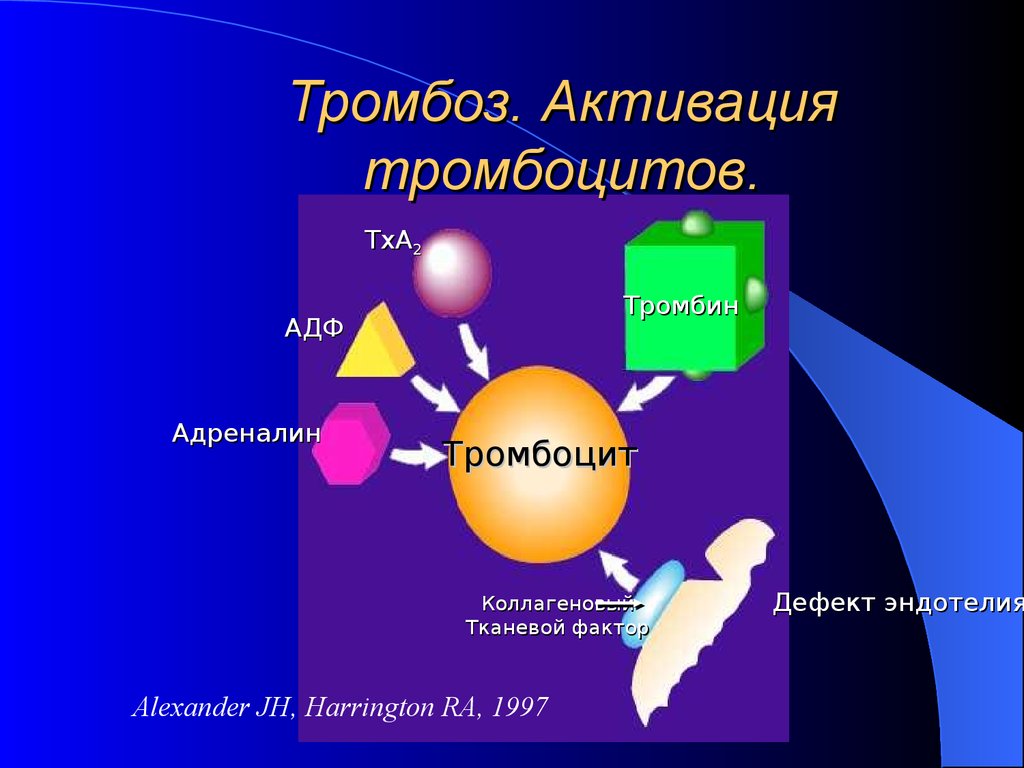
7. Тромбоз. Активация тромбоцитов.
TxA2Тромбин
АДФ
Адреналин
Тромбоцит
Коллагеновый
Тканевой фактор
Alexander JH, Harrington RA, 1997
Дефект эндотелия
8. Тромбоз. Агрегация.
ФибриногенGP IIb/IIIa
Рецептор
VW
F
F
W
V
Дефект эндотелия
Alexander JH, Harrington RA, 1997
GP Ib
рецептор
9.
Тромбоцитарный агрегат (серый тромб,гемостатическая пробка Рескома)
способен остановить кровотечение в
капиллярах и мелких венулах, однако его
прочность недостаточна, чтобы
остановить кровотечение при больших
повреждениях сосудистой стенки или
противостоять высокому давлению в
артериальной системе.
10. Свертывающая система крови.
Внутренний путь – активация свертывающейсистемы происходит при контакте крови с
отрицательно заряженной поверхностью
(коллаген субэндотелиального матрикса).
Внешний путь свертывания – запуск процесса
свертывания тканевым тромбопластином,
высвобождающимся из поврежденных
эндотелиальных клеток.
11.
Каскад свертыванияВнутренний путь
(контакт поверхностей)
Внешний путь
(тканевой фактор)
XIIa
VIIa
XIa
Фондапаринукс
Гепарин
IXa
Xa
АЧТВ
ПВ
Гирурудин
Тромбин (IIa)
Тромбин-фибриновый
сгусток
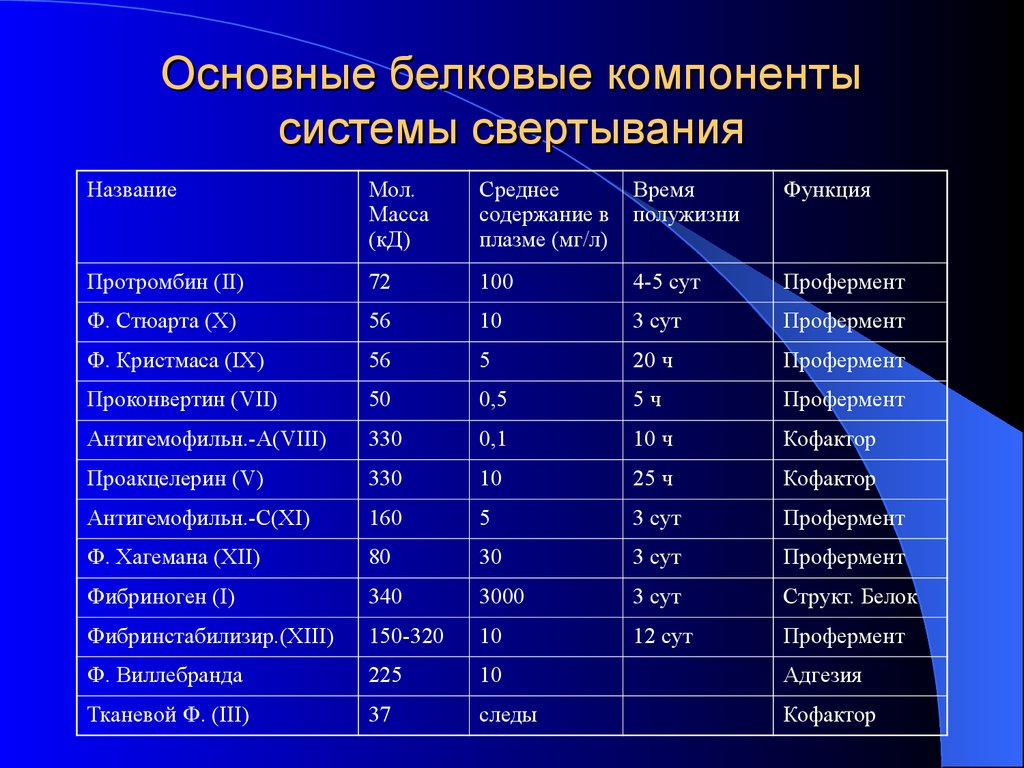
12. Основные белковые компоненты системы свертывания
НазваниеМол.
Масса
(кД)
Среднее
содержание в
плазме (мг/л)
Время
полужизни
Функция
Протромбин (II)
72
100
4-5 сут
Профермент
Ф. Стюарта (X)
56
10
3 сут
Профермент
Ф. Кристмаса (IX)
56
5
20 ч
Профермент
Проконвертин (VII)
50
0,5
5ч
Профермент
Антигемофильн.-А(VIII)
330
0,1
10 ч
Кофактор
Проакцелерин (V)
330
10
25 ч
Кофактор
Антигемофильн.-С(XI)
160
5
3 сут
Профермент
Ф. Хагемана (XII)
80
30
3 сут
Профермент
Фибриноген (I)
340
3000
3 сут
Структ. Белок
Фибринстабилизир.(XIII)
150-320
10
12 сут
Профермент
Ф. Виллебранда
225
10
Адгезия
Тканевой Ф. (III)
37
следы
Кофактор
13. Механизм свертывания
VIIXa
протромбин
Тромбин
Фибриноген
Фибрин
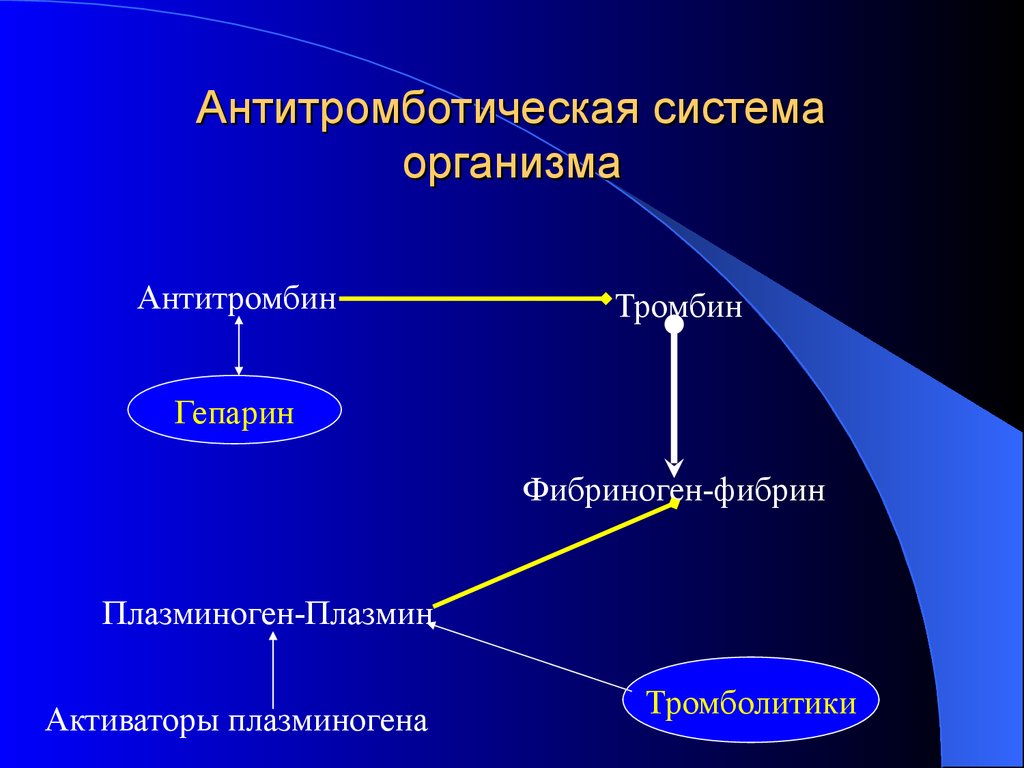
14. Антитромботическая система организма
АнтитромбинТромбин
Гепарин
Фибриноген-фибрин
Плазминоген-Плазмин
Активаторы плазминогена
Тромболитики
15. Причины тромборезистентности сосудистой стенки.
Отрицательный электрический заряд тромбоцитов и клетокэндотелия вызывает их взаимное отталкивание.
Синтез клетками эндотелия простациклина (PgI2) и эндотелийзависимого фактора расслабления (NO) – мощных
антитромбоцитарных фаторов.
Локализация фермента, расщепляющего АДФ - АДФазы на
мембранах эндотелия (АДФ – сильный фактор агрегации
тромбоцитов).
Локализация на клетках эндотелия тромбомодуллина –
гликопротеида, связывающего тромбин и стимулирующего
расщепление фаторов свертывания крови.
Локализация на мебранах эндотелия натурального геприна и
гепариноидов.
Синтез клетками эндотелия тканевого и урокиназного активаторов
плазминогена.
16. Тромбофилия (предрасполагающие факторы)
Врожденный дефицит АТIII, плазминогена.Гипервискозность крови (гиповолемия, полицитемия)
Застой крови в венозной сети (расширение вен, нарушение
венозного оттока)
Застой крови в полостях сердца (мерцательная аримия,
аневризма)
Повреждение стенки сосудов (атеросклеротические бляшки,
воспаление интимы)
Наличие искусственных клапанов, протезов сосудов
17. Тромбофилия (последствия)
Острый коронарный синдромИнфаркт головного мозга
Тромбоэмболия легочной артерии
Мезентериальный тромбоз
Синдром ДВС
Тромбозы и эмболии периферических сосудов
Тромбоз вен сетчатки
18.
АНТИКОАГУЛЯНТЫ Антикоагулянты препятствуютобразованию фибринных тромбов. Их классифицируют на
антикоагулянты прямого и непрямого действия. Антикоагулянты
прямого действия инактивируют циркулирующие в крови
факторы свертывания, эффективны in vitro и in vivo, применяются
для консервирования крови, лечения и профилактики
тромбоэмболических заболеваний и осложнений. Антикоагулянты
непрямого действия (оральные) являются антагонистами
витамина К и нарушают зависимую от этого витамина активацию
факторов свертывания в печени, эффективны только in vivo,
применяются с лечебно-профилактической целью.
19. Механизм действия гепарина
Катализ антитромбина (AT III)Активированный антитромбин
ингибирует тромбин (IIa) и фактор Xa.
20.
Взаимодействие ко-факторов гепарина с тромбиномF
Тромбин
S
H
C
AT
Антитромбин (AT) и
Ко-фактор гепарина II
(HC II).
AT – эффективный
антитромбин
HC II – очень слабый
антитромбин
F
Тромбин
S
H
C
HC II
+
++-+- -
21.
Инактивация тромбина гепарин-антитромбиновым комплексом.Гепарин
F
Тромбин
S
H
C
AT
Нейтрализация тромбина антитромбином осуществляется
медленно (в течение нескольких минут). Гепарин значительно
усоряет (катализирует) этот процесс.
22. Прямые ингибиторы тромбина.
Гирудин и его синтетичекие аналоги оказывают прямое ингибирующеедействие на тромбин (эффект не зависит от АТ III).
Сайт связи с фибрином
Тромбин
Каталити
ческий
сайт
ин
р
б
и
Ф
Тромбин
Гирудин
Rihal, Flather, Hirsh, Yusuf, 1995
ин
Фибр
Тромбин
ATIII/
Гепарин
23. Ингибиторы GP IIb/IIIa рецепторов
1983 год – описание Coller роли гликопротеидныхрецепторов тромбоцитов
90-е годы – исследования, а затем активное внедрение
абциксимаба, тирофибана и эпифибатида
Неудовлетворительные результаты практически всех
исследований с пероральными GP-блокторами
олигопептидной природы.
24. Ингибиторы GP IIb/IIIa рецепторов
GP IIb/IIIaрецептор
Фибриноген
GP IIb/IIIa
блокаторы
25.
АНТИКОАГУЛЯНТЫ Антикоагулянты препятствуютобразованию фибринных тромбов. Их классифицируют на
антикоагулянты прямого и непрямого действия.
Антикоагулянты прямого действия инактивируют
циркулирующие в крови факторы свертывания, эффективны
in vitro и in vivo, применяются для консервирования крови,
лечения и профилактики тромбоэмболических заболеваний
и осложнений. Антикоагулянты непрямого действия
(оральные) являются антагонистами витамина К и
нарушают зависимую от этого витамина активацию
факторов свертывания в печени, эффективны только in vivo,
применяются с лечебно-профилактической целью.
26.
АНТИКОАГУЛЯНТЫ ПРЯМОГО ДЕЙСТВИЯ (ИНГИБИТОРЫТРОМБИНА) Антикоагулянты прямого действия снижают
ферментативную активность тромбина (фактор свертывания IIа) в
крови. Различают две группы антикоагулянтов в зависимости от
механизма ингибирования тромбина. Первая группа —
селективные, специфические ингибиторы, независимые от
антитромбина III (олигопептиды — гирудин, аргатробан; препарат
для приема внутрь — ксимелагатран). Они нейтрализуют
тромбин, блокируя его активный центр. Другую группу
составляет гепарин — активатор антитромбина III.
27.
ГИРУДИН — одноцепочечный полипептид (65 — 66 аминокислот) слюныпиявок (Hirudo medicinalis) 1 с молекулярной массой около 7 кДа.
Стабилизирован в характерной конформации тремя дисульфидными
мостиками. В настоящее время гирудин получают методом генной
инженерии . Гирудин избирательно и обратимо ингибирует тромбин, образуя с
его активным центром стабильный комплекс , не влияет на дрфугие факторы
свертывания крови. Гирудин устраняет все эффекты тромбина — превращение
фибриногена в фибрин, активацию факторов V (проакцелерин, Ас-глобулин
плазмы), VIII (антигемофильный глобулин ), XIII (фермент, вызывающий
переплетение нитей фибрина ), агрегацию тромбоцитов. Рекомбинантный
препарат гирудина — ЛЕПИРУДИН (РЕФЛЮДАН) получают из культуры
дрожжевых клеток. При введении в вену он удлиняет активированное
частичное тромбопластиновое время (АЧТВ) в 1,5 — 3 раза. Элиминируется
почками (45% — в виде метаболитов). Период полуэлиминации в первой фазе
— 10 мин, во второй фазе — 1,3 ч. Применяется в качестве дополнительного
средства при тромболитической терапии острого инфаркта миокарда, для
лечения нестабильной стенокардии и профилактики тромбоэмболических
осложнений у ортопедических больных . Аргатробан является N-замещенным
производным аргинина, в большей степени инактивирует тромбин, чем
трипсин, плазмин, фактор Ха, калликреин
28.
КСИМЕЛАГАТРАН (ЭКСАНТА) — единственный из доступных прямых ингибиторов тромбина,который можно назначать внутрь. Он является пролекарством, транспортной формой и после
всасывания в кровь (биодоступность — 18 — 24%) подвергается метаболическим превращениям с
образованием мелагатрана — прямого ингибитора тромбина. Трансформация ксимелагатрана в
мелагатран происходит в два этапа. На первом этапе гидроксильная группа в молекуле
ксимелагатрана восстанавливается с образованием этилового эфира мелагатрана . Реакция
восстановления протекает в основном в печени, но также в слизистой оболочке кишечника и почках.
На втором этапе эстеразы крови и тканей гидролизуют этиловую группу этилмелагатрана . В
результате этой реакции появляется мелагатрана гидроксиамидин. Мелагатран мало связывается с
белками плазмы крови (20%), не метаболизируется и не взаимодействует с другими лекарственными
средствами, выводится почками (80%). При острой почечной недостаточности дозу ксимелагатрана
требуется снижать . Ксимелагатран назначают внутрь для профилактики тромбоза глубоких вен
голени и тромбоэмболических осложнений после ортопедических и хирургических операций .
Доказана эффективность ксимелагатрана как средства профилактики ишемического инсульта и
системных эмболий при хронической фибрилляции предсердий. Во время терапии ксимелагатраном
не требуется проводить лабораторный контроль . Ксимелагатран безопасен в плане кровотечений, у 5
— 10% пациентов вызывает бессимптомное повышение активности печеночных аминотрансфераз.
29.
В 1916 г. американский студент-медик Джей МакЛенисследовал растворимый в эфире прокоагулянт,
выделенный из печени. В этом эксперименте был
открыт неизвестный ранее антикоагулянт
фосфолипидной природы. В 1922 г. физиолог Уильям
Генри Хауэлл получил гепарин 1 В слюне пиявки
содержится также мощный ингибитор плазмина —
бделластазин. — водорастворимый антикоагулянт,
сульфатированный гликозаминогликан. МакЛен в то
время был сотрудником лаборатории, руководимой
Хауэллом в медицинской школе Джона Хопкинса в
Балтиморе.
30.
ГЕПАРИН (лат. hepar — печень) состоит из остатков N-ацетил-D-глюкозамина иD- глюкуроновой кислоты (или ее изомера L-идуроновой кислоты), депонирован
в секреторных гранулах тучных клеток. В одной грануле к белковому ядру
присоединено 10 — 15 цепей, включающих 200 — 300 субъединиц
моносахаридов (молекулярная масса пептидогликана — 750 — 1000 кДа).
Внутри гранул моносахариды подвергается сульфатированию. Перед секрецией
гепарин расщепляется до фрагментов с молекулярной массой 5 — 30 кДа (в
среднем — 12 — 15 кДа) ферментом эндо-β-D-глюкуронидазой. В крови он не
определяется, так как быстро разрушается. Только при системном мастоцитозе,
когда происходит массивная дегрануляция тучных клеток, полисахарид
появляется в крови и значительно снижает ее свертывание. На поверхности
клеток и во внеклеточном матриксе находятся гликозаминогликаны, близкие
гепарину (гепариноиды), — гепарана сульфат и дерматана сульфат. Они
обладают свойствами слабых антикоагулянтов. При распаде клеток
злокачественных опухолей гепаран и дерматан освобождаются в кровоток и
вызывают кровотечение.
31.
В 1939 г. К. Brinkhous и его сотрудники открыли, что противосвертывающий эффектгепарина опосредован эндогенным полипептидом плазмы крови. Спустя 30 лет этот
фактор противосвертывающей системы был идентифицирован как антитромбин III.
Он синтезируется в печени и представляет собой гликозилированный одноцепочечный
полипептид с молекулярной массой 58 — 65 кДа, гомологичен ингибитору протеаз —
a1 -антитрипсину. Сродством к антитромбину III и биологическим действием
обладают только 30 % молекул гепарина, имеющие пентасахаридный активный центр.
Этот центр связывается со специфическим катионным участком антитромбина III.
Гепарин служит матрицей для связывания антитромбина III с факторами свертывания
и изменяет стереоконформацию его активного центра. В комплексе с гепарином
антитромбин III инактивирует факторы свертывания группы сериновых протеаз — IIа
(тромбин), IХа (аутопротромбин II), Ха (аутопротромбин III, фактор Стюарта —
Прауэра), ХIа (плазменный предшественник тромбопластина), ХIIа (фактор Хагемана),
а также калликреин и плазмин. Гепарин ускоряет протеолиз тромбина в 1000 — 2000
раз. Для деполимеризации тромбина гепарин должен иметь молекулярную массу 12 —
15 кДа, для деполимеризации фактора Ха достаточно молекулярной массы 7 кДа.
Инактивация тромбина сопровождается антитромботическим и антикоагулянтным
эффектами, инактивация фактора Ха — только антитромботическим действием. При
отсутствии антитромбина III возникает резистентность к гепарину. Различают
врожденный и приобретенный (при длительной гепаринотерапии, гепатите, циррозе
печени, нефротическом синдроме, беременности) дефицит антитромбина III.
32.
Гепарин обладает противоатеросклеротическими свойствами:· активирует липопротеидлипазу (этот фермент катализирует гидролиз
триглицеридов в составе хиломикронов и липопротеинов очень низкой
плотности);
· тормозит пролиферацию и миграцию эндотелиальных и
гладкомышечных клеток сосудистой стенки.
· Клиническое значение имеют и другие фармакологические эффекты
гепарина:
· иммунодепрессивное действие (нарушает кооперацию Т- и Влимфоцитов, ингибирует систему комплемента);
· связывание гистамина и активация гистаминазы; · ингибирование
гиалуронидазы со снижением проницаемости сосудов; · торможение
избыточного синтеза альдостерона;
· повышение функции паратиреоидина (выполняет функцию тканевого
кофактора этого гормона);
· обезболивающее, противовоспалительное, коронарорасширяющее,
гипотензивное, мочегонное, калийсберегающее, гипогликемическое
действие.
33.
Лекарственный препарат гепарин получают из кишечника свиней и легкихкрупного рогатого скота Свиной гепарин более активен, так как сильнее и
длительнее инактивирует фактор Ха, реже вызывает тромбоцитопению.
Натриевая и кальциевая соли гепарина обладают одинаковой клинической
эффективностью, однако натриевая соль приводит к образованию гематом в
месте инъекции у 3,6 % больных, кальциевая соль — у 4,5 % Коммерческие
препараты гепарина отличаются по происхождению, степени очистки и
содержанию воды, поэтому их дозы выражают не в граммах , а в
международных единицах . Спектр клинического использования гепарина
широкий. Его применяют для профилактики и лечения тромбоза глубоких вен
нижних конечностей, лечения острой тромбоэмболии легочной артерии,
нестабильной стенокардии, острого инфаркта миокарда, периферических
тромбозов, ишемического (тромбоэмболического) инсульта, синдрома
диссеминированного внутрисосудистого свертывания крови. Гепарин назначают с
профилактической целью у ортопедических, хирургических, неврологических и
терапевтических больных с высоким риском тромбоза сосудов нижних
конечностей, а также при гемодиализе, операциях с искусственным
кровообращением, ревматизме, бронхиальной астме, гломерулонефрите,
фибрилляции предсердий до и после операции кардиоверсии. С лечебной целью
гепарин вливают в вену в виде болюса и капельно, для профилактики вводят под
кожу. Контроль осуществляют измерением АЧТВ или времени свертывания крови.
Эти показатели допустимо увеличивать соответственно в 1,5 — 2 раза (до 30 — 35
с) и 2 — 2,5 раза (до 11 — 14 мин). Исследуют также тромбоэластограмму.
34.
Натриевую соль гепарина в форме геля ЛИОТОН 1000 наносят накожу при тромбофлебите поверхностных вен, хронической
варикозной болезни, асептических инфильтратах, ушибах, подкожных
гематомах. При местном действии гепарин подавляет воспаление,
боль, уменьшает тромбообразование. Самое частое осложнение
терапии гепарином — кровотечения (при использовании гепарина в
малых дозах — у 5 — 10 % больных, при введении в больших дозах
— у 10 — 33 %). Риск кровотечений повышается при частом
прерывистом назначении, неадекватном контроле над показателями
свертывания крови, почечной и печеночной недостаточности,
сочетании с кислотой ацетилсалициловой и тромболитическими
средствами, у пожилых больных Для остановки кровотечений
используют химический антагонист гепарина — положительно
заряженный белок ПРОТАМИНА СУЛЬФАТ. Этот препарат вводят в
вену, 1 мг протамина связывает 100 ЕД гепарина Следует помнить,
что протамина сульфат может вызывать анафилактический шок, при
передозировке усиливает кровотечение. Комплекс гепарина и
протамина, освобождая тромбоксан А2 вызывает легочную
гипертензию и правожелудочковую сердечную недостаточность.
35.
У 6 — 16 % больных, получающих гепаринотерапию, возможно развитиетромбоцитопении. Умеренная тромбоцитопения возникает на 2 — 4-й дни
и обусловлена задержкой тромбоцитов в депо. Опасная тромбоцитопения
появляется между 6-м и 12-м днями лечения. Ее патогенез — образование
иммуноглобулинов IGG и IGM против тромбоцитов. Тромбоцитарные
агрегаты вызывают некроз кожи, гангрену конечностей, инфаркт
миокарда, эмболию сосудов легких. Гепаринотерапию отменяют, если
количество тромбоцитов в крови снижается вдвое по отношению к
исходному уровню. Другие побочные эффекты гепарина — аллергические
реакции (кожная сыпь, артралгия, миалгия), гематомы в месте инъекций,
обратимая алопеция (облысение), остеопороз, гипоальдостеронизм, рост
в крови активности ферментов печеночного происхождения. Отмена
гепарина у больных нестабильной стенокардией создает опасность
острого инфаркта миокарда. Для профилактики этого осложнения
рекомендуют после прекращения введения гепарина принимать кислоту
ацетилсалициловую в малых дозах.
36.
Антикоагулянты прямого действия противопоказаны прииндивидуальной непереносимости, внутренних кровотечениях,
недавнем (в течение 10 дней) кровотечении, геморрагическом
инсульте (в том числе в анамнезе), недавней (в течение двух
месяцев) травме или операции на головном и спинном мозге,
недавней (в течение 10 дней) травме или операции с
повреждением внутренних органов, геморрагическом диатезе,
неконтролируемой артериальной гипертензии (АД выше 180/120
мм рт. ст.), ортостатической гипотензии, подозрении на
расслаивающую аневризму аорты или острый панкреатит, остром
перикардите, инфекционном эндокардите, диабетической
геморрагической ретинопатии, тяжелой тромбоцитопении,
печеночной и почечной недостаточности, лучевой терапии.
Антикоагулянты этой группы с осторожностью применяются при
беременности.
37.
Преимущества по сравнению с нефракционированным гепарином (НФГ)имеет НИЗКОМОЛЕКУЛЯРНЫЙ ГЕПАРИН (НМГ). НМГ получают
ионообменной и аффинной хроматографией, мембранной фильтрацией,
частичной деполимеризацией НФГ. НМГ обладает молекулярной массой
меньше 7 кДа, поэтому способен инактивировать только фактор Ха, но не
тромбин. Соотношение активности НМГ против фактора Ха и тромбина
составляет 4:1 или 2:1, у НФГ — 1:1. Как известно, тромбогенное действие
фактора Ха в 10 — 100 раз больше, чем тромбина. Фактор Ха совместно с
фактором V, ионами кальция и фосфолипидами образует ключевой фермент
превращения протромбина в тромбин — протромбокиназу; 1 ЕД фактора Ха
участвует в образовании 50 ЕД тромбина. НМГ не снижает агрегацию
тромбоцитов, повышает эластичность эритроцитов, тормозит миграцию
лейкоцитов в очаг воспаления, стимулирует секрецию эндотелием активатора
плазминогена тканевого типа и липопротеин-ассоциированного ингибитора
свертывания. Особенности фармакокинетики НМГ следующие: ·
биодоступность при инъекции под кожу достигает 90 % (у препаратов НФГ 15-20 %); · связь с гепарин-нейтрализующими белками крови, эндотелием и
макрофагами незначительная; · период полуэлиминации составляет 1,5 —
4,5 ч, длительность действия — 8 — 12 ч (вводят 1 — 2 раза в сутки).
38.
Лекарственные препараты НМГ имеют молекулярнуюмассу 3,4 — 6,5 кДа и значительно отличаются по
противосвертывающему эффекту (табл. 81). НМГ
применяют по тем же показаниям, что и НФГ. НМГ
эффективнее предупреждает венозный тромбоз и
эмболию легочной артерии у ортопедических больных,
оказывает лечебное действие при нестабильной
стенокардии и инфаркте миокарда без зубца Q. НМГ
вводят под кожу без регулярного контроля показателей
свертывания крови. НМГ реже НФГ вызывает
кровотечения и тромбоцитопению.
39.
В последние годы созданы новые препараты гликозаминогликанов —сулодексид и данапароид. СУЛОДЕКСИД (ВЕССЕЛ) содержит два
гликозаминогликана слизистой оболочки кишечника свиней, — дерматана
сульфат (20%) и быструю фракцию гепарина (80%). Быстро движущаяся
при электрофорезе фракция гепарина имеет молекулярную массу около 7
кДа, но в отличие от НМГ богата эфирносульфатными группами. Препарат
эффективен при приеме внутрь , введении в мышцы и вену (под контролем
АЧТВ и протромбинового времени). Показан для профилактики
тромбоэмболии легочной артерии у больных тромбозом глубоких вен
нижних конечностей , вторичной профилактики после острого инфаркта
миокарда, лечения облитерирующего атеросклероза нижних конечностей.
Сулодексид вызывает геморрагические осложнения только у 0,5 — 1,3 %
больных. ДАНАПАРОИД (ЛОМОПАРИН, ОРГАРАН) — смесь
гликозаминогликанов слизистой оболочки кишечника свиней: НМГ,
гепарана сульфата (80%), дерматана сульфата и хондроитина. Средняя
молекулярная масса данапароида — 6,5 кДа, соотношение активности
против фактора Ха и тромбина равно 20:1. При введении под кожу препарат
обладает биодоступностью 100%, его период полуэлиминации — 14 ч.
Показания к применению данапароида такие же, как у сулодексида. Терапия
протекает без геморрагических и тромбоцитопенических осложнений.
40. Непрямые антикоагулянты
Подавление активности Кэпоксиредуктазы, снижение запасоввитамина К.
Уменьшение синтеза витамин-Кзависимых фаторов свертывания (II, VII,
IX, X)
41.
Антикоагулянты непрямого действия (оральные антикоагулянты)устраняют активирующее влияние жирорастворимого витамина К
на факторы свертывания крови.
Противосвертывающее действие кумаринов было открыто
случайно. В начале XX в. в Северной Америке появилось новое
заболевание крупного рогатого скота, для которого были
характерны серьезные кровотечения. В 1924 г. Канадский
ветеринар F. Schofield установил связь между кровотечениями у
коров и кормлением их сеном с заплесневелым клевером. В 1939
г. К. Link и его сотрудники выделили вещество группы кумаринов
— дикумарин и доказали, что он служил причиной кровотечений
при «болезни сладкого клевера». С 1941 г. дикумарин
применяется в медицинской практике. В 1947 г. препарат группы
монокумаринов варфарин был успешно применен для лечения
больных инфарктом миокарда. В настоящее время варфарин
занимает четвертое место в мире среди выписываемых сердечнососудистых препаратов и 11-е место — среди всех назначаемых
препаратов.
42.
Витамин К — объединенное название для группы производныхнафтохинона:
· витамин К1 содержится в растениях (шпинат, цветная капуста,
плоды шиповника, хвоя, зеленые помидоры, корка апельсина,
зеленые листья каштана, крапива), выпускается под названием
фитоменадион;
· витамин К2 синтезируется микрофлорой толстого кишечника;
· Витамин К3 — синтетическое соединение (его бисульфитное
производное — водорастворимый препарат викасол).
Витамин К находится в печени в виде гидрохинона, эпоксида и
хинона. В момент окисления гидрохинона в эпоксид активируется
фермент эндоплазматического ретикулума гепатоцитов,
карбоксилирующий остатки глутаминовой кислоты. При
карбоксилировании активируются факторы свертывания — II
(протромбин), VII (проконвертин, аутопротромбин I), IX
(аутопротромбин II) и X (аутопротромбин III, фактор Стюарта —
Прауэра). Эпоксид витамина К восстанавливается в хинон
ферментом НАД•Н-зависимой эпоксидредуктазой, затем хинон
восстанавливает в гидрохинон при участии хинонредуктазы.
43.
Антикоагулянты непрямого действия хорошо (80 —90%) всасываются из кишечника, в значительной
степени (90%) связываются с альбуминами, окисляются
цитохромом Р-450 печени с образованием неактивных
метаболитов, выводимых из организма с мочой.
Варфарин представляет собой рацемическую смесь
равных количеств R- и S-изомеров. S-варфарин в 4 — 5
раз активнее R-изомера, окисляется в печени и
выводится с желчью; R-варфарин экскретируется
почками. Период полуэлиминации S-варфарина — 54 ч,
R-варфарина — 32 ч
44.
Антикоагулянты непрямого действия являются средствами выбора для профилактики и лечениятромбоза глубоких вен нижних конечностей и связанных с ним тромбоэмболических осложнений;
профилактики тромбоэмболии после протезирования клапанов сердца и при фибрилляции
предсердий; вторичной профилактики ишемической болезни сердца у Пациентов, перенесших
инфаркт миокарда при наличии высокого риска системных тромбоэмболий. Существуют два
подхода к назначению антикоагулянтов непрямого действия. Если нет экстренной необходимости в
противосвертывающей терапии (например, при постоянной форме фибрилляции предсердий),
антикоагулянты назначают в средней поддерживающей дозе, обеспечивающей стабильное
удлинение протромбинового времени через 4 — 7 дней. В начале терапии протромбиновое время
определяют ежедневно, пока оно не увеличится до терапевтического уровня, затем три раза в
неделю на протяжении одной-двух недель. В неотложных ситуациях, когда необходимо получить
быстрый противосвертывающий эффект, применяют гепарин и антикоагулянты непрямого
действия в большой дозе. После повышения протромбинового времени до желаемого уровня
гепарин отменяют. Результаты определения протромбинового времени выражают в виде
протромбинового индекса — отношения среднего протромбинового времени нормальной плазмы
(11 — 14 с) к протромбиновому времени у больного. Для предупреждения венозного тромбоза
протромбиновое время необходимо увеличивать в 1,5 — 2,5 раза, для профилактики артериального
тромбоза — в 2,5 — 4,5 раза. Протромбиновый индекс снижают до 30 — 50%.
45.
В период лечения антикоагулянтами непрямого действия следует избегатьколебаний свертывания крови. Для этого из диеты исключают продукты,
богатые витамином К, не назначают лекарственные средства, как ослабляющие
действие антикоагулянтов (препараты витамина К, индукторы метаболизма
ксенобиотиков, адсорбенты), так и усиливающие их эффект (ингибиторы
метаболизма, антибиотики широкого спектра). Противосвертывающее влияние
антикоагулянтов уменьшается при гипотиреозе, гиперлипидемии, синдроме
мальабсорбции и, напротив, возрастает при заболеваниях печени, нарушении
секреции желчи, лихорадке, тиреотоксикозе, хронической сердечной
недостаточности, злокачественных опухолях. При терапии антикоагулянтами
непрямого действия у 3 — 8 % больных возникают кровотечения, при этом у 1
% пациентов они становятся фатальными. Антикоагулянты вызывают также
диспепсические расстройства, синдром «пурпурных пальцев»,
геморрагические некрозы кожи и гепатит. При приеме неодикумарина больные
отмечают его неприятный вкус. У 1,5 — 3 % людей наблюдается повышенная
чувствительность к фенилину в виде сыпи, лихорадки, лейкопении, головной
боли, нарушений зрения, токсического поражения почек.
46.
При кровотечениях применяют витамин К1 (ФИТОМЕНАДИОН) внутрь, вмышцы или в вену, чтобы повысить протромбиновый индекс до 40 — 60 %. В
случае массивных кровотечений и у больных с тяжелым нарушением функций
печени, когда витамин К малоэффективен, вводят свежезамороженную плазму.
Витамин К внутрь по 1 — 2 мг можно использовать для профилактики
кровотечений. ВИКАСОЛ оказывает тромбогенное действие при приеме внутрь
через 12 — 24 ч, после внутримышечной инъекции — спустя 2 — 3 ч, так как в
печени предварительно преобразуется в витамин K1 . Викасол обладает
свойствами сильного окислителя и может вызывать гемолиз и образование
метгемоглобина, особенно при дефектах метгемоглобинредуктазы, глюкозо-6фосфатдегидрогеназы и глутатионредуктазы. Фитоменадион таких нарушений
не вызывает. Противопоказания к назначению антикоагулянтов непрямого
действия такие же, как у гепарина. Следует обратить внимание на
недопустимость приема антикоагулянтов непрямого действия при беременности.
Варфарин и другие препараты этой группы могут вызывать в 5 % случаев
«варфариновый синдром плода». Его признаки — выступающая форма лба,
седловидный нос, обструкция верхних дыхательных путей вследствие
недоразвития хрящей трахеи и бронхов, кальцификация эпифизов. Наиболее
опасно лечение антикоагулянтами непрямого действия женщин на 6 — 9-й
неделях беременности.
47.
При авитаминозе факторы свертывания синтезируются, но остаются неактивными (акарбоксифакторы II, VII,IX, X). Акарбоксифактор II является антагонистом протромбина и получил название PIVKA — protein induced
by vitamin K absence. Витамин К карбоксилирует также факторы противосвертывающей системы — протеины
С и S. Комплекс этих протеинов инактивирует факторы свертывания V (проакцелерин, Ас-глобулин плазмы) и
VIII (антигемофильный глобулин), усиливает фибринолиз. Таким образом, витамин К необходим для активации
факторов свертывающей и противосвертывающей систем. Витамин К1 обладает антигипоксическим влиянием,
так как способствует транспорту водорода от НАД•Н к КоQ, минуя флавопротеин II (НАД•Н-дегидрогеназа);
усиливает синтез альбуминов, белков миофибрилл, фактора эластичности сосудов, поддерживает активность
АТФ-азы, креатинкиназы, ферментов поджелудочной железы и кишечника. Антикоагулянты непрямого
действия являются стереоструктурными аналогами витамина К. По конкурентному принципу они блокируют
НАД•Н-эпоксидредуктазу и, возможно, хинонредуктазу. При этом нарушается восстановление неактивного
окисленного эпоксида витамина К в активный гидрохинон. Прекращается карбоксилирование II, VII, IX, X
факторов свертывания, а также противосвертывающих протеинов С и S(рис. 12). Период полуэлиминации
факторов свертывания длительный, поэтому антикоагулянты действуют после латентного периода (8 — 72 ч).
На протяжении латентного периода элиминируются факторы свертывания, активированные ранее, до приема
антикоагулянтов. В латентном периоде свертывание крови может даже возрастать из-за быстро возникающего
дефицита эндогенного антикоагулянта протеина С, так как его период полуэлиминации короче, чем у факторов
свертывания II, IX и X (табл. 82). После отмены антикоагулянтов непрямого действия свертывание крови
возвращается к исходному уровню спустя 24 — 72 ч.
48. Антитромботическая терапия (антикоагулянтная терапия)
Применение при нестабильной стенокардииуменьшает частоту развития инфаркта на 28%,
летальность на 14%.
Внутривенное болюсное введение 5000 Ед + 2-5
суточная инфузия в дозе 800-1000 Ед/час
49. Гепарин+аспирин vs аспирин (Метаанализ)
6 РКИ (рандомизированныхконтролируемыхисследований)
(n = 1,353)
Конечные точки смерть/ИМ в течение
периода лечения (2-7 дней)
Результаты: СОР (снижениее
относительного риска) в группе
гепарин+асприн=33%, p = 0.04
Ohler, et al, 1996
50. Номограммы для рассчета дозы при гепаринотерапии
Подкожное введениеАЧТВ, с
Изменение дозировки
< 50
+ 2000 Ед
50 - 55
+ 1000 Ед
56 – 80
Дозу не изменять
81 – 95
- 1000 Ед
> 95
- 2000 Ед
51. Номограмма для рассчета дозы гепарина внутривенное введение (50 Ед/мл)
АЧТВ, сИзменение дозировки
< 50
+ 5000 Ед болюсом, + 3 мл/ч
50 - 59
+ 3 мл/ч
60 – 95
Дозу не изменять
96 – 120
Остановить на 30’, - 2 мл/ч
> 120
Остановить на 60’, - 4 мл/ч
52. Противопоказания к назначению гепарина
Острое внутреннее кровотечениеНедавнее (10 дней) кровотечение из ЖКТ или мочеполовых путей
Геморрагический инсульт, недавняя (2 мес) травма или операция мозга.
Недавняя (10 дней) обширная операция с возможным повреждением
внутренних органов.
Геморрагический диатез.
Неконтролируемая артериальная гипертензия.
Гепарининдуцированная тромбоцитопения в анамнезе.
Подозрение на расслаивающую аневризму аорты или острый панкреатит.
Острый перикардит, инфекционный эндокардит, диабетическая
геморрагическая ретинопатия.
53. Recommendations of a Task Force of the The European Society of Cardiology and The European Resuscitation Council
(A) Management of non-complicated chest pain of presumed cardiac origin5. Give short acting nitrate if pain is still present and systolic blood pressure >90 and no bradycardia.
6. Take 12-lead ECG.
8. Establish i.v. access.
9. Give aspirin 150 to 300 mg orally (or i.v. If available) unless contraindicated.
10. If no pain relief obtained with a nitrate, give morphine i.v. starting with 5 mg (or equivalent
dose if other opioid used) titrated up to a maximum pre-hospital dose of 20 mg for acceptable
pain control.
11. Give antiemetic such as metoclopramide 20 mg i.v. if necessary.
12. If patient remains anxious despite opioid give benzodiazepine.
13. If indications are present for thrombolysis (and in the absence of contraindications or
arrangements for primary angioplasty) initiate thrombolysis if
appropriate in the pre-hospital phase (recom-mended especially if journey time may be more than
30 min or the delay or call-to-needle time for in-hospital thrombolysis may exceed 60 min).
14. If indications for thrombolysis are not present, but the ECG shows evidence of ischaemia, a
bolus of heparin should be given. This will not preclude subsequent thrombolysis or primary
PTCA in the hospital.
Br Med J 1998; 316: 1065–70.
Eur Heart J, Vol. 19, August 1998
54. Гепарин и инфаркт миокарда
Класс IПациенты, подвергшиеся хирургической реваскуляризации.
Класс IIа
Внутривенно пациентам, получившим ТАП 70 Ед/кг болюсом, затем инфузия 15
Ед/кг в час до АЧТВ 50-75 сек в течение 48 часов.
У пациентов с высоким риском тромбоэмболий:
При наличии высокого риска тромбоэмболий - продолжение инфузии >48 часов,
подкожное введение 7500 Ед 2 раза в сутки.
При введении стрептокиназы или урокиназы - задержка с введением гепарина до
снижения АЧТВ до 70 сек.
В случае, когда ТЛТ не проводится - в/в введение гепарина как возможной
альтернативы тромболитику.
Класс IIb
Пациенты без высокого риска тромботических осложнений.
Класс III
Рутинное применение гепарина.
55. Недостатки НФ гепарина
Относительно низкая биодоступностьБыстрая элиминация
Значительное количество геморрагических
осложнений
Необходимость мониторинга АЧТВ
Относительно частое развитие тромбоцитопении
Относительная “непредсказуемость” эффекта
Высокий риск развития остеопороза при длительном
применении
56. Преимущества НМГ
Не требуется лабораторный мониторингВысокая биодоступность - 90% vs 30%
(НГ)
Длинный период полужизни
– 4 - 6 часов против 0.5 - 1 (НГ)
– почечный (медленный) клиренс
57. Преимущества НМГ
Фармакокинетические параметры не зависят отуровня белка плазмы, свойств поверхности
эндотелия, макрофагов и т.д.
58. Преимущества НМГ
Меньше воздействие на тромбоциты– Потенциально меньший риск кровотечения
Меньше риск тромбоцитопении и
тромбоза (HIT-синдром)
– меньше взаимодействие с 4 тромбоцитарным
фатором
– не образуются гепарин-зависимые антитела
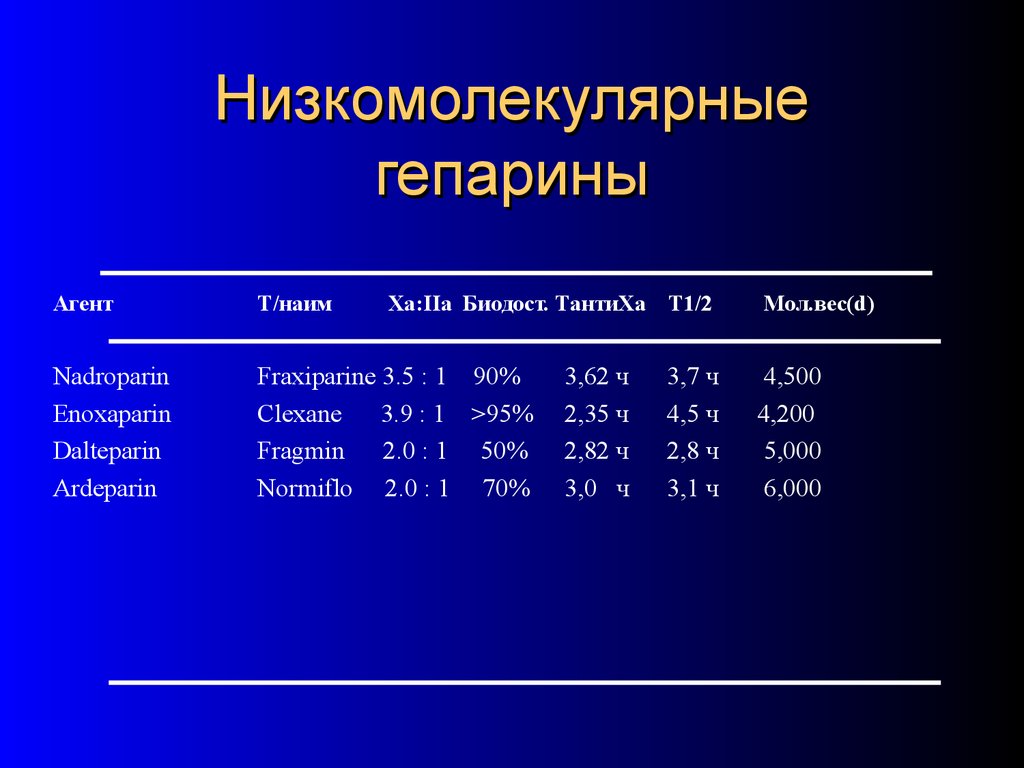
59. Низкомолекулярные гепарины
АгентТ/наим
Xa:IIa Биодост. TантиXa T1/2
Nadroparin
Enoxaparin
Dalteparin
Ardeparin
Fraxiparine 3.5 : 1 90%
Clexane
3.9 : 1 >95%
Fragmin
2.0 : 1 50%
Normiflo 2.0 : 1 70%
3,62 ч
2,35 ч
2,82 ч
3,0 ч
3,7 ч
4,5 ч
2,8 ч
3,1 ч
Мол.вес(d)
4,500
4,200
5,000
6,000
60. Низкомолекулярные гепарины vs плацебо
FRISCДальтепарин vs Плацебо [+апирин в обеих
группах]
Пациенты: НС или Не-Q-ИМ; n=1,506
Конечные точки: смерть/ИМ/реваскуляризация
или необходимость в/в введения НФ гепарина
Результаты:
@6 д. СОР=48%, p < 0.001
@40 д. СОР=21%, p = 0.011
@150 д. СОР=6%, p = 0.28
61. Низкомолекулярные гепарины vs НФГ
TIMI-IIBЭноксапарин vs НФГ
Пациенты: НС/Не-Q-ИМ; n = 3,910
Конечные точки:
смерть/ИМ/реваскуляризация
Результаты:
@48ч
@14д
@43d
СОР=24%, p = 0.02
СОР=15%, p = 0.03
СОР=11.7%, p = 0.049
62. Низкомолекулярные гепарины vs НФГ или плацебо
FRICДальтепарин vs НФГ (короткий период) vs Placebo
(длительный период) [+АСА в обеих гру




































































 medicine
medicine biology
biology








