Similar presentations:
Аллергодиагностика in vitro
1.
2.
В настоящее время современные лабораторныеметоды исследования уверенно входят в
практику
диагностики
аллергических
заболеваний (АЗ), позволяя идентифицировать
тип
аллергических
реакций,
провести
дифференциальную
диагностику
с
псевдоаллергическими проявлениями
Такие методы облегчают процесс установления
правильного
диагноза,
назначения
рациональной
терапии,
что
повышает
комплаенс между врачом и пациентом и
улучшает качество жизни больных.
3.
Возможность выборатест-системы
при
современном
арсенале
диагностической
лаборатории
4.
Преимуществами методов лабораторнойдиагностики, применяемых в аллергологии,
являются:
• безопасность для пациента;
• отсутствие противопоказаний;
• возможность проведения исследований в любом, в
том числе раннем детском возрасте, в период
обострения, при высокой степени сенсибилизации;
• выявление реакции на большое число аллергенов
за 1 исследование-батарейный скрининг;
• отсутствие влияния измененной реактивности
кожи;
• проведение исследования возможно на фоне
лечения.
5.
Использованиеспецифических
методов
лабораторной
диагностики аллергии показано:
• для подтверждения наличия сенсибилизации;
• для выявления скрытой (субклинической) сенсибилизации;
при наличии противопоказаний к проведению кожных проб
(обострение основного заболевания; в период развития острых
инфекционных, нервных и психических заболеваний; в случае
возникновения декомпенсированных состояний болезней сердца,
печени, почек и системы крови; вскоре после острой
аллергической реакции; в период лечения гормонами);
;
в случаях необходимости дифференциальной диагностики
положительных/ложноположительных
или
отрицательных/ложноотрицательных результатов, полученных при
кожном тестировании
6.
Основными задачами лабораторнойдиагностики АЗ являются:
• установление сенсибилизации к аллергенам
(специфическая аллергодиагностика);
• определение типа (типов) аллергической
реакции (специфическая аллергодиагностика);
• выявление характера и степени иммунных
нарушений (иммунодиагностика);
• характеристика патогенетических изменений,
типичных для данного АЗ (клиническая
лабораторная диагностика);
• установление неиммунологических
(псевдоаллергических) механизмов заболевания
путем исключения иммунологических.
7.
иммунологическиетесты
в
аллергодиагностике условно могут быть
разделены
на
2
большие
группы:
неспецифические
(направленные
на
выявление общих изменений иммунной
системы
при
аллергии
• специфические (определение участвующих в
иммунологической
фазе
аллергической
реакции
антител
и
клеток).
лимфоциты.
8.
Неспецифические тесты выявляют характер и степеньиммунных нарушений,
определение субпопуляций Т- и В-лимфоцитов, уровня
иммуноглобулинов, комплемента, циркулирующих
иммунных комплексов, медиаторов аллергического
воспаления и цитокинов, в большей степени
участвующих в иммунном ответе на аллергены:
IL-4 (активация продукции IgE), IL-10, IL-5, интерферонаγ и других.
Через 6-18 ч после реакции с аллергеном на
сенсибилизированных
лимфоцитах
усиливается
экспрессия рецепторов к IL-2,
С этой же целью можно определять наличие на
лимфоцитах других молекул активации – CD69, CD71.
Известно,
что
при
стимуляции
лимфоцитов
аллергенами усиливается выделение IL-5, IL-4,
интерферона-γ, но не IL-2 и фактора некроза опухолей[2].
.
9.
10. СКРИНИНГ Возможности скрининга весьма ограничены
11.
ОАКПо
данным большинства авторов
для
гиперчуствительности
немедленного типа
характерным
является лейкопения в связи с
усилением апоптоза лимфоцитов
Более характерна лейкопения
при ассоциации с инфекционными
заболеваниями,
вирусными
инфекциями, лечение системными
ГКС
12.
ЦИТОЛОГИЧЕСКОЕ ИССЛЕДОВАНИЕНАЗАЛЬНОГО СЕКРЕТА И МОКРОТЫ
Можно проводись у детей
Быстро получаемый результат
исследования
Неинвазивный
Скринирующий
Недорогой
Информативный
Может проводиться в лабораториях
клинического профиля
13.
1 способ больного просят высморкаться в вощаную бумагуили в чашку Петри
У детей раннего возраста используют резиновую
грушу или ватную палочку
Для сбора мокроты больного просят откашляться
Содержимое переносят на предметное стекло и
Распределяют на небольшом участке
Красят по Романовскому-Гимза или по Паппенгейму
2 Способ
Ватный томпон помещают в носовой ход на 2-3 мин
слизь переносят на предметное стекло распределяют
ровным слоем
•3 способ
Исследование соскоба
Больного просят высморкаться
У грудных детей удаляют содержимое с помощью груши
Делают соскоб с забнего отдела нижней носовой раковины
Материал распределяют на небольшом участке
предметного стекла высушивают красят по Романовскому или
по Папангейму Крюкову
14.
При 1 и 2 способеподсчитывают %
соотношение клеточных элементов
При 1 и 2 способе в мазках преобладают
эпителиальные клетки ( до 60-70 %) без
признаков деструкции
Другие клеточные элементы- нейтрофилы и
лимфоциты не более
30 -40 %
эозинофилы не более 5 %
При 3 способе клеточность ниже.
Подсчитывают среднее число клеток в 10
полях зрения
В норме
выявляют эпительальные
и
бокаловидные клетки
нейтрофилов
лимфоцитов
и
эозинофилов мало
15.
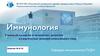
Увеличение числа эозинофиловУвеличение числа нейтрофилов +
бактерии
Увеличение числа нейтрофилов
Эпителиальные клетки с
конденсированным хроматином
Увеличение базофилов
Увеличение бокаловидных клеток
Увеличение лимфоцитов
Лимфоцитоз с плазматизацией ( > 40
%) в сочетании с эозинофилией
Умеренный нейтрофилез ( 20-40 %) в
сочетании с эозинофилией
Аллергический ринит
Эозинофильный неаллергический ринит
Полипоз носа
Ринит при непереносимости аспирина
Инфекционный ринит
НазоФарингит
ОРВИ
Вазомоторный ринит
Синусит Аллергический ринит ( поздняя
фаза аллергический реакций
ОРВИ
Сопровождается эозинофилией при
адллергическом рините
Аллергический или Инфекционный ринит
ОРВИ
Круглогодичный аллергический ринит
Поздняя фаза аллергической реакции
16.
Выделяют по риноцитограммеУМЕРЕННУЮ ЭОЗИНОФИЛИЮ (0т 7 до 13 %)
Круглогодичный аллергический ринит –диф. дз с
инфекционным ринитом
ВЫСОКУЮ ЭОЗИНОФИЛИЮ
( от 13 %)
Сезонный аллергический ринит
Сочетанный аллергический ринит с
Бронхиальной астмой
Обострение круглогодичного АР
ОЧЕНЬ ВЫСОКУЮ ЭОЗИНОФИЛИЮ ( от 40 до
90 % )
Обострение круглогодичного АР
Обострение сочетанного с БА АР
17.
18.
19.
20.
ОАКЭОЗИНОФИЛИЯ
УМЕРЕННАЯ ( до 15-20 %)не потогномонична для аллергических заболеваний ,
но
позволяет предположить этот диагноз
лямблиоз ,хроническое течение, особенно при длительном
инфицировании ( подтвержденным высоким титром суммарных
антител
токсокароз,
энтеробиоз ( некоторые глистные инвации)
злокачественные новообразования лимфогранулематоз
иммунодефициты
пороки сердца
Циррозы печени
Применении некоторых лекарств
21.
ВЫСОКАЯ ( более 20 % )Некоторые формы глистных инвазийаскаридоз,
трихиннелез и др
ОЧЕНЬ ВЫСОКАЯ ( > 50 %)
Некоторые глистные инвазии ( цепень и др)
Абсолютное содержание
эозинофилов ( 0,05- 0,7 х 10 9/л )
Используется в основном для оценки
эффективности терапии бронхиальной астмы
22.
Иммуноферментный анализ, или ИФА (англ.Enzyme-Linked ImmunoSorbent Assay, ELISA) — это
лабораторный
иммунологический
метод
качественного определения и количественного
измерения антигенов, а также иммуноглобулинов
и гормонов.
Метод ИФА обладает высокой чувствительностью
и специфичностью, которая в настоящее время
составляет более 90%.
23. Определение общих и спецефических Ig Е
• Иммуноферментный анализ,или ИФА (англ. Enzyme-Linked
ImmunoSorbent Assay, ELISA) — это
лабораторный иммунологический метод
качественного определения и
количественного измерения антигенов, а
также иммуноглобулинов и гормонов.
• Метод ИФА обладает высокой
чувствительностью и специфичностью,
которая в настоящее время составляет более
90%.
24.
Использование твердой фазы позволяетупростить
процесс
разделения
компонентов
реакции
за
счет
иммобилизации
компонентов на
твердой фазе и удаления субстанций, не
участвующих в реакции.
В качестве твердой фазы в большинстве
коммерческих
диагностических
препаратов используют полистироловые
96-ти
луночные
планшеты
или
полистироловые
шарики
25.
26.
Иммуноферментный анализ по сравнению с другимиметодами детекции антигенов и антител обладает
следующими преимуществами:
— высокой чувствительностью, позволяющей
выявлять концентрации до 0, 05 нг/мл.
— возможностью использовать минимальные
объемы исследуемого материала;
— стабильностью при хранении всех ингредиентов,
необходимых для проведения ИФА (до года и более);
— простотой проведения реакции;
— наличием как инструментального (в качественном
и количественном варианте), так и визуального учета;
— возможностью автоматизации всех этапов реакции
— относительно низкой стоимостью диагностических
наборов.
27.
Твердофазный ИФАОпределение антител проводят следующим
образом
Исследуемую жидкость вносят в лунки планшетов
Антитела связываются с антигеном во время
инкубации
Планшет отмывают от несвязавшихся антител
Добавляют вторые антитела ( в основном к
иммуноглобулинам ) меченые ферментами в
основном используют пероксидазу хрена
Добавляют субстрат фермента и хромоген
Концентрацию
антител
определяют
спектрофотометрически
на оптической
плотности на вертикальном спектрофотометре
типа Мультискан
28.
29.
Возможна классификация по типу иммунохимическоговзаимодействия на первой стадии анализа (в которой
происходит связывание определяемого вещества). Если в
системе присутствуют только анализируемое соединение и
соответствующие ему центры связывания (антиген и
специфические
антитела),
то
метод
является неконкурентным.
Если же на первой стадии в системе одновременно
присутствует анализируемое соединение и его аналог
(меченное ферментом анализируемое соединение или
анализируемое соединение, иммобилизованное на
твердой фазе), конкурирующие за ограниченное
количество центров специфического связывания, то метод
является конкурентным.
30.
Примером неконкурентного формата ИФА является«сэндвич»-метод.
К носителю с иммобилизованными антителами добавляют
раствор, содержащий анализируемый антиген. В процессе
инкубации на первой стадии на твердой фазе образуется
комплекс антиген-антитело. Затем носитель отмывают от
несвязавшихся компонентов и добавляют меченные
ферментом специфические антитела.
После вторичной инкубации и удаления избытка конъюгата
антител с ферментом определяют ферментативную
активность носителя, которая пропорциональна начальной
концентрации исследуемого антигена.
На стадии выявления специфического иммунокомплекса
антиген оказывается как бы зажатым между молекулами
иммобилизованных и меченных антител, что послужило
поводом для широкого распространения названия
«сэндвич»-метод
31.
Прямой конкурентный формат ИФА используетиммобилизованые
на
твердой
фазе
специфические антитела, а меченый ферментом
и немеченыйантиген конкурируют за связь с
иммобилизованным
антителом.
.В непрямом конкурентном формате ИФА
используются
меченные
ферментом антитела (специфические или
вторичные) и иммобилизованный на твердой
фазе
конъюгат
антиген-белок-носитель.
Непрямая схема с использованием меченых
антивидовых антител является одной из
наиболее распространенных схем ИФА
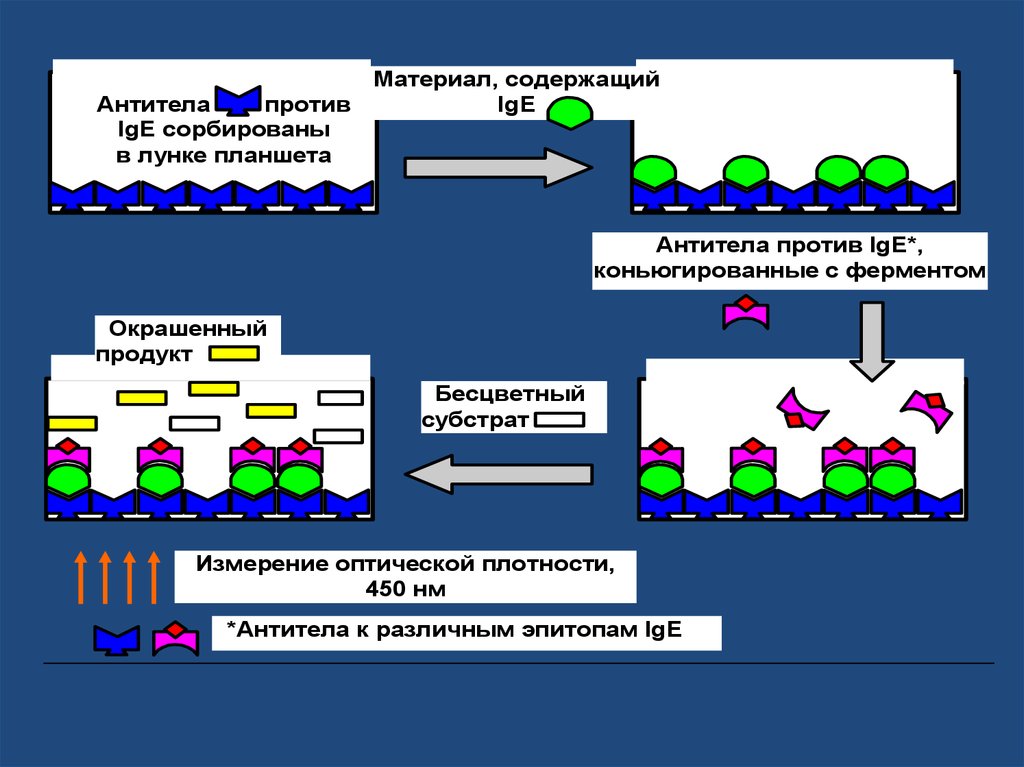
32.
Антителапротив
IgE сорбированы
в лунке планшета
Материал, содержащий
IgE
Антитела против IgE*,
коньюгированные с ферментом
Окрашенный
продукт
Бесцветный
субстрат
Измерение оптической плотности,
450 нм
*Антитела к различным эпитопам IgE
33.
ИММУНОБЛОТИММУНОБЛОТ (western blot) – это более точный
анализ, чем ИФА, и используется для подтверждения
результатов ИФА. он считается более чувствительным и
специфичным, хотя более сложным и дорогим.
Иммунный
блоттинг
сочетает
в
себе
иммуноферментный анализ (ИФА) с предварительным
электрофоретическим разделением антител или
антигенов в геле и их переносом на нитроцеллюлозную
мембрану.
Иммунный блоттинг чаще всего используют для
подтверждения диагноза ВИЧ-инфекции. Открыл новые
возможности в аллергологической диагностике
34. Иммуноглобулин Е Метод сэндвич –неконкурентный ИФА Фирмы производители Алкор-Био Вектор-Бест Хема и др.
35.
Определение общих и спецефических Ig ЕМожно проводить независимо от возраста
Скрининг атопии
Можно проводить в периоде обострения
Можно проводить на фоне лечения
Небольшой объем исследований
Быстрый результат
36.
У новорожденных повышенный уровень общего Ig Е рискразвития атопии
У детей с рецидивирующим бронхитом повышенный
уровень свидетельствует о развитии БА
У детей с атопическим дерматитом свидетельствует от
атопическом механизме заболевания, низкий о
неиммунных механизмах АД
Повышенный уровень Ig Е подтверждает диагноз
атопического заболевания
Отрицательный не исключает наличия атопического
заболевания
Метод высмокоинформативен на основе твердофазного
ИФА
37.
Особенности интерпретации данных исследования общего IgE:1. Повышение уровня общего IgE может быть вызвано не только
атопией, но и целым рядом других заболеваний, в т. ч. глистными
инвазиями, иммунодефицитными состояниями,
бронхопульмональным аспергиллезом и др.
2. Нормальный уровень общего IgE в сыворотке крови не отрицает
наличия сенсибилизации. Примерно у трети больных
атопическими заболеваниями уровень общего IgE может
находиться в пределах нормы (30-100 кЕ/л).
3. При сенсибилизации к одному (нескольким) аллергенам
содержание общего IgE может быть в пределах нормы, а
специфического – повышено.
4. Концентрация общего IgE в сыворотке крови может быть в
пределах нормы при неатопических состояниях неиммунной
природы, хронической рецидивирующей крапивнице и
ангионевротическом отеке.
5. Верхняя граница нормы общего IgE (100 кЕ/л) у лиц,
проживающих в регионах, эндемичных по гельминтозам, может
быть выше обычной.
38.
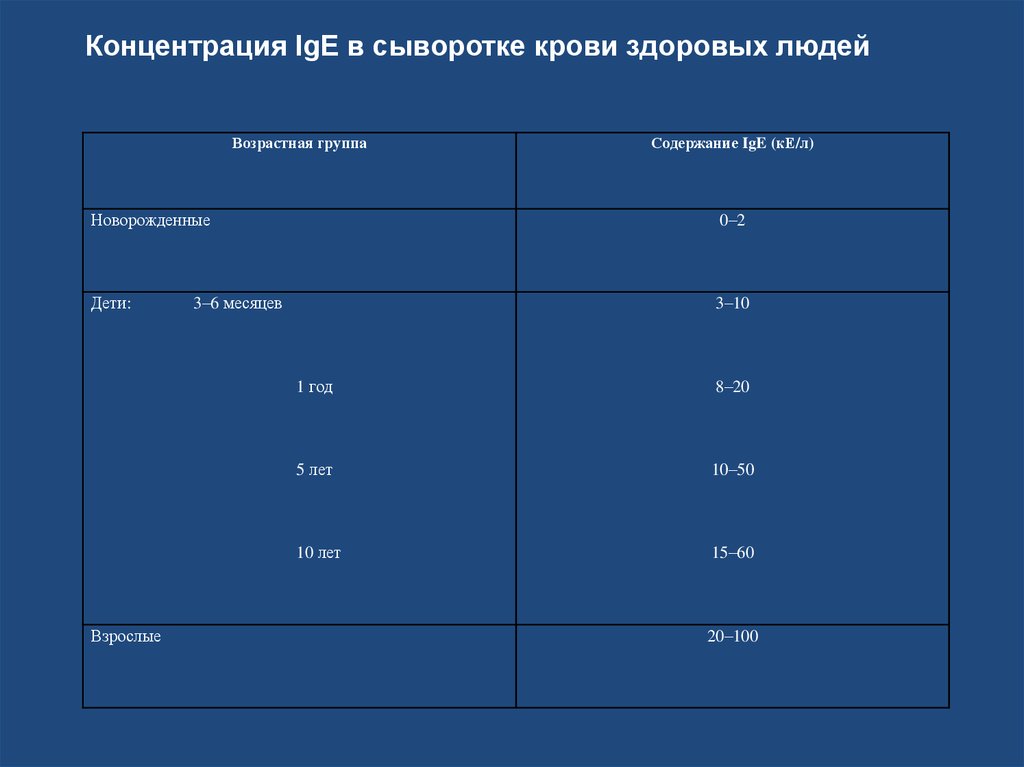
Концентрация IgE в сыворотке крови здоровых людейВозрастная группа
Содержание IgE (кЕ/л)
Новорожденные
0–2
Дети:
3–10
Взрослые
3–6 месяцев
1 год
8–20
5 лет
10–50
10 лет
15–60
20–100
39.
Дополнительныеисследования,
рекомендуемые при дифференциальной
диагностике аллергий и псевдоаллергий:
-обследование на скрытые паразитарные
инфекции
(гельминты,
лямблии,
токсоллазмоз);
- обследование на скрытые системные
вирусные
инфекции;
- исследование на микогенные инфекции.
40.
41.
Преимущества• Безопасность.
• На проведение не влияет состояние
кожи и принимаемые ЛС.
• Не зависит от кооперации с пациентом
(особенно с ребенком).
• Хорошая воспроизводимость.
• Элиминация ложноположительных и
ложноотрицательных результатов кожных
прик-тестов.
• Однократная инвазивность
(однократный забор крови
42.
43.
44.
45.
46.
47.
48.
49.
«50. CARLA RADIM ADALTIS Алкор БИО Хема Вектор-Бест
51.
Особенности интерпретации исследования специфических IgE:1. Отрицательный результат исследования на специфический IgE может
быть обусловлен стратегией скрининга – отсутствием теста на данный
аллерген. Отсутствие специфического IgE в сыворотке периферической
крови не исключает возможности участия в патогенезе IgE-зависимого
механизма аллергической реакции, так как возможен местный синтез
IgE, или связывания синтезированного IgE тканями, что может
происходить без изменения концентрации специфического IgE в
периферической крови.
2. Антитела других классов, особенно IgG (IgG4), специфичные к
аллергену, в определенных случаях могут быть причиной
ложноотрицательных результатов.
3. Высокий уровень аллерген-специфического IgЕ характеризует
наличие высокого уровня сенсибилизации только по отношению к
конкретному изучаемому аллергену.
52.
4. При высоких концентрациях общего IgE чаще могутвозникать
ложноположительные
результаты
исследований на специфические IgE, т. к. в таких
условиях
повышается
вероятность
связывания
неспецифических
IgE
с
аллергеном.
5. Идентичные количественные результаты определения
специфического IgE для разных аллергенов не означают
их
одинакового
клинического
значения.
6. Окончательное заключение и интерпретация
лабораторных данных должны быть сделаны
специалистом-аллергологом
на
основании
сопоставления результатов лабораторных исследований
с клинической картиной и данными аллергологического
анамнеза
53. Все большее значение в современной аллергодиагностике приобретает концепция “батарейного скрининга “ Использует варианты
иммуноблотинга,хемилюминесцентного анализа
54.
Аллерготест МАСТМНОЖЕСТВЕННАЯ ДИАГНОСТИКА АЛЛЕРГИИ С ПРИМЕНЕНИЕМ
ХЕМИЛЮМИНЕСЦЕНТНОГО АНАЛИЗА (МАSТ-CLA)
Компания "Люминери" - официальный и эксклюзивный дистрибьютор по
России и СНГ компании "Хитачи Кемикал Диагностикс Инк." (США) - мирового
лидера в области диагностики, лечения и профилактики аллергии.
Компания "Хитачи Кемикал Диагностикс Инк." (США) представляет в России
один из самых чувствительных на сегодняшний день хемилюминесцентных
методов в определении специфических IgE - множественный
аллергосорбентный тест с применением хемилюминесцентного анализа (MASTCLA) или аллерготест МАСТ.
Аллерготест МАСТ имеет несомненные преимущества перед другими методами
аллергодиагностики in vitro; малый объем сыворотки (0,75 мл), позволяющий
одномоментно определить до 36 аллергенов, безопасность и достоверность
хемилюминесцентной технологии анализа, высокая специфичность и
чувствительность, быстрота воспроизводства, большой спектр исследуемых
аллергенов.
55.
Преимущества аллерготеста МАСТ:абсолютная безопасность для пациента и врача;
возможность широкого применения в педиатрии;
наивысшая точность и достоверность результата
благодаря хемилюминесцентной технологии анализа;
простота, легкость и надежность в обращении
(отсутствие плашек, пробирок);
полностью автоматическое исследование MAСT-панелей
в люминометре CLA-1 с распечаткой информации в
удобной форме;
возможность производства единичных исследований
(одна панель для одного пациента) без удорожания
теста;
удобное сочетание аллергенов в российских МАСТпанелях;
56.
Сущностьаллерготеста
МАСТ заключается в проведении
реакции аллергенспецифический IgE с
последующей
меткой
образовавшегося
комплекса
фотореагентом и определение его
свечения, интенсивность которого
пропорциональна
концентрации
специфического IgE в сыворотке
пациента.
57.
58. Фирма RIDA панели -панели Фирма Qwantiscan-панели На основе ИФА и иммуноблота-сорбция на нитроцеллюлозную пленку
Фирма RIDA панели -панелиФирма Qwantiscan-панели
На основе ИФА и иммуноблотасорбция на нитроцеллюлозную
пленку
59.
60.
ImmunoCAPИдея технологии заключается в возможности обнаружения
сверх низких концентраций IgE-антител в сверх малом
количестве крови которые указывают на определенную болезнь
и/или состояние человека.
Технически это реализуется путем использования специального
вспененного
материала,
производного
бромцианактивированной
целлюлозы.
Благодаря
своей
пористой структуре, материал имеет большую поверхность
взаимодействия и обеспечивает высокую связывающую способность с нанесенным на него антигеном или антителом.
Поверхность взаимодействия такого материала в 150 раз больше
внутренней
поверхности
обычной
пробирки.
61.
62.
63.
Для использования в автоматических установках, хранения и маркированияэтот материал помещают в миниатюрный специальный открытый
пластмассовый колпачок - CAP. Колпачок сделан таким образом, что
специальная система промывки позволяет за несколько секунд получить
полное отделение несвязанного вещества от пористого материала. Все
вместе обеспечивает высокую точность исследований, воспроизводимость и
быстроту выполнения. Колпачки собраны один в другой и помещены в
специальный футляр-держатель, похожий на фломастер - ImmunoCAP
Carrier Колпачки, размещенные в герметичном футляре-держателе,
надежно защищены от пыли, грязи и высыхания. Их удобно хранить в
холодильнике и использовать в оборудовании. Система ImmunoCAP (UniCAP)
100 автоматически извлекает из футляра-держателя необходимое количество
колпачков, а системы ImmunoCAP (UniCAP) 1000 и ImmunoCAP 250 имеют
небольшой встроенный автоматизированный склад для размещения
футляров-держателей. Более того, помимо удобной текстовой и цветовой
маркировки, на каждый футляр нанесен штрих-код, который считывается
системой
для
идентификации
содержимого
футляра-держателя.
64.
65.
Технологияведущего
мирового
производителя в данной области
«Pharmacia Diagnostics AB» (создатель
метода RAST®), которая отмечена как
золотой стандарт аллергодиагностики
Всемирной
Организацией
Здравоохранения
и
согласно
независимым исследованиям является
наиболее точной и стабильной.
ImmunoCAP рекомендован FDA с 2001
г. для точной диагностики аллергии.
66.
67.
• ImmunoCAP ® Phadia - ТриптазаМаркер дегрануляции тучнйых клеток
• Повышение уровня триптазы в крови
указывает на активацию тучных клеток
• фактор риска острых аллергических реакций.
Временное повышение уровня служит
клиническим маркером, подтверждающим
тяжелые реакции, такие как анафилаксия.
• Увеличение базального уровня служит
маркером риска развития анафилактических
реакций, например, после укуса пчел / ос или
введения лекарствв
68. Триптаза-новый скрининговый маркер Увеличение базового уровня Триптазы – фактор риска развития острых аллергических реакций
Пациенты зоны риска развития острых реакций приконтакте с ядом насекомых и лекарственными
препаратами
Увеличение базового уровня Триптазы указывает на
активацию тучных клеток и может служить фактором
риска острых реакций при хирургических манипуляциях
Триптазу необходимо измерять перед началом
иммунотерапии.
69.
70.
71.
72.
73.
74.
Некоторые виды аллергии (на лекарственные средства, пищевые добавки) очень плохо выявляются кожными тестами илисерологически (sIgE), для них в настоящее время достоверны
только дорогостоящие и опасные провокационные тесты.
CAST –оценка активации базофилов аллергенами in vitro
(иммуноферментный анализ)
компания Buhlmann
Laboratories, Швейцария
Активация базофилов специфическими АлГ
Базофилы и тучные клетки (Тк) играют центральную роль в ГНТ.
При контакте аллергенов (АлГ) с молекулами IgE на
специализированных эффекторных клетках базофилах и Тк
происходит каскад ферментных реакций, приводящий к
дегрануляции и высвобождению медиаторов из гранул
г
75.
Тест стимуляции базофилов in vitro – CAST.Технология CAST (Cellular Antigen Stimulation Test, тест антигенной
стимуляции клеток) основана на определении ЛТ (LTC4, LTD4, LTE4),
секретируемых примированными IL-3 базофилами под действием АлГ in vitro. Его также называют провокационным тестом in vitro.
обладает высочайшей специфичностью по сравнению с классическим тестом высвобождения гистамина.
Исследование включает три этапа: выделение популяции лимфоцитов из
стабилизированной ЭДТА крови (кровь стабильна 24 часа при температуре 2-8°C!), стимуляция суспензии лимфоцитов специфическими АлГ и
иммуноферментное определение концентрации синтезированных
базофилами во время стимуляции ЛТ
Компанией Buhlmann Laboratories также был разработан цитометрический
вариант теста стимуляции
базофилов – FLOW-CAST®.
•
76.
77.
Тест высоко чувствителени специфичен для выявления аллергических реакций:
• на лекарства (бета-лактамные антибиотики, аспирин и другие
нестероидные противовоспалительные средства, миорелаксанты и т.д.)
• на латекс
• на яды насекомых
• на ингаляционные аллергены
• на пищевые добавки
• для выявления пищевой непереносимости
• у пациентов, у которых проведение кожных тестов затруднено:
пациенты с аллергодерматозом или получающие терапию
антигистаминными, кортикостероидными препаратами, дети с низким порогом кожной
чувствительности и беременные с
неспецифической кожной чувствительностью
78.
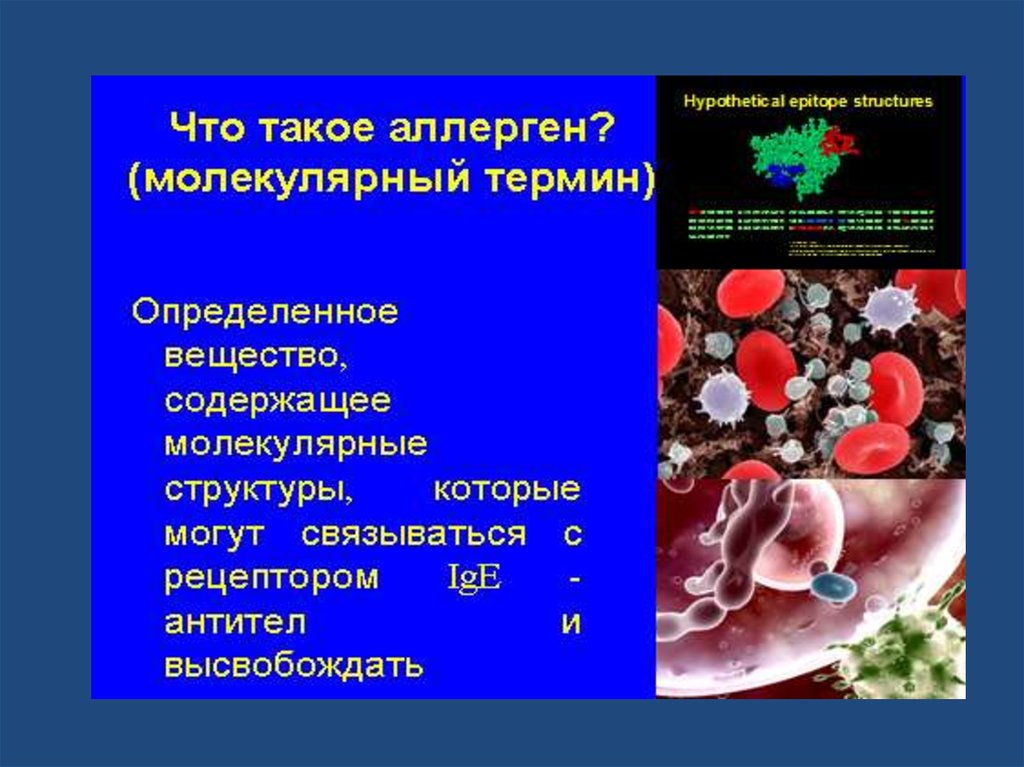
Молекулярныйдиагностики
уровень
Компонентная аллергодиагностика –новые подходы
Рекомбинантные аллергены открывают большие
перспективы диагностики кмолекулярным
компонентам. С их помощью
возможно определение сенсибилизациипациента к
полному аллергенному
профилю, включающему как аллергенные компоненты,
вызывающие заболевание, таки перекрестнореагирующие. Компонентная
аллергодиагностика – революционное
направление аллергологии.
79.
80.
81.
82.
Рекомбинантные аллергены – это аллергенные молекулы,полученные
методом генной инженерии, первоначально выделенные из
аллергенного экстракта. Большинствосуществующих рекомбинантных
аллергенов экспрессированы в клетке Esherichia coli, и по своим
структурными
иммунологическим
свойствам
полностью
соответствуют
натуральным
протеинам.
Другие
высокотехнологические системы основаны на воспроизведении
рекомбинантных аллергенов в дрожжевой,
бактериальной или инсектной клетке.
Рекомбинантные аллергены обладаюттем же специфичным
свойством к
индукции IgE-антител, что и компоненты натуральных экстрактов и
обычно
демонстрируют высокую чувствительностьи специфичность в тестах in
vitro и in vivo.
Сегодня множество аллергенных молекул из различных натуральных
источниковаллергенов могут быть клонированы, секвинированы и
экспрессированы как рекомбинантные аллергены.
83.
Новые возможности с рекомбинантными аллергенамиДиагностические инструменты будущего уже сейчас
Современные технологии позволяют не только
определить структуру аллергенных протеинов, но и
получить их в больших количествах с использованием
методов генной инженерии.
Использование рекомбинантных аллергенов в тестах in
vitro открывает новые возможности для создания более
качественных тестов и предлагает новые инструменты
для решения клинических и иммунологических
вопросов. Рекомбинантные аллергены открывают
новые перспективы для диагностики IgE
опосредованных реакций.
84.
Революционное направлениев аллергологии –
биочипы
Биочиповая технология позволяет одновременно
проводить
высокоспецефический анализ
большого количества определенных маркеров
(антител, антигенов, ферментов и их субсттратов
на небольшой ограниченной матрице )
Биочиповая технология универсальна
Биочип-небольшого размера матрица с набором
иммобилизированных спотов
(микроточек) - образцов биологически активных
веществ (антигенов, антител, аллергенов и т.д.)
85.
Разработаныавтоматические
устройства для считывания чипов
–споттеры
Основное преимущество белковых
биочипов
по
сравнению
с
традиционными ИФА и иммунным
блотингом является возможность
раздельного определения множества
интересующих
маркеров
с
использованием
минимального
количества исследуемого образца
86.
В составе специфических аллергенов, например, пыльцы березы,сейчас возможно идентифицировать наиболее активные белковые
компоненты, вызывающие индукцию IgE антител и аллергические
симптомы.
Таким образом, тесты in vitro, с использованием рекомбинантных
аллергенов – это важнаяинформация о триггерных стимулах на
молекулярном
уровне.
Исследование
реактивности
к
рекомбинантным аллергенам дает возможность изучать более
сложные популяционные явления, такие как географические
различия в IgE-опосредованной чувствительности и перекрестные
реакции между различными
аллергенами.
87.
Компоненты аллергена пыльцы березыBet v 1
PR-10 protein Патогенреактивный
протеин
Bet v 2 Профилин
Актин-связывающий протеин
Bet v 3 4 EF- Кальций-связывающий протеин
Bet v 4 2-ЕF- кальций связывающий белок,
полькальцин
Bet v 6 Изофлавоновая редуктаза
Bet v 7 Циклофилин
88.
Традиционный тестна аллергию выявляет
источник аллергена, например, пыльцу березы. Но
этот сложный аллерген включает несколько
аллергенных компонентов.
Использование
рекомбинантных аллергенов позволяет выявить
сенсибилизацию к компонентам (специфичным
белкам)
89.
Возможность высокоспецифической диагностики,объективные критерии для назначения специфической
иммунотерапии (СИТ).
Тесты с рекомбинантными аллергенами открывают новые возможности
прогнозирования, будет ли назначение СИТ эффективным или нет, и
назначения адекватной терапии. Если аллергические реакции у
пациента обусловлены сенсибилизацией к основному компоненту
аллергена (например, Bet v 1 пыльцы березы), с высокой степенью
вероятности можно прогнозировать высокий терапевтический эффект от
СИТ с экстрактом пыльцы березы, который будет содержать
высокую концентрацию этого компонента.
С другой стороны, если пациент чувствителен к другому, не к главному
компоненту аллергена (например, к Bet v 2 или Bet v 4 пыльцы березы),
иммунотерапия с экстрактом, возможно, содержащим Bet v 1
будет недостаточно эффективной. Есть также опасения, что СИТ с
аллергенными компонентами, к которым пациент не чувствителен, может
вызвать развитие новой сенсибилизации, что скорее ухудшит симптомы,
чем устранит их.
90.
Phadia – идет впередиРазработки в области исследования реактивности к рекомбинантным
аллергенам проводились в компании Phadia в течение
многих лет. В испытаниях использовали, как очищенные натуральные
аллергенныекомпоненты, так и рекомбинантные аллергены.
Более 10 лет назад были запущеныисследования с первыми
рекомбинантнымиаллергенами, после чего количество
компонентов для диагностики in vitro
неуклонно растет.
Компонентная аллергодиагностика – новые революционные подходы к
диагностике аллергических заболеваний
Рекомбинантные аллергены открывают большие перспективы
диагностики к молекулярным компонентам. С их помощью
возможно определение сенсибилизации пациента к полному
аллергенномупрофилю, включающему как аллергенные
компоненты, вызывающие заболевание, таки перекрестно-реагирующие.
91.
12
3
92.
Компонентнаяаллергодиагностика –
революционное
направление
аллергологии.





















































































 medicine
medicine