Similar presentations:
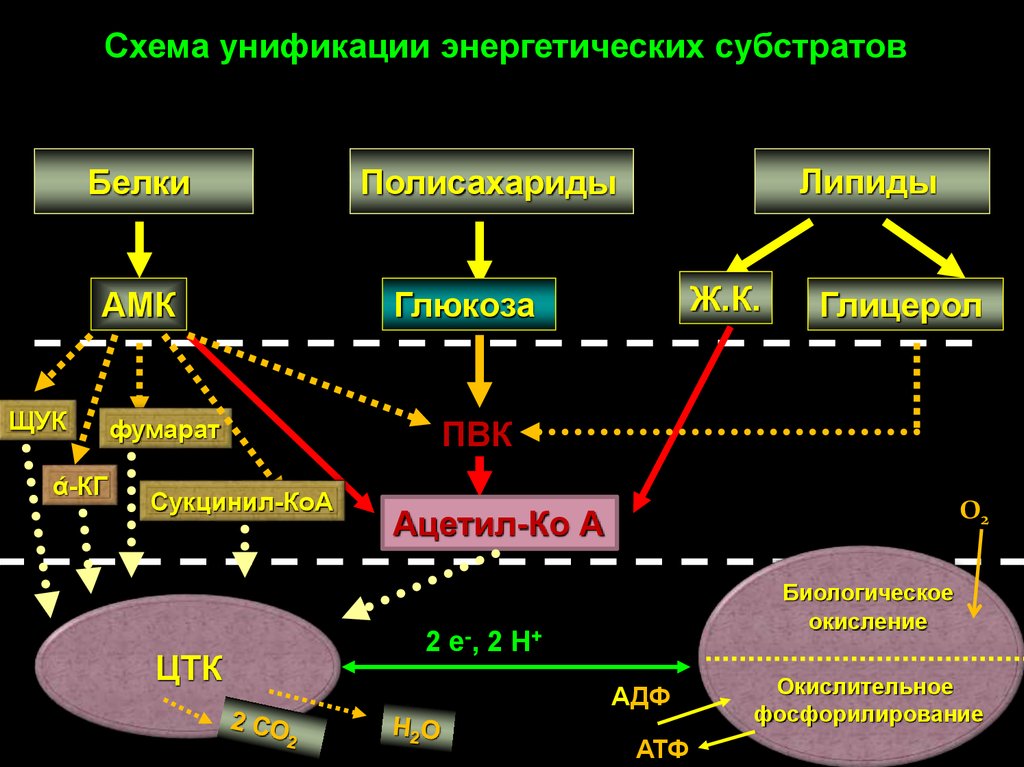
Схема унификации энергетических субстратов
1.
Схема унификации энергетических субстратовБелки
АМК
ЩУК
ά-КГ
фумарат
Сукцинил-КоА
ЦТК
Липиды
Полисахариды
Ж.К.
Глюкоза
Глицерол
ПВК
О2
Ацетил-Ко А
Биологическое
окисление
2 е-, 2 Н+
АДФ
АТФ
Окислительное
фосфорилирование
2.
БИОЛОГИЧЕСКОЕ ОКИСЛЕНИЕIn vivo
S
½ О2
SН2 ДГ
→НАДН•Н+ → Н2О
Е
Тепло 60%
АТФ 40%
Синтез АТФ
3.
МатриксВнутренняя
мембрана
Рибосомы
Наружная
мембрана
Межмембранное пространство
Кристы
4. Современная теория биологического окисления
1.Путем отнятия водорода от окисляемого
субстрата – митохондриальное окисление
и внемитохондриальное окисление
оксидазного типа
2.
Путем присоединения кислорода к
окисляемому субстрату –
внемитохондриальное окисление
оксигеназного типа (старое название
микросомальное окисление)
5. Типы окисляемых субстратов
1. Субстраты 1 типа (углеводородные) – сукцинат, ацетил-КоА. ∆G = 150 кДж/моль. Это меньше, чем энергия е- в
НАДН. Поэтому НАД не может участвовать в
дегидрировании этих субстратов.
2. Субстраты 2 типа (спиртовые) – при их дегидрировании
возникают кетоны. ∆G = 200 кДж/моль, следовательно,
НАД может участвовать в дегидрировании этих
субстратов.
3. Субстраты 3 типа (альдегидные) – энергия отщепления
пары е- около 250 кДж/моль. Дегидрогеназы субстратов 3
типа часто содержат несколько коферментов. При этом
часть энергии запасается до ЦПЭ.
В зависимости от типа субстрата окисления (т.е.
энергии отщепления пары е-) выделяют полную и
укороченную ЦПЭ.
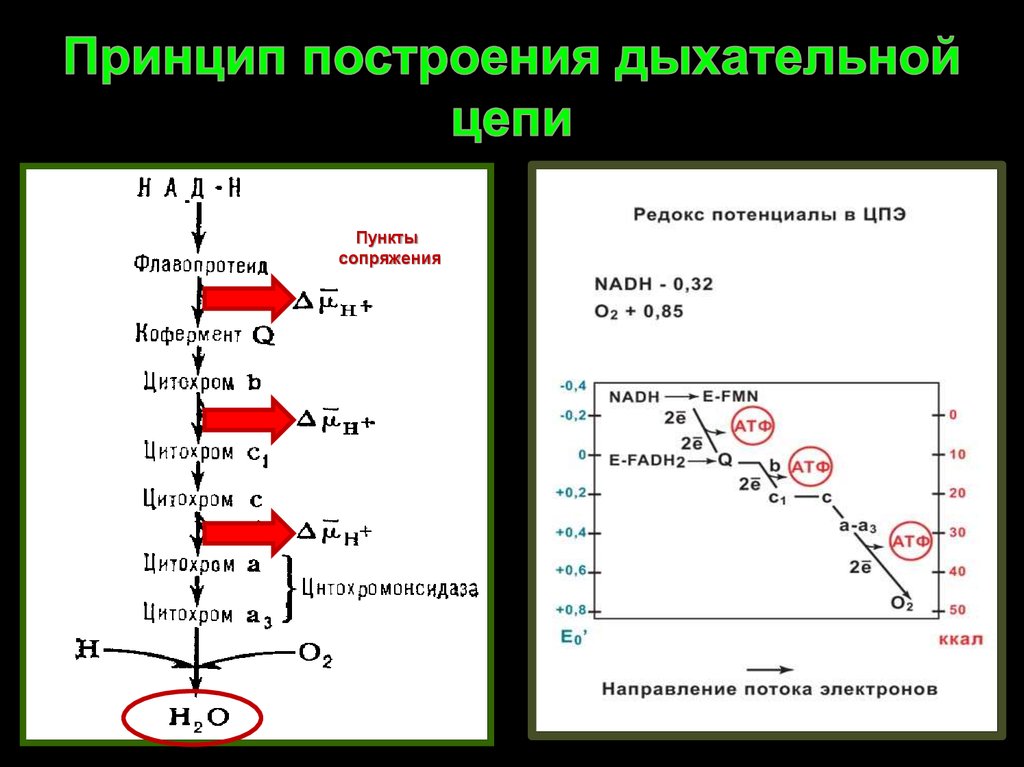
6. Принцип построения дыхательной цепи
Пунктысопряжения
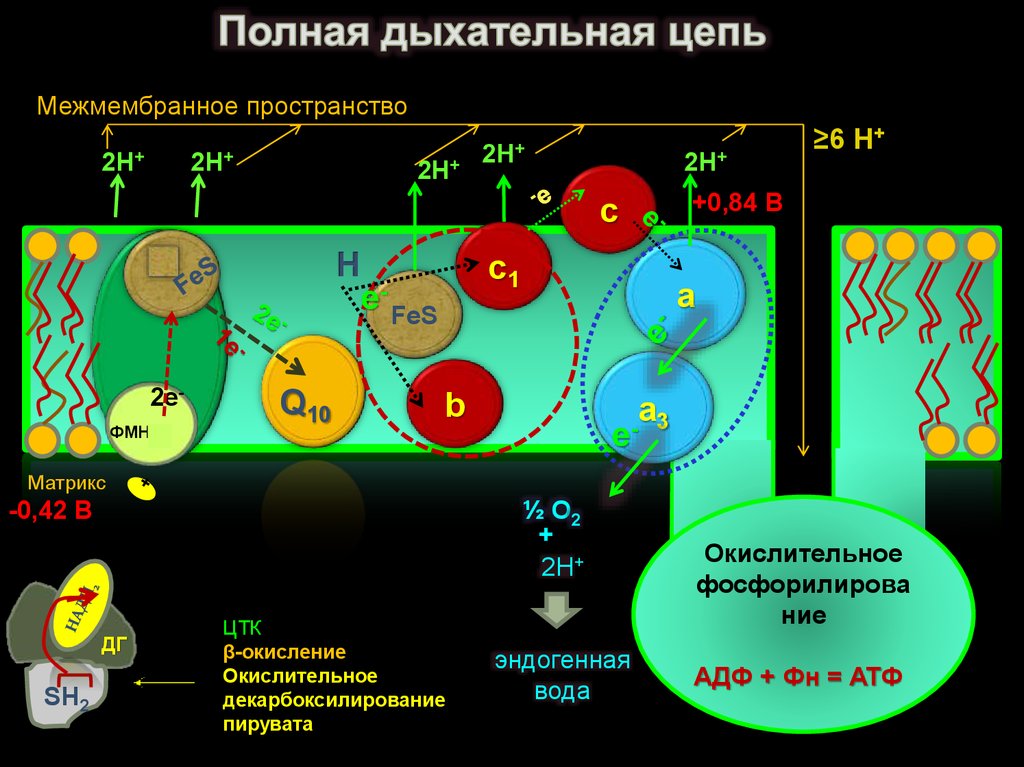
7. Полная дыхательная цепь
1.2.
3.
4.
Комплекс I – НАДН-КоQ (убихинон) –
оксидоредуктаза, обеспечивает передачу е- от
НАДН+Н+ к убихинону (Ко-Q)
Комплекс II – сукцинат –КоQ – оксидоредуктаза,
катализирует перенос е- от сукцината (ацилов ЖК) на
Ко-Q
Ферментный комплекс III – Ко-Q Н – цитохром с –
оксидоредуктаза (комплекс bc), передает е- от Ко-Q Н
на цитохром с
Ферментный комплекс IV – цитохромоксидаза,
катализирует перенос е- от цитохрома с на О2. В этот
комплекс входят цитохром а и а3, содержащие 2 гема
и 2 иона Cu2+.
8. Полная дыхательная цепь
Межмембранное пространство2Н+
2Н+
2Н+
2Н+
2Н+
c
Н
е- FeS
2еФМНН2
Q10
c1
≥6 Н+
+0,84 В
a
b
a3
е
Матрикс
-0,42 В
½ О2
+
2Н+
ДГ
SH2
ЦТК
β-окисление
Окислительное
декарбоксилирование
пирувата
эндогенная
вода
Окислительное
фосфорилирова
ние
АДФ + Фн = АТФ
9. Принцип построения дыхательной цепи
Последовательность переносчиков определяется их способностью отдаватьэлектроны окислителю, т.е. стандартным восстановительным потенциалом Е0
(редокс-потенциалом).
Редокс-потенциал численно равен Э.Д.С. в вольтах, возникающей в
полуэлементе между растворами окислителя и восстановителя, взятыми в 1 М
концентрации при стандартных условиях (рН=7,0; t=250 С).
В качестве стандарта принят ОВП реакции:
Н2 → 2Н+ + е- ; ОВП = - 0,42
В дыхательной цепи все реакции направлены по термодинамической
лестнице от компонента с самым отрицательным редокс-потенциалом НАДН (0,32 В) к кислороду, имеющему самый положительный редокс-потенциал (+ 0,82).
При прохождении 2е- по ЦПЭ падение редокс-потенциала составляет 1,14 В:
((0,82 – (-0,32) = 0,82 + 0,32 = 1,14 В)
Это соответствует изменению
– 220 кДж.
стандартной свободной энергии,
равному
Для синтеза 1 молекулы АТФ необходимо ≈ 32 кДж. Для этого достаточной
является разность потенциалов между окислителем и восстановителем ≥ 0,2 В.
Б. Чанс установил, что таких участков (где разность потенциалов ≥ 0,2 В) в
ЦПЭ три. Эти участки были названы им
пунктами сопряжения и
фосфорилирования. Эти участки соответствуют I. III и IV комплексам.
10. Дыхательная цепь
Это последовательность переносчиков электронов на кислород,локализованная во внутренней мембране митохондрий
Активные формы витамина В2 –
ФМН, ФАД
Атомы Fe2+, Сu2+ в составе
цитохромов
Цитохромы (различаются по строению гема)
переносят только электроны
Fe3+ + е- → Fe2+
Сu2+ + е- → Сu+
b → С1 →С → а→ а3
Железосерные белки (FeS – белки)
Содержат негемовое железо;
переносят только электроны
Убихинол (Ко-Q) –
жирорастворимый переносчик
е- и Н+
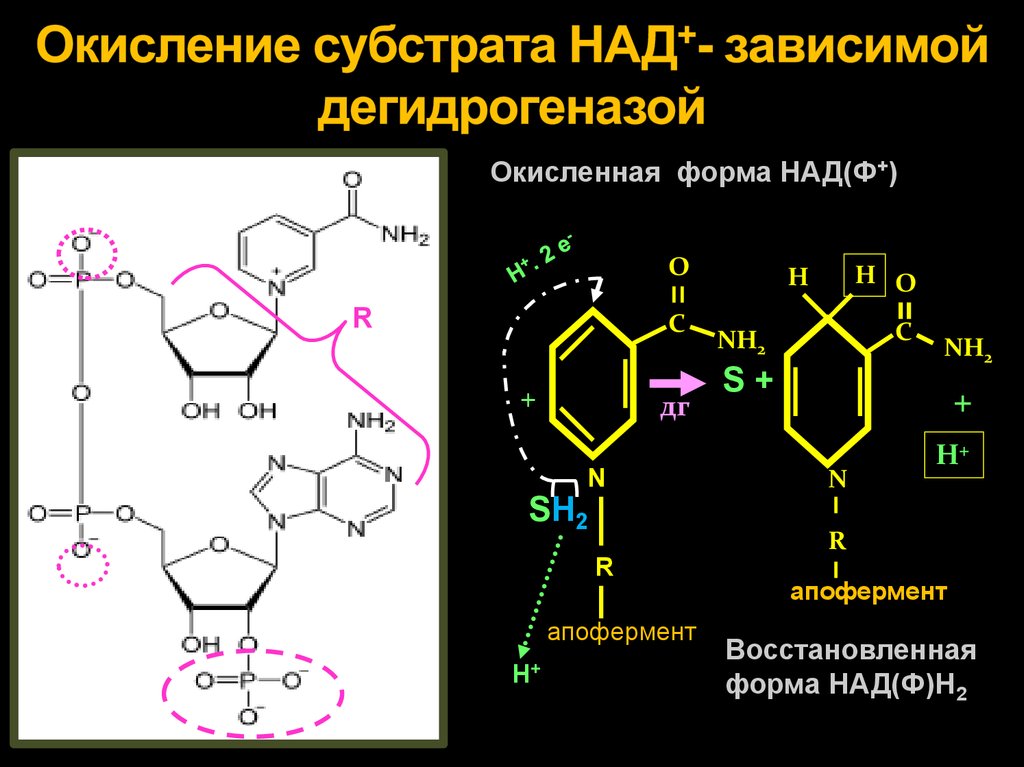
11. Окисление субстрата НАД+- зависимой дегидрогеназой
Окисленная форма НАД(Ф+)О
R
С
+
дг
N
SH2
С
NH2
S+
NH2
+
N
H+
R
R
апофермент
H+
Н О
H
апофермент
Восстановленная
форма НАД(Ф)Н2
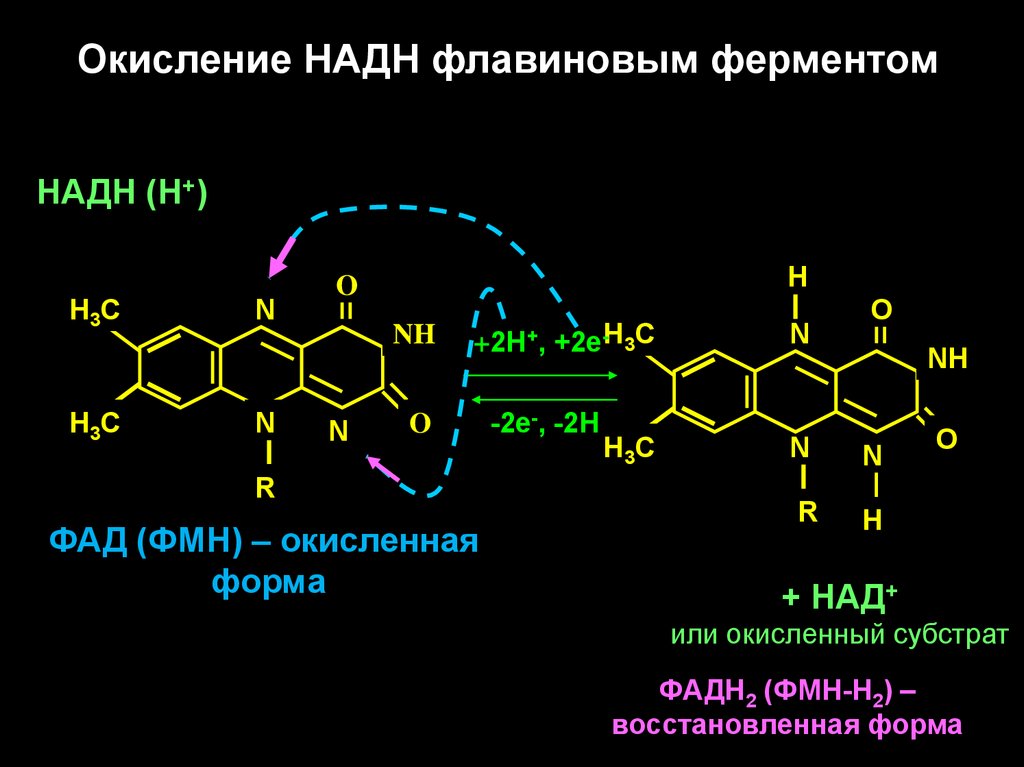
12.
Окисление НАДН флавиновым ферментомНАДН (Н+)
Н 3С
Н 3С
N
N
Н
O
NH
N
+2Н+, +2е-Н3С
O
R
ФАД (ФМН) – окисленная
форма
-2е-, -2Н
Н 3С
N
O
NH
N
N
R
Н
O
+ НАД+
или окисленный субстрат
ФАДН2 (ФМН-Н2) –
восстановленная форма
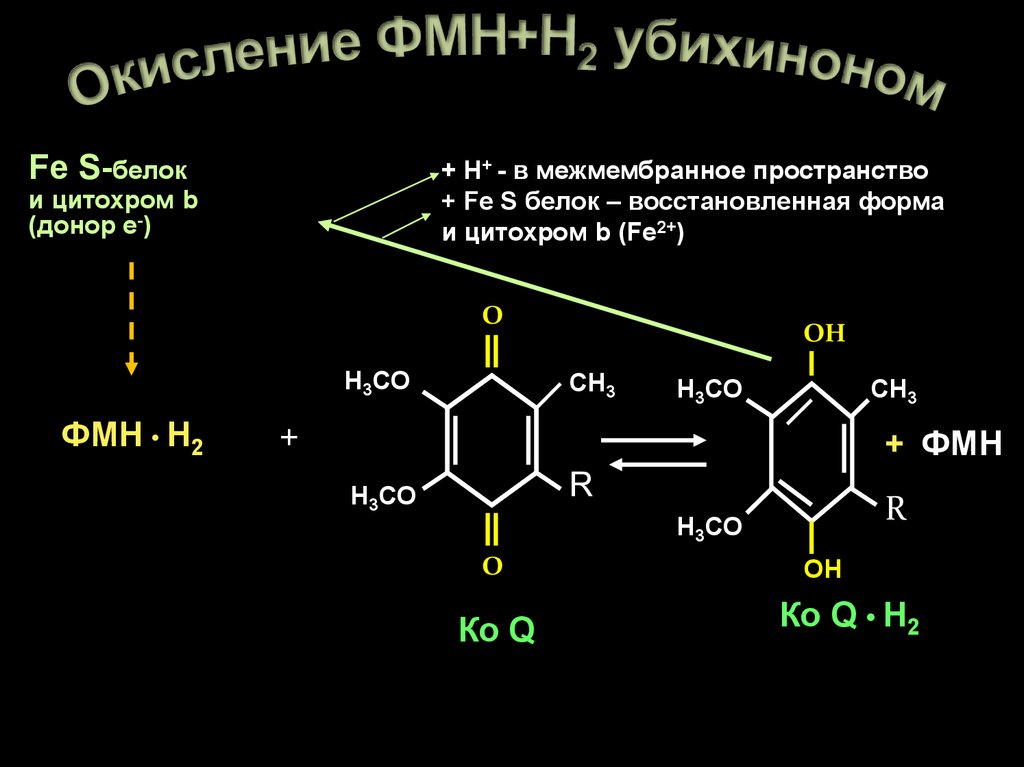
13. Окисление ФМН+Н2 убихиноном
Fe S-белок+ Н+ - в межмембранное пространство
+ Fe S белок – восстановленная форма
и цитохром b (Fe2+)
и цитохром b
(донор е-)
О
Н3СО
ФМН • Н2
ОН
СН3
Н3СО
СН3
+
+ ФМН
R
Н3СО
R
Н3СО
О
Ко Q
ОН
Ко Q • Н2
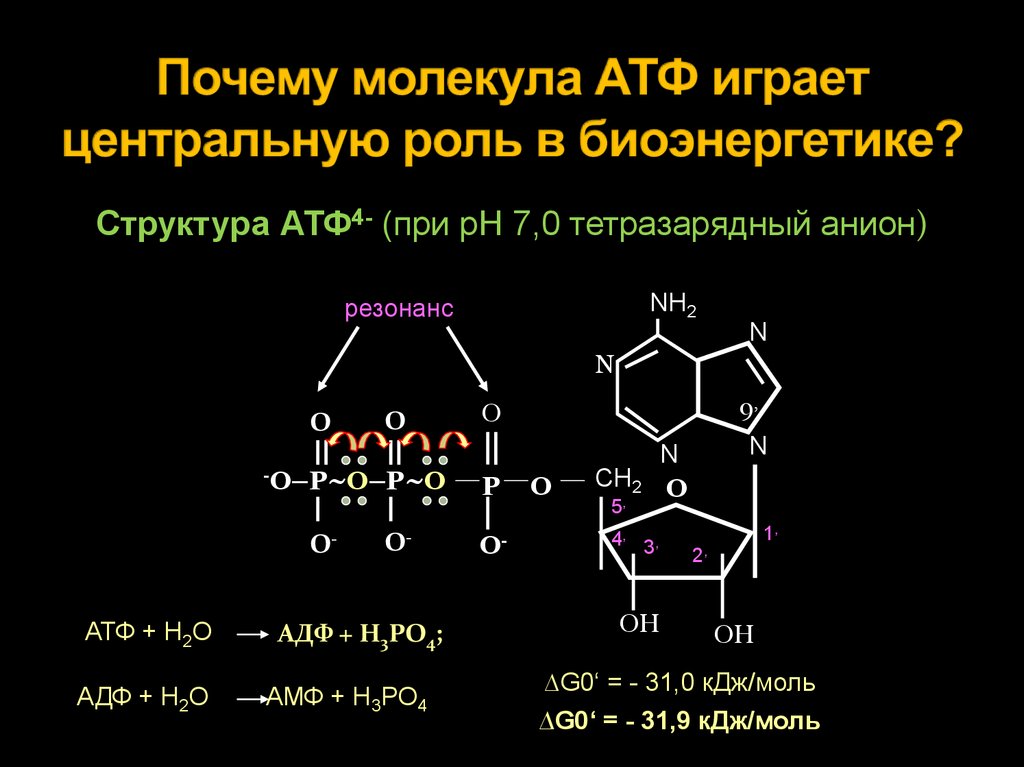
14. Почему молекула АТФ играет центральную роль в биоэнергетике?
Структура АТФ4- (при рН 7,0 тетразарядный анион)NH2
резонанс
N
N
О
О
~О–Р~О
-О–Р
ОАТФ + Н2О
АДФ + Н2О
О-
АДФ + Н3РО4;
АМФ + Н3РО4
9,
N
О
Р
О-
О
СН2
5,
4, 3,
ОН
N
О
1,
2,
ОН
∆G0‘ = - 31,0 кДж/моль
∆G0‘ = - 31,9 кДж/моль
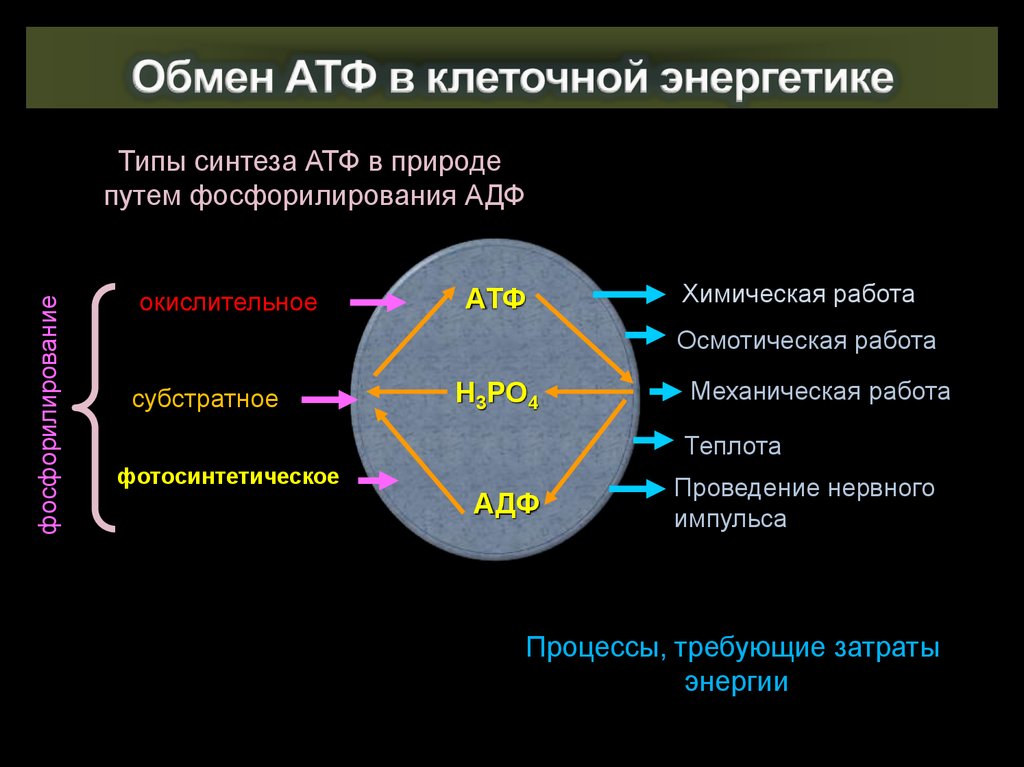
15. Обмен АТФ в клеточной энергетике
фосфорилированиеТипы синтеза АТФ в природе
путем фосфорилирования АДФ
окислительное
АТФ
Химическая работа
Осмотическая работа
субстратное
Н3РО4
Механическая работа
Теплота
фотосинтетическое
АДФ
Проведение нервного
импульса
Процессы, требующие затраты
энергии
16. Окислительное фосфорилирование – это синтез АТФ из АДФ и неорганического фосфата, сопряженный с переносом протонов и электронов
17. Окислительное фосфорилирование
Это сопряжение двух клеточных процессов:1. Экзергонической реакции окисления
восстановительных молекул (НАДН•Н+ или
ФАДН2)
2. Эндергонической реакции
фосфорилирования АДФ и образования АТФ.
О.Ф. происходит в митохондриях. Процесс
может происходить только в аэробных условиях
с участием ферментов ЦПЭ и АТФ-синтазы
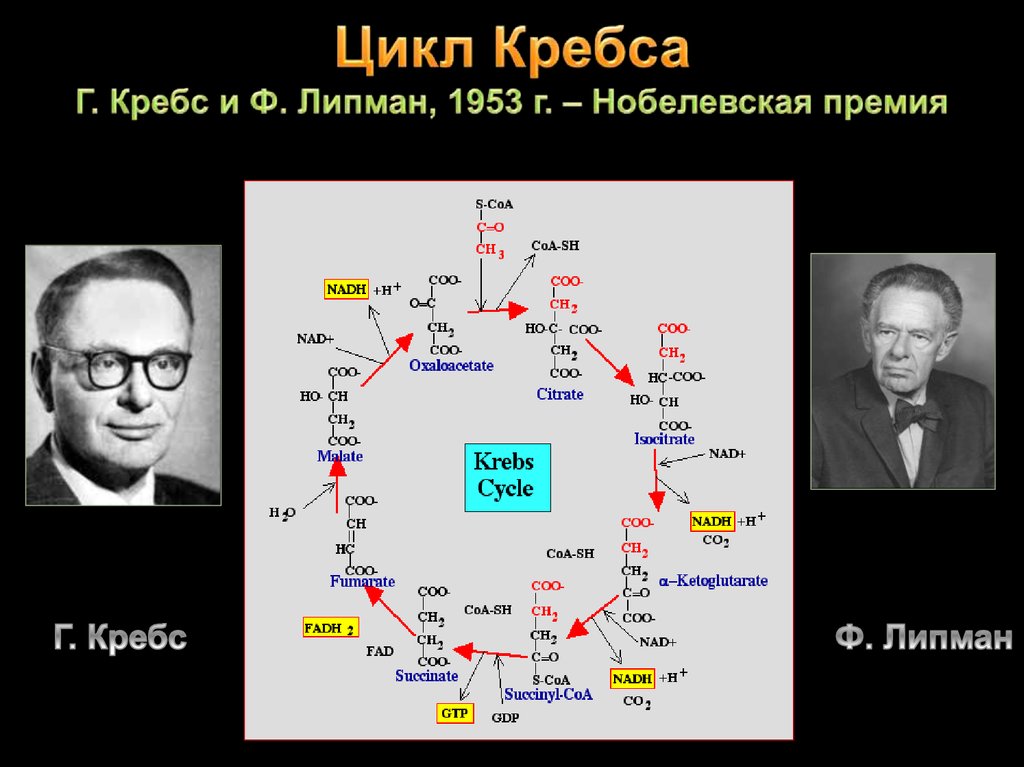
18. Цикл Кребса Г. Кребс и Ф. Липман, 1953 г. – Нобелевская премия
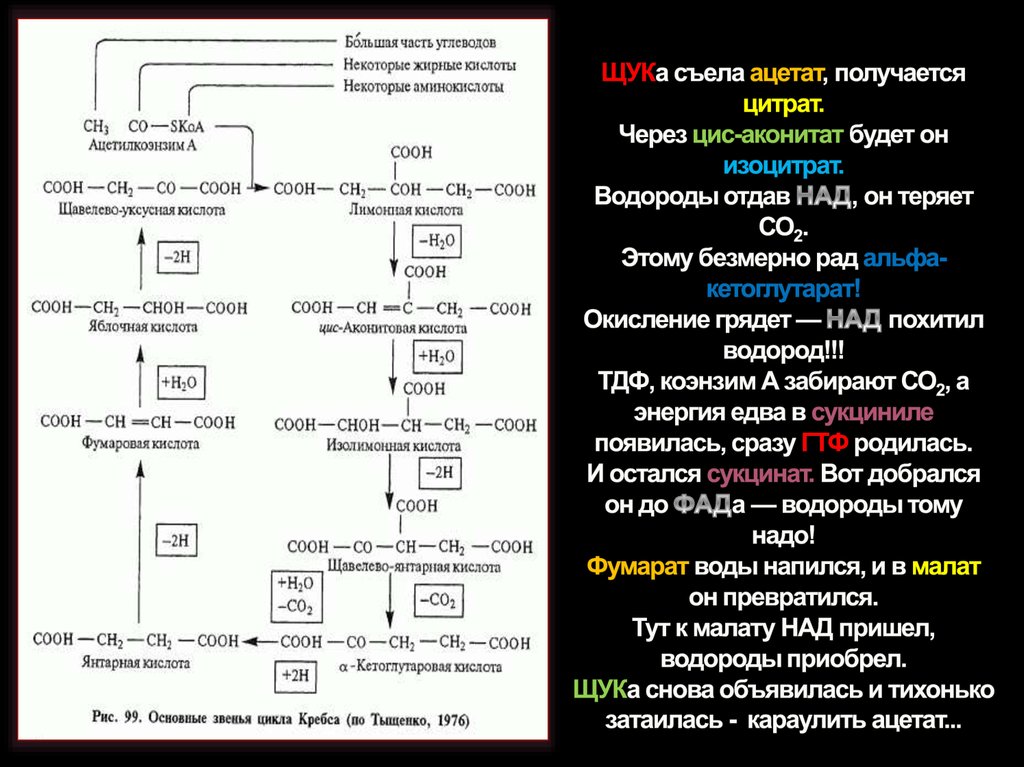
19. ЩУКа съела ацетат, получается цитрат. Через цис-аконитат будет он изоцитрат. Водороды отдав НАД, он теряет СО2. Этому безмерно
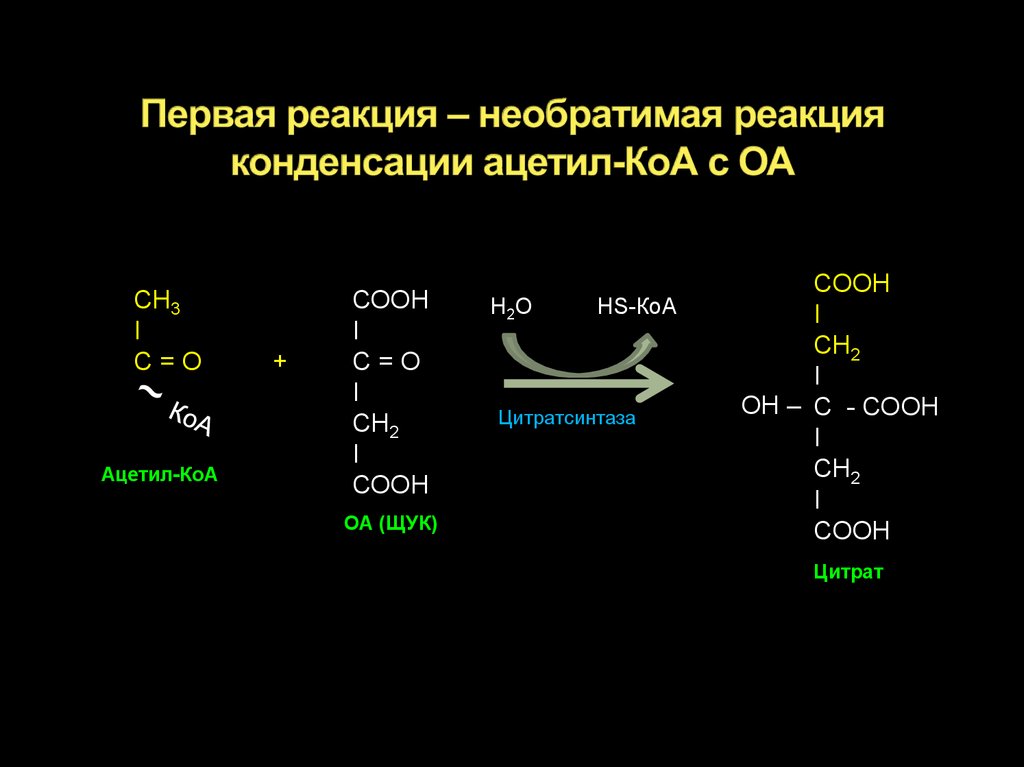
20. Первая реакция – необратимая реакция конденсации ацетил-КоА с ОА
СН3I
С=О
Ацетил-КоА
+
СООН
I
С=О
I
СН2
I
СООН
ОА (ЩУК)
Н2О
HS-КоА
Цитратсинтаза
СООН
I
СН2
I
ОН – С - СООН
I
СН2
I
СООН
Цитрат
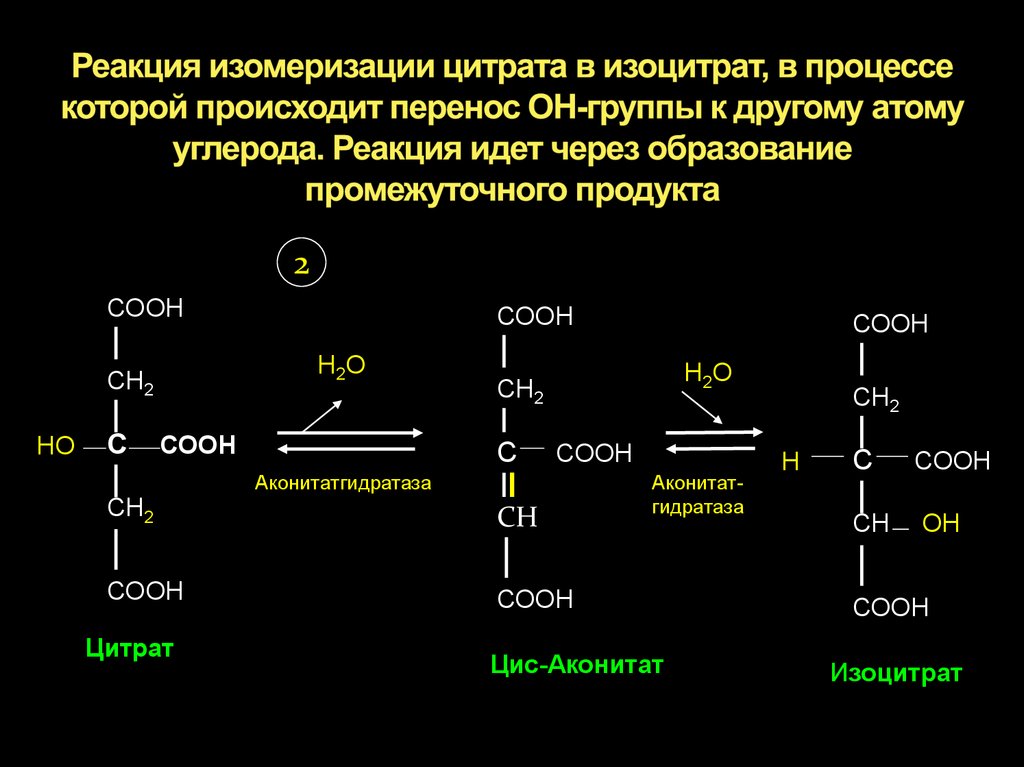
21. Реакция изомеризации цитрата в изоцитрат, в процессе которой происходит перенос ОН-группы к другому атому углерода. Реакция
2СООН
Н2О
СН2
НО
С
СООН
СООН
СН2
СООН
Цитрат
СООН
Н2О
СН2
С
СООН
Аконитатгидратаза
СН
Аконитатгидратаза
СООН
Цис-Аконитат
СН2
Н
С
СООН
СН
ОН
СООН
Изоцитрат
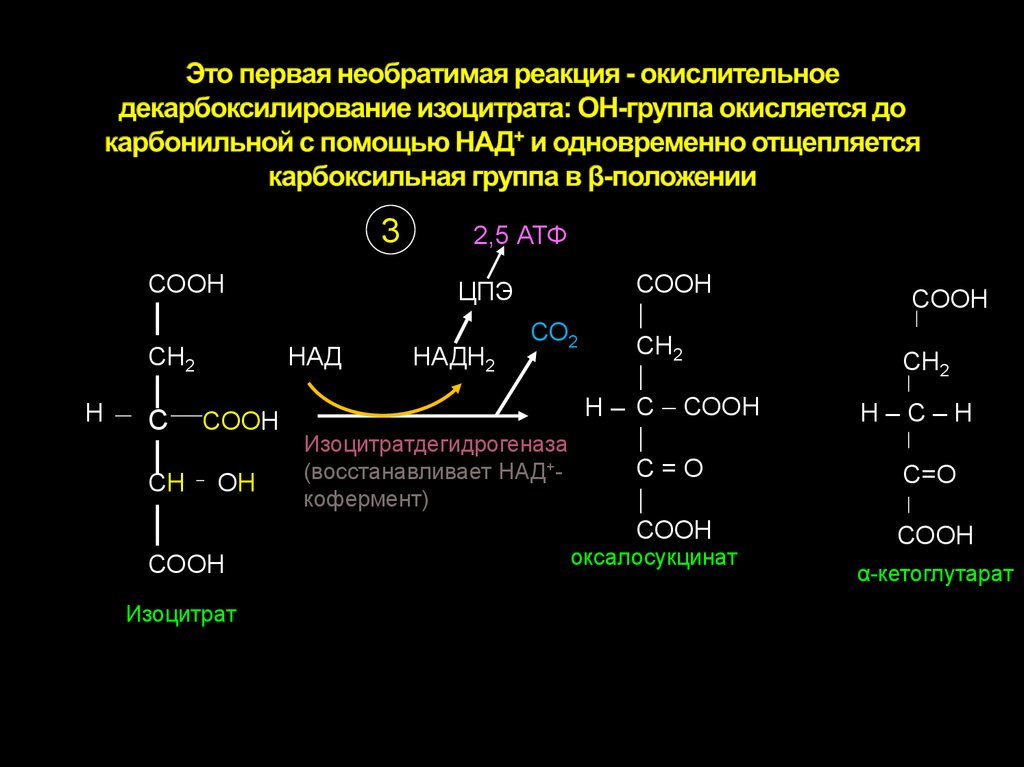
22. Это первая необратимая реакция - окислительное декарбоксилирование изоцитрата: ОН-группа окисляется до карбонильной с помощью
3СООН
Н
2,5 АТФ
СООН
|
СО2
СН2
СН2
НАД
НАДН2
|
Н – С – СООН
С СООН
|
Изоцитратдегидрогеназа
С=О
(восстанавливает НАД+СН ОН
кофермент)
|
СООН
оксалосукцинат
СООН
Изоцитрат
ЦПЭ
СООН
СН2
Н–С–Н
С=О
СООН
α-кетоглутарат
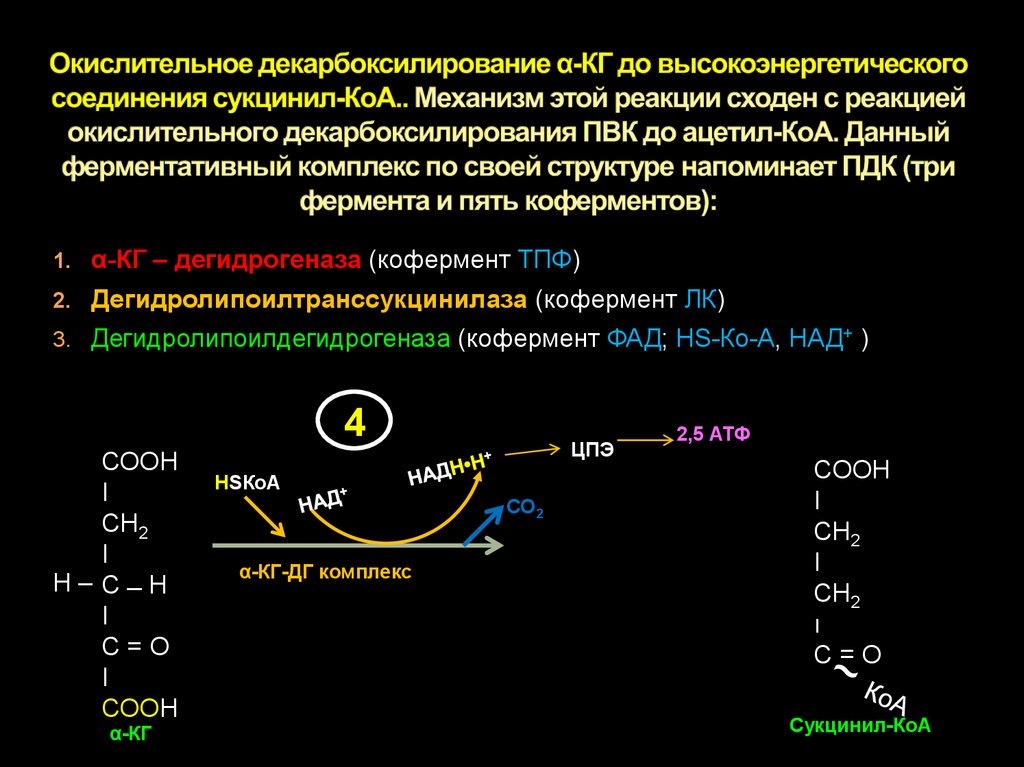
23. Окислительное декарбоксилирование α-КГ до высокоэнергетического соединения сукцинил-КоА.. Механизм этой реакции сходен с
1. α-КГ – дегидрогеназа (кофермент ТПФ)2. Дегидролипоилтранссукцинилаза (кофермент ЛК)
3. Дегидролипоилдегидрогеназа (кофермент ФАД; НS-Ко-А, НАД+ )
4
СООН
I
СН2
I
Н–С ̶ Н
I
С=О
I
СООН
α-КГ
ЦПЭ
НSКоА
СО2
α-КГ-ДГ комплекс
2,5 АТФ
СООН
I
СН2
I
СН2
ı
С=О
Сукцинил-КоА
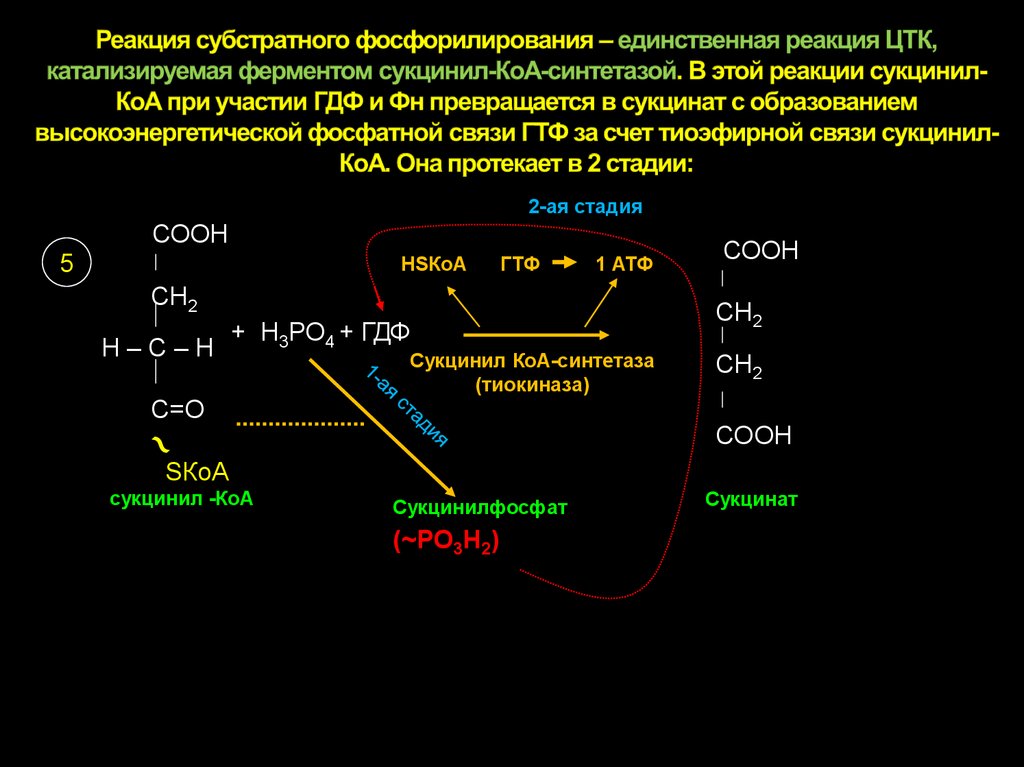
24. Реакция субстратного фосфорилирования – единственная реакция ЦТК, катализируемая ферментом сукцинил-КоА-синтетазой. В этой
2-ая стадияСООН
НSКоА
5
ГТФ
1 АТФ
СН2
Н–С–Н
+ Н3РО4 + ГДФ
С=О
Сукцинил КоА-синтетаза
(тиокиназа)
СООН
СН2
СН2
СООН
SКоА
сукцинил -КоА
Сукцинилфосфат
(~РО3Н2)
Сукцинат
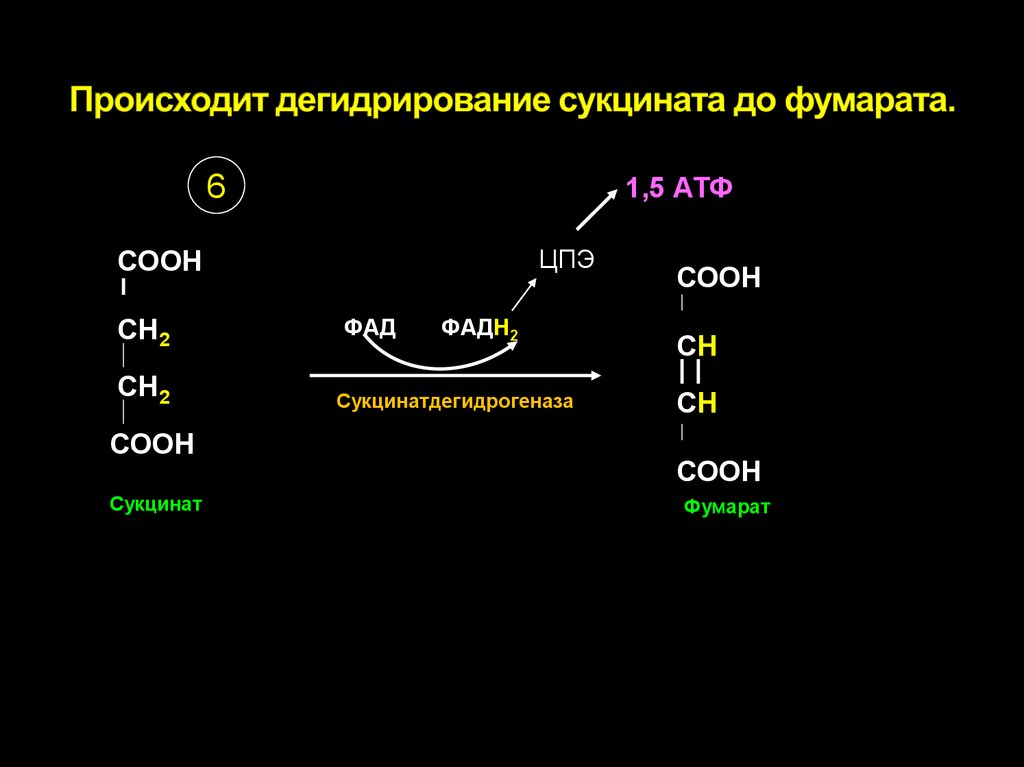
25. Происходит дегидрирование сукцината до фумарата.
1,5 АТФ6
ЦПЭ
СООН
СН2
СН2
СООН
Сукцинат
ФАД
ФАДН2
Сукцинатдегидрогеназа
СООН
СН
СН
СООН
Фумарат
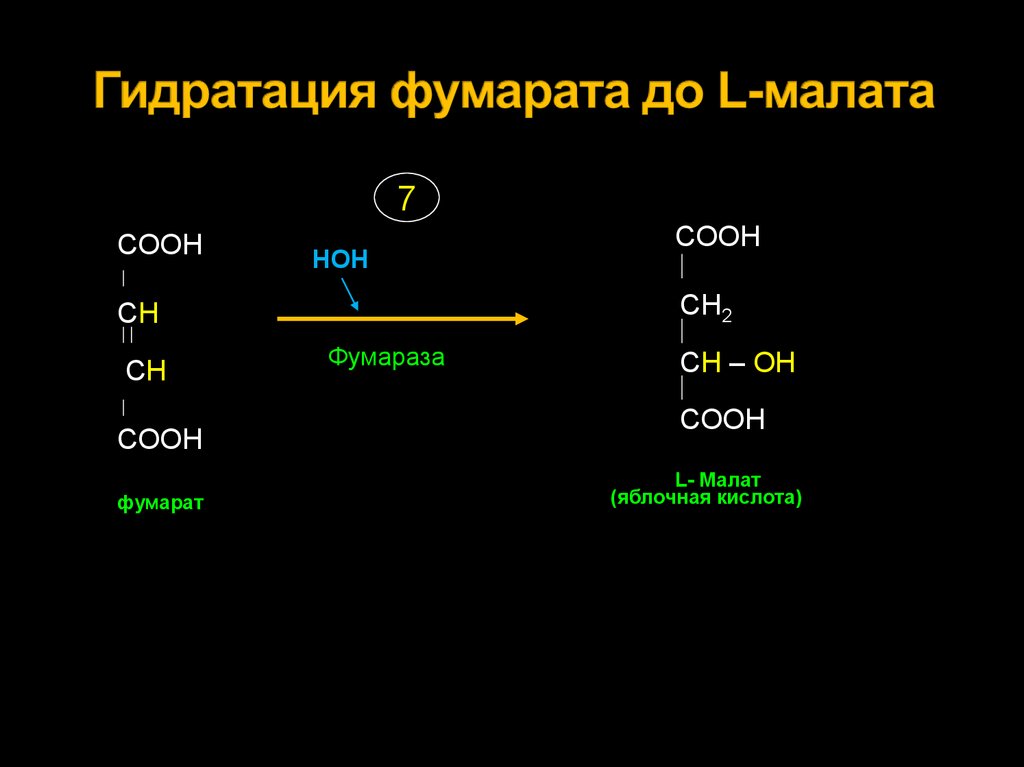
26. Гидратация фумарата до L-малата
7СООН
НОН
СН2
СН
СН
СООН
фумарат
СООН
Фумараза
СН – ОН
СООН
L- Малат
(яблочная кислота)
27. Происходит регенерация оксалоацетата. Под действием НАД+-зависимой малатдегидрогеназы L-малат дегидрируется и превращается в
82,5 АТФ
СООН
СН2
СООН
ЦПЭ
НАД
НАДН2
СН - ОН
Малатдегидрогеназа (МДГ)
СООН
L- Малат
(яблочная кислота)
СН2
С=О
СООН
Оксалоацетат
ЦТК
28. Стехиометрия ЦЛК:
Цикл Кребса:окисляется: 2 «С»-ацетил КоА
поглощается: 2 молекулы Н2О
выделяется: 1 молекула Н2О
2 молекулы СО2
образуется: 3НАДНН+
ЦПЭ
1ФАДН2
ЦПЭ
Энергетический выход цикла Кребса:
3 НАДН2
1 ФАДН2
ЦПЭ
ЦПЭ
2,5 (3) АТФ х3 =8,5 АТФ
1,5 (2) АТФ
5 реакция-субстратное фосфорилирование 1 АТФ
10(12) АТФ
29.
ОКИСЛИТЕЛЬНОЕ ДЕКАРБОКСИЛИРОВАНИЕ α-КЕТОГЛУТАРАТАСООН
I
СН2
ı
Н-С–Н
ı
С=О
I
СООН
R
-
N
C
CН3
S
С
СН2
С
+
СН2
Карбонион ТПФ
α-Кетоглутарат
СООН
I
СО2 СН
2
I
α-Кетоглутарат
R
дегидрогеназа СН
2
I
N C CН3
О
ОН - С – С
ı
S C СН2 СН2
Р
ı
ı
|
Н
О
О
|
Р
Гидроксиэтилтиамин пирофосфат
l
Р
I
О
I
Р
30.
СООНI
СН2
I
СН2
R
I
N
ОН - С
С
S
СООН
ТПФ
+
C
CН3
C
Н
Гидроксиэтилтиаминпирофосфат
СН2
S
L
SЛипоамид
СН2
ı
О
I
Р
I
О
I
Р
Липоамидсукцинил
трансфераза
ı
СН2
I
СН2
I
С=О
I
S
I
L
НS
Сукциниллипоамид
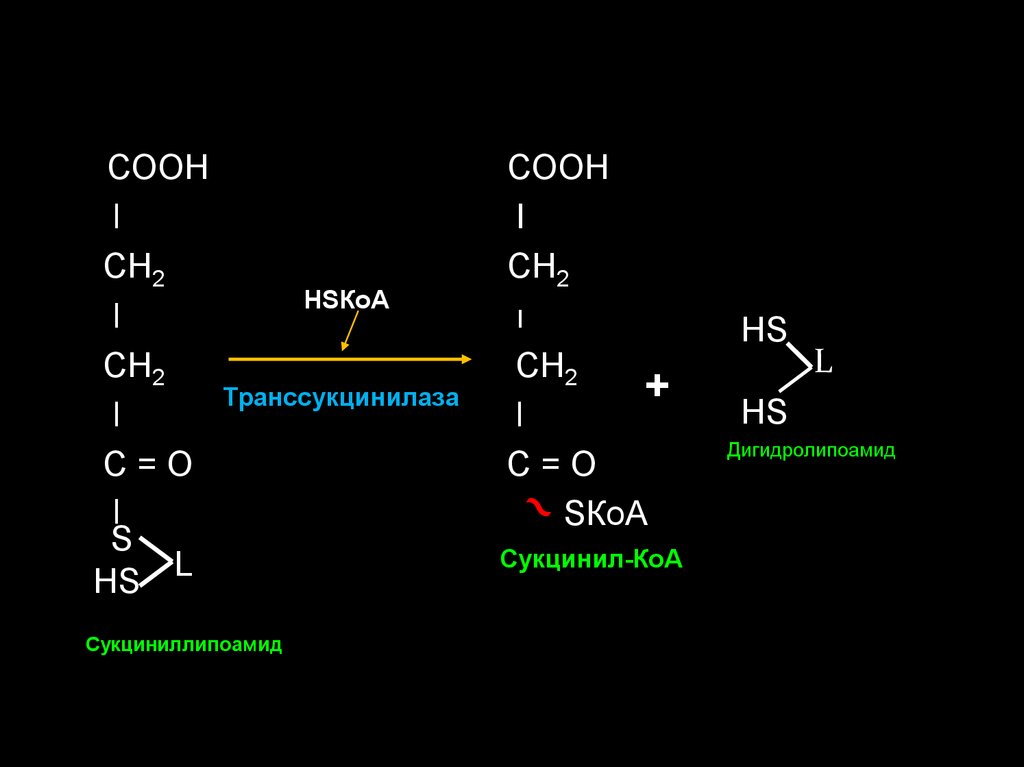
31.
СООНl
СН2
l
СН2
l
С=О
l
S
НS L
НSКоА
Транссукцинилаза
Сукциниллипоамид
СООН
I
СН2
ı
СН2
+
l
С=О
SКоА
Сукцинил-КоА
НS
L
НS
Дигидролипоамид
32.
ΣНАДНS
L
НS
Дигидролипоамид
ΣФАД
ΣНАДН2
ΣФАДН2
3АТФ
S
L
Дегидролипоилдегидрогеназа
S
Липоамид
(окисленная форма)
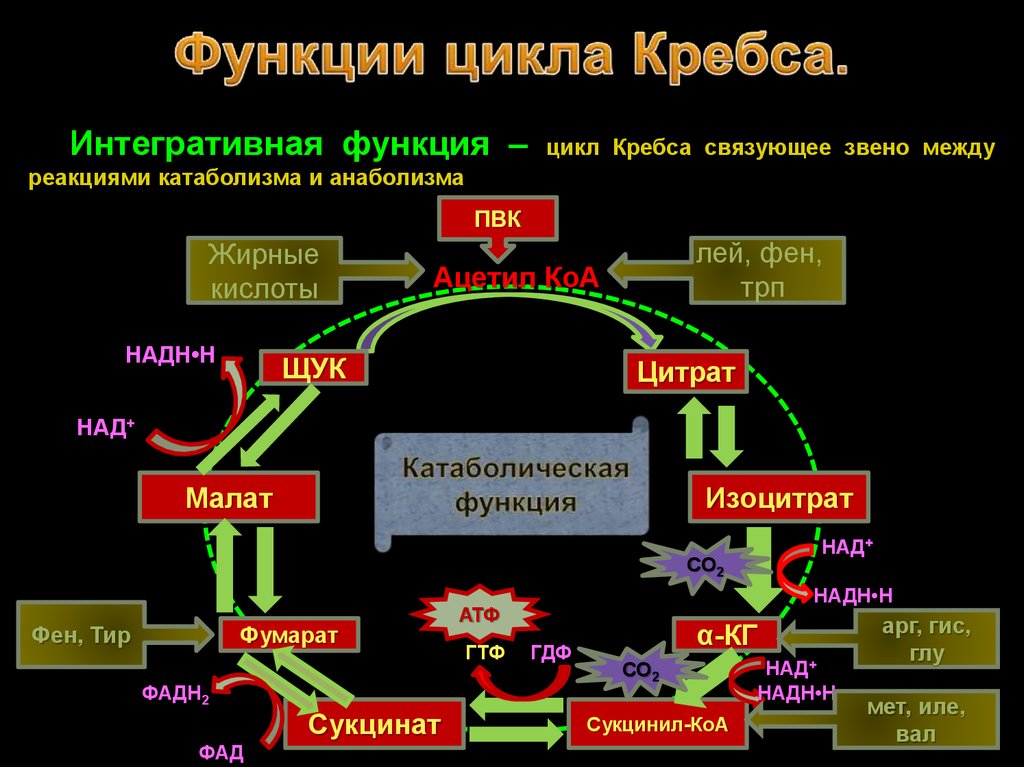
33. Функции цикла Кребса.
Интегративная функция –цикл Кребса связующее звено между
реакциями катаболизма и анаболизма
ПВК
Жирные
кислоты
НАДН•Н
лей, фен,
трп
Ацетил КоА
ЩУК
Цитрат
НАД+
Малат
Изоцитрат
СО2
Фен, Тир
Фумарат
ФАДН2
Сукцинат
ФАД
НАДН•Н
АТФ
ГТФ
НАД+
ГДФ
α-КГ
СО2
Сукцинил-КоА
НАД+
НАДН•Н
арг, гис,
глу
мет, иле,
вал
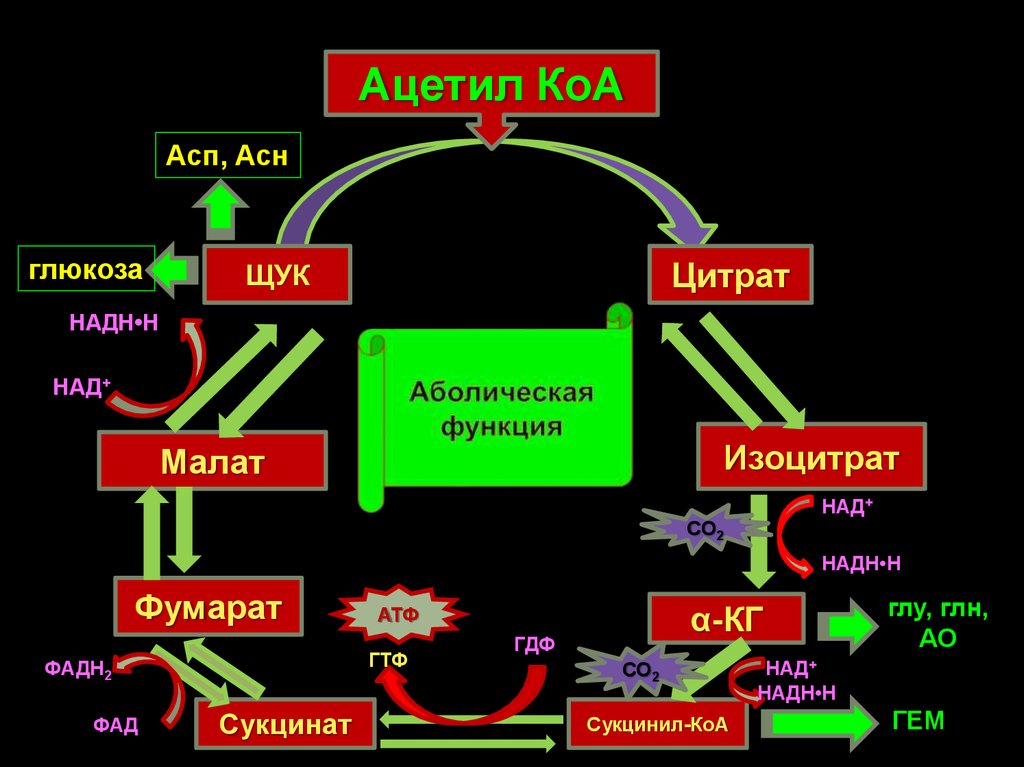
34.
Ацетил КоААсп, Асн
глюкоза
Цитрат
ЩУК
НАДН•Н
НАД+
Изоцитрат
Малат
НАД+
СО2
НАДН•Н
Фумарат
ГТФ
ФАДН2
ФАД
Сукцинат
α-КГ
АТФ
ГДФ
СО2
Сукцинил-КоА
глу, глн,
АО
НАД+
НАДН•Н
ГЕМ
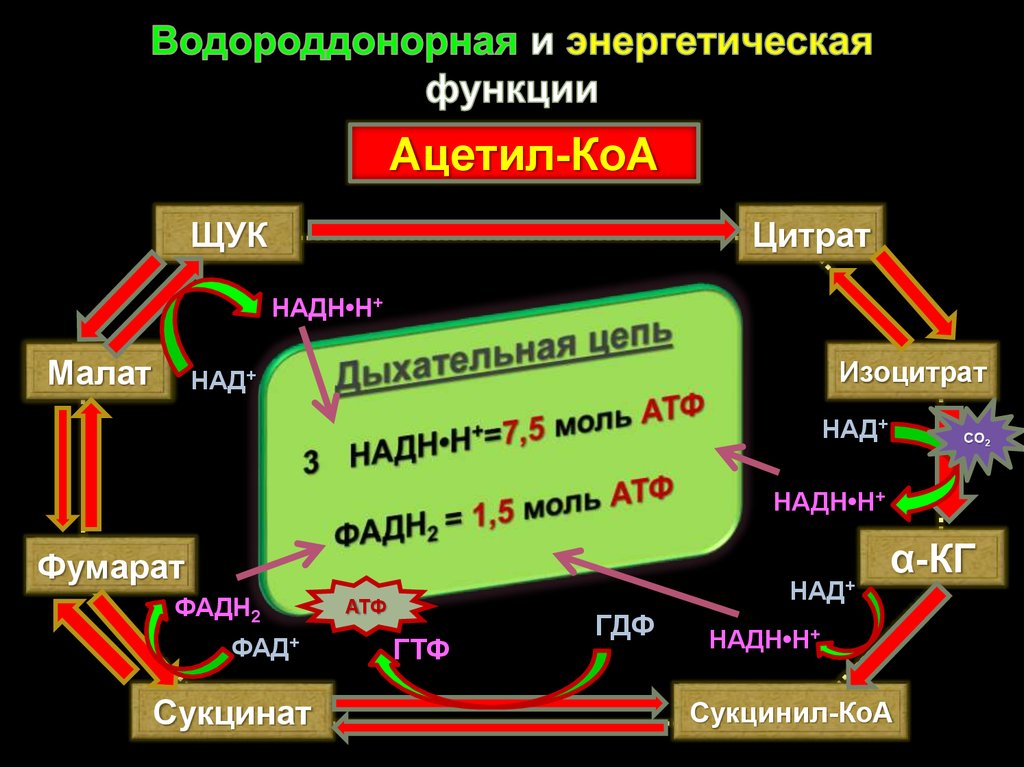
35. Водороддонорная и энергетическая функции
Ацетил-КоАЩУК
Цитрат
НАДН•Н+
Малат
Изоцитрат
НАД+
НАД+
СО2
НАДН•Н+
Фумарат
ФАДН2
ФАД+
Сукцинат
НАД+
АТФ
ГТФ
ГДФ
α-КГ
НАДН•Н+
Сукцинил-КоА
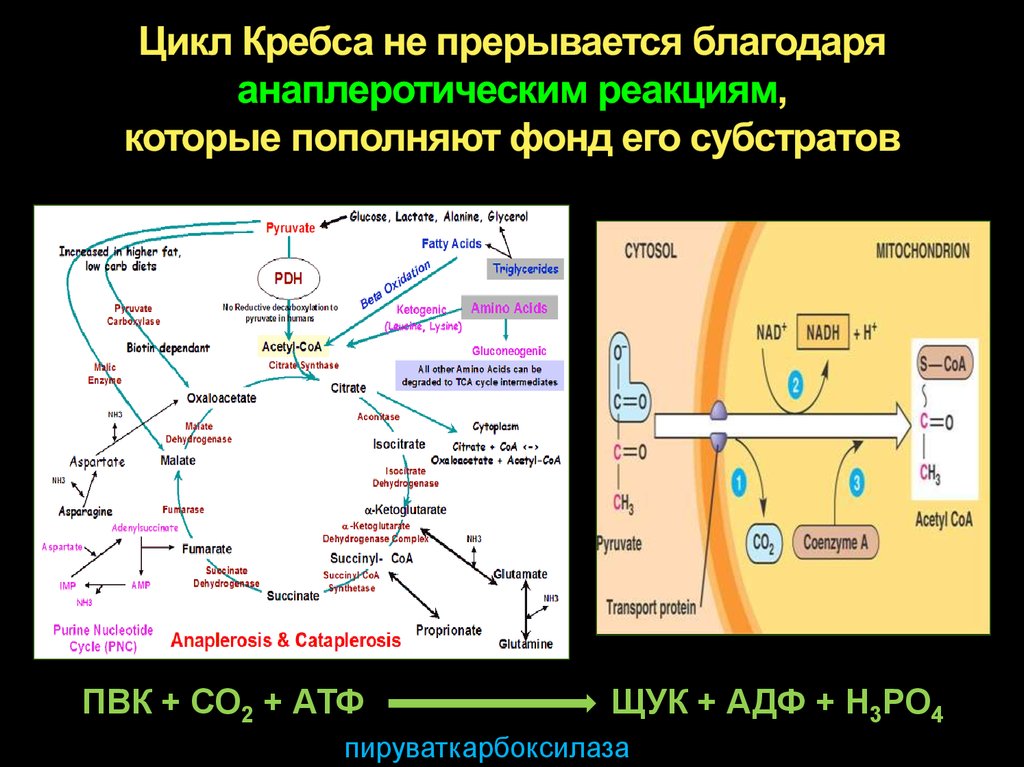
36. Цикл Кребса не прерывается благодаря анаплеротическим реакциям, которые пополняют фонд его субстратов
ПВК + СО2 + АТФЩУК + АДФ + Н3РО4
пируваткарбоксилаза
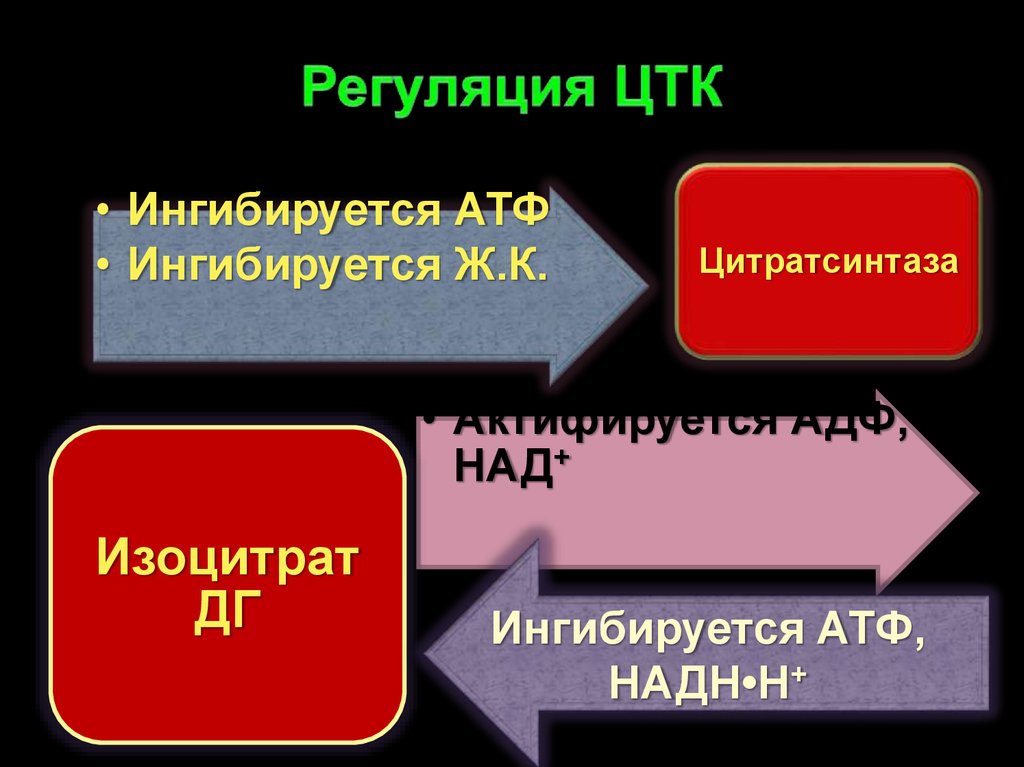
37. Регуляция ЦТК
• Ингибируется АТФ• Ингибируется Ж.К.
Цитратсинтаза
• Актифируется АДФ,
НАД+
Изоцитрат
ДГ
Ингибируется АТФ,
НАДН•Н+















 biology
biology








