Similar presentations:
Физиология гемостаза
1. ГБУ Санкт-Петербургский НИИ скорой помощи им. И.И. Джанелидзе Отдел лабораторной диагностики
ФИЗИОЛОГИЯ ГЕМОСТАЗА2018
Л.П.Пивоварова
2.
СИСТЕМА ГЕМОСТАЗА – физиологическая система, обеспечивающаягемостатический потенциал крови, необходимый для циркуляции крови в
сосудистом русле и остановки кровотечения при повреждении сосудов
(Дуткевич И.Г. и соавт., 2010).
Гемостатический потенциал крови – способность крови находиться в
жидком состоянии или свертываться
Система гемостаза является важнейшей из систем сохранения
гомеостаза организма как в физиологических, так и критических
состояниях.
Система работает благодаря многочисленным клеточным
взаимодействиям и последовательным ферментативным реакциям
активации, усиления и ингибирования.
Гомеостаз – относительное динамическое постоянство показателей
внутренней среды организма, а также все процессы адаптации и
координации физиологических процессов, обеспечивающие единство и
жизнедеятельность организма как в норме, так и в изменившихся
условиях существования (Горизонтов М.Д.,1981).
3. ФУНКЦИИ СИСТЕМЫ ГЕМОСТАЗА
Обеспечение жидкого состояния крови в сосудистом русле,необходимого для нормального кровообращения
Участие в регуляции микроциркуляции в органах и тканях и
транскапиллярного обмена
Обеспечение нормального функционального состояния сосудистой
стенки
Участие в формировании воспаления
Остановка кровотечения при повреждении сосудов – гемостаз
Участие в репарации поврежденной сосудистой стенки
Участие в заживлении повреждений тканей и ран
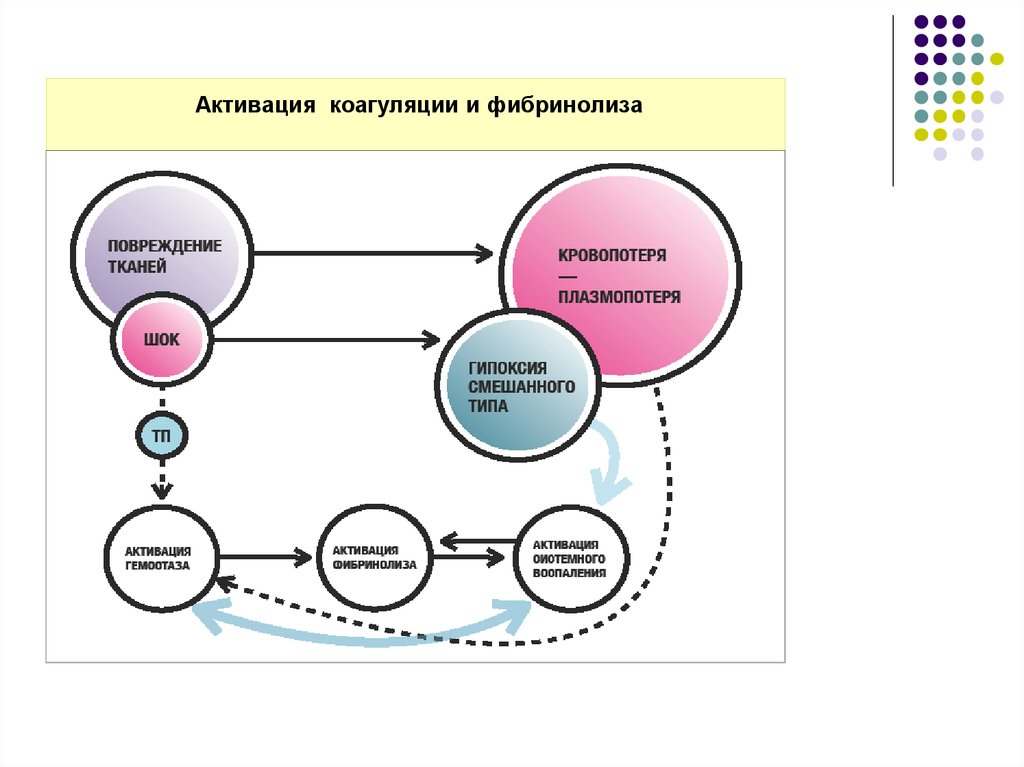
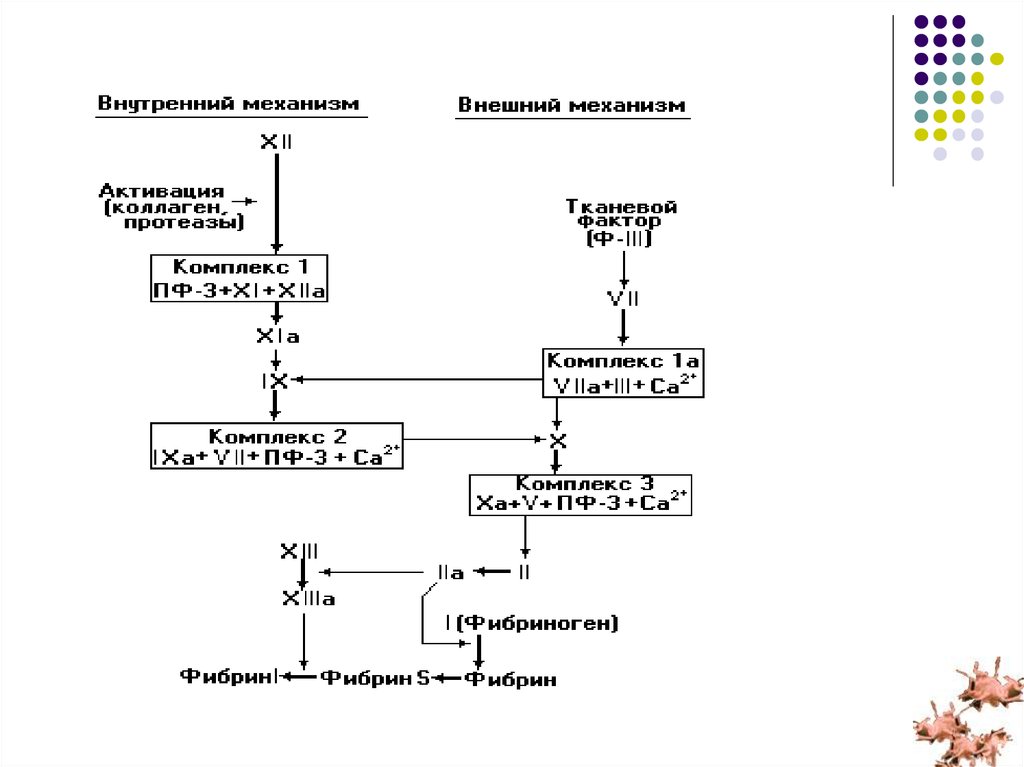
4. Активация коагуляции и фибринолиза
5. Компоненты системы гемостаза
Органы системы гемостаза –органы, где продуцируются или разрушаются факторы системы гемостаза:
костный мозг,
кровь,
стенки сосудов,
печень, селезенка, легкие, почки.
Факторы системы гемостаза - физиологически активные вещества,
взаимодействующие в реализации функций системы гемостаза:
плазменные, клеточные, тканевые
Центры нервной и гуморальной регуляции функционального состояния
гемостаза – центральная и периферическая нервная система, гипоталамус,
гипофиз, железы внутренней секреции
6. Факторы системы гемостаза
1. Свертывающее (прокоагулянтное) звеноПрокоагулянты участвуют в образовании тромбоцитарного и кровяного тромба.
1) Плазменные – нормальные компоненты плазмы крови;
2) Тромбоцитарные – тромбоциты и продуцируемые ими факторы;
3) Тканевые – в клетках тканей: макрофагах, тучных клетках, фибробластах;
4) Лейкоцитарные (моноциты, НГ, базофилы);
5) Эритроцитарные.
2. Противосвертывающее звено
1) физиологические антикоагулянты – препятствуют образованию кровяного
тромба;
2) антиагрегационные факторы– препятствуют образованию тромбоцитарного
тромба;
3) факторы фибринолиза – растворяют кровяной тромб.
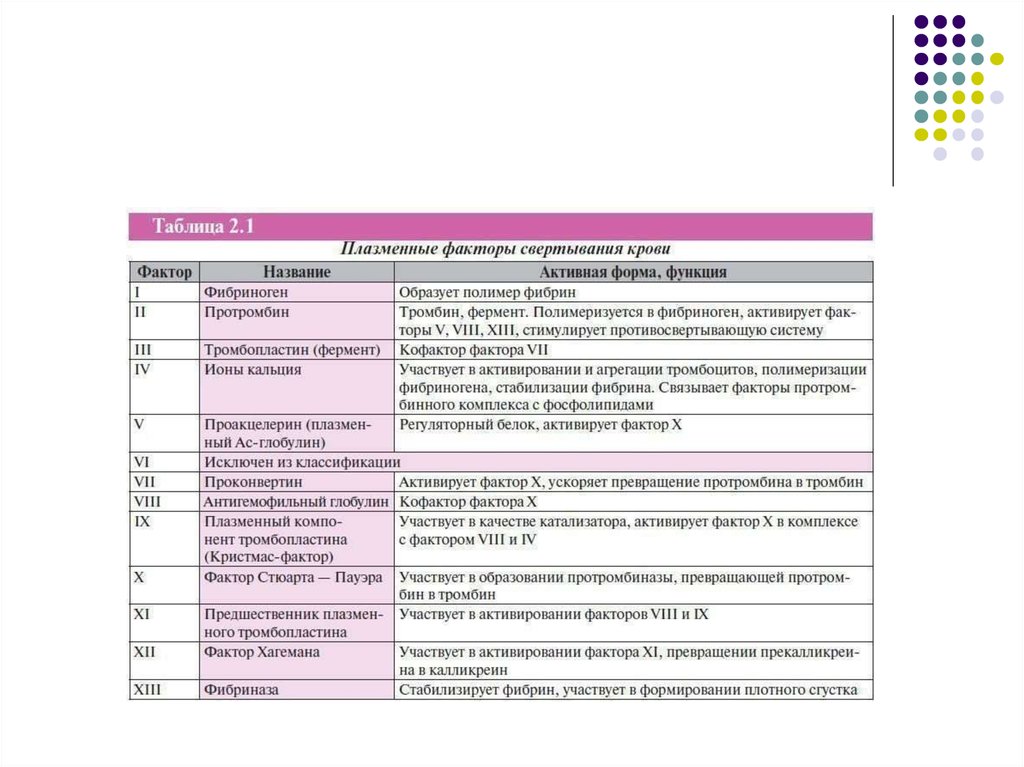
7. 1.1. ПЛАЗМЕННЫЕ ФАКТОРЫ СВЕРТЫВАНИЯ КРОВИ
По Международной номенклатуре плазменные факторы свертываниякрови обозначаются римскими цифрами, за исключением факторов
Виллебранда, Флетчера и Фитцджеральда. Для обозначения
активированного фактора к этим цифрам добавляется буква «а».
Помимо цифрового обозначения, используют и другие наименования
факторов свертывания:
по их функции (например, фактор VIII – антигемофильный глобулин),
по фамилиям больных с впервые обнаруженным дефицитом того или
иного фактора (фактор XII – фактор Хагемана, фактор X – фактор
Стюарта-Прауэра),
по фамилиям авторов (фактор Виллебранда).
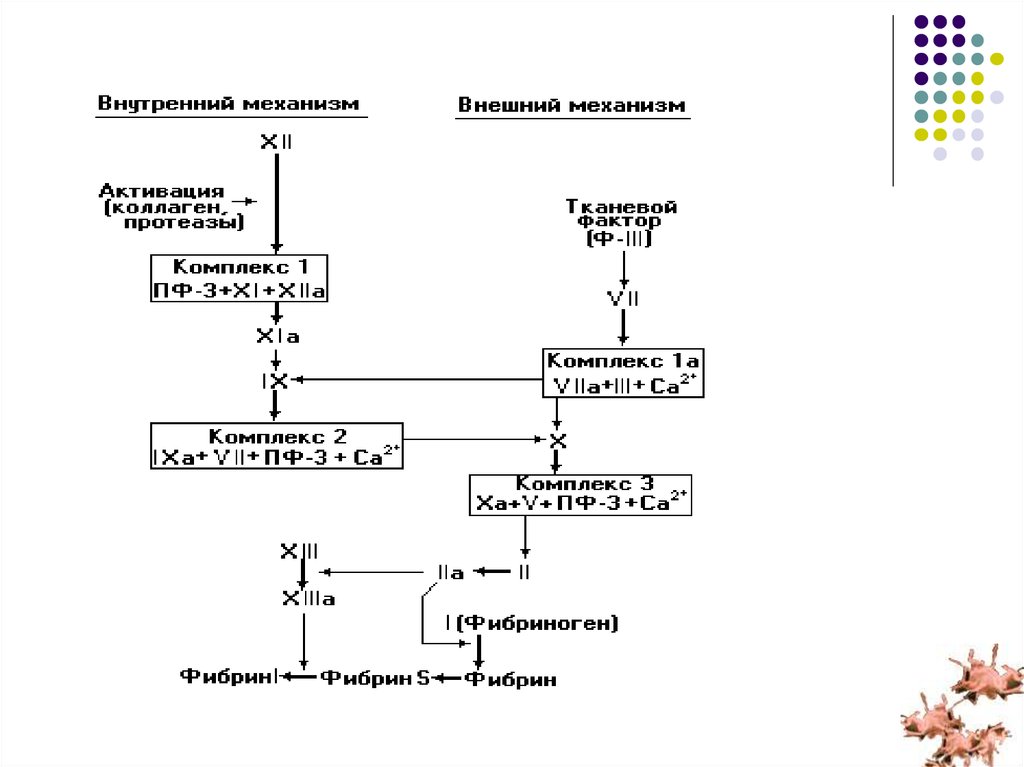
8.
9. 1.1. ПЛАЗМЕННЫЕ ФАКТОРЫ СВЕРТЫВАНИЯ КРОВИ
1.1. ПЛАЗМЕННЫЕ ФАКТОРЫ СВЕРТЫВАНИЯ КРОВИI. Фибриноген - белок, основа для образования фибриновых сгустков.
Постоянно присутствует в плазме. Образуется в гепатоцитах.
Под влиянием тромбина от его молекул отщепляются
фибринопептиды и образуются фибрин-мономеры, которые затем
самопроизвольно полимеруются и перекрестно сшиваются. Также под
влиянием тромбина фибриноген переходит в фибрин.
Участвует в агрегации тромбоцитов.
Белок острой фазы воспаления. Необходим для восстановления
целостности сосудистой стенки и репарации тканей.
II. Протромбин - гликопротеид. Образуется в гепатоцитах в присутствии
витамина К. Под влиянием протромбиназы переходит в
тромбин (фактор IIa)
III фактор – тканевой фактор – тканевой тромбопластин
термостабильный липопротеид, активация внешнего пути свертывания.
Подробнее – в разделе тканевых прокоагулянтных факторов
10. 1.1. ПЛАЗМЕННЫЕ ФАКТОРЫ СВЕРТЫВАНИЯ КРОВИ
IV - ионы Са++ участвуют во всех трех фазах свертывания крови:активации протромбиназы (I фаза),
превращении протромбина в тромбин (II фаза) и
фибриногена в фибрин (III фаза).
Кальций способен связывать гепарин, благодаря чему
свертывание крови ускоряется.
Принимает участие в ретракции сгустка и тромбоцитарной пробки.
При отсутствии кальция нарушаются агрегация тромбоцитов и
ретракция кровяного сгустка.
Всасывается из кишечника.
11. 1.1. ПЛАЗМЕННЫЕ ФАКТОРЫ СВЕРТЫВАНИЯ КРОВИ
V. Проакцелерин, АС-глобулин – белок,продуцируется гепатоцитами и мегакариоцитами.
Активизируется тромбином (фактор IIа).
Создает оптимальные условия для взаимодействия фактора Ха и
протромбина (фактора II)
VII. Проконвертин - гликопротеид.
Образуется в гепатоцитах под влиянием витамина К.
Принимает участие в формировании протромбиназы по внешнему
механизму. Активируется факторами ХIIа, Ха, IХа, IIа и при
взаимодействии с ТФ.
VIII. Антигемофильный глобулин (АГГ) - гликопротеид.
Синтезируется гепатоцитами, клетками селезенки, почек, эндотелия,
лейкоцитами.
Образует комплексную молекулу с фактором Виллебранда (FW) и
специфическим антигеном. Активизируется тромбином. Создает
оптимальные условия для взаимодействия факторов IХа и X. При его
отсутствии возникает заболевание гемофилия А.
FW - компонент комплекса фактора VIII.
Образуется эндотелиальными клетками и мегакариоцитами.
Обеспечивает устойчивость фактора VIII в кровотоке и необходим для
адгезии тромбоцитов. При его недостатке развивается болезнь
Виллебранда, сопровождающаяся нарушением сосудисто-тромбоцитарного
гемостаза.
12. 1.1. ПЛАЗМЕННЫЕ ФАКТОРЫ СВЕРТЫВАНИЯ КРОВИ
IX. Фактор Кристмаса – гликопротеид, плазменный компоненттромбопластина.
Образуется в печени под влиянием витамина К.
Активируется факторами XIa, VIla и IIа.
Переводит фактор X в Ха.
При его отсутствии возникает заболевание гемофилия В
X. Фактор Стюарта-Прауэр - протромбиназа - гликопротеид.
Образуется в печени под влиянием витамина К. Фактор Ха
Активируется факторами VIla и IХа, трипсином и ферментом из яда
гадюки.
Переводит фактор II (протромбин) в IIа (тромбин).
XI. Плазменный предшественник тромбопластина (РТА) - фактор
Розенталя, антигемофильный фактор C – термолабильный
гликопротеид.
Синтезируется в печени. Активируется фактором ХIIа, калликреином
совместно с высокомолекулярным кининогеном (ВМК)
13. 1.1. ПЛАЗМЕННЫЕ ФАКТОРЫ СВЕРТЫВАНИЯ КРОВИ
XII. Фактор Хагемана, контактный фактор - белок.Активируется в организме при контакте с кожей, волокнами
коллагена, хондроитинсерной кислотой, мицеллами насыщенных
жирных кислот.
Активаторами фактора XII являются также фактор Флетчера,
калликреин, фактор XIа, плазмин.
Фактор Хагемана участвует во «внутреннем» пути
формирования протромбиназы, активируя фактор XI.
Последовательно запускает внутренний и внешний и механизмы
образования протромбиназы и фибринолиза,
14. 1.1. ПЛАЗМЕННЫЕ ФАКТОРЫ СВЕРТЫВАНИЯ КРОВИ
ХIII. Фибрин-стабилизирующий фактор (ФСФ) – фибриназа плазменная трансглутаминаза. Синтезируется гепатоцитами.С участием Са++ стабилизирует фибрин.
Необходим для нормального течения репаративных процессов.
Прекалликреин, фактор Флетчера - является компонентом
калликреин-кининовой системы.
Белок. Продуцируется гепатоцитами.
Участвует в активации фактора XII, плазминогена и
высокомолекулярных. кининогенов (ВМК)
Высокомолекулярный кининоген (ВМК), фактор ФитцджеральдаФложак.
Продуцируется гепатоцитами.
Активируется калликреином, принимает участие в активации факторов
XII, XI и фибринолиза
15. 1.1. ПЛАЗМЕННЫЕ ФАКТОРЫ СВЕРТЫВАНИЯ КРОВИ
Факторы I, II, V, VII, VIII, IX, X, XII, XIII, прекалликреинвысокомолекулярный кининоген синтезируются в печени.
Факторы II, VII, IX, X являются витамин К-зависимыми.
Сериновые протеазы: II, VII, IX, X, XI, XII, прекалликреин
высокомолекулярный кининоген (ВМК).
Факторы контакта: XI, XII, ВМК, прекалликреин (ф.Флетчера)
16. Контактные факторы
XII, XI, высокомолекулярный кининоген (ВМК), прекалликреин(ПК)
Синтезируются в печени, активируются при контакте с
отрицательно заряженной поверхностью.
in vivo - коллаген
in vitro - стекло, каолин
Большая мол. масса (80-173 кДа).
Не потребляются в ходе свертывания, присутствуют в сыворотке
крови
Функция: активация свертывания крови по внутреннему пути
17. Факторы протромбинового комплекса
II, VII, IX, X, протеин C, протеин S, протеин ZСинтезируются в печени
Малая мол. Масса (50-100 кДа)
Витамин К-зависимые
Содержат участки связывания Ca++
Ингибируются антагонистами витамина К
Функции:
проферменты (II, VII, IX, X, протеин С) и
кофакторы (протеин S, протеин Z)
18. Основные лабораторные методы исследования плазменных факторов СК
Внешний путь СКПротромбиновое время – ПТВ
– время образования сгустка после добавления в плазму тканевого фактора.
Отражает содержание и активность в крови:
I - фибриногена,
II – протромбина*,
V – проакцелерина
VII – проконвертина*
X – ф. Стюарта-Прауэр*
* - витамин К-зависимые факторы.
Наблюдают удлинение ПТВ при дефиците вит. К, ДВС, печеночной
недостаточности, врожденной афибриногенемии, дефиците ф. V, дефиците ф. X.
Производные показатели: ПТИ и МНО
Внутренний путь СК
Активированное частичное тромбиновое время – АЧТВ
ф. XI, XII (факторы контакта)
Определение уровня и активности отдельных показателей
19. 1.2. ТРОМБОЦИТАРНЫЕ ПРОКОАГУЛЯНТЫ
Тромбоциты – безъядерные дисковидные клетки,образующиеся из мегакариоцитов в костном мозге. Тромбоциты
имеют двухслойную фосфолипидную мембрану с многочисленными
инвагинациями. Зрелые формы имеют размер 2-3,5 мкм.
После выхода в кровь тромбоциты в течение 7-10 сут
циркулируют в кровотоке и частично депонируются в селезенке.
Утилизируются клетками РЭС.
При активации тромбоцит изменяет форму и может
увеличивать свою площадь. Имеют на мембране многочисленные
гликопротеиновые рецепторы для плазменных факторов гемостаза,
медиаторов эндокринной, нервной, иммунной систем, медиаторов
воспаления.
Гранулы тромбоцитов и их мембраны содержат множество
биологически активных веществ (БАВ).
20. Функции тромбоцитов в системе гемостаза
Тромбоциты поддерживают нормальную структуру и функцию стеноксосудов микроциркуляторного русла за счет прилипания к
эндотелиальным клеткам, которые поглощают до 10% циркулирующих
тромбоцитов.
Обеспечивают длительный спазм поврежденных сосудов посредством
секреции вазопрессорных веществ (адреналина, серотонина).
Закупоривают просвет поврежденных сосудов первичной
тромбоцитарной пробкой (тромбом), образующейся после адгезии и
агрегации тромбоцитов.
На поверхности активированных тромбоцитов фиксируются и
взаимодействуют плазменные прокоагулянты для образования
кровяного тромба, а также – лейкоциты и эритроциты.
Защищают плазменные прокоагулянты от действия физиологических
антикоагулянтов и факторов фибринолиза, что обеспечивает
формирование полноценного тромба при повреждении сосуда.
Стимулируют процесс репарации поврежденных тканей и сосудистой
стенки, секретируя ростовые факторы (PDGF, TGFβ, VEGF, EGF, FGF,
IGF).
21. ТРОМБОЦИТЫ
на различных этапах активации продуцируют:Адреналин, норадреналин
Тромбоспондин
Фибронектин
Ионы кальция
FW
Ростовые факторы
Кислые гидролазы
Тромбоглобулины (РВР, СТАР-III, β-тромбоглобулин) –
освобождаются при активации из α-гранул, регулируют
функциональную активность и направленную миграцию к тромбу НГ и
фибробластов.
Исследования:
количество Тр в крови, морфология, рецепторы
оценка внутрисосудистой активации Тр,
агрегационная активность,
определение содержания отдельных факторов и рецепторов,
выявление аутоантител к определенным факторам,
генетика факторов
22. 1.2. ТРОМБОЦИТАРНЫЕ ПРОКОАГУЛЯНТЫ
РF1 – тромбоцитарный Ас-глобулин, аналогичный ф. V (проакцелерину);РF2 – акцелератор тромбина, ускоряет превращение фибриногена в фибрин;
РF3 – тромбоцитарный тромбопластин, представлен на мембране тромбоцитов
фосфолипидными комплексами, являющимися лигандами плазменных
прокоагулянтов;
РF4 – антигепариновый фактор, высвобождается при активации тромбоцитов из
α-гранул, обладает антигепариновой активностью;
РF5 – тромбоцитарный фибриноген;
РF6 – тромбостенин – тромбоцитарный актомиозин, необходимый для ретракции
тромбоцитарного и кровяного тромбов;
РF7 – антифибринолитический фактор;
РF9 – фибринстабилизирующий фактор, аналогичный ф. XIII (фибриназе).
РF10 – серотонин – вызывает сужение сосудов;
РF11 – АДФ – аденозиндифосфорная кислота – стимулирует агрегацию
23. Рецепторы тромбоцитов - гликопротеиновые белки, встроенные в цитоплазматическую мембрану
АктивационныеGP 1b/V/IX
Активация происходит под
влиянием коллагена
сосудистой стенки.
Проявляется в изменении
формы, экспрессии адгезивных
рецепторов и усилении
секреции факторов
свертывания и БАВ.
Адгезивные
Интегрины:
GP Ib/IIIa
GP Ia/Iia
Агрегация происходит
преимущественно с участием
фибриногена, фактора фон
Виллебранда.
24.
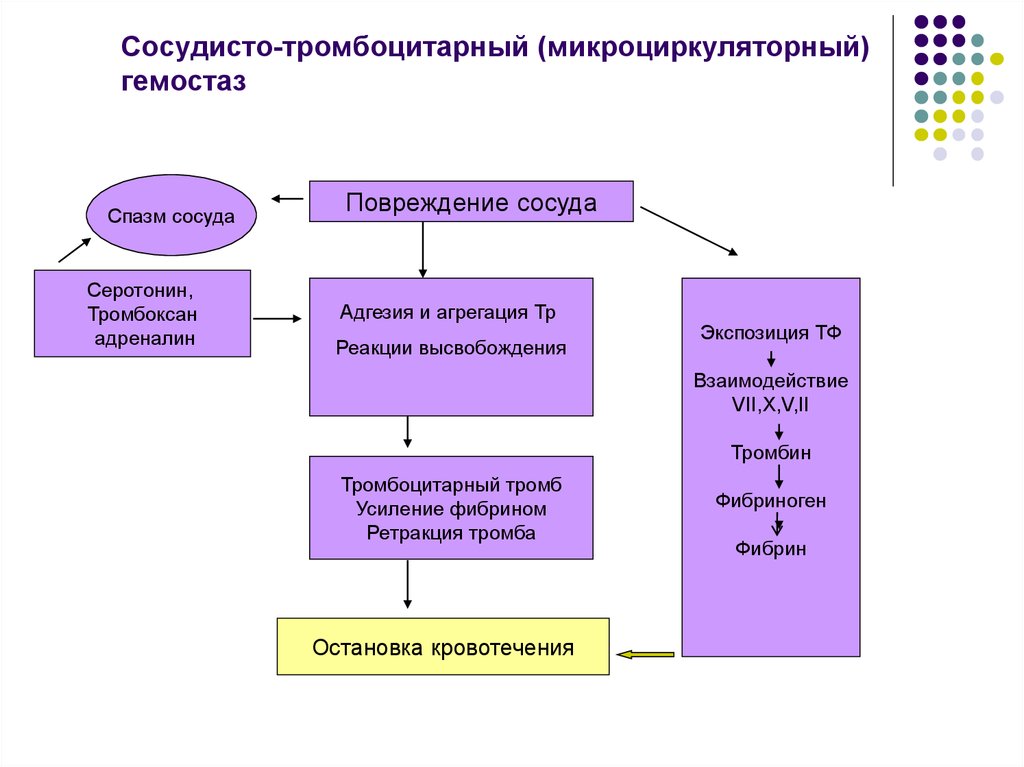
25. Сосудисто-тромбоцитарный (микроциркуляторный) гемостаз
Спазм сосудаСеротонин,
Тромбоксан
адреналин
Повреждение сосуда
Адгезия и агрегация Тр
Реакции высвобождения
Экспозиция ТФ
Взаимодействие
VII,X,V,II
Тромбин
Тромбоцитарный тромб
Усиление фибрином
Ретракция тромба
Остановка кровотечения
Фибриноген
Фибрин
26.
27.
28. 1.3. ТКАНЕВЫЕ ФАКТОРЫ СВЕРТЫВАНИЯ КРОВИ
III – тканевой прокоагулянт, тканевой тромбопластин, ТФ, CD142трансмембранный гликопротеин, комплекс белка апопротеина III и
фосфолипидов. Входит в состав мембран клеток многих тканей, в том
числе клеток субэндотелиального слоя сосудистых стенок.
В условиях патологии он образуется в клетках эндотелия, моноцитах
и макрофагах под влиянием эндотоксина, тромбина, иммунных
комплексов, ИЛ-1β, ТНФα, ИЛ-6 и других воспалительных цитокинов.
Активный комплекс ТФ с фосфолипидами появляется в крови при
повреждении клеточных мембран. Контакт крови с ТФ инициирует
процесс свертывания крови.
Является матрицей для развертывания реакций, направленных на
образование протромбиназы по внешнему механизму.
29. 1.4. Лейкоцитарные
Лейкоциты, как и другие форменные элементы крови, содержатвещества, участвующие в процессе свертывания крови и фибринолиза.
Особенно большое влияние на гемостаз лейкоциты оказывают при
заболеваниях, сопровождающихся увеличением их количества.
Моноциты продуцируют факторы, усиливающие свертывание крови
(тромбоксаны, тромбопластин), и факторы, стимулирующие фибринолиз
(активаторы плазминогена).
Тромбопластический фактор лейкоцитов. При травме сосудистой
стенки лейкоциты, как и тромбоциты, способны прилипать к
поврежденной поверхности. Освобождение при этом
тромбопластического фактора лейкоцитов способствует быстрому
образованию тромбина, активирующего тромбоциты и плазменный
каскад свертывания крови.
Антигепариновый фактор лейкоцитов, подобный PF4 тромбоцитов
находится в их ядре и различных структурах цитоплазмы.
Антигемофильный глобулин лейкоцитов подобен фактору VIII
плазмы.
30. 1.4. Лейкоцитарные
Фактор Хагемана моноцитов подобен фактору Хагемана плазмы.Этот фактор способен ускорять процесс гемокоагуляции, а также
принимать участие в образовании фибриновых воспалительных
экссудатов.
АДФ. Усиливает адгезивность и агрегацию лейкоцитов. Большей
адгезивной способностью обладают нейтрофилы, значительно меньшей
– лимфоциты.
В месте повреждения сосудистой стенки сначала происходит
адгезия и агрегация тромбоцитов, а приблизительно через 1 час к
плотному тромбоцитарному слою начинают присоединяться отдельные
гранулоциты, достигая максимума через 2 – 6 часов после повреждения
эндотелия. Можно предположить, что гранулоциты в кровотоке,
прилипая к слою адгезированных тромбоцитов, прекращают их
дальнейшую агрегацию и тем самым способствуют сохранению
кровотока в травмированном сосуде.
31. 1.4. Эритроцитарные
К числу внутриэритроцитарных гемостатических факторов относят:Тромбопластический фактор (эритроцитин). Представляет собой
термостабильный мембранный фосфолипид. Воздействует на процесс
свертывания крови независимо от наличия тканевого тромбопластина и
тромбоцитов.
Активность выделения эритроцитина в плазму зависит от уровня
адреналина, норадреналина, ацетилхолина, гистамина и тромбина. Это
обусловлено влиянием этих веществ на проницаемость мембраны эритроцитов
для ионов, их осмотическую резистентность вследствие уменьшения
отрицательного электрокинетического заряда. Доказано, что наибольшую
активность эритроцитин проявляет при гемолизе эритроцитов.
Антигепариновый фактор может выделяться в плазму как интактными
эритроцитами, так и в результате их разрушения.
Ac-глобулин (акцелерин) обнаруживается в разрушенных и интактных
эритроцитах.
Тромбиноподобный фактор способствует превращению фибриногена в
фибрин. По своим свойствам сходен с фактором II тромбоцитов.
Фибринстабилизирующий фактор участвует в формировании плотного
стабилизированного нерастворимого фибрина.
32. 1.5. Тромбогенные факторы эндотелия
Тромбоцитарный фактор роста (PDGF) синтезируется в мегакариоцитах вкостном мозге и запасается в α-гранулах тромбоцитов. Высвобождение
происходит при активации тромбоцитов под влиянием тромбомодулина.
Ингибитор тканевого активатора плазминогена-1 (ИТАП-1) – продуцируется
эндотелиоцитами, гладкомышечными клетками, мегакариоцитами и клетками
мезотелия. Также депонируется в Тр а неактивной форме.
Активация продукции происходит под влиянием тромбина, TGFβ, PGF, IL-1,
глюкокортикоидов, инсулиноподобного фактора роста.
Основная функция ИТАП-1 – ограничить фибринолиз в зоне образования
гемостатической пробки посредством ингибирования урокиназы, т.е.
предупредить преждевременный лизис тромба. Его содержание в
эндотелиоцитах выше, чем содержание ТАП.
33. 2. Противосвертывающее звено
Жидкое состояние крови поддерживается благодаря:ее движению,
адсорбции факторов свертывания эндотелием и
действию естественных антикоагулянтов.
Важнейшие из них – антитромбин III, гепарин, протеин С, протеин S
и ингибитор внешнего механизма свертывания.
1) физиологические антикоагулянты – препятствуют образованию
кровяного тромба;
2) антиагрегационные факторы препятствуют образованию
тромбоцитарного тромба;
3) факторы фибринолиза – растворяют кровяной тромб.
34. 2. Противосвертывающее звено 2.1.Физиологические антикоагулянты
Препятствуют образованию кровяного тромба.2.1.1.Первичные физиологические антикоагулянты
Антитромбин III (AT III)
- α2- глобулин, синтезируемый гепатоцитами и эндотелиальными клетками,
ингибирует тромбин (IIа) и ф. Стюарта-Прауэра (Ха, тромбиназа). Действует в
комплексе с гепарином.
аминопептидаза A
аминопептидаза N
АТ II
АТ III
ангиотензин IV
Гепарин – гликозоаминогликан, синтезируется тучными клетками и
базофилами крови. Также как и AT III, является медленно действующим
поливалентным антикоагулянтом.
При образовании комплекса гепарин+ AT III создается быстрый и
мощный антикоагулянтный эффект. Комплекс обеспечивает 80-90%
антикоагулянтного потенциала крови. Для эффективного действия гепарина
уровень AT III в крови должен быть не менее 80%.
35. 2.1.1. Первичные физиологические антикоагулянты
Протеин С – витамин К зависимая серинамидаза, синтезируетсягепатоцитами. Ингибирует факторы VIIIa и Va, прекращая образование
фибрина. Циркулирует в крови в неактивном состоянии.
Активация происходит под влиянием комплекса «тромбинтромбомодулин» на поверхности эндотелиальных клеток.
Кофактор протеина С – протеин S. В присутствии протеина S частично
разрушает неферментные плазменные факторы Vа и VIIIа, тем самым
сдерживая коагуляционный процесс.
Активирует плазминоген.
Ингибитор тканевого пути свертывания (TFPI)
т.е. протромбиназного комплекса «ТФ+VIIа+Ха+Са»*
(внешнего пути свертывания).
* тканевой фактор + активированный проконвертин + ф. Старта-Прауэра
– протромбиназа)
36. 2.1.2. Антикоагулянты, образующиеся при свертывании крови и фибринолизе
Фибриноген, связывая рецепторы тромбина, инактивирует тромбинФибрин-пептиды А и В, образующиеся при расщеплении молекулы
фибриногена тромбином
Продукты деградации фибрина/фибриногена (ПДФ): фибрин-мономеры ранние
– X, Y
и поздние – фибрин-мономеры D, E и D-димеры
Ранние ПДФ – антикоагулянтное антитромбиновое действие,
антиполимеразное (блокируют образование фибрин-полимера),
повышают проницаемость сосудов.
Поздние ПДФ – блокируют рецепторы тромбоцитов, снижая их гемостатическую
функцию.
Д-димеры возникают только при разрушении молекулы фибрина.
Увеличение содержания в крови может наблюдаться как при защитном
фибринолизе, так и при усилении внутрисосудистого свертывания, при
патологическом фибринолизе при плазминемии
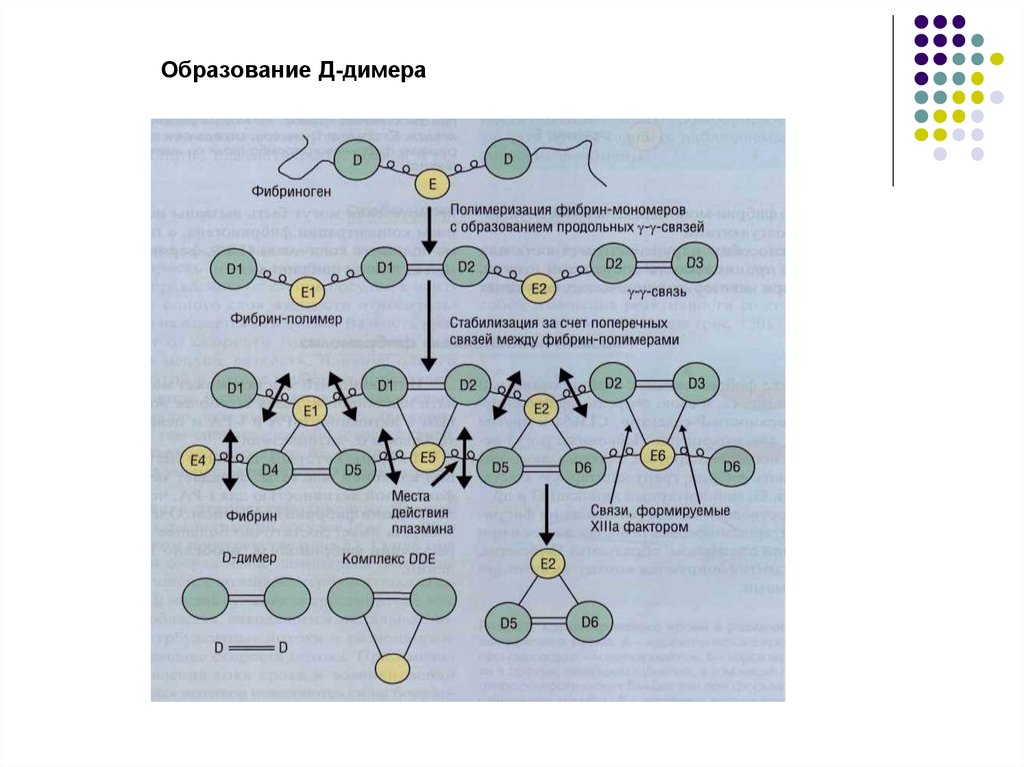
37. Образование Д-димера
Активация тромбоцитовОбразование протромбиназного комплекса и тромбина.
Регулирующее влияние АТ III.
Образование фибриногена.
Фибринолиз
Д-димер фибрина представляет собой продукт
деградации ковалентно сшитого фибрина.
Плазмин вызывает последовательное
асимметричное расщепление фибрина на все более и
более мелкие фрагменты: D-димеры и тримеры D-ED, поскольку плазмин не способен разрезать
ковалентную связь между D-доменами.
Таким образом, уровень D-димера является
маркером фибринолитической деградации
повышенного количества внутрисосудистого фибрина
при ДВС
Литическое расщепление связей D-Е также
осуществляет эластаза нейтрофильных
гранулоцитов (НГ) , которую в большом количестве
секретируют активированные при воспалении
клетки. При активации НГ также секретируют
проактиватор плазминогена.
При заболеваниях, не связанных с травмами,
количественное определение D-димера успешно
используют для исключения ТГВ и ТЭЛА при условии
претестовой оценки клинической вероятности
тромбоза (шкалы Well’s 2000,2006).
В рекомендациях ACCP (Аmerican College of Chest
Phisicians, 2012, 2016 ) рассматривается как тест
второй линии для оценки вероятности тромбоза и
включен в число показаний к продлению
антикоагулянтной терапии при его повышенной
концентрации после курса терапии, но не могут быть
самостоятельным критерием определения тактики
ведения больных.
D-димер – биомаркер с высоким
отрицательным прогностическим значением для
развития тромбообразования.
38. 2.2. Антиагрегационные факторы
Простациклин – простагландин I2 – метаболит арахидоновой кислоты,синтезируется в мембранах ЭК и тромбоцитов. Является мощным
вазодилятатором, подавляет адгезивную и агрегационную активность
тромбоцитов.
Оксид азота – NO cинтезируется из аминокислоты аргинина в клетках
различных тканей организма, но больше всего в ЭК. Более сильный
вазодилятатор, чем простациклин, но слабее влияет на агрегационные
свойства тромбоцитов.
Как простациклин, так и NO являются факторами
антитромбогенных свойств эндотелия сосудов.
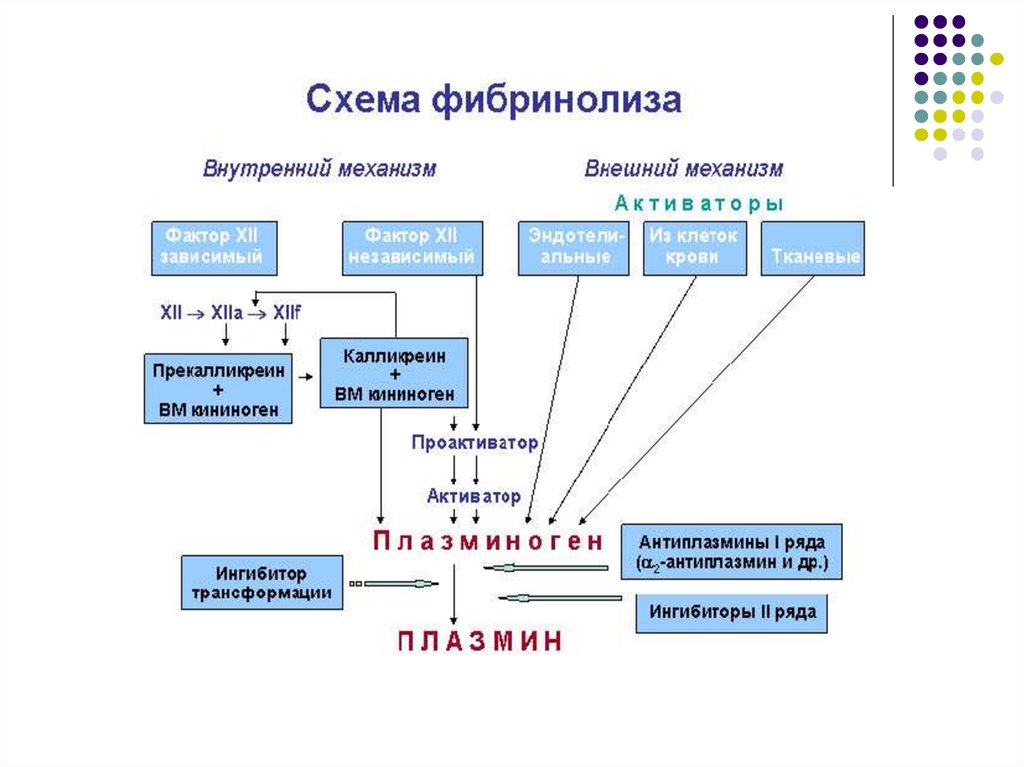
39. 2.3. Фибринолитические факторы
Фибринолитическую активность крови определяют содержание и взаимодействиеплазминогена, активаторов плазминогена и их ингибиторов, плазмина и его
ингибиторов.
Плазминоген – гликопротеин, неактивная форма протеолитического фермента
плазмина. Синтезируется в печени, присутствует во многих биологических
жидкостях организма.
Плазмин разрушает фибрин и фибриноген до ранних и поздних ПДФ. Время
лизиса фибрина составляет 1-2 часа.
Также, разрушает рецепторы тромбоцитов, нарушая активацию, адгезию и
агрегацию тромбоцитов и препятствует их участию в гемостазе.
Активаторы плазминогена:
тканевой активатор (t-PA) синтезируется в эндотелии, присутствует в НГ и
моноцитах. Его действие направлено на активацию лизиса фибрина в сосудистом
русле;
урокиназный тип активатора (u-PA), который синтезируется в почках, активирует
плазминоген на поверхности эндотелиальных и других клеток.
Комплекс XIIa+калликреин и протеиновый комплекс С+S.
40.
Ингибиторы активаторов плазминогенаPAI-I – гликопротеин, синтезируется в тромбоцитах, ЭК, моноцитах,
гладкомышечных клетках, в печени. Способствует местному
торможению фибринолиза и кратковременному сохранению тромба.
Ингибитор плазмина – α2-антиплазмин.
Синтезируется в печени, связывает свободный плазмин плазмы,
инактивируя его. Содержится в лейкоцитах крови.
41.
42. 3. Нарушения функционирования системы гемостаза
Система гемостаза немедленно реагирует на различные внешние ивнутренние воздействия. Устойчивый дисбаланс при взаимодействии
клеточных и ферментативных участников гемостаза у пациентов с
различными заболеваниями, или еще не определенными
заболеваниями,
является причиной развития как геморрагических, так и тромботических
состояний и осложнений, нередко опасных для жизни.
Основные понятия:
1. Тромбофилия – состояние, объединяющее как наследственные, так
и приобретенные нарушения гемостаза, которым свойственна
предрасположенность к раннему появлению и рецидивированию
тромбозов, тромбоэмболий, ишемий и инфарктов органов (Баркаган
З.С., 2005).
Клиническое понятие.
2. Гиперкоагуляционный синдром/состояние – лабораторный
феномен, когда с помощью специальных методов анализа гемостаза in
vitro распознаются активация тромбоцитов, образование фибрина,
подавление реакций фибринолиза, повреждения эндотелия
кровеносных сосудов. Состояние может проявляться и гипокоагуляцией
при наличии ВА, дисфибриногенемии, гепарин-индуцированной
тромбоцитопении 2 типа (ГИТ-2).
43. Определения
Международное общество по тромбозу и гемостазу (ISTH) 1995 год:Наследственная тромбофилия – необычная наклонность к тромбозу с ранним
возрастным началом, отягощенностью семейного анамнеза, степенью тяжести
тромбоза, непропорциональной известному этиологическому фактору,
склонность к рецидивам.
2008 год. Обновленная версия практических торакальных врачей по
антитромботической и тромболитической терапии (АССР):
Наследственная тромбофилия – наличие одного или более признаков:
дефицита антитромбина, дефицита протеина С, дефицита протеина S,
резистентности активированному протеину С (см. таблицу) + увеличение
активности фактора VIII или сниженный уровень протеина S.
44.
3. Факторы тромбогенного рискаТромбофилия не всегда проявляется тромбозами.
Врожденные факторы:
- дефицит физиологических антикоагулянтов – антитромбина III, витамин
К зависимых протеинов С,S,Z, ингибитора внешнего пути свертывания;
- стойкое увеличение концентрации или активности факторов
свертывания
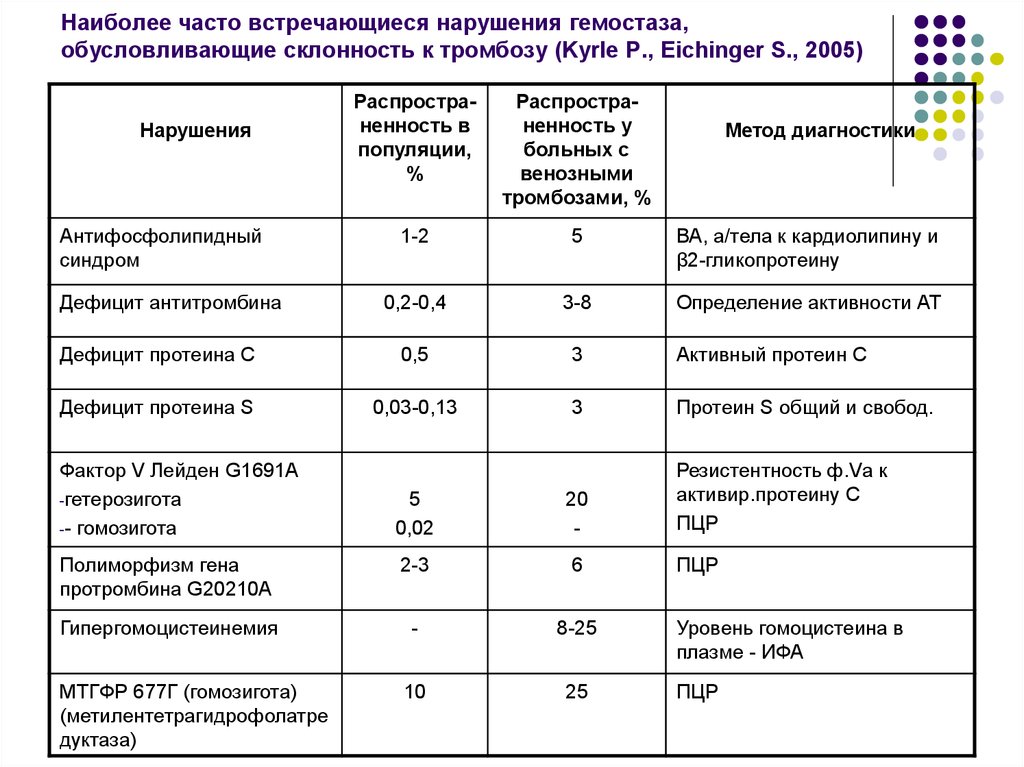
45. Наиболее часто встречающиеся нарушения гемостаза, обусловливающие склонность к тромбозу (Kyrle P., Eichinger S., 2005)
Распространенность впопуляции,
%
Распространенность у
больных с
венозными
тромбозами, %
1-2
5
ВА, а/тела к кардиолипину и
β2-гликопротеину
0,2-0,4
3-8
Определение активности АТ
Дефицит протеина С
0,5
3
Активный протеин С
Дефицит протеина S
0,03-0,13
3
Протеин S общий и свобод.
5
0,02
20
-
Резистентность ф.Vа к
активир.протеину С
ПЦР
Полиморфизм гена
протромбина G20210А
2-3
6
ПЦР
Гипергомоцистеинемия
-
8-25
10
25
Нарушения
Антифосфолипидный
синдром
Дефицит антитромбина
Фактор V Лейден G1691А
-гетерозигота
-- гомозигота
МТГФР 677Г (гомозигота)
(метилентетрагидрофолатре
дуктаза)
Метод диагностики
Уровень гомоцистеина в
плазме - ИФА
ПЦР
46. Основные типы кровоточивости
Тип кровоточивостиМикроциркуляторный
(петехиально-пятнистый, синячковый)
Основные виды и причины патологии
Тромбоцитопении, тромбоцитопатии,
дефецит факторов X, II, VII.
Гематомный (кровоизлияния в мягкие Гемофилии А и В
ткани, крупные суставы)
Смешанный
(микроциркуляторно-гематомный)
Острый и подострый ДВС-синдром, резкое
снижение протромбинового комплекса и
фактора XIII, передозировка
антикоагулянтами и антиагрегантами,
избыточная тромболитическая терапия
Васкулитно-пурпурный
(воспалительные изменения в
микрососудах и периваскулярной
ткани)
Микротромбоваскулиты
Ангиоматозный
Микроангиоматоз, телеангиэктазия
(болезнь Рандю Ослера)
47. Лабораторные показатели, отражающие проявления кровоточивости
ПоказателиОтклонения
Время кровотечения
Более 12 мин
Количество тромбоцитов в крови
Менее 80-100 ·10 9/л
АЧТВ
Гипокоагуляция
Протромбиновое время
Гипокоагуляция
Концентрация фибриногена
Менее 1,0 г/л
Факторы VIII и IX
Менее 40% активности
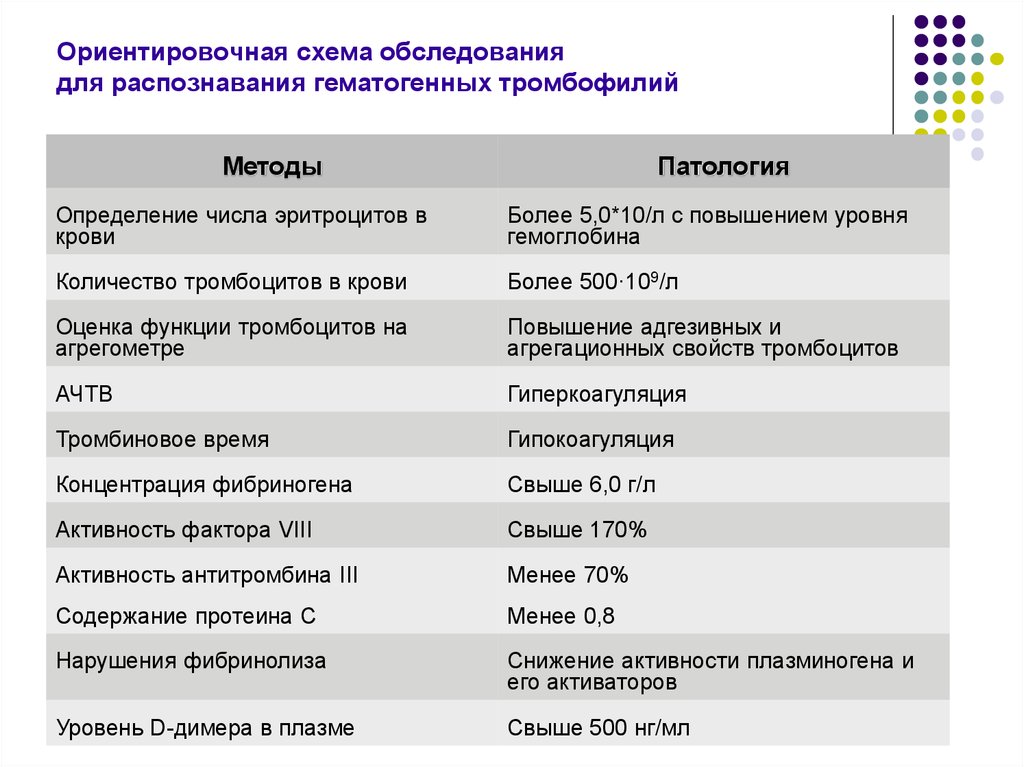
48. Ориентировочная схема обследования для распознавания гематогенных тромбофилий
МетодыПатология
Определение числа эритроцитов в
крови
Более 5,0*10/л с повышением уровня
гемоглобина
Количество тромбоцитов в крови
Более 500·109/л
Оценка функции тромбоцитов на
агрегометре
Повышение адгезивных и
агрегационных свойств тромбоцитов
АЧТВ
Гиперкоагуляция
Тромбиновое время
Гипокоагуляция
Концентрация фибриногена
Свыше 6,0 г/л
Активность фактора VIII
Свыше 170%
Активность антитромбина III
Менее 70%
Содержание протеина С
Менее 0,8
Нарушения фибринолиза
Снижение активности плазминогена и
его активаторов
Уровень D-димера в плазме
Свыше 500 нг/мл
49.
Эффективность лабораторной диагностики тромбофилийповышается в остром периоде тромбоза.
Исследование на фоне лечения противотромботическими
средствами затрудняет диагностику.
Примеры:
При оценке нарушений в системе протеина С допускается
диагностическое обследование больного только спустя 2-3 недели после
прекращения приема препарата.
При гепаринотерапии кровь на анализ забирается перед
введением очередной дозы гепарина.
50.
Скрининговая коагулограммаи маркеры активации свертывания
51. 4. Методы исследования гемостаза и их диагностическое значение
52. Биологические маркеры тромбообразования, ДВС, фибринолиза
«Биологический маркер» представляет собойпоказатель, который: можно параметрически оценить,
может быть индикатором как нормальных, так и патологических
биологических процессов;
позволяет оценивать эффективность проводимых лечебных
мероприятий.
на:
Исходя из определения биомаркеры можно подразделять
диагностические,
прогностические,
маркеры для мониторинга патологического процесса
53. Важнейшие характеристики биомаркеров: чувствительность, специфичность и прогностическая ценность
Чувствительность (Se) - это способность диагностического тестадавать правильный результат, который определяется как доля истинно
положительных результатов среди всех проведенных тестов.
Чем выше чувствительность теста, тем он более эффективен. Такие
тесты используют для исключения заболеваний на ранних этапах
диагностического процесса, когда требуется сузить круг предполагаемых
заболеваний.
Специфичность (Sp) - это способность диагностического теста не
давать при отсутствии заболевания ложноположительных результатов.
Чем выше специфичность метода, тем надежнее с его помощью
подтверждается заболевание, и тем он более эффективен.
Исследование эффективно на втором этапе диагностики, когда круг
предполагаемых заболеваний сужен и необходимо с большой уверенностью
доказать наличие болезни.
С практической точки зрения для оценки результатов исследования
интерес представляет вероятность совпадения заключения с окончательным
диагнозом. Для этих целей оценивается прогностичность теста.
Прогностическая ценность (predictive value) теста - вероятность
наличия заболевания при условии известного результата диагностического
исследования; она рассчитывается на основании данных о чувствительности
и специфичности.
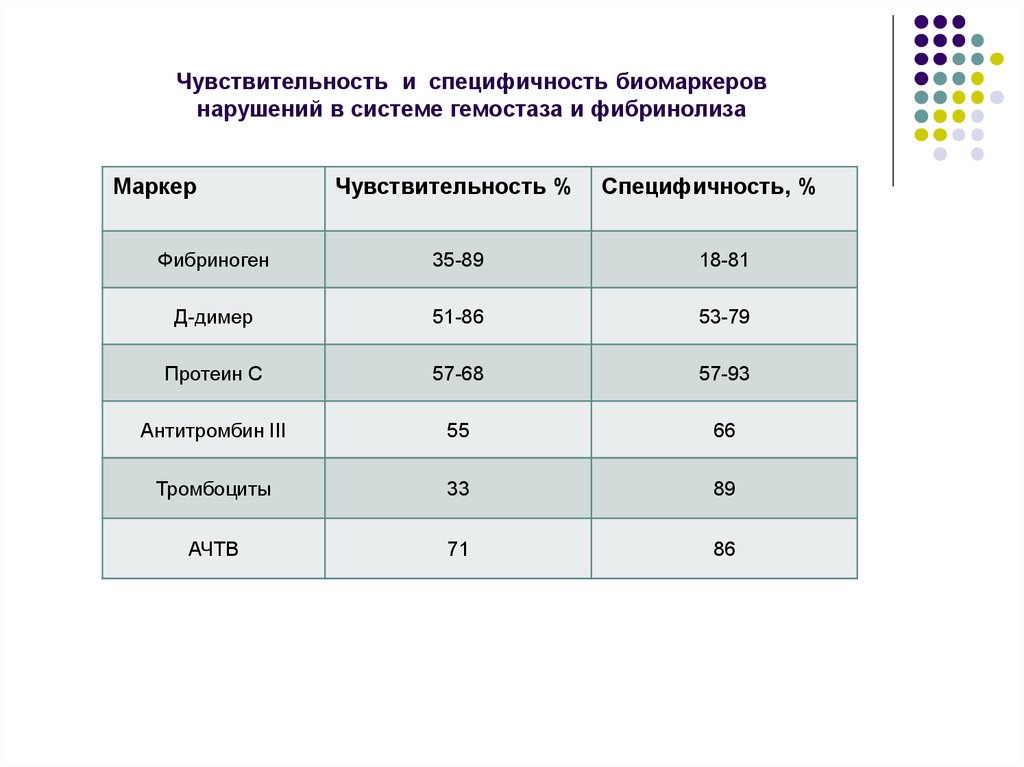
54. Чувствительность и специфичность биомаркеров нарушений в системе гемостаза и фибринолиза
МаркерЧувствительность %
Специфичность, %
Фибриноген
35-89
18-81
Д-димер
51-86
53-79
Протеин С
57-68
57-93
Антитромбин III
55
66
Тромбоциты
33
89
АЧТВ
71
86
55. Исследование сосудисто-тромбоцитарного звена
Время кровотечения - это время от момента нанесения стандартнойраны кожи до момента прекращения вытекания крови.
Характеризует функциональную активность тромбоцитов и их
взаимодействие с сосудистой стенкой. Позволяет заподозрить
тромбоцитопатии, болезнь Виллебранда.
Тест не используют для оценки эффективности приема антиагрегантов.
Норма: 2-5 мин от начала до полной остановки кровотечения.
56. Исследование сосудисто-тромбоцитарного звена
Количество тромбоцитов - в крови здорового человека колеблется всреднем между 180-320*109/л.
Нарушения гемостаза могут быть результатом изменения количества
тромбоцитов и/или их функции (качественные расстройства).
Тромбоцитопения – уменьшение количества тромбоцитов.
Тромбоцитоз или тромбоцитемия - увеличение количества тромбоцитов.
Тромбоцитопатии — нарушения функции тромбоцитов.
57. Исследование плазменного гемостаза Протромбиновое время (ПВ).
Выявляет нарушение во внешнем пути свертывания крови,точнее дефицит или снижение активности факторов II, V, VII, X,
которые наблюдаются при:
- при заболеваниях печени;
- геморрагическом диатезе новорожденных;
- дефиците витамина К (дисбактериоз слизистой оболочки кишок,
механическая желтуха, синдром мальабсорбции);
Используют для мониторинга терапии
антагонистами витамина К - непрямыми антикоагулянтами.
Удлинение ПВ - снижение % по Квику - увеличение МНО.
58. Оценка результатов измерения ПВ
Увеличение ПВ отражается в снижении % протромбина по Квикуи увеличении МНО и информирует о риске кровотечения.
Уменьшение ПВ - возрастание активности протромбина по
Квику, снижение значения МНО - может отражать гиперактивность
факторов свертывания, нарушение процедуры взятия крови.
Не имеет клинического значения.
При величине МНО>3,0 требуется обязательное повторное
исследование!
59. Исследование плазменного гемостаза Международное нормализованное отношение (МНО)
В 1983г. Комитет по стандартизации в гематологии ВОЗ принялстандартизированный показатель – МНО, который рассчитывают при
контроле лечения непрямыми антикоагулянтами.
Расчет МНО производится на основании одновременного
измерения ПВ исследуемой плазмы пациента и ПВ нормальной
донорской плазмы.
Расчетный показатель протромбинового теста исключает
колебания показателя в зависимости от используемых реагентов.
Величина МНО у лиц, не принимающих непрямые
антикоагулянты, составляет 0,8-1,2.
У пациентов, получающих антикоагулянтную терапию,
терапевтический интервал МНО выбирается в зависимости от
показаний к назначению препаратов.
60. Периодичность исследования МНО во время приема антикоагулянтов непрямого действия
Первое исследование МНО должно быть выполнено не позднее36 часов от начала терапии.
При подборе дозы варфарина МНО определяют не реже 1 раза в
3 дня. При медленном наращивании дозы в амбулаторных условиях не реже 1 раза в неделю.
После получения 2 последовательных значений МНО в
терапевтическом интервале частота исследования снижается до 1 раза
в неделю в течение 3 недель, а затем - 1 раз в месяц.
Одновременно с МНО измеряют АЧТВ не менее 2 раз в периоде
подбора дозы.
61. Исследование плазменного гемостаза Активированное частичное тромбопластиновое время (АЧТВ)
ТестАЧТВ выявляет сдвиги внутреннего пути активации
свертывания (активности факторов XII, XI, X, IX, VII, V, II).
Клиническое значение имеет удлинение АЧТВ.
Тест рекомендован для выявления
- гипокоагуляционных сдвигов,
- гемофилий,
- тромбофилии,
- синдрома ДВС,
- патологических ингибиторов свертывания,
- для контроля терапии гепарином.
62. Исследование плазменного гемостаза Активированное частичное тромбопластиновое время (АЧТВ)
Причины удлинения АЧТВ:- снижение активности факторов XII, XI, IX, VII, X, V, II;
- наличие в пробе гепарина натрия (введенный пациенту или
попавший из катетера),
- наличие в пробе продуктов деградации фибрина/
фибриногена (ДВС, гиперфибринолиз), патологических
ингибиторов плазменных факторов;
- умеренное удлинение АЧТВ может наблюдаться во время
приема непрямых антикоагулянтов за счет снижения
активности фактора IX.
63. Исследование плазменного гемостаза Активированное частичное тромбопластиновое время (АЧТВ)
Укорочение значений АЧТВ может быть связано:- со стрессом,
- физической нагрузкой,
- послеродовым состоянием у женщин,
- хирургическим вмешательством,
- недавним тромбозом глубоких вен,
- тромбоэмболиями,
- приёмом эстрогенов.
64. Исследование плазменного гемостаза Фибриноген
Один из основных белков системы свертывания крови иодновременно – белок острой фазы воспаления. Определение
содержания используется для оценки остроты воспалительного процесса
и в диагностике ДВС.
Клинически значимым является как снижение, так и увеличение
содержание фибриногена в плазме.
Уменьшение концентрации фибриногена наблюдается при:
- при снижении белково-синтетической функции печени,
- в фазе потребления при синдроме ДВС.
При воспалительном процессе содержание фибриногена в плазме
увеличивается.
Референтное значение 2-4 г/л.
65. Исследование плазменного гемостаза Тромбиновое время (ТВ)
отражает конечный этап свертывания крови - превращениефибриногена в фибрин.
Назначают:
- при заболеваниях печени: циррозе, хроническом и остром
гепатите, гепатомах;
- при симптомах повышенной кровоточивости или склонности к
тромбозам;
- при двух и более самопроизвольных прерываниях беременности в
сроки до 22 недель (АФС);
- при заболеваниях, сопровождающихся высоким риском развития
ДВС-синдрома;
- у пациентов с известным высоким риском артериальных
тромбозов (при гипергомоцистеинемии и др. генетических и
приобретенных факторах риска) и высокой концентрацией Среактивного белка.
66. Исследование плазменного гемостаза
Причины увеличения ТВ:-цирроз печени, хронический активный гепатит;
- ДВС-синдром;
- острый лейкоз;
- осложнения беременности и роды;
- дисфибриногенемия.
Причины снижения ТВ:
- тромбоцитоз.
На результат оказывают влияние:
- переливание свежезамороженной плазмы (маскирует нарушение образования
фибриногена),
- терапия нефракционным гепарином приводит к увеличению ТВ.
Референтные значения ТВ: 14-21 сек.
67. Исследование плазменного гемостаза D-димер
образуется при растворении фибринового сгустка.Диагностическое значение определения D-димера:
диагностика тромбоза глубоких вен (ТГВ) и тромбоэмболии
легочной артерии (ТЭЛА).
Исследование D-димера имеет высокую отрицательную
прогностическую значимость: при значении D-димера менее 0,5
мкг/мл – с вероятностью около 80% можно сказать, что тромбоза у
больного нет.
Исследование D-димера используют для исключения ТВГ и
ТЭЛА, но не для подтверждения заболевания.
68. Исследование плазменного гемостаза Диагностическое значение определения D-димера
- Диагностика синдрома ДВС и оценка состояния больного сподозрением на ДВС в динамике (повышение концентрации более
0,5 мкг/мл).
-
Прогностическая оценка состояния больных с сердечно-сосудистой
патологией (повышение концентрации более 0,25 мкг/мл).
-
Дополнительный критерий эффективности антикоагулянтной терапии
как при однократном исследовании, так и в динамике ( повышение
концентрации более 0,5 мкг/мл).
D-димер - маркер тромбообразования и фибринолиза.
69. Aнтитромбин III (AТ III) специфический белок системы свертывания крови
AT III блокирует факторы свертывания — тромбин, Xa, IXa, способствуяжидкому состоянию крови.
-
Когда назначается анализ:
вместе с тестами на протеин С и протеин S и на волчаночный
антикоагулянт;
при выявлении у пациента венозного тромбоза;
после удаления тромба;
у пациентов, организм которых не реагирует на гепарин, когда
необходимо применять большие дозы этого препарата.
70. Aнтитромбин III (AТ III)
Повышение уровня AT III связано с повышенным риском кровотечений.Причины повышения AT III:
- длительный прием непрямых антикоагулянтов (варфарин, фенилин);
- дефицит витамина К;
- заболевания печени;
- острый вирусный гепатит;
- воспалительный процесс;
- менструация.
Причины понижения уровня AT III:
- склонность к тромботическим осложнениям;
-поздние сроки беременности;
- середина менструального цикла.
71. Преаналитический этап
источник большинства диагностических ошибок при определениипоказателей системы гемостаза.
72. Внелабораторная часть ПЭ в гемостазиологии
Направление на анализ должно содержать:- Ф.И.О. обследуемого больного с указание пола и возраста, отделение
- указание наблюдаемых гемостазиологических нарушений
(кровоточивость, тромбозы)
- применяемые лекарственные средства (антикоагулянты,
тромболитики, ингибиторы фибринолиза и тд)
- время взятия пробы крови для анализа.
73. Образцы
Для исследования системы гемостаза используется плазма.Исследование сыворотки не информативно т.к. она:
- не содержит фибриноген,
- не содержит, или содержит в малых количествах факторы II,V, VIII, XIII
74. Венозная кровь собирается в пробирки, в качестве антикоагулянта используется цитрат натрия, который смешивается с кровью во
Взятие крови для исследования гемостазаВремя наложения жгута не должно превышать 60 сек.
- компрессия свыше 1 мин. повышает уровень фибриногена
- при 3-минутном стазе
укорачивается ПВ, АЧТВ и ТВ,
повышается уровень АТIII
и активность
факторов VII и VIII
75. Взятие крови для исследования гемостаза
Первые несколько мл крови непригодны для исследованиясистемы гемостаза т.к. в ней содержится тканевой
тромбопластин, который может фальсифицировать результаты
исследования
После взятия образца венозной крови следует немедленно
перевернуть пробирку 3-4 раза
Если перемешивание выполнено слишком поздно или
недостаточно тщательно, то возможно частичное свертывание в
образце .
76.
В случае, если у пациента стоит центральный венозныйкатетер
На результат исследования влияют факторы:
- мертвое пространство внутри катетера с возможным стазом
крови,
- активация свертывания на стенке катетера,
- применение инфузионных растворов и гепарина для
поддержания проходимости катетера
Исследование крови из центрального катетера должно
проводиться только в исключительных случаях!
77. В случае, если у пациента стоит центральный венозный катетер
Если необходимо забрать кровь из центрального катетераРекомендуется следующая процедура:
1) сбросить первые 10-20 мл. крови, или использовать эту кровь для других
видов исследований.
2) приоритет в коагуляционных тестах должны получать гепариннезависимые тесты (ПВ, фибриноген, антитромбин).
3) не выполнять гепаринзависимые тесты в течение нескольких часов после
инъекции гепарина в катетер или добавить в образец плазмы
гепариназу - фермент, разрушающий гепарин.
78. Если необходимо забрать кровь из центрального катетера
ТранспортировкаУсловия:
- исключить встряхивание и транспортировку во льду (возможна
активация свертывания (VII, XII), которые укорачивают время
образования сгустка при выполнении исследования.
79. Транспортировка
Возможные источники ошибок1. Неправильное соотношение кровь/цитрат
Недостаточное количество крови:
- повышенная концентрация цитрата
- ложно завышенные результаты
Слишком большой обьем крови
- использование шприца для внесения крови в пробирку
80. Возможные источники ошибок
2. Образцы со сгустками3. Гемолиз образца
4. Иктеричные или липемичные образцы
81. Возможные источники ошибок
Благодарю за внимание!82.
АнтикоагулянтыПрямого действия – оказывают непосредственное влияние на активность циркулирующих
в крови факторов свертывания
- зависимые от АТ III ингибиторы тромбина:
нефракционированный гепарин,
НМГ: ардепарин, дальтепарин и др.,
сулодексид (вессел)
гепариноид данапароид (ломопарин, оргаран и др.).
- независимые от AT III ингибиторы тромбина:
гирудин
олигопептиды аргатробан, иногатран, новостан и др.
Непрямого действия
83. Антикоагулянты
Наиболее частые формы приобретенных тромбофилий1. Дефицит антитромбина III
2. Дефицит протеинов C и S
3. Снижение атромбогенности сосудистой стенки
(антифосфолипидный синдром)
4. Увеличение активности факторов II, VIII, XII
5. Повышение функциональной активности тромбоцитов
6. Снижение фибринолитической активности крови
7. Повышение активности или синтеза фактора Виллебранда
84. Наиболее частые формы приобретенных тромбофилий
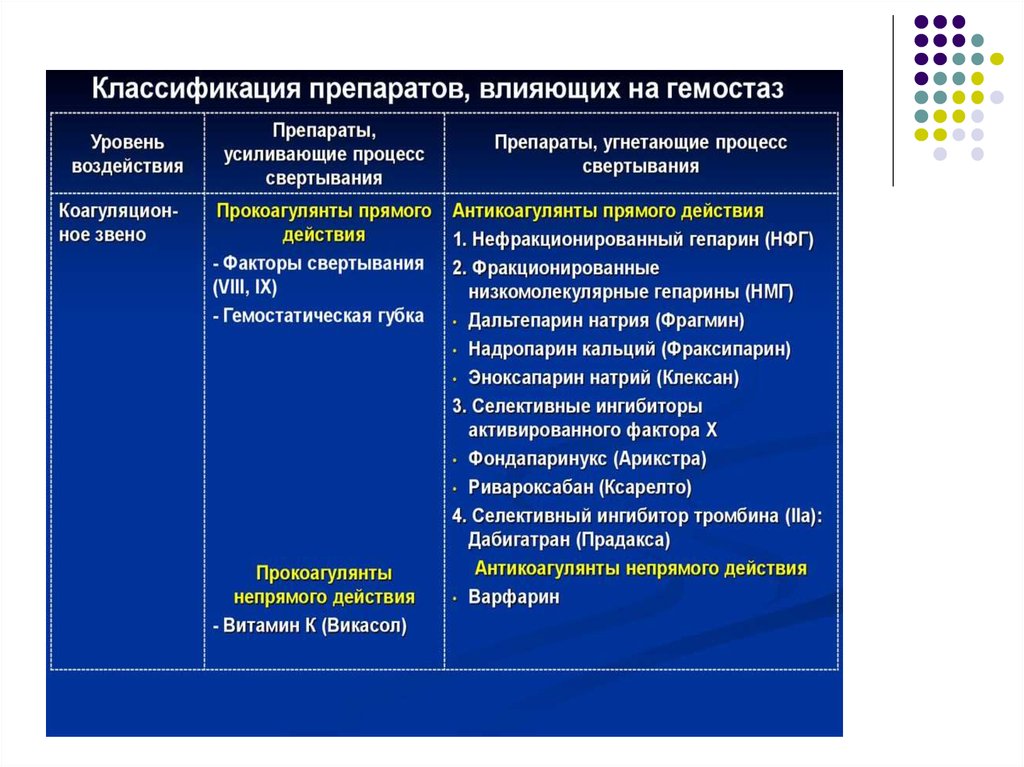
ПРОКОАГУЛЯНТЫ85.
Образование Д-димера86. Образование Д-димера
87.
88.
Тромбофилиясостояние, при котором увеличен риск
тромбоэмболических проявлений, а фактором риска
являются нарушения гемостаза, включая фибринолиз.












































































 medicine
medicine








