Similar presentations:
Распределение выбросов производственной пыли
1.
12.
23. Распределение выбросов производственной пыли, %
строительные материалы — 34,7;тепловые электростанции — 29,5;
автотранспорт — 15,8;
черная металлургия — 12,4;
химическая промышленность — 4,6;
цветная металлургия — 2,2;
нефтеперерабатывающая
промышленность — 0,5;
прочие — 0,3
3
4.
Пылевые частицы имеют большую суммарнуюповерхность (высокую биологическую и химическую
активность).
Некоторые вещества в аэродисперсном состоянии
приобретают новые, опасные свойства (способность
взрываться).
4
5.
Частицы промышленной пыли имеют разнообразнуюформу и размеры и даже при одной и той же массе
оседают с разной скоростью.
Поэтому аппаратура пылеулавливания многообразна,
хотя в ее основе лежат немногие основные принципы
5
6. 4 группы современных аппаратов для обеспыливания отходящих газов
1. механические обеспыливающие устройства,в которых пыль отделяется под действием
гравитационных,
инерционных
или
центробежных сил;
2. мокрые или гидравлические аппараты, в
которых твердые частицы улавливаются
жидкостью;
3. пористые фильтры, удерживающие тонкую
пыль;
4. электрофильтры, в которых осаждение
пыли осуществляется за счет ионизации
газа и содержащихся в нем пылинок.
6
7. Механические обеспыливающие устройства используются для предварительной очистки отходящих газов; выбор оптимального типа
аппаратурыопределяется гранулометрическим составом пыли.
7
8.
Простейшие аппараты - осадительные камеры. Дляосвобождения газов от грубодисперсной пыли (размер
частиц 500—50 мкм) и обеспечивают степень очистки
40—50%.
Из инерционных аппаратов центробежного действия
наибольшее распространены циклоны.
8
9.
Распростанены мокрый (гидравлический) способочистки промышленных газов от пыли, имеющий
высокую эффективность и требующий значительно
меньших затрат по сравнению с методом сухой очистки.
9
10. Мокрая очистка
В полых и насадочных аппаратах запыленные газыпропускают
через
поток
распыляемой,
разбрызгиваемой или стекающей по насадке жидкости.
Частицы пыли захватываются потоками промывной
жидкости и осаждаются в аппарате, а очищенные газы
выбрасываются в атмосферу, для частиц пыли
размером более 10 мкм.
10
11.
1112. Мокрая очистка
В барботажных и пенных аппаратах запыленныегазы пропускаются сквозь слой жидкости или пены;
большая
поверхность
соприкосновения
газа
с
жидкостью (пеной) обеспечивает высокую степень его
очистки от взвешенных частиц, улавливается до 99%
частиц размером от 2 мкм и более.
12
13. Мокрая очистка
Мокрыегазоочистные
аппараты
ударноинерционного типа по принципу инерционного
осаждения частиц во время преодоления очищаемыми
газами препятствия или при резком изменении
направления
движения
газового
потока
над
поверхностью жидкости.
Их производительность по газу составляет от 2500 до 90 000 м3/ч,
а эффективность очистки составляет 98— 99,6%.
13
14. Фильтрация через пористые перегородки
Высокая степень очистки, чем сухое или мокроепылеулавливание; стабильная работа в широком
диапазоне температур, физико-химических свойств
улавливаемых частиц и расхода газа.
Недостаток: необходимая регенерация фильтра
14
15. Промышленные фильтры условно делят на два класса: тканевые и зернистые.
тканевые рукавные фильтры, состоящие из рядатканевых рукавов с заглушенным верхним отверстием,
которые укреплены в металлическом кожухе.
15
16. Зернистые фильтры
Возможность работы в агрессивныхсредах и при высоких температурах,
выдерживать
большие
механические нагрузки и перепады
давления.
В
качестве
фильтрующих
материалов
используют
песок,
гальку,
шлаки,
кокс,
графит,
древесные
опилки
и
другое
дешевое и доступное сырье.
.
16
17.
Различают фильтры насыпные снеподвижным
фильтрующим
веществом
и
фильтры
с
движущейся
средой
и
непрерывным
удалением
из
установки частиц зерен.
Недостаткок:частая регенерация
17
18. Электрофильтры
Принцип действия электрофильтра - пылевидным частицамсообщается заряд, после чего они осаждают на противоположно
заряженном (осадительном) электроде, откуда пыль периодически
удаляют.
18
19.
В сухих электрофильтрах улавливают твердые частицы,которые удаляются с осадительного электрода
встряхиванием.
В мокрых электрофильтрах можно улавливать не
только твердые, но и жидкие примеси отходящих газов
(туманы) которые смываются с поверхности электродов
водой.
19
20. Очистка атмосферных выбросов от кислых компонентов.
Основные методы очистки:• Адсорбционные методы основаны на избирательном
поглощении газов или паров жидкостями на
поверхности раздела фаз.
• Абсорбционные методы очистки газов основываются
на физической сорбции компонентов отходящих
газов твердыми телами.
• Каталитические
методы
основаны
на
каталитических
реакциях
окисления
или
восстановления кислых компонентов с последующим
их выделением.
20
21. Очистка газов от оксидов углерода.
1. Поглощение СО2 растворами этаноламинов:2RNН2 + С02 + Н20 = (RNН3)2СО3
(RNН3)2СО3 + С02 + Н20 = 2RNН3НСО3
2RNН2 + С02 = RNНСООNH3R
2. Поглошение СО2 холодным метанолом, цеолитами
21
22. Очистка газов от диоксида серы
Диоксид серы S02 оказываетсильное токсическое действие
уже при концентрации в воздухе
0,25 - 0,50 мг/м3, а при средней
концентрации более 0,50 мг/м3
отмечается
повышение
смертности
и
числа
госпитализаций.
В
нашей
стране
на
S02
установлены
следующие
предельно
допустимые
концентрации: ПДКр.з. - 10 мг/м3,
ПДКм.р - 0,03 мг/м3 и ПДКс.с 0,005 мг/м3. (рабочей зоны,
максимально
разовая,
среднесуточная)
22
23. Очистка газов от диоксида серы
Три основные группы методов очистки:1) аммиачные методы, позволяющие получать
сульфит и гидросульфит аммония, которые
используются как товарные продукты;
23
24. Аммиачный метод
NH4OH + S02 + Н20 = (NН4)2S03 + 2Н20S02 + (NН4)2S03 + Н20 = 2NН4НS03
2(NН4)2S03 +O2 = 2(NН4)2S04
(NН4)2S03 + 2HNO3 = NH4NO3 + SO2 + H2O
2NН4НS03 + HNO3 = NH4NO3 + SO2 + H2O
товарный диоксид серы и соли аммония находят
широкое применение в качестве удобрений (газ
содержит 15-30% SO2):
24
25.
2)методы нейтрализации - высокая степень очисткигазов, но образуются побочные продукты сульфиты и
сульфаты, не имеющие широкого спроса в народном
хозяйстве
25
26. Метод нейтрализации
Содовый метод - пропускание отходящих газовчерез раствор соды
2Nа2СО3 + S02 + Н20 2NаНСО3 + Nа2S03
2NаНСО3 + S02 Nа2S03 + 2С02 + Н20
Nа2S03 + S02 + Н20 2NаНS03
Образующийся раствор взаимодействует
оксидом цинка:
NаНS03 + ZnO ZnSO3 + NaOH
Сульфит цинка обжигают:
ZnSO3 = ZnO + S02
с
26
27. Метод нейтрализации
При очистке отходящих газов сернокислотнойпромышленности используется известковый
метод - поглощение S02 и тумана серной
кислоты суспензией оксида кальция СаО.
Н2S04 + СаО = СаS04 + Н20
S02 + СаО + 2Н20 = СаS03 * 2Н20
СаS03 + 2Н20 + 1/202 = CaSO4 * 2Н20
Степень очистки газов известковым методом
достигает
85%,
а
технологическое
оборудование
отличается
простотой
и
надежностью
27
28.
3) методы каталитического окисления S02 до S03 споследующим получением разбавленной серной
кислоты.
В качестве катализаторов для доокисления S02 до S03
используются пиролюзит, активированный уголь и ряд
других веществ,
в качестве окислителей - кислород воздуха, озон О3,
надсерная кислота Н2S208.
28
29.
2930. Очистка отходящих газов от сероводорода
Сероводородсильный
нервнотоксичный яд, при
вдыхании которого в
концентрации 1мг/л
почти
мгновенно
развивается
отравление, которое
оканчивается
смертью от остановки
дыхания.
Выброс, млн. т. в год
Автомобили Электростан
ции, заводы
и т.д.
Оксид
углерода
59,7
5,2
Оксиды
азота
5,5
6,5
Серосодерж
ащие
соединения
1,0
22,4
Макрочасти
цы
1,0
9,8
30
31. Окислительные методы
Поглощение H2S водными растворами Na2CO3,K2CO3, NH3 с последующим окислением
кислородом воздуха до элементарной серы.
31
32.
2Н2S + 02 = 2Н2О + 2Sмышьяково- содовый метод
Nа4АsS502 + Н2S = Nа4Аs2S6О + Н2О
Nа4Аs2S6О + 1/202 = Nа4АsS502 + S
Достоинства: высокая степень очистки (90 98%) и селективность поглощения Н2S, в
присутствии больших количеств С02.
32
33. Фосфатный метод
Для газов содержащих смесь СО2 и Н2S:Н2S + К3Р04 = К2НР04 + КНS
Для очистки газов, не содержащих С02,
обычно используют 40 - 50%-ный раствор
К3Р04;
в присутствии С02, во избежание
осаждения гидрокарбоната - 35%-ный
раствор.
33
34.
При пропускании газов через слой болотной рудыпротекала реакция
Fе203 + ЗН2S = Fе2S3 + ЗН20
после чего через аппарат пропускали воздух:
2Fе2S3 + 302 = 2Fе203 + 6S
В последующем эти стадии совместили, добавляя
необходимое количество кислорода или воздуха.
34
35. Очистка отходящих газов от оксидов азота
ПромышленностьНаиболее устойчив в
атмосферном
воздухе
диоксид азота N02, в Тепловые электростанции
который
переходят
Автотранспорт
постепенно
другие
оксиды
азота,
Черная металлургия
выброшенные
в
атмосферу. ПДКм.р, и Строительные материалы
ПДКс.с для этого газа
Химическая
составляют 0,085 мг/м3 ,
промышленность
а в воздухе рабочих зон
промышленных
Нефтеперерабатывающая
промышленность
предприятий ПДКр.з N02
равна 5 мг/м3 .
Выбросы
NO2, %
72,5
17,3
6,1
1,8
1,7
0,6
35
36. Классы методов очистки газов от соединений азота в зависимости от источника выброса
Окислительные , восстановительные, сорбционныеВыбросы в атмосферу при сжигании топлив, т/год
выбросы
Диоксид азота
Природный
газ
280000
Мазут
(топочный)
23000
Уголь (бурый)
45000
Оксид углерода
30000
28000
53000
Диоксид серы
-
150000
270000
36
37. Окислительные методы
Основаны на окислении оксида азота кислородомвоздуха, озоном, водными растворами Н202, КМn04,
K2Cr2O7, КClO3, HNO3 и ряда других.
Окисление NО до N02 проводится в газообразной или
жидкой фазе с последующим получением азотной
кислоты.
Окисление NО в жидкой фазе протекает с несколько
меньшей скоростью, чем в газообразной, причем
лимитирующей стадией процесса является скорость
растворения кислорода.
37
38.
Для интенсификации процесса улавливания оксидовазота используют более сильные окислители, чем
кислород, например озон или озоно-кислородную
смесь.
При введении озона в жидкую рабочую смесь
протекает реакция:
2N0 + О3 + Н20 = 2НNО3
А окисление NО в газовой фазе позволяет использовать
лишь один атом О в молекуле О3:
N0 + О3 = NO2 + 02
38
39. Альтернативные окислители
Скорость процесса окисления NО существенновозрастает при замене кислорода или озона жидкими
окислителями, т. е. водными растворами Н202, КМn04,
КBrО3, НNО3, (NН4)2Сr207, Nа2Сr04, К2Сr207
39
40.
4041. Аппараты
Высокие скорости процесса достигаются в полыхраспылительных
аппаратах
за
счет
развитой
поверхности взаимодействующих фаз, такие аппараты
широко используются в очистных сооружениях.
41
42. Катализаторы
Эффективность очистки отходящих газов, скоростьокисления NO существенно возрастают в присутствии
катализаторов.
В качестве которых используются гранулы полиэтилена,
шамот, известняк, динас, кокс, пропитанный солями Mn,
Сu, Сr, доломит, оксид алюминия, стекловолокно,
силикагель и др.
42
43. Восстановительные методы
Восстановление до нейтральных продуктов жидкимиили газообразными восстановителями в присутствии
катализаторов или под действием высоких температур.
При нормальной температуре в присутствии кислорода
самопроизвольно протекает процесс окисления оксида
азота NО:
NО N203 N02 N204 N205
43
44. Процессы NO
С возрастанием температуры идет обратныйпроцесс:
В-во
N2 0 5
N 204
N02
NО
N2 + 0 2
Т С
-11,2
21,5
140
600
10 000
44
45.
КатализаторыНаиболее
высокой
каталитической
активностью
отличаются катализаторы на основе сплавов платины,
родия, палладия. Их содержание в катализаторах
колеблется от 0,1 до 2%, а в качестве носителя
применяют оксид алюминия, керамику, силикагель,
металлическую ленту и другие материалы.
Высокая степень очистки газов от оксидов азота остаточное содержание в газовых выбросах не
превышает 5 * 10-4 %.
45
46. Восстановители
В качестве восстановителей в очистных сооруженияхиспользуют метан, водород, природный газ, пары
керосина, аммиак, нефтяной и коксовый газы,
азотоводородную смесь.
46
47. Схемы реакции
Восстановление оксидов азота протекает по схемам:4NО + СН4 = 2N2 + С02 + 2Н20
2N02 + СН4 = N2 + С02 + 2Н20
или
2NО + 2СО = N2 + 2С02
2N02 + 4СО = N2 + 4С02
или
2NО + 2Н2 = N2 + 2Н20
2N02 + 4Н2 = N2 + 4Н20
или
6NО + 4NН3 = 5N2 + 6Н20
6N02 + 8NН3 = 7N2 + 12Н20
47
48.
4849. Очистка отходящих газов от аммиака.
Аммиак NН3, являющийся исходным сырьемдля
производства
азотной
кислоты
и
находящий применение во многих химических
производствах,
обладает
токсическими
свойствами и вызывает раздражение слизистых
оболочек, ожоги, удушье.
В воздухе рабочей зоны его ПДКр.з. составляет
20 мг/м3, а в воздухе населенных пунктов
ПДКм.р. и ПДКс.с. не превышают 0,2 мг/м3.
49
50. Способы очистки
Простейшимспособом
очистки
отходящих газов от аммиака является его
абсорбция водой.
Иногда водную очистку дополняют
доочисткой раствором серной кислоты с
получением сульфата аммония:
2NНЗ + Н2S04 = (NH4)2S04
Этот процесс практически необратим и
его
можно
проводить
в
простых
одноступенчатых аппаратах.
50
51.
5152. Очистка отходящих газов от галогенов и их соединений
Основными источниками поступления в атмосферусоединений фтора являются производства фосфорных
удобрений, фтороводородной кислоты и ее солей,
фторорганических соединений и металлического
алюминия.
В дымовые газы фтор поступает в виде НF, SiF4 и
тумана Н2SiF6. Для их выделения используют методы
сухой и мокрой абсорбции
52
53.
5354. Сухая очистка от НF
В качестве сухих хемосорбентов используютизвестняк СаСО3, активированный оксид
алюминия Аl203.
При пропускании сквозь слой молотого
известняка отходящих газов протекает реакция:
2НF + СаСО3 = СаF2 + Н20 + СО2
Отработанный хемосорбент содержит 80—95%
СаF2 и используется как товарный флюорит.
Степень очистки газовых выбросов от НF
достигает 95%.
54
55. Мокрая очистка от НF
В основе очистки фторсодержащих газов методоммокрой абсорбции лежит улавливание НF и SiF4
водой в насадочных или пенных колоннах.
Газообразный фтороводород растворяется в воде:
НF(г) +Н20 = НF(ж) = Н3О+ + Fравновесие сильно сдвинуто вправо.
Парциальное давление НF над водным раствором
очень мало и зависит от температуры и содержания
НF в жидкой фазе: при повышении ее до 1 % и выше
орошающая жидкость заменяется.
55
56. Основные источники поступления хлора и его соединений в атмосферу
1. Промышленное получение хлора и щелочейметодом электролиза хлоридов.
2. Переработке руд титана, ниобия, тантала и
других металлов методом хлорирующего
обжига.
3.Получение соляной кислоты и многих
хлорорганических соединений.
4.Печи сжигания хлорсодержащих промышленных
отходов
и
бытового
мусора,
содержащего полимерные материалы.
56
57. Способы очистки от хлора
1.Абсорбционные2.Хемосорбционные
Сорбенты: вода, растворы щелочей,
водорастворимых органических соединений и в ряде случаев органические
растворители;
чаще всего едкий натр, сода, известковое
молоко.
57
58. Проблемы выделения НСl
НСlвыделяют
абсорбцией
водой
или
щелочными растворами в разнообразных
аппаратах - насадочных скрубберах, в
аппаратах пенного типа и т. п.
58
59.
Недостатком поглощения НСl водой в насадочныхаппаратах является интенсивное образование тумана
капельно-жидкой соляной кислоты, улавливание
которой происходит менее интенсивно, чем
газообразного НСl. Поэтому степень извлечения НСl
этим методом не превышает 88%.
59
60. Проблема утилизации НСl
Утилизация НСl отходящих газов представляетсложную
проблему
современной
химической
промышленности.
Ряд
направлений
возможного
использования
хлороводорода из промышленных газов:
1) переработка в концентрированную соляную кислоту;
2) получение хлоридов некоторых металлов (СаСl2,
FеСl2, ZnCl2, ВаСl2 и др.);
3) использование для целей гидрохлорирования и
окислительного
хлорирования
органических
соединений;
4)
переработка в хлор методами простого
каталитического
окисления,
электролиза
химической конверсии
и
и
60
61. Очистка отходящих газов от углеводородов
Для рекуперации газообразных углеводородови паров органических веществ наибольшее
распространение
получили
методы
адсорбции.
Адсорбент - активные угли. Периодические
адсорберы
со
стационарным
слоем
адсорбента работающие по четырех-, трехи двухфазному циклам:
1. адсорбция
2. десорбция
3. сушка
4. охлаждение
61
62. Источники поступления Hg в атмосферу
1.Предприятия цветной металлургии2.Теплоэнергетики
3.Химической и др. отраслях
В
зависимости
от
состава
и
объема
ртутьсодержащих выбросов их очистку проводят:
1.Физическими
методами
(конденсационные,
абсорбционные, адсорбционные)
2.химическими (хемосорбционные) методами.
62
63. Очистка от ртути
Для предварительной очистки концентрированных портути газов используют физические методы- адсорбцию
активным углем.
Присутствующий в сухих газовых потоках диоксид серы
дезактивирует
адсорбент,
резко
снижая
его
поглотительную способность по отношению к ртути.
При наличии в очищаемых газах кислорода и паров
воды в адсорбенте происходит окисление SO2:
SO2 + H2O + 0,5O2 H2SO4
Образующаяся серная кислота взаимодействует с
ртутью с образованием HgSO4.
63
64. Высокотемпературное обезвреживание газов
Прямое сжигание применяют для обезвреживания газовот легко окисляемых токсичных, а также дурно
пахнущих
веществ.
Оно
применяется
для
обезвреживания практически любых паров и газов
продукты сжигания, которых менее токсичны, чем
исходные вещества. Процесс проводят в обычных
топочных устройствах, в промышленных печах и топках
котельных агрегатов, а также в открытых факелах.
64
65.
6566. Тема 4. ОЧИСТКА СТОЧНЫХ ВОД
Методы очистки сточных вод можно условноподразделить на:
Деструктивные
методы
очистки
сводятся
к
разрушению загрязняющих воду веществ путем их
окисления или восстановления. Образующиеся при
этом продукты распада удаляются из воды в виде
осадков или газов или остаются в ней в форме
растворимых минеральных солей.
Регенеративные методы позволяют извлекать и
утилизировать содержащиеся в воде ценные
вещества. Регенеративные методы далеко не всегда
очищают воду до такого состояния, в котором ее
можно сбрасывать в водоемы. В этих случаях воду
доочищают деструктивными методами
66
67. Основные стадии очистки сточных вод
1. механическая очистка, предназначенная дляосвобождения воды от взвешенных и
коллоидных частиц.
2. удаление из воды растворенных в ней
химических
соединений
физикохимическими,
химическими,
электрохимическими,
биологическими
методами.
Во многих случаях приходится применять
комбинации из указанных методов
67
68. Основные методы очистки сточных вод
1) для удаления грубодисперсных частиц - отстаивание,флотация, фильтрация, осветление, центрифугирование;
2) для удаления мелкодисперсных и коллоидных частиц коагуляция,
флокуляция,
электрические
методы
осаждения;
3)
для очистки от неорганических соединений дистилляция, ионообмен, обратный осмос, реагентное
осаждение, методы охлаждения, электрические методы;
68
69. Основные методы очистки сточных вод
4)для очистки от органических соединений экстракция, абсорбция, флотация, ионообмен,
реагентные методы; биологическое окисление;
жидкофазное
окисление,
озонирование,
хлорирование, электрохимическое окисление;
5) для очистки от газов и паров - отдувка, нагрев,
реагентные методы;
6) для уничтожения вредных веществ - термическое
разложение.
69
70. Очистка сточных вод от взвешенных частиц
Сравнительно крупные частицы размером более 15 - 20мм задерживают методом процеживания.
С этой целью на пути движения сточных вод
устанавливают разнообразные решетки, сетки и сита,
которые могут быть подвижными или неподвижными;
нередко их совмещают с дробилками для измельчения
загрязнений.
70
71. Основные стадии очистки СВ
7172. Песколовки
После процеживаниясточные
воды
поступают
в
песколовки,
предназначенные для
отделения
более
мелких минеральных
примесей
с
относительно высокой
плотностью.
72
73.
При движении воды в резервуарепесколовки на ее дно оседают взвеси с
диаметром зерен более 0,25 мм.
Осадок
с
помощью
скребков
перемещается в специальный бункер,
откуда удаляется на песковую площадку
для обезвреживания.
Песколовки облегчают условия работы
сооружений для дальнейшей очистки
стоков.
73
74.
Для выделения более мелких органических иминеральных взвесей используется метод
отстаивания с использованием первичных и
вторичных отстойников:
первичные устанавливают перед сооружениями
для биологической очистки воды,
вторичные используют для осветления сточных
вод, уже прошедших биологическую очистку.
Различают
отстойники
периодического
и
непрерывного действия. По направлению
движения воды они делятся на горизонтальные,
вертикальные и радиальные.
74
75.
7576.
Для удаления всплывающих примесей:масел,
жиров,
смол,
нефти
и
нефтепродуктов,
плавающих
на
поверхности сточных вод используют
различной конструкции маслоуловители,
жироловки, нефтеловушки.
Отделение этих примесей от воды
осуществляется за счет разности их
плотностей.
76
77.
7778.
Механическиепримеси
нередко
отделяют
на
гидроциклонах и центрифугах, где частицы взвеси
выделяются из воды под действием центробежных сил.
Гидроциклоны очень просты по устройству и
обслуживанию, компактны, дешевы и имеют высокую
производительность.
Механическая очистка сточных вод обычно является
предварительной и предшествует более глубоким
методам очистки стоков.
78
79.
Для отделения тонкодиспергированных твердых илижидких веществ, не осевших при отстаивании,
используется фильтрование. При очистке сточных вод
используют фильтры с сетчатыми элементами и
фильтры с фильтрующим зернистым слоем.
79
80. Физико-химические методы очистки сточных вод
ФХ - методы для освобождения стоков оттонкодиспергированных взвесей, не улавливаемых
фильтрацией, и растворимых газов, неорганических и
органических соединений. Удаляются
токсичные,
биохимически не окисляемые соединения.
80
81. Флотация
Для удаления из сточных вод тонкодисперсныхнерастворимых взвесей, которые отстаиваются очень
медленно, применяют флотацию.
81
82. Флотация
Флотационные установки широко применяют дляочистки
сточных
вод
нефтеперерабатывающих,
целлюлозно-бумажных,
кожевенных,
машиностроительных, пищевых, химических и других
производств, при производстве клея и искусственного
волокна, рафинировании масел, также для выделения
активного ила после биохимической очистки.
82
83.
8384. Метод адсорбции
Для глубокой очистки сточных вод от растворимыхорганических соединений (фенолов, пестицидов,
ароматических нитросоединений, ПАВ, красителей и т.
д.) используют метод адсорбции, эффективность
которого колеблется от 80 до 95% в зависимости от
химической
природы
адсорбента,
величины
адсорбирующей поверхности, а также от структуры и
свойств улавливаемых примесей.
84
85. Метод адсорбции
Очищаемуюводу
пропускают
через
фильтр,
загруженный сорбентом (динамическая адсорбция),
после насыщения загрязняющими веществами сорбент
отделяют от очищенной воды отстаиванием или
фильтрацией (статическая адсорбция).
Самым эффективным, но и самым дорогим сорбентом,
применяемым в схемах водоочистки, является
активированный уголь. Дешевле – торф, его сжигают.
85
86. Ионообменная очистка
Для извлечения из сточных вод металлов (цинка, меди,хрома, никеля, свинца, ртути, кадмия, ванадия,
марганца), а также соединений мышьяка, фосфора,
цианидов
используется
ионообменная
очистка,
позволяющая не только освобождать воду от
загрязнения токсичными элементами, но и улавливать
для повторного использования ряд ценных химических
соединений.
86
87.
В процессах водоочистки используют природныенеорганические и органические иониты
цеолиты,
глинистые
минералы,
фторапатит,
гидроксилапатит
К органическим - гуминовые кислоты почв и углей.
И синтетические иониты: неорганические (силикагели и
труднорастворимые оксиды и гидроксиды алюминия,
хрома, циркония) и органические (главным образом
ионообменные смолы).
87
88.
8889. Ионообменные смолы
В водоочистных сооружениях - синтетические ионообменныесмолы, высокомолекулярные соединения:
при контакте с катионитом
RS03Н + NаСl = RSО3Nа + НСl
при контакте с анионитом
RОН + NаСl = RСl + NаОН
В воде иониты не растворяются, а набухают, причем размеры их
микропор возрастают от 0,5 - 1,0 нм до 4 нм, а объем ионита
увеличивается в 1,5 - 3,0 раза. Набухание влияет на селективность
ионита, так как при малом размере его пор крупные ионы не могут
достичь внутренних функциональных групп.
89
90. Экстракция
Для очистки сточных вод от фенолов, масел,органических кислот и других вредных органических
примесей. Экстрагенты - органические раствори-тели,
нерастворимые в воде: бензол и некоторые его
производные, серо-углерод, тетрахлорид углерода,
минеральные масла.
90
91. Требования к экстрагенту:
1) растворять извлекаемое вещество гораздо лучше,чем вода,
т. е. обладать высоким коэффициентом
распределения;
2) обладать хорошей селективностью по отношению к
извлекаемым примесям;
3) иметь низкую растворимость в сточной воде и не
образовывать с ней устойчивых эмульсий;
4) существенно отличаться от сточной воды по
плотности, так как значительная разность плотностей
обеспечивает быстрое и полное разделение фаз;
5) регенерироваться простым и дешевым способом;
6) не взаимодействовать с извлекаемым веществом,
так как это может затруднить регенерацию
экстрагента и увеличить его потери;
7) по возможности не быть токсичным и взрывоопасным
и не вызывать коррозии материала аппарата.
91
92. Экстракция
Экстракция осуществляется в колонных и другихаппаратах с насадкой.
Если плотность экстрагента меньше плотности воды,
его подают в аппарат снизу, в противном случае сверху. После насыщения извлекаемой примесью
экстрагент направляют в отстойники, где происходит
разделение жидкостей, а воду - на дальнейшую
обработку.
92
93. Целесообразность
Определяется ценностью извлекаемых примесей и ихконцентрацией. Для каждого вещества существует
«концентрационный предел» рентабельности его
экстрагирования.
93
94. Эвапорация и десорбция
Сточные воды с летучими примесями (сероводородом,сероуглеродом, аммиаком и др) используются методы
эвапорации и десорбции.
Эвапорацию (отгонку с водяным паром) сточных вод
осуществляют в периодически действующих аппаратах
или в дистилляционных колоннах непрерывного
действия.
94
95.
Десорбциюлетучих
примесей
инертными
малорастворимыми газами (азот, диоксид углерода)
обычно проводят в тарельчатых, насадочных и
распылительных колоннах.
Степень удаления летучих веществ из сточных вод
увеличивается с ростом температуры газо - жидкостной
смеси и поверхности контакта фаз.
95
96. Аэрация
Если сточные воды содержат дурно пахнущие вещества- меркаптаны, амины, сероводород, альдегиды,
некоторые
углеводороды,
они
обязательно
подвергаются
дезодорации,
т.
е.
устранению
неприятного запаха.
96
97.
Метод аэрации заключается в продувании воздухачерез сточную воду. Недостаток метода - не все
загрязнения удается удалить и часть их остается в
сточной воде.
97
98. Коагуляция и флокуляция
Эти методы требуют расхода реагентов и потому дороги.Коагуляция - это процесс укрупнения диспергированных частиц и
объединения их в агрегаты под влиянием физических и химических
процессов, самопроизвольно протекающих в растворе, или под
влиянием внесенных в раствор специальных веществ коагулянтов.
98
99.
В процессах водоочистки в качестве коагулянтовиспользуют соли железа (FeCl3), алюминия (Al2(SO4)3),
кремниевую кислоту, полиакриламид и вещества,
обладающие высокими адсорбционными свойствами:
глину, золы и шлаки, активированный уголь, гуминовые
вещества.
Иногда для коагулирования достаточно изменить рН.
Например, при подкислении бытовых стоков выпадают
в осадок мыла и труднорастворимые в воде
высокомолекулярные
жирные
кислоты.
Удобно
использовать в качестве коагулянтов феррохромовые
шлаки: они одновременно нейтрализуют кислые стоки и
освобождают их от взвесей и коллоидов
99
100.
Метод коагулирования широко применяется приочистке сточных вод текстильных предприятий, фабрик
искусственного
волокна,
нефтеперерабатывающих
заводов и заводов химической промышленности, а
также стоков банно-прачечных предприятий.
100
101. Флокуляция
Процесс агрегации взвешенных частиц при добавлениив сточную воду высокомолекулярных соединений.
Флокуляцию проводят для интенсификации процесса
образования хлопьев гидроксидов алюминия и железа
и повышения скорости их осаждения. Использование
флокулянтов позволяет снизить расход коагулянтов и
при этом ускорить процесс осветления сточных вод.
101
102.
102103. Электрохимические методы очистки сточных вод
Электрофлотация,электрокоагуляция,
электродиализ,
анодное
окисление и катодное восстановление - методы позволяют проводить
очистку сточных вод непрерывно или периодически, использовать
автоматизированные
технологические
схемы
и
извлекать
из
промышленных стоков ценные продукты.
• Электрофлотация – процесс очистки сточных вод от взвешенных
частиц при помощи пузырьков газа, образующихся при электролизе
воды. На аноде образуются пузырьки кислорода, а на катоде –
водорода.
• Электрокоагуляция – процесс очистки сточных вод от взвешенных
частиц. Под действием тока происходит растворение металла анода
(железа или алюминия), которые в виде катионов встречаясь с
гидроксидными группами, образуют гидроксиды металлов в виде
хлопьев. Наступает интенсивная коагуляция.
• Электродиализ - процесс очистки сточных вод основанный на
разделении ионизированных веществ под действием электродвижущей
103
силы, создаваемой в растворе по обе стороны мембраны.
104.
104105.
105106.
Процессы анодного окисления разработаны для очистки сточныхвод от цианидов, тиоцианатов, аминов, спиртов, альдегидов,
нитросоединений, азокрасителей, меркаптанов.
В процессе электрохимического окисления все эти, в том числе и
достаточно сложные органические соединения полностью
распадаются с образованием С02, Н20, NН3 или переходят в более
простые и нетоксичные вещества, которые можно удалить из
сточных вод другими методами.
Например:
CN- + 2OH- - 2e CNO- + H2O
CNO- + 2H2O NH4+ + CO32или
CNO- + 4OH- - 6e 2CO2 + N2 + 2H2O
Процессы катодного восстановления используют для извлечения
из сточных вод и последующей рекуперации ионов тяжелых и
редких металлов (свинца, ртути, хрома, олова).
Например:
Cr2O72- +14H+ + 12e 2Cr3+ + 7H2O
106
107. Химические методы очистки сточных вод
Нейтрализация загрязняющих примесей, их окислениеи восстановление.
Сточные
воды
металлургических,
химических,
машиностроительных и некоторых других производств
содержат большие количества кислот или щелочей.
Перед сбросом таких вод в водоемы или перед,
использованием в технологических процессах их
необходимо
нейтрализовать.
Практически
нейтральными считаются воды, имеющие рН 6,5 - 8,5.
107
108. Способы проведения нейтрализации
1. смешение кислых и щелочных стоков,2. фильтрование сквозь нейтрализующие материалы,
3. добавление реагентов,
4. сорбция кислых газов щелочными водами
5. сорбция аммиака кислыми водами.
Выбор способа нейтрализации зависит от объема и
концентрации сточных вод, от режима их
поступления, наличия и стоимости реагентов.
Нейтрализация смешением может быть осуществлена,
если на одном или соседних предприятиях имеются
и кислые, и щелочные стоки, не загрязненные
другими компонентами.
108
109.
109110. Реагенты
• Для нейтрализации кислых сточных вод в качествереагентов используются щелочи (NаОН, КОН), сода
(Nа2СО3), аммиачная вода (NН40Н), карбонаты
кальция и магния (СаСО3, МgСО3) и известковое
молоко с содержанием извести ( Ca(OH)2 5 - 10% ).
• При нейтрализации кислых стоков твердыми
реагентами (магнезит, доломит, известняк и т. д.) или
твердыми промышленными отходами (золы, шлаки
сталеплавильного и доменного производства и т. д.)
сточные воды очищают, фильтруя их сквозь слой
реагента.
• Для нейтрализации щелочных стоков используют
отходящие газы, содержащие С02, S02, N02, N203 …
Это позволяет не только нейтрализовать сточные
воды,
но
и
одновременно
производить
высокоэффективную очистку самих газов от вредных
компонентов.
110
111. Очистка сточных вод с помощью окислителей и восстановителей.
Для перевода токсичных соединений, содержащихся вряде промышленных стоков, в менее токсичные с
последующим удалением последних из сточных вод.
Этот метод связан с большим расходом реагентов и
используется в тех случаях, когда опасные токсиканты
(цианиды, соединения мышьяка) нельзя извлечь из
сточных вод другими способами.
111
112. Окислители
В качестве окислителей используют хлор, озон О3,пероксид
водорода
Н202,
пиролюзит
Мn02,
перманганат калия КМn04.
Чаще всего в системах водоочистки используют хлор и
хлорсодержащие соединения, способные выделять
«активный» хлор. При введении хлора в воду
образуются соляная и хлорноватистая кислоты:
Сl2 + Н20 = НСl + НСl0
Хлорноватистая кислота частично диссоциирует:
НСl0 = H+ +ClOСумма соединений Сl2 + НСl0 + Сl0- называется
свободным «активным» хлором.
Его источниками могут быть также хлорная известь
Са(Сl0)2, гипохлориты (например, NаСlO), хлориты
(например, NаСl02, диоксид хлора СlO2).
112
113.
Процесс хлорирования проводят в хлораторахпериодического и непрерывного действия.
В этих установках сточные воды очищаются от
сероводорода,
гидросульфидов,
метилсернистых
соединений, фенолов, цианидов.
113
114. Очистка от цианидов
При обезвреживании вод от цианидов процесс проводят вщелочной среде (рН=9).
1)
CN- + 2OH- + Cl2 CNO- + 2Cl- + H2O
(цианаты)
2CN0- + 4OH- + 3Cl2 CO2 + 6Cl- + N2 + 2H2O
При окислении цианидов «активным» хлором процесс
можно проводить в одну ступень до получения
цианатов.
CN- + ClO- CNO- + Cl(1)
Образовавшиеся цианаты легко гидролизуются до
карбонатов:
CNO- + 2Н2О CO32- + NН4+
Скорость гидролиза зависит от рН среды.
При рН=5,3 за сутки гидролизуется ~ 80% цианатов.
114
115.
В двухступенчатом процессе цианиды окисляются до N2и CO2.
На первой стадии процесс протекает по реакции (1)
На второй стадии:
2CNO- + 3ClO- + Н2О 2CO2 + N2 +2ОН- + 3ClрН в пределах 8-11.
Контроль полноты окисления проводят по остаточному
«активному» хлору, концентрация которого должна быть не
менее 5-10 мг/л.
Товарный хлорат кальция содержит до 33 % «активного»
хлора, а гипохлорит кальция до 60%.
115
116. Пероксид водорода
Окислитель - пероксид водорода легко разлагает нитраты,нитриты, альдегиды и фенолы, содержащиеся в сточных
водах.
В кислой и щелочной средах он разлагается по уравнениям:
2H+ + H2O2 +2e- 2H2O
2OH- + H2O2 + 2e- 2H2O +2O2В кислой среде более отчетливо выражена окислительная
функция, а в щелочной – восстановительная.
В кислой среде пероксид водорода переводит соли
двухвалентного железа в соли трехвалентного, азотистую
кислоту – в азотную, сульфиды в сульфаты. Цианиды в
цианаты окисляются в щелочной среде (рН=9-12).
В разбавленных растворах процесс окисления органических
веществ
протекает
медленно,
поэтому
используют
катализаторы - ионы металлов переменной валентности (Fe2+,
Cu2+, Mn2+, Co2+...)
116
117. Пероксид водорода
Впроцессах
водообработки
используют
и
восстановительные свойства H2O2 .
В нейтральных и слабощелочных средах он легко
взаимодействует с хлором и гипохлоридами, переводя
их в хлориды:
H2O2 +Cl2 O2 + 2HCl
H2O2 +NaClO NaCl + O2 + H2O
Эти реакции используют при дехлорировании воды.
Н2О2 используется также для обесцвечивания
сточных вод: при рН 7-10 пероксид водорода быстро
разлагает активные красители, причем присутствие
катализаторов (сульфатов железа или меди) ускоряет
процесс разложения в 8 - 10 раз.
117
118. Окисление кислородом воздуха
Используют при очистке сточной воды отжелеза
для
окисления
соединений
двухвалентного железа в трехвалентное с
последующим отделением от воды гидроокиси
железа.
4Fe2+ + O2 +2H2O 4Fe3+ + 4OHFe3+ + 3H2O Fe(OH)3 + 3H+
Окисление проводят при аэрировании воздуха
через сточную воду в башнях с насадкой.
Образующийся гидроксид железа отстаивают в
контактном
резервуаре,
а
затем
отфильтровывают.
118
119. Окисление кислородом воздуха
Кислородом воздуха окисляют такжесульфидные
стоки
целлюлозных,
нефтеперерабатывающих
и
нефтехимических заводов.
Процесс окисления гидросульфидной и
сульфидной серы :
S2- S S4O62- S2O32- SO32-
SO42При этом идет изменение рН.
119
120. Окисление пиролюзитом
Для очистки промышленных стоков от соединениймышьяка (Ш) успешно применяют пиролюзит ,
состоящий в основном из диоксида марганца - Мn02,
используя аппараты с мешалкой или фильтрование
сточных вод сквозь слой пиролюзита
Н3АsО3 + Мn02 + Н2S04 = Н3Аs04 + МnS04 + Н2О
причем мышьяк (III) переходит в менее токсичный
мышьяк (V).
Повышение температуры способствует увеличению
степени окисления.
Оптимальный режим окисления - расход Мn02
четырехкратный по сравнению со стехиометрическим,
кислотность воды 30-40 г/л, температура воды 708000С.
120
121. Озонирование
Отфенолов,
нефтепродуктов,
сероводорода,
соединений мышьяка, поверхностно-активных веществ,
цианидов,
канцерогенных
ароматических
углеводородов, пестицидов и многих других токсичных
примесей. Соединения металлов окисляются озоном до
соединений высшей валентности. А патогенные
микроорганизмы погибают в несколько тысяч раз
быстрее, чем при ее хлорировании.
121
122. Озонирование
В сточную воду озон подают в виде озоновоздушной или озоно-кислородной смеси ссодержанием озона не более 3%.
Озонирование промышленных сточных вод
осуществляют в барботажных, насадочных,
тарельчатых колоннах и других контактных
аппаратах.
Процесс очистки ускоряют при совместном
применении озона и ультразвуковой обработки
или ультрафиолетового облучения сточных вод.
Так, ультрафиолетовое облучение ускоряет
процесс окисления примесей в промышленных
стоках в 102 - 104 раз.
122
123.
123124. Восстановительная очистка
Используются для сточных вод, содержащих легковосстанавливаемые вещества. Часто применяются дляудаления из сточных вод соединений хрома, ртути,
мышьяка. Хром (VI), содержащийся в некоторых
промышленных стоках, восстанавливают до Сr3+ с
последующим осаждением его в щелочной среде в
форме гидроксида Сr(ОН)3.
124
125. Восстановители
В качестве восстановителей используютактивированный
уголь,
органические
отходы (например, газетную бумагу),
сульфат железа FeS04, гидросульфит
натрия NаНS03, диоксид серы S02,
водород.
125
126. Очистка от соединений Сr и Hg
4Н2Сr04 + 6NаНS03 + ЗН2S04 = 2Сr2(S04)3 +ЗNа2S04 + 10Н20
или
2СrО3 + ЗН2S03 (SO2 + H2O) = Cr2(S04)3 + ЗН20
Последний
процесс
позволяет
сочетать
улавливание хрома из сточных вод с очисткой
отходящих газов от диоксида серы.
Ртуть
неорганических
соединений,
содержащихся в сточных водах, сравнительно
легко восстанавливается до металлической,
которая затем выделяется отстаиванием,
фильтрованием или флотацией.
126
127. Удаление тяжелых металлов
Hg, Cr, Cd,Co, Zn, Pb, Cu, Ni, Mn, As и т.д.В
различных
отраслях
промышленности
используются соединения тяжелых металлов,
что приводит к загрязнению ими сточных вод.
Для удаления распространены реагентные
методы очистки.
Перевод растворимых в воде веществ в
нерастворимые при добавлении различных
реагентов
с
последующим
отделением
образующихся осадков.
127
128. Осадение ионов металлов
В качестве реагентов для осаждения тяжелыхметаллов используют гидроксиды кальция и
натрия,
карбонат
натрия,
сульфиды
феррохромовый шлак и др.
Осаждение ионов металлов происходит в виде
гидроксидов, при различных значениях рН,
которое
зависит
от
природы
металла,
концентрации,
температуры,
содержанию
примесей.
Эффективность больше при совместном
осадении нескольких ионов металлов
128
129. Характеристика процесса осаждения
Вид катионаЖелезо Fe2+
Значения рН
Начало осаждения
Полное осаждение
(при С=0,01моль/л) (С в р-ре 10-5моль/л)
7,5
9,7
Железо Fe3+
2,3
4,1
Цинк Zn2+
6,4
8,0
Хром Cr3+
4,9
6,8
Никель Ni2+
7,7
9,5
Кадмий Cd2+
8,2
9,7
129
130. Очистка от соединений ртути Неорганические соединения ртути
В производственных сточных водах можетприсутствовать
металлическая
ртуть,
неорганические и органические соединения Hg.
Неорганические соединения ртути : оксид HgO,
хлорид (сулема) HgCl2 ,сульфат HgSO4 ,
сульфид (киноварь) HgS , нитрат Hg(NO3)2 и др.
В них токсичны ионы Hg2+, поэтому наиболее
опасны
хорошо
растворимые
и
легко
диссоциирующие соли.
130
131. Органические соединения Hg
Органические соединения ртути применяют приконсервировании древесины, для защиты
пластмасс, текстиля, бумажной массы и т.д. от
плесневых грибов, а также как ядохимикаты.
Органические соединения ртути весьма
токсичны и отличаются от неорганических
солей тем, что не дают реакции на ионы Hg.
В водоемах ртуть под влиянием органических
соединений, содержащихся в природных водах,
превращается в сильнотоксичные соединения.
131
132. Очистка от металлической Hg
Металлическая ртуть может быть удалена изсточных вод в процессах отстаивания или
фильтрования.
Частицы, прошедшие с фильтратом или не
успевшие осесть, окисляют хлором или NaOCl
до HgCl2.
Затем воду обрабатывают восстановителем
(NaHSO4 , Na2SO3) для их удаления и
связывания остатков свободного хлора. Ртуть
осаждают сульфидом натрия с последующим
коагулированием образующегося сульфида
ртути хлоридом железа.
132
133. Очистка от неорганической ртути
Для удаления из сточных вод ионов неорганическойртути используют методы восстановления.
В качестве восстановителей применяют сульфид
натрия Na2S, гидросульфит натрия NаНS03 или
сероводород, которые переводят растворимые ионы
ртути в труднорастворимый сульфид.
Произведение растворимости HgS в воде = 1,6*10-52,
что отвечает остаточной концентрации в растворе =
2.5*10-21 мг/л.)
Затем обрабатывают раствор хлоридами натрия, калия,
магния, кальция в количестве 0,1 г/л. В этих условиях
сульфид ртути осаждается в виде гранул (добавляют
коагулянты: сульфаты Al, Fe), который затем
отфильтровывают.
133
134. Органические соединения
Их сначала разрушают с помощьюсильных
окислителей
(например,
газообразным хлором), а затем после
удаления
избытка
хлора,
восстанавливают ее катионы Hg2+ до
металлической Hg или переводят в
труднорастворимые
сульфиды
с
последующим удалением осадка.
134
135. Очистка от соединений Zn,Cu, Ni, Pb, Cd, Co.
При обработке кислых сточных вод оксидомкальция и гидроксидом натрия ионы данных
тяжелых
металлов
связываются
в
труднорастворимые
соединения,
состав
которых зависит от рН среды.
При рН=7 осаждается гидроксид-сульфат цинка
состава ZnSO4 3Zn(OH)2, а при повышении рН
до 8,8 составу осадка соответствует формула
ZnSO4 5Zn(OH)2.
В сильнощелочной среде твердая фаза
представляет собой в основном гидроксид.
135
136. Общая схема выделения ионов металлов
В общем выделение данных ионов Ме2+ щелочамиосновано на переводе их в труднорастворимые
гидроксиды.
Ме2+ + 2ОН- = Ме(ОН)2
Для цинка выпадение в осадок его гидроксида
соответствует рН=5,4. При рН=10,5 начинается
растворение амфотерных гидроксидов цинка, а при
достижении рН=12 происходит образование комплекса:
Zn(OH)2 + 2OH- = [Zn(OH)4]2Осаждение гидроксида меди происходит при рН=5,3.
Осаждение гидроксида никеля начинается при рН=6,7.
Как и для меди его растворимость сильно зависит от
рН.
Перечисленные металлы также хорошо отделяются от
раствора в виде карбонатов или гидроксид-карбонатов
((МеОН)2СО3) .
136
137. Очистка от ионов свинца
Находящиеся в растворе переводят в осадок в виде одногоиз трех труднорастворимых соединений:
Pb2+ + 2OH- = Pb(OH)2
2Pb2+ + 2OH- +CO32- = (PbOH)2CO3
Pb2+ + CO32- = PbCO3
Выпадение в осадок гидроксида свинца начинается при
рН=6,0.
Наиболее дешевым методом является получение
карбоната свинца с использованием в качестве реагента осадителя известняка, мела или мрамора, которыми
загружают фильтры, через которые профильтровывают
очищаемые стоки.
При увеличении рН 7 эффективность очистки от ионов
свинца значительно повышается вследствие появления
гидроксид - ионов наряду с карбонат - ионами и
образование гидроксид - карбоната свинца. Наибольшая
степень очистки достигается при рН=9,5. Степень очистки
137
составляет 90%.
138.
Концентрации ионов кобальта и кадмия встоках обычно чрезвычайно малы по
сравнению с содержанием катионов
других тяжелых металлов. рН среды при
выпадении этих гидроксидов в осадок
соответственно равен 6,7 - 7,7 и 7,2 - 8,2.
Поэтому
при
обработке
стоков
известковым молоком они могут быть
максимально очищены от растворенных
солей кобальта и кадмия.
138
139.
Обработка сточных вод щелочнымиреагентами позволяет снизит содержание
тяжелых металлов в растворе до
величин, сопоставимых с ПДК для
водоемов
санитарно-бытового
пользования.
Более
глубокая
очистка
при
использовании щелочных реагентов не
достигается.
139
140. Очистка от солей железа
В природных водах содержание железаколеблется от 0,01 до 26мг/л.
В
значительных
количествах
железо
содержится в сточных водах химических,
металлургических,
машиностроительных,
нефтехимических, химико-фармацевтических и
др. производств.
При содержании железа более 1мг/л вода
приобретает бурый цвет. При движении такой
воды по трубопроводам на их стенках
откладываются
соединения
железа
и
железобактериии,
уменьшая
сечение
трубопровода.
140
141. Методы обезжелезивания вод
Аэрация,реагентные
электродиализ, адсорбция,
осмос.
методы,
обратный
141
142. Аэрирование
В процессе аэрирования происходит окислениедвухвалентного железа в трехвалентное
4Fe2+ + O2 + 2H2O = 4Fe3+ + 4OHFe3+ + 3H2O = Fe(OH)3 + 3H+
или суммарно
4Fe2+ + O2 + 10H2O = 4Fe(OH)3 + 8H+
В присутствии гидрокарбонатных ионов в воде процесс
протекает по следующей реакции
4Fe2+ +8HCO3- + O2 + 2H2O = 4Fe(OH)3 +
8CO2
На окисление 1мг двухвалентного железа расходуется
0,143 мг кислорода. Для обеспечения высокой скорости
химической реакции содержание кислорода в воде
должно быть 0,5-0,9 мг на 1 мг железа.
142
143. Реагентные методы
При высоком содержании железа в воде аэрационнымметодом его полностью удалить нельзя, поэтому
применяют реагентные методы.
Для этой цели используют хлор, хлорат кальция (хлорную
известь), перманганат калия, озон, оксид кальция
(известь), карбонат натрия (соду) и др. Реагенты
дозируются
в
воду
перед
осветлителями
или
отстойниками.
Fe(HCO3)2 + Cl2 + Ca(HCO3)2 = 4Fe(OH)3 + CaCl2+ 6CO2
Скорость данной реакции больше с повышением рН.
В случае использования хлората кальция его используют в
виде
1-2%-го
раствора,
который
дозируют
непосредственно в сточную воду.
143
144. Окисление перманганатом калия
проходит по уравнению3Fe(HCO3)2 + KMnO4 + 2H2O = 3Fe(OH)3 +
MnO2 + 5CO2 + KHCO3
Если железо содержится в виде органических
соединений или коллоидных частиц, применяют
озонирование.
При этом на 1 масс. ч. железа требуется 1 масс. ч.
озона.
144
145. Очистка от соединений марганца
Соединения марганца содержатся в сточных водахметаллургических,
машиностроительных
и
химических производств.
При концентрации марганца более 0,05 мг/л вода
окрашивается в темный цвет.
Удаление из воды марганца может быть достигнуто
следующими методами :
• обработкой воды перманганатом калия;
• аэрацией, совмещенной с известкованием;
• фильтрованием воды через марганцевый песок или
марганцевый катионит;
• окислением озоном, хлором или диоксидом хлора.
145
146.
При обработке воды перманганатом калиядостигается
одновременная
очистка
от
марганца и от железа.
3Mn2+ + 2MnO4- + 2H2O = + MnO2 + 4H+
Удаление
марганца
аэрацией
с
подщелачиванием
воды
применяют
при
одновременном присутствии в ней марганца и
железа.
При аэрации воды удаляется часть диоксида
углерода
и
происходит
ее
насыщение
кислородом воздуха. При удалении СО2
возрастает рН сточной воды, что способствует
ускорению процессов окисления и гидролиза
железа и частично марганца с образованием
гидроксидов.
146
147. Биохимические методы очистки сточных вод
Основаны на способности микроорганизмовиспользовать
для
своего
развития
и
жизнедеятельности
те
органические
соединения, которые не были удалены из
очищаемой воды на предшествующих стадиях
обработки.
Потребляя
органические
вещества,
микроорганизмы частично разрушают их,
превращая в СО2, Н2О, нитрат-, и сульфатионы, частично используют для образования
собственной биомассы.
147
148.
Биохимическую очистку сточных вод можно проводитькак в искусственных условиях – в биологических
фильтрах и аэротенках, так и в естественных
условиях – на полях фильтрации, земледельческих
полях орошения, биологических прудах.
148
149. Аэробные и анаэробные методы
Анаэробная очистка сточных вод протекает без доступакислорода и используется преимущественно для
обезвреживания осадков.
149
150. Аэробная очистка
Для аэробной очистки используют аэробные группымикроорганизмов, для жизнедеятельности которых
необходим постоянный приток кислорода и
температура 20-400С.
150
151. Биологические фильтры
Резервуары,заполненные
крупнозернистыми
материалами - гравием, керамзитом, шлаком, крупным
песком, сквозь которые фильтруются сточные воды,
поступающие сверху по всей площади фильтра.
151
152.
Проходя сквозь загрузку биофильтра, сточные водыоставляют на ней органические вещества, не
отделенные на предшествующих стадиях водоочистки.
Эти вещества образуют на поверхности зерен фильтра
биопленку, в которой развиваются микроорганизмы. В
результате из сточных вод удаляются органические
загрязнения.
Биопленка
имеет
вид
слизистых
обрастаний толщиной 1 - 3 мм и более. Цвет ее
изменяется с изменением состава сточных вод от
серовато-желтого до темно-коричневого.
152
153.
153154. Бактерии
Биоценоз активной пленки включает несколько группаэробных бактерий, грибы, дрожжи; развивающиеся
представители простейших, коловратки, черви, личинки
комаров и мух, клеши поедают активный ил,
способствуя его рыхлению, повышая эффективность
водоочистки.
154
155. Аэротенки
В них медленно движется смесь активного ила источной воды, постоянно перемешиваемая при помощи
сжатого воздуха или специальных приспособлений.
Активный ил включает биоценоз микроорганизмов минерализаторов, которые сорбируют на своей
поверхности и окисляют органические примеси сточных
вод.
155
156.
156157. Основные проблемы
В результате биохимической образуются сильновлажные осадки, которые необходимо утилизировать во
избежание загрязнения ими окружающей среды.
Как правило, осадки сточных вод представляют собой
труднофильтрующиеся суспензии.
157
158.
158159. Уплотнение осадка
Обработканачинается
с
уплотнения
осадка
гравитационным или флотационным методом - осадок
разбавляют
определенным
количеством
воды,
предварительно насыщенной воздухом.
При снижении давления растворенный воздух
выделяется в виде мелких пузырьков, а осадок
активного ила становится более плотным.
159
160. Стабилизация осадка
Уплотненныйосадок
подвергается
стабилизации - разрушению его органической
составляющей до диоксида углерода, воды,
метана.
Стабилизация осуществляется с помощью
микроорганизмов в анаэробных и аэробных
условиях.
В анаэробных условиях осадок сбраживается в
двухъярусных отстойниках, осветлителях перегнивателях, метантенках.
160
161.
161162. Аэробная стабилизация
Это продолжительное аэрирование осадка;в результате пневматического или механического
аэрирования
происходит
распад
разлагаемых
органических веществ, а наиболее устойчивые
соединения теряют способность к загниванию, т. е.
стабилизируются.
Эффективность
аэробной
стабилизации
определяется
его
длительностью,
температурой, интенсивностью аэрации, а также
зависит от состава и свойств окисляемого осадка.
162
163. Кондиционирование
Стабилизированный осадок подвергают коагуляции.Далее проводят процесс изменения структуры осадка и
улучшения
его
водоотдающих
свойств
(кондиционирование).
Его можно проводить и безреагентным методом, в том
числе тепловой обработкой, замораживанием с
последующим оттаиванием, электрокоагуляцией.
Влажность кондиционированного осадка снижается с
92 - 94 до 70 - 75%, он хорошо уплотняется и поступает
на обезвоживание.
163
164. Обезвоживание осадков
Производят на иловых площадках - обвалованных совсех сторон участках земли. Рабочая глубина такой
площадки, как правило, лежит в пределах 0,7 - 1,0 м; их
площадь зависит от количества осадков, характера
грунта, климатических условий.
Обычно иловые площадки делают для очистных
сооружений производительностью
10 000 м3/сут.
Их располагают в виде каскада из 4 - 8 площадок.
164
165.
Обезвоженный осадок высушивается на барабанных,ленточных, распылительных и других сушилках, в
которых в качестве осушителя используются дымовые
газы при температуре 500 - 800°С, перегретый пар или
горячий воздух.
Твердые осадки сточных вод могут стать важным
ресурсом органических удобрений, если не содержат
тяжелых
металлов
или
других
токсических
компонентов.
165
166.
166167.
167168. Поля фильтрации
Перспективна биохимическая очистка сточныхвод в естественных условиях - на полях
фильтрации и земледельческих полях
орошения (ЗПО).
В этих случаях для очистки сточных вод
используется очищающая способность самой
почвы. Фильтруясь сквозь слой почвы, вода
оставляет в ней взвешенные, коллоидные и
растворенные примеси.
Микроорганизмы почвы окисляют органические
загрязняющие вещества, превращая их в
простейшие
минеральные
соединения
диоксид углерода, воду, соли.
168
169.
169170.
Наиболее интенсивно протекают эти процессыв верхних горизонтах почвы (0,2-0,4 м), где
расходуемые запасы кислорода пополняются
достаточно быстро.
Регулируя водно-воздушный режим территории,
орошаемой сточными водами, можно достичь
высоких степеней очистки и повышения
плодородия орошаемых земель, которые
извлекают из сточных вод и удерживают
элементы
питания
растений.
Почвенная
очистка сточных вод существенно эффективнее
искусственной.
170
171. Поля фильтрации
Используют только для биохимической очисткиводы; их территории отчуждаются у сельского
хозяйства.
Высокие нормы нагрузки (15 - 90 м3/га сточных
вод в сутки) позволяют устраивать их лишь на
хорошо фильтрующих почвах, а многолетнее
обильное орошение приводит к вымыванию из
почвы питательных веществ и ее деградации.
Поэтому биохимическая очистка воды на полях
фильтрации значительно менее выгодна, чем
на земледельческих полях орошения (ЗПО).
171
172. ЗПО
На земледельческих полях орошения очисткасточных
вод
происходит
непосредственно
на
производственных полях и при благоприятных условиях
способствует повышению плодородия земель.
Норма сточных вод, подаваемых на единицу площади
ЗПО,
должна
соответствовать
потребности
в
удобрениях и воде произрастающих культур.
Для устройства ЗПО пригодны любые, даже бросовые
земли, объем подготовительных работ сравнительно
невелик, которые в основном сводятся к устранению
неровностей рельефа.
Подача сточных вод в почву происходит либо с
поверхности, либо из труб, проложенных на небольшой
глубине.
172
173.
Дляобезвреживания
яиц
гельминтов,
содержащихся в фекальных городских стоках,
перед выпуском на поля их предварительно
отстаивают,
а
образовавшийся
осадок
подвергают брожению при 50 - 60°С.
Болезнетворные бактерии, содержащиеся в
сточных водах, при попадании в почву
довольно быстро погибают.
Тем не менее на ЗПО не рекомендуется
выращивать культуры, идущие в пищу человеку.
Обычно поля орошения используют под
технические и кормовые культуры.
173
174. Биологические пруды
Используетсяспособность
природных
вод
к
самоочищению.
Биологические пруды представляют собой водоемы
площадью 0,5 - 1,0 га, в которых сточные воды могут
очищаться в аэробных и анаэробных условиях.
Анаэробные пруды служат для предварительной
очистки высококонцент-рированных сточных вод;
глубина таких прудов достигает 2,5 - 3 м.
174
175. Аэробные пруды
Их располагают секциями, от двух до пяти прудов вкаждой. Вода поступает последовательно из одного
пруда в другой по мере ее очистки. Для более
равномерного распределения сточной воды по
акватории прудов впуск и выпуск воды устраивают
рассредоточенными.
Глубина воды в первом пруду составляет 1 м, в
последующих - до 1,5 - 2,0 м.
Если аэробные пруды предназначены для полной
биологической очистки, то время пребывания в них
сточных вод должно быть не менее 15 - 20 сут; если они
используются для доочистки, то время сокращается до
2 сут.
175
176.
После биологической очистки сточныхвод на искусственных сооружениях
общее содержание в них бактерий
уменьшается на 95%, а при очистке на
ЗПО - на 99 %.
Для полного обеззараживания сточных
вод их необходимо хлорировать или
уничтожить болезнетворные бактерии
другими методами.
176
177. Термические методы очистки сточных вод
На химических предприятиях образуютсясточные воды, содержащие различные
минеральные соли, а также органические
вещества.
Такие воды могут быть обезврежены
термическими методами.
177
178.
178179. К термическим методам относятся:
концентрирование
сточных
вод
с
последующим выделением растворенных
веществ:
жидкофазное
окисление
органических
веществ
окисление
органических
веществ
в
присутствии
катализатора
при
атмосферном и повышенном давлениях
огневое обезвреживание.
179
180. Концентрирование сточных вод
Используют для обезвреживания минеральныхсточных вод.
Он позволяет выделять из стоков соли с
получением условно чистой воды, пригодной
для оборотного водоснабжения.
Данный процесс обычно проводят в две стадии:
• стадия концентрирования и
• стадия выделения сухих веществ.
180
181. Методы концентрирования
С использованием одноступенчатых имногоступенчатых
выпарных
установок. Недостатки:
• энергоемкость проведения процесса
• накипеобразование, которое приходится
преодолевать различными способами.
181
182. Методы концентрирования
Установки вымораживания.Данный процесс заключается в том, что при
температуре ниже температуры замерзания
чистая вода образует кристаллы пресного льда,
а рассол с растворенными в нем солями
размещается
в
ячейках
между
этими
кристаллами.
Вымораживание проводят под вакуумом либо
при помощи специального холодильного агента.
Наиболее распространенными хладоагентами
являются аммиак, диоксид углерода, бутан,
пропан, изобутан, хладоны (CCl2F2, CCl3F,
CClF3).
182
183. Методы концентрирования
Кристаллогидратные установки. В данном процессеконцентрирование сточной воды происходит с
применением гидратообразующего агента М (пропан,
хлор, хладоны, диоксид углерода и др.) и образованием
кристаллогидратов, имеющих формулу М nН2О.
При этом концентрация растворенных веществ в воде
повышается, а при плавлении кристаллов образуется
вода,
из
которой
выделяются
пары
гидратообразующего агента.
Температуру при гидратообразовании поддерживают
выше и ниже температуры окружающей среды.
183
184. Выделение веществ из концентрированных растворов
Длявыделения
веществ
из
концентрированных
растворов
используют методы кристаллизации и
сушки.
184
185. Кристаллизация
Вещества,растворимость
которых
существенно
возрастает
с
повышением
температуры
(положительная растворимость), кристаллизуют при
охлаждении
их
насыщенных
растворов
политермическая
кристаллизация,
идущая
при
неизменном содержании воды в системе.
Если с ростом температуры растворимость веществ
уменьшается, то кристаллизацию проводят при
нагревании раствора.
Вещества мало изменяющие растворимость при
изменении
температуры,
кристаллизуют
путем
испарения воды при постоянной температуре изотермическая кристаллизация.
Положительной растворимостью обладают, например,
растворы MgCl2, MgSO4, NaCl; отрицательной растворы CaSO4, CasiO3 и др.
185
186. Кристаллизация
Кристаллизацию соли проводят такжевведением в концентрированный раствор
веществ,
уменьшающих
ее
растворимость.
Это
вещества,
содержащие одинаковый ион с данной
солью
или
связывающие
воду.
Кристаллизацию такого типа называют
высаливанием.
186
187.
После кристаллизации в аппаратах любойконструкции полученные кристаллы отделяют
от маточного раствора в вакуум-фильтрах,
отстойниках и фильтрующих центрифугах.
После промывки их используют как готовую
продукцию или перерабатывают в другие
вещества.
Маточный раствор и промывные воды должны
быть возвращены на стадию концентрирования
или направлены на очистку с целью
дальнейшего использования.
В
процессе
кристаллизации
основного
вещества образующиеся кристаллы часто
бывают загрязнены примесями.
187
188. Сушка
Наиболее удобны для данного процессараспылительные
сушилки.
(Высокая
скорость сушки, до сотых долей секунды).
Для отделения высушенного материала
от газового потока используют циклоны,
рукавные
фильтры,
скрубберы,
электрофильтры
188
189. Термоокислительные методы обезвреживания
Потеплотворной
способности
химические
промышленные стоки делят на сточные воды,
способные гореть самостоятельно, и на воды, для
термоокислительного
обезвреживания
которых,
необходимо добавлять топливо.
При использовании термоокислительных методов все
органические вещества, загрязняющие сточные воды,
полностью окисляются кислородом воздуха при
высоких температурах до нетоксичных соединений.
Выбор конкретного метода зависит от объема сточных
вод, их состав и теплотворной способности,
экономичности процесса и требований предъявляемых
к очищенным водам.
189
190. Метод жидкофазного окисления
Этот метод очистки основан на окислении органическихвеществ, растворенных в воде, кислородом при
температурах 100 - 350 С и давления 2 - 28 МПа.
При высоких давлениях растворимость в воде
кислорода значительно возрастает, что способствует
ускорению процесса окисления органических веществ.
Эффективность процесса окисления увеличивается с
повышением температуры. Летучие вещества при
условиях процесса окисляются в основном в
парогазовой фазе, а нелетучие - в жидкой фазе. С
увеличением концентрации органических примесей в
воде экономичность процесса жидкофазного окисления
возрастает.
190
191. Метод парофазного каталитического окисления
Этогетерогенное
каталитическое
окисление
кислородом воздуха при высокой температуре летучих
органических веществ, находящихся в промышленных
сточных водах.
Процесс протекает весьма интенсивно в паровой фазе
в присутствии медно-хромового, цинк-хромового,
медно-марганцевого или другого катализатора.
Установки
характеризуются
высокой
производительностью по сточной воде и высокой
степенью
обезвреживания,
достигающей
99,8%.
Основной недостаток установок - возможность
отравления катализаторов соединениями фосфора,
фтора, серы. Поэтому необходимо предварительное
удаление каталитических ядов из сточных вод.
191
192. Огневой метод
Сущность метода - распыление сточных вод непосредственно втопочные газы, нагретые до 900-1000 С. При этом вода полностью
испаряется, а органические примеси сгорают. Содержащиеся в
воде минеральные вещества образуют твердые или оплавленные
частицы, которые улавливают в циклонах или фильтрах.
Если сточные воды содержат только минеральные вещества,
огневой метод нецелесообразно применять.
В процессах обезвреживания сточных вод различного состава
могут образовываться оксиды щелочных и щелочно - земельных
металлов (CaO, MgO, BaO, K2O и др.). Некоторые из этих оксидов
могут взаимодействовать с компонентами дымовых газов,
например
Na2O + CO2 = Na2CO3
При диссоциации хлоридов в дымовых газах образуются хлор и
хлороводород. Органические соединения содержащие серу,
фосфор, галогены могут образовывать SO2, SO3, P2O5 и др.
Присутствие этих веществ в дымовых газах вызывает
значительную коррозию аппаратуры.
192
193. ЗАЩИТА ЛИТОСФЕРЫ ОТ ЗАГРЯЗНЕНИЙ
Твердые отходы, поступающие в биосферу за счеттехногенной деятельности, можно подразделить на три
основные
категории:
промышленные,
сельскохозяйственные и коммунально-бытовые.
Наибольшую сложность представляет обезвреживание
и утилизация промышленных отходов, существенно
превосходящих сельскохозяйственные и бытовые как
по масштабам их скапливания, так и по разнообразию
состава и свойств.
Практически все виды отходов содержат ценные
вещества, и их рациональная утилизация дает
дополнительные сырьевые ресурсы, охраняя в то же
время биосферу от загрязнения.
193
194. Утилизация отходов горнодобывающей промышленности
Исследованияи
полупромышленные
испытания этих отходов показали, что они
могут быть прекрасным сырьем для пористых
заполнителей бетона, строительного кирпича и
керамики, штукатурных и кладочных растворов,
щебня и других строительных материалов.
Обогащение
угля
с
целью
снижения
содержания в нем серы сопровождается
образованием серного колчедана, содержащего
42 -46% серы и 5 - 8% углерода.
Н-р,в Подмосковном угольном бассейне запасы
серного колчедана достигают 60 млн. т.
194
195.
Серныйколчедан
FeS2
является
потенциальным сырьем для производства
серной кислоты.
Использование
его
вместе
с
другим
крупнотоннажным промышленным отходом сульфатом железа FeSO4, образующимся в
производстве пигмента диоксида титана TiO2,
позволяет получать S02 для последующего
производства серной кислоты.
Процесс совместной термической обработки
может быть выражен уравнением:
2 FeSO4 + 6 FeS2 + 1602 = 14S02 + 4Fe2O3
195
196.
Породы основные и попутно извлекаемыечасто содержат мел СаСОз, который может
быть использован для производства белого
цемента, строительной извести, стекла.
Основой для производства почти всех
известных видов строительных материалов
могут служить так называемые горелые породы
- пустые породы, обожженные при подземных
пожарах или при самовозгорании терриконов.
196
197.
Среди извлекаемых при горных работахпород нередко встречаются пластичные
глины, которые являются сырьем для
производства керамзита - хорошего
тепло- и звукоизолирующего материала,
служащего
пористым
заполнителем
бетонов, фильтрующим материалом
и
т. п.
197
198. Утилизация твердых отходов металлургии и энергетики
Металлургические шлаки также представляютсобой ценное сырье для производства ряда
строительных материалов.
Так,
гранулированные
доменные
шлаки
являются
прекрасным
материалом
для
дорожного строительства. В смеси с вязкими
битумами они успешно заменяют горячие
асфальтобетонные смеси, причем их возможно
укладывать даже на влажное основание.
Битумошлаковые покрытия дорог в 2,5 раза
дешевле железобетонных.
198
199.
Сталеплавильные шлаки используются вкачестве оборотного продукта (в виде флюса в
доменной шихте и вагранках), и до 50% их идет
на изготовление щебня
Ряд шлаков с высоким содержанием оксида
кальция и фосфатов находит применение в
сельском хозяйстве и используется в качестве
известковых мелиорантов для кислых почв.
Отвальные
шлаки
полиметаллических
рудников,
обогатительных
фабрик
и
предприятий цветной металлургии содержат
большое количество железа, меди, цинка,
свинца и др.
199
200. По химическому составу их можно условно подразделить на три группы:
• К первой следует отнести шлаки никелевых заводов инекоторую
часть
отходов
медеплавильных
заводов,
отличающихся низким содержанием цветных металлов и
железа. Извлечение металлов из таких шлаков экономически
нецелесообразно,
поэтому
наиболее
целесообразно
перерабатывать их в строительные материалы.
• Вторую группу составляют медные шлаки, содержащие цинк,
свинец, значительные количества железа и малые количества
меди. Из этих шлаков целесообразно извлекать Zn, Pb, Sn.
• В третью группу можно объединить оловянные и свинцовые
шлаки и некоторые медные шлаки с высоким содержанием Zn,
Pb, Sn из которых экономически целесообразно извлечение этих
ценных металлов даже без комплексной переработки шлаков.
200
201.
Золошлаковыеотходы
тепловых
электростанций, выход которых в России и
странах ближнего Зарубежья составляет около
70 млн. т в год, близки по составу к
металлургическим и также используются в
промышленности
стройматериалов:
силикатного кирпича, гравия, цемента.
Высокое содержание СаО в золе сланцев и
торфа позволяет использовать ее в качестве
известкового мелиоранта для улучшения
кислых почв.
201
202. Зола некоторых углей и нефтей содержит многие металлы, причем их содержание нередко бывает довольно значительным
МеталлCo
Ni
Zn
Ga
Ge
V
Sn
Содержание,
г/т
300
700
200
100
500
400
200
202
203.
В зависимости от концентрации металлов взоле
иногда
становится
экономически
выгодным их извлечение.
Так,
зола
бурых
углей
некоторых
месторождений содержит до 1 кг/т урана;
зола торфа содержит значительные количества
V, Са, Cu, Ni, Zn, РЬ;
в золе нефтей содержание V205 достигает 65%.
Однако, несмотря на это, утилизация огромных
масс зол и шлаков, скапливающихся на
золоотвалах ТЭС, в настоящее время
осуществляется совершенно недостаточно.
203
204. Утилизация твердых отходов химической промышленности
Впромышленности
неорганического
синтеза
наибольшее количество твердых отходов дают
производства минеральных удобрений и серной
кислоты.
При
производстве
двойного
суперфосфата,
фосфорной кислоты и в ряде других химических
производств образуется крупнотоннажный твердый
отход фосфогипс, содержащий 80-90% гипса, 0,50,6%фосфорной кислоты, 5-6% глины.
Основная масса фосфогипса сбрасывается в отвалы, в
которых содержатся десятки миллионов тонн этого
отхода.
Возможна переработка фосфогипса в серную кислоту и
известь, а также использование его в качестве
химического мелиоранта для солонцовых почв.
204
205. Утилизация твердых отходов химической промышленности
При переработке и обогащении сырья вкалийной
промышленности
ежегодно
образуются миллионы тонн твердых галитовых
отходов и сотни тысяч тонн глинисто - солевых
шлаков, занимающих большие площади под
отвалы и шламохранилища.
Галитовые отходы могут быть использованы в
качестве вторичного сырья для получения
соды, хлора, поваренной соли, однако их
переработка
затруднена
присутствием
сульфатов, хлорида калия и других примесей.
205
206.
В производстве серной кислотыосновными отходами являются пиритный
огарок и различные шламы.
На 1 тонну кислоты приходится не менее
0,55 т огарка. В настоящее время огарок
используют
главным
образом
в
цементной промышленности, однако, он
может найти применение в производстве
чугуна и для получения минеральных
пигментов - железного сурика, охры.
206
207. Опасные отходы
Особо токсичные и радиоактивные отходы, которые поразным причинам не подлежащие переработке, должны
быть захоронены.
Для
захоронения
отходов
их
заключают
в
металлические капсулы, а затем в кубы из
отвердевшего жидкого стекла, рассчитанные на
неопределенно долгое время хранения, и помещают
под землей, в геологических выработках (брошенные
угольные шахты, соляные копи, иногда специально
созданные полости). Иногда в контейнерах из
материалов, стойких к действию морской воды, отходы
опускают в глубокие впадины морского дна.
Захоронение особо опасных отходов - одна из
наиболее
трудноразрешимых
проблем
охраны
окружающей среды, так как места для их абсолютно
безопасного изолирования от биосферы пока не
найдено.
207
208. Использование промышленных и коммунально-бытовых отходов в сельском хозяйстве
Использование промышленных и коммунальнобытовых отходов в сельском хозяйствеВесьма перспективным является использование ряда
промышленных и коммунально-бытовых отходов в
сельском хозяйстве, где они могут найти применение в
качестве мелиорантов или удобрений-мелиорантов.
В большинстве случаев мелиоративное использование
промышленных отходов имеет высокую экономическую
эффективность.
Для успешного использования промышленных отходов
в сельском хозяйстве необходимо глубокое и
всестороннее изучение их свойств и влияния на
основные агрохимические характеристики почвы и
качество сельскохозяйственной продукции.
208
209. Применение промышленных отходов для мелиорации кислых почв
Большинство пахотных земель в основныхэкономических районах относится к кислым
почвам: на Дальнем Востоке они составляют 94
% пашни, в Центрально-Нечерноземном районе
- 83%, в Волго-Вятском - до 80%.
Неблагоприятные агрохимические свойства
кислых почв могут быть устранены их
известкованием.
При
этом
происходит
вытеснение катионов водорода из ППК, а
образующаяся Н2СО3 распадается до Н20 и
С02.
209
210. В качестве известковых мелиорантов
могут быть использованы кальций содержащие промышленныеотходы:
отходы
металлургической
промышленности
(доменные,
мартеновские, электроплавильные шлаки, шлак магниевого
литья, шлак ванадиевого производства, отходы производства
феррохромовых сплавов);
золы (зола горючих сланцев, золы уноса ТЭС, каменноугольные
и буроугольные золы, торфяная зола);
отходы промышленности строительных материалов (карьерные
отходы, отходы производства известнякового щебня, отходы
цементных заводов, мраморная крошка);
отходы свеклосахарного производства (дефекационная и
фильтр-прессная грязь);
крупнотоннажные отходы ряда других производств, в том числе
отходы бумажной, кожевенной, содовой, асбестовой и других
отраслей промышленности, а также флотационные отходы,
получаемые при обогащении некоторых руд.
210







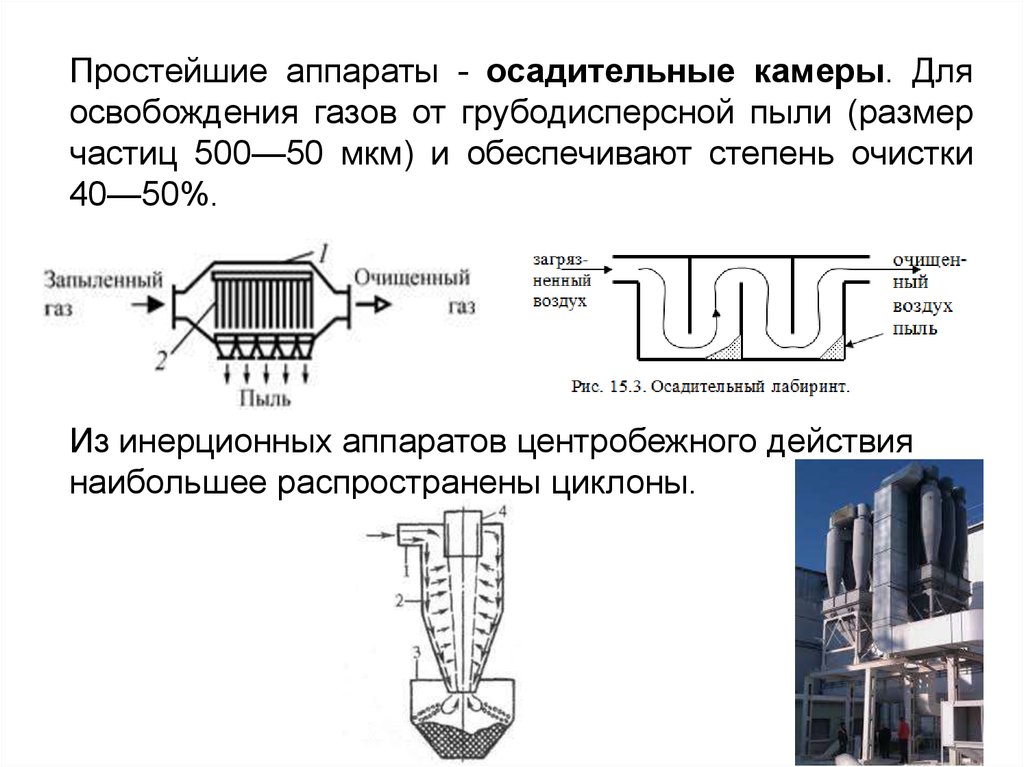
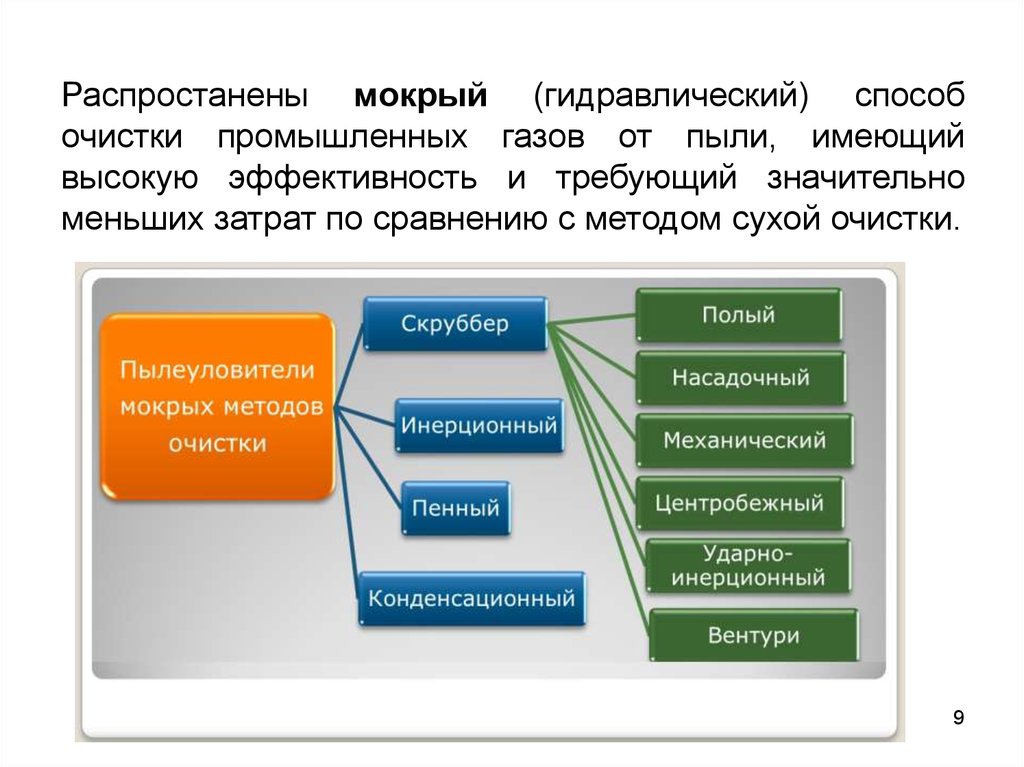

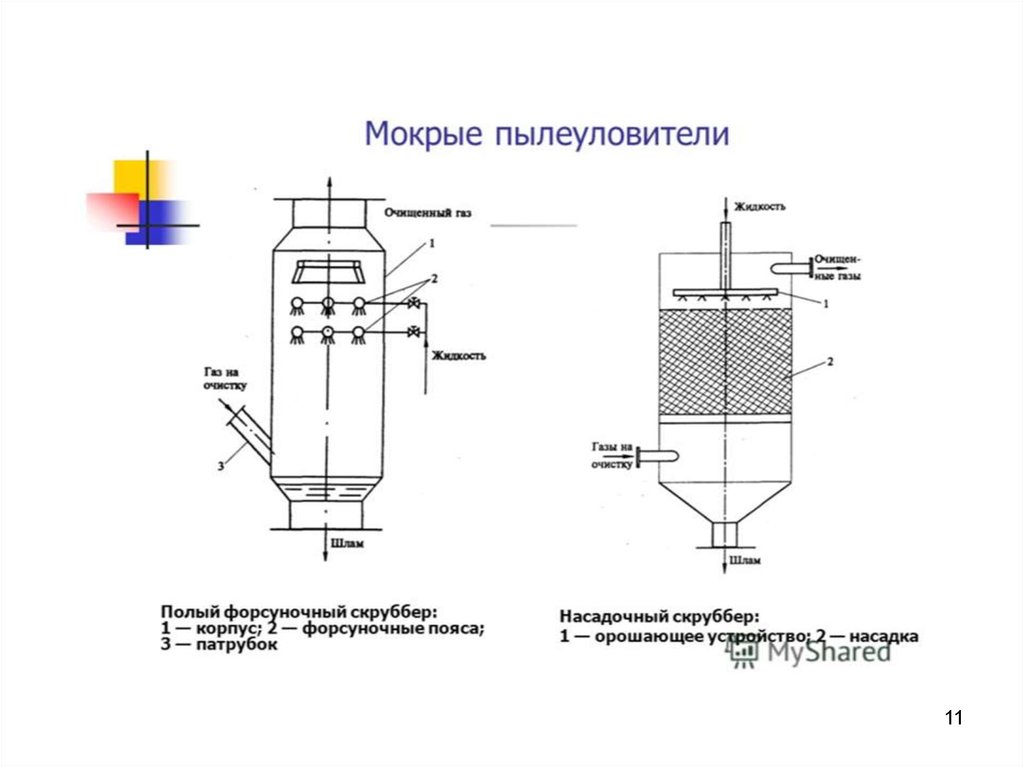
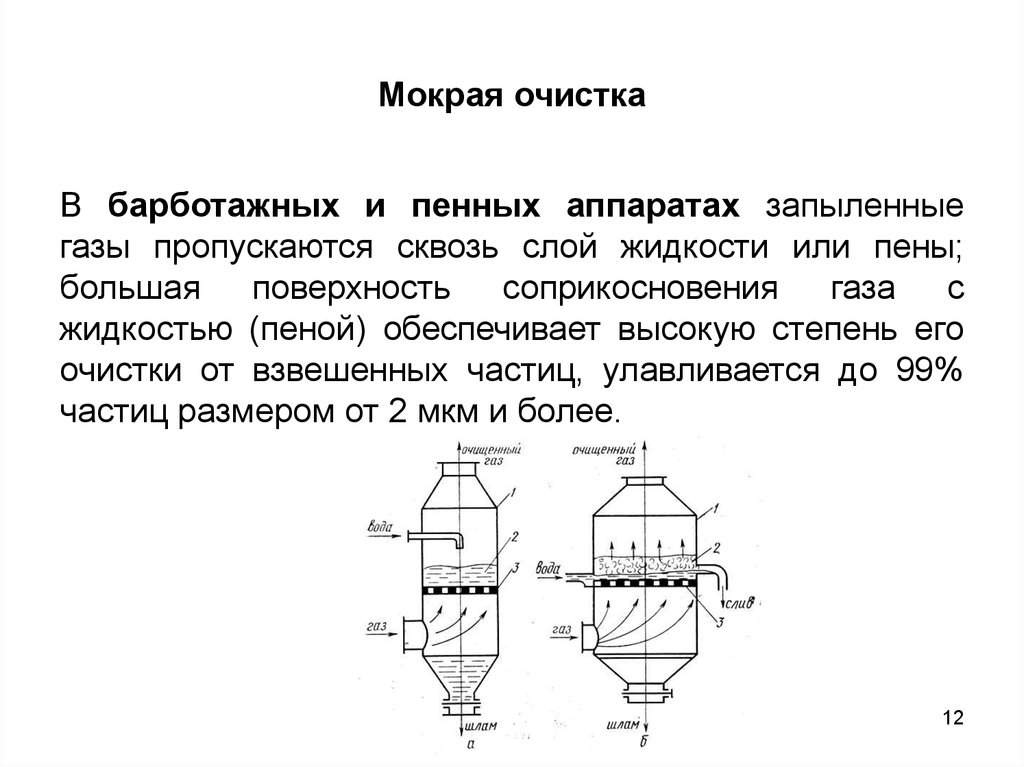
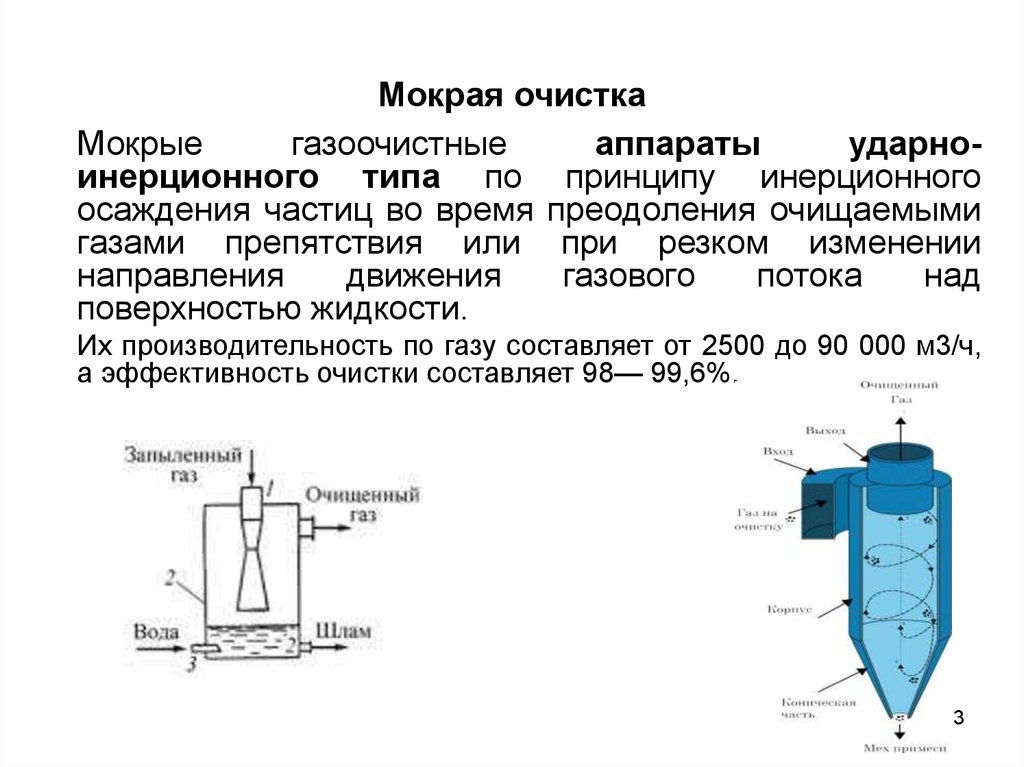


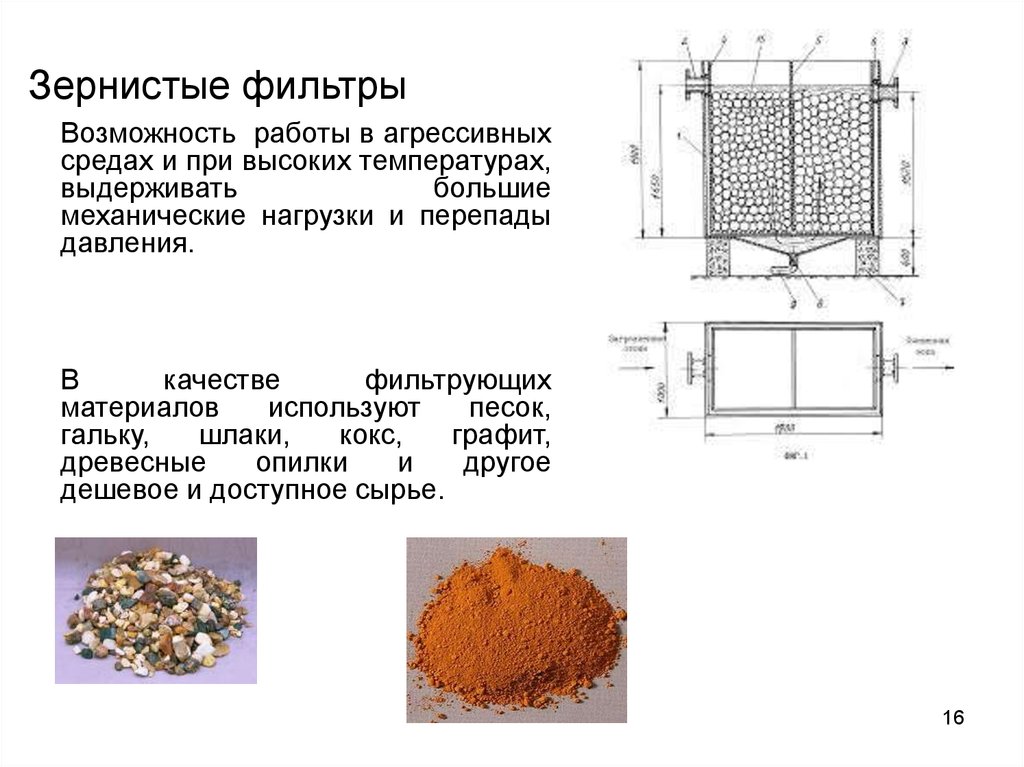

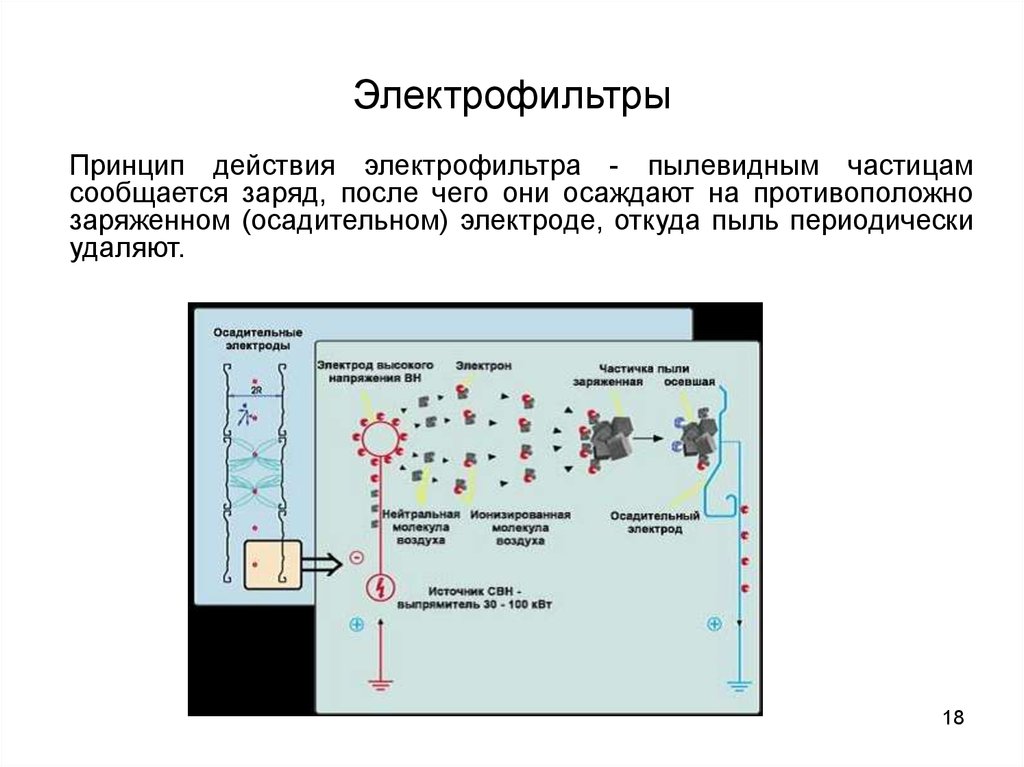
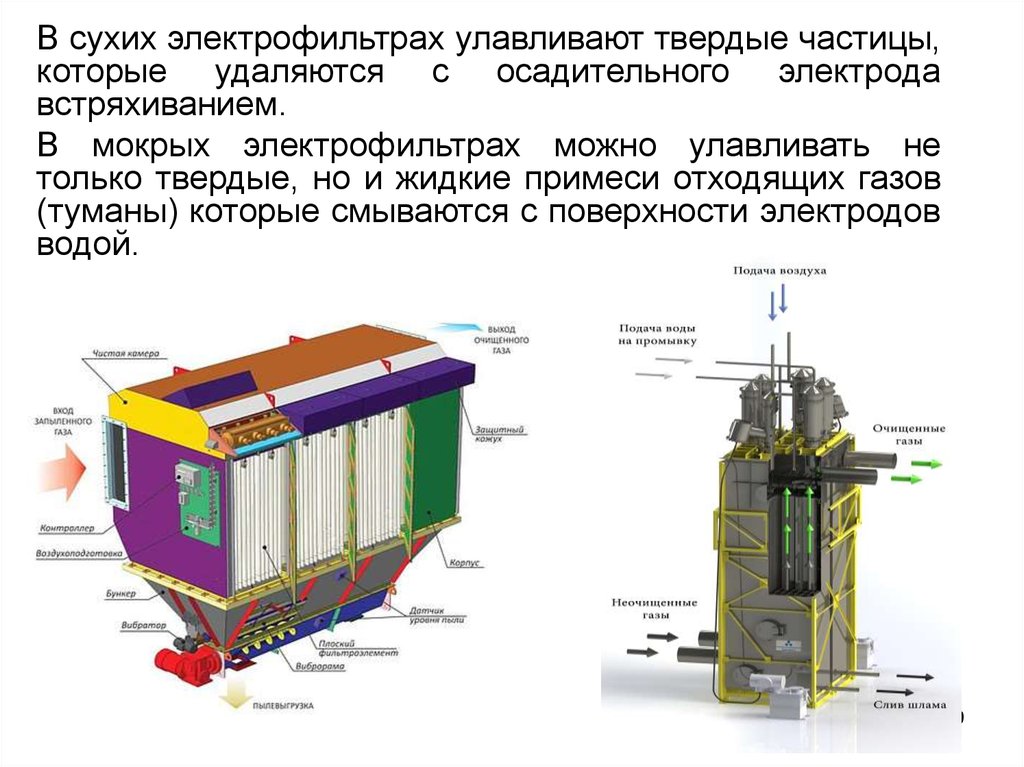

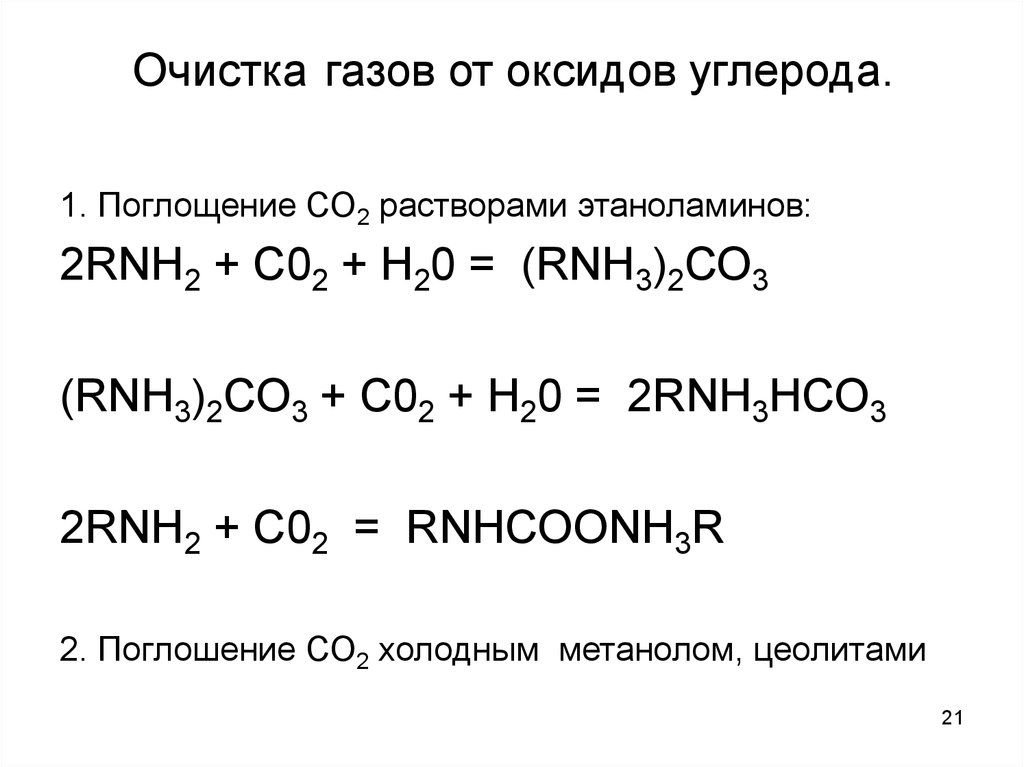

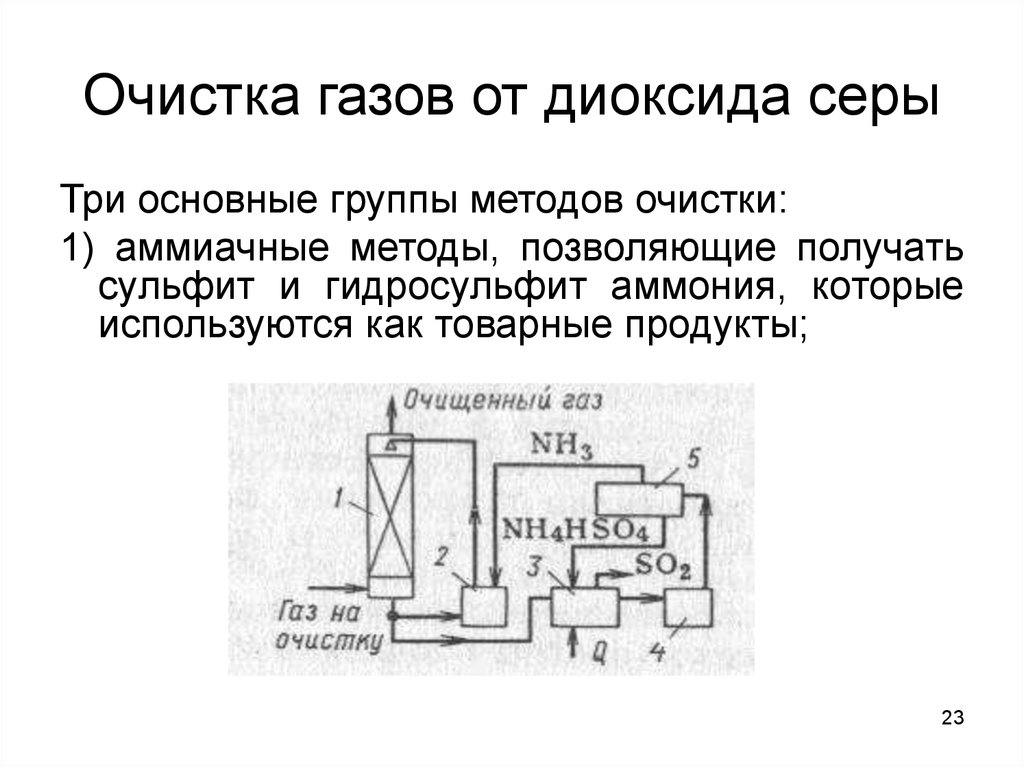
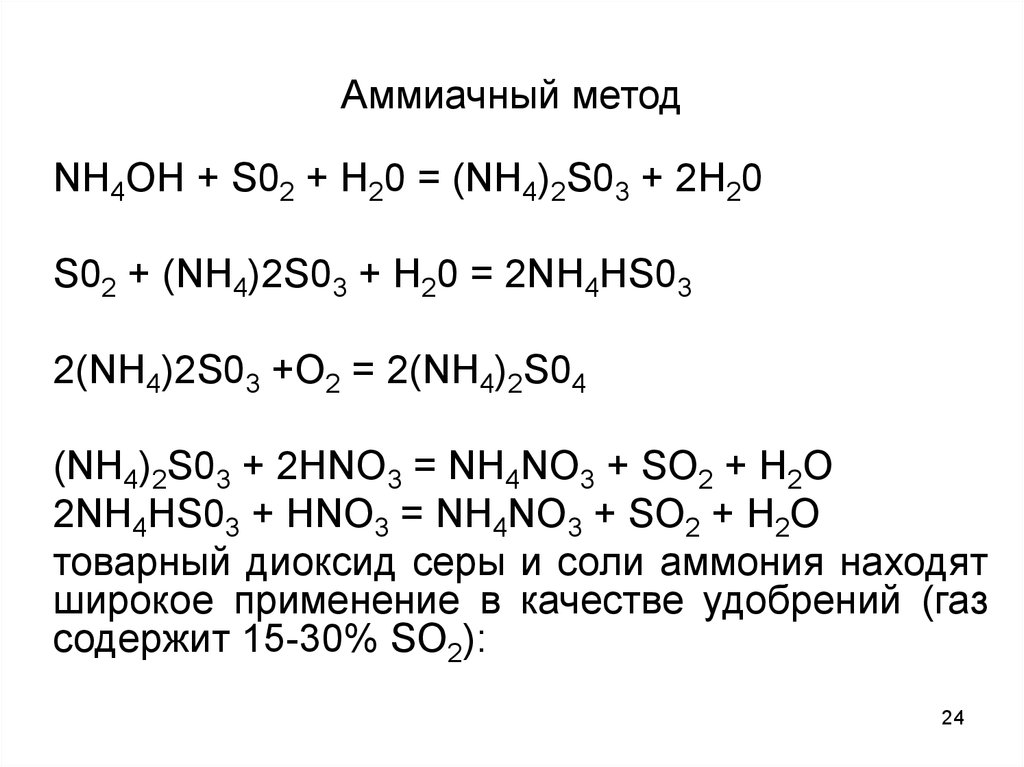
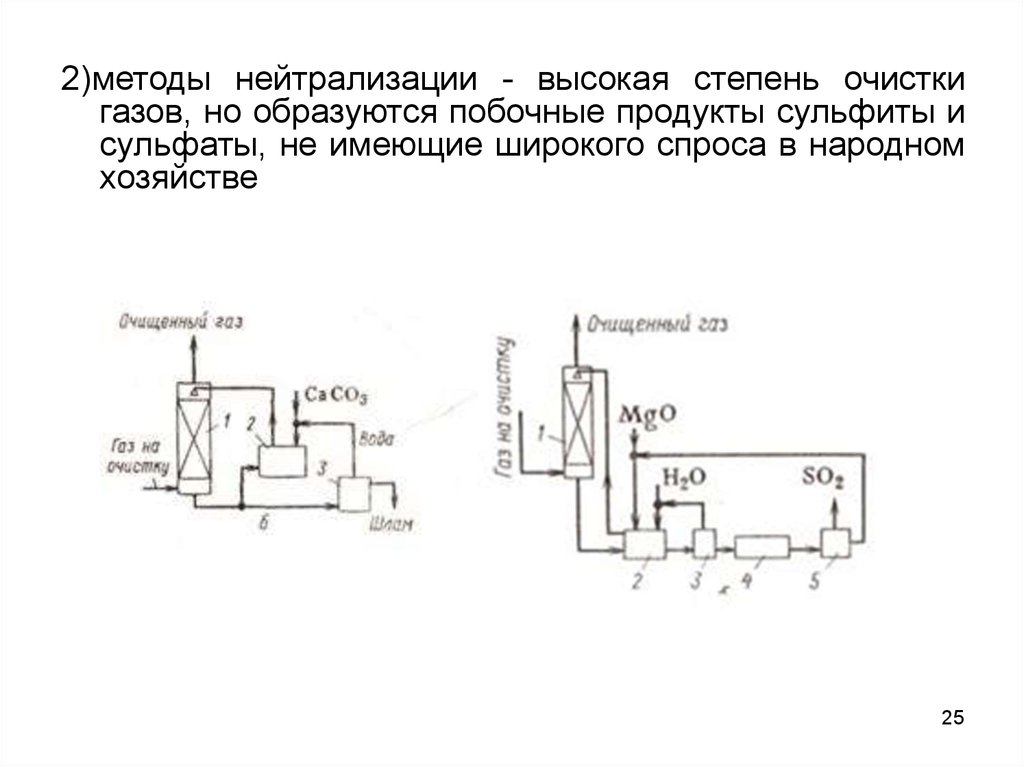



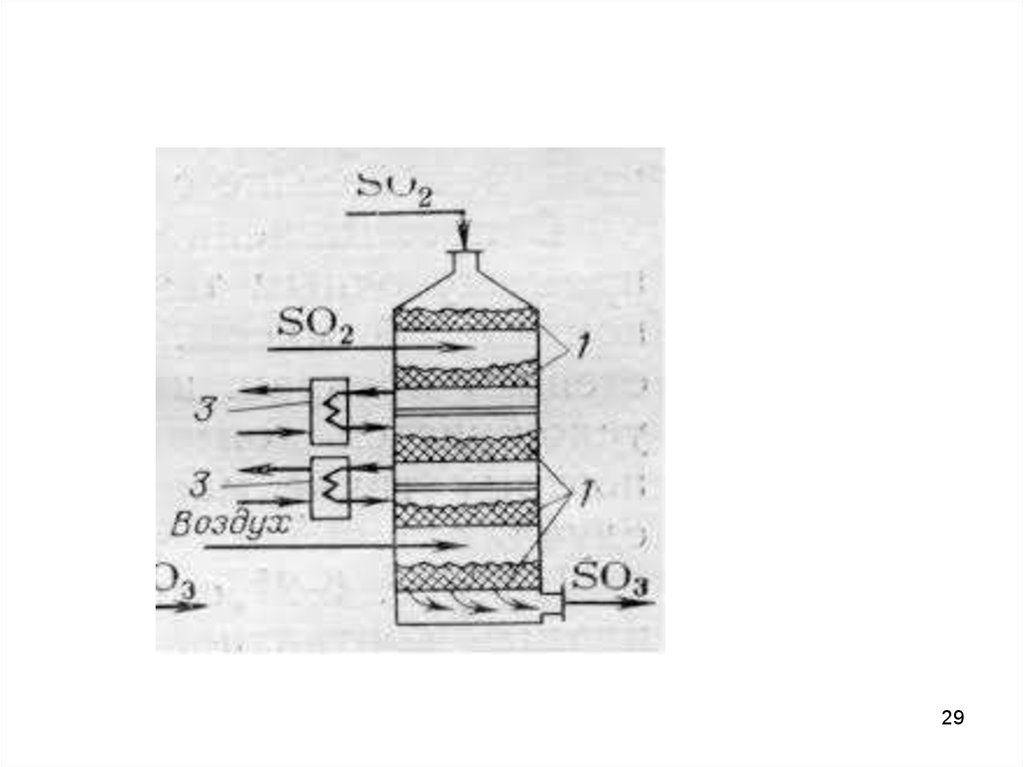
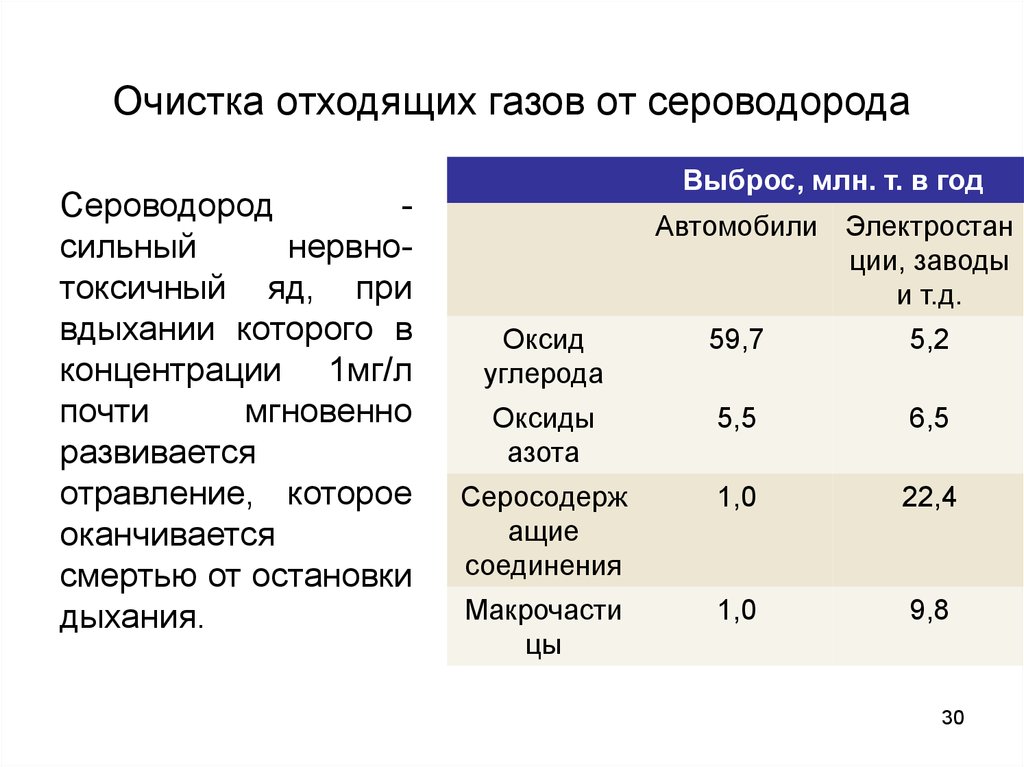





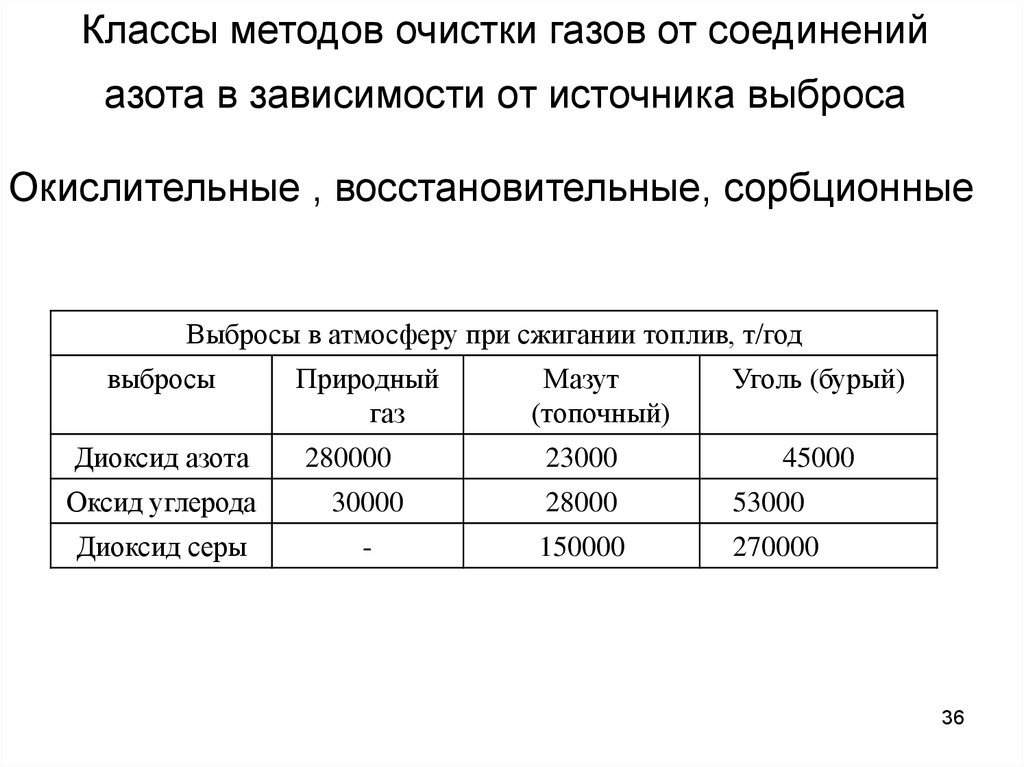

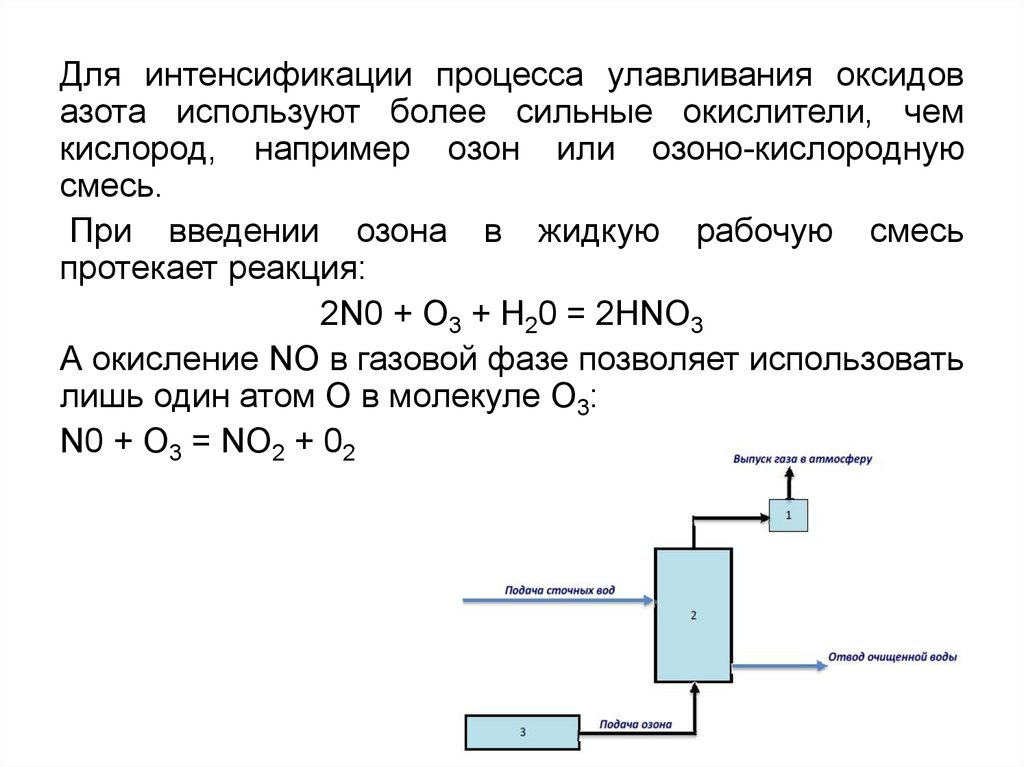


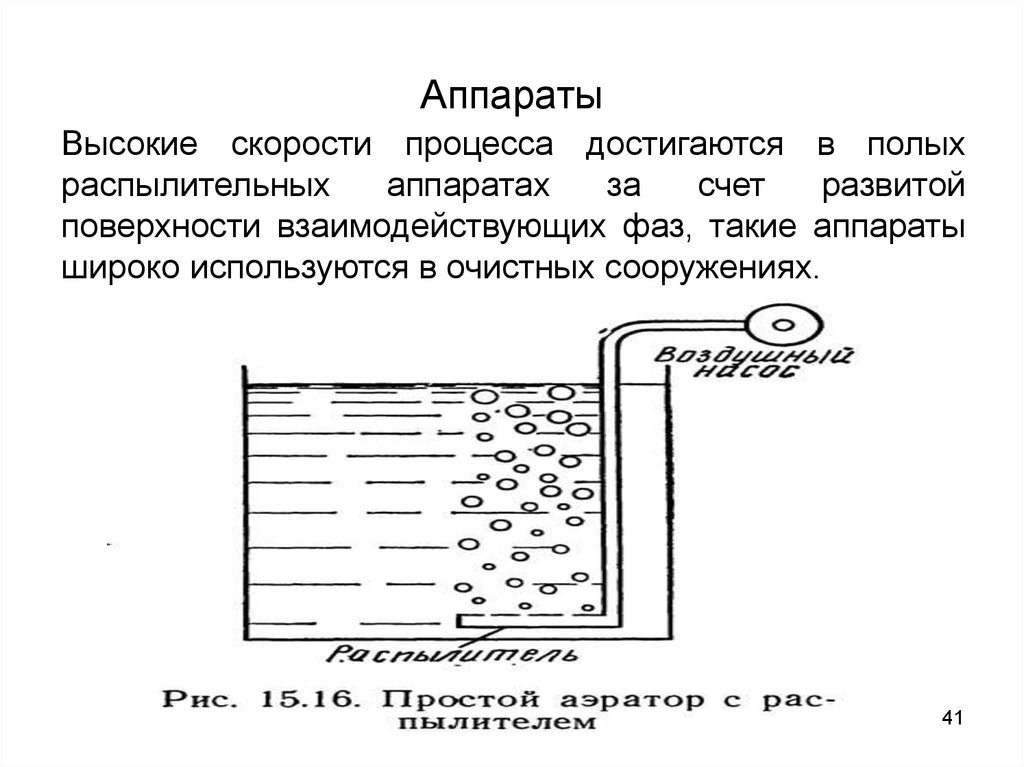


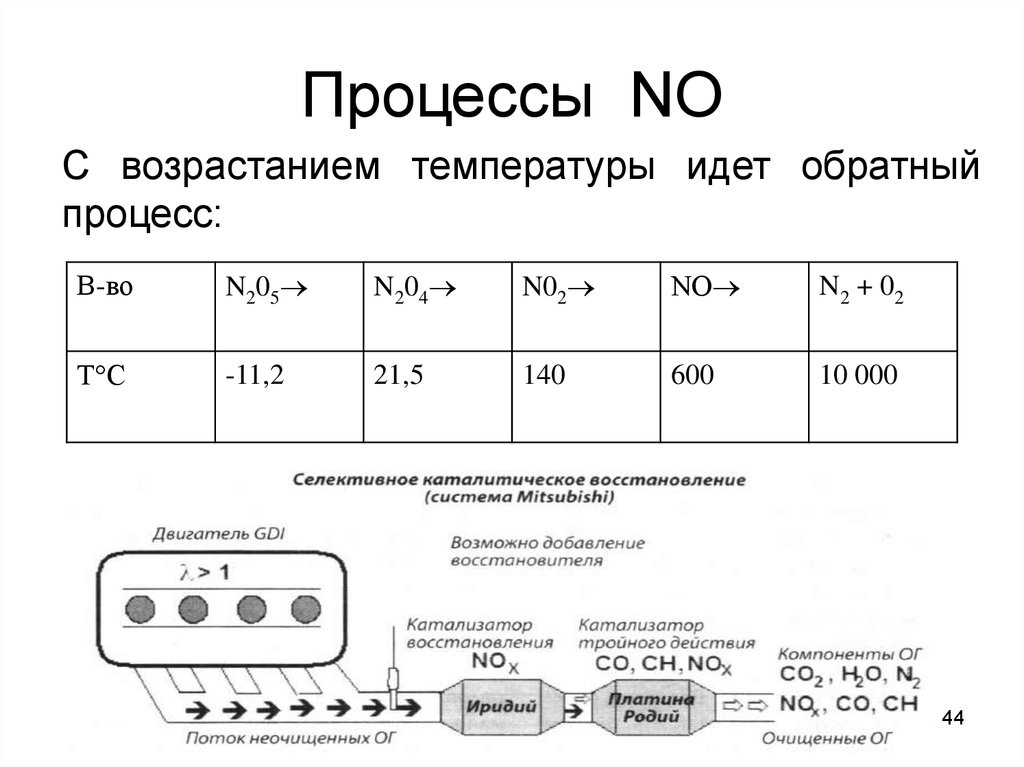
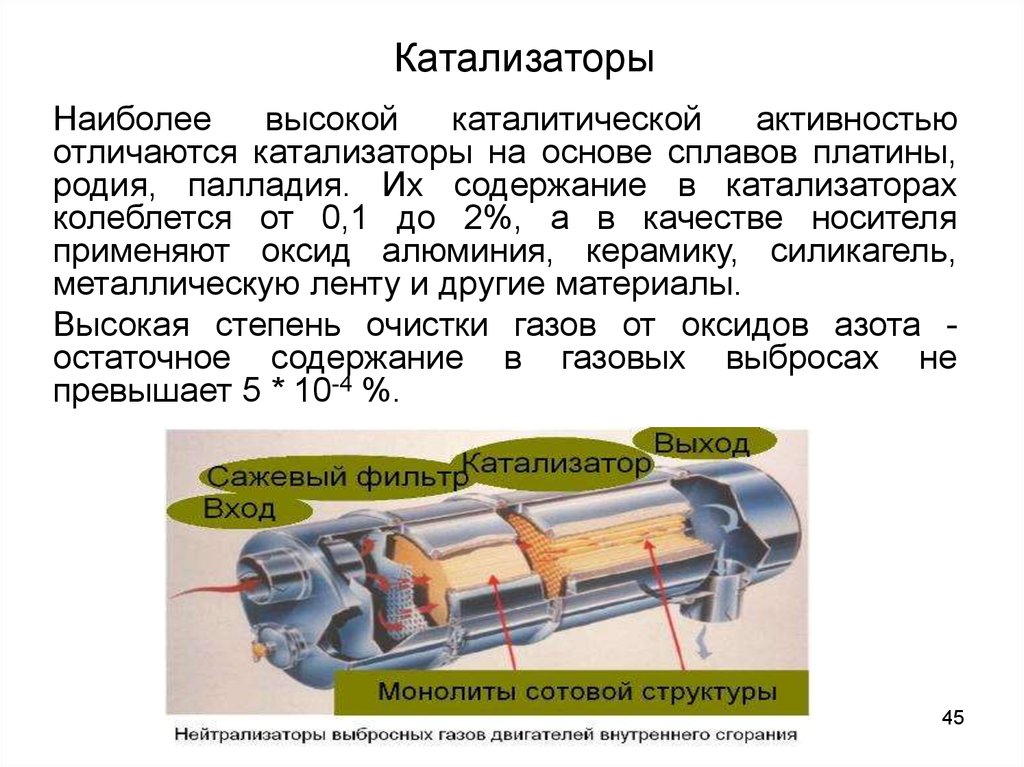


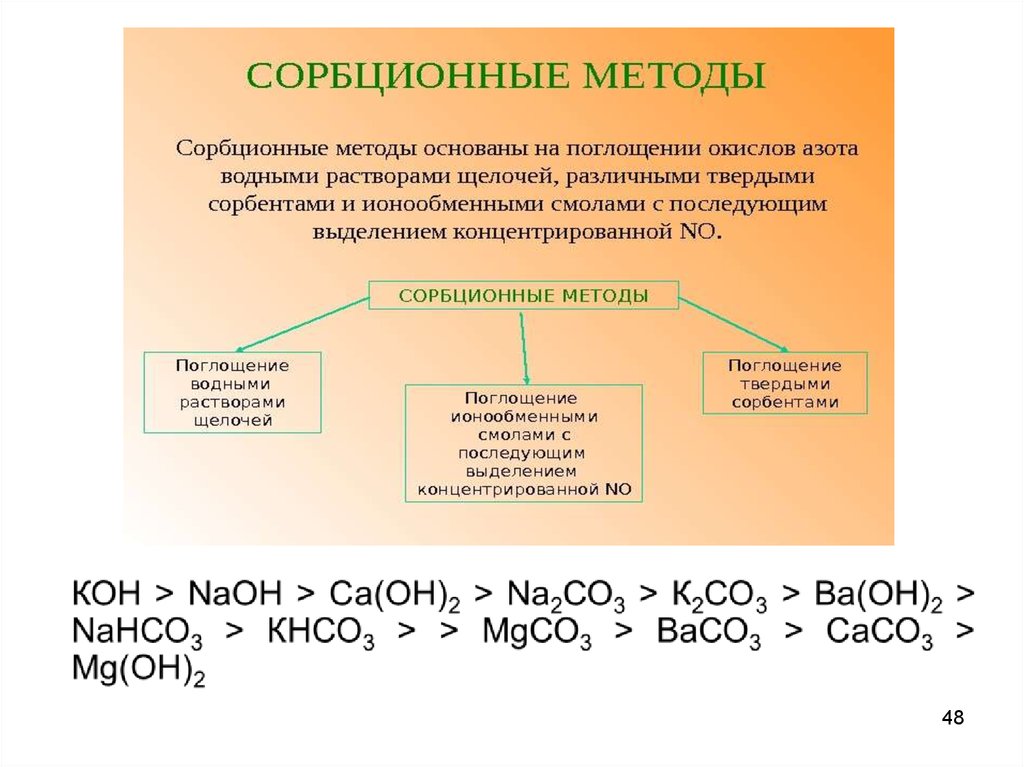


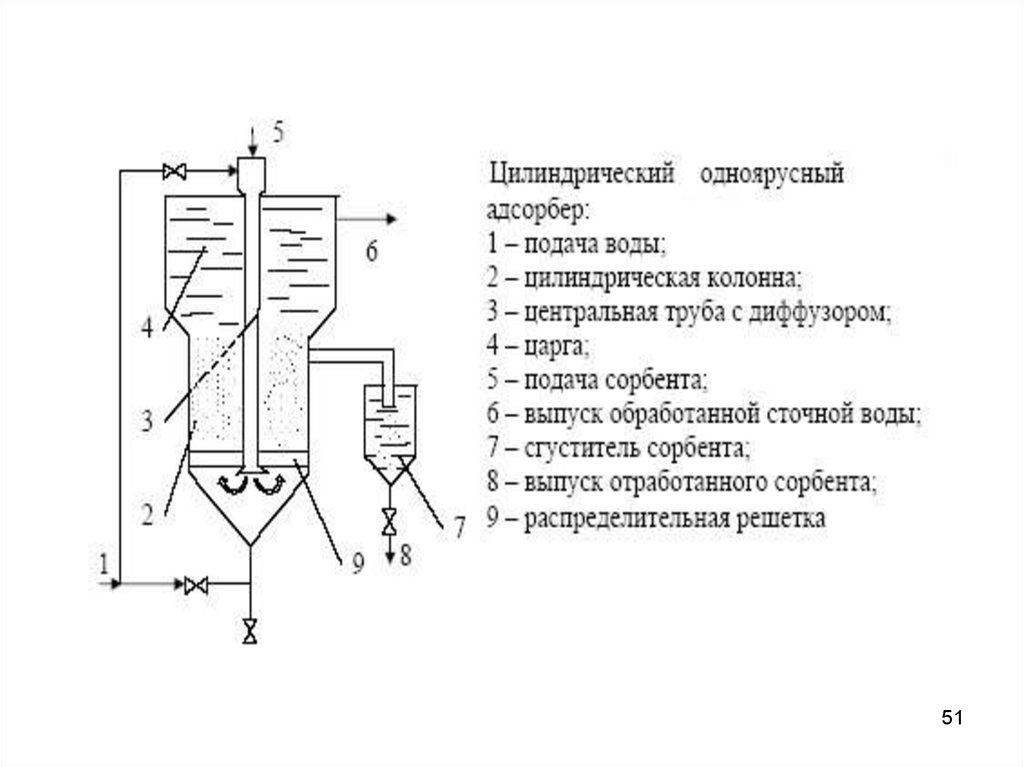

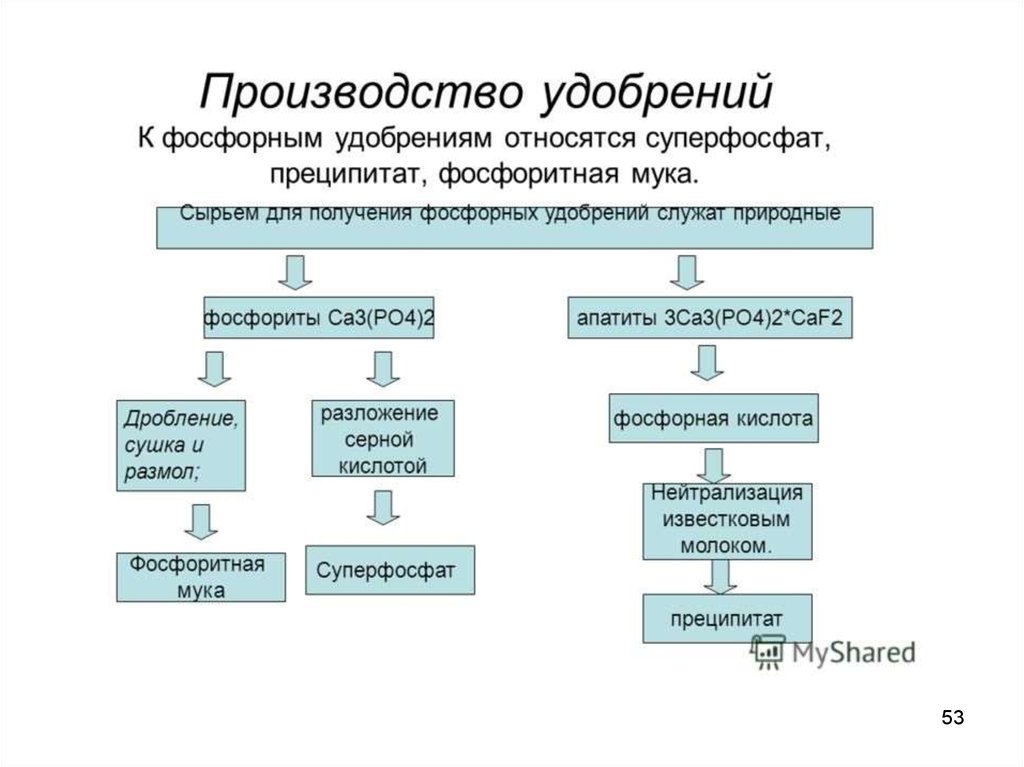




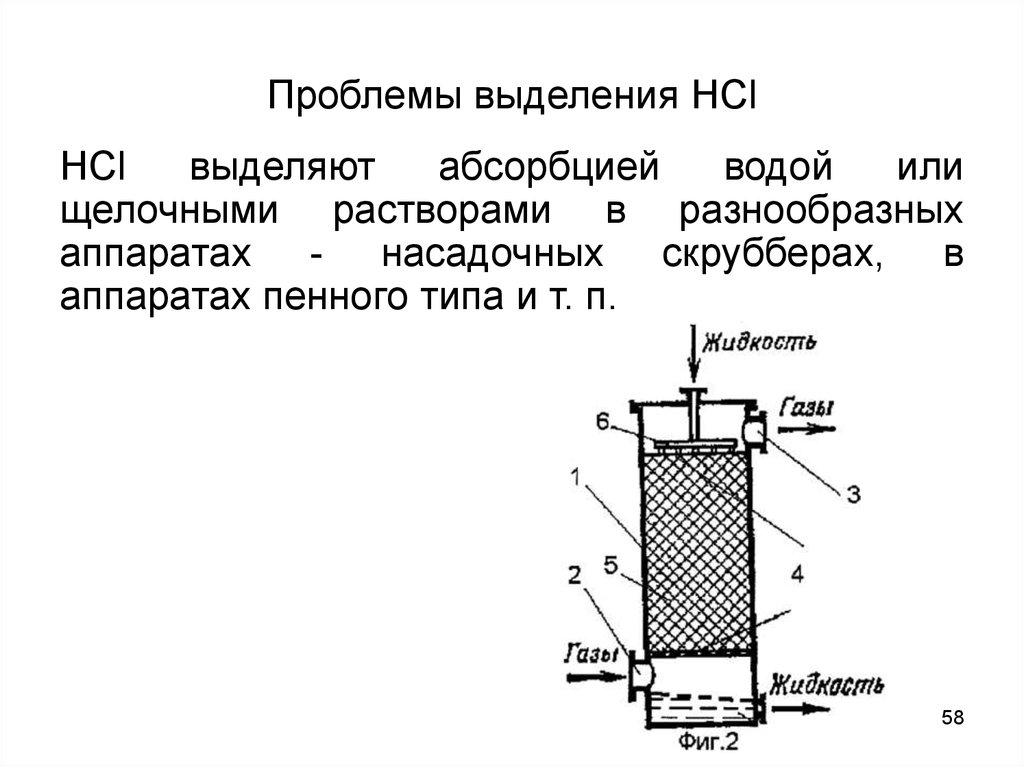






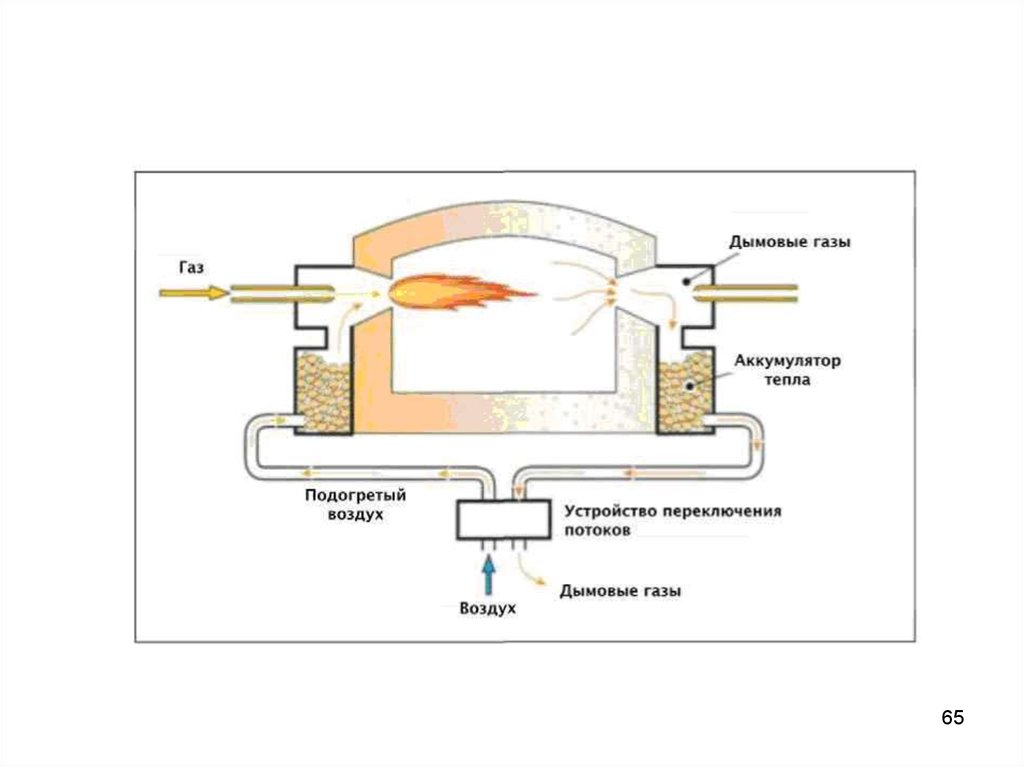




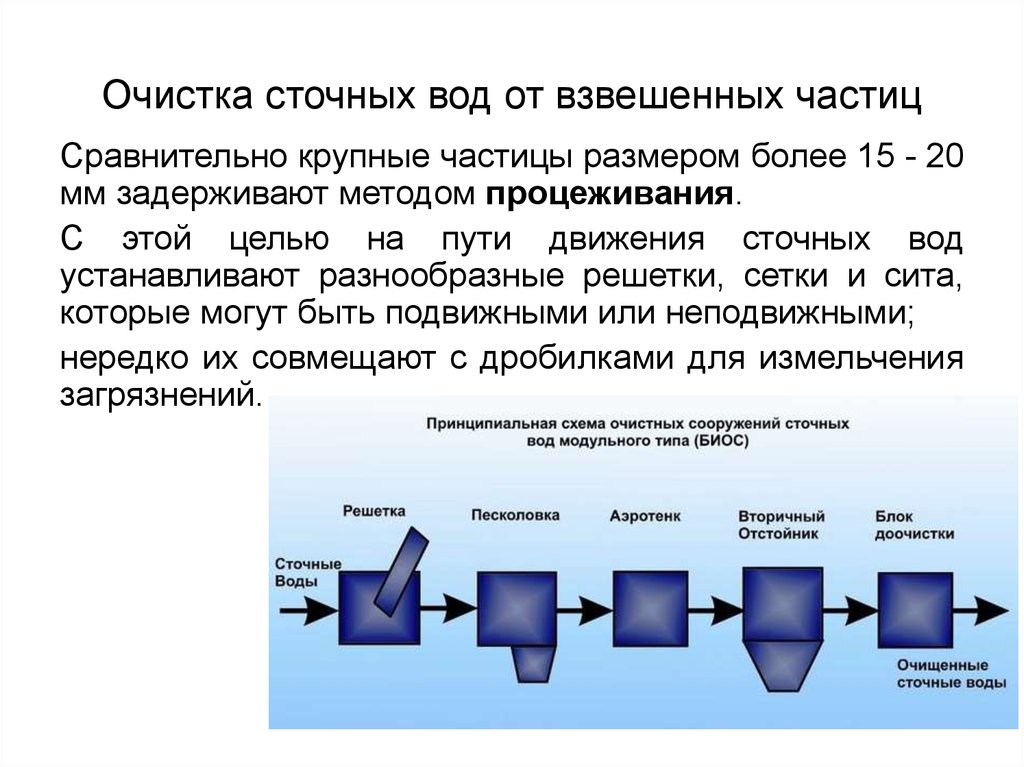
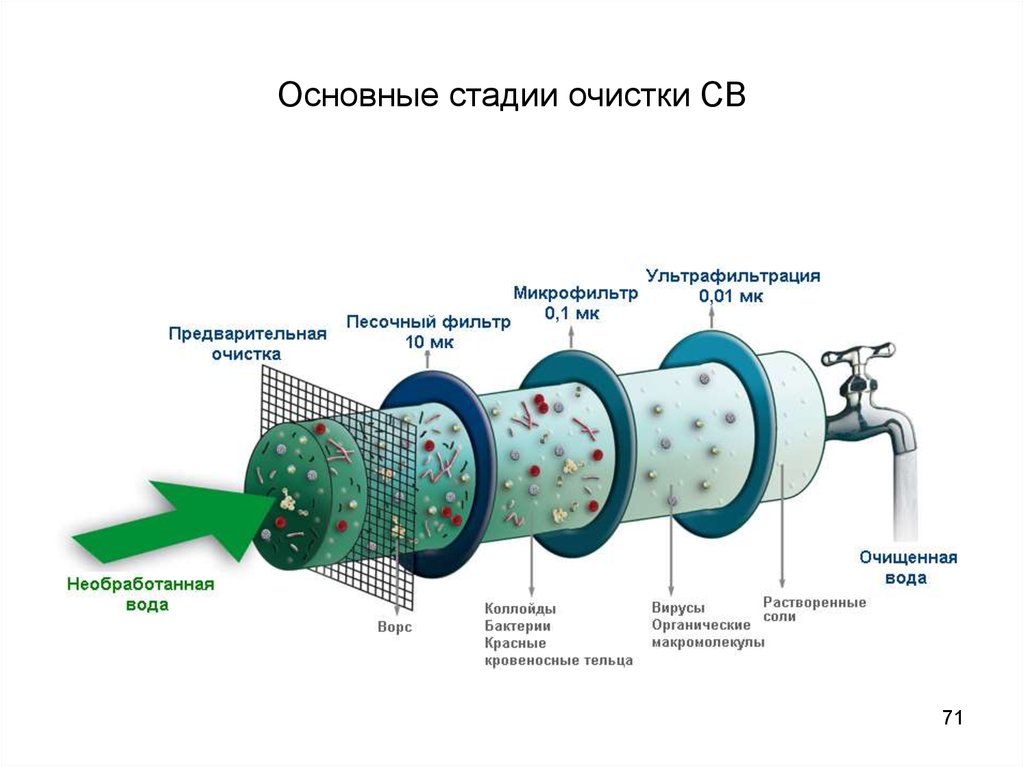









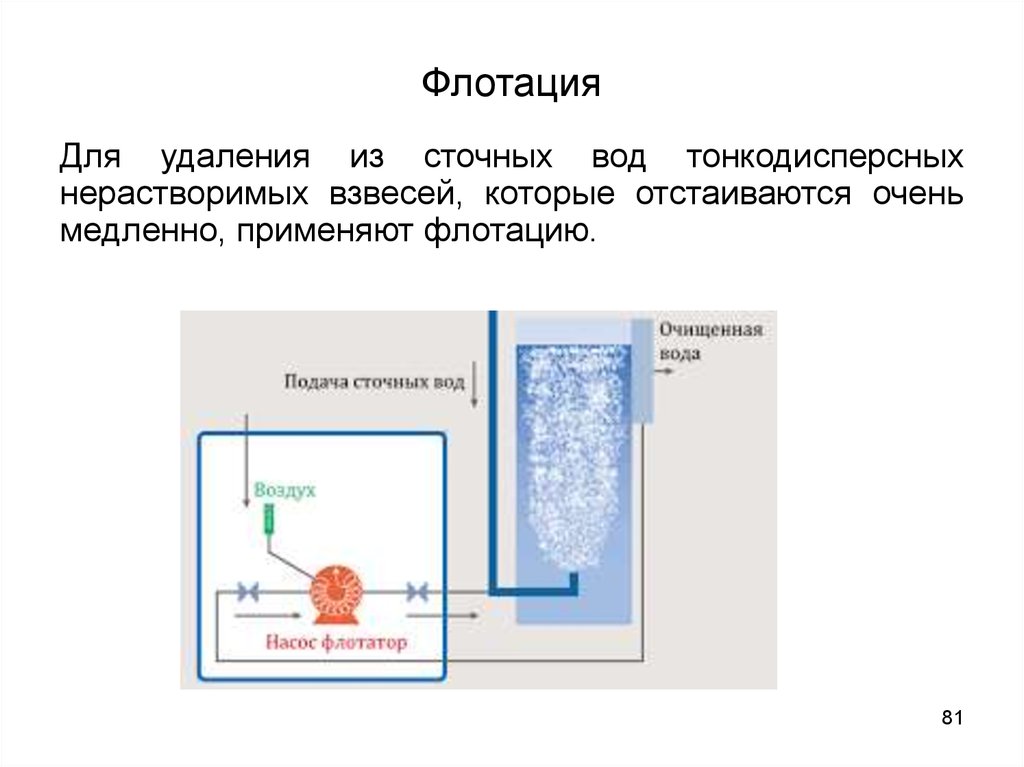



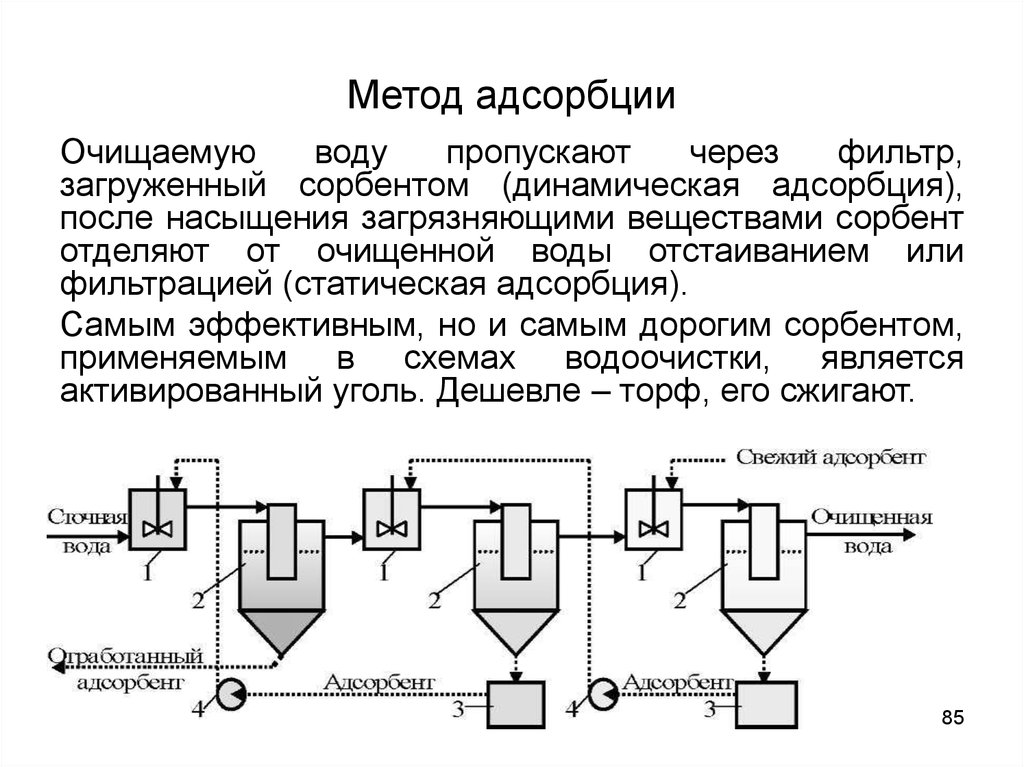
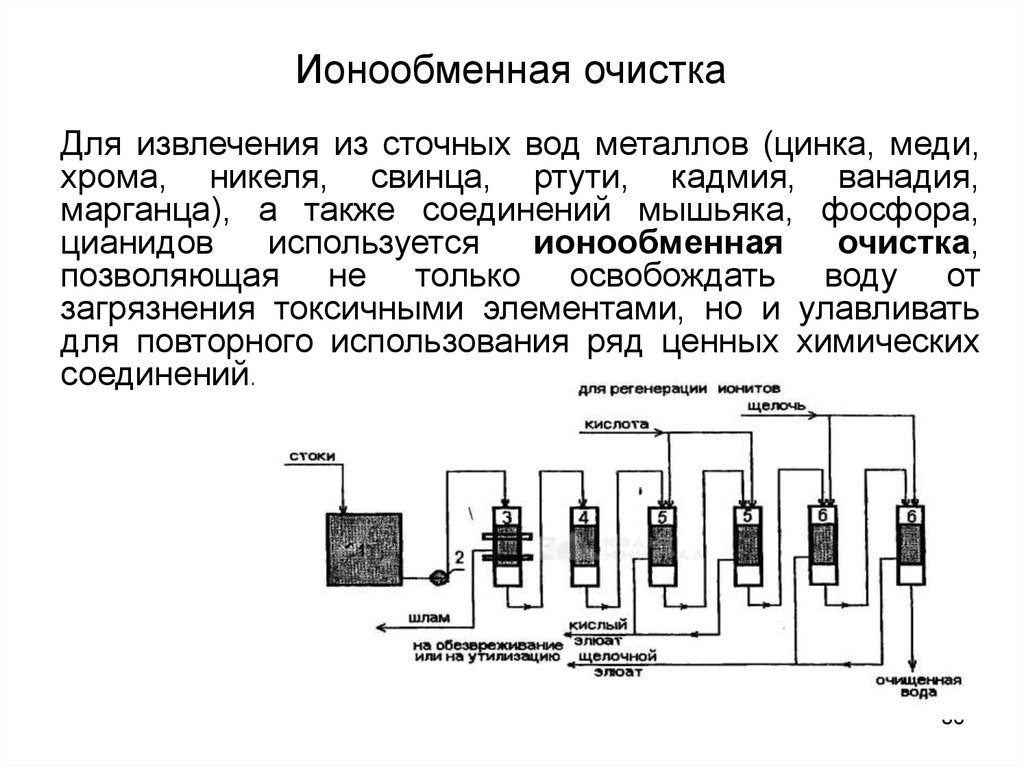


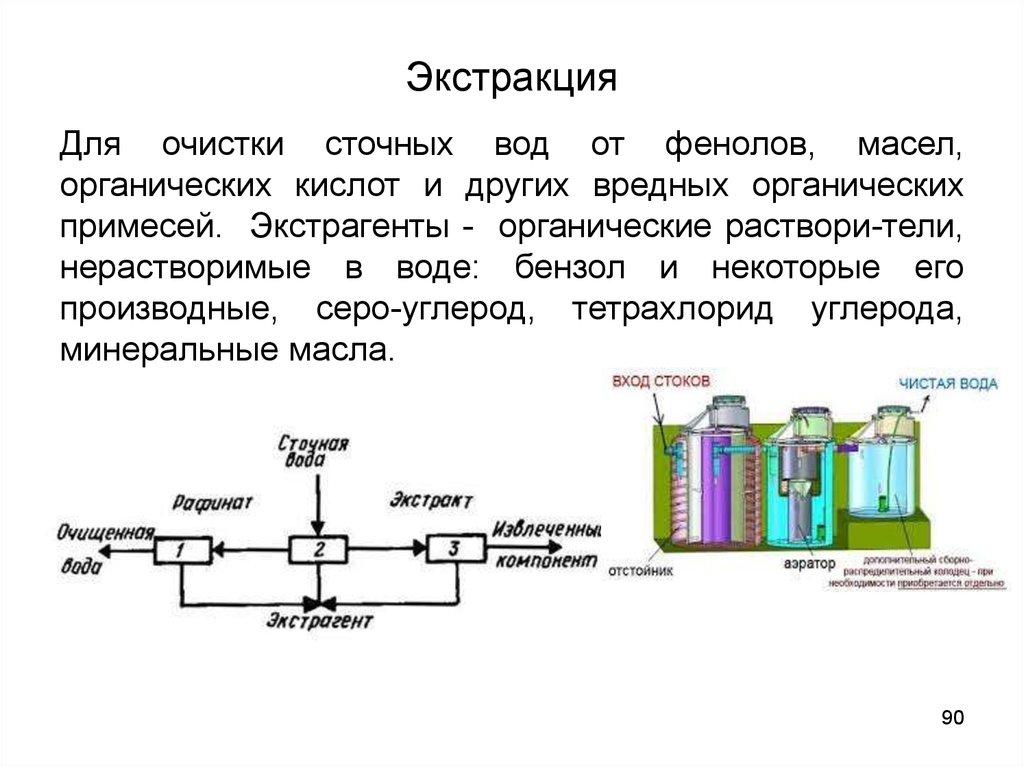

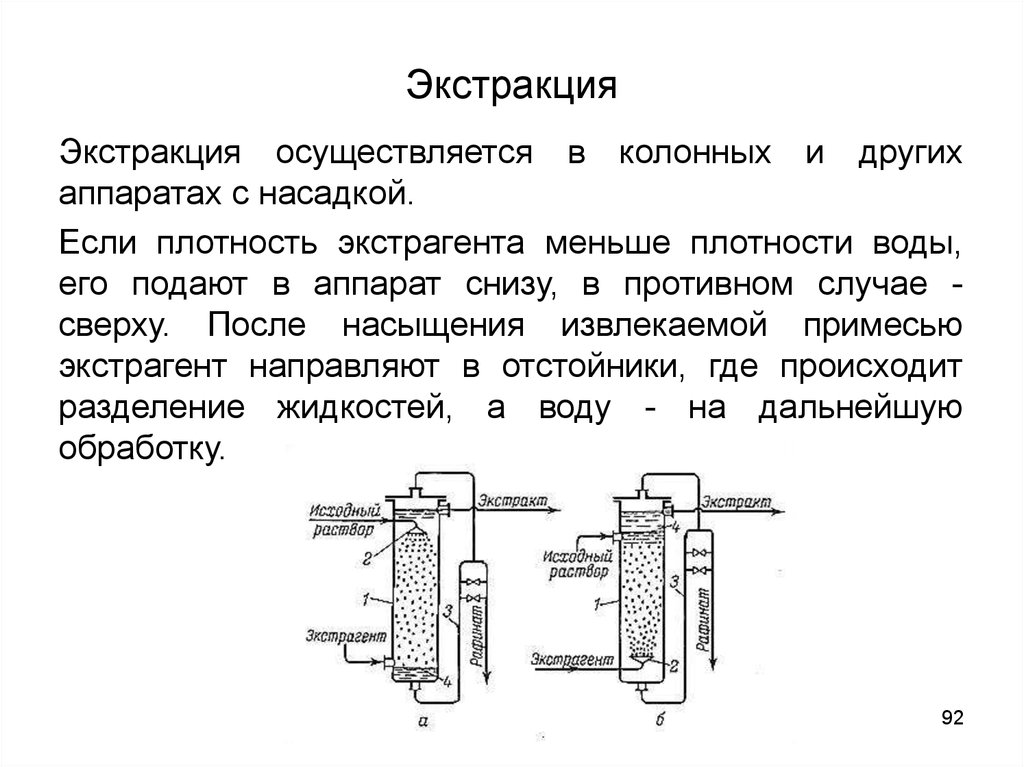

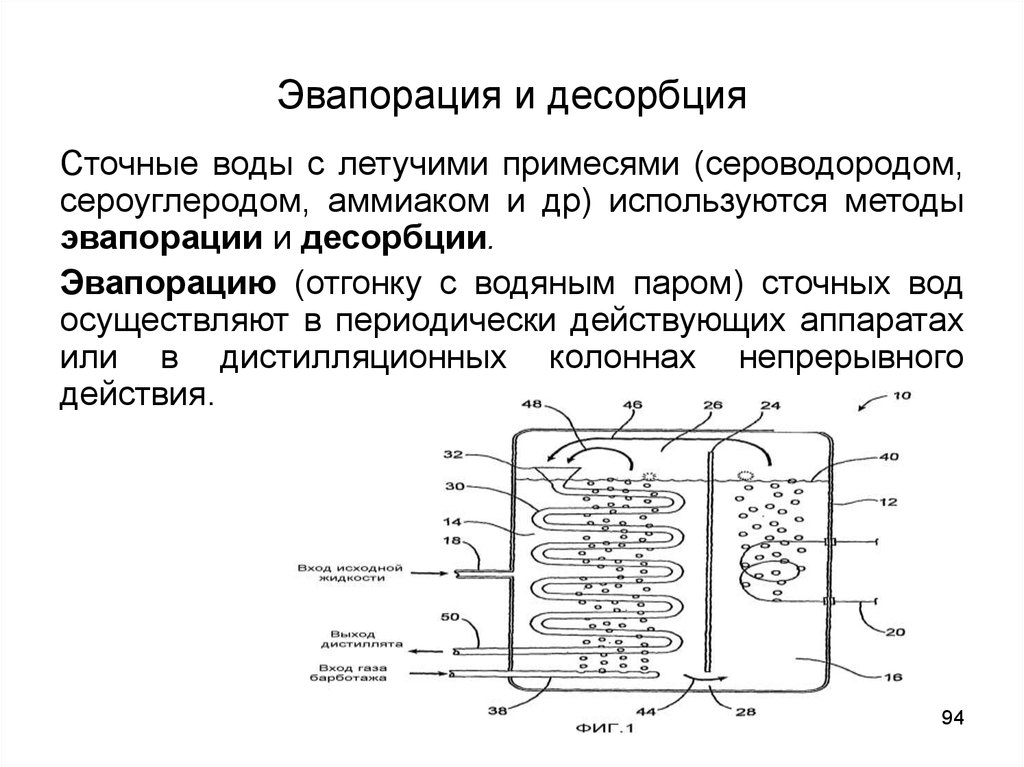


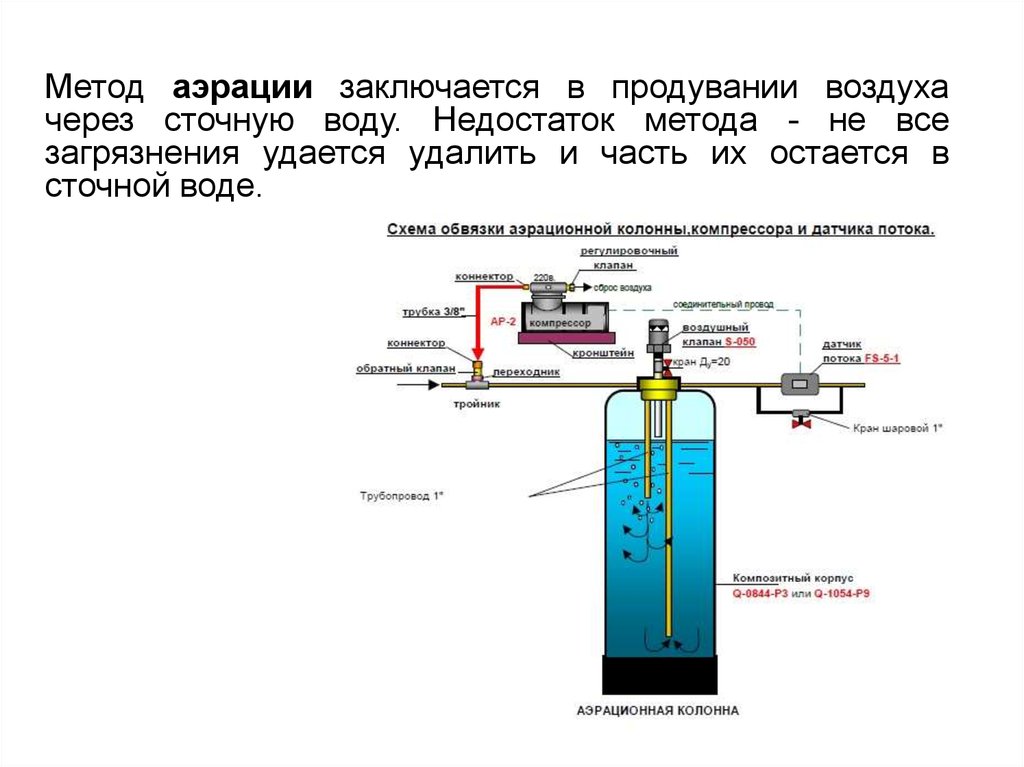
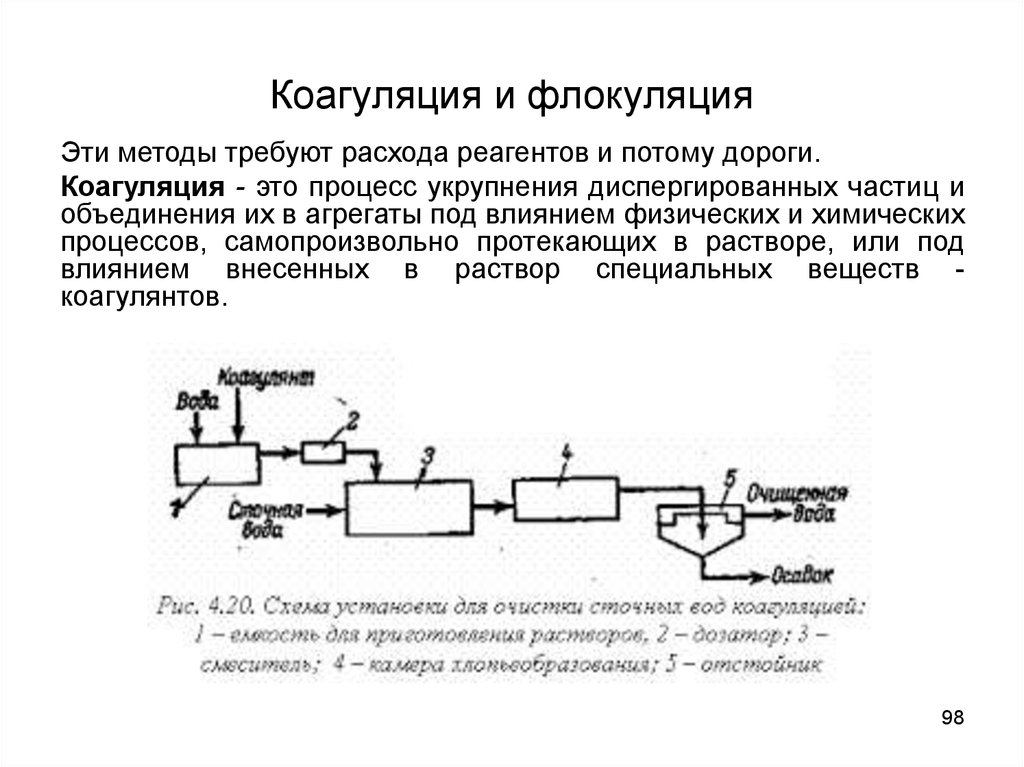

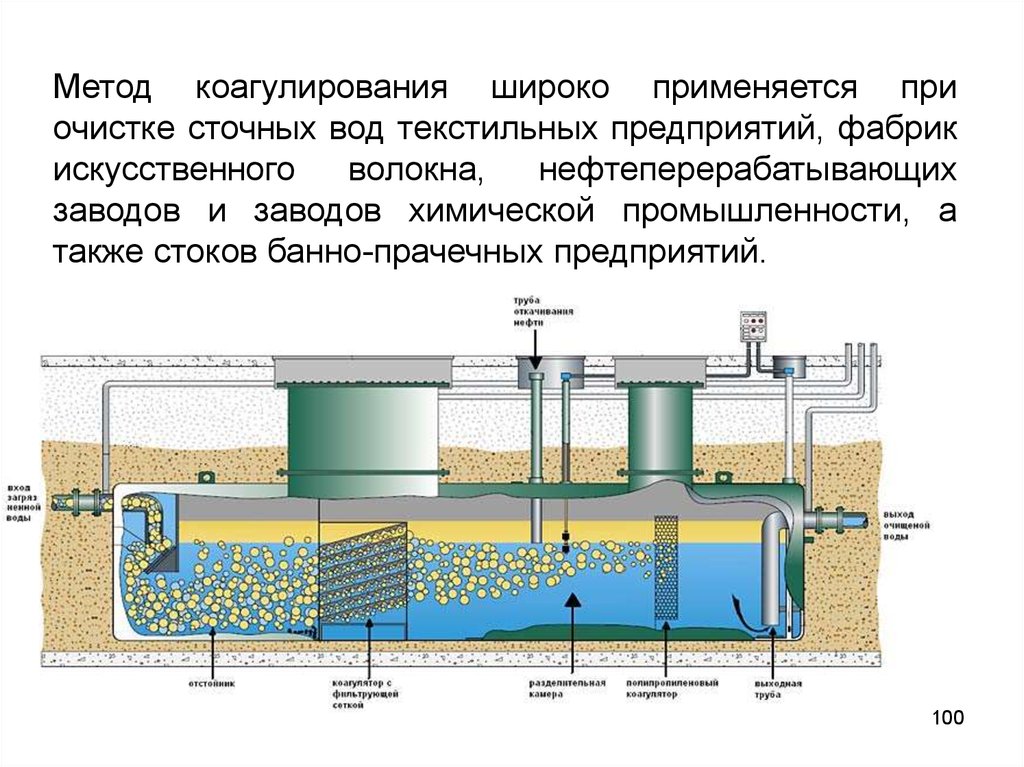

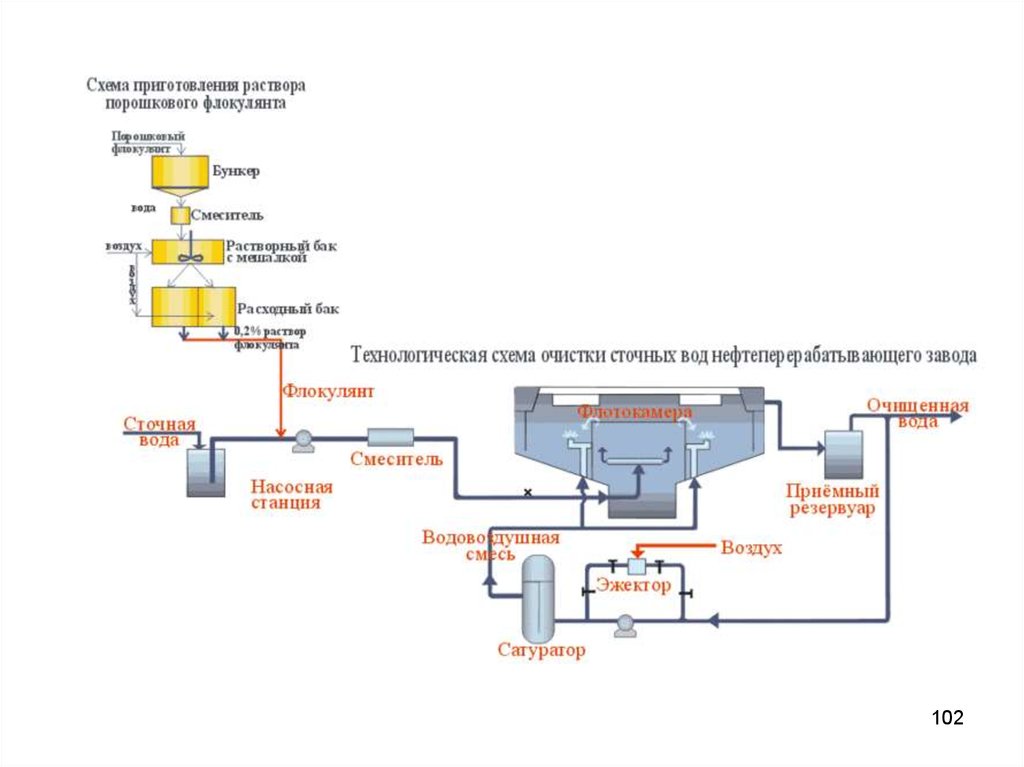

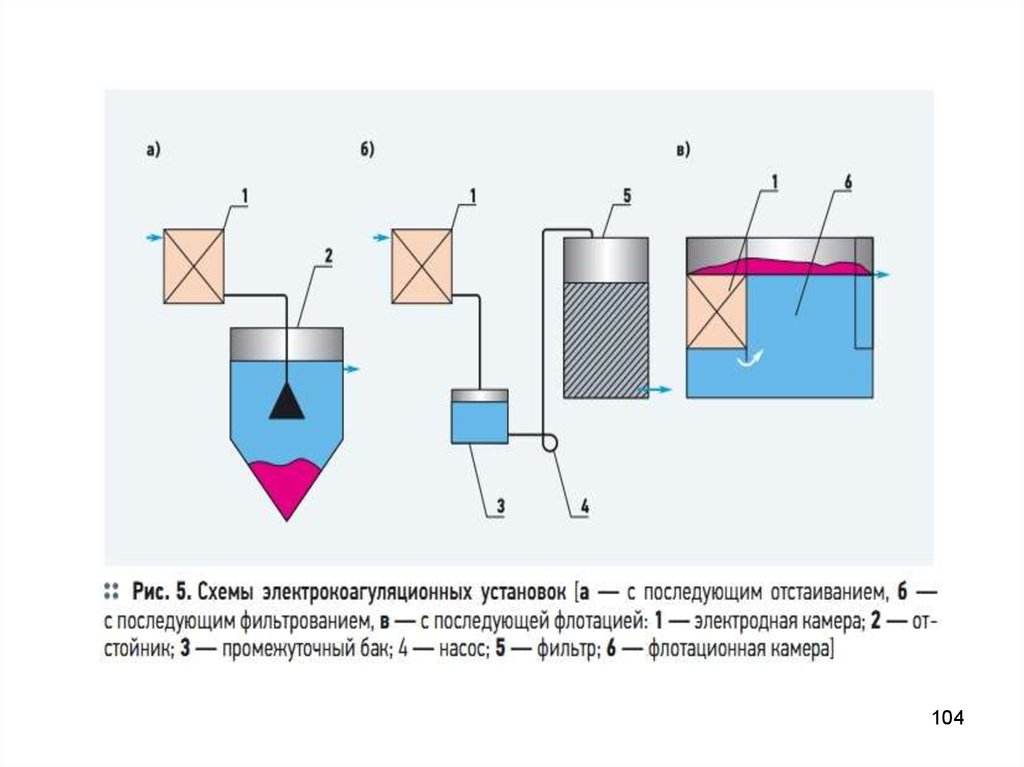
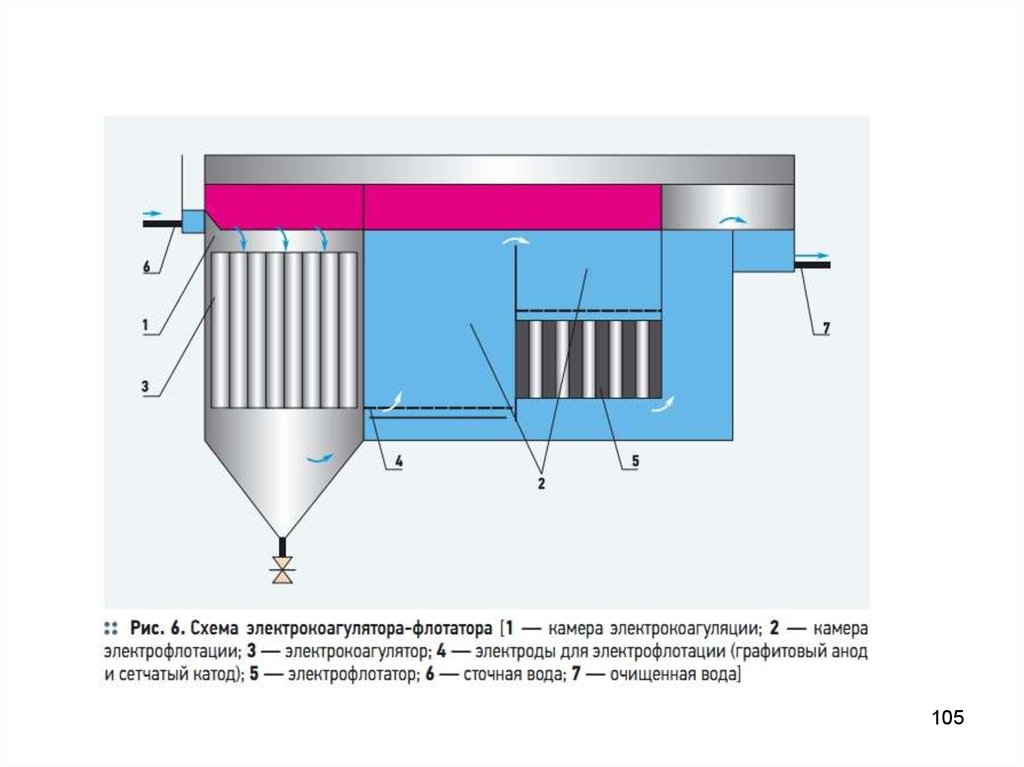

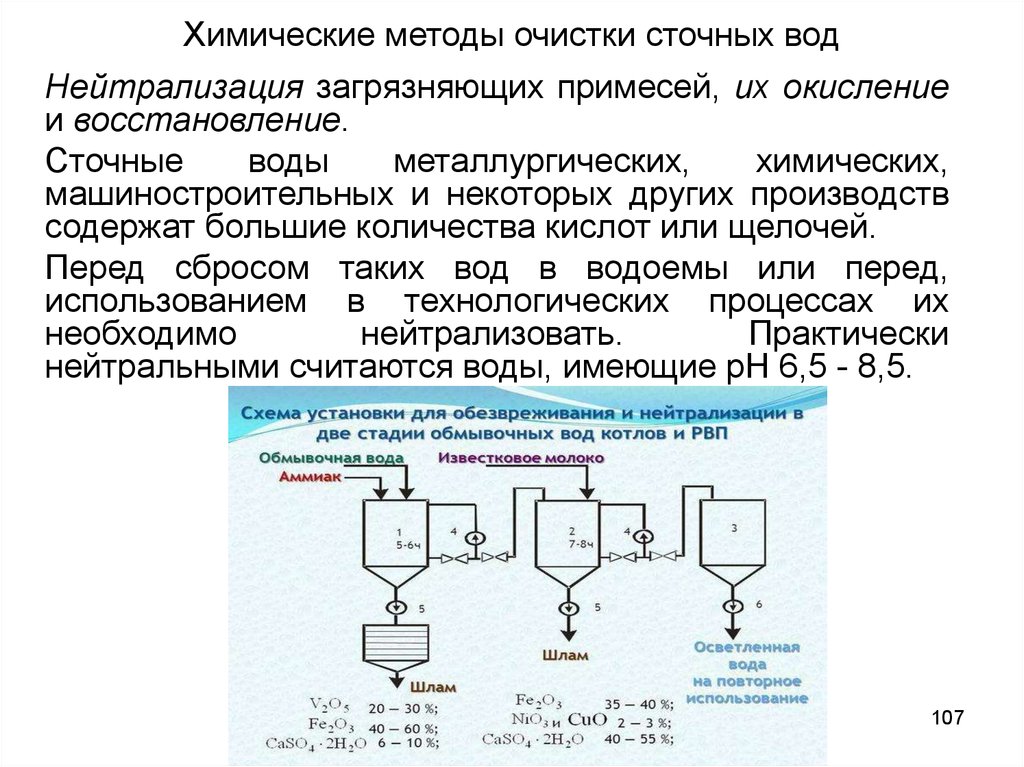

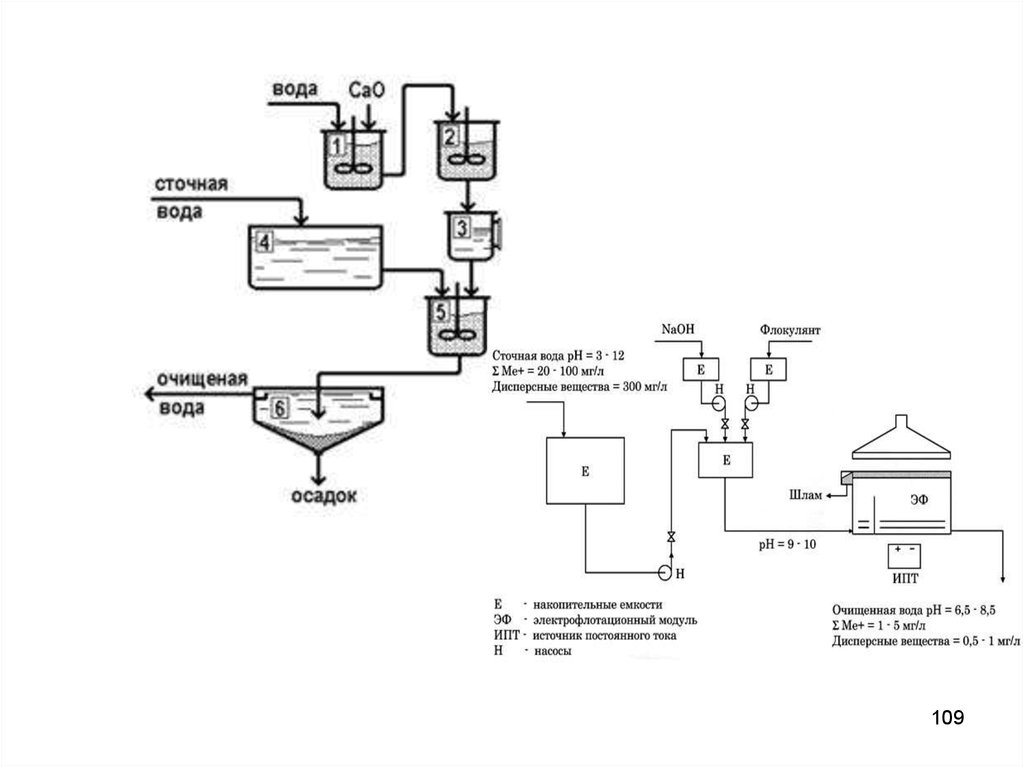

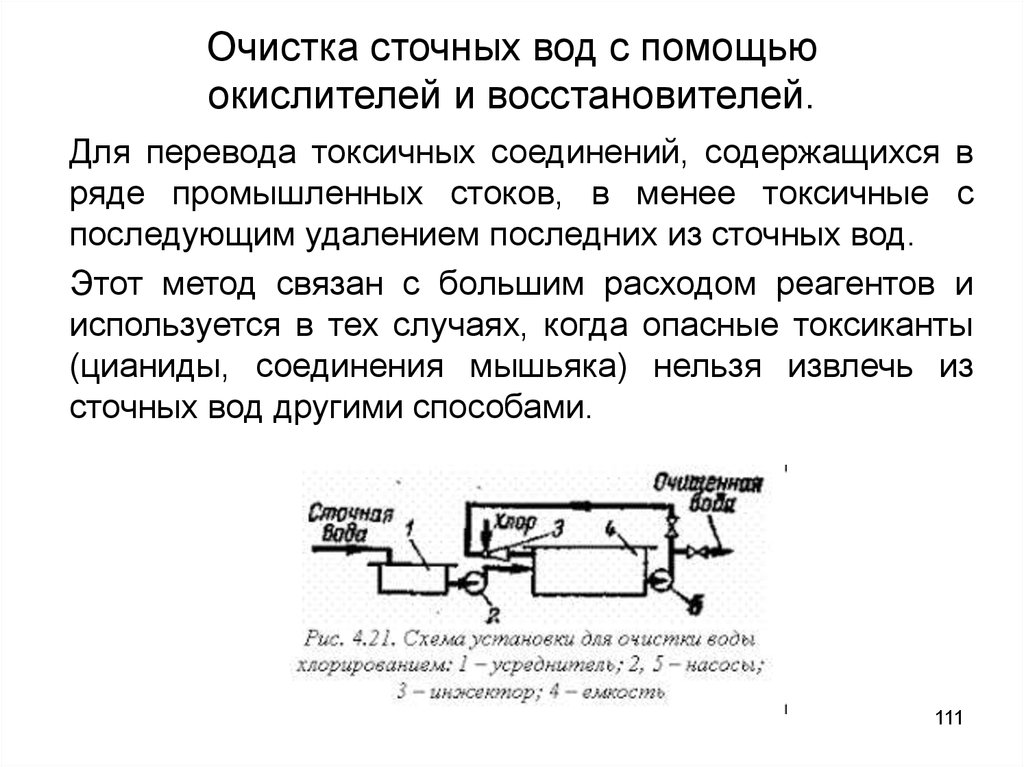
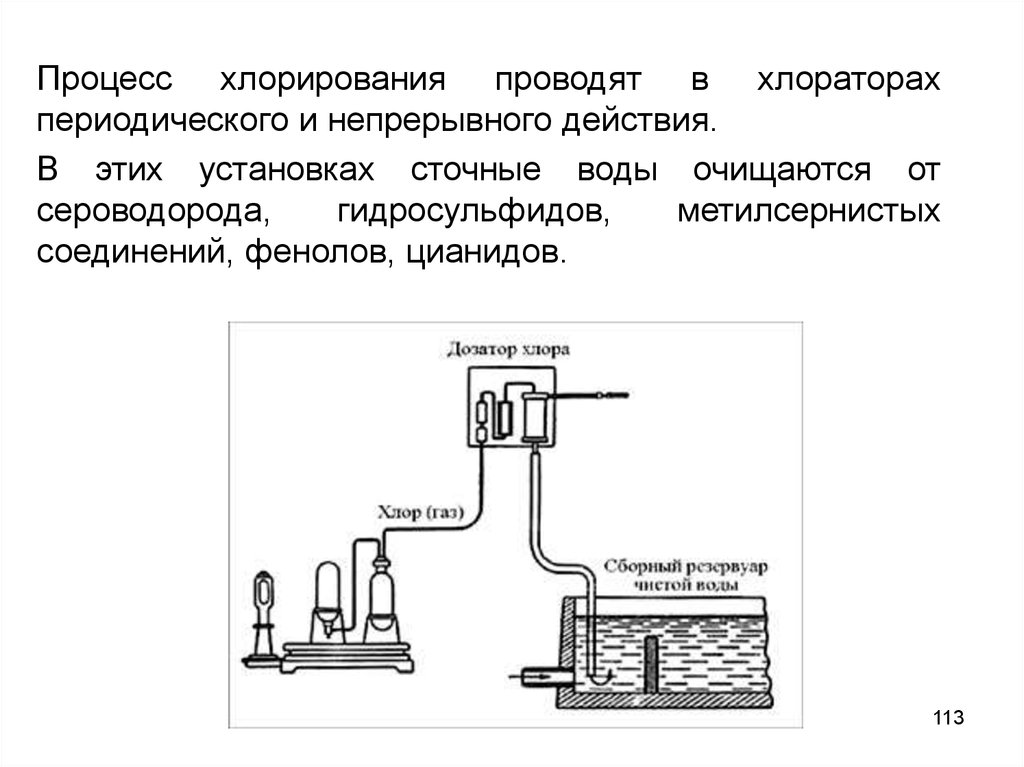









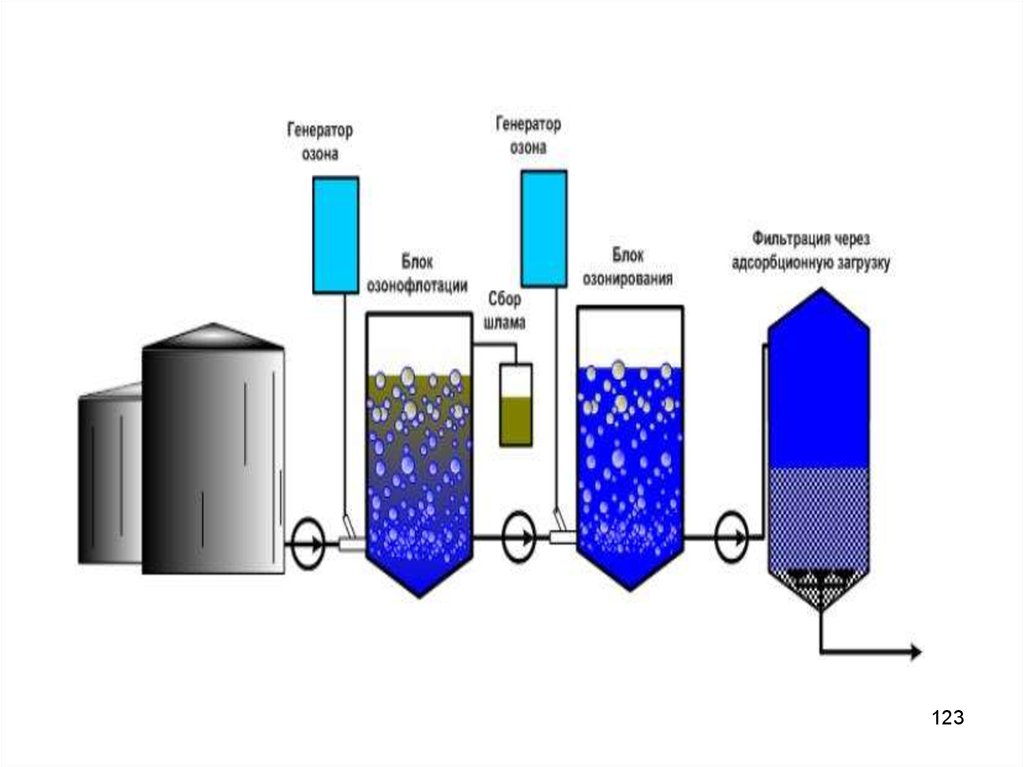





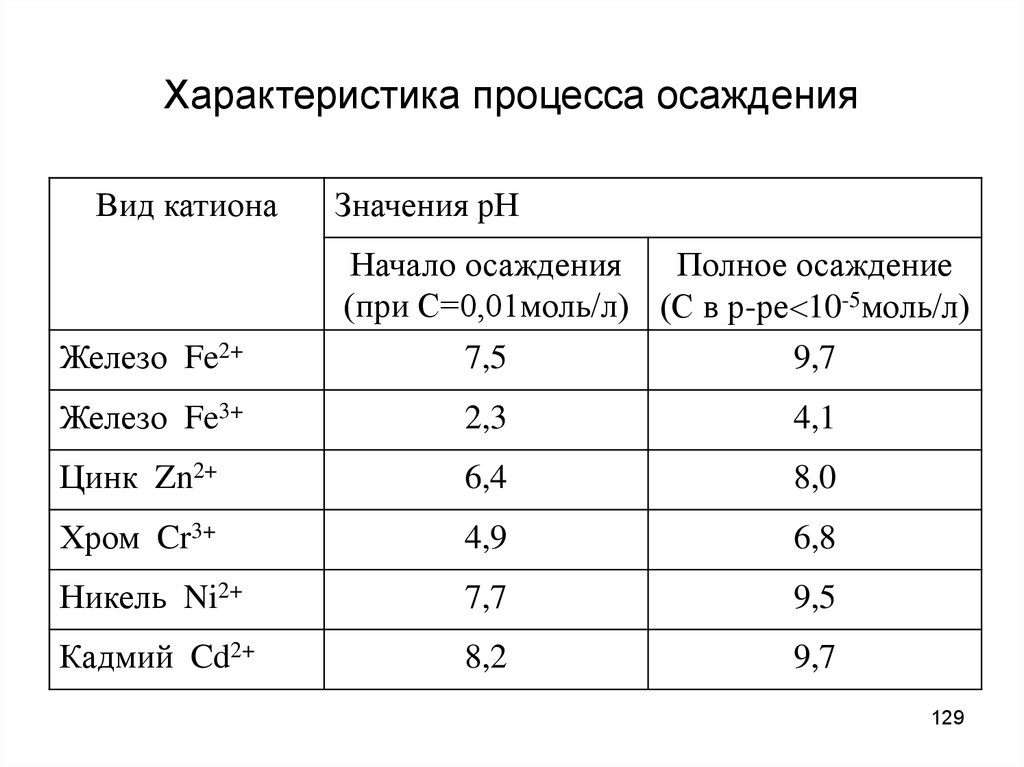











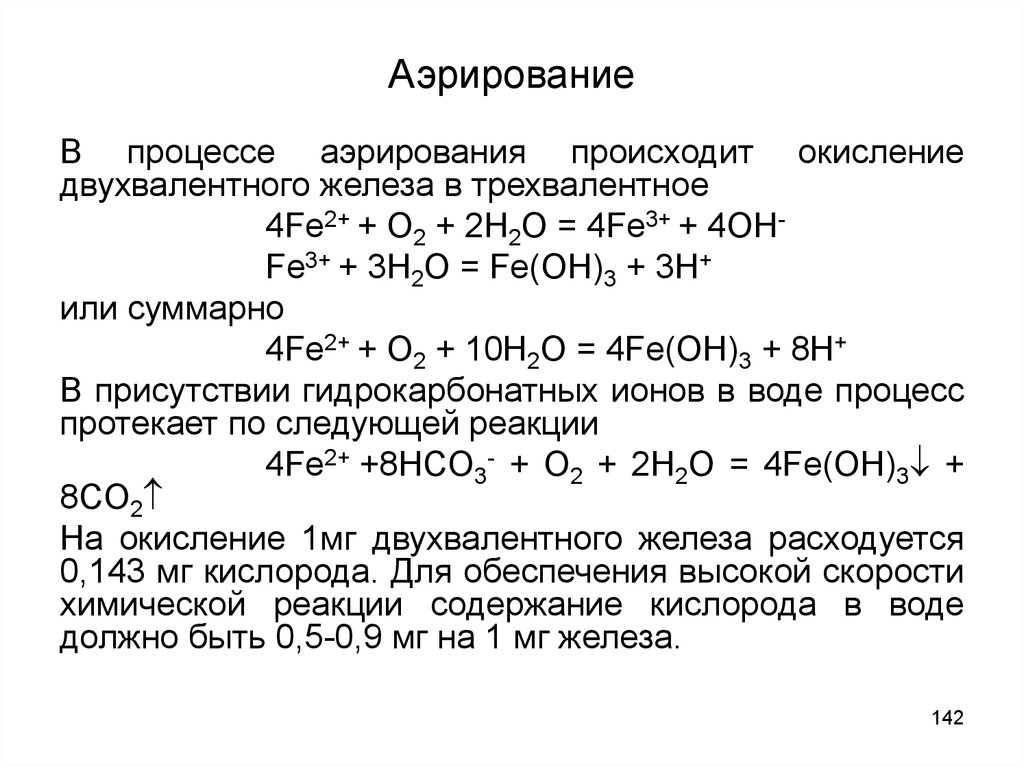






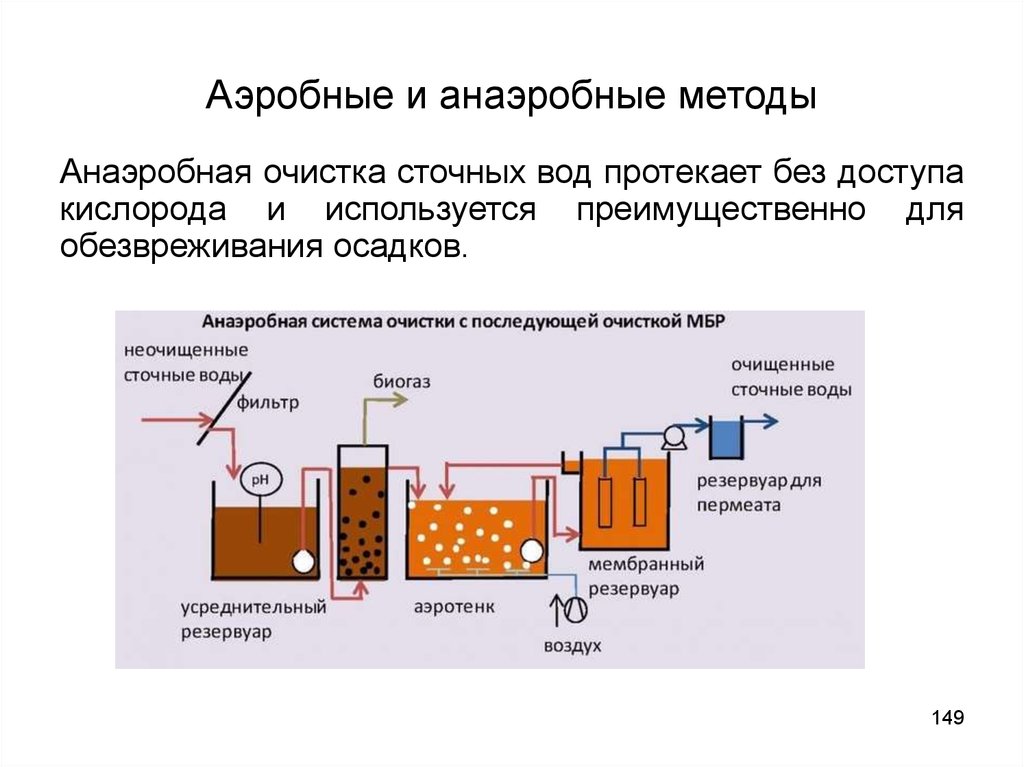
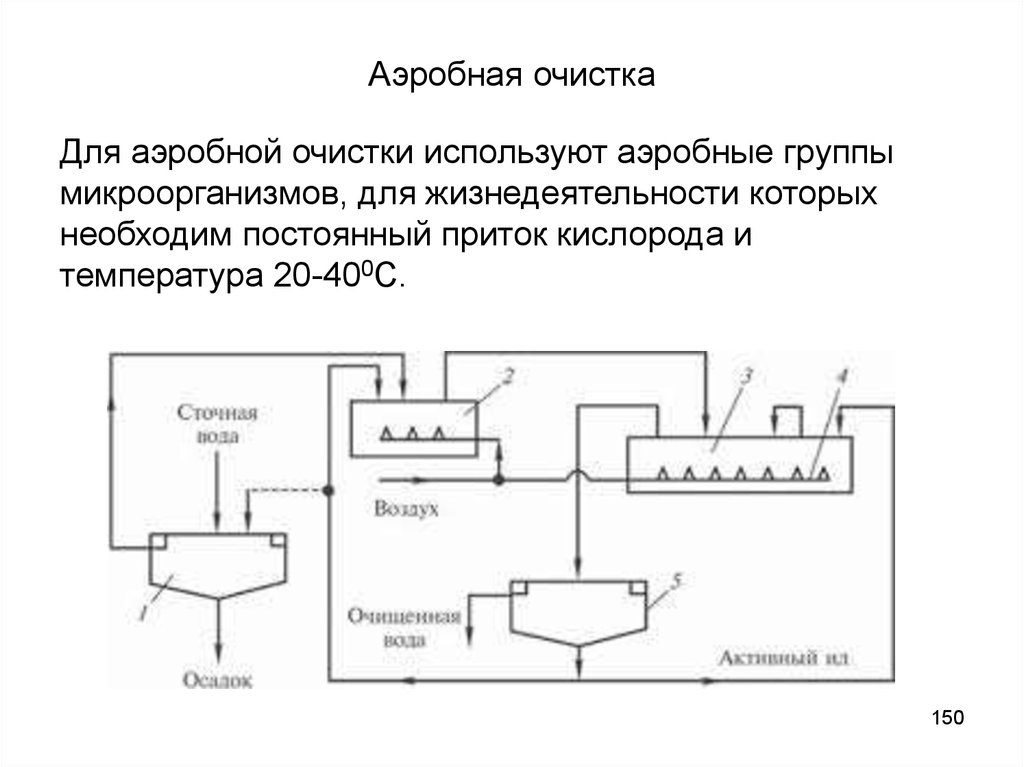
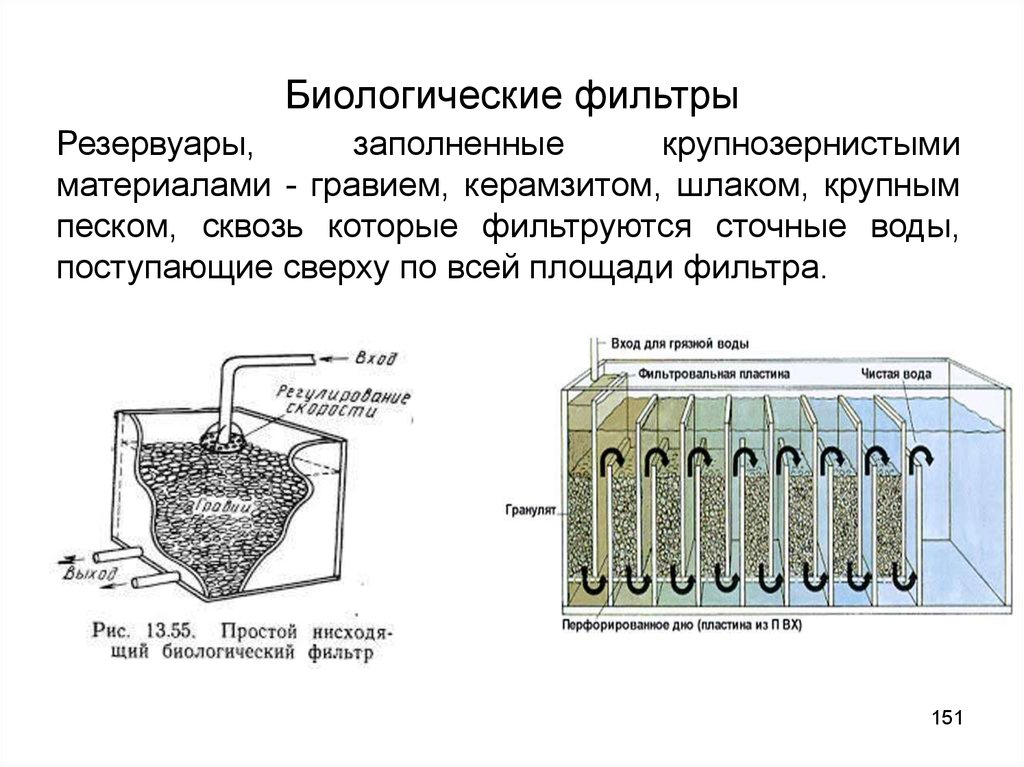

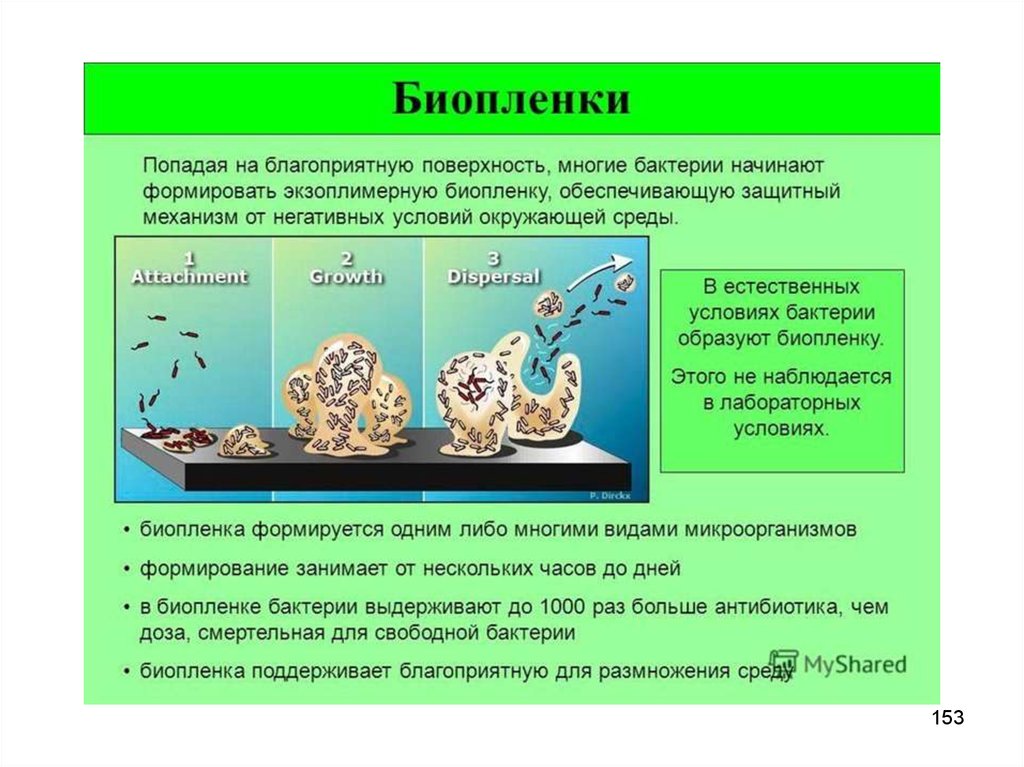
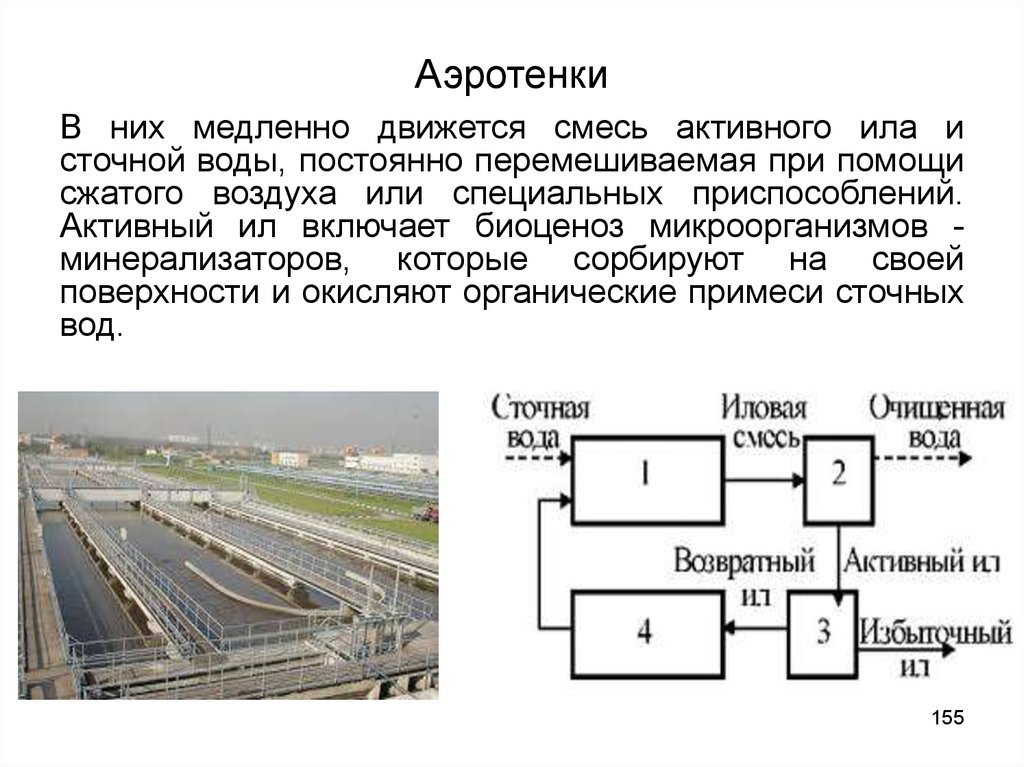
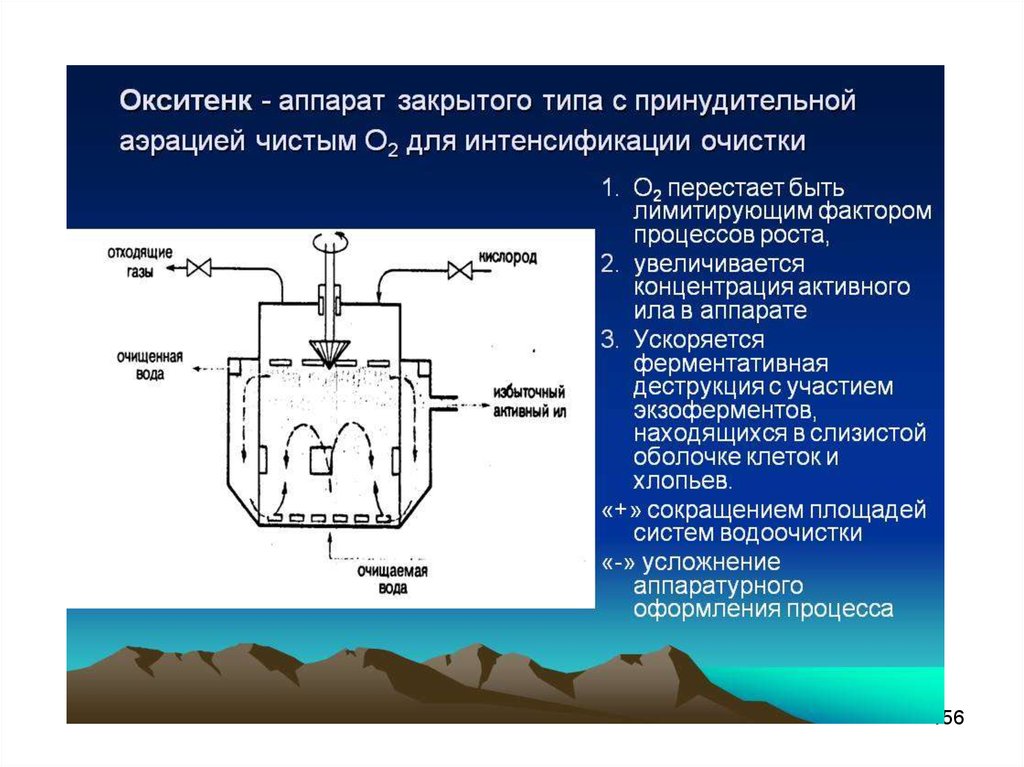








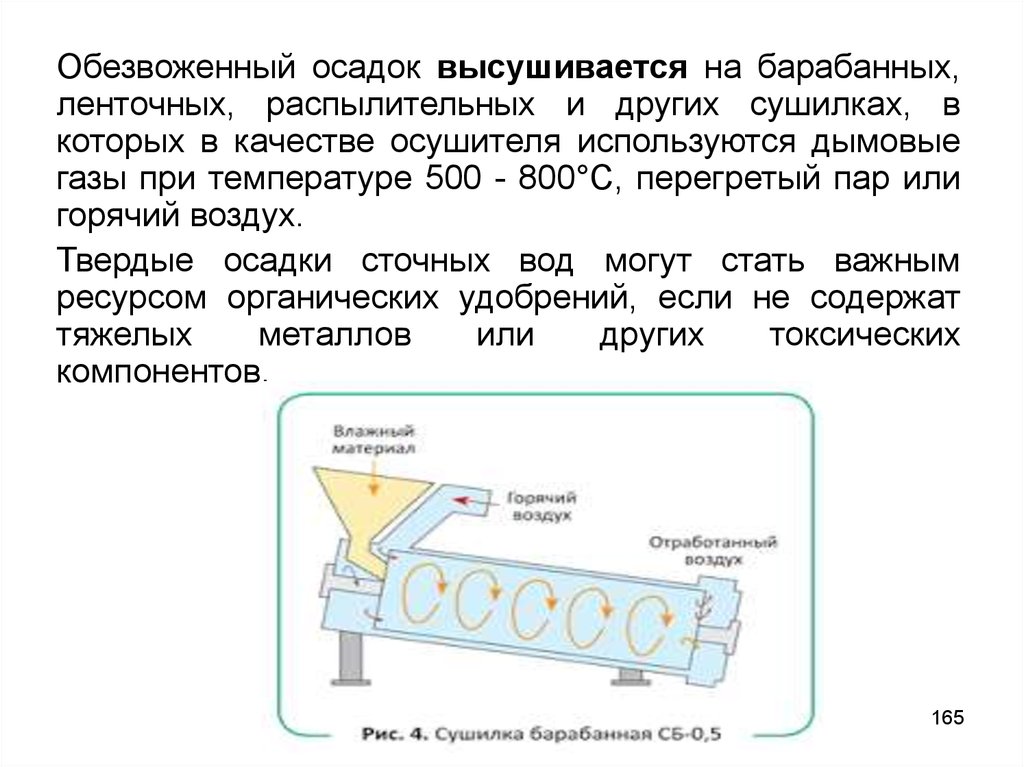
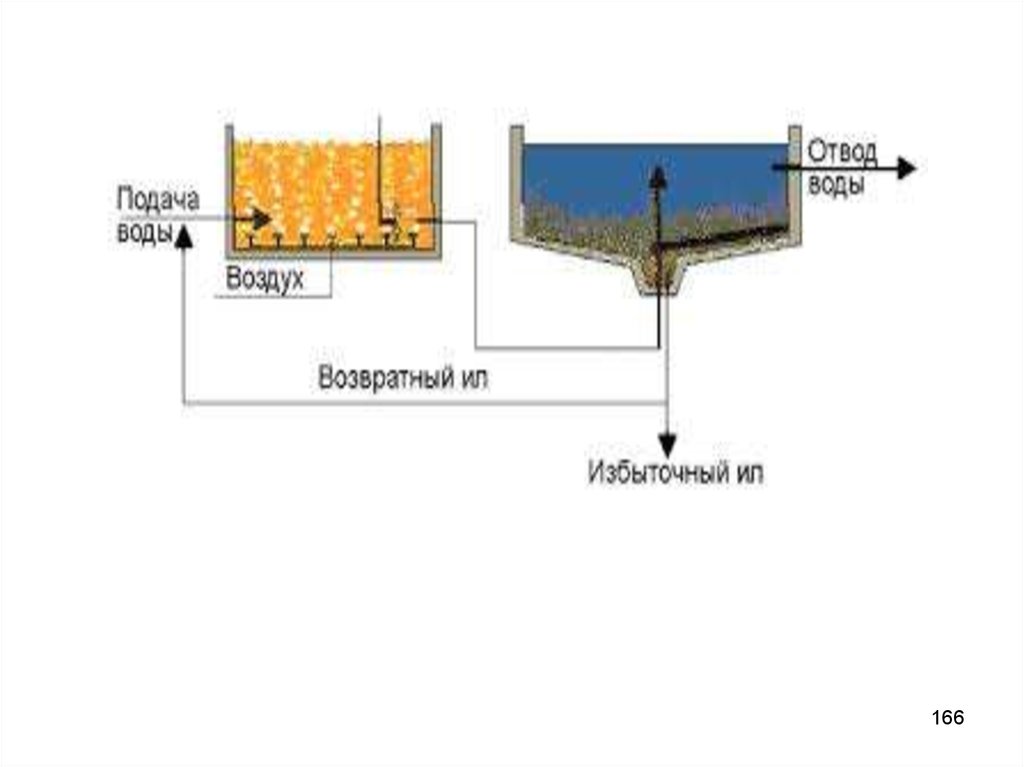
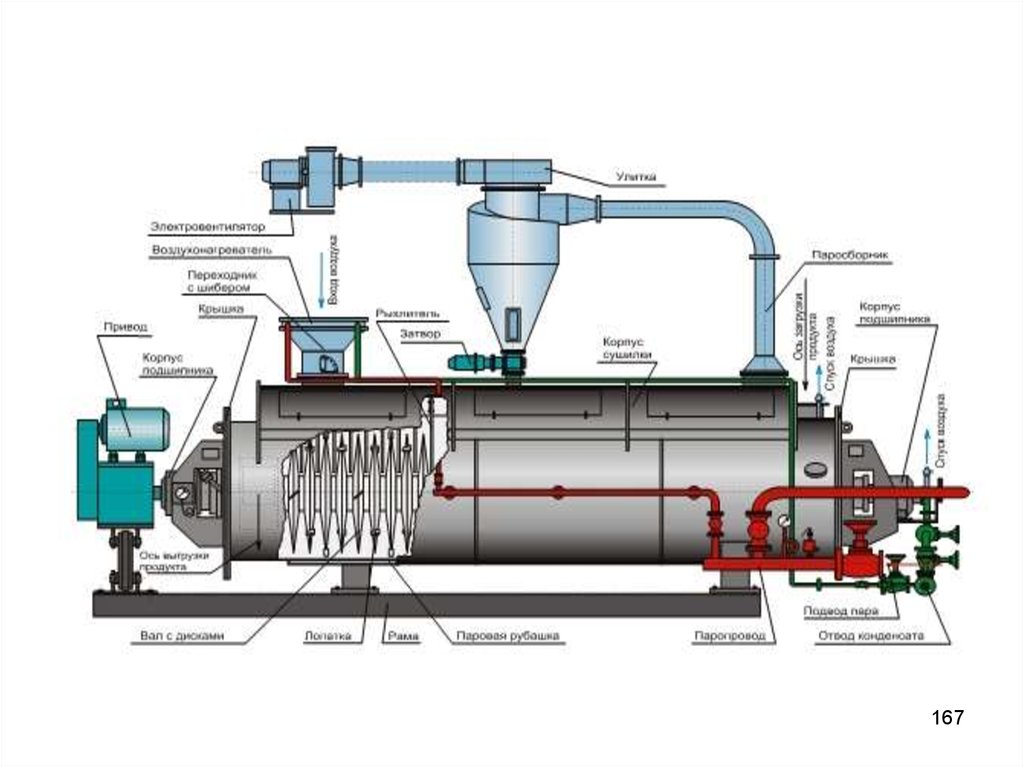

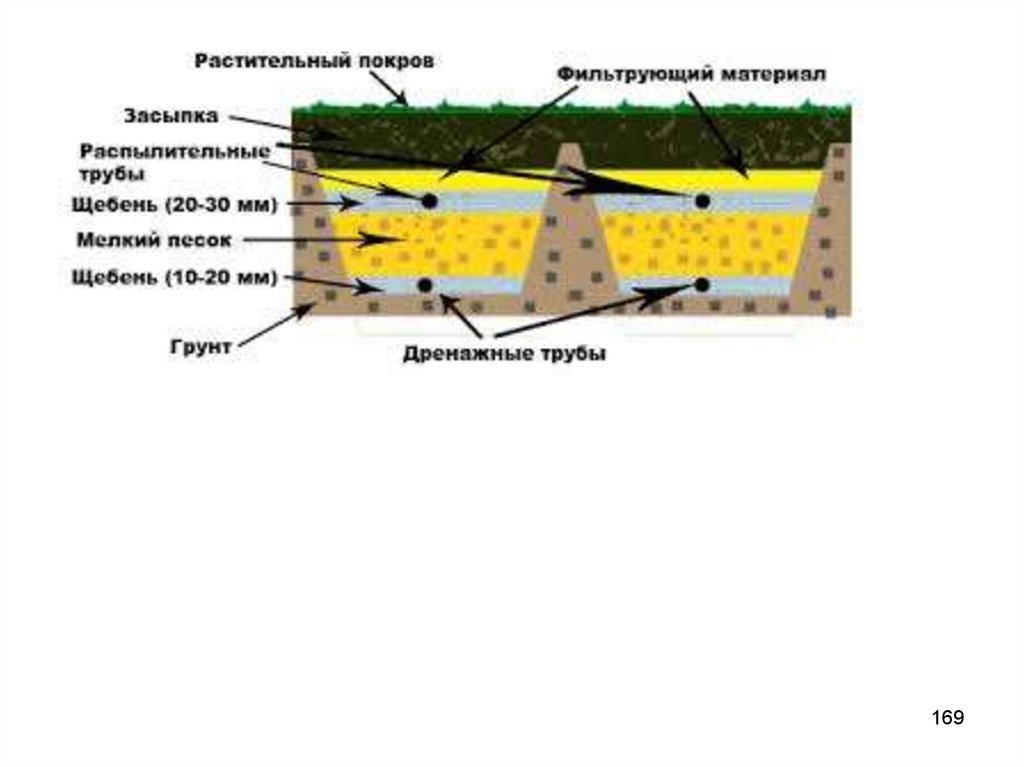










































 ecology
ecology








