Similar presentations:
Методика расчета горения топлива
1. 3.2 Методика расчета горения топлива
2.
Общие положения методики расчета горения топливаРасчет горения топлива включает:
• определение расхода окислителя
(воздуха или дутья, обогащенного
кислородом);
• нахождение количества и состава
газообразных продуктов сгорания,
образующихся в процессе горения;
• расчет теплоты сгорания топлива;
• определение температур горения.
3.
Характеристики окислителя. Коэффициент расхода воздуха21%
О2
30%
О2
40%
О2
50%
О2
75%
О2
79%
N2
70%
N2
60%
N2
50%
N2
25%
N2
k=3,76
k=2,33
k=1,5
k=1,0
k=0,33
100%
О2
k=0,0
Обычный окислитель для
сжигания топлива –
окружающий воздух. Для
улучшения показателей
горения может применяться
обогащенный кислородом
воздух. Обогащение воздуха
кислородом характеризуют
коэффициентом k:
%N2
k=
.
%O2
4.
Характеристики окислителя. Коэффициент расхода воздухаТеоретический расход воздуха L0, м3/кг(м3) необходимый для
сжигания единицы топлива (1 кг для жидкого и твердого и 1м3 для
газообразного) вычисляют из стехиометрических соотношений
реакций горения компонентов.
Реальный (практический) расход воздуха Lα, м3/кг(м3) ,
подаваемый в топливосжигающее устройство, всегда выше для
обеспечения условий полного дожигания всех горючих компонентов.
Коэффициент расхода (избытка) воздуха
Lα
α= .
L0
5.
Расчет процесса горения твердого и жидкого топлива1 моль О2
22,4 м3
1 моль С
12 кг
С+О2=СО2
На окисление 1кг
углерода потребуется
VOC2 =
Выполняют на рабочую массу топлива:
Cp + Hp + Op + Np + Sp + Ap + Wp = 100%.
Для полного окисления всех горючих элементов потребуется чистого
кислорода
м 3О2
р
р
р
р
VO = 0,01(1,867С +5,6 Н +0,7 S - 0,7О ),
кг
2
6.
Расчет процесса горения твердого и жидкого топливаСухого воздуха при α=1 и α>1 потребуется для окисления 1 кг
топлива:
м 3с.в.
м 3с.в.
L0 = (1 + k )VO2 ,
; Lα = αL0 ,
.
кг
кг
Влажного воздуха с содержанием влаги
потребуется для окисления 1 кг топлива:
g вс.вл . ,
г
м3
при α=1 и α>1
3
3
м
в.в.
м
в.в.
в
с.в.
в
в
L0 = (1 + 0,001244 g вл ) L0 ,
; Lα = αL0 ,
.
кг
кг
7.
Расчет процесса горения твердого и жидкого топливаВыход продуктов сгорания при α=1:
CO2
0
V
N2
0
V
Н 2О
0
V
м 3СО2
= 0,01×1,867C ,
;
кг
р
SO2
0
V
м 3 SО2
= 0,01× 0,7 S ,
;
кг
р
м3 N 2
= 0,01× 0,8 N + 0,79 L0 ,
;
кг
р
м 3 Н 2О
= 0,01×11,2 Н + 0,01×1,244W + 0,001244 g ,
.
кг
р
р
Суммируя все компоненты, получим
V0 = V0СО2 + V0SО2 + V0N 2 + V0H 2O .
с.в.
вл
8.
Расчет процесса горения твердого и жидкого топливаВыход продуктов сгорания при α>1:
м СО2
;
кг
3
VαCO2 = 0,01×1,867C р ,
N2
α
V
Н 2О
α
V
N2
0
=V
V
м 3 SО2
= 0,01× 0,7 S ,
;
кг
м3 N 2
+ (α - 1) × 0,79 L0 ,
;
кг
Н 2О
0
=V
SO2
α
р
O2
α
V
м 3О2
= (α - 1)VO2 ,
;
кг
м 3 Н 2О
+ (α - 1) × 0,001244 g L ,
.
кг
с.в.
вл 0
Суммируя все компоненты, получим
Vα = VαСО2 + VαSО2 + VαN 2
3
м
+ VαH 2O + VαО2 , .
кг
9.
Расчет процесса горения твердого и жидкого топливаСостав продуктов сгорания при α=1:
N2
H 2O
V0CO2
V0SO2
V
V
0
0
CO2 =
×100,%; SO2 =
×100,%; H 2O =
×100,%; N 2 =
×100,%.
V0
V0
V0
V0
Состав продуктов сгорания при α>1:
VαSO2
VαCO2
VαH 2O
VαN 2
×100,%; H 2O =
CO2 =
×100,%; SO2 =
×100,%; N 2 =
×100,%;
Vα
Vα
Vα
Vα
V О2
О2
100,%.
V
10.
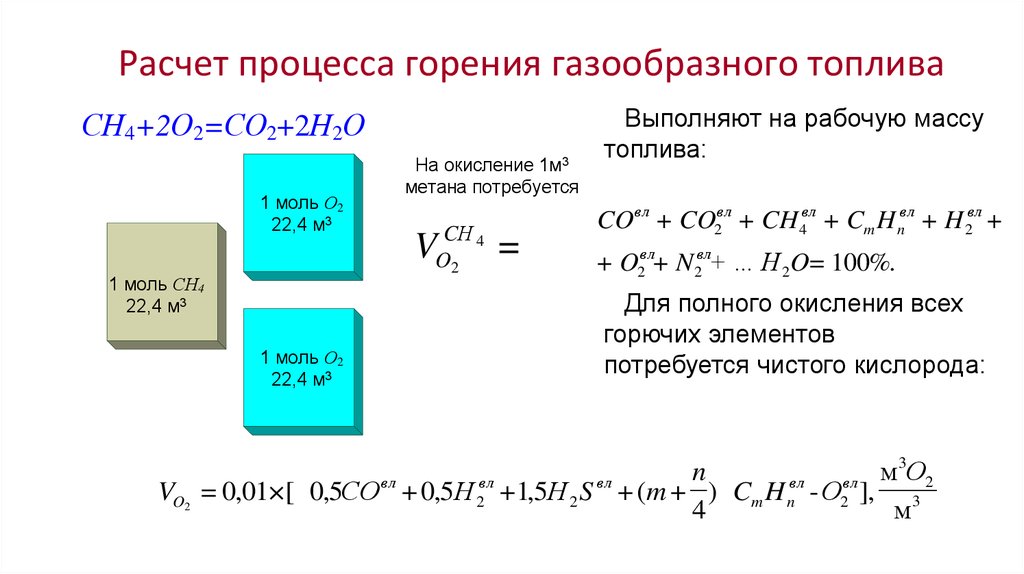
Расчет процесса горения газообразного топливаСН4+2О2=СО2+2Н2О
На окисление 1м3
метана потребуется
1 моль О2
22,4 м3
4
VOCН
=
2
1 моль СН4
22,4 м3
Выполняют на рабочую массу
топлива:
COвл + CO2вл + CH 4вл + Cm H nвл + H 2вл +
+ O2вл+ N 2вл+ … H 2O= 100%.
Для полного окисления всех
горючих элементов
потребуется чистого кислорода:
1 моль О2
22,4 м3
3
n
вл
вл м О2
VO2 = 0,01×[ 0,5СО + 0,5Н + 1,5Н 2 S + (m + ) Cm H n - О2 ], 3
4
м
вл
вл
2
вл
11.
Расчет процесса горения газообразного топливаСухого воздуха при α=1 и α>1 потребуется для окисления 1 м3
топлива:
м 3с.в.
м 3с.в.
L0 (1 k )VO2 ,
; L L0 ,
.
3
3
м
м
Влажного воздуха с содержанием влаги
потребуется для окисления 1 м3 топлива:
g вс.вл . ,
г
м3
при α=1 и α>1
3
3
м
в.в.
м
в.в.
с.в.
в
в
Lв0 (1 0,001244 g вл
) L0 ,
;
L
L
,
.
0
3
3
м
м
12.
Расчет процесса горения газообразного топливаВыход продуктов сгорания при α=1:
3
м3СО2
SO2
вл
вл м SО2
= 0,01× (СО + СО + СН + mCm H ),
; V0 = 0,01× ( SО2 + Н 2 S ),
;
м3
м3
вл
2
CO2
0
V
N2
0
V
вл
4
вл
n
м3 N 2
= 0,01× N + kVО2 , 3 ;
м
Н 2О
0
V
вл
вл
2
n
м 3 Н 2О
вл
с.в.
= 0,01× ( Н 2О + Н + Н 2 S + Сm Н n ) + 0,001244 g вл L0 ,
.
2
м3
вл
вл
2
вл
Суммируя все компоненты, получим
V0 = V0СО2 + V0SО2 + V0N 2 + V0H 2O .
13.
Расчет процесса горения газообразного топливаВыход продуктов сгорания при α>1:
CO2
α
V
3
м3СО2
SO2
вл
вл м SО2
= 0,01× (СО + СО + СН + mCm H ),
; Vα = 0,01× ( SО2 + Н 2 S ),
;
м3
м3
вл
2
VαN 2 = V0N 2
Н 2О
0
V
м3 N 2
+ (α - 1)kVО2 , 3 ;
м
Н 2О
0
=V
вл
вл
4
вл
n
O2
α
V
м 3О2
= (α - 1)VO2 , 3 ;
м
м 3 Н 2О
+ (α - 1) × 0,001244 g L ,
.
м3
с.в.
вл 0
Суммируя все компоненты, получим
V V СО2 V SО2 V N 2 V H 2O V O2 .
14.
Определение температур горения топливаОпределение температур горения производят на основе анализа
теплового баланса процесса горения.
т
т
t
t
Выделяют теоретическую температуру горения 0 (при α=1) и α
(α>1).
Она достижима только при условиях отсутствия теплообмена камеры
горения с окружающей средой при учете физической теплоты, вносимой
подогретым воздухом (Qв) и топливом (Qт). В теоретической температуре
дисс
горения учитывают потери теплотыQвследствие
высокотемпературной
3
диссоциации продуктов сгорания (
):
Qнр + Qв + Qт - Q3дисс
t =
, С;
V0с2
т
0
Qнр + Qв + Qт - Q3дисс
t =
, С.
Vα с2
т
α
15.
Определение температур горения топливаб
б
Выделяют балансовую температуру горения t 0 (при α=1) и t α (α>1).
Она достижима только при условиях отсутствия теплообмена камеры
горения с окружающей средой при учете физической теплоты, вносимой
подогретым воздухом (Qв) и топливом (Qв). В теоретической температуре
горения учитывают потери теплоты вследствие химического и
механического недожога ( Q3 + Q4 ):
Qнр + Qв + Qт - (Q3 + Q4 )
t =
, С;
V0с2
б
0
Qнр + Qв + Qт - (Q3 + Q4 )
t =
, С.
Vα с2
б
α
16.
Определение температур горения топливаИнженерный метод определения теоретической и балансовой
температур горения предполагает определение теплосодержания
продуктов горения, кДж/м3 с учетом физической теплоты, вносимой
подогретым воздухом и топливом и потерь с химическим и механическим
недожогом.
т
дисс
3
i =iх+iв+iт - i
;
i б=iх+iв+iт - (i3 i4 ).
Qнр
Lα(Lвα )св tв
стtт
iх=
;iв=
;iт=
.
Vα
Vα
Vα
17.
Определение температур горения топливаVL = 0
5000
tт
tб
4500
VL =
VL = 20%
Lα - L0
×100,%
Vα
VL = 40%
VL = 0
Теплосодержание i, кДж/м3
VL = 20%
VL = 40%
4000
3500
3000
2500
2000
1200
1400
1600
1800
2000
Температура, °С
2200
2400
















 chemistry
chemistry








