Similar presentations:
Алкены – непредельные углеводороды. Получение, химические свойства и применение
1. АЛКЕНЫ – НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ. ПОЛУЧЕНИЕ, ХИМИЧЕСКИЕ СВОЙСТВА И ПРИМЕНЕНИЕ.
900igr.net2. Учебная цель:
изучить способы получения,химические свойства
и применение алкенов
на примере непредельного
углеводорода - этилена
3. Эпиграф к уроку
«Границнаучному
познанию и
предсказанию
предвидеть
невозможно»
Д.И.Менделеев
4. Лист самоанализа учебной деятельности учащегося ___________ по теме «Получение, химические свойства и применение алкенов»
Я ЗНАЮХОЧУ УЗНАТЬ
ЧТО УЗНАЛ
5. Ответьте, пожалуйста, на следующие вопросы:
1.2.
3.
4.
5.
6.
7.
Какие углеводороды называются алкенами?
Какова общая формула алкенов?
Какова структурная формула первого представителя
гомологического ряда алкенов? Назовите его.
Почему в отличие от алканов алкены в природе
практически не встречаются?
Какие способы получения алкенов вы знаете? Каким
лабораторным способом можно получить алкены?
Какие химические свойства обуславливает наличие
кратной (двойной) связи в молекулах алкенов?
Для чего используют алкены?
6.
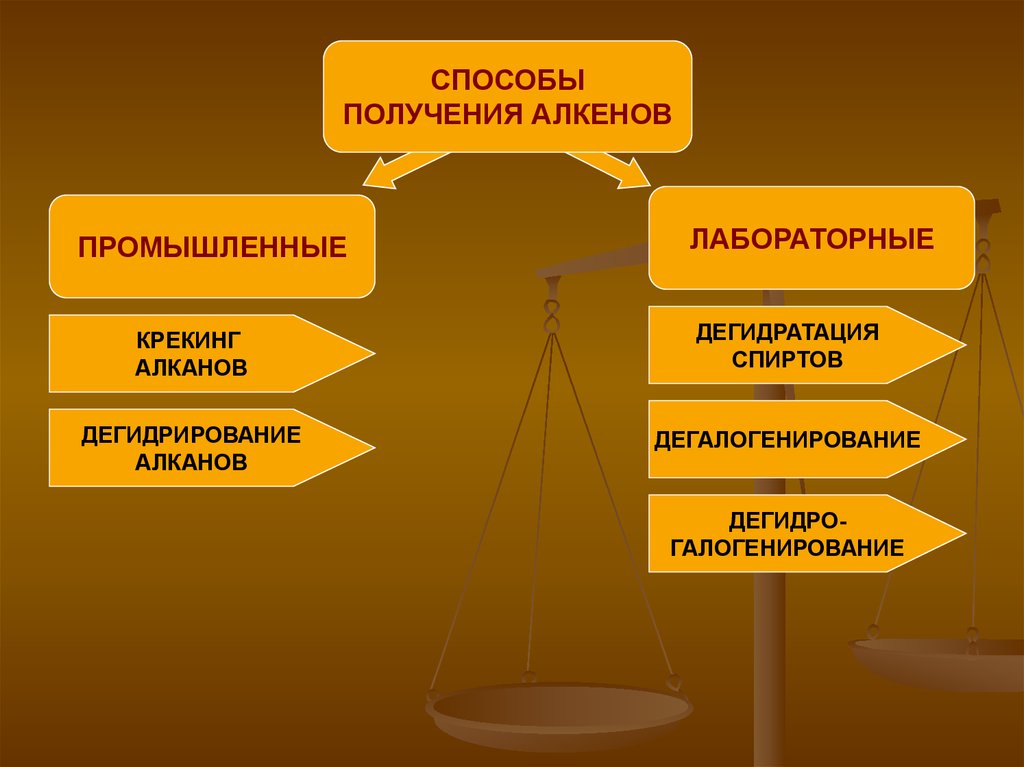
СПОСОБЫПОЛУЧЕНИЯ АЛКЕНОВ
ПРОМЫШЛЕННЫЕ
ЛАБОРАТОРНЫЕ
КРЕКИНГ
АЛКАНОВ
ДЕГИДРАТАЦИЯ
СПИРТОВ
ДЕГИДРИРОВАНИЕ
АЛКАНОВ
ДЕГАЛОГЕНИРОВАНИЕ
ДЕГИДРОГАЛОГЕНИРОВАНИЕ
7. ПРОМЫШЛЕННЫЙ СПОСОБ ПОЛУЧЕНИЯ
КРЕКИНГ АЛКАНОВАЛКАН → АЛКАН + АЛКЕН
С БОЛЕЕ ДЛИННОЙ
УГЛЕРОДНОЙ
ЦЕПЬЮ
С МЕНЕЕ ДЛИНОЙ
УГЛЕРОДНОЙ
ЦЕПЬЮ
ПРИМЕР:
t=400-700C
С10Н22
декан
→
C5H12 + C5H10
пентан пентен
8. ПРОМЫШЛЕННЫЙ СПОСОБ ПОЛУЧЕНИЯ
ДЕГИДРИРОВАНИЕ АЛКАНОВАЛКАН → АЛКЕН + ВОДОРОД
ПРИМЕР:
Ni, t=500C
Н3С - СН3 → Н2С = СН2 + Н2
этан
этен
(этилен)
9. ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ
ДЕГИДРАТАЦИЯ СПИРТОВСПИРТ → АЛКЕН + ВОДА
ПРИМЕР:
t≥140C,
Н Н Н2SO4(конц.)
Н-С – С-Н → Н2С = СН2 + Н2О
Н ОН
этен
(этилен)
10. ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ
ДЕГАЛОГЕНИРОВАНИЕПРИМЕР:
t
Н2С – СН2 + Zn → Н2С = СН2 + ZnBr2
Br Br
этен
1,2-дибромэтан
(этилен)
11. ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ
ДЕГИДРОГАЛОГЕНИРОВАНИЕУДАЛИТЬ ВОДОРОД
ГАЛОГЕН
ДЕЙСТВИЕ
ПРИМЕР:
спиртовой
H H
раствор
Н-С–С-Н+KOH→Н2С=СН2+KCl+H2O
Н Cl
этен
хлорэтан
(этилен)
12. СХЕМЫ РЕАКЦИИ ПРИСОЕДИНЕНИЯ
АЛКЕНН Н
Н-С=С-Н
РЕАГЕНТ
ПРОДУКТ
ВИД РЕАКЦИИ
Применение
реакции, её
продуктов
+ Н2
Н Н
Н-С - С-Н
ГИДРИРОВАНИЕ
(ВОССТАНОВЛЕНИЕ)
НЕ ИМЕЕТ
ПРАКТИЧЕСКОГО
ЗНАЧЕНИЯ
ГАЛОГЕНИРОВАНИЕ
(БРОМИРОВАНИЕ)
РАСПОЗНАВАНИЕ НЕПРЕДЕЛЬНЫХ СОЕДИНЕНИЙ
(ОБЕСЦВЕЧИВАНИЕ
БРОМНОЙ ВОДЫ).
ПОЛУЧЕНИЕ РАСТВОРИТЕЛЯ.
→
?
Н Н
Н-С=С-Н
+ Br2
→
Н Н
Н-С - С-Н
?
Н Н
Н-С=С-Н
+ HCl
→
+ H2 O
→
?
Н Н
Н-С - С-Н
?
Н Н
Н-С=С-Н
?
?
Н Н
Н-С - С-Н
ГИДРОГАЛОГЕНИРОВАНИЕ
(ГИДРОХЛОРИРОВАНИЕ)
ГИДРАТАЦИЯ
ПОЛУЧЕНИЕ ХЛОРЭТАНА,
ИСПОЛЬЗУЕМОГО
ДЛЯ
МЕСТНОЙ АНАСТЕЗИИ, В
КАЧЕСТВЕ
РАСТВОРИТЕЛЯ И В СЕЛЬСКОМ
ХОЗЯЙСТВЕ
ДЛЯ
ОБЕЗЗАРАЖИВАНИЯ
ЗЕРНОХРАНИЛИЩ
ПОЛУЧЕНИЕ ЭТИЛОВОГО
СПИРТА (РАСТВОРИТЕЛЬ
В МЕДИЦИНЕ, В ПРОИЗВОДСТВЕ
СИНТЕТИЧЕСКОГО КАУЧУКА).
13. РЕАКЦИЯ ПОЛИМЕРИЗАЦИИ
Это процесс соединениямолекул в более крупные.
ПРИМЕР:
n CH2=CH2
этилен
(мономер)
одинаковых
(-CH2-CH2-)n
полиэтилен
(полимер)
n – степень полимеризации, показывает
число молекул, вступивших в реакцию
-CH2-CH2- структурное звено
14. РЕАКЦИИ ОКИСЛЕНИЯ
ГОРЕНИЕ АЛКЕНОВПРИМЕР:
2С2Н6 + 7О2
4СО2 + 6Н2О
15. РЕАКЦИИ ОКИСЛЕНИЯ
МЯГКОЕ ОКИСЛЕНИЕ –ВЗАИМОДЕЙСТВИЕ С РАСТВОРОМ
ПЕРМАНАГАНАТА КАЛИЯ
(реакция Е.Е.Вагнера)
Н2С=СН2 + [O] + H2O
H2C - CH2
OH OH
этиленгликоль
(этандиол-1,2)
!
Качественная реакция на непредельность
углеводорода – на кратную связь.
16. Применение этилена
Свойство1. Полимеризация
2. Галогенирование
3. Гидрогалогенирование
Применение
Производство
полиэтилена, пластмасс
Получение
растворителей
Для местная анестезия,
получения растворителей, в с/х для
обеззараживания
зернохранилищ
Пример
17.
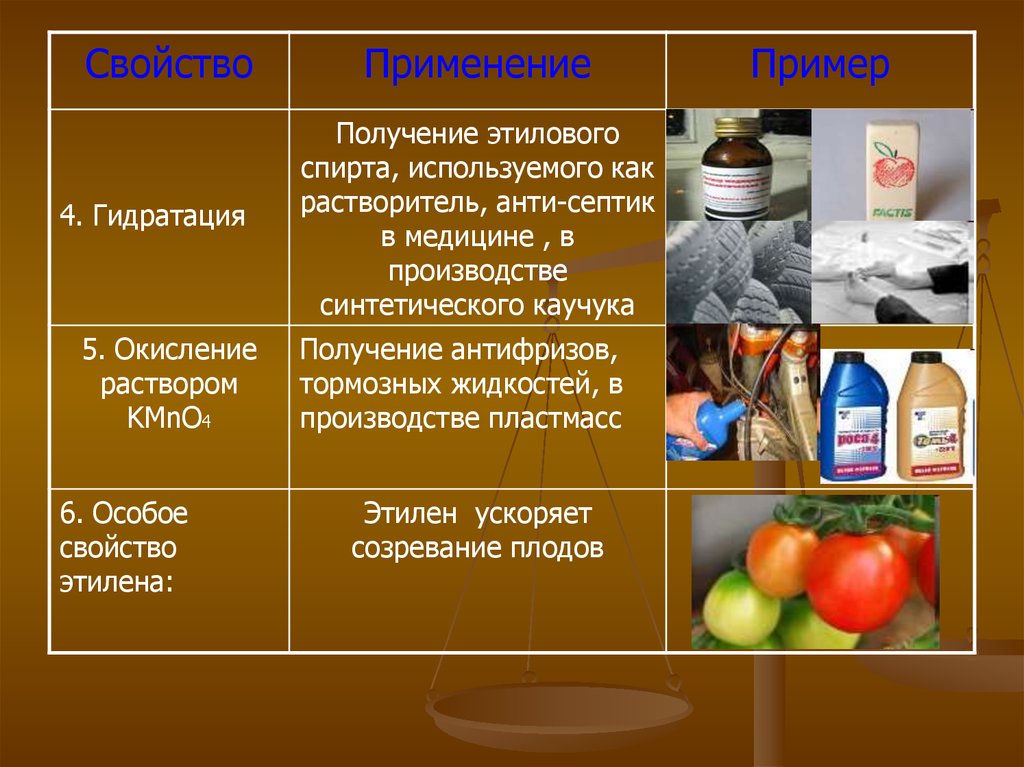
Свойство4. Гидратация
5. Окисление
раствором
KMnO4
6. Особое
свойство
этилена:
Применение
Получение этилового
спирта, используемого как
растворитель, анти-септик
в медицине , в
производстве
синтетического каучука
Получение антифризов,
тормозных жидкостей, в
производстве пластмасс
Этилен ускоряет
созревание плодов
Пример
18. СИНКВЕЙН
1 строка – имя существительное (тема синквейна)2 строка – два прилагательных
(раскрывающие тему синквейна)
3 строка – три глагола
(описывают действия)
4 строка – фраза или предложение
(высказывают своё отношение к теме)
5 строка – синоним (слово-резюме)
19.
1.2.
3.
4.
5.
Этилен
Ненасыщенный, активный
Горит, обесцвечивает, присоединяет
Этилен – представитель непредельных
углеводородов
Алкен
20. ДОМАШНЕЕ ЗАДАНИЕ
Оценка «3»: параграф 4, ТПО стр. 24-25, № 5-7Оценка «4»: Хомченко И.Г.: 20.21
Оценка «5»: Составить цепочку превращений,
используя материал по темам
«Алканы» и «Алкены»
21.
СПАСИБОЗА РАБОТУ!



















 chemistry
chemistry








