Similar presentations:
Общий путь катаболизма
1. Общий путь катаболизма
2.
Углеводы, белки и жиры — основные компоненты пищичеловека, являются многокомпонентными веществами и, прежде
чем включиться в метаболизм, подвергаются гидролизу
в желудочно-кишечном тракте. Продукты гидролиза, способные
всасываться из кишечника в кровь, затем в ходе катаболизма в
клетке полностью окисляются, освобождая энергию, используемую
для синтеза АТФ.
Одной из основных характеристик процесса катаболизма
является соединение метаболических путей в единый процесс, то
есть образование в ходе катаболизма общих метаболитов,
окисление которых до конечных продуктов осуществляется с
использованием одних и тех же реакций, составляющих общий
этап катаболизма. Таким образом, конечным этапом окисления
практически всех веществ в организме, имеющих исходно разное
строение, являются реакции общего пути катаболизма, изучение
которого позволяет понять основные принципы организации
процесса метаболизма в организме человека, в ходе которого
субстраты полностью окисляются до СО2 и Н2О.
3. Основные этапы общего пути катаболизма
В процессе катаболизма можно выделить триосновные его части (рис. 1):
1.Расщепление в пищеварительном тракте. Это
гидролитические реакции, превращающие сложные
пищевые вещества в относительно небольшое число
простых метаболитов: глюкозу, аминокислоты, глицерол,
жирные кислоты.
2.Специфические пути катаболизма. На этом этапе
простые метаболиты подвергаются специфическим
реакциям расщепления, в результате которых образуется
либо пировиноградная кислота, либоацетил-КоА. АцетилКоА может образоваться из пирувата, а также из жирных
кислот и аминокислот. В специфических путях катаболизма
могут образоваться соединения, которые непосредственно
включаются в цитратный цикл.
4.
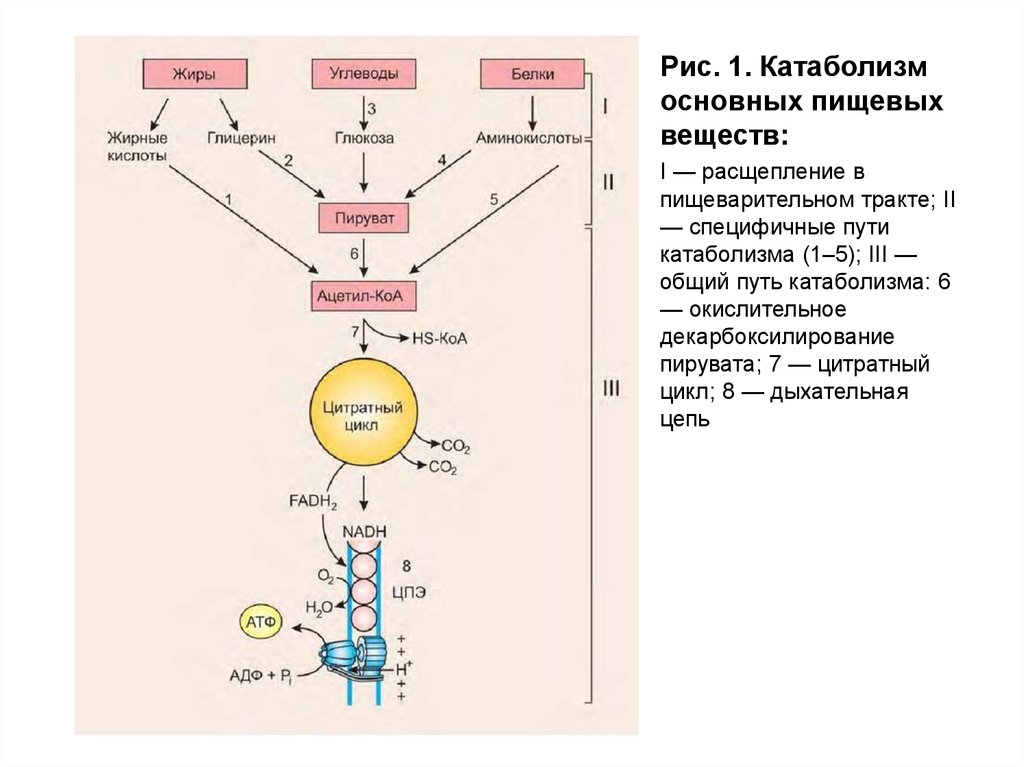
Рис. 1. Катаболизмосновных пищевых
веществ:
I — расщепление в
пищеварительном тракте; II
— специфичные пути
катаболизма (1–5); III —
общий путь катаболизма: 6
— окислительное
декарбоксилирование
пирувата; 7 — цитратный
цикл; 8 — дыхательная
цепь
5. Основные этапы общего пути катаболизма
3. Окислительное декарбоксилированиепирувата, цитратный цикл и дыхательная
цепь завершают расщепление пищевых веществ до
конечных продуктов — СО и Н2О.
Следовательно, начиная со стадии образования
пирувата, происходит унификация путей катаболизма.
Из большого числа исходных соединений образуется
всего два — пируват и ацетил-КоА. Процесс,
начинающийся с окисления пирувата, называется
общим путем катаболизма. Именно в общем пути
катаболизма образуется основное количество
субстратов для реакций дегидрирования. Совместно с
дыхательной цепью и окислительным
фосфорилированием общий путь катаболизма является
основным источником энергии в форме АТФ.
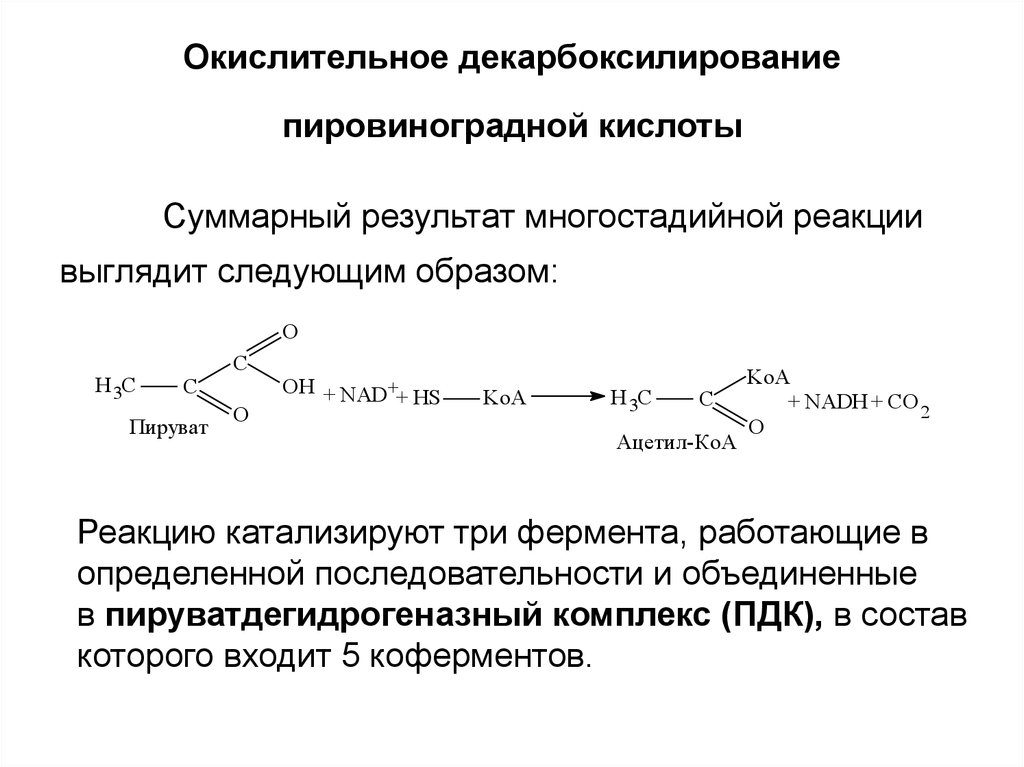
6. Окислительное декарбоксилирование пировиноградной кислоты
Суммарный результат многостадийной реакциивыглядит следующим образом:
O
H 3C
C
Пируват
C
O
OH + NAD++ HS
KoA
H 3C
C
Ацетил-КоА
KoA
+ NADH + CO 2
O
Реакцию катализируют три фермента, работающие в
определенной последовательности и объединенные
в пируватдегидрогеназный комплекс (ПДК), в состав
которого входит 5 коферментов.
7. Окислительное декарбоксилирование пировиноградной кислоты
Этот комплекс ферментов работаетподобно конвейеру, в котором промежуточные
продукты передаются от фермента к ферменту.
Такой принцип повышает эффективность
работы ферментов, так как снижает
случайность в контакте реагирующих веществ.
В табл. 1 и на рис. 2 приводятся названия
ферментов (ПДК) и характеристика
катализируемых реакций.
8. Окислительное декарбоксилирование пировиноградной кислоты
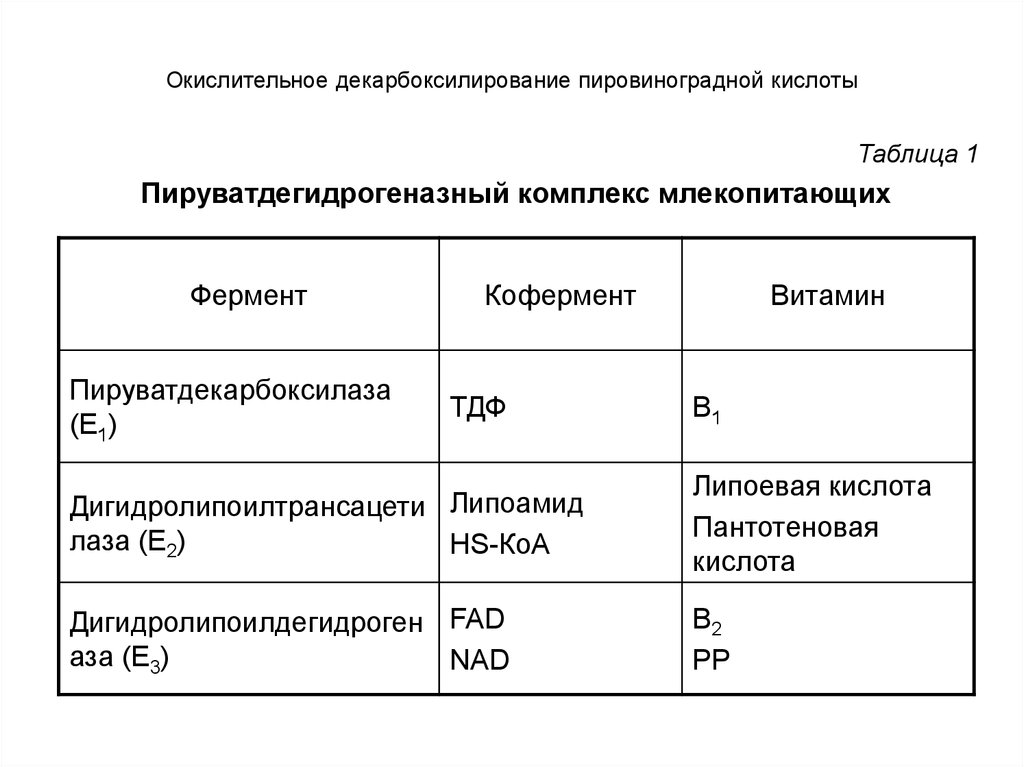
Таблица 1Пируватдегидрогеназный комплекс млекопитающих
Фермент
Пируватдекарбоксилаза
(Е1)
Кофермент
ТДФ
Витамин
В1
Дигидролипоилтрансацети Липоамид
лаза (Е2)
HS-КоА
Липоевая кислота
Пантотеновая
кислота
Дигидролипоилдегидроген FAD
аза (Е3)
NAD
В2
РР
9. Окислительное декарбоксилирование пировиноградной кислоты
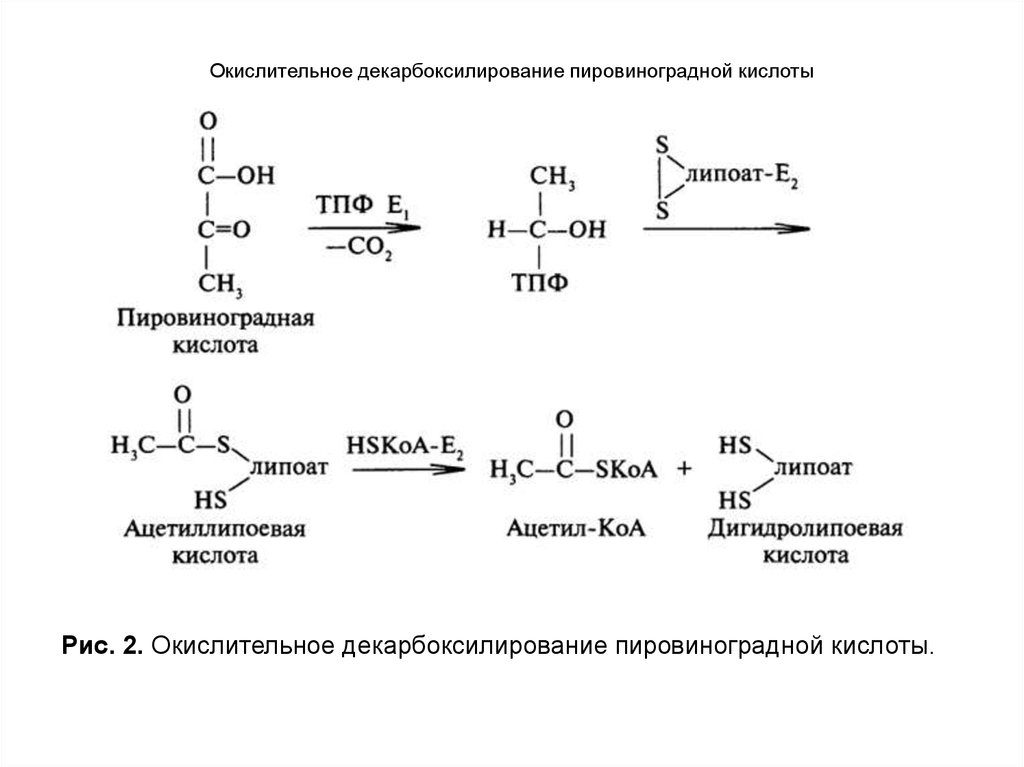
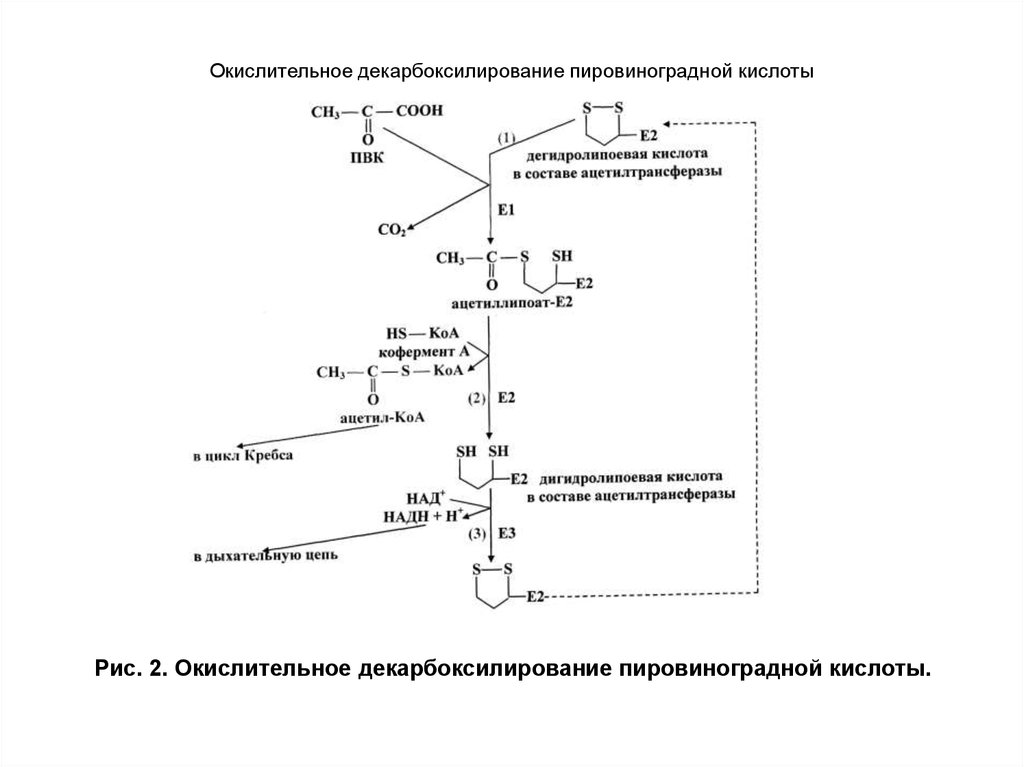
Рис. 2. Окислительное декарбоксилирование пировиноградной кислоты.10. Окислительное декарбоксилирование пировиноградной кислоты
Рис. 2. Окислительное декарбоксилирование пировиноградной кислоты.11. Окислительное декарбоксилирование пировиноградной кислоты
Пируватдекарбоксилаза (Е1). В качествекофермента в реакции участвует
тиаминдифосфат (ТДФ) — производное
витамина В1. Фермент катализирует
отщепление карбоксильной группы в виде
СО2 и присоединение ацетильного остатка к
коферменту ТДФ.
Дигидролипоилтрансацетилаза (Е2) —
второй фермент комплекса. Катализирует
окисление гидроксиэтильной группы и перенос
ацетильной группы на липоевую кислоту, а
затем на HS-КоАс образованием ацетил-КоА.
12. Окислительное декарбоксилирование пировиноградной кислоты
Таким образом, в этой реакции участвуют двакофермента: липоевая кислота, прочно соединенная
с ферментом, икофермент А, объединяющийся с
ферментом в момент реакции. Водород остается
связанным с липоевой кислотой, которая превращается
в дигидролипоат.
Дигидролипоилдегидрогеназа (Е3) — FAD,
содержащий флавопротеин, катализирует
дегидрирование восстановленной формы липоевой
кислоты и перенос водорода на FAD (прочно связанный
с ферментом), а затем на свой второй кофермент
NAD+, который включается в состав комплекса только
во время реакции.
13. Окислительное декарбоксилирование пировиноградной кислоты
Е1 — пируватдекарбоксилаза катализируетдекарбоксилирование пирувата и перенос С2фрагментана ТДФ. Е2-трансацетилаза катализирует
окисление гидроксиэтильной группы и перенос С2фрагментана липоевую кислоту; ацетилированная
трансацетилаза взаимодействует с HSKoA с
образованием восстановленной формы липоевой
кислоты и ацетил-КоА; Е3 —
дигидролипоилдегидрогеназа — FAD-содержащий
фермент окисляет дигидролипоат с образованием
FADH2 в составе фермента, который затем
регенерируется при участии NAD+. Липоевая кислота,
связанная в молекуле фермента Е2 с остатками лизина,
функционирует как «поворотный кронштейн»,
переносящий атомы водорода и ацетильные группы от
одного фермента к другому.
14. Окислительное декарбоксилирование пировиноградной кислоты
Главные продукты реакций ПДК — этоNADH + H+ иацетил-КоА. NADH + H+ далее
окисляется в дыхательной цепи, где энергия
используется на синтез 3 моль АТФ, а ацетилКоА окисляется в цитратном цикле.
Пируватдекарбоксилазный комплекс находится
на внутренней мембране митохондрий и
соединен с ней со стороны матрикса.
На рис. 3, 4, 5 представлено строение
коферментов ПДК.
15. Окислительное декарбоксилирование пировиноградной кислоты
Рис. 3. Строение тиаминдифосфата16. Окислительное декарбоксилирование пировиноградной кислоты
SNH
S
NH
CH2
CH2
CH2
CH2
CH2
Дегидролипоевая кислота
C
O
( CH2 )4
CH
C
O
Лизин
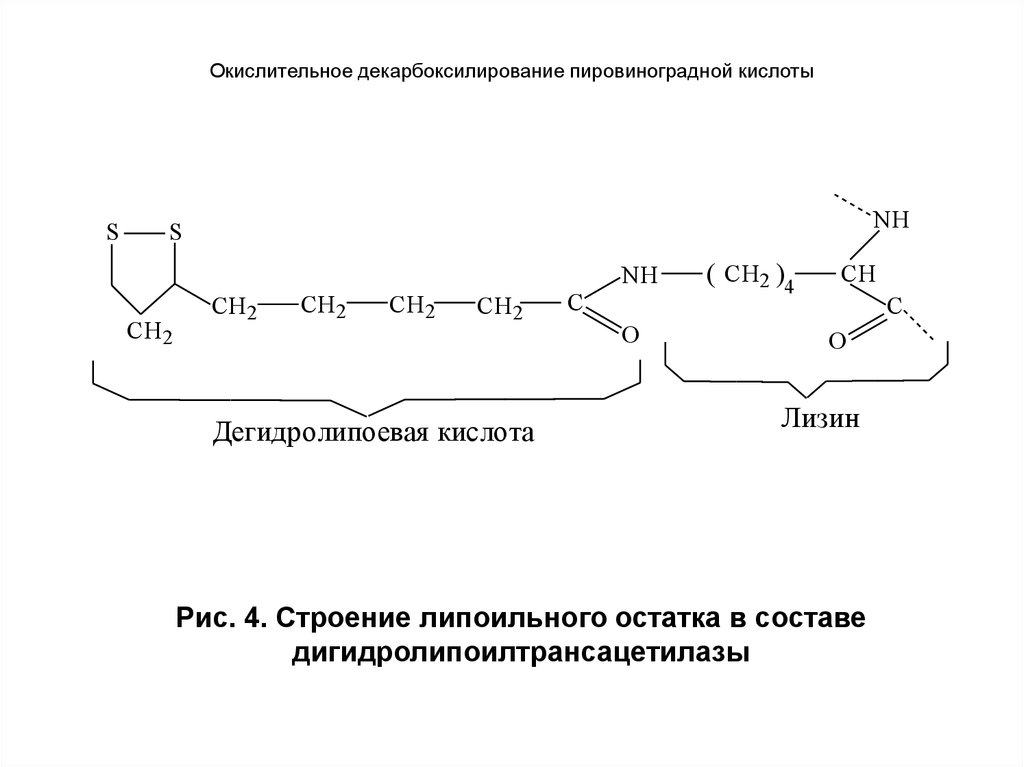
Рис. 4. Строение липоильного остатка в составе
дигидролипоилтрансацетилазы
17. Окислительное декарбоксилирование пировиноградной кислоты
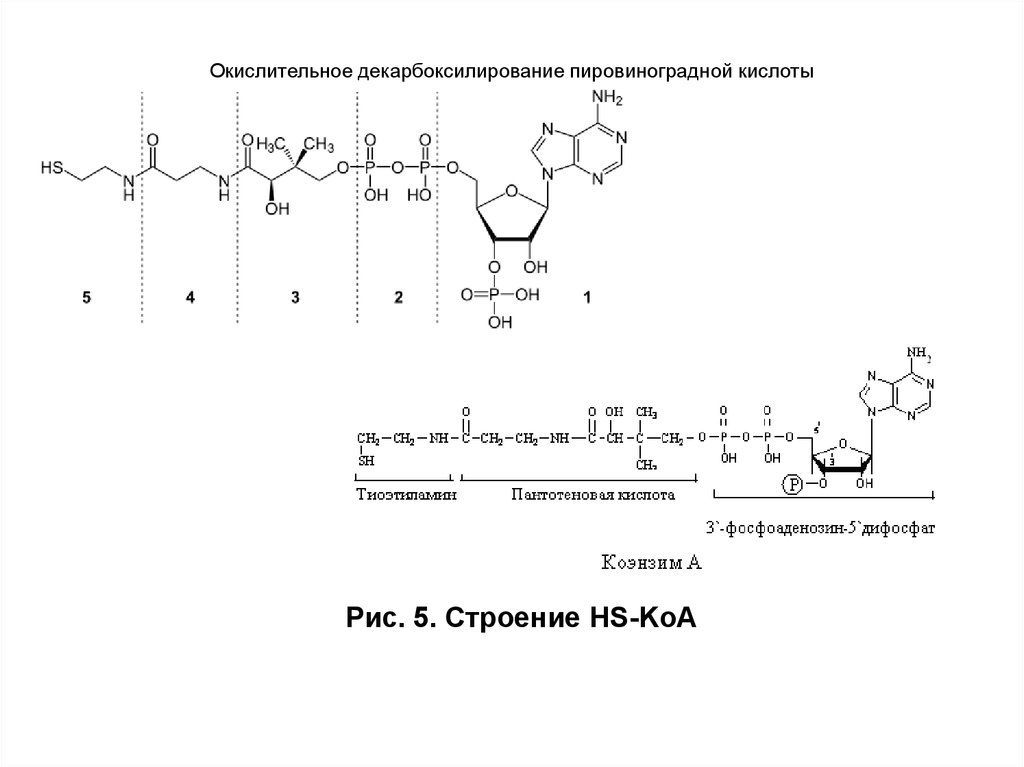
Рис. 5. Строение HS-KoA18. Цитратный цикл
Цитратный цикл (цикл Кребса, цикл трикарбоновых кислот)— это система реакций, приводящая к полному окислению
двухуглеродного ацетильного остатка, который мог образоваться в
различных метаболических путях. Цитратный цикл является общим
конечным путем окисления белков, жиров и углеводов. Все
реакции цитратного цикла, как и окислительного
декарбоксилирования пирувата, локализованы в митохондриях. В
ходе одного полного цикла происходит:
• полное окисление ацетильного остатка до двух молекул СО2;
• образование трех молекул восстановленного NADH + H+ и
одной молекулы FADH2;
• синтез одной молекулы ГТФ в результате субстратного
фосфорилирования.
Реакции цитратного цикла, ферменты и их характеристика
приведены на рис. 6.
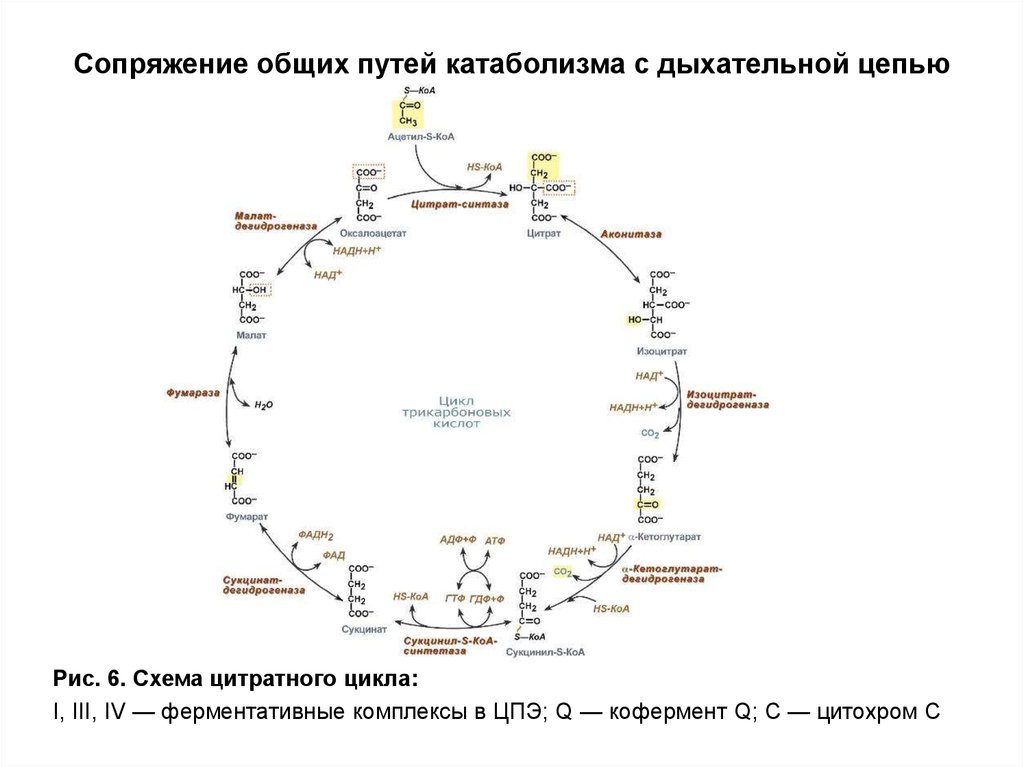
19. Сопряжение общих путей катаболизма с дыхательной цепью
В общих путях катаболизма происходит пятьреакций дегидрирования: одна на стадии
окислительного декарбоксилирования пирувата и
четыре в цитратном цикле. Все 10 атомов водорода
переносятся на коферменты дегидрогеназ, которые, в
свою очередь, окисляются в дыхательной цепи.
Окисленные коферменты возвращаются в реакции
общих путей катаболизма. Регенерация коферментов
— это обязательное условие для протекания
реакции дегидрирования. Таким образом, общий путь
катаболизма и дыхательная цепь неразрывно связаны
между собой и отдельно функционировать не могут.
20. Сопряжение общих путей катаболизма с дыхательной цепью
Рис. 6. Схема цитратного цикла:I, III, IV — ферментативные комплексы в ЦПЭ; Q — кофермент Q; C — цитохром С
21. Значение общих путей катаболизма в энергетическом обмене
За один оборот цитратного цикла синтезируется 12молекул АТФ (рис. 7.6). Девять из них образуются за счет
энергии транспорта электронов в дыхательной цепи от трех
молекул NADH + H+. Две молекулы АТФ синтезируются при
окислении 1 молекулы FADH2, так как в дыхательной цепи в
данном случае действуют только два пункта сопряжения
ЦПЭ с окислительным фосфорилированием AДФ. Кроме
того, в цитратном цикле происходит одна реакция
субстратного фосфорилирования (реакция 5), дающая 1
моль ГТФ (АТФ). В общих путях катаболизма
синтезируется 15 молекул АТФ. Три из них при
окислительном декарбоксилировании пирувата и 12 — в
цитратном цикле.
22. Регуляция общих путей катаболизма
Главным фактором, регулирующим скорость дыхания ифосфорилирования, является потребность организма в
энергии. Синтез АТФ осуществляется в ЦПЭ, но основная масса
восстановленных эквивалентов для дыхательной цепи поступает
из общих путей катаболизма. Следовательно, регуляция общих
путей катаболизма и дыхательной цепи тесно связана.
Для оценки энергетического состояния клетки используют
величину энергетического заряда, отражающего соотношение
концентрации ATФ к продуктам ее распада — AДФ и AMФ.
При увеличении энергетического заряда в клетке (в
состоянии покоя) скорость реакций общих путей катаболизма
снижается, а при уменьшении энергетического заряда —
увеличивается. Это достигается за счет того, что ATФ действует
как аллостерический ингибитор, а AДФ и AMФ – как
аллостерические активаторы некоторых ферментов ОПК (рис.
7).
23.
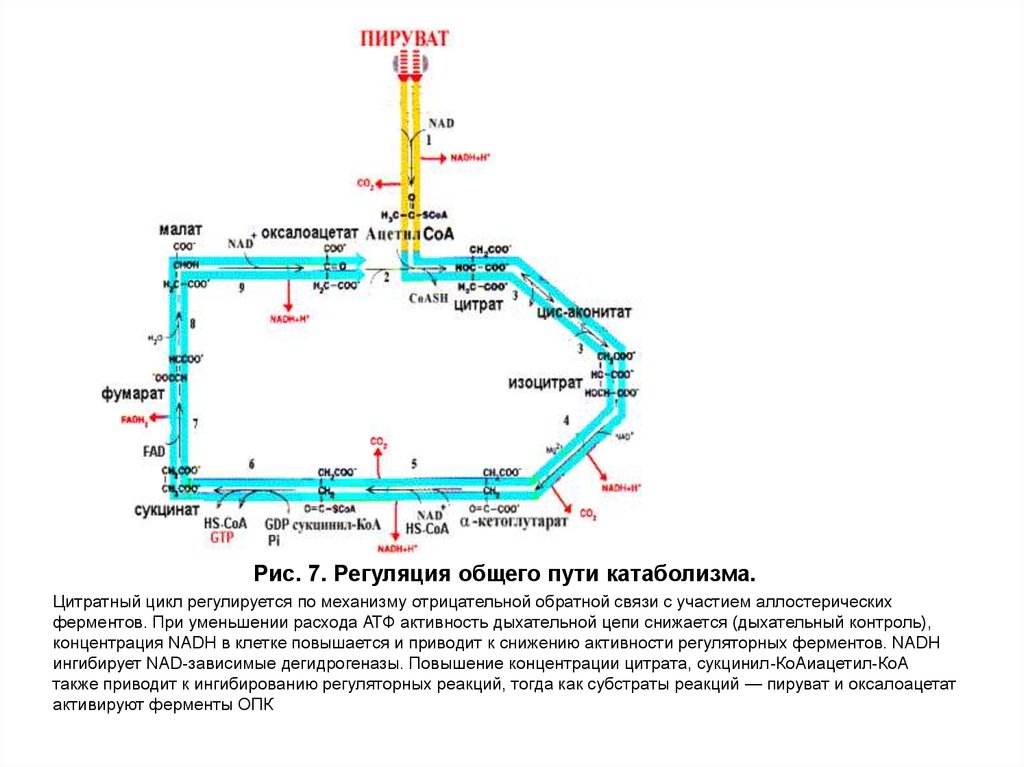
Рис. 7. Регуляция общего пути катаболизма.Цитратный цикл регулируется по механизму отрицательной обратной связи с участием аллостерических
ферментов. При уменьшении расхода АТФ активность дыхательной цепи снижается (дыхательный контроль),
концентрация NADH в клетке повышается и приводит к снижению активности регуляторных ферментов. NADH
ингибирует NAD-зависимые дегидрогеназы. Повышение концентрации цитрата, сукцинил-КоАиацетил-КоА
также приводит к ингибированию регуляторных реакций, тогда как субстраты реакций — пируват и оксалоацетат
активируют ферменты ОПК
24. Регуляция общих путей катаболизма
Другой механизм регуляции связан с необходимостьюрегенерации NAD+ в дыхательной цепи. При уменьшении расхода АТФ
в клетке скорость дыхания митохондрий снижается (дыхательный
контроль), уменьшается также скорость окисления NADH в
дыхательной цепи и увеличивается концентрация NADH. В этом
случае NADH ингибирует некоторые ферменты общих путей
катаболизма, что приводит к замедлению реакций катаболизма и,
следовательно, замедлению наработки восстановленных
коферментов и уменьшению синтеза АТФ. При увеличении
энергетических потребностей организма происходит все наоборот.
В регуляции скорости ОПК существенную роль играет
концентрация субстратов (например, активатором
пируватдегидрогеназного комплекса является пируват) и
концентрация продуктов реакции, которые оказывают ингибирующее
действие на активность некоторых ферментов. К тому же,
регулирующим действием обладают ионы Са2+, что особенно важно
для мышц, так как при мышечном сокращении происходит увеличение
концентрации ионов Са2+, которые вместе с другими эффекторами
быстро активируют ферменты ОПК и обеспечивают синтез АТФ для
работы мышц.
25. Регуляция общих путей катаболизма
Регуляция ОПК осуществляется на уровне 4-хреакций,катализируемых:
• ПДК;
• цитратсинтазой;
• изоцитратдегидрогеназой;
• α-кетоглутаратдегидрогеназным комплексом.
Реакция, катализируемая ПДК, является ключевой
реакцией, так как находится в центре пересечения метаболических
путей и обеспечивает взаимосвязь таких процессов, как гликолиз,
глюконеогенез, синтез и окисление жирных кислот. ПДК
обеспечивает цитратный цикл субстратом — ацетил-КоА.
Активность ПДК регулируется различными способами (рис. 8):
• активацией субстратами;
• ингибированием продуктами;
• соотношением NAD+/NADH и АМФ/АТФ;
• путем ковалентной модификации — фосфорилированием и
дефосфорилированием.
26. Регуляция общих путей катаболизма
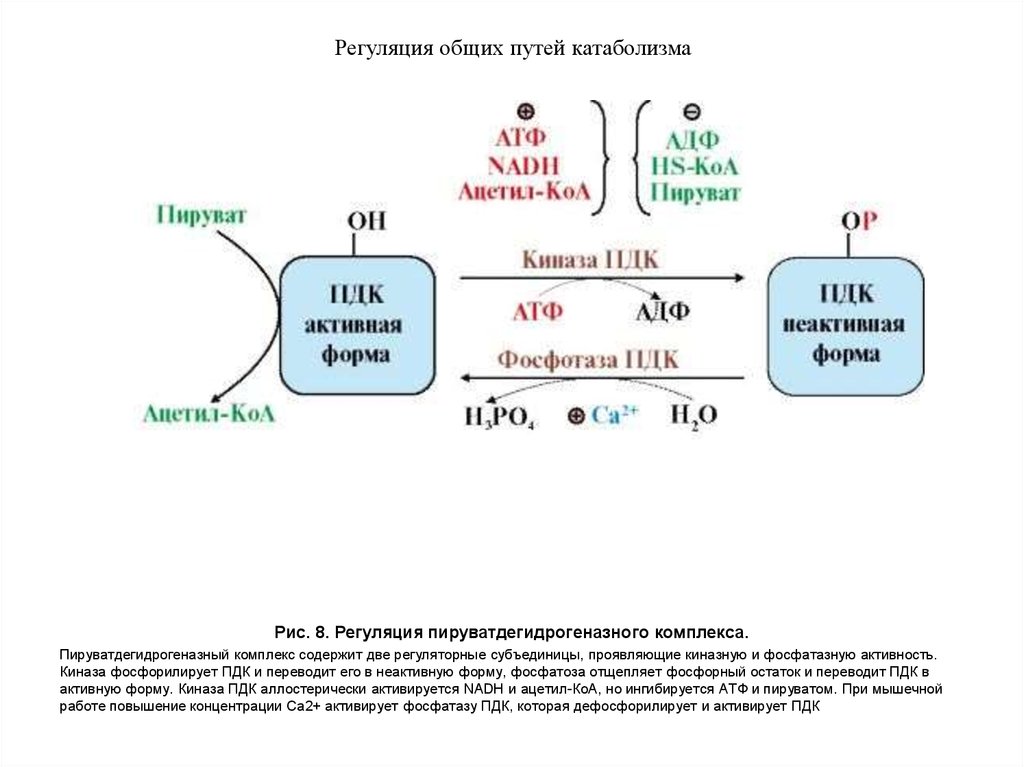
Рис. 8. Регуляция пируватдегидрогеназного комплекса.Пируватдегидрогеназный комплекс содержит две регуляторные субъединицы, проявляющие киназную и фосфатазную активность.
Киназа фосфорилирует ПДК и переводит его в неактивную форму, фосфатоза отщепляет фосфорный остаток и переводит ПДК в
активную форму. Киназа ПДК аллостерически активируется NADH и ацетил-КоА, но ингибируется АТФ и пируватом. При мышечной
работе повышение концентрации Са2+ активирует фосфатазу ПДК, которая дефосфорилирует и активирует ПДК
27. Регуляция общих путей катаболизма
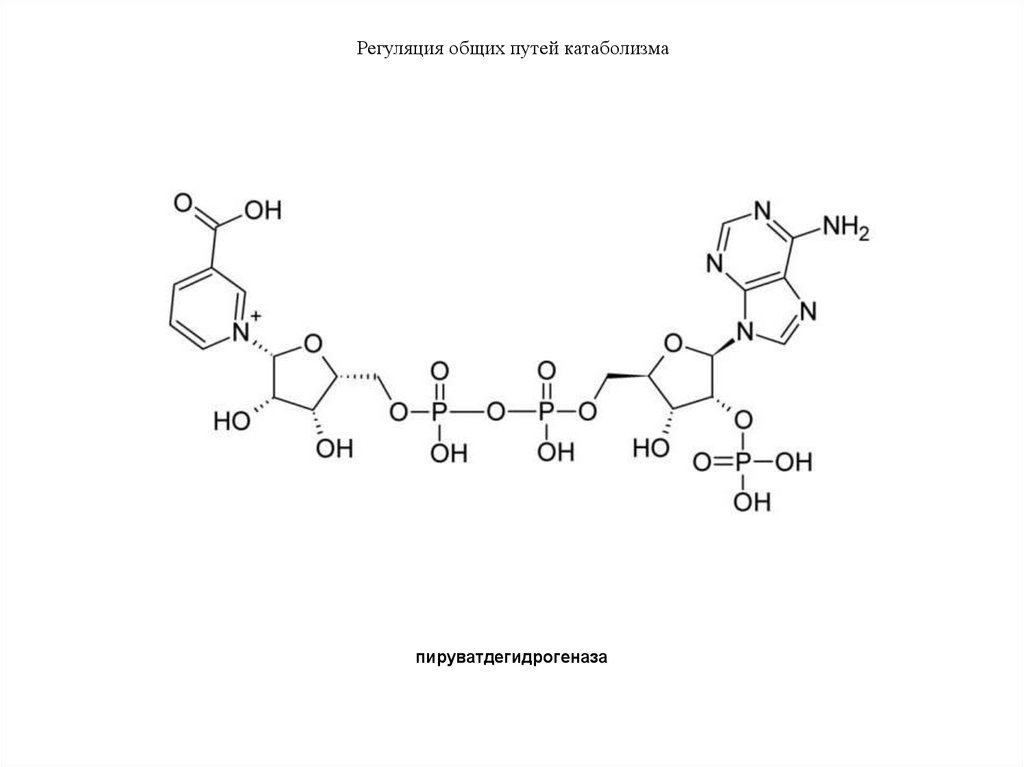
пируватдегидрогеназа28. Амфиболическое значение общего пути катаболизма
Общий путь катаболизма выполняет какэнергетическую, так и анаболическую функцию (рис. 9).
Анаболическая функция ОПК проявляется в том, что
ряд промежуточных продуктов используется для
синтеза необходимых организму веществ. Так
пируват, α-кетоглутарати оксалоацетат являются
кетокислотами, которые путем трансаминирования
могут превращаться в аланин, глутаминовую и
аспарагиновую кислоты соответственно. Сукцинил-КоА
используется для синтеза гема, а пируват и
оксалоацетат могут включаться в процесс синтеза
глюкозы.
29.
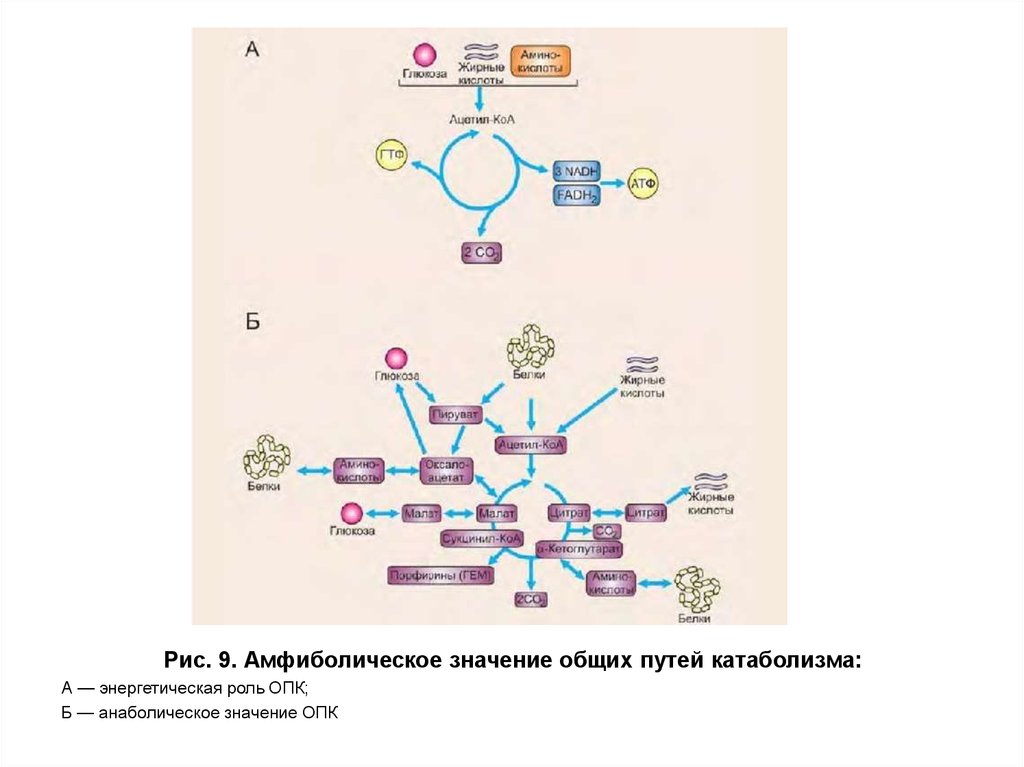
Рис. 9. Амфиболическое значение общих путей катаболизма:А — энергетическая роль ОПК;
Б — анаболическое значение ОПК
30. Амфиболическое значение общего пути катаболизма
выведение хотя бы одного метаболита цикла нарушает егоработу, так как уменьшает регенерацию оксалоацетата. Для компенсации
убыли метаболитов цикла в митохондриях происходит реакция
карбоксилирования пирувата с образованием оксалоацетата. Таким
образом, пируват включается в цитратный цикл двумя путями:
окислительным декарбоксилированием с образованием ацетил-КоА и
карбоксилированием с образованием оксалоацетата. Последнюю
реакцию катализирует пируваткарбоксилаза
пируваткарбоксилаза
Пируват + СО2 + АТФ → Оксалоацетат + АДФ + Н3РО4.
Пируваткарбоксилаза содержится только в митохондриях. Фермент
построен из четырех субъединиц, каждая из которых содержит прочно
связанный ион Mn2+ и витамин биотин, выполняющий коферментную
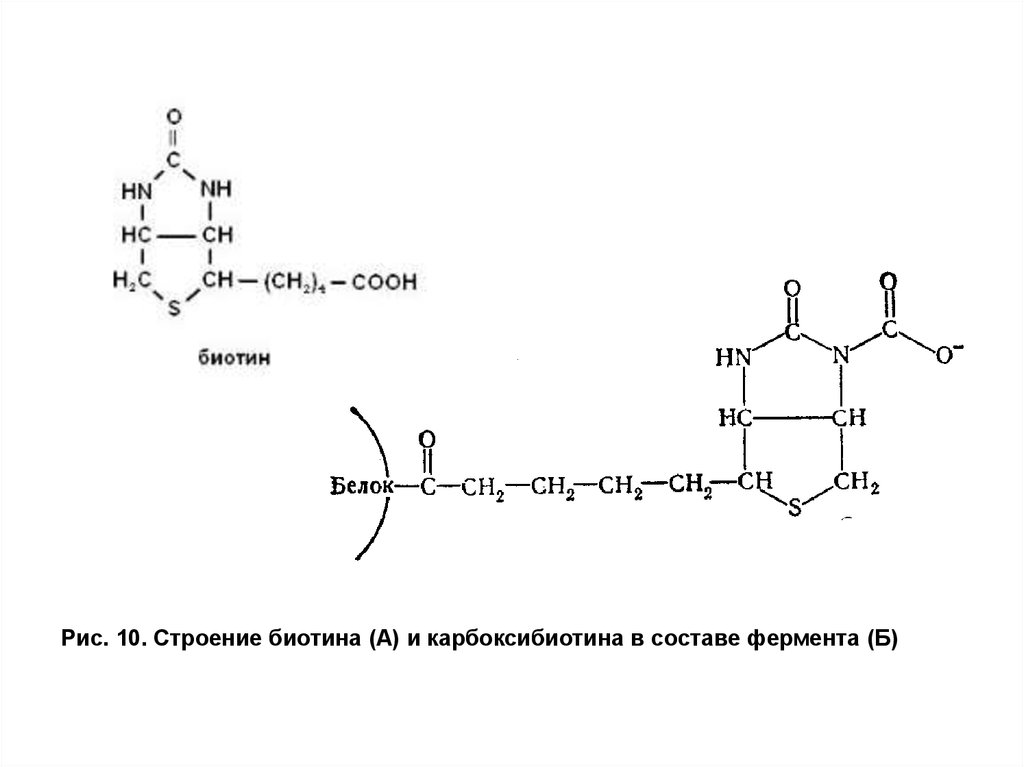
функцию. Биотин соединен с ферментом амидной связью через εаминогруппу остатка лизина (рис. 10).
31.
Рис. 10. Строение биотина (А) и карбоксибиотина в составе фермента (Б)32. Гипоэнергетические состояния
Наиболее частой причиной гипоэнергетических состоянийявляется гипоксия, возникновение которой, в свою очередь, связано с
нарушением:
• поступления кислорода в кровь, что наблюдается при
недостаточности О2 во вдыхаемом воздухе или недостаточности
легочной вентиляции;
• транспорта кислорода в ткани при патологии кровообращения
или снижении транспортной функции гемоглобина;
• функций митоходрий, вызванных действием ядов и
разобщителей. Кроме того, причиной гипоэнергетических состояний
могут быть гиповитаминозы, так как в реакциях общих путей
катаболизма и дыхательной цепи участвуют коферменты,
содержащие витамины. Так, витамин В1 входит в состав
тиаминдифосфата, В2 является составной частью FMH и FAD,
витамин РР в виде никотинамида входит в состав NAD+ и NADР,
пантотеновая кислота — в состав кофермента А; биотин выполняет
коферментную функцию в реакции карбоксилирования пирувата.



















 biology
biology








