Similar presentations:
Острые лейкозы
1. Лекция 10 Опухолевые заболевания системы крови
Острые лейкозы2. Острый лейкоз
• Острый лейкоз — клональное(онкологическое) заболевание, первично
возникающее в костном мозге в результате
мутации стволовой клетки крови. Следствием
мутации является потеря потомками
мутировавшей клетки способности к
дифференцировке до зрелых клеток крови.
• Морфологический субстрат острых лейкозов —
бластные клетки.
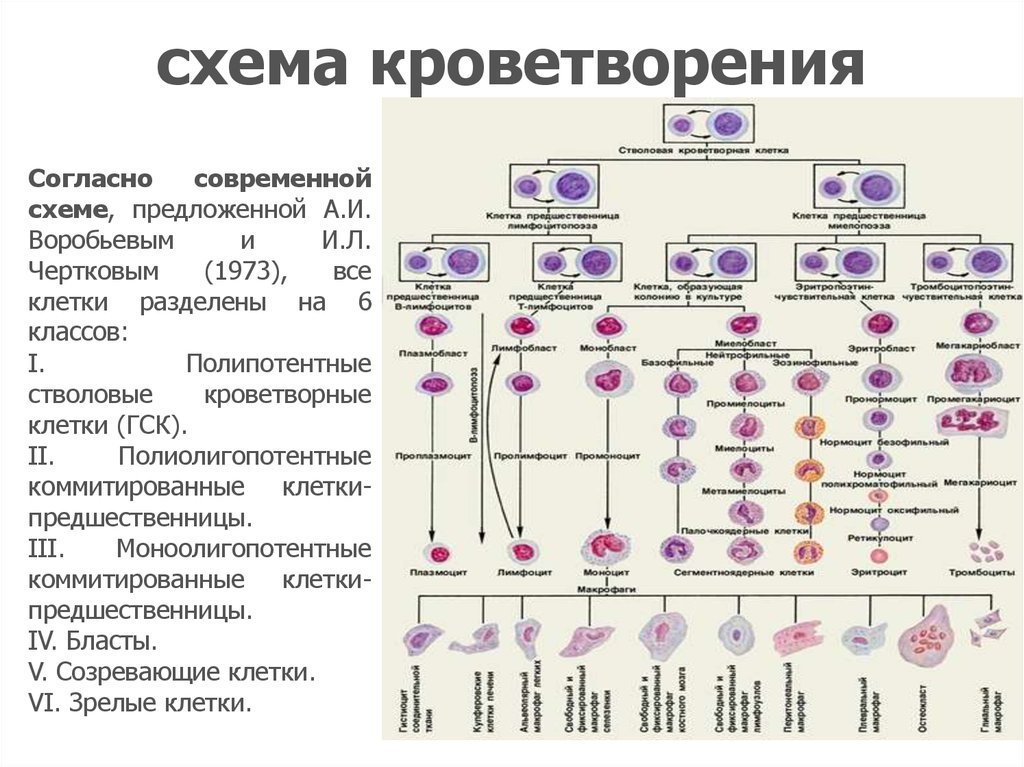
3. схема кроветворения
Согласносовременной
схеме, предложенной А.И.
Воробьевым
и
И.Л.
Чертковым
(1973),
все
клетки разделены на 6
классов:
I.
Полипотентные
стволовые
кроветворные
клетки (ГСК).
II.
Полиолигопотентные
коммитированные клеткипредшественницы.
III.
Моноолигопотентные
коммитированные клеткипредшественницы.
IV. Бласты.
V. Созревающие клетки.
VI. Зрелые клетки.
4. Особенности ОЛ
• характеризуются первичным поражением костного мозганезрелыми кроветворными клетками (бластами)
• с вытеснением ими нормальных клеток
• и инфильтрацией различных тканей и органов, т.е.
отличительной чертой опухолей кроветворной ткани является их
системный характер роста.
• Все острые лейкозы клональны, т.е. возникают из одной
мутировавшей кроветворной клетки.
• В отличие от хронических лейкозов, при которых опухолевые
клетки сохраняют способность к дифференцировке и
созреванию, при острых лейкозах бласты утрачивают эту
способность.
• Принадлежность бластных клеток к той или иной линии
кроветворения, степень их дифференцировки обусловливают
клиническое течение острого лейкоза, терапию,
эффективность лечения и прогноз заболевания
5. Патогенез ОЛ
• Озлокачествование нормальной клетки есть результат каскадногонакопления определенных изменений в ее геноме. В канцерогенез
могут вовлекаться:
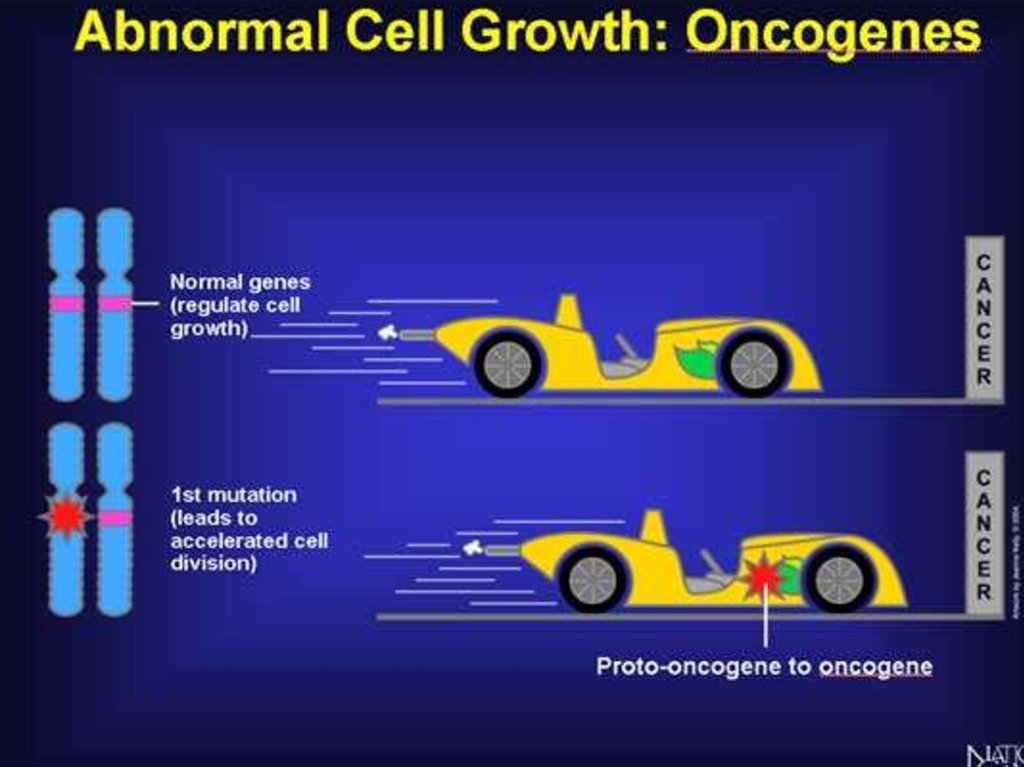
• 1) протоонкогены- нормальные клеточные гены, участвующие в
ключевых процессах жизнедеятельности клетки: регуляции
транскрипции, роста, клеточного цикла, предаче сигнала и т.д. В
случае структурных изменений или повышении уровня экспрессии
этих генов нарушается контроль нормального клеточного роста и
дифференцировки, что приводит к трансформации клетки. Такие
активированные протоонкогены принято называть онкогенами,
• 2) гены-супрессоры (антионкогены) – гены кодирующие ключевые
регуляторные белки, потеря которых влечет за собой нарушения
контроля пролиферации.
• Продуктами большинства генов, составляющих обе группы,
являются так называемые факторы транскрипции – белки,
связывающиеся с ДНК, и влияющие на ее транскрипцию. Н
• Нарушения факторов транскрипции, происходящие в результате
хромосомных перестроек, играет важнейшую роль в лейкозогенезе.
6. Патогенез ОЛ
• Процесс лейкогенеза упрощенно можно представитьследующим образом:
• под влиянием канцерогенных факторов в геноме клетки
происходят мутации ведущие к возникновению активно
функционирующих онкогенов, начинается выработка
онкобелков, которые нарушают механизмы
пролиферации, дифференцировки и апоптоза
изменившейся клетки.
• Возникает клон изменившихся клеток. В таких клетках
легко возникают повторные мутации, появляются более
автономные и агрессивные субклоны, которые являются
причиной нарастающей прогрессии опухолевого
процесса. Распространение опухоли по органам и тканям
происходит путем метастазирования.
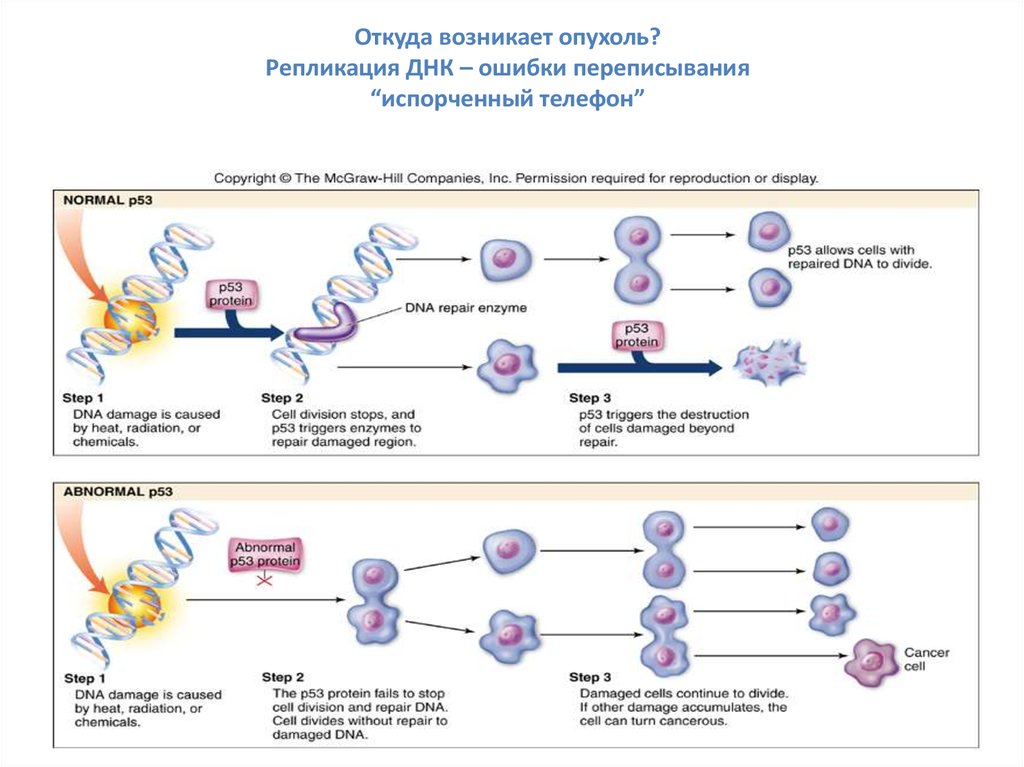
7.
Откуда возникает опухоль?Репликация ДНК – ошибки переписывания
“испорченный телефон”
8. Не все мутации одинаковы
Мутации* Нейтральные
• Остаются
* Негативные/вредные
Элиминируются
(клетка погибает)
* Выгодные
Бесконтрольный рост
9.
Для развития опухоли необходимо выключениегенов-опухолевых супрессоров и активация
протоонкогенов
10.
11. Эпидемиология ОЛ
• Ежегодно регистрируется 35 новых случаевострых лейкозов на 1 млн населения.
• Структура заболеваемости в значительной
степени зависит от возраста.
• ОЛЛ чаще развивается в детском возрасте и
после 40 лет.
• Заболеваемость ОМЛ увеличивается с
возрастом.
• Мужчины и женщины болеют с одинаковой
частотой.
12. Классификация острых лейкозов ВОЗ пересмотр 2016 года
• Острые миелобластные лейкозы (ОМЛ)• Острые лимфобластные лейкозы (ОЛЛ)
B-лимфобластный лейкоз
T-лимфобластный лейкоз
• Острые лейкозы неясной линии
дифференцировки ***
***Бывают такие подвиды острого лейкоза, при которых
изменённые лейкоциты невозможно определить как
лимфоциты или гранулоциты, или когда присутствуют
злокачественно изменённые клетки обоих ростков. Такие
лейкозы иногда называют бифенотипными острыми
лейкозами.
13. Острый миелоидный лейкоз
• Группа лейкозов, затрагивающих миелоидный росток кроветворения• Накапливаясь в костном мозге, они подавляют рост нормальных
клеток крови, что приводит к снижению количества эритроцитов,
тромбоцитов, и нормальных лейкоцитов.
• Болезнь проявляется быстрой утомляемостью, одышкой, частыми
мелкими повреждениями кожи, повышенной кровоточивостью,
частыми инфекционными поражениями.
• До сих пор явная причина заболевания неизвестна.
• ОМЛ является острым заболеванием, развивается быстро, и без
лечения приводит к смерти больного за несколько месяцев, иногда
— недель.
• Самые часто используемые схемы классификации ОМЛ — это давняя
франко-американо-британская (ФАБ) система и более современная
система Всемирной организации здравоохранения (ВОЗ)
14. Классификация ОМЛ ВОЗ пересмотр 2016 года
Название подвидаОМЛ с характерными
генетическими
изменениями
Описание
ОМЛ с транслокациями между хромосомой 8 и хромосомой 21 — [t(8;21)(q22;q22);] RUNX1/RUNX1T1
ОМЛ с инверсиями в хромосоме 16 — [inv(16)(p13.1q22);] или с внутрихромосомной транслокацией в ней —
[t(16;16)(p13.1;q22);] CBFB/MYH11
Острый промиелоцитарный лейкоз с транслокациями между хромосомой 15 и хромосомой 17 —
[t(15;17)(q22;q12);] ПМЛ — протеин/АРРК
ОМЛ с транслокациями между хромосомой 9 и хромосомой 11 — [t(9;11)(p22;q23);] MLLT3/MLL
Мегакариобластный ОМЛ с транслокациями между хромосомой 1 и хромосомой 22 —
[t(1;22)(p13;q13);] RBM15/MKL1 и другие
ОМЛ с изменениями,
связанными с
миелодисплазией
Этот подвид включает больных с предшествующим миелодиспластическим синдромом (МДС)
или миелопролиферативной болезнью (МПБ) или с характерными для него цитогенетическими изменениями. Этот
подвид ОМЛ чаще встречается у пожилых людей и отличается неблагоприятным прогнозом.
ОМЛ и МДС, связанные с
предыдущим лечением
Миелоидная саркома
Миелопролиферативные
заболевания, связанные
с Синдромом Дауна
Бластная плазмацитоидная
дендритноклеточная
опухоль
Этот подвид ОМЛ включает больных, получавших химиотерапию и/или лучевое лечение, после которых возник ОМЛ
или МДС. При этих лейкозах могут быть характерные изменения в хромосомах, прогноз при них часто бывает хуже.
Этот подвид включает больных с миелоидной саркомой
ОМЛ, не подпадающие под
признаки перечисленных
подвидов
Этот подвид включает больных как с кратковременными (преходящими) миелопролиферативными состояниями на
фоне синдрома Дауна, так и с ОМЛ на фоне синдрома Дауна
Этот подвид включает больных с бластными дендритноклеточными опухолями
Включает подвиды ОМЛ, не входящие в перечисленные выше, в том числе:
Острый миелобластный лейкоз с минимальной дифференциацией
Острый миелобластный лейкоз без созревания
Острый миелобластный лейкоз с созреванием
Острый миеломоноцитарный лейкоз
Острый монобластный лейкоз и острый моноцитарный лейкоз
Острый эритроидный лейкоз
Острый мегакариобластный лейкоз
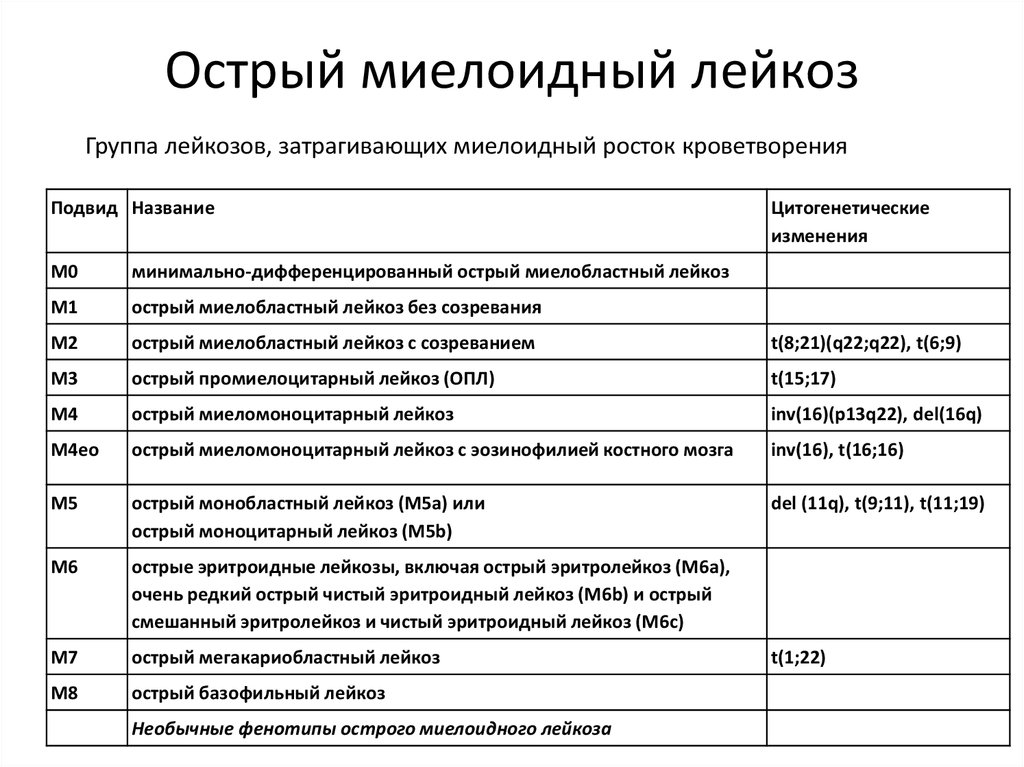
15. Острый миелоидный лейкоз
Группа лейкозов, затрагивающих миелоидный росток кроветворенияПодвид Название
Цитогенетические
изменения
M0
минимально-дифференцированный острый миелобластный лейкоз
M1
острый миелобластный лейкоз без созревания
M2
острый миелобластный лейкоз с созреванием
t(8;21)(q22;q22), t(6;9)
M3
острый промиелоцитарный лейкоз (ОПЛ)
t(15;17)
M4
острый миеломоноцитарный лейкоз
inv(16)(p13q22), del(16q)
M4eo
острый миеломоноцитарный лейкоз с эозинофилией костного мозга
inv(16), t(16;16)
M5
острый монобластный лейкоз (M5a) или
острый моноцитарный лейкоз (M5b)
del (11q), t(9;11), t(11;19)
M6
острые эритроидные лейкозы, включая острый эритролейкоз (M6a),
очень редкий острый чистый эритроидный лейкоз (M6b) и острый
смешанный эритролейкоз и чистый эритроидный лейкоз (M6c)
M7
острый мегакариобластный лейкоз
M8
острый базофильный лейкоз
Необычные фенотипы острого миелоидного лейкоза
t(1;22)
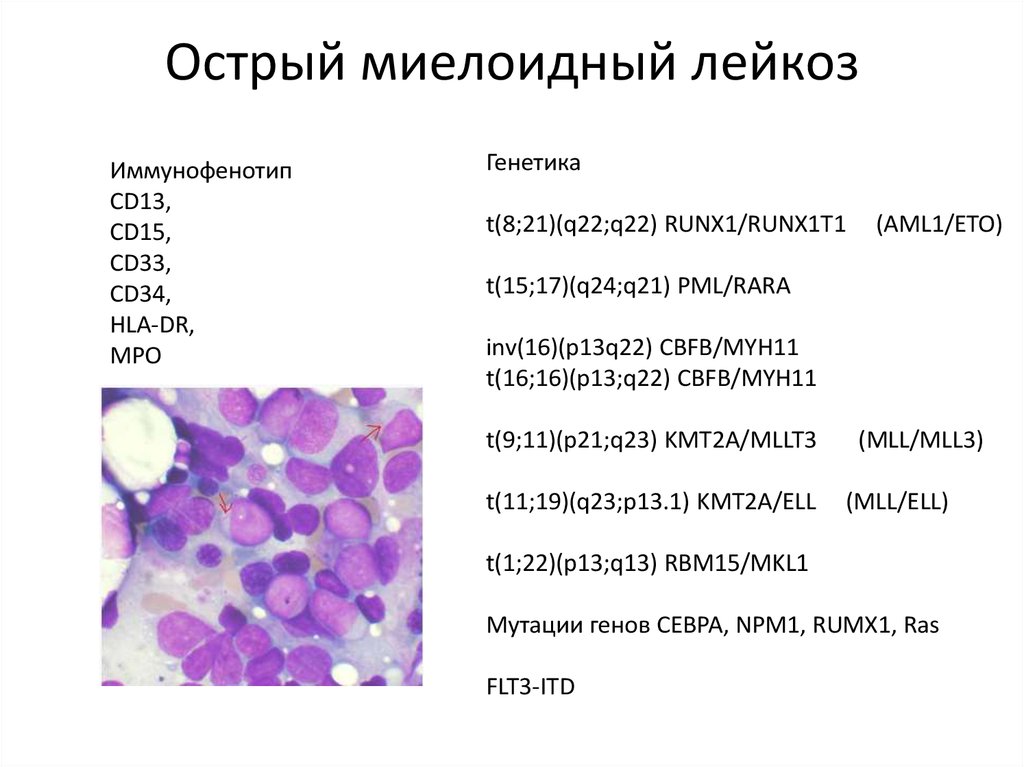
16. Острый миелоидный лейкоз
ИммунофенотипCD13,
CD15,
CD33,
CD34,
HLA-DR,
MPO
Генетика
t(8;21)(q22;q22) RUNX1/RUNX1T1
(AML1/ETO)
t(15;17)(q24;q21) PML/RARA
inv(16)(p13q22) CBFB/MYH11
t(16;16)(p13;q22) CBFB/MYH11
t(9;11)(p21;q23) KMT2A/MLLT3
t(11;19)(q23;p13.1) KMT2A/ELL
(MLL/MLL3)
(MLL/ELL)
t(1;22)(p13;q13) RBM15/MKL1
Мутации генов CEBPA, NPM1, RUMX1, Ras
FLT3-ITD
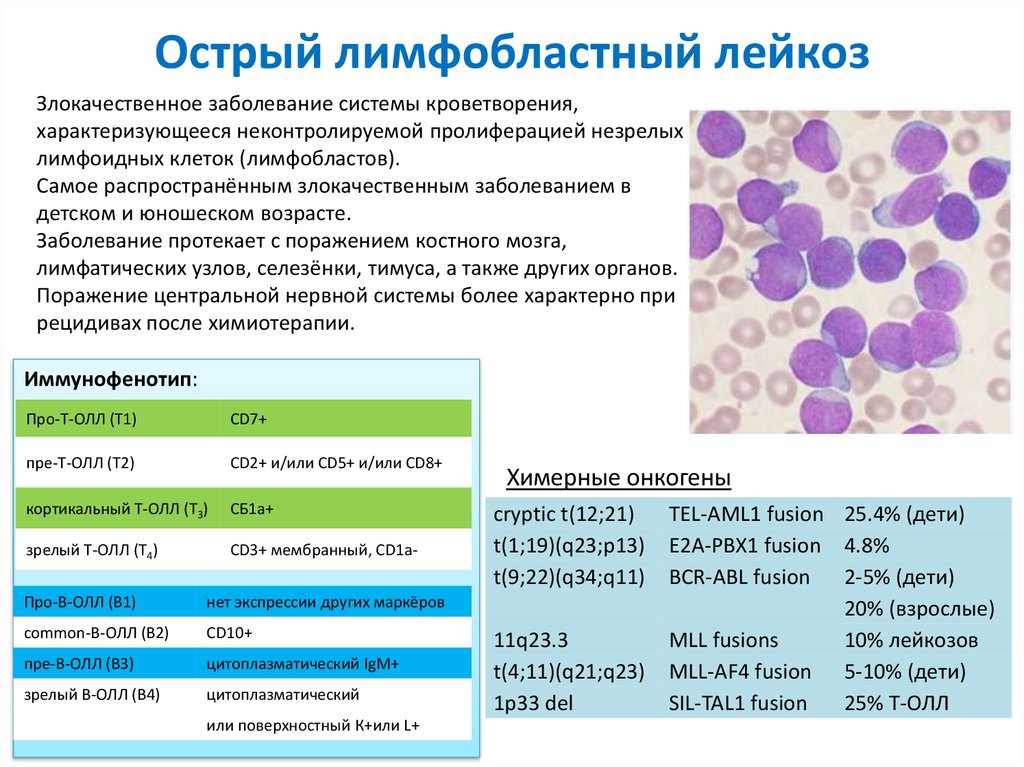
17. Острый лимфобластный лейкоз
Злокачественное заболевание системы кроветворения,характеризующееся неконтролируемой пролиферацией незрелых
лимфоидных клеток (лимфобластов).
Самое распространённым злокачественным заболеванием в
детском и юношеском возрасте.
Заболевание протекает с поражением костного мозга,
лимфатических узлов, селезёнки, тимуса, а также других органов.
Поражение центральной нервной системы более характерно при
рецидивах после химиотерапии.
Иммунофенотип:
Про-Т-ОЛЛ (Т1)
CD7+
пре-Т-ОЛЛ (Т2)
CD2+ и/или CD5+ и/или CD8+
кортикальный Т-ОЛЛ (T3)
СБ1а+
зрелый Т-ОЛЛ (T4)
CD3+ мембранный, СD1а-
Про-В-ОЛЛ (В1)
нет экспрессии других маркёров
common-В-ОЛЛ (В2)
CD10+
пре-В-ОЛЛ (В3)
цитоплазматический IgM+
зрелый В-ОЛЛ (В4)
цитоплазматический
или поверхностный К+или L+
Химерные онкогены
cryptic t(12;21)
t(1;19)(q23;p13)
t(9;22)(q34;q11)
11q23.3
t(4;11)(q21;q23)
1p33 del
TEL-AML1 fusion 25.4% (дети)
E2A-PBX1 fusion 4.8%
BCR-ABL fusion 2-5% (дети)
20% (взрослые)
MLL fusions
10% лейкозов
MLL-AF4 fusion 5-10% (дети)
SIL-TAL1 fusion
25% T-ОЛЛ
18. Иммунофенотипирование Пример выделения регионов
CD10SSC
CD20
FSC
SYTO-16
CD10
CD19
CD10
CD45
19. Классификация ОЛЛ
ФАБ-классификация острых лимфобластных лейкозов основана на разделении ОЛЛ по морфологическим особенностям бластов:
* L1 (микролимфобласты) - размер клетки малый; популяция гомогенная; ядро круглое, структура гомогенная нежная; цитоплазма скудная,
базофилия средней или слабой степени;
* L2 (менее дифференцированные клетки) - преобладают крупные клетки, популяция гетерогенна; распределение хроматина в ядре может
быть как нежным, так и грубым, одна крупная нуклеола или более; цитоплазма чаще обильная, базофилия различной степени выраженности;
* L3 (большие клетки) - популяция гомогенна; ядро круглой или овальной формы с грубым распределением хрматина, содержит одну крупную
нуклеолу или более; умеренное количество интенсивно базофильной цитоплазмы с множеством вакуолей.
ФАБ-классификация ОЛЛ большого практического значения не имеет.
Гораздо более важное значение для определения прогноза и выбора тактики лечения имеет фенотипическая классификация ОЛЛ,
основанная на представлениях о стадиях дифференцировки нормальных Т-лимфоцитов и В-лимфоцитов, у которой выделяют 4 варианта
Т-ОЛЛ и В-ОЛЛ.
Все Т-ОЛЛ имеют экспрессию в цитоплазме или на мембране Т-лимфоцитов CD3+:
Про-Т-ОЛЛ (Т1) вариант имеет один мембранный пан-Т-маркер CD7+;
Пре-Т-ОЛЛ (Т2) вариант обладает дополнительной экспрессией одного или двух пан-Т-маркеров CD2+ и CD5+ при отсутствии на мембране
CD1+ и CD3+;
Кортикальный Т-ОЛЛ (Т3) вариант имеет CD1a+;
зрелый Т-ОЛЛ (Т4) вариант имеет CD3+ мембранный, CD1a-.
Для В-лимфоцитов на всех стадиях дифференцировки характерна экспрессия антигенов CD19+, CD22+, CD79a+. ОЛЛ из В-лимфоцитов
отличается постоянной и высокой экспрессией антигенов гистосовместимости второго класса и терминальной
деоксинуклеотидилтрансферазы:
Про-В-ОЛЛ (В1) вариант - не имеет экспрессии других маркеров;
Common-В-ОЛЛ (В2) вариант - CD10+;
Пре-В-ОЛЛ (В3) вариант - цитоплазматический IgM+;
Зрелый В-ОЛЛ (В4) вариант - цитоплазматический или поверхностный K+ или L+.
20. Клинические проявления ОЛ
Клинические проявления одинаковы для всех вариантов острых лейкозов и могут быть
довольно полиморфными.
Начало заболевания может быть внезапным или постепенным. Для них не существует
характерного начала, каких-либо специфических клинических признаков. Только тщательный
анализ клинической картины позволяет распознать скрывающееся под видом «банального»
заболевания более серьёзное.
Характерна комбинация синдромов недостаточности костного мозга и признаков
специфического поражения (признаки интоксикации: снижение массы тела, лихорадка,
слабость, потливость, снижение аппетита.Может наблюдаться инфильтрация десен лейкозными
клетками, при этом десны гиперплазированы, нависают над зубами, гиперемированы.
Пролиферативный синдром может проявляться увеличением размеров лимфатических узлов
(лимфоаденопатия), селезенки, печени. В ряде случаев на коже появляются лейкемиды —
приподнимающиеся над поверхностью кожи образования мягкой или плотной консистенции.
Цвет их может соответствовать цвету кожи или быть светло-коричневым, желтым, розовым.)
Поражение ЦНС (нейролейкемия) возникает особенно часто при ОЛЛ.
В связи с лейкозной инфильтрацией слизистых оболочек полости рта и ткани миндалин
появляются некротический гингивит, тонзиллит (некротическая ангина). Иногда присоединяется
вторичная инфекция и развивается сепсис, приводящий к смерти.
Тяжесть состояния больного может быть обусловлена выраженной интоксикацией,
геморрагическим синдромом, дыхательной недостаточностью (вследствие сдавления
дыхательных путей увеличенными внутригрудными лимфатическими узлами).
21. Клинические проявления ОЛ
22. Клинические проявления ОЛ
Клиническая характеристика.
Клинические проявления ОЛ неспецифичны.
Но при клинической диагностике наблюдаются три главных синдрома:
1) пролиферативный – проявляется в связи с инфильтрацией лейкозными клетками различных
органов и тканей. Проявляется увеличением л.узлов, селезенки, печени, поражением кожи, легких,
мозговых оболочек, миндалин и т.д.
2) Синдром миелодепрессии выражается в развитии анемии, нейтропении, тромбоцитопении.
3) Синдром интоксикации связан с распадом опухолевых клеток.
Начало заболевания нередко протекает без выраженных клинических симптомов. Больные
отмечают общую слабость, утомляемость, боль в костях, субфебрильную температуру. Однако у
некоторых больных можно выявить небольшое увеличение периферических лимфоузлов,
селезенки,
при исследовании крови обнаруживается немотивированное повышение или снижение количества
лейкоцитов, лимфоцитоз, моноцитоз, тенденция к анемии и тромбоцитопении.
В других случаях больные обращаются к врачу в связи с симптомами ОРЗ, ангины, стоматита,
кровоточивостью, что указывает на стадию уже развернутой клинической картины заболевания. Для
нее характерны выраженная интоксикация, температура, язвенно-некротические поражения
миндалин и слизистой. Геморрагический синдром обусловлен тромбоцитопенией, дефицитами 5, 8
факторов свертывания, протромбина, фибриногенна. В дальнейшем у ряда больных наблюдается
гиперплазия лимфоузлов, селезенки и печени, обусловленные лейкозной инфильтрацией. У
больных возникает иммунодефицитное состояние. Поэтому заболевание часто осложняется
сепсисом, пневмонией. У больных может возникать нейролейкоз, проявляющийся симтомами
менингита, менингоэнцефалита, локального поражения вещества головного мозга, черепных и
периферических нервов.
23. Диагностика ОЛ
• Для постановки диагноза лейкоза необходима пункция костногомозга.
• Диагноз ставится если количество бластных клеток в мазке
к.мозга составляет 30% (30-90 %).
• В пунктате обнаруживается высокое содержание бластных клеток,
угнетение эритроидного, мегакариоцитарного и
гранулоцитарного ростка.
• В периферической крови – анемия, тромбоцитопения, количество
лейкоцитов может быть повышенным.
• Характерен лейкемический провал (зияние), выражающийся в
отсутствии промежуточных форм между бластными клетками и
зрелыми нейтрофилами. Эозинофилы и базофилы как правило
отсутствуют.
• ОЛ необходимо дифференцировать также с инфекционным
мононуклеозом. При инфекционном мононуклеозе в крови
отсутствуют бласты, наряду с лимфоцитозом и моноцитозом
определяются мононуклеары. Анемия и тромбоцитопения не
характерны.
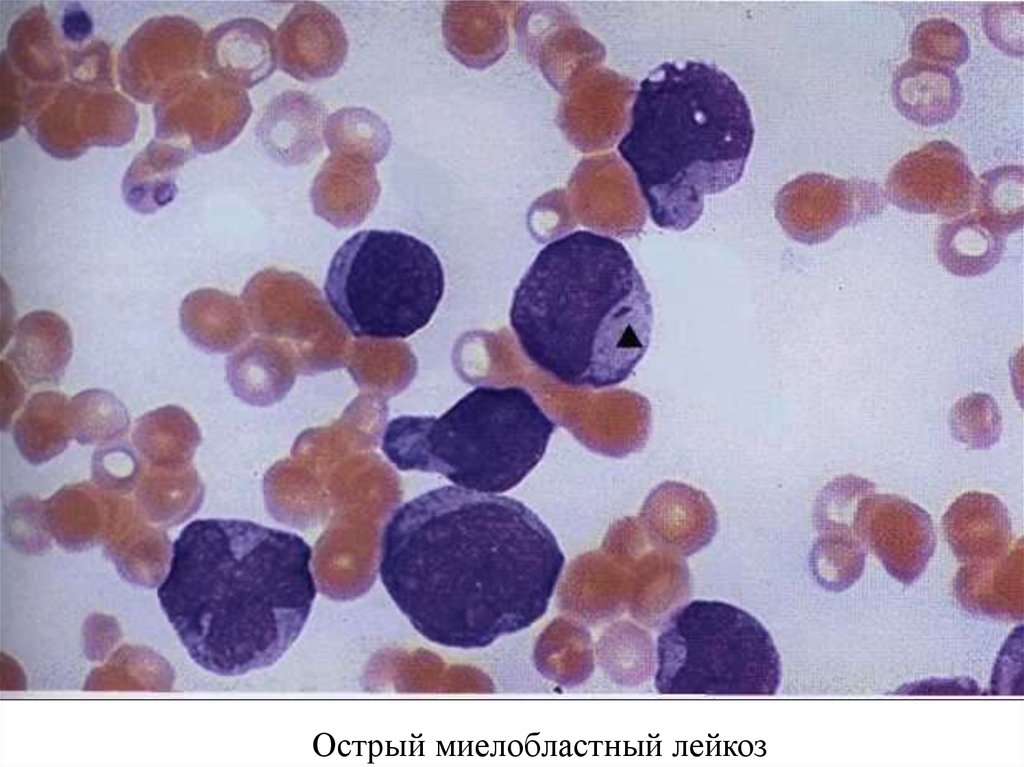
24. Диагностика ОЛ
• Бластные клетки при всех ОЛхарактеризуются крупными размерами,
большим ядром, занимающим почти всю
клетку и отличающимся нежно-сетчатым
строением хроматина с крупными
единичными ядрышками. Цитоплазма
клеток в виде узкого ободка голубоватого
или серо-голубого цвета, с единичными
мелкими гранулами или без грануляции.
25.
Острый лимфобластный лейкоз26.
Острый миелобластный лейкоз27.
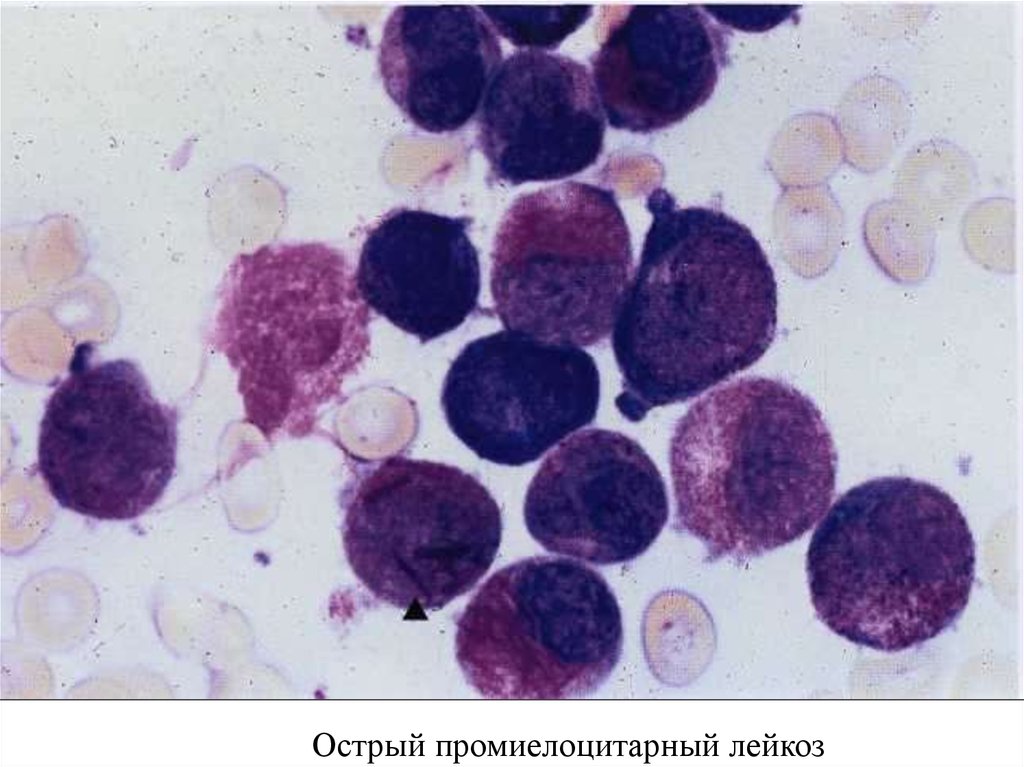
Острый промиелоцитарный лейкоз28.
Характеристики бластных клеток при ОЛ:1. Изменение ядра и цитоплазмы (вместо крупных появляются
клетки
и
неправильной формы с увеличением площади ядра
цитоплазмы;
2. Способность расти вне органов гемопоэза (пролифераты из
лейкозных клеток находят в коже, почках, головном мозге и
в
мозговых оболочках)
3. Имеют скачкообразный уход опухоли из-под цитостатического
воздействия, а также лучевого, гормонального;
4. Нарастание процесса в виде выхода бластных элементов в
периферическую кровь, перехода от лейкопении к
лейкоцитозу.
29.
Изменение ядра и цитоплазмы30. Лечение ОЛ
1) Химиотерапия
Первый этап химиотерапии – это индукция ремиссии, основная цель которой
заключается в уменьшении количества бластных клеток до необнаруживаемого
доступными методами диагностики уровня.
Второй этап – консолидация, направленная на ликвидацию оставшихся лейкозных клеток.
За этим этапом следует реиндукция – повторение этапа индукции.
Помимо этого, обязательным элементом лечения является поддерживающая терапия
оральными цитостатиками.
Выбор протокола в каждом конкретном клиническом случае зависит от того, в какую
группу риска входит больной (играет роль возраст человека, генетические особенности
заболевания, количество лейкоцитов в крови, реакция на проводимое ранее лечение и
т.п.).
Общая длительность химиотерапии при острых лейкозах составляет около 2 лет.
2) Аллогенная трансплантация гемопоэтических клеток
Больным острыми лейкозами пересаживают стволовые клетки, которые могут стать
родоначальниками форменных элементов крови. Трансплантация, проводимая таким
пациентам, должна быть аллогенной, то есть от родственного или неродственного
донора.
При рецидиве ОМЛ единственным испытанным способом лечения, который может
оказаться действенным, оказывается пересадка стволовых клеток .
31. Лечение ОЛ
• Основным методом лечения острого лейкоза является использованиецитостатических средств – химиотерапия направленная на полное
уничтожение лейкозного клона. Большинство цитостатиков действует
на делящиеся клетки и не влияет на элементы находящиеся в фазе
митотического покоя. Митотический цикл состоит из 4 фаз:
пресинтетический (G1), фазы синтеза ДНК (S), премитотический (G2) и
митоза (M). После окончания митоза часть клеток сразу входит в
клеточный цикл, а другая остается в состоянии покоя (G0).
• Монотерапия одним препаратом имеет ограниченое применение.
Широко применяется полихимиотерапия – схемы, из нескольких
цитостатиков с учетом их различного действия на разные опухолевые
клетки и фазы клеточного цикла. Прием препарата назначается курсами
3-14 дней с перерывами 10-11 дней. Перерыв необходим для того,
чтобы покоящаяся популяция бластов перешла в митотический цикл.
• При химиотерапии, наряду со злокачественными, могут поражаться и
нормальные клетки и ткани, что ведет к развитию, так называемой
цитостатической болезни, которая представляет собой комплекс
синдромов, главный из которых связан с возникновением дефицита
клеток крови. Наиболее частые проявления цитостатической болезни миелотоксический агранулоцитоз, некротическая энтеропатия, мукозит,
рвота.
32. Лечение ОЛ
• Существует несколько направлений использования цитокинов вмедицинской практике. Наибольшее клиническое применение
получили цитокины способствующие более быстрому преодолению
повреждения костного мозга, связанного с цитостатической терапией.
Большинство химиопрепаратов, воздействуя в основном на быстро
делящиеся клетки, повреждают и предшественники гемопоэза.
Наиболее опасным при этом является развитие нейтропении. От
степени и тяжести нейтропении в значительной степени зависит
количество инфекционных осложнений и летальность. Для борьбы с
миелотоксичностью химиотерапии предложено использовать
цитокины, вызывающее увеличение продукции зрелых клеток. Это в
первую очередь Г-КСФ и ГМ-КСФ, а также эритропоэтин и тромбопоэтин.
Г-КСФ и ГМ-КСФ могут также применяться для стимуляции
противоинфекционных свойств фагоцитов у больных с тяжелой
инфекцией.
33. Иммунотерапия
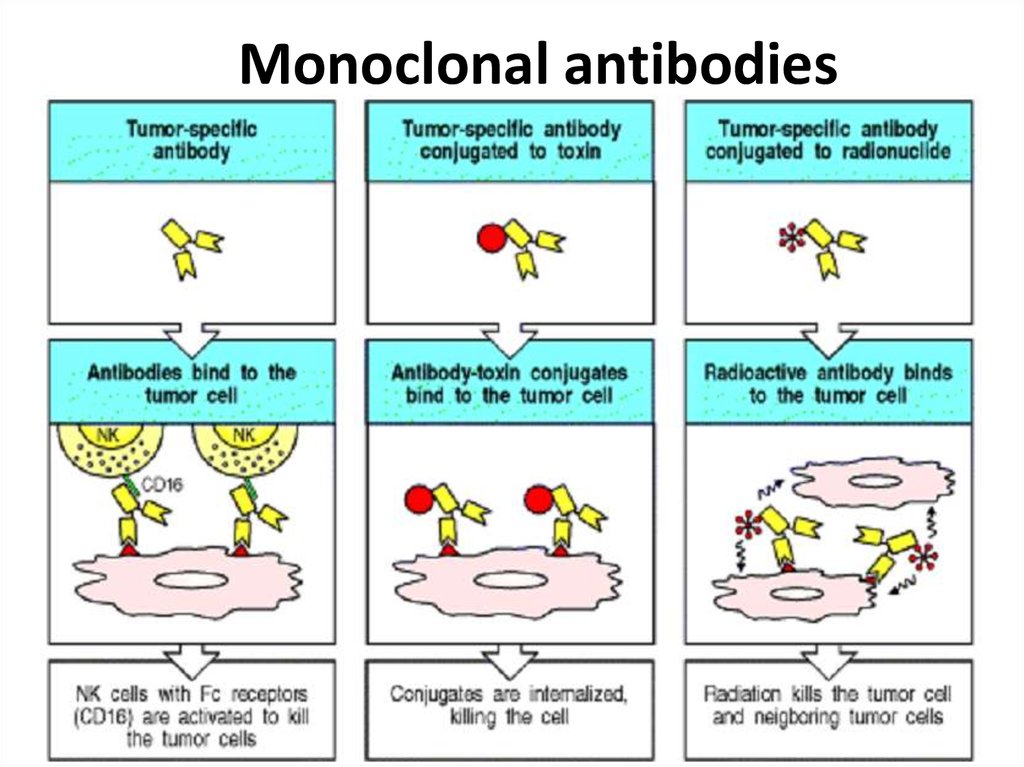
• Моноклонаяльные антитела.• Противоопухолевые вакцины:
Vaccines are substances put into the body to start an immune response
against certain diseases.
• Неспецифическая иммунотерапия
These treatments boost the immune system in a general way, but this
can still help the immune system attack cancer cells.
34. Monoclonal antibodies
35.
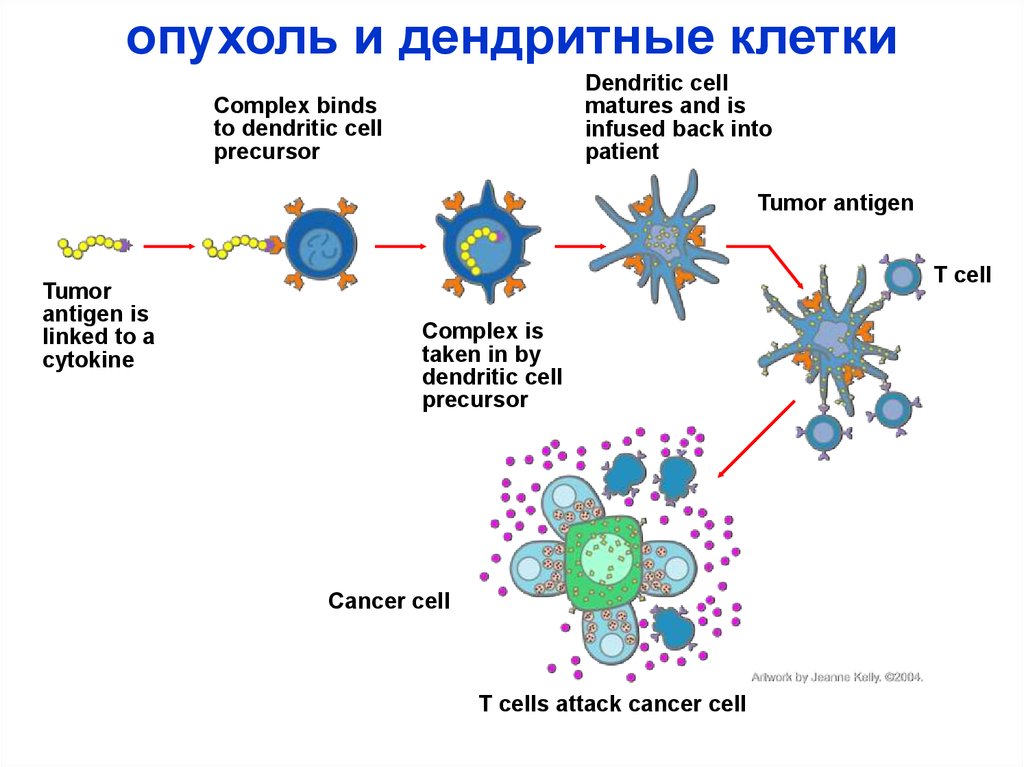
опухоль и дендритные клеткиDendritic cell
matures and is
infused back into
patient
Complex binds
to dendritic cell
precursor
Tumor antigen
Tumor
antigen is
linked to a
cytokine
T cell
Complex is
taken in by
dendritic cell
precursor
Cancer cell
T cells attack cancer cell
36. Прогноз при остром лейкозе
• Острый лимфобластный лейкозУ детей в 95% и более случаев наступает полная ремиссия.
У 70—80% больных детей болезнь не проявляется в течение 5 лет, их считают
здоровыми.
При возникновении рецидива в большинстве случаев можно достичь второй полной
ремиссии.
Больные со второй ремиссией — кандидаты на трансплантацию костного мозга с
вероятностью долговременного выживания 35-65%.
Взрослые редко болеют ОЛЛ. Длительной ремиссии (более 5 лет) удаётся достичь в
15-25% случаев.
* Острый миелобластный лейкоз
Полной ремиссии при большинстве вариантов острого миелобластного лейкоза
удаётся добиться у 60—70% больных.
При различных постиндукционных схемах средняя длительность ремиссии — 12-15
мес; у 25-35% больных нет рецидивов в течение 24 мес, часть из них достигает
стойкой ремиссии («излечивается»).
Опубликованные в 2015 г. в журнале Lancet данные сравнительного анализа
выживаемости для пациентов из 67 стран свидетельствуют о том, что по лечению
острого лимфобластного лейкоза у детей Беларусь занимает 10 место в мире,
опережая такие страны, как США, Израиль, Япония, Финляндия и др.(Lancet 2015;
385: 977–1010).

























 medicine
medicine








