Similar presentations:
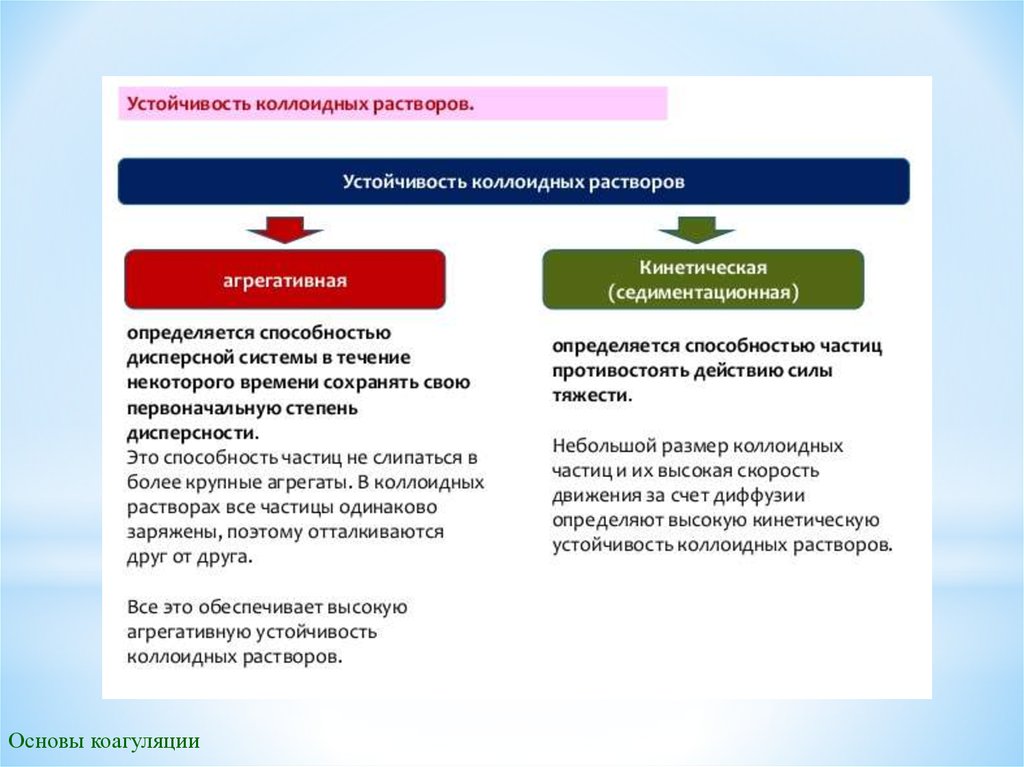
Основы коллоидной химии и коагуляции загрязняющих веществ в процессах очистки воды
1.
Основы коагуляции2.
Основы коагуляции3.
Основы коагуляции4.
Основы коагуляции5.
Основы коагуляции6.
Основы коагуляции7.
Основы коагуляции8.
Основы коагуляции9.
Основы коагуляции10.
Основы коагуляции11.
Основы коагуляции12.
Основы коагуляции13.
Основы коагуляции14.
Основы коагуляции15.
Основы коагуляции16.
Основы коагуляции17.
Основы коагуляции18.
Основы коагуляции19.
Основы коагуляции20.
1. Рассеяние светаОсновы коагуляции
21.
Интенсивность вторичного излучения описываетсяуравнением Релея. Упрощенный вид уравнения Релея для
сферических частиц с d<0,1λ (40-70 нм), не проводящих
электрического тока
Основы коагуляции
22.
Опалесценция золей больше опалесценции растворов ВМС из-забольшей плотности, т.е. большего значения показателя преломления
дисперсной фазы. Чем больше разность показателей преломления, тем
заметнее рассеяние света (и мутность раствора).
Основы коагуляции
23.
Основы коагуляции24.
Основы коагуляции25.
Основы коагуляции26.
Основы коагуляции27.
Основы коагуляции28.
Основы коагуляции29.
Основы коагуляции30.
Основы коагуляции31.
Основы коагуляции32.
Основы коагуляции33.
Основы коагуляции34.
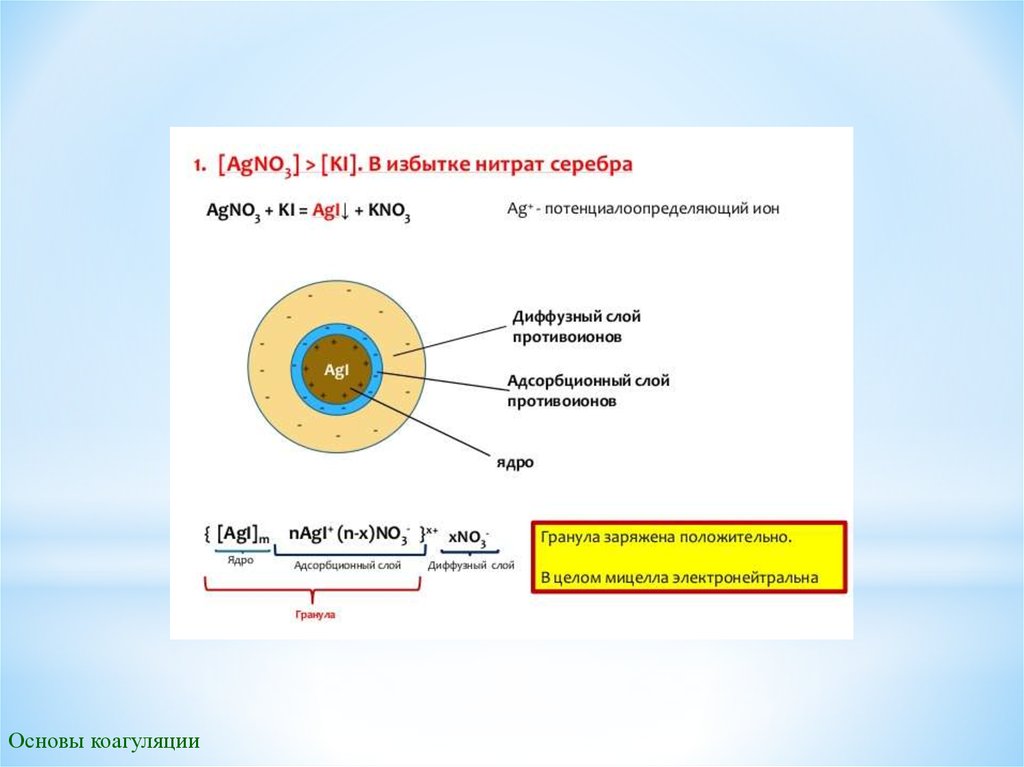
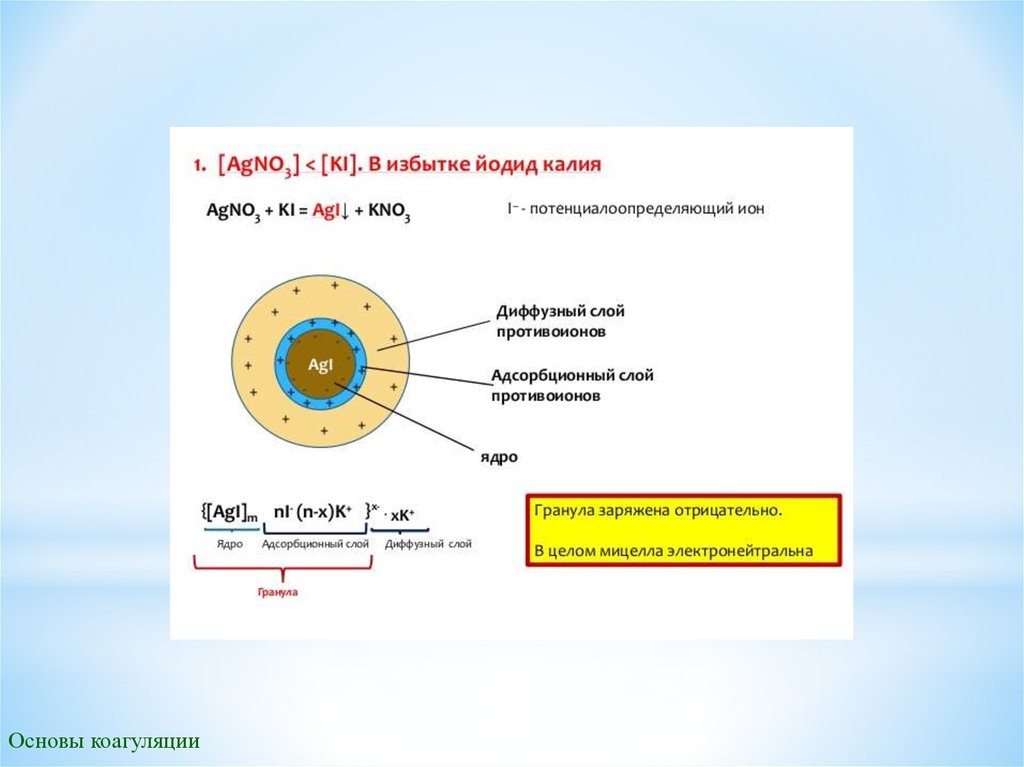
Строение мицелл коллоидных растворов и способы их образованияМицеллой называется коллоидная частица с прилегающим к ней слоем ионов. Мицелла в целом
электронейтральна, а коллоидная частица заряжена. Мицелла представляет собой сложный многокомпонентный
агрегат переменного состава. Мицелла состоит из агрегата, адсорбированного слоя потенциалопределяющих ионов,
адсорбционного слоя противоионов и диффузного слоя противоионов.
Агрегат (ядро)
Потенциалоопределяющие
ионы
Адсорбционный
слой противоионов
Диффузный слой
противоионов
Коллоидная частица
(гранула): ядро с
противоионами
адсорбционного слоя
Мицелла: гранула с
противоионами
диффузного слоя
Основы коагуляции
35.
Основы коагуляции36.
Основы коагуляции37.
Основы коагуляции38.
Основы коагуляции39.
γ = k*(1/z6)(1)
В соответствии с уравнением (1), соотношение порогов коагуляции для трех -, двух - и
одновалентных ионов равно (правило значности):
γ1 : γ2 : γ3 = (1/36) : (1/26) : (1/16) = 729 : 11 : 1
Следовательно, коагулирующая способность трёхзарядного иона в 729 раз выше коагулирующей
способности однозарядного иона.
Основы коагуляции
40.
Основы коагуляции41.
Основы коагуляции42.
Основы коагуляции43.
Основы коагуляции44.
Основы коагуляции45.
Основы коагуляции46.
Основы коагуляции47.
Основы коагуляции48.
Основы коагуляции49.
Основы коагуляции50.
Основы коагуляции51.
Основы коагуляции52.
Основы коагуляции53.
Основы коагуляции54.
Основы коагуляции55.
Основы коагуляции56.
Эффективная толщина двойного слоя уменьшается с ростомконцентрации электролита и возрастает с повышением
температуры. I – ионная сила раствора, I = 1/2ΣCoZi. F –
постоянная Фарадея,
Основы коагуляции
57.
Основы коагуляции58.
Основы коагуляции59.
Основы коагуляции60.
Основы коагуляции61.
Основы коагуляции62.
Основы коагуляции63.
Основы коагуляции64.
Основы коагуляции65.
Основы коагуляции66.
Основы коагуляции67.
Основы коагуляции68.
Основы коагуляции69.
Основы коагуляции70.
Основы коагуляции71.
Физико-химические основы процесса коагуляцииКоагуляцией называют процесс дестабилизации коллоидных частиц путем добавления химического реагента,
называемого коагулянтом, привносящего в коллоидную среду многовалентные катионы, которые могут
быть как свободными, так и связанными с органической макромолекулой (катионные полиэлектролиты).
Основы коагуляции
72.
Физико-химические основы процесса коагуляцииОсновы коагуляции
73.
Физико-химические основы процесса коагуляцииОсновы коагуляции
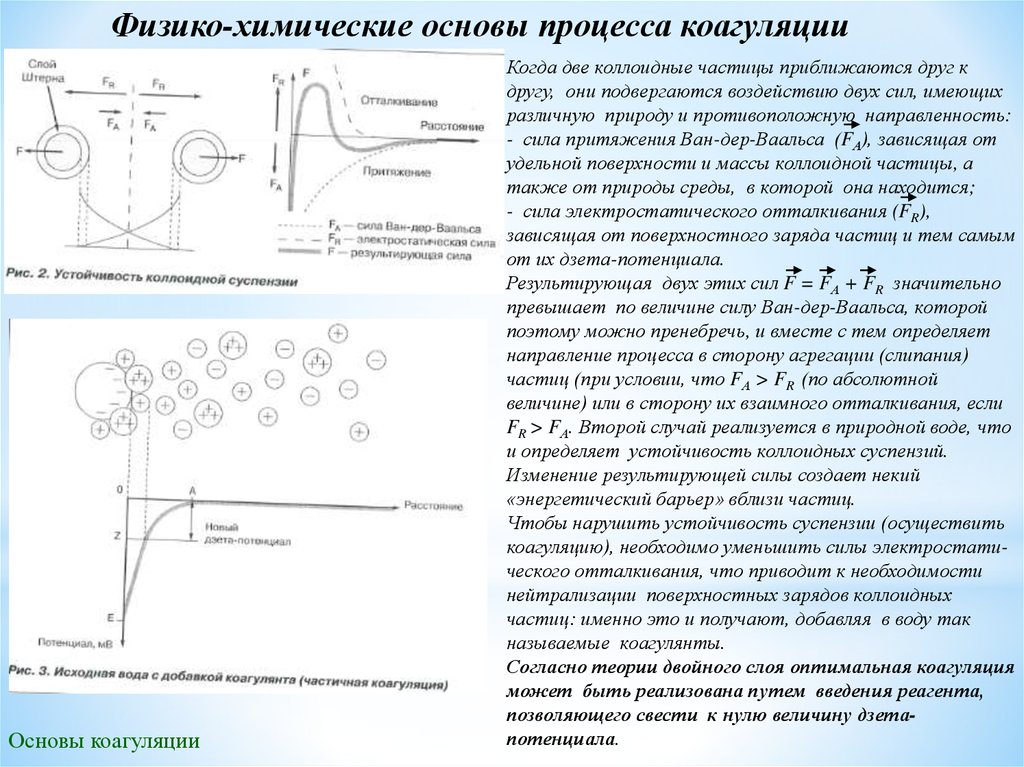
Когда две коллоидные частицы приближаются друг к
другу, они подвергаются воздействию двух сил, имеющих
различную природу и противоположную направленность:
- сила притяжения Ван-дер-Ваальса (FА), зависящая от
удельной поверхности и массы коллоидной частицы, а
также от природы среды, в которой она находится;
- сила электростатического отталкивания (FR),
зависящая от поверхностного заряда частиц и тем самым
от их дзета-потенциала.
Результирующая двух этих сил F = FА + FR значительно
превышает по величине силу Ван-дер-Ваальса, которой
поэтому можно пренебречь, и вместе с тем определяет
направление процесса в сторону агрегации (слипания)
частиц (при условии, что FА > FR (по абсолютной
величине) или в сторону их взаимного отталкивания, если
FR > FА. Второй случай реализуется в природной воде, что
и определяет устойчивость коллоидных суспензий.
Изменение результирующей силы создает некий
«энергетический барьер» вблизи частиц.
Чтобы нарушить устойчивость суспензии (осуществить
коагуляцию), необходимо уменьшить силы электростатического отталкивания, что приводит к необходимости
нейтрализации поверхностных зарядов коллоидных
частиц: именно это и получают, добавляя в воду так
называемые коагулянты.
Согласно теории двойного слоя оптимальная коагуляция
может быть реализована путем введения реагента,
позволяющего свести к нулю величину дзетапотенциала.
74.
потенциалобразующих ионов и противоионов адсорбционногоОсновы коагуляции
75.
Основы коагуляции76.
Коагуляция коллоидных форм гуминовых веществ солями алюминияДвойной электрический слой, образуемый коллоидными частицами гуминовых веществ
―С˭ О
Na+
\
О-
Na+
Cl-
―С˭ О
Na+
\
О-
―С˭ О
Na+
\
О-
Na+
Na+
―С˭ О
\
Na+
О-
адсорбционный слой
противоионов
диффузный
слой
противоионов
Cl-
Cl-
межмицеллярная жидкость
В качестве потенциалообразующих ионов выступают карбоксильные группы гуминовых веществ
Основы коагуляции
77.
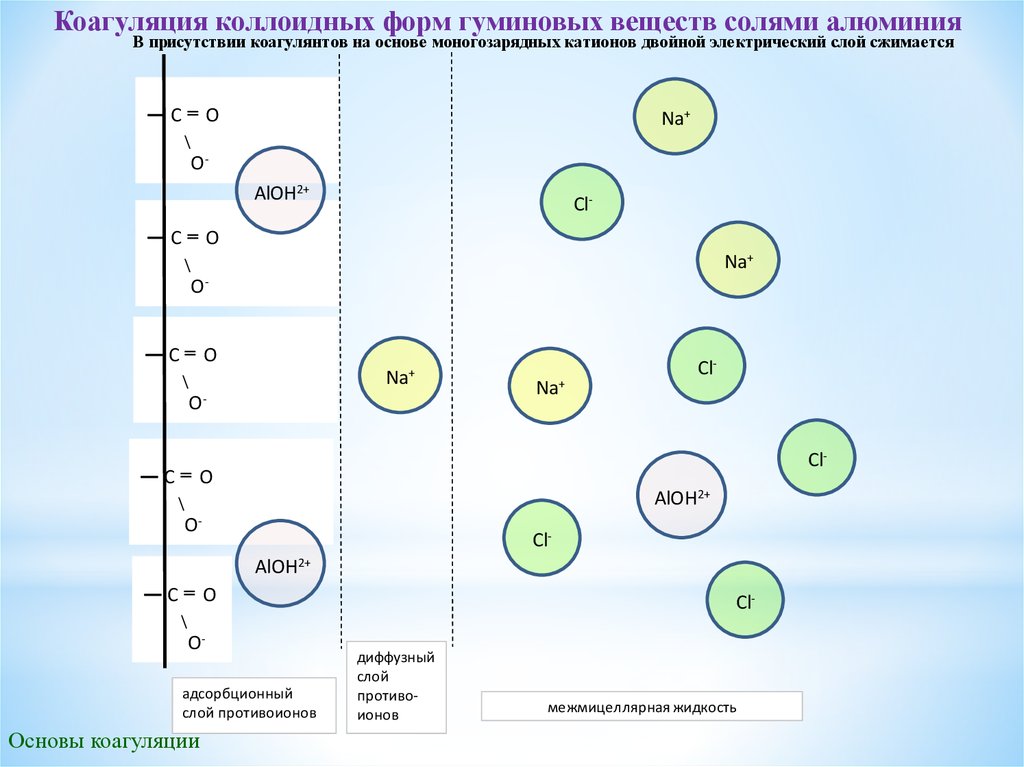
Коагуляция коллоидных форм гуминовых веществ солями алюминияВ присутствии коагулянтов на основе моногозарядных катионов двойной электрический слой сжимается
―С˭ О
Na+
\
ОAlOH2+
Cl-
―С˭ О
Na+
\
О-
―С˭ О
Na+
\
О-
Na+
Cl-
Cl-
―С˭ О
AlOH2+
\
О-
ClAlOH2+
―С˭ О
Cl-
\
Оадсорбционный
слой противоионов
Основы коагуляции
диффузный
слой
противоионов
межмицеллярная жидкость
78.
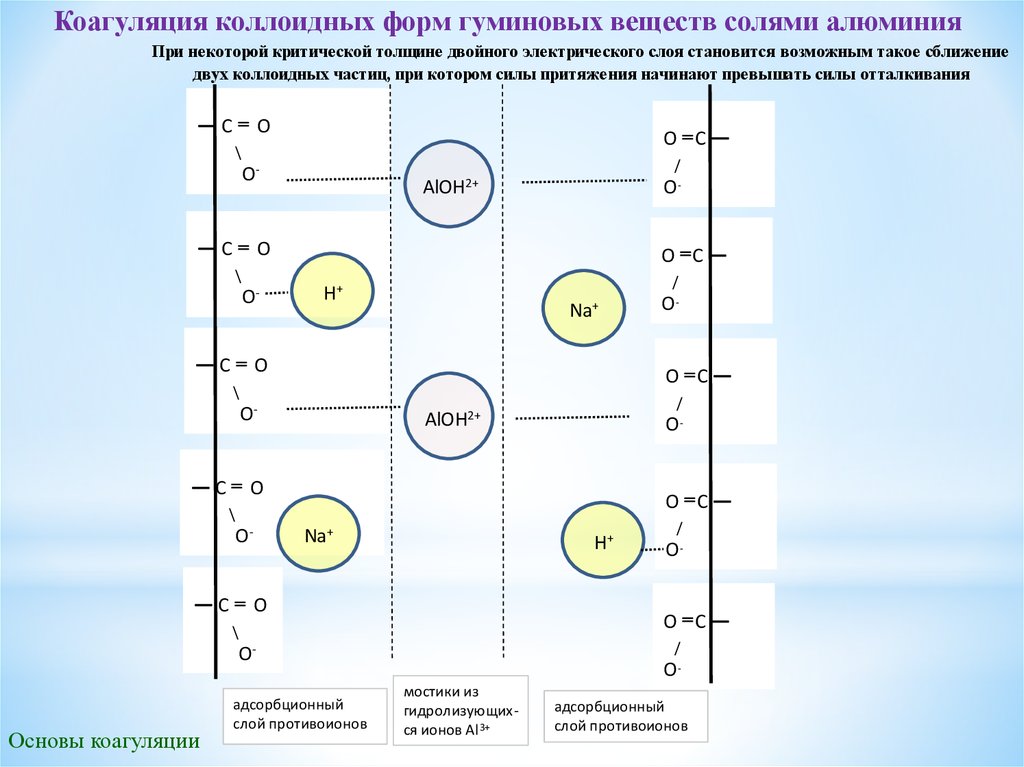
Коагуляция коллоидных форм гуминовых веществ солями алюминияПри некоторой критической толщине двойного электрического слоя становится возможным такое сближение
двух коллоидных частиц, при котором силы притяжения начинают превышать силы отталкивания
―С˭ О
O ˭С ―
\
/
О-
AlOH2+
О-
―С˭ О
\
О-
O ˭С ―
/
H+
Na+
―С˭ О
O ˭С ―
\
О-
/
AlOH2+
О-
―С˭ О
O ˭С ―
\
О-
Na+
H+
―С˭ О
О-
/
Оадсорбционный
слой противоионов
/
O ˭С ―
\
Основы коагуляции
О-
Омостики из
гидролизующихся ионов Al 3+
адсорбционный
слой противоионов
79.
Стадии процесса коагуляцииФактически последовательные процессы
агрегации, приводящие к образованию флокул,
управляются двумя явлениями переноса, которые и
определяют скорость флокуляции:
- перикинетическая флокуляция, связанная с
броуновской диффузией (тепловое движение),
когда все частицы обладают одной и той же
кинетической. энергией, так что самые маленькие
из них имеют наибольшую скорость движения и,
следовательно, наибольшую вероятность
столкновений. В этом случае скорость флокуляции,
или изменение количества слипающихся частиц во
времени, описывается выражением
Стадия
Добавка
коагулянта
Сущность процесса
реакция с водой:
- ионизация;
-гидролизполимеризация
Название
процесса
Гидролиз
Селективная
адсорбция ионов
коагулянта на
поверхности частицы
Коагуляция
Селективная связь
ионов с
поверхностью
частицы
Дестабилизация Включение коллоида
во взвесь
гидроксида
Связь между
Флокуляция
частицами за счет
действия
полимерных
компонентов
коагулянта
Броуновское
Перикинетическая
движение
флокуляция
Перенос
Рассеиваемая
энергия (градиент
Ортокинетическая
скорости)
флокуляция
Кинетика
Мгновенная
Замедленная
(зависит от
температуры и
ионной силы)
Очень быстрая,
требует
повышенного
значения G
Быстрая (зависит от
T, μ,рН, G)
Замедленная
где: n - количество частиц на единицу объема:
(зависит от
а - доля эффективных столкновений;
температуры и
k - константа Больцмана;
ионной силы)
Быстрая (зависит от
Т - абсолютная температура.
T, μ, n)
Эта закономерность справедлива лишь для малых
частиц размерами менее 10 мкм. Она описывает
Медленная (зависит
от T, μ, рН, n)
образование микрофлокул и отражает влияние на
этот процесс «плотности» частиц (п) и
температуры;
ламинарный турбулентный - ортокинетическая флокуляция, связанная с энергией,
режим
режим
рассеиваемой в зоне флокуляции. Можно видеть, что градиент
2 3
2 3
dn/dt
-1/6·αn d G
-Kn d G
скорости является важным параметром, определяющим скорость
флокуляции
Основы коагуляции
.
80.
Основы коагуляции81.
Основы коагуляции82.
Основы коагуляции83.
Основы коагуляции84.
2Al(OH)3 + 3H2SO4 + aq → Al2(SO4)3·nH2O + aqОсновы коагуляции
85.
Основы коагуляции86.
Основы коагуляции87.
Основы коагуляции88.
Основы коагуляции89.
Основы коагуляции90.
Основы коагуляции91.
Основы коагуляции92.
Основы коагуляции93.
Основы коагуляции94.
Основы коагуляции95.
Основы коагуляции96.
Основы коагуляции97.
Основы коагуляции98.
Основы коагуляции99.
Основы коагуляции100.
100Основы коагуляции



















































































 chemistry
chemistry industry
industry








