Similar presentations:
Виды химической связи
1.
ВИДЫХИМИЧЕСКОЙ
СВЯЗИ
Попова Светлана Анатольевна
Учитель химии
ГБОУ СОШ № 1465 имени Н.Г.
Кузнецова г. Москва
2.
ВИДЫ ХИМИЧЕСКОЙ СВЯЗИковалентная
неполярная
ионная
полярная
металлическая
3.
Металлическая –в простых веществах-металлах
Al
Na
Ba
Fe
Mg
4.
Ковалентная неполярнаяв простых веществах –
неметаллах
O2 ; N2 ; H2 ; S8 ;P ;O3
5.
КНС образуют атомы одного и того же химическогоэлемента.
Механизм образования связи.
Каждый атом неметалла отдает в общее пользование
другому атому наружные неспаренные электроны.
Образуются общие электронные пары. Электронная
пара принадлежит в равной мере обоим атомам.
Примеры образования КНС:
H.+.H
H:H
H-H H2
..
..
.
.
.+.F:
:F
..
..
: O. : + : O
:
.
..
..
:F
.. : F..:
:O
:: O.. :
..
F-F F2
O=O O2
6.
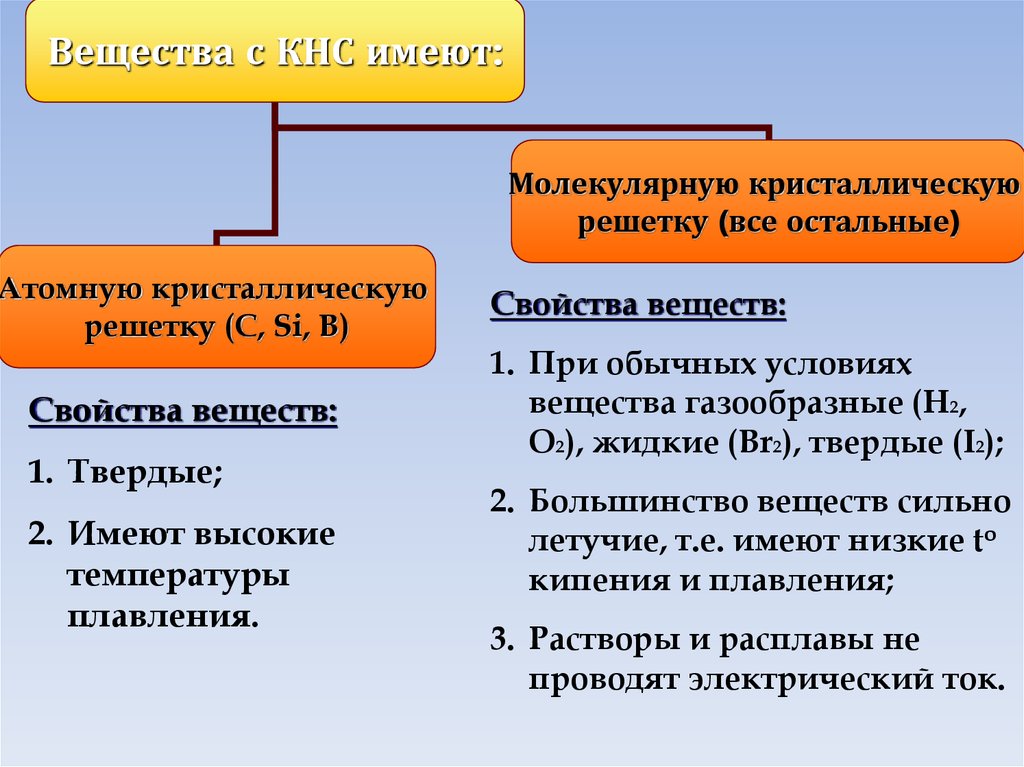
Вещества с КНС имеют:Молекулярную кристаллическую
решетку (все остальные)
Атомную кристаллическую
решетку (C, Si, B)
Свойства веществ:
1. Твердые;
2. Имеют высокие
температуры
плавления.
Свойства веществ:
1. При обычных условиях
вещества газообразные (H2,
O2), жидкие (Br2), твердые (I2);
2. Большинство веществ сильно
летучие, т.е. имеют низкие to
кипения и плавления;
3. Растворы и расплавы не
проводят электрический ток.
7.
Ковалентная полярнаяв сложных веществах,
состоящих из атомов
разных неметаллов:
НСl , N2O5, SF6 , H3BO3 , Р2О5
8.
КПС образуют атомы разных неметаллов (с разнойэлектороотрицательностью). Электроотрицательность
(ЭО)- это свойство атомов одного элемента притягивать к
себе электроны от атомов других элементов.
Самый электроотрицательный элемент – F.
Механизм образования связи.
Каждый атом неметалла отдает в общее пользование
другому атому свои наружные неспаренные электроны.
Образуются общие электронные пары. Общая
электронная пара смещена к более
электроотрицательному элементу.
Примеры образования связи.
..
H + . Cl
..
. ..
H Cl :
..
+
H
-
Cl
+
- Диполь
9.
Вещества с КПС имеют:Молекулярную кристаллическую
решетку (все остальные)
Атомную крисаллическую
Решетку (SiC, SiO2)
Свойства веществ:
1. Твердые;
2. Имеют высокие to
плавления.
Свойства веществ:
1. При обычных условиях
вещества газообразные,
жидкие, твердые;
2. Большинство веществ
сильнолетучие, т.е. имеют
низкие to кипения и
плавления;
3. Растворы и расплавы
проводят электрический ток.
10.
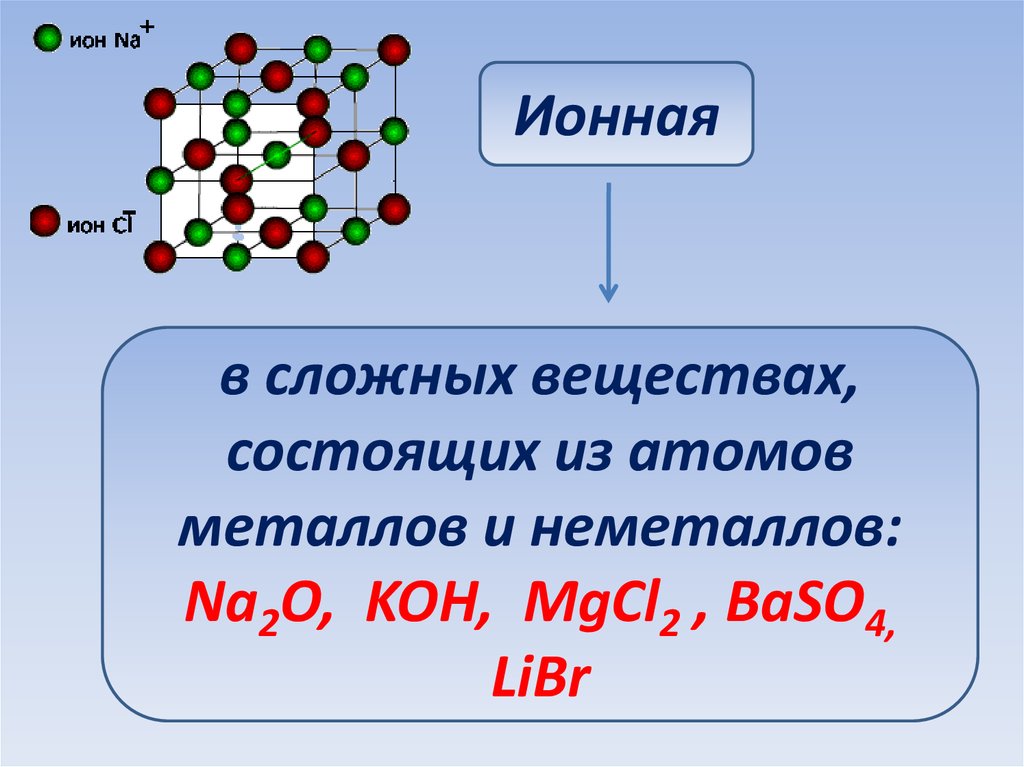
Ионнаяв сложных веществах,
состоящих из атомов
металлов и неметаллов:
Na2O, KOH, MgCl2 , BaSO4,
LiBr
11.
ИС образуется между атомами металлов и неметаллов,т.е. между атомами резко отличающимися друг от друга
по электроотрицательности.
Механизм образования связи.
Атом неметалла забирает наружные электроны у атома
металла и превращается в анион (отрицательно
заряженный ион). Атом металла теряет электроны и
превращается в катион (положительно заряженный
ион). Ионы связаны электростатическими силами.
Пример образования связи.
Na
..
+ . Cl :
..
..
[ Na ] + [ . Cl : ]..
или
Na+ Cl-
12.
Вещества с ИС имеют :Ионную кристаллическую решетку
1.
2.
3.
Свойства веществ:
Все вещества при обычных условиях твердые.
Имеют высокие температуры кипения и плавления.
Расплавы и растворы проводят электрический ток.
13.
Определите вид химическойсвязи в каждом из данных
соединений
H2S
N2
LiCl
BaO
Ca(NO3)2
Pb
F2
14.
В каких соединенияхионный тип связи
NaCL
HNO3
MgO
CO2
ALBr3
H 2O
15.
Какие соединения имеютковалентно -полярный тип
связи
CaO
CH4
KCL
NH3
CL2
HBr
16.
Из перечня веществ выберитеформулы с ковалентной
неполярной связью
Cl2
CO2
H 2O
Mg
O3
N2
17.
Ссылки на источники информации и изображенияУчебник для общеобразовательных учреждений , 8 класс авторы: Г.Е. Рудзитис ,Ф .Г. Фельдман
Таблица неметаллов
http://im6-tub-ru.yandex.net/i?id=84160916-38-72&n=21
Таблица Менделеева
http://www.motto.net.ua/download.php?file=201209/1280x10
24/motto.net.ua-7741.jpg
Строение металлической решетки
http://im5-tub-ru.yandex.net/i?id=10651948-07-72&n=21
Строение ионной решетки
http://im6-tub-ru.yandex.net/i?id=460183781-67-72&n=21
Железо
http://im0-tub-ru.yandex.net/i?id=389614815-46-72&n=21













 chemistry
chemistry