Similar presentations:
Окислительно-восстановительные процессы
1.
Лекция № 6Окислительно-восстановительные
процессы
1. Понятие степени окисления.
2. Способы выражения концентрации растворов.
3. Коллигативные свойства растворов.
4. Основные положения теории электролитической диссоциации.
5. Количественные характеристики процесса диссоциации.
6. Степень электролитической диссоциации. Классификация
растворов по величине α.
7. Закон разбавления Оствальда.
8. Ионное произведение воды. Водородный и гидроксильный
показатель.
9. Гидролиз, сущность процесса.
10. Произведение растворимости.
1
2.
ТИПЫ РЕАКЦИЙ2
3.
Степень окисления1. Окислительно-восстановительные реакции –
это реакции, сопровождающиеся переходом электронов от одних
атомов или ионов к другим, другими словами – это реакции, в
результате которых изменяются степени окисления элементов.
2. Степень окисления – это заряд атома элемента в соединении,
вычисленный из условного предположения, что все связи в
молекуле являются ионными.
3. Правила определения степеней окисления
0
0
0
0
1 1
0
1 1
H Cl 1... 1 0
NO 3
0
-1
-3
-2
2 1
Na H, Сa H 2 .
H 2 , Cl2 , O 2 , C, Me
1 1
2 1
H 2 O 2 , Ba O 2
2 1
O F2
5 2
( N O 3 ) 1 5 3 ( 2) 1
N 2 , N H 3 , N 2 H 4 , N H 2 OH .
3
4.
Степень окисления4
5.
Окисление и восстановление5
6.
Окисление и восстановление• Число электронов, отдаваемых атомами восстановителя (калия),
равно числу электронов, присоединяемых молекулами
окислителя (хлора). Поэтому одна молекула хлора может
окислить два атома калия.
6
7.
Окислители и восстановители7
8.
Окислители и восстановители8
9.
Окислительно-восстановительнаядвойственность
степень окисления азота в соединениях изменяется в пределах
от (– 3) до (+5)
9
10.
Окислительно-восстановительнаядвойственность
10
11.
Метод электронного баланса11
12.
Ионно-электронный метод(полуреакций)
12
13.
Ионно-электронный метод(полуреакций)
13
14.
Ионно-электронный метод(полуреакций)
14
15.
Ионно-электронный метод(полуреакций)
15
16.
Типы Red/Ox реакций3
3
0
N H N O N 2 4H 2 O
4 2
в ль ок ль
16
17.
Типы Red/Ox реакций17
18.
Типы Red/Ox реакций18
19.
Типы Red/Ox реакций4. Окислительно-восстановительные реакции с участием
более двух элементов изменяющих степень окисления
FeS2 + HNO3 = Fe2(SO4)3 + NO + …
2FeS2+10НNО3 = Fe2(SO4)3 + 10NО + Н2SO4 + 4H2O
19
20.
Влияние факторов20
21.
Влияние факторов21
22.
Влияние факторов22
23.
Энергетикa Red/Ox процессовИтак, если условием самопроизвольного протекания процесса
является неравенство ∆G° < 0, то это возможно, когда n·F·ε° > 0. Если
n и F числа положительные, то необходимо, чтобы ε° > 0, а это
возможно, когда Е°ок > Е°в. Отсюда следует, что условием
самопроизвольного протекания окислительно-восстановительной
реакции является неравенство Е°ок > Е°в
23
24.
Энергетикa Red/Ox процессов24
25.
Энергетикa Red/Ox процессовn 10 (1,52 0,77)
lg K c
127,
0,059
0,059
Кс = 10127
25
26.
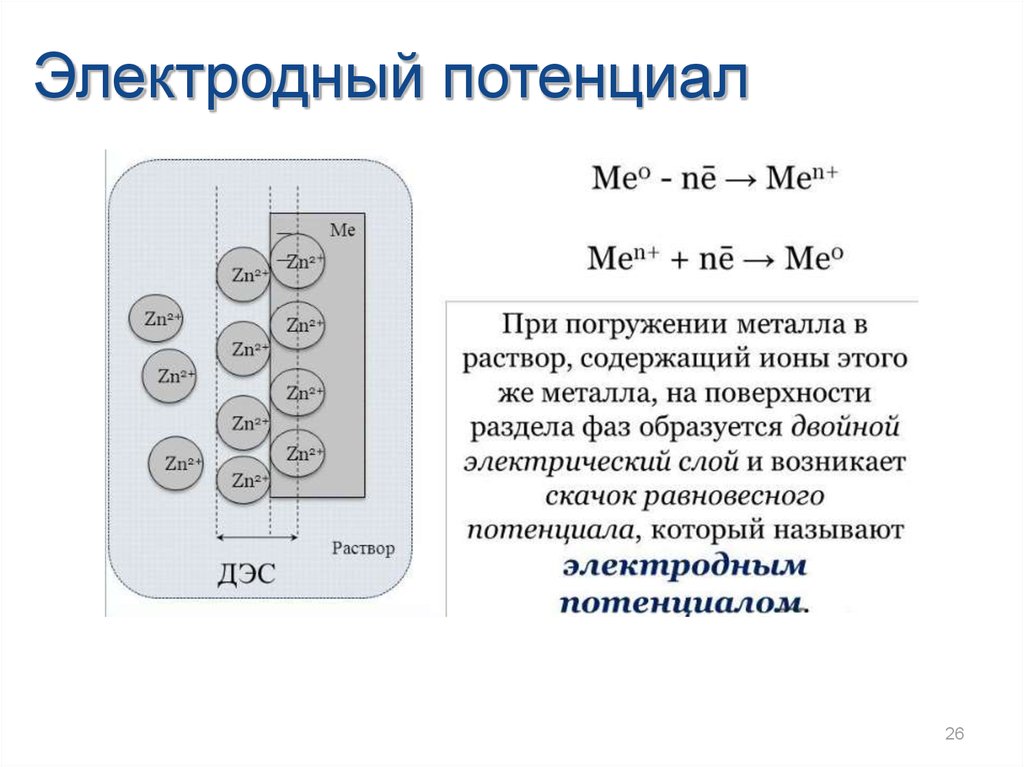
Электродный потенциал26
27.
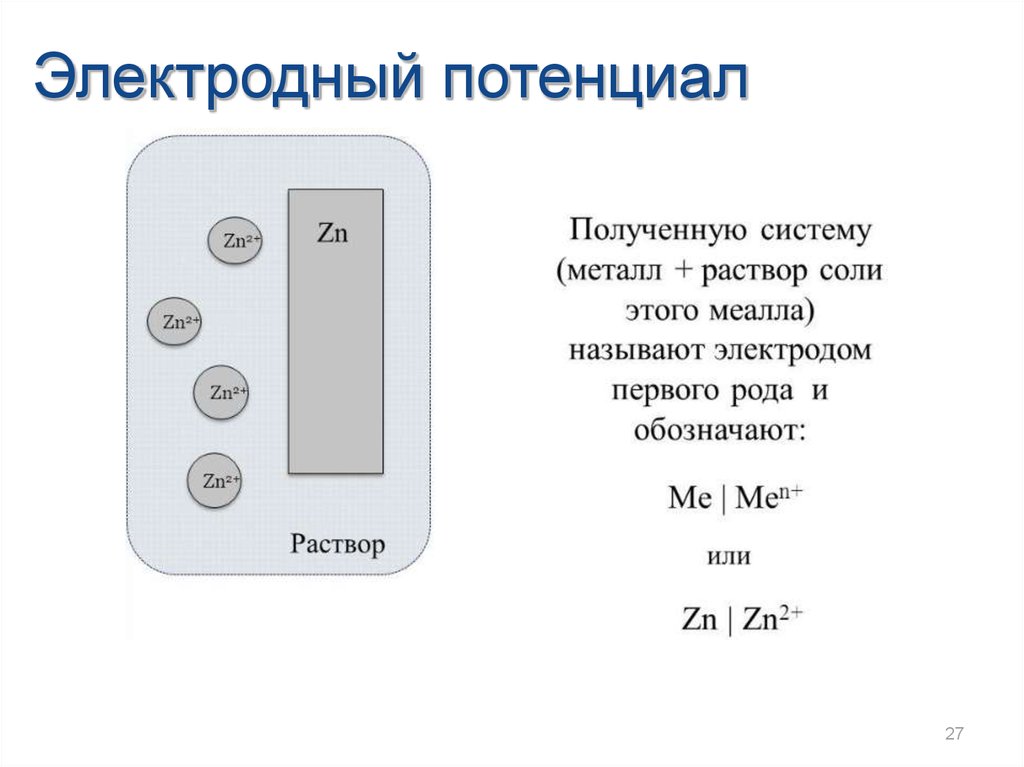
Электродный потенциал27
28.
Электродный потенциал28
29.
Электродный потенциал29
30.
Электродный потенциал30
31.
Электродный потенциал31
32.
Электродный потенциал32
33.
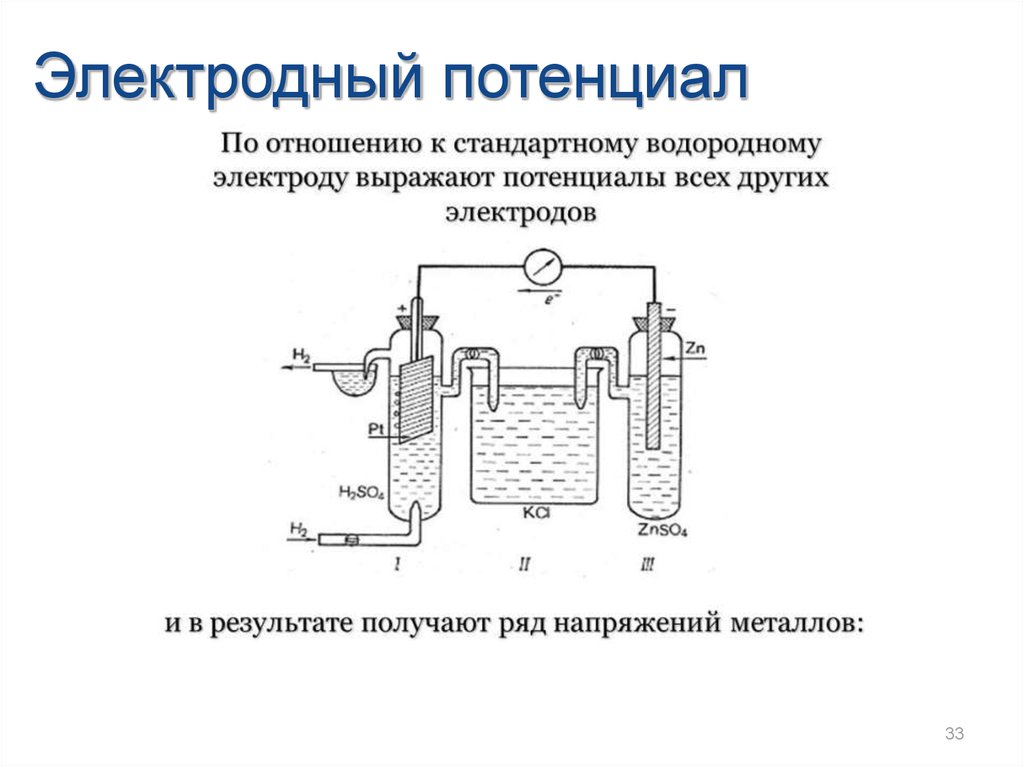
Электродный потенциал33
34.
Электродный потенциал34
35.
Электродный потенциал35
36.
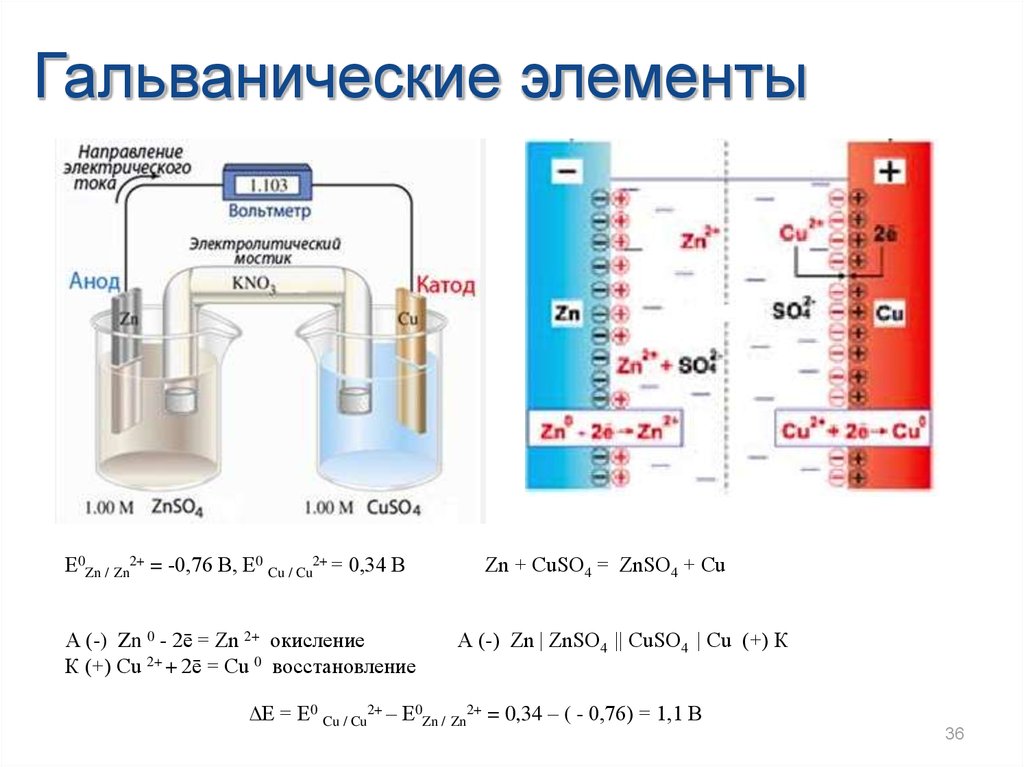
Гальванические элементыЕ0Zn / Zn2+ = -0,76 В, Е0 Cu / Cu2+ = 0,34 В
А (-) Zn 0 - 2ē = Zn 2+ окисление
К (+) Сu 2+ + 2ē = Сu 0 восстановление
Zn + СuSО4 = ZnSО4 + Сu
А (-) Zn | ZnSО4 || СuSО4 | Cu (+) К
∆Е = Е0 Cu / Cu2+ – Е0Zn / Zn2+ = 0,34 – ( - 0,76) = 1,1 В
36
37.
Гальванические элементы∆Е = (0,059 / z) lg C2 / C1
37
38.
ЭлектролизЭлектролиз — физико-химический процесс,
состоящий в выделении на электродах
составных частей растворённых веществ или
других веществ, который возникает при
прохождении электрического тока через раствор
либо расплав электролита
38
39.
Электролиз39
40.
Электролиз1. Электролиз водного раствора соли, образованной активным металлом и бескислородной
кислотой, например, NaCl
2. Электролиз водного раствора соли образованной активным металлом и
кислородосодержащей кислотой
40
41.
Электролиз3. Электролиз водного раствора соли, образованной малоактивным металлом и
кослородосодержащей кислотой
4. Электролиз соли, образованной малоактивным металлом и безкислородной кислотой
41
42.
Электролиз5. Электролиз водного раствора щелочи и кислоты
42
43.
Электролиз6. Электролиз раствора соли малоактивного металла с растворимым анодом
43
44.
Электролиз7. Соль образована металлом, стоящем в раду напряжений после алюминия до водорода
Законы электролиза
m=kQ
(1)
где: m – масса
образовавшегося или
подвергшегося превращениям
вещества, г; Q - количество
электричества, Кл; А-ч. Так
как Q=I*t, то m=kIt, где I сила тока, А;
t – время электролиза, с, ч;
44
45.
Законы электролизадля выделения одного эквивалента вещества необходимо затратить 96484 Кл (26,8
А*ч) электричества. Эту величину называют постоянной Фарадея.
45
46.
Электрохимическая коррозия46
47.
Электрохимическая коррозия47
48.
Электрохимическая коррозия48
49.
Электрохимическая коррозия49
50.
Электрохимическая коррозиядиаграммами Пурбе
50














































 chemistry
chemistry








