Similar presentations:
Биологически важные химические элементы. Неорганические соединения
1. Биологически важные химические элементы. Неорганические соединения
2. Элементарный состав клетки
3. В состав живых организмов входят 24 элемента.
4.
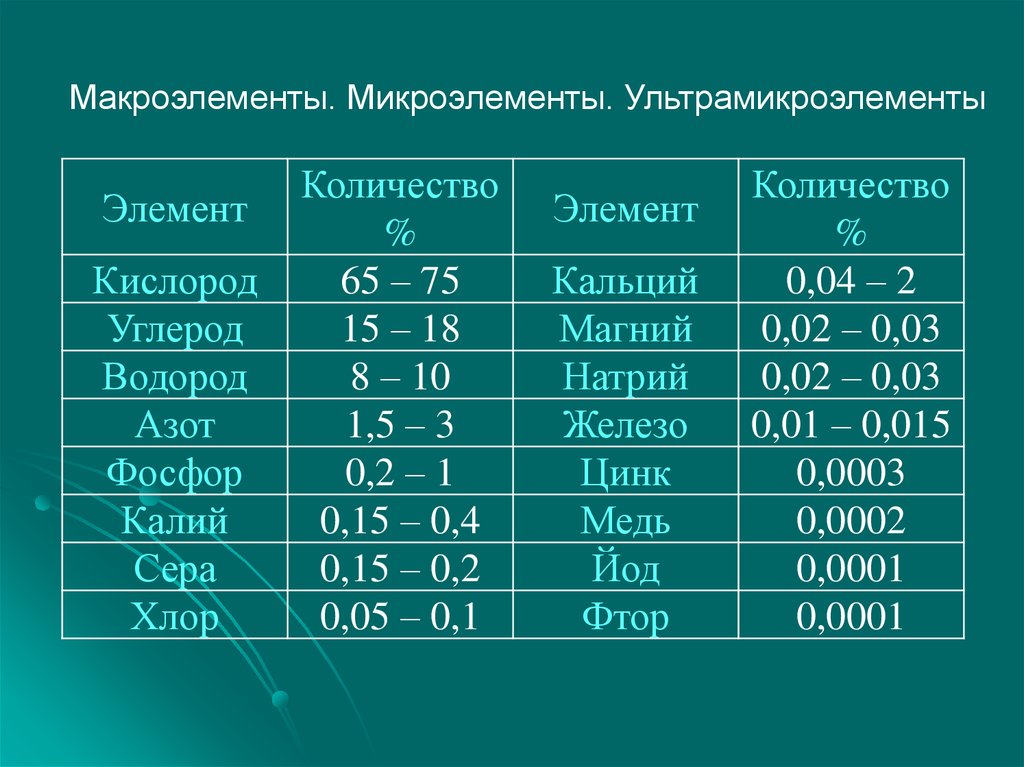
Макроэлементы. Микроэлементы. УльтрамикроэлементыЭлемент
Кислород
Углерод
Водород
Азот
Фосфор
Калий
Сера
Хлор
Количество
%
65 – 75
15 – 18
8 – 10
1,5 – 3
0,2 – 1
0,15 – 0,4
0,15 – 0,2
0,05 – 0,1
Элемент
Кальций
Магний
Натрий
Железо
Цинк
Медь
Йод
Фтор
Количество
%
0,04 – 2
0,02 – 0,03
0,02 – 0,03
0,01 – 0,015
0,0003
0,0002
0,0001
0,0001
5. Элементы
Макроэлементы –элементы, содержание которых в
клетке составляет целые проценты.
На долю 4-х элементов (H, O, C и N)
в сумме приходится почти 98%.
6. Элементы
Микроэлементы –элементы, содержание которых в
клетке составляет десятые и сотые
доли процента.
На долю 8 элементов (P, K, S, Cl, Ca, Mg, Na, Fe)
в сумме приходится 1,9%.
7. Элементы
Ультрамикроэлементы –элементы, содержание которых в
клетке составляет менее тысячной доли
процента.
На долю всех остальных элементов (Zn, Cu, I, F,
Au, Ag, Hg и др.) в сумме приходится
не более 0,01%.
8. Неорганические вещества клетки
9. Минеральные соли
10.
11. Буферностью называют
способность клетки поддерживатьслабощелочную реакцию среды своего
содержимого на постоянном уровне.
Роль буфера в клетке выполняют ионы
НРО42- и Н2РО4-, во внеклеточной
жидкости и в крови – ионы НСО3-
12. Ионы натрия и калия
обеспечивают активный транспортвеществ в клетку.
Во внешней среде (например, в морской
воде, в плазме крови) ионов натрия
всегда больше, чем калия,
а в клетке наоборот.
13. Вода
14. Функции воды
Обеспечивает тургор (упругость)клетки.
Участвует в терморегуляции,
(предохраняет клетку от резких
изменений температуры, от
перегрева и переохлаждения).
Равномерно распределяет тепло
по клетке.
Способствует перемещению
веществ в клетке.
Участвует в химических
реакциях, происходящих в
клетке.
Играет роль растворителя.
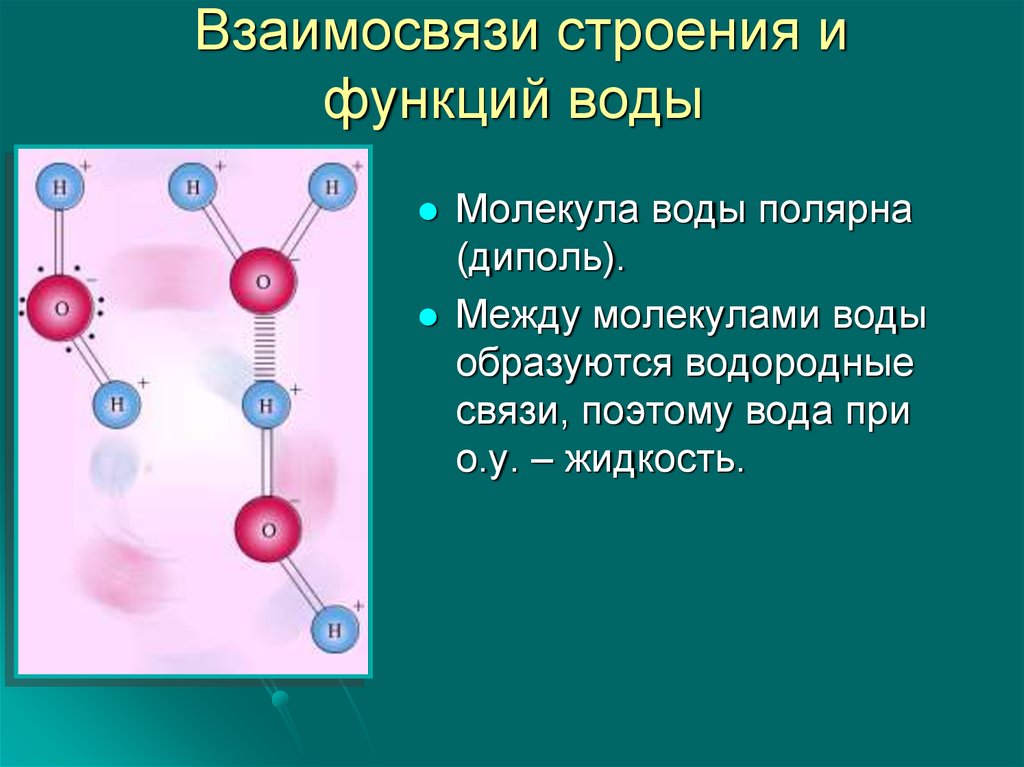
15. Взаимосвязи строения и функций воды
16. Взаимосвязи строения и функций воды
17. Взаимосвязи строения и функций воды
Молекула воды полярна(диполь).
Между молекулами воды
образуются водородные
связи, поэтому вода при
о.у. – жидкость.
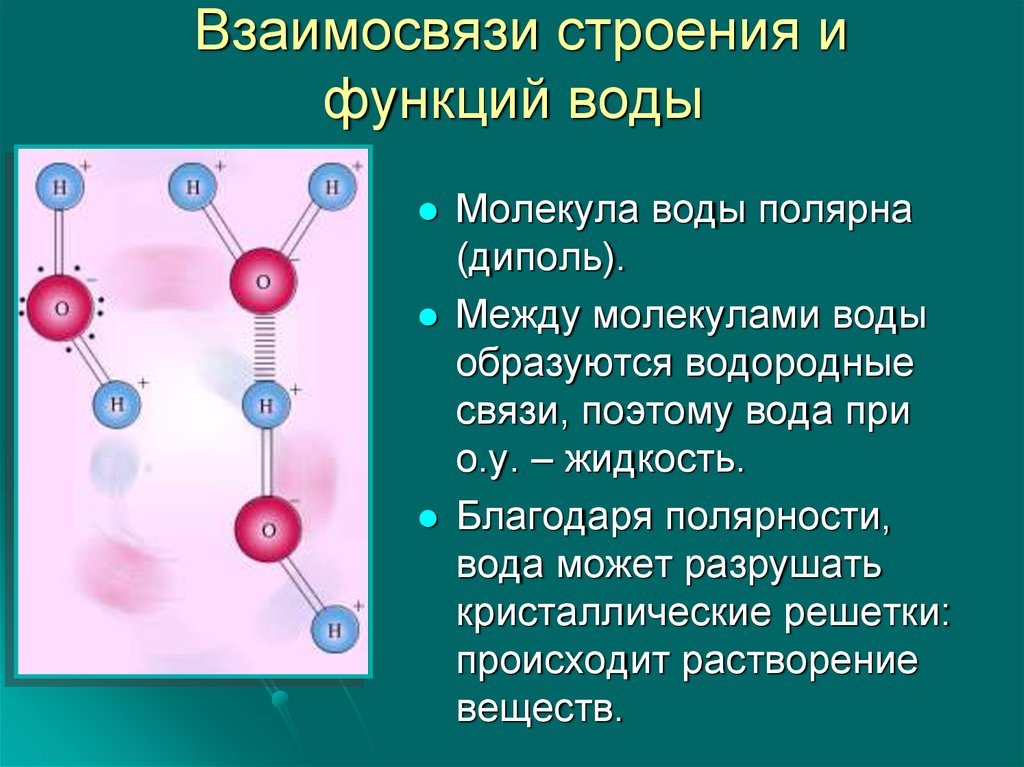
18. Взаимосвязи строения и функций воды
Молекула воды полярна(диполь).
Между молекулами воды
образуются водородные
связи, поэтому вода при
о.у. – жидкость.
Благодаря полярности,
вода может разрушать
кристаллические решетки:
происходит растворение
веществ.
19. Взаимосвязи строения и функций воды
Молекулы воды могутобразовывать водородные
связи с молекулами
некоторых веществ,
благодаря этому данные
вещества растворяются в
воде.
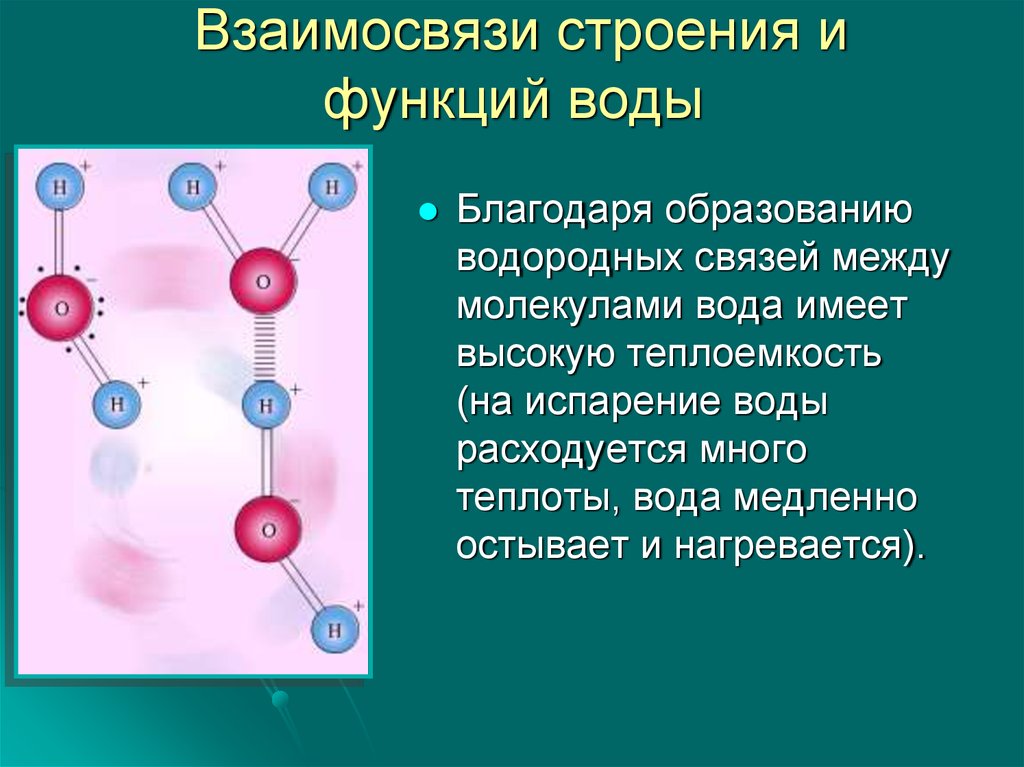
20. Взаимосвязи строения и функций воды
Благодаря образованиюводородных связей между
молекулами вода имеет
высокую теплоемкость
(на испарение воды
расходуется много
теплоты, вода медленно
остывает и нагревается).
21. По отношению к воде вещества бывают:
Гидрофильные (греч. «гидр» и «филио»- любящий воду) –
вещества, растворимые в воде
(некоторые соли, аминокислоты,
некоторые белки, сахар и др.).
Гидрофобные (греч. «гидр» и «фобос» боящийся воды) –
вещества, не растворимые в воде
(жиры, многие белки).
22. Механизмы растворения веществ в воде
Образование водородных связейТак растворяются спирты (молекулы
спирта образуют с диполями воды
водородные связи).
23. Механизмы растворения веществ в воде
Ионный механизмТак разрушаются кристаллические
решетки растворимых солей
(например, NaCl).
24. Механизмы растворения веществ в воде
Донорно-акцепторный механизмТак растворяются аминокислоты,
аммиак.
25. Механизмы растворения веществ в воде
Образование водородных связей.Ионный механизм.
Донорно-акцепторный механизм.
Вода – универсальный
растворитель
26. Задания
1. Какая особенность строения молекулыводы делает ее хорошим
растворителем?
1) хорошая теплопроводность;
2) малые размеры;
3) ионная связь;
4) полярность молекул.
27. Задания
2. Вода играет большую роль в жизниклетки, так как она:
1) участвует во многих химических
реакциях;
2) обеспечивает нейтральную реакцию
среды;
3) ускоряет химические реакции;
4) является источником энергии.
28. Задания
3. В состав клеток всех организмоввходят одни и те же органические
вещества, что служит
доказательством:
1)
2)
3)
4)
единства живой и неживой природы;
единства органического мира;
эволюции органического мира;
приспособленности организмов.
29. Задания
4. Укажите элемент, который не входит вгруппу макроэлементов:
1) О;
2) Р;
3) Н;
4) С.
30. Задания
5. Какие особенности строения и свойствмолекул воды определяют ее большую роль
в клетке?
1) способность образовывать водородные связи;
2) наличие богатых энергией связей;
3) полярность молекул;
4) способность к образованию ионных связей;
5) способность образовывать пептидные связи;
6) способность взаимодействовать с ионами.


























 chemistry
chemistry








