Similar presentations:
Современные методы фармацевтического анализа
1. Современные методы фармацевтического анализа
СОВРЕМЕННЫЕ МЕТОДЫФАРМАЦЕВТИЧЕСКОГО
АНАЛИЗА
Казань, 2017
2. Методы физического и физико-химического анализа (ГФ 13, Том 1)
Методы физического и физикохимического анализа (ГФ 13, Том 1)1.2.1.1. Спектроскопические методы анализа
1.2.1.1.2. Спектрометрия в инфракрасной области (ОФС. 1.2.1.1.0002.15)
1.2.1.1.3. Спектрофотометрия в ультрафиолетовой и видимой областях
(ОФС. 1.2.1.1.0002.15)
1.2.1.2. Хроматографические методы анализа
1.2.1.2.3. Тонкослойная хроматография (ОФС. 1.2.1.2.0003.15)
1.2.1.2.5. Высокоэффективная жидкостная хроматография (ОФС.
1.2.1.2.0005.15)
1.2.1.17. Рефрактометрия (ОФС. 1.2.1. 0017.15)
1.2.1.18. Поляриметрия (ОФС. 1.2.1. 0018.15)
1.4.2. Фармацевтико-технологические испытания лекарственных форм
(ГФ 13, Том 2)
1.4.2.14. Растворение для твердых дозированных лекарственных форм
(ОФС. 1.4.2. 0014.15)
3. Спектроскопические методы анализа
Основанына
избирательном
поглощении
электромагнитного излучения анализируемым веществом и
служат для исследования строения, идентификации и
количественного
определения
светопоглащающих
соединений.
Io
Ii
Io – интенсивность падающего светового потока
Ii – интенсивность светового потока,
прошедшего через раствор
4. Спектроскопические методы анализа
Спектрофотометрия в видимой и УФ-областиСпектрометрия в ИК-области
Атомно-эмиссионная спектрометрия
Атомно-абсорбционная спектроскопия
Флуориметрия
Спектроскопия ядерного магнитного резонанса
Масс-спектрометрия
Рамановская спектрометрия
Рентгеновская флуоресцентная спектрометрия
Ренгеновская порошковая дифрактометрия
5. Спектрофотометрия в УФ- и видимой областях
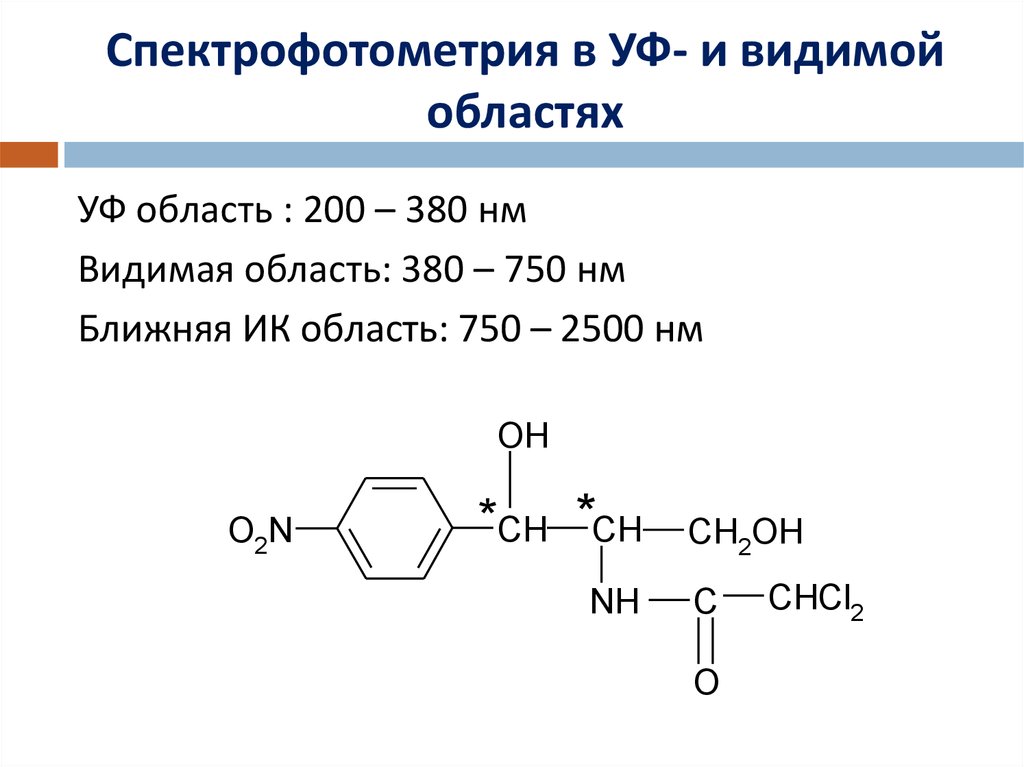
УФ область : 200 – 380 нмВидимая область: 380 – 750 нм
Ближняя ИК область: 750 – 2500 нм
OH
O2N
*CH *CH
NH
CH2OH
C
O
CHCl2
6. Спектрофотометрия в УФ- и видимой областях
Закон Бугера-Ламберта-Бера:А= ·l·С
А - оптическая плотность
- молярный показатель поглощения
l – длина оптического пути или толщина слоя, см
С – молярная концентрация вещества в растворе
Оптическая плотность раствора прямо пропорциональна
толщине поглощающего слоя и концентрации
7. Спектрофотометрия в УФ- и видимой областях
Удельный показатель погашения Е1% - оптическая плотность 1%раствора при толщине поглощающего слоя 1 см
Молярный показатель погашения - оптическая плотность
одномолярного раствора при толщине поглощающего слоя 1 см
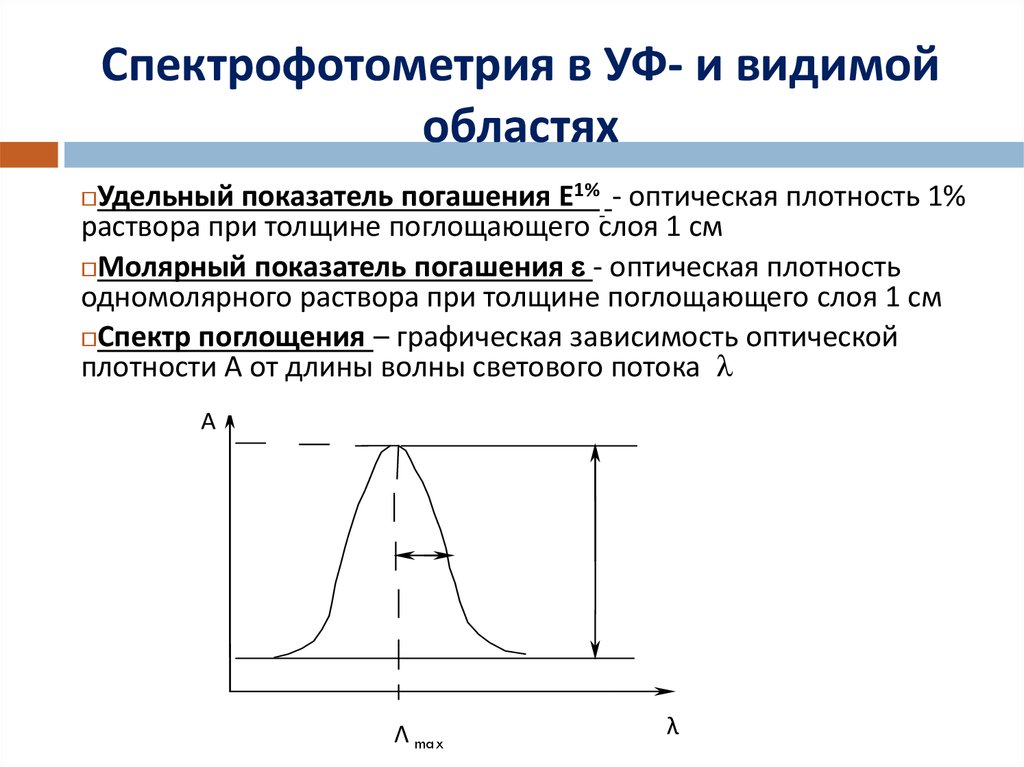
Спектр поглощения – графическая зависимость оптической
плотности А от длины волны светового потока
А
Λ max
λ
8. Спектрофотометрия в УФ- и видимой областях
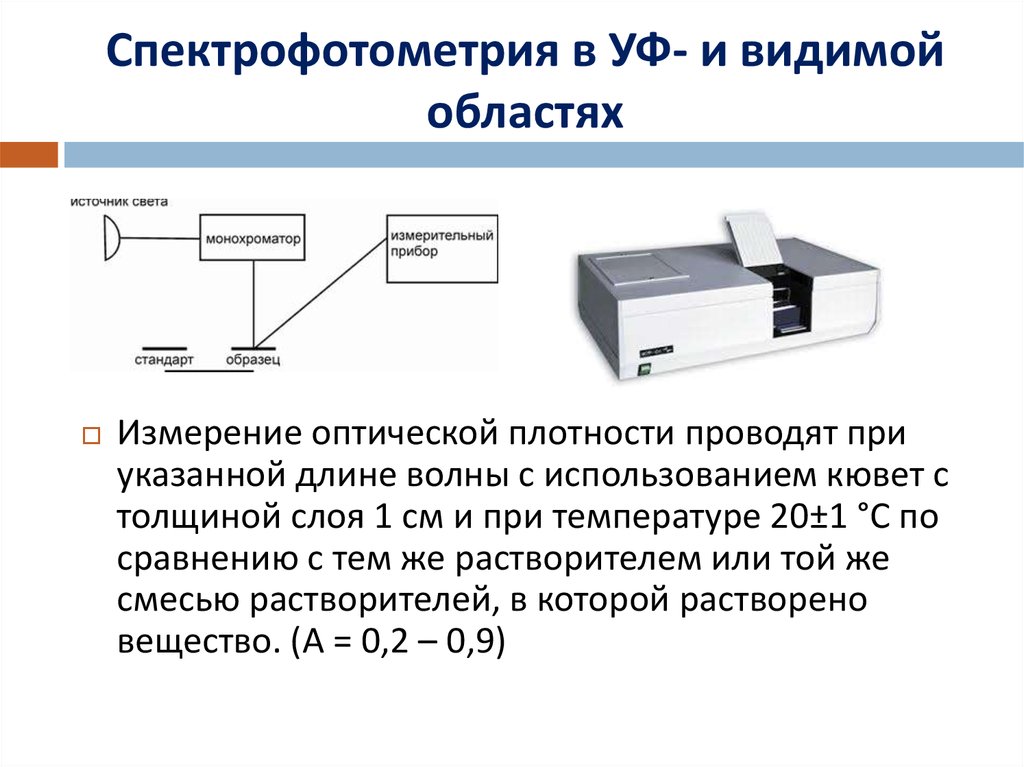
Измерение оптической плотности проводят приуказанной длине волны с использованием кювет с
толщиной слоя 1 см и при температуре 20±1 °С по
сравнению с тем же растворителем или той же
смесью растворителей, в которой растворено
вещество. (А = 0,2 – 0,9)
9. Спектрофотометрия в УФ- и видимой областях. Идентификация:
Сравнение спектров поглощения испытуемогораствора
и
раствора
стандартного
образца(совпадение положений максимумов,
минимумов, плеч и точек перегиба);
Указания положений максимумов, минимумов,
плеч и точек перегиба спектра поглощения
испытуемого раствора (расхождение не должно
превышать ± 2 нм)
10. Спектрофотометрия в УФ- и видимой областях. Количественное определение:
По градуировочному графикуС использованием стандартного образца
Аст
Сст
—— = ——
Ах
Сх
С использованием показателя поглощения
Ах
Сх = ———
·l
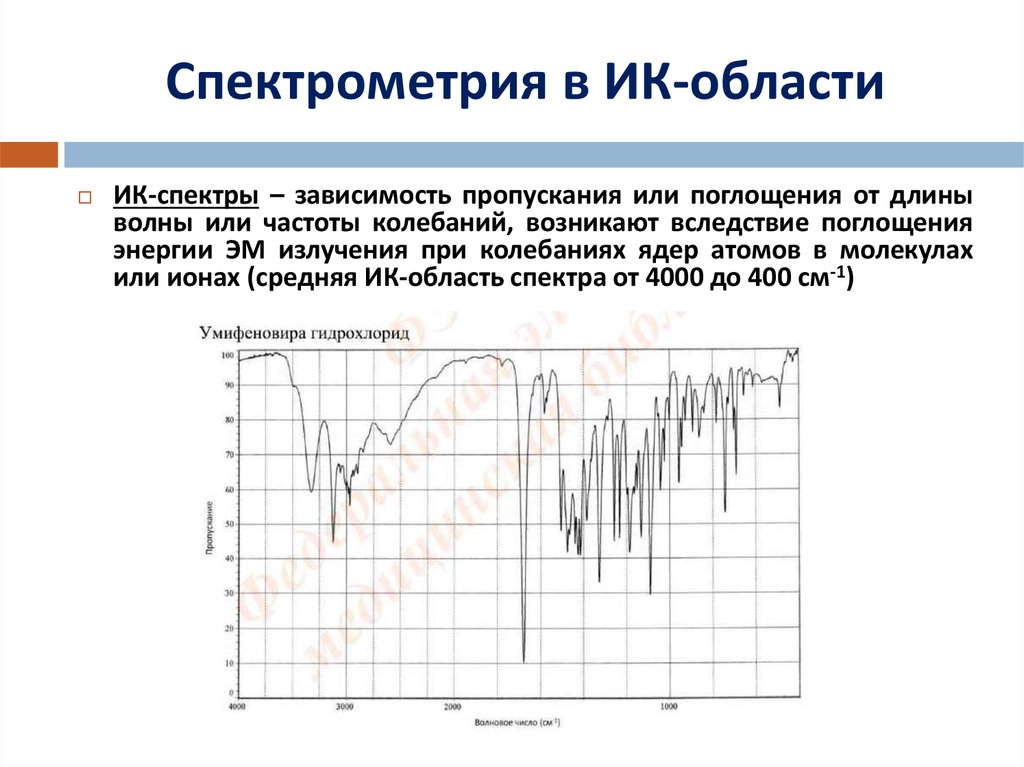
11. Спектрометрия в ИК-области
ИК-спектры – зависимость пропускания или поглощения от длиныволны или частоты колебаний, возникают вследствие поглощения
энергии ЭМ излучения при колебаниях ядер атомов в молекулах
или ионах (средняя ИК-область спектра от 4000 до 400 см-1)
12. Спектрометрия в ИК-области. Подготовка образца.
Жидкости: в форме пленки между двумяпластинками или в кювете;
Твердые вещества: диски с калия бромидом
или суспензия в вазелиновом масле
Метод нарушенного полного внутреннего
отражения
13. Спектрометрия в ИК-области. Идентификация.
С использованием стандартного образца(полосы поглощения в спектре испытуемого
образца должны полностью соответствовать по
положению полосам поглощения в спектре
стандартного образца)
С использованием эталонных спектров
14. Методы физического и физико-химического анализа (ГФ 13, Том 1)
Методы физического и физикохимического анализа (ГФ 13, Том 1)1.2.1.1. Спектроскопические методы анализа
1.2.1.1.2. Спектрометрия в инфракрасной области (ОФС. 1.2.1.1.0002.15)
1.2.1.1.3. Спектрофотометрия в ультрафиолетовой и видимой областях
(ОФС. 1.2.1.1.0002.15)
1.2.1.2. Хроматографические методы анализа
1.2.1.2.3. Тонкослойная хроматография (ОФС. 1.2.1.2.0003.15)
1.2.1.2.5. Высокоэффективная жидкостная хроматография (ОФС.
1.2.1.2.0005.15)
1.2.1.17. Рефрактометрия (ОФС. 1.2.1. 0017.15)
1.2.1.18. Поляриметрия (ОФС. 1.2.1. 0018.15)
1.4.2. Фармацевтико-технологические испытания лекарственных форм
(ГФ 13, Том 2)
1.4.2.14. Растворение для твердых дозированных лекарственных форм
(ОФС. 1.4.2. 0014.15)
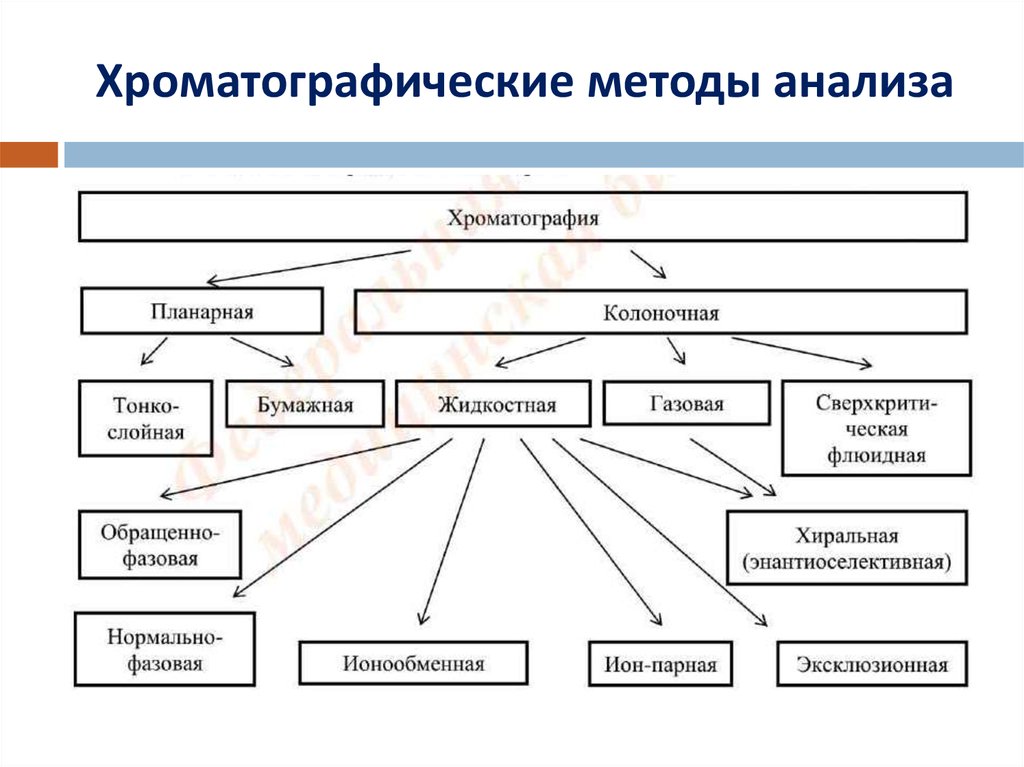
15. Хроматографические методы анализа
Хроматография – метод разделения смесейвеществ , основанный на их многократном
перераспределении
между
двумя
контактирующими фазами, одна из которых
неподвижна, а другая имеет постоянное
направление движения.
16. Хроматографические методы анализа
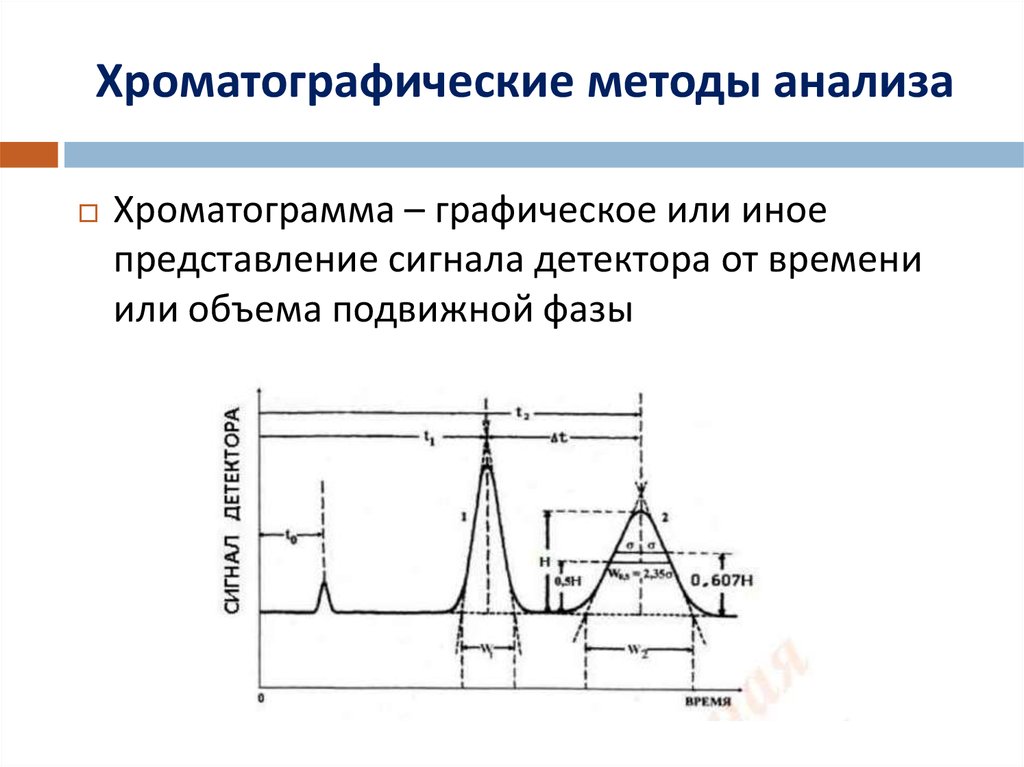
17. Хроматографические методы анализа
Хроматограмма – графическое или иноепредставление сигнала детектора от времени
или объема подвижной фазы
18. Хроматографические методы анализа
Базовая линия – сигнал от подвижной фазыПик – часть хроматограммы, регистрирующая отклик детектора
Основание пика – продолжение базовой линии, соединяющее начало и коне пика
Площадь пика – площадь хроматограммы, заключенная между кривой, описывающей
пик, и его основанием
Высота пика – расстояние от максимума пика до его основания, измеренное
параллельно оси отклика детектора
Время удерживания – время, необходимое для элюирования вещества. Соответствует
времени появления максимума пика на хроматограмме.
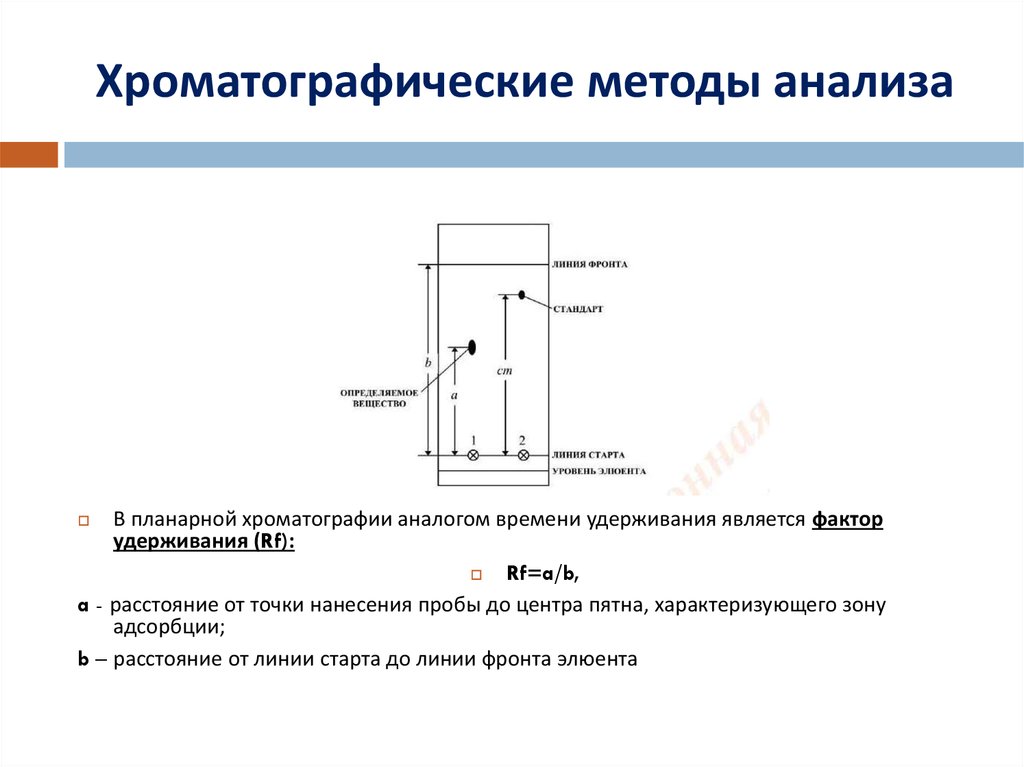
19. Хроматографические методы анализа
В планарной хроматографии аналогом времени удерживания является факторудерживания (Rf):
Rf=a/b,
a - расстояние от точки нанесения пробы до центра пятна, характеризующего зону
адсорбции;
b – расстояние от линии старта до линии фронта элюента
20. Расчет содержания определяемых веществ
1. Метод нормирования (метод внутреннейнормализации). Основан на предположении,
что на хроматограмме зарегистрированы все
вещества, входящие в состав анализируемой
смеси, и что доля площади каждого пика от
суммы площадей всех пиков соответствует
содержанию вещества в массовых процентах.
21. Расчет содержания определяемых веществ
2. Метод внешнего стандарта. Концентрациюиспытуемого вещества определяют путем
сравнения сигнала (пика), полученного на
хроматограммах
испытуемого
раствора,
сигнала, полученного на хроматограммах
раствора стандартного образца.
22. Расчет содержания определяемых веществ
3. Метод внутреннего стандарта. Основан на введении в анализируемуюсмесь определенного количества стандартного вещества (внутренний
стандарт). В испытуемый и стандартные растворы вводят известные
количества внутреннего стандарта, хроматографируют растворы и
определяют отношения площадей пиков определяемого вещества к площади
пика внутреннего стандарта в испытуемом и стандартном растворах.
23. Расчет содержания определяемых веществ
4. Метод стандартных добавок. Основан на введении ванализируемую
смесь
известного
количества
определяемого вещества и сравнении сигналов,
полученных для испытуемого раствора со стандартной
добавкой и без добавки определяемого вещества.
24. Высокоэффективная жидкостная хроматография
ВЭЖХ – метод колоночной хроматографии, в котором подвижной фазой служитжидкость, движущаяся через хроматографическую колонку, заполненную
неподвижной фазой (сорбентом).
Варианты:
Адсорбционная – разделение веществ за счет различной способности адсорбироваться
и десорбироваться с поверхности сорбента.
Распределительная - разделение веществ за счет различия коэффициентов
распределения между неподвижной и подвижной фазами.
Нормально-фазовая – неподвижная фаза – полярная, подвижная – неполярная
Обращенно-фазовая – неподвижная фаза – неполярная, подвижная фаза – полярная.
Ионообменная – разделение смеси веществ, диссоциированных в растворе на ионы, за
счет различной силы взаимодействия определяемых ионов с ионными группами
сорбента
Эксклюзионная (ситовая, гель-проникающая, гель-фильтрационная) – молекулы
веществ разделяются по размеру за счет их разной способности проникать в поры
неподвижной фазы.
Хиральная – разделение оптически активных соединений.
25. ВЭЖХ. Область применения
«Подлинность»«Посторонние примеси»
«Растворение»
«Однородность дозирования»
«Количественное определение»
26. ВЭЖХ. Оборудование
Узел подготовки подвижной фазыНасосная система
Смеситель подвижной фазы
Система ввода пробы (инжектор)
Хроматографическая колонка
Детектор
Система управления хроматографом, сбора и
обработки данных
27. Высокоэффективная жидкостная хроматография
Полное коммерческое наименование колонки суказанием производителя
Размеры колонки
Тип сорбента с указанием размера частиц
Температура колонки
Объем вводимой пробы
Состав подвижной фазы
Скорость подачи подвижной фазы
Типе детектора
Время хроматографирования
28. Методы физического и физико-химического анализа (ГФ 13, Том 1)
Методы физического и физикохимического анализа (ГФ 13, Том 1)1.2.1.1. Спектроскопические методы анализа
1.2.1.1.2. Спектрометрия в инфракрасной области (ОФС. 1.2.1.1.0002.15)
1.2.1.1.3. Спектрофотометрия в ультрафиолетовой и видимой областях
(ОФС. 1.2.1.1.0002.15)
1.2.1.2. Хроматографические методы анализа
1.2.1.2.3. Тонкослойная хроматография (ОФС. 1.2.1.2.0003.15)
1.2.1.2.5. Высокоэффективная жидкостная хроматография (ОФС.
1.2.1.2.0005.15)
1.2.1.17. Рефрактометрия (ОФС. 1.2.1. 0017.15)
1.2.1.18. Поляриметрия (ОФС. 1.2.1. 0018.15)
1.4.2. Фармацевтико-технологические испытания лекарственных форм
(ГФ 13, Том 2)
1.4.2.14. Растворение для твердых дозированных лекарственных форм
(ОФС. 1.4.2. 0014.15)
29. Тест «Растворение»
Определение количества действующего вещества,которое в условиях, указанных в фармакопейной
статье или нормативной документации, за
определенный промежуток времени должно
высвобождаться в среду растворения из твердой
дозированной лекарственной формы.
Проводится при контроле качества лекарственной
формы для подтверждения постоянства ее свойств
и
надлежащих
условий
производственного
процесса
30. Тест «Растворение»
Аппарат I «Вращающаяся корзинка»Аппарат II «Лопастная мешалка»
Сосуд для растворения с
полусферическим дном
Двигатель
Перемешивающий элемент
Термостат – водяная баня (37±0,5°С)
31. Тест «Растворение»
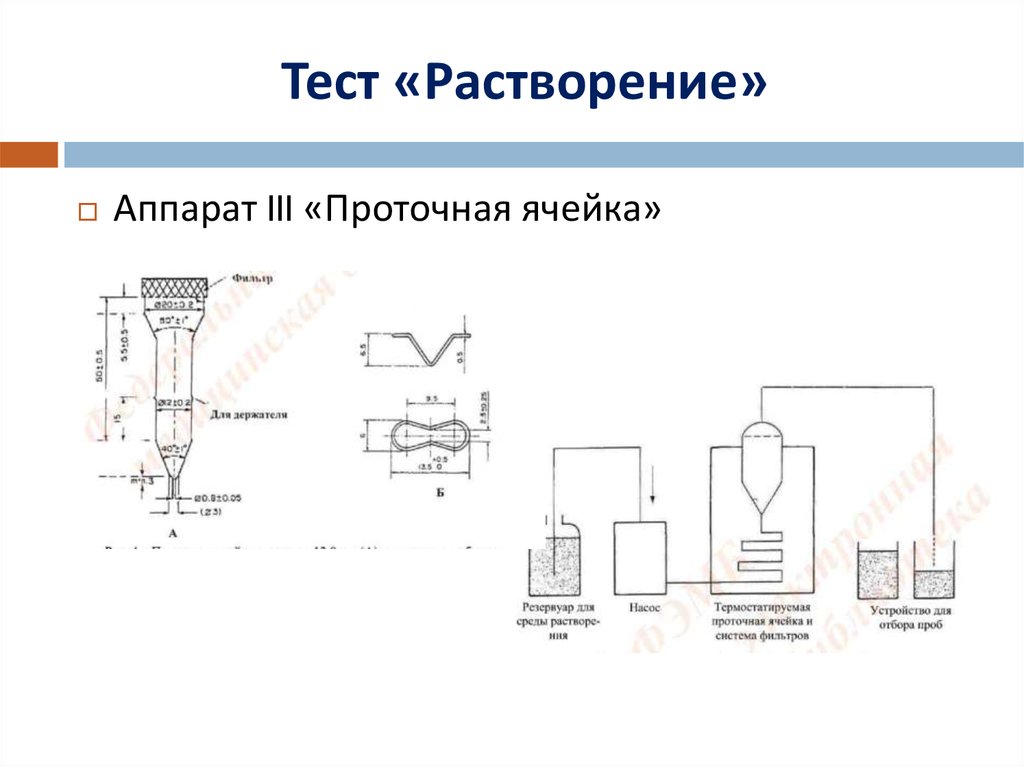
Аппарат III «Проточная ячейка»32. Тест «Растворение»
33. Тест «Растворение»
Вода очищеннаяРаствор хлористоводородной кислоты 0,1М
Буферные растворы с рН 6,8 – 7,8
Другие растворы, указанные в ФС или НД
Объем среды 900 мл
Температура 37±0,5°С
Деаэрация
Скорость вращения 100 об/мин (вращающаяся
корзинка), 50 об/мин (лопастная мешалка),
скорость потока – 4, 8 или 16 мл/мин (проточная
ячейка)
























 medicine
medicine physics
physics chemistry
chemistry








