Similar presentations:
Лабораторная диагностика ВИЧ инфекции
1. Лабораторная диагностика ВИЧ инфекции
Зав. КДЛ: Т.Н. ЕмельяноваУльяновск 2014
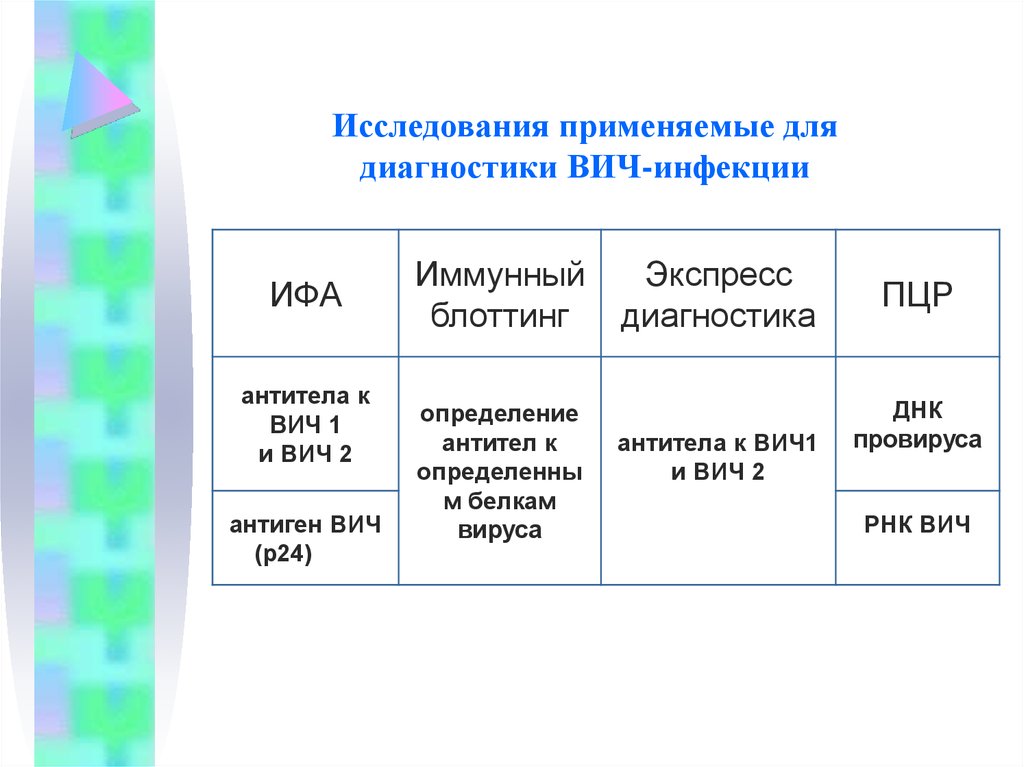
2. Исследования применяемые для диагностики ВИЧ-инфекции
ИФАантитела к
ВИЧ 1
и ВИЧ 2
антиген ВИЧ
(р24)
Иммунный
блоттинг
определение
антител к
определенны
м белкам
вируса
Экспресс
диагностика
антитела к ВИЧ1
и ВИЧ 2
ПЦР
ДНК
провируса
РНК ВИЧ
3. Иммуноферментный анализ
Использование тест-систем 4 поколенияпозволяет одновременно определять как
антитела к ВИЧ 1-го и 2-го типа, так и
антигены (р 24).
1 этап – скрининговый
2 этап – референтный
3 этап – экспертный
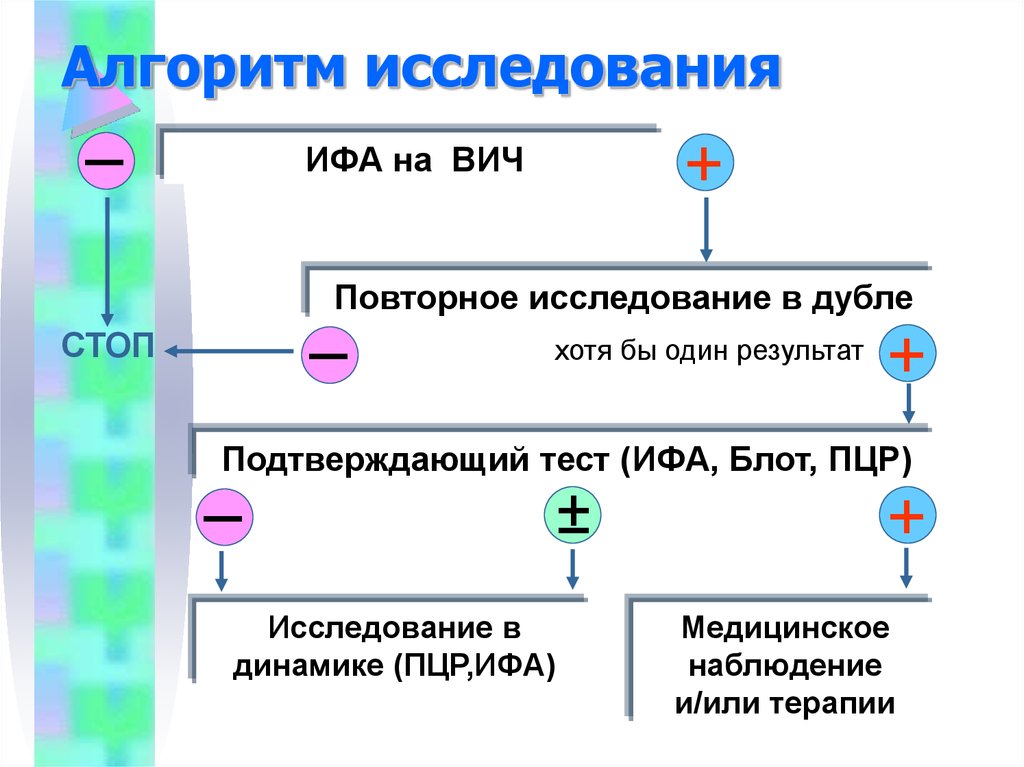
4. Алгоритм исследования
–+
ИФА на ВИЧ
Повторное исследование в дубле
–
СТОП
хотя бы один результат
+
Подтверждающий тест (ИФА, Блот, ПЦР)
–
Исследование в
динамике (ПЦР,ИФА)
±
+
Медицинское
наблюдение
и/или терапии
5.
Иммунные реакции – это специфические реакции связывания
антигена с антителом с образованием иммунного комплекса.
Двух одинаковых копий индивидуальных антигенов в природе
не существует! В диагностике используют только один вид антител,
который наиболее специфичен в отношении определяемого
возбудителя. То есть связывание данного вида антител с
определяемым антигеном происходит всегда. Чаще всего
применяются IgG и IgM.
Именно этот принцип иммунной реакции (уникальная точность и
специфичность узнавания определяемого биологического объекта)
лежит в основе иммуноферментного анализа.В силу высокой
точности антител в узнавании антигенов, точность всего метода
иммуноферментного анализа оказывается также высочайшей.
6. Иммунный блоттинг
Обозначение ГеномGp 160
ENV
Gp 120
P 68/66
ENV
POL
Р55
GAG
Р52/51
POL
Gp 41
ENV
Р 40
GAG
Р 34/31
Р 24/25
Р18/17
POL
GAG
GAG
Природа
Гликопротеин
предшественник Gp 120 и
Gp41
Гликопротеин оболочки
Обратная транскриптаза
Предшественник ядерных
белков
Обратная транскриптаза
Трансмембранный
гликопротеин
Предшественник ядерных
белков
эндонуклеаза
Ядерный белок
Ядерный белок
7. Интерпретация результатов ИБ
интерпретацияпрофиль
Положительный
2ENV+/- GAG+/POL
Неопределенны
й
ENV +/-GAG+/POL или GAG+
POL
или GAG
илиPOL
Отрицательный
Полосы
отсутствуют
вообще,
нет
специфических
полос
8. Антиген р 24
Заявленная чувствительность тест-систем0,5 пг/мл
• Антиген р24 может быть выявлен в крови методом
иммуноферментного анализа уже через 1-2 недели
после заражения и определяться до 8-й недели, затем
его содержание резко снижается.
• Далее в клиническом течении ВИЧ-инфекции
отмечается второй подъем содержания в крови белка р
24. Он приходится на период формирования СПИД.
9. Полимеразная цепная реакция - ДНК
Обнаружение ДНК провируса ВИЧ в мононуклеарныхклетках периферической крови. Используется как
диагностическая методика для прямой диагностики
ВИЧ-инфекции в следующих случаях:
• При обследовании детей, родившихся от ВИЧинфицированных матерей. Использование ПЦР в
этом случае позволяет сократить сроки постановки
диагноза ВИЧ-инфекции с 18 месяцев до 3-6 месяцев.
• В случае сомнительного результата ИБ.
• В период серологического "окна".
10.
Обнаружение РНК ВИЧ -«вирусная нагрузка».• Используется для количественного измерения
концентрации вируса в крови с целью прогноза и
мониторинга уже установленной ВИЧ-инфекции.
• Вирусная нагрузка отражает интенсивность
репликативного процесса в инфицированных клетках.
• ВН при первичной инфекции высокая и находится в
интервале 104-106, но с началом сероконверсии
содержание РНК в плазме крови начинает резко
снижаться вплоть до уровня, не выявляемого обычными
методами
11. Иммунный статус
Подсчёт CD4+ лимфоцитов являетсякритическим параметром в мониторинге
ВИЧ-инфекции и позволяет:
• Оценивать состояние иммунной системы.
• Наряду с клинической информацией определять
момент начала антиретровирусной терапии.
• Определять сроки для профилактики
оппортунистических инфекций .
• Оценивать эффективность лечения.
12. Экспресс диагностика ВИЧ
13.
проточный Цитофлюориметр«Citomics FC500»
ПЦМ позволяет проводить иммунофенотипирование
любых клеток, к поверхностным или внутренним
антигенам которых получены моноклональные
антитела
14.
Амплификатор в режиме реального времени “Abbottm2000rt”
15.
Станции пробоподготовки позволяютавтоматически подготовить пробы к
измерению и свести ручной труд к
минимуму.
16.
Скорость, достоверность, воспроизводимость, точность,информативность и объективность полученных ПЦМ
цитологических характеристик настолько высоки, что
существующие сегодня другие методы оценки иммуногенетических
и фенотипических свойств клеток не могут серьезно конкурировать
17. Факторы, влияющие на результаты диагностики
• выбор соответствующего метода лабораторногоисследования;
• правильная подготовка пациента к исследованию;
• правильный забор крови;
• правильная предварительная подготовка крови и
своевременное проведение исследований;
• правильное хранение и доставка материала в
лабораторию;
• материально-техническое обеспечение
лабораторного исследования;
• уровень квалификации медицинского персонала,
проводящего исследование.
18. ПОДГОТОВКА ОБРАЗЦОВ
Сыворотка крови.• Завершённое формирование фибринового сгустка
(фибрин – источник ложноположительных результатов)
• Исключение возможности контаминации одного образца
другим (использование индивидуальных палочек или наконечников для
обведения сгустка, использование закрывающихся пробирок при
транспортировке).
• Сыворотки должны быть прозрачными, без признаков
хилёза, гемолиза, «проростов», клеточной взвеси.
Плазма.
• Должна быть свободна от тромбоцитов.
• Сроки хранения: На ИС 48 часов при комнатной
температуре в темном месте.
• На ИФА : сыворотка хранится в холодильнике не более 7
суток.
• На ВН : если плазма не исследуется сразу, то должна быть
заморожена при t – 20 град.
19. Для повышения уровня качества исследований, проводимых в лаборатории необходимо:
• Регулярно участвовать в системах внешнейоценки качества;
• для оценки правильности проводимых
исследований применять стандартные
контрольные материалы;
• для оценки воспроизводимости исследований
проводить внутрилабораторный контроль
качества каждой постановки ИФА, с последующим
построением контрольной карты и анализом
полученных результатов;
• постоянное повышать квалификацию персонала;
• строго соблюдать инструкции к тест-системам


















 medicine
medicine