Similar presentations:
Антимикробные лекарстенные средства
1. Кафедра фармакологии
АНТИМИКРОБНЫЕЛЕКАРСТЕННЫЕ СРЕДСТВА:
• АНТИБАКТЕРИАЛЬНЫЕ
•АНТИМИКОБАКТЕРИАЛЬНЫЕ
•ПРОТИВОГРИБКОВЫЕ
•ПРОТИВОВИРУСНЫЕ
•АНТИПРОТОЗОЙНЫЕ
2. ОСОБЕННОСТИ АНТИМИКРОБНЫХ СРЕДСТВ
• В отличие от большинства других ЛС,мишень (рецептор) для антимикробного
препарата находится не в тканях
человека, а в клетке микроорганизма.
3. ОСОБЕННОСТИ АНТИМИКРОБНЫХ СРЕДСТВ
• Активность антимикробных ЛС непостоянна,что
обусловлено
развитием
устойчивости
(резистентности)–
неизбежное
биологическое
явление
обусловленное высокими адаптационными
способностями
микроорганизмов
и
предотвратить ее на современном этапе
практически
невозможно !
4. Особенности появления антимикробных средств
• ПРОБЛЕМА: Пандемия стрептокковыхинфекций ХIХ-XX вв.
Сульфаниламиды
Пенициллин
• ПРОБЛЕМА: Неэффективность
пенициллина против стафилококков,
продуцируюших пенициллиназу
Оксациллин
5. Особенности появления антимикробных средств
• ПРОБЛЕМА: Аллергия/анафилаксия напенициллины
Цефалоспорины I-II поколения
• ПРОБЛЕМА: актуализация Гр(-)флоры
Аминогликозиды, защищенные
пенициллины, цефалоспорины III
поколения
6. Особенности появления антимикробных средств
• ПРОБЛЕМА: Появление резистентныхГр(-) неферментирующих бактерий
Карбапенемы, цефалоспорины IV
поколения,тигециклин
• ПРОБЛЕМА: Появление Гр(+)
резистентной флоры
Линезолид, даптомицин,
цефтобипрол и др.
7. Ключева проблема антимикробных средств
• ПРОБЛЕМА:Появление панрезистентной флоры
(приближается время некурабельных
инфекций?)
Улучшение ФД/ФК,
повышение дозировок,
новые комбинации антимикробных
средств ?
8. ВОЗ сообщила о вступлении мира в пост-антибиотиковую эру : http://medportal.ru/mednovosti/news/2014/05/05/191who/ (май 2014 г.)
ВОЗ сообщила о вступлении мирав пост-антибиотиковую эру :
http://medportal.ru/mednovosti/news/2014/05/05/191who/ (май 2014 г.)
• Устойчивость к карбапенемам Klebsiella pneumoniae,
вызывающей внутрибольничные инфекции –
пневмонию, сепсис, инфекции у новорожденных и
пациентов отделений реанимации.
• По данным ВОЗ, в некоторых странах мира
карбапенемы не работают более, чем в
половине случаев инфицирования Klebsiella
pneumoniae.
9. ВОЗ сообщила о вступлении мира в пост-антибиотиковую эру : http://medportal.ru/mednovosti/news/2014/05/05/191who/ (май 2014 г.)
ВОЗ сообщила о вступлении мирав пост-антибиотиковую эру :
http://medportal.ru/mednovosti/news/2014/05/05/191who/ (май 2014 г.)
• Серьезную опасность представляет возбудитель
инфекций мочевыводящих путей Escherichia coli,
устойчивая к одному из самых широко
распространенных классов
противобактериальных средств фторхинолонам. В 1980-х годах, когда они были
впервые введены в клиническую практику,
устойчивость к ним практически равнялась нулю.
Сегодня во многих регионах мира фторхинолоны
неэффективны более, чем в половине случаев.
10. ВОЗ сообщила о вступлении мира в пост-антибиотиковую эру : http://medportal.ru/mednovosti/news/2014/05/05/191who/(май 2014 г.)
ВОЗ сообщила о вступлении мирав пост-антибиотиковую эру :
http://medportal.ru/mednovosti/news/2014/05/05/191who/(май 2014 г.)
• Еще одним предметом беспокойства авторов
доклада является рост устойчивости возбудителя
гонореи Neisseria gonorrhoeae к цефалоспоринам
третьего поколения, назначаемым обычно в
качестве средства «крайней меры». Эта тенденция
подтверждена в Австралии, Австрии, Канаде,
Норвегии, Словении, Соединенном Королевстве,
Швеции, Франции, Южной Африке и Японии. При
этом ежедневно в мире гонореей заражается более
одного миллиона человек, отмечается в докладе
ВОЗ.
11. Мультирезистентные штаммы (MDR)
MDRPs.aeruginosae
Европейское региональное
бюро ВОЗ - в 29 странах
Европейского региона
ежегодно умирают 25000
человек в результате
устойчивых к антибиотикам
инфекций (10.06.2011)!
MDR
Kl.pneumoniae
MDR
Acinetobacter
MRSA
VRE
12.
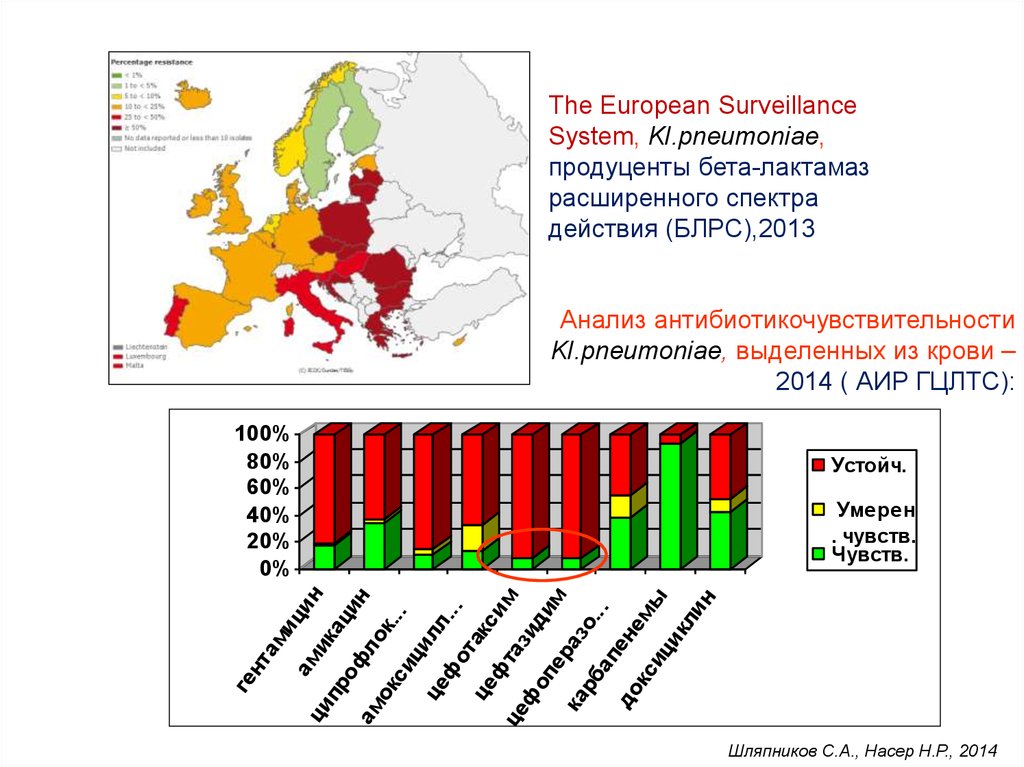
The European SurveillanceSystem, Kl.pneumoniae,
продуценты бета-лактамаз
расширенного спектра
действия (БЛРС),2013
Анализ антибиотикочувствительности
Kl.pneumoniae, выделенных из крови –
2014 ( АИР ГЦЛТС):
Устойч.
Умерен
. чувств.
Чувств.
ге
нт
а
ми
ам ци н
ци
ик
пр
а
о ф цин
ам
ло
ок
к..
си
.
ци
лл
це
ф
.
от . .
ак
це
си
ф
т
це
аз м
ф
оп иди
м
ер
а
ка
рб зо..
.
ап
е
до
не
кс
мы
иц
ик
ли
н
100%
80%
60%
40%
20%
0%
Шляпников С.А., Насер Н.Р., 2014
13. АНТИБИОТИКИ:
• Вещества биологического происхождения,продуцируемые плесневыми грибами,
лучистыми грибами (актиномицетами) и
некоторыми бактериями, а также их
производные и синтетические аналоги,
обладающие способностью избирательно
подавлять в организме больного
возбудителей различных инфекционных
заболеваний.
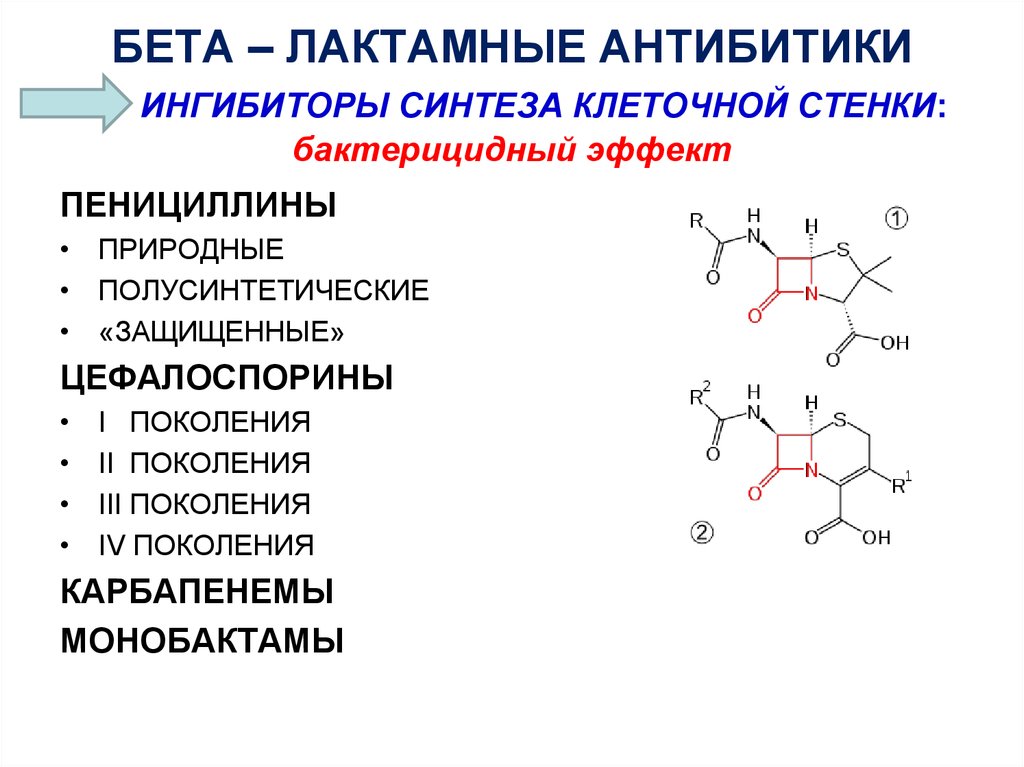
14. БЕТА – ЛАКТАМНЫЕ АНТИБИТИКИ ИНГИБИТОРЫ СИНТЕЗА КЛЕТОЧНОЙ СТЕНКИ: бактерицидный эффект
ПЕНИЦИЛЛИНЫ• ПРИРОДНЫЕ
• ПОЛУСИНТЕТИЧЕСКИЕ
• «ЗАЩИЩЕННЫЕ»
ЦЕФАЛОСПОРИНЫ
I ПОКОЛЕНИЯ
II ПОКОЛЕНИЯ
III ПОКОЛЕНИЯ
IV ПОКОЛЕНИЯ
КАРБАПЕНЕМЫ
МОНОБАКТАМЫ
15.
ПенициллиныСтруктурная основа: 6аминопенициллановая кислота. Отличия
разных пенициллинов определяются
присоединением различных радикалов к
этой молекуле: изменение
чувстительности к бета-лактамазам,
антимикробной активности и ряда других
фармакологических свойств.
16. ИСТОРИЯ БЕНЗИЛПЕНИЦИЛЛИНА
• 1928 г. - А. Флеминг (открыл пенициллин)• 1940 г. – Э. Чейн и Г. Флори получили пенициллин
для системного применения
• 1941 г.- попытка пролечить первых пациентов с
тяжелыми стрептококковыми и стафилококковыми
инфекциями,которые не поддавались лечению другими
известными ЛС
• Г. Флори (в Америку к фармацевтической компании
"Мерк»)
• 1942 г. ( "Мерк" - массовые испытания пенициллина на
людях)
•1942 г. – З.В. Ермольева – автор советского
пенициллина
17. ПРИРОДНЫЕ ПЕНИЦИЛЛИНЫ (РАЗРУШАЮЩИЕСЯ ПЕНИЦИЛЛИНАЗОЙ)
Для парентерального введения:• Непродолжительного действия (до 3-6 ч)
• Бензилпенициллин (натриевая, калиевая
соли)
• Продолжительного (от 10-12ч до 4 недель)
• Бензилпенициллин (новокаиновая соль)
• Бензатина бензилпенициллин ( N,N-дибензил-
этилендиаминовая соль бензилпенициллина):
• БИЦИЛЛИН-1, 3, 5
• БИЦИЛЛИН-5: + бензилпенициллина новокаиновая соль)
Для энтерального введения:
• Феноксиметилпенициллин
18. ПРИРОДНЫЕ ПЕНИЦИЛЛИНЫ CПЕКТР ПРОТИВОМИКРОБНОГО ДЕЙСТВИЯ
ПРИРОДНЫЕ ПЕНИЦИЛЛИНЫ1.
CПЕКТР ПРОТИВОМИКРОБНОГО ДЕЙСТВИЯ
Грамположительные кокки (стафилококки не
продуцирующие пенициллиназу *, стрептококкибета-гемолитические и пневмококки (Streptococcus
pneumoniae)
2.
Грамотрицательные
кокки (Neisseria meningitidis, Neisseria
gonorrhoeae)
3.
4.
5.
6.
7.
Listeria monocytogenes
Дифтерийная палочка (Corynebcterium diphthyeriae)
Сибиреязвенная палочка (Bacillus anthracis)
Анаэробы (Clostridium)
Спирохеты (Treponema pallidum)
* - до 60- 90% штаммов Staphyllococcus аureus и epidermidis
в настоящее время устойчивы к бензилпенициллину
19. Показания для применения природных пенициллинов
* Стрептококковые инфекции (стрептококковая ангина,тонзиллофарингит, в том числе при скарлатине; рожа, инфекции
мягких тканей, неонатальный сепсис)
* Газовая гангрена
* Сибирская язва
* Сифилис
• Менингит (менингококковый, пневмококковый при
доказанной чувствительности)
• Листериоз
• Гонорея
• Дифтерия (при носительстве)
20. ПОЛУСИНТЕТИЧЕСКИЕ ПЕНИЦИЛЛИНЫ 1.(УСТОЙЧИВЫЕ К ДЕЙСТВИЮ ПЕНИЦИЛЛИНАЗЫ)
• Для энтерального и парентеральноговведения – кислотоустойчивые -
включение ацильной боковой цепи в структуру
пенициллина позволило защитить бета-лактамную
связь в молекуле и значительно уменьшило
возможность ее разрушения бета-лактамазами
стафилококков ▼
Изоксазолиловые пенициллины:
• Оксациллин
• Клоксациллин (самый активный)
• Диклоксациллин
21. ПОЛУСИНТЕТИЧЕСКИЕ ПЕНИЦИЛЛИНЫ (УСТОЙЧИВЫЕ К ДЕЙСТВИЮ ПЕНИЦИЛЛИНАЗЫ)
• Стафилококки, продуцирующиепенициллиназу ► пенициллинрезистентные
штамма St. аureus и St. epidermidis
Существенно уступают, природным
пенициллинам по уровню активности в
отношении большинства микроорганизмов.
Применяют преимущественно при тяжелых
стафилококковых инфекциях (кожи, мягких
тканей, костей, суставов, внебольничной пневмонии,
менингите, сепсисе).
• Низкая биодоступность оксациллина –
парентерально !!! (только затем возможен
переход на прием внутрь)
22. ПОЛУСИНТЕТИЧЕСКИЕ ПЕНИЦИЛЛИНЫ (УСТОЙЧИВЫЕ К ДЕЙСТВИЮ ПЕНИЦИЛЛИНАЗЫ)
• !!! Оксациллин не действует на стафилококки, резистентность которых к пенициллинамсвязана не с выработкой бета-лектамаз, а
с появлением атипичных ПСБ – так
называемые метициллинрезистентные
штаммы S.aureus (MRSA) и S.epidermidis
(MRSE)
23. 2. ПОЛУСИНТЕТИЧЕСКИЕ ПЕНИЦИЛЛИНЫ
• РАЗРУШАЮЩИЕСЯ ПЕНИЦИЛЛИНАЗОЙ:Аминопенициллины
(включение аминогруппы в
бензильную боковую цепь молекулы пенициллина)
• АМПИЦИЛЛИН
• АМОКСИЦИЛЛИН
РАСШИРЕНИЕ СПЕКТРА В ОТНОШЕНИИ
ГРАМОТРИЦАТЕЛЬНЫХ БАКТЕРИЙ:
• Чувствительные штаммы шигелл, сальмонелл, Е.
coli, P. мirabilis (не индолположительные штаммы)
• Преимущество по сравнению с природными
пенициллинами отмечено отношении листерий;
Амоксициллин - Helicobacter pylory.
24. 3. ПОЛУСИНТЕТИЧЕСКИЕ ПЕНИЦИЛЛИНЫ АНТИПСЕВДОМОНАДНЫЕ
• Карбоксипенициллины(включение карбоксигруппы
в молекулу пенициллина привело к созданию в 1967г карбенициллина):
• КАРБЕНИЦИЛЛИН
• ТИКАРЦИЛЛИН
• * Карбенициллин первый из пенициллинов, активных
отношении P. aerugenosa и многих штаммов и грам
(-) бактерий семейства Entobacteriaceae (Proteus
mirabilis,Escherichia coli, Shigella spp., Salmonella spp),
но в настоящее время утратил свое клиническое
значение как антипсевдомонадный пенициллин.
• * Тикарциллин 2-4 раза активнее, но и он сущестенно
уступает уреидопенициллинам (появление беталактамаз, к которым они высокочустительны.
25. ПОЛУСИНТЕТИЧЕСКИЕ ПЕНИЦИЛЛИНЫ АНТИПСЕВДОМОНАДНЫЕ
• Уреидопенициллины (боковая цепь ацильное производное мочевой кислоты):• Пиперациллин
• Азлоциллин
• Мезлоциллин
26. РАСШИРЕНИЕ СПЕКТРА В ОТНОШЕНИИ ГРАМОТРИЦАТЕЛЬНЫХ БАКТЕРИЙ:
• синегнойная палочка (P. aerugenosa),большинство энтеробактерий, в том числе
индолположительные штаммы протея,
cеррации, клебсиеллы, грамотрицательные
анаэробы, включая B. fragilis
▼ тяжелые госпитальные инфекции –
дыхательных путей, мочевыводящих путей,
интраобдоминальные, гинекологические.
☻ Проблема развития резистентности:
комбинация с аминогликозидами,
фторхинолонами, ингибиторами беталактамаз
27. “ЗАЩИЩЕННЫЕ ПЕНИЦИЛЛИНЫ”
1. Комбинация внутри группы:Ампициллин + Оксациллин
= АМПИОКС
!!! Мала доза ампициллина, устойчиво большинство
грамотрицательных штаммов
Ампициллин + Клоксациллин = КЛОНАКОМ –Р
Амоксициллин+ Клоксациллин = КЛОНАКОМ –Х
Комбинация ампициллина или амоксициллина с
пенициллиназоустойчивым клоксациллином
расширяет спектр и в ряде случаев усиливает
действие каждого препарата в отдельности
28. “ЗАЩИЩЕННЫЕ ПЕНИЦИЛЛИНЫ”
2. Комбинации с ингибиторами беталактамаз:АМОКСИЦИЛЛИН+ КЛАВУЛАНОВАЯ КИСЛОТА
АМОКСИЦИЛЛИН+ СУЛЬБАКТАМ
АМПИЦИЛЛИН+ СУЛЬБАКТАМ
ТИКАРЦИЛЛИН + КЛАВУЛАНОВАЯ КИСЛОТА
ПИПЕРАЦИЛЛИН+ ТАЗОБАКТАМ
29. Ингибиторы бета-лактамаз используются для защиты аминопенициллинов и «антисинегнойных» пенициллинов от разрушений бета-лактамазами Про
Ингибиторы бета-лактамаз используютсядля защиты аминопенициллинов и
«антисинегнойных» пенициллинов от
разрушений бета-лактамазами
Проявляют умеренную противомикробную
активность в отношении микробов,
вырабатывающих
бета-лактамазы
30. ИНГИБИТОРЗАЩИЩЕННЫЕ ПЕНИЦИЛЛИНЫ
• Ингибиторы бета-лактамаз действуют как«суицидные» ингибиторы энзима, вызывая
необратимую инактивацию фермента путем
реакции ацетилирования
• Эффект обусловлен тем, что обратной
реакции –
деацетилирования не
происходит и бета-лактамаза
не
регенерирует
31. РЕЗУЛЬТАТ
• Грам(+) кокки:стафилококки (включаяпенициллиноустойчивые штаммы S.aureus и
S.epidermidis), стрептококки, энтерококки.
• Грам(-) микробы:Н.influenzae, M.catarrhalis, E.coli,
Proteus spp., Klebsiella spp., N.gonorrhoeae, и др.,
включая β-лактамазопродуцирующие штаммы.
• Анаэробы:спорообразующие и неспорообразующие,
включая В.fragilis.
• * P.aeruginosa (но не превосходят
тикарциллин или пиперациллин )
• Актиномицеты (превосходят по эффективности
природные и полусинтетические пенициллины)
32. Пиперациллин + тазобактам (Тазоцин)
Широкий антимикробныйспектр:–Грам(+): стафилококки, стрептококки, энтерококки
–Грам(-): энтеробактерии, P.aeruginosa, Acinetobacter
–Анаэробы, вкл. Bacteroide spp., Clostridium spp.
•Возможность монотерапии полимикробных
инфекций
•Более высокая(посравнению с сульперазоном и
цефтазидимом) активность против Грам(+)
• Возможность применения при внебольничных
инфекциях
• •В отличие от цефалоспоринов III-IV и
фторхинолонов не вызывает селекцию БЛРСпродуцентов
• Возможность замены ЦФС III и ФХ в качестве
базовой терапии НИ
33. МЕХАНИЗМ ДЕЙСТВИЯ ПЕНИЦИЛЛИНОВ:
Антибактериальная активностьбета-лактамных антибиотиков
определяется:
• Скоростью проникновения препарата через
наружную мембрану микроорганизма
• Устойчивостью к бета-лактамазам бактерий
• Взаимодействием со специфическими
мишенями –«пенициллиносвязывающими»
белками (ПСБ)
34. МЕХАНИЗМ ДЕЙСТВИЯ ПЕНИЦИЛЛИНОВ:
• Мишень бета-лактамов – ПСБ (PBP):выполняют роль ферментов на
завершающем этапе синтеза
пептидогликана – основного компонента
клеточной стенки бактерий.
• Самые крупные ПСБ 1a и 1b –
транспептидазы (это только один вид
белков, на которые действуют беталактамы)– завершают синтез
пептидогликана. При их инактивации
образуются клеточно-дефицитные бактерии,
которые быстро разрушаются.
35. МЕХАНИЗМ ДЕЙСТВИЯ ПЕНИЦИЛЛИНОВ:
• Взаимодействие с ПСБ 2 - образованиенежизнеспособных форм с большим
количеством цитоплазматических
выпячиваний, однако они разрушаются
медленнее, чем при инактивации
транспептидаз.
• ПСБ 3 необходимы для образования
клеточной перегородки при делении. При его
инактивации неразделившиеся бактерии
принимают вид вид длинных тонких нитей.
ПСБ есть у всех бактерий (например, Staph.
аureus -четыре, а у E. colli – не менее семи)
36. ОСОБЕННОСТИ ФАРМАКОКИНЕТИКИ ПЕНИЦИЛЛИНОВ:
• Пенициллины применяемые внутрь:феноксиметилпенициллин, ампициллин,
амоксициллин, оксациллин:
• Низкая биодоступность (20-40%), клинически
значимое снижение их всасывания пищей
прием натощак, либо через 2 часа после
приема пищи.
• Исключение амоксициллин
бидоступность не менее 80-90%,
отсутствие влияния пищи на всасывание
препарата – более высокие и стабильные
концентрации в крови и тканях.
37. ОСОБЕННОСТИ ФАРМАКОКИНЕТИКИ ПЕНИЦИЛЛИНОВ:
• Хорошо проникают в пазухи черепа, ухо,легкие, бронхи, эндокард, мышцы,
суставы, а пенициллины, устойчивые к
пенициллиназе и в костную ткань. Более
низкие концентрации отмечаются в тканях
глаза, предстательной железе и ЦНС
• При воспалении мозговых оболочек
(бактериальном менингит) концентрации
пенициллинов при их парентеральном
введении являются клинически
значимыми, поскольку проницаемость
мозговых оболочек увеличивается
38. ОСОБЕННОСТИ ФАРМАКОКИНЕТИКИ ПЕНИЦИЛЛИНОВ:
• Для некоторыхполусинтетических
пенициллинов (оксациллин, ампициллин,
амоксициллин) характерно наличие высокой
концентрации в желчи
возможность
применения при инфекциях желчевыводящих
путей; снижение риска замедления
выведения при ХПН
39. ПОБОЧНЫЕ ЭФФЕКТЫ ПЕНИЦИЛЛИНОВ:
• Наиболее характерный нежелательный эффектпенициллинов (в первую очередь природных) сенсибилизирующее действие ► аллергические
реакции как немедленного, так и замедленного типа
• Характерна перекрестная сенсибилизация и
перекрестные аллергические реакции
• Действие пенициллинов направлено только
на
бактериальную клеточную стенку, на
большинство животных клеток они
практически не оказывают какого-либо
действия
• Токсическое влияние
пенициллинов может
проявляться только на фоне очень больших доз
(например, для бензилпенициллина более 30 млн.
ЕД/сутки) – снижение судорожного порога.
В
мегадозах возможна прямая катионная (Na+/K+)токсичность
40. ПОБОЧНЫЕ ЭФФЕКТЫ ПЕНИЦИЛЛИНОВ:
• На фоне приема карбоксипенициллиноввозможно развитие кровоточивости
(дисфункция мембран тромбоцитов)
• Возможно местнораздражающее действие
• Для препаратов широкого спектра действия
возможно развитие дисбактериоза,
колонизации кишечника C. dificile и развитие
псевдомембранозного колита
41.
ЦефалоспориныИз гриба Cephalosporinum acremonium в
1945 из морской воды, взятой в Сардинии у
места слива в него сточных вод, был
выделен ряд пенициллин-продуцирующих
антибиотиков, в том числе
цефалоспорин С (7аминоцефалоспориновая кислота).
42.
• Полусинтетические производные илисинтетические аналоги получили название –
цефалоспорины.
• В структуре содержат бета-лактамное
кольцо.
• Реально используются в клинике с 60-х
годов прошлого века.
• Каждый второй из используемых в мире
антибиотиков является
цефалоспориновым
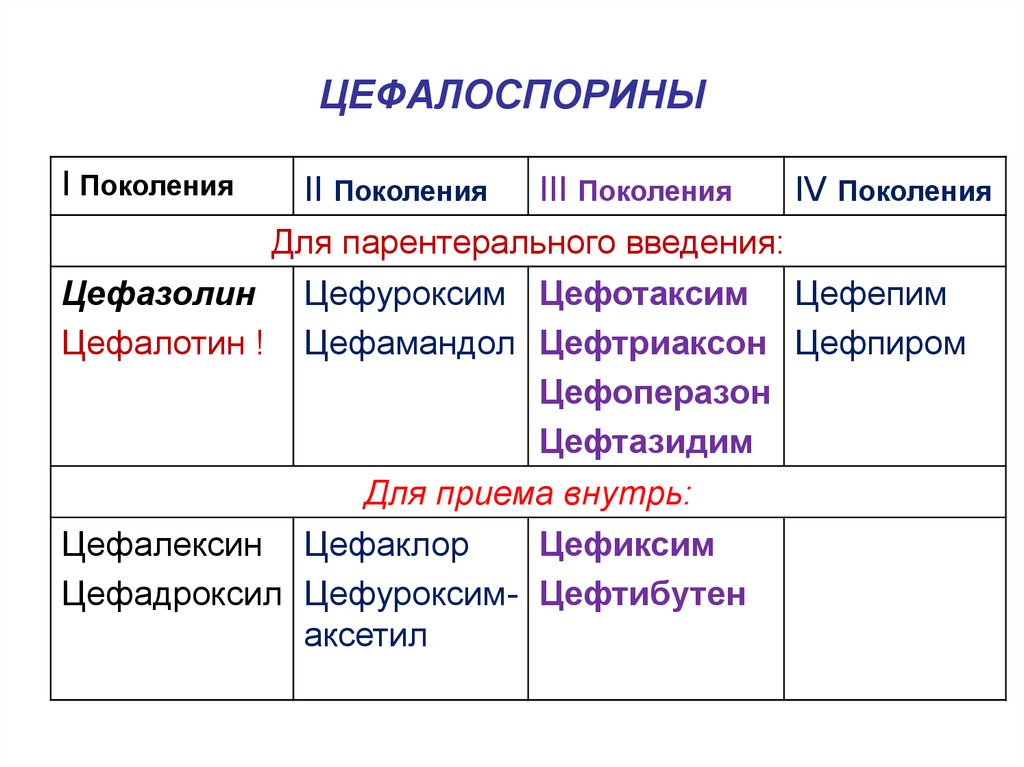
43. ЦЕФАЛОСПОРИНЫ
I ПоколенияII Поколения
III Поколения
IV Поколения
Для парентерального введения:
Цефазолин
Цефалотин !
Цефуроксим Цефотаксим Цефепим
Цефамандол Цефтриаксон Цефпиром
Цефоперазон
Цефтазидим
Для приема внутрь:
Цефалексин Цефаклор
Цефиксим
Цефадроксил Цефуроксим- Цефтибутен
аксетил
44. ЦЕФАЛОСПОРИНЫ
• По своей структуре ЦФ близки к пенициллинам иимеют в
основе своей структуры
7аминоцефалоспорановую кислоту
• ЦФ имеют принципиально сходный с
пенициллинами механизм действия, ингибируя
синтез клеточной стенки микроорганизмов
• Фармакодинамические преимущества ЦФ (III-IV)
объясняются особенностями их строения,
обуславливающими лучшую проницаемость
через наружные слои клеточной мембраны,
влиянием на иные, чем у пенициллинов ПСБ,
большей устойчивостью к плазмидным и
хромосомным бета-лактамазам различных
микроорганизмов (в зависимости от поколения ЦФ)
45. ЦЕФАЛОСПОРИНЫ I ПОКОЛЕНИЯ:
• Обладают наиболее высокой активностьюсреди ЦФ в отношении
грамположительных кокков
(стафилококки, стрептококки, пневмококки)
• Стабильны к бета-лактамазам,
продуцируемым стафилококками
• Активны в отношении
грамотрицательных кокков
(менингококки, гонококки)
• Спирохеты
• Сибироязвенная палочка
• Дифтерийная палочка
46. ЦЕФАЛОСПОРИНЫ I ПОКОЛЕНИЯ:
• Умеренная активность в отношенииограниченного круга
грамотрицательных микроорганизмов:
E. coli, Proteus mirabilis *(широко
распространены устойчивые бета-лактамазопродуцирующие штаммы),
** Salmonella, Shigella (не имеет клинической
значимости)
• Полохо проникают через ГЭБ, что не
позволяет использовать их для лечения
менингита
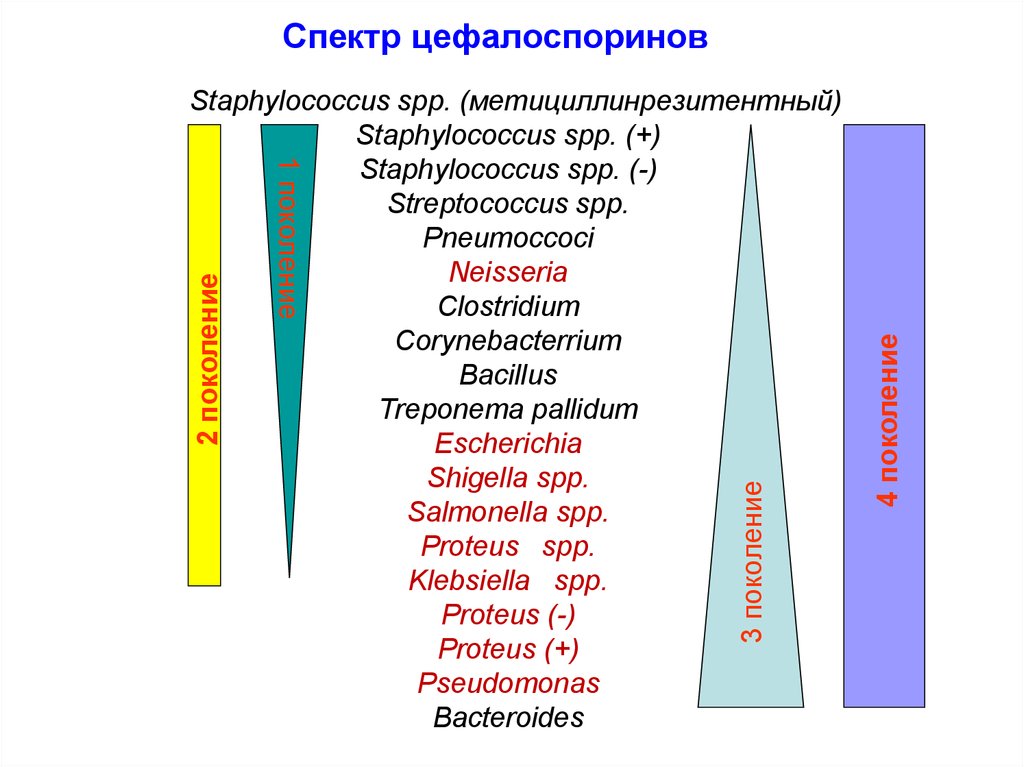
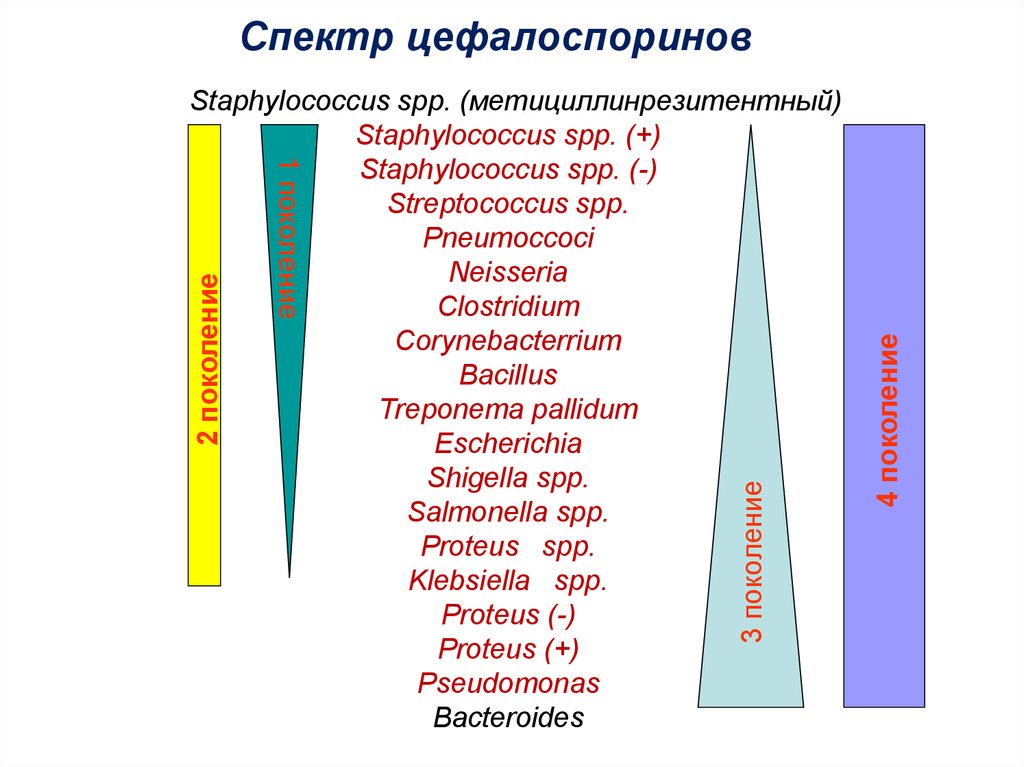
47. Спектр цефалоспоринов
4 поколение3 поколение
2 поколение
1 поколение
Staphylococcus spp. (метициллинрезитентный)
Staphylococcus spp. (+)
Staphylococcus spp. (-)
Streptococcus spp.
Pneumoccoci
Neisseria
Clostridium
Corynebacterrium
Bacillus
Treponema pallidum
Escherichia
Shigella spp.
Salmonella spp.
Proteus spp.
Klebsiella spp.
Proteus (-)
Proteus (+)
Pseudomonas
Bacteroides
48. ЦЕФАЛОСПОРИНЫ I ПОКОЛЕНИЯ:
• Доказанная или предполагаемаястафилококковая инфекция кожи, мягких
тканей, при стафилококковом сепсисе
и
эндокардите.
• Препараты второго ряда при лечении
стрептококкового тонзиллофарингита (P/O)
• Хорошо проникают в большинство тканей,
низкая токсичность и стоимость периоперационная профилактика в хирургии
• У пациентов со слабой
гиперчувствительностью к пенициллинам
(не анафилактический шок в анамнезе)
49. ЦЕФАЛОСПОРИНЫ II ПОКОЛЕНИЯ:
• Расширение спектрапротивомикробной
активности в отношении грамотрицательных
бактерий. Стабильны к бета-лактамазам,
продуцируемым Moraxella catarralis,
H. influenzae, большинством энтеробактерий,
включая индолположительные штаммы
протея
• Незначительно уступают ЦФ I поколения по
влиянию на грамположительные кокки
• Цефуроксим единственный препарат II
поколения, который проникает через ГЭБ и
может использоваться для лечения
менингитов.
50. Спектр цефалоспоринов
4 поколение3 поколение
2 поколение
1 поколение
Staphylococcus spp. (метициллинрезитентный)
Staphylococcus spp. (+)
Staphylococcus spp. (-)
Streptococcus spp.
Pneumoccoci
Neisseria
Clostridium
Corynebacterrium
Bacillus
Treponema pallidum
Escherichia
Shigella spp.
Salmonella spp.
Proteus spp.
Klebsiella spp.
Proteus (-)
Proteus (+)
Pseudomonas
Bacteroides
51. ЦЕФАЛОСПОРИНЫ II ПОКОЛЕНИЯ:
• Применение для лечения внебольничнойпневмонии (иногда в сочетании с
макролидами), инфекциях кожи и мягких
тканей, инфекциях мочевыводящих путей,
для периоперационной профилактики в
хирургии.
• Цефуроксим: менингит, вызванный менингои пневмококками, гемофильной палочкой
52. ЦЕФАЛОСПОРИНЫ III ПОКОЛЕНИЯ:
• Расширение спектра показаний и болеевысокая
активность
в
отношении
грамотрицательной флоры,
включая
госпитальные
и
множественные
устойчивые
штаммы.
Особенно
эффективны
против
представителнй
семейства
энтеробактерий,
Serratia
marcescens, а также продуцирующих беталактамазу
Haemophilus
и
Neisseria
gonorrhoeae
• Цефоперазон и цефтазидим активны в
отношении P. aeruginosa
53. Спектр цефалоспоринов
4 поколение3 поколение
2 поколение
1 поколение
Staphylococcus spp. (метициллинрезитентный)
Staphylococcus spp. (+)
Staphylococcus spp. (-)
Streptococcus spp.
Pneumoccoci
Neisseria
Clostridium
Corynebacterrium
Bacillus
Treponema pallidum
Escherichia
Shigella spp.
Salmonella spp.
Proteus spp.
Klebsiella spp.
Proteus (-)
Proteus (+)
Pseudomonas
Bacteroides
54. ЦЕФАЛОСПОРИНЫ III ПОКОЛЕНИЯ:
• Большинство препаратов данной генерации(за исключением цефоперазона) хорошо
проникает через ГЭБ и могут быть
использованы у больных менингитом,
вызванным грамотрицательными
бактериями
• Существенное снижение активности в
отношении грамположительных кокков,
особенно стафилококков в сравнении с ЦФ I и
II поколений
• Экскреция цефоперазона и цефтриаксона, в
отличие от других препаратов данной группы
осуществляется в основном с желчью
55. ЦЕФАЛОСПОРИНЫ III ПОКОЛЕНИЯ:
• Лечение внебольничных и нозокомиальныхпневмоний, а также бронхита, абсцессов
легких, эмпиемы плевры), лор-инфекции,
инфекции кожи и мягких тканей,
мочевыводящих путей, органов малого таза
(в т.ч. простатит), костей и суставов,
инфекции ЖКТ, желчных путей и брюшной
полости, сепсис, менингит, инфекции,
связанные с диализом; гонорея, особенно
при гиперчувствительности к антибиотикам
пенициллинового ряда. Инфекции,
вызванные Pseudomonas aeruginosa.
56. ЦЕФАЛОСПОРИНЫ IV ПОКОЛЕНИЯ:
• Имеют свойства цвиттериона - одновременногоносителя положительного и отрицательного заряда,
что определяет высокую растворимость в воде и
быстрое проникновение через клетку бактериальной
клетки
• Проникают в периплазматическое пространство
бактерий в 5-7 раз быстрее, чем ЦФ III поколения и
содержаться в нем в значительно более высоких
концентрациях (место гидролиза и снижения
концентрации антибиотиков)
• Большинство бета-лактамаз, продуцируемых
грамотрицательными бактериями (Enterobacter,
Serratia, Klebsiella, Pseudomonas), обладают низкой
аффинностью к препаратам IV поколения
57. ЦЕФАЛОСПОРИНЫ IV ПОКОЛЕНИЯ:
• Повышение эффективности терапии притяжелых госпитальных инфекциях
дыхательных путей, инфекций кожи и мягких
тканей, мочевыводящих путей,
интраабдоминальных инфекций, септецимии
и бактеримии, в том числе у больных со
сниженным иммунитетом и нейтропенией
• Не активны против метициллинрезистентных
штаммов стафилококков
58. Спектр цефалоспоринов
4 поколение3 поколение
2 поколение
1 поколение
Staphylococcus spp. (метициллинрезитентный)
Staphylococcus spp. (+)
Staphylococcus spp. (-)
Streptococcus spp.
Pneumoccoci
Neisseria
Clostridium
Corynebacterrium
Bacillus
Treponema pallidum
Escherichia
Shigella spp.
Salmonella spp.
Proteus spp.
Klebsiella spp.
Proteus (-)
Proteus (+)
Pseudomonas
Bacteroides
59. ПОБОЧНЫЕ ЭФФЕКТЫ ЦЕФАЛОСПОРИНОВ:
• При лечении ЦФ примерно в 2% случаев возникаюталлергические реакции, у 1-20% возможна
перекрестная с пенициллинами
гиперчувствительность
• Токсическое действие ЦФ на почки минимально и
наблюдается в основном при комбинации их с
аминогликозидами
• Возможны случаи временного небольшого увеличения показателей активности печеночных
трансаминаз (АЛТ, АСТ, щелочной фосфатаза)
• Возможно возникновение тошноты, рвоты, диареи. В
ряде случаев диарея может отражать развитие
дисбактериоза и псевдомембранозного колита,
вызываемого Сlostridium difficile. Дисбактериоз чаще
возникает при использовании пероральных форм с
низкой биодоступностью, а также перентеральных
препаратов, элиминирующихся с желчью
• Может отмечаться лейко- и нейротопения
60. ПОБОЧНЫЕ ЭФФЕКТЫ ЦЕФАЛОСПОРИНОВ:
• Ряд ЦФ (цефамандол, цефаперазон) имеют в своемхимическом составе N-метилтиотетразоловую
группу, что определяет две побочные реакции:
• Гипопротромбинемия, увеличение протромбинового
времени свертывания крови, что обусловлено
взаимодействием N-метилтиотетразоловой группы с
витамином К и нарушением его утилизации,
особенно у больных с печеночной недостаточностью,
плохим питанием и онкологическими заболеваниями.
Эффективно устраняется препаратами витамина К.
• Взаимодействие N-МТТ
группы с алкогольной
дегидрогеназой и накоплением ацетальдегида. В
результате при приеме алкоголя на фоне лечения
этими препаратами возникает реакция, идентичная
приему дисульфирама
61.
КарбапенемыВ молекуле корбапенемов бета-лактамное
кольцо соединено с пятиатомным кольцом.
Последнее, в отличие от аналогичного
кольца у пенициллинов, не насыщено и
вместо атома серы содержит атом
углерода.
Из всех бета-лактамов – самый широкий
спектр действия ( по сравнению с
пенициллинами и цефалоспоринами более
устойчивы к бета-лактамазам, в том числе и
расширенного спектра)
62.
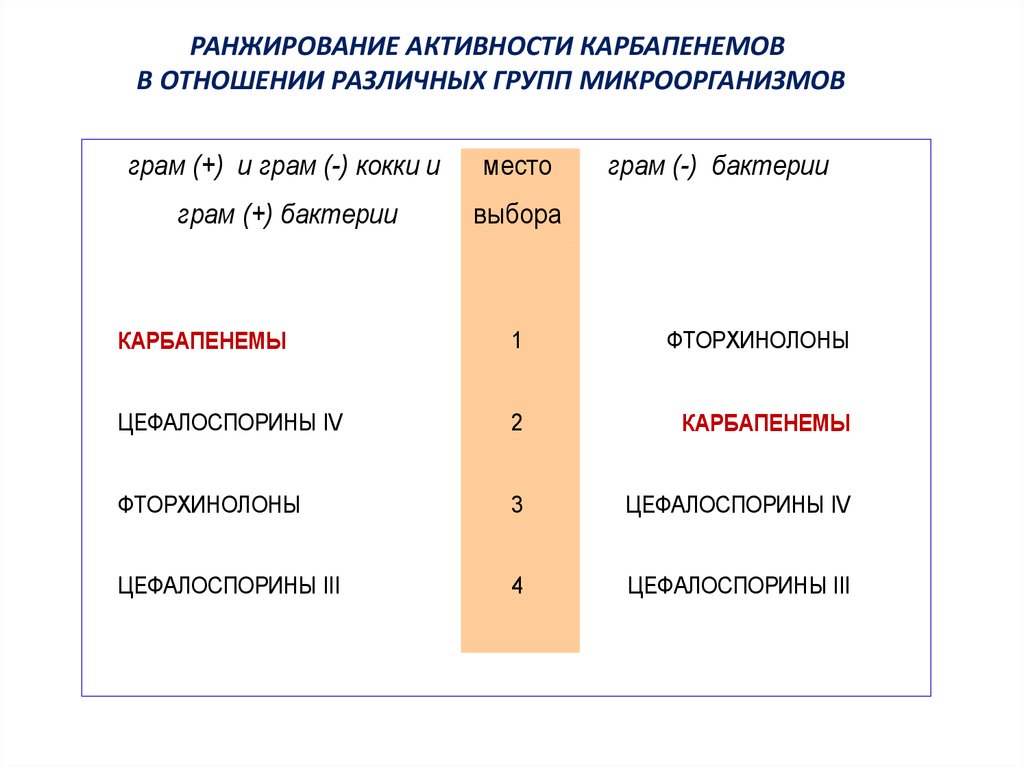
РАНЖИРОВАНИЕ АКТИВНОСТИ КАРБАПЕНЕМОВВ ОТНОШЕНИИ РАЗЛИЧНЫХ ГРУПП МИКРООРГАНИЗМОВ
грам (+) и грам (-) кокки и
место
грам (+) бактерии
выбора
грам (-) бактерии
КАРБАПЕНЕМЫ
1
ФТОРХИНОЛОНЫ
ЦЕФАЛОСПОРИНЫ IV
2
КАРБАПЕНЕМЫ
ФТОРХИНОЛОНЫ
3
ЦЕФАЛОСПОРИНЫ IV
ЦЕФАЛОСПОРИНЫ III
4
ЦЕФАЛОСПОРИНЫ III
63. КАРБАПЕНЕМЫ:
ИМИПЕНЕМ + ЦИЛАСТАТИН* (ТИЕНАМ)
МЕРОПЕНЕМ
ЭРТАПЕНЕМ
ДОРИПЕНЕМ
*- является высокоспецифическим ингибитором
фермента дегидропептидазы-I в почках, который
быстро
разрушает имипенем, резко снижая
длительность его действия и эффективность
выделение до 70% имипенема в активной форме,
значительное повышение его эффективности и
длительности действия. Обладает также
нефропротективным действием.
64. КАРБАПЕНЕМЫ:
• Подобно ЦФ IV поколения быстро проникаютчерез порины внешней мембраны бактерий и
создают высокую концентрацию в
периплазматическом пространстве
• Высокая аффинность в нескольким типам
ПСБ: 1b, 2, 4 и 7 типы, с которыми слабее
взаимодействуют другие бета-лактамные АБ.
Повышение эффективности в отношении
наиболее устойчивых возбудителей
инфекций, в том числе, резистентных к ЦФ.
65. КАРБАПЕНЕМЫ:
• Широкий спектр действия: большинствоклинически значимых грамположительных
и грамотрицательных аэробных и
анаэробных возбудителей.
• Высокая чувствительность резистентных ко
многим бета-лактамным АБ возбудителей:
энтерококки (исключая S. faecium),
пенициллинустойчивые штаммы
стафилококков, синегнойная палочка, в том
числе, цефтазидим-резистентные штаммы;
бактероиды
66. КАРБАПЕНЕМЫ:
• Препараты резерва для терапии полирезистентных(внутрибольничных), полимикробных и смешанных
аэробно-анаэробных инфекций в качестве
альтернативы комбинированной терапии
(цефалоспорины + аминогликозиды +метронидазол)
• Полимикробные инфекции мягких тканей и костей,
при тяжелых пневмониях, интраабдоминальных,
гинекологических, ожоговых инфекциях, сепсисе
• Среди побочных эффектов: аллергические
реакции (перекрестная аллергия с пенициллинами и
цефалоспоринами), флебиты, диспептические
нарушения, нейротоксичность (тремор, судороги),
нефротоксичность
67. ОБЩИЕ ВЫВОДЫ ДЛЯ КАРБАПЕНЕМОВ
ПЛЮС1.
2.
МИНУС
наиболее широкий
противомикробный спектр
быстрый бактерицидный
эффект
3. устойчивость к действию беталактамаз, в том числе,
расширенного спектра
действия, за исключением
содержащих
металлоферменты
4. самая высокая клиническая и
бактериологическая
эффективность в
контролируемых клинических
исследованиях
1.
риск селекции
резистентных штаммов к
бета-лактамам
P. aeruginosa
2.
3.
высокая стоимость
суперинфекции,
дизбактериоз, инвазивные
микозы
68. Воспоминания о предыдущей встрече
69. ПРИРОДНЫЕ ПЕНИЦИЛЛИНЫ CПЕКТР ПРОТИВОМИКРОБНОГО ДЕЙСТВИЯ
ПРИРОДНЫЕ ПЕНИЦИЛЛИНЫ1.
CПЕКТР ПРОТИВОМИКРОБНОГО ДЕЙСТВИЯ
Грамположительные кокки (стафилококки не
продуцирующие пенициллиназу *, стрептококкибета-гемолитические и пневмококки (Streptococcus
pneumoniae)
2.
Грамотрицательные
кокки (Neisseria meningitidis, Neisseria
gonorrhoeae)
3.
4.
5.
6.
7.
Listeria monocytogenes
Дифтерийная палочка (Corynebcterium diphthyeriae)
Сибиреязвенная палочка (Bacillus anthracis)
Анаэробы (Clostridium)
Спирохеты (Treponema pallidum)
70. ПОЛУСИНТЕТИЧЕСКИЕ ПЕНИЦИЛЛИНЫ (УСТОЙЧИВЫЕ К ДЕЙСТВИЮ ПЕНИЦИЛЛИНАЗЫ)
• Стафилококки, продуцирующиепенициллиназу
пенициллинрезистентные штамма St.
аureus и St. epidermidis
Применяют преимущественно при тяжелых
стафилококковых инфекциях (кожи, мягких
тканей, костей, суставов, внебольничной пневмонии,
менингите, сепсисе).
71. ПОЛУСИНТЕТИЧЕСКИЕ ПЕНИЦИЛЛИНЫ
• РАЗРУШАЮЩИЕСЯ ПЕНИЦИЛЛИНАЗОЙ:РАСШИРЕНИЕ СПЕКТРА В ОТНОШЕНИИ
ГРАМОТРИЦАТЕЛЬНЫХ БАКТЕРИЙ:
• Чувствительные штаммы шигелл, сальмонелл, Е.
coli, P. мirabilis (не индолположительные штаммы)
• Преимущество по сравнению с природными
пенициллинами отмечено отношении листерий,
гемофильной палочки; Амоксициллин - Helicobacter
pylory.
72. РАСШИРЕНИЕ СПЕКТРА В ОТНОШЕНИИ ГРАМОТРИЦАТЕЛЬНЫХ БАКТЕРИЙ:
Антипсевдомонадные пенициллины• синегнойная палочка (P. aerugenosa),
большинство энтеробактерий, в том числе
индолположительные штаммы протея,
cеррации, клебсиеллы, грамотрицательные
анаэробы, включая B. fragilis
▼ тяжелые госпитальные инфекции –
дыхательных путей, мочевыводящих путей,
интраобдоминальные, гинекологические.
73. Ингибиторзащищенные пенициллины
• Грам(+) кокки:стафилококки (включаяпенициллиноустойчивые штаммы S.aureus и
S.epidermidis), стрептококки, энтерококки.
• Грам(-) микробы:Н.influenzae, M.catarrhalis, E.coli,
Proteus spp., Klebsiella spp., N.gonorrhoeae, и др.,
включая β-лактамазопродуцирующие штаммы.
• Анаэробы:спорообразующие и неспорообразующие,
включая В.fragilis.
• * P.aeruginosa (но не превосходят
тикарциллин или пиперациллин )
74. Спектр цефалоспоринов
4 поколение3 поколение
2 поколение
1 поколение
Staphylococcus spp. (метициллинрезитентный)
Staphylococcus spp. (+)
Staphylococcus spp. (-)
Streptococcus spp.
Pneumoccoci
Neisseria
Clostridium
Corynebacterrium
Bacillus
Treponema pallidum
Escherichia
Shigella spp.
Salmonella spp.
Proteus spp.
Klebsiella spp.
Proteus (-)
Proteus (+)
Pseudomonas
Bacteroides
75. КАРБАПЕНЕМЫ:
• Самыйширокий
спектр
действия:
большинство
клинически
значимых
грамположительных
и
грамотрицательных
аэробных
и
анаэробных возбудителей.
• Высокая чувствительность резистентных ко
многим бета-лактамным АБ возбудителей:
энтерококки
(исключая
S.
faecium),
пенициллинустойчивые
штаммы
стафилококков, синегнойная палочка, в том
числе, цефтазидим-резистентные штаммы;
бактероиды
76. МОНОБАКТАМЫ:
АЗТРЕОНАМ• Имеет типичный для бета-лактамных антибиотиков
механизм действия, индуцирует образование
нежизненоспособных вытянутых бактериальных
структур
• Активен только против грамотрицательных
бактерий, устойчив к действию их бета-лактамаз.
Высокая эффективность против P.aeruginosa и
представителей семейства энтеробактерий
• Разрушается бета-лактамазами грамположительных
аэробных и анаэробных возбудителей, большинство
штаммов которых устойчивы к препарату
• Вводится парентерально. Хорошо проникает во многие
органы, ткани и среды; при воспалении мозговых оболочек и
через ГЭБ. Выделяется почками ( 80%), не подвергаясь
метаболизму в печени (коррекция дозы при нарушении
выделитильной функции почек)
77. МОНОБАКТАМЫ:
• Показания при применению определяются наличиему пациента грамотрицательной инфекции, включая
инфекции, вызыванные синегнойной палочкой
(препарат резерва для лечения инфекций,
вызванных аэробными грам(-) бактериями).
• Действует на штаммы микроорганизмов, устойчивых
к антипсевдомонадным пенициллинам,
цефалоспоринам III поколения и аминогликозидам:
• Внебольничные и нозокомиальные пневмонии,
пиелонефрит, цистит, уретрит, простатит, гонорея;
менингит; сепсис; заболевания органов брюшной
полсти и малого таза; послеоперационные
инфекционные осложнения; перитонит; инфекции
костной ткани, суставов, кожи, мягких тканей
78. МОНОБАКТАМЫ:
Побочные эффекты:
Гиперчувствительность: сыпь, крапивница
(отсутствует перекрестных аллергических
реакций с другими бета-лактамными
антибиотиками)
Повышение в крови печеночных
трансаминаз и щелочной фосфотазы
Анемия, нейтропения
Тошнота, рвота, диарея; при в/в введении –
флебиты; в редких случаях спутанность
сознания, диплопия, судороги
79.
Гликопептиды(природные АБ, продуцируемые почвенными
актиномицетами)
• ВАНКОМИЦИН
• ТЕЙКОПЛАНИН
80. ГЛИКОПЕПТИДЫ
• ИНГИБИТОРЫ СИНТЕЗА КЛЕТОЧНОЙСТЕНКИ, но действуют на более ранних этапах
синтеза пептидогликана. Прочно связываются с
карбоксильным окончанием D-Ala- D-Ala-цепочки
строящегося пептидогликана и нарушает его
дальнейшее удлинение и образование поперечных
сшивок.
• Нарушают структуру и функцию цитоплазмотической
мембраны
• В основном бактерицидный тип действия.
81. ГЛИКОПЕПТИДЫ
• Активны в отношении практически всех грам(+)аэробных и анаэробных микроорганизмов,
включая стафилококки (в том числе MRSA и
MRSE, стрептококки групп A,B,C,G, пневмококки,
энтерококки (бактериостатический эффект),
пептококки, клостридии, включая C.difficile,
листерии, коринобактерии.
• Появилось достаточное количество устойчивых к
ванкомицину штаммов Entrerococcus faecium –частые
возбудители больничных инфекций.
• Практически не всасываются в ЖКТ –в/в путь
введения
82. ПОКАЗАНИЯ К ИСПОЛЬЗОВАНИЮ ГЛИКОПЕПТИДОВ
1.кокковый грам (+) сепсис;
2.
стафилококковый и стрептококковый эндокардит;
3.
болезни инфицированных шунтов, катетеров, клапанов
и тд.;
4.
псевдомембранозный колит - Cl.diffecile
5.
стафилококковый энтероколит
83. Нежелательные явления
• Нефротоксичность (чаще ванкомицин): обратимоенарушение функции почек (увеличение уровня
креатинина и мочевины в крови): факторы риска –
доза/длительность, пожилой возраст.
• ЦНС: головокружение, головная боль, проявления
ототоксичности (понижение слуха, вестибулярные
нарушения)
• Местные реакции: гиперемия лица и верхней
половины туловища (синдром “красного человека”)при быстром в/в введении
• Аллергические реакции: редко
• Гематологические реакции: обратимая лейкопения,
тромбоцитопения (редко).
• ЖКТ: тошнота, рвота, диарея.
84.
Аминогликозидыпервым аминогликозидом был стрептомицин,
выделенный в 1944 году из актиномицета
Streptomyces griseus. Он также был одним из первых
известных антибиотиков вообще, вторым после
пенициллина.
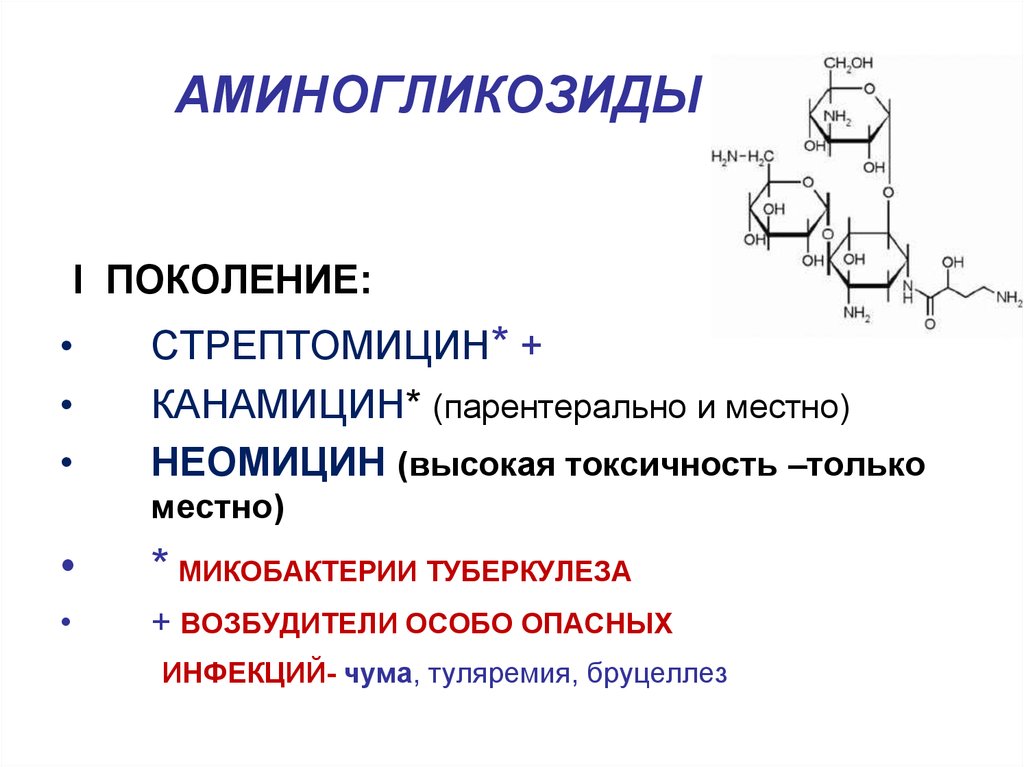
85. АМИНОГЛИКОЗИДЫ
I ПОКОЛЕНИЕ:СТРЕПТОМИЦИН* +
КАНАМИЦИН* (парентерально и местно)
НЕОМИЦИН (высокая токсичность –только
местно)
* МИКОБАКТЕРИИ ТУБЕРКУЛЕЗА
+ ВОЗБУДИТЕЛИ ОСОБО ОПАСНЫХ
ИНФЕКЦИЙ- чума, туляремия, бруцеллез
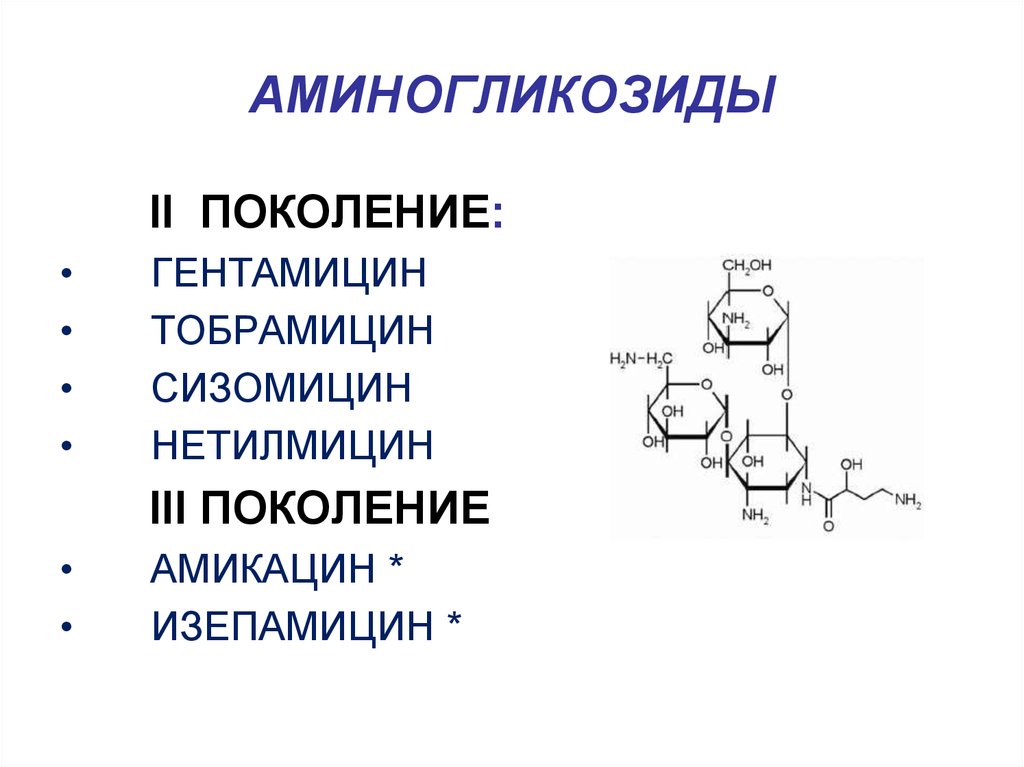
86. АМИНОГЛИКОЗИДЫ
II ПОКОЛЕНИЕ:ГЕНТАМИЦИН
ТОБРАМИЦИН
СИЗОМИЦИН
НЕТИЛМИЦИН
III ПОКОЛЕНИЕ
АМИКАЦИН *
ИЗЕПАМИЦИН *
87. АМИНОГЛИКОЗИДЫ
ПРЕПАРАТЫ II И III ПОКОЛЕНИЙ:• ПРОТИВОМИКРОБНАЯ АКТИВНОСТЬ В
ОСНОВНОМ НАПРАВЛЕНА НА
ГРАМОТРИЦАТЕЛЬНЫЕ ЭНТЕРОБАКТЕИИ
(кишечная палочка, протей, клебсиеллы,
энтеробактеры,серрации и др.) и
нечувствительные к препаратам I поколения
неферментирующие грамотрицательные
палочки (P.aeruginosa, Acinobacter)
• Стафилококки (кроме MRSA)
88. Показания для применения аминогликозидов
синегнойная инфекция (аминогликозиды II-III поколения)
сепсис
инфекционный эндокардит
нозокомиальная пневмония
интраабдомиальные инфекции, инфекции органов малого
таза
Специфическая терапия:
чума (стрептомицин)
туляремия (стрептомицин, гентамицин)
бруцеллёз (стрептомицин)
туберкулёз (стрептомицин, канамицин)
• Антибиотикопрофилактика:
• деконтаминация кишечника перед плановыми операциями
на толстом кишечнике (неомицин-внутрь)
89. АМИНОГЛИКОЗИДЫ
• Проникновение в клетку путем активноготранспорта и пассивной диффузии
связывание с рецепторами на 30Sсубъединице рибосом и нарушение ее
взаимодействия с т-РНК:
блокада
инициаторного комплекса образования
белка (и-РНК + формил-метионил-т-РНК) на
стадии трансляции белкового синтеза
(преждевременное окончание трансляции –
подавление синтеза белка)
• Бактерицидный эффект
90. АМИНОГЛИКОЗИДЫ
• Рецепторы 30S-субъединиц рибосом,связывающихся с АГ отличны от
«тетрациклиновых» рецепторов.
• Нарушение функции и структуры
цитоплазматической мембраны
микроорганизма выход в окружающую
среду АК, нуклеотидов, ионов калия гибель
микробной клетки
• Бактерицидное действие (дозозависимая
активность)
91. АМИНОГЛИКОЗИДЫ
• Пассивная диффузия АГ в клетку бактерииклинически значимо усиливается при
нарушении синтеза клеточной стенки
синнергизм с бета-лактамными
антибиотиками
• Активный транспорт АГ в клетку –
кислородозависимый процесс и затруднен в
анаэробных условиях низкая
эффективность АГ в отношении
анаэробной флоры
92. Фармакокинетика АМИНОГЛИКОЗИДОВ
• Практически не всасываются из ЖКТ,поэтому прием внутрь ► исключительно
местный эффект
• Основной путь введения парентеральный .
• Практически не подвергаются
биотрансформации, высокая проникающая
способность в ткани и жидкости
макроорганизма
• T1/2 у всех аминогликозидов в норме 2-4
часа
• При почечной недостаточности T1/2 может
возрастать до 70 часов и более (выводятся в
неизмененном виде !!!!)
93. ПОБОЧНЫЕ ЭФФЕКТЫ АМИНОГЛИКОЗИДОВ
• Нейротоксическое действие (ототоксичность,вестибулярные расстройствапоражение VIII пары черепно-мозговых
нервов)
• Снижение слуха необратимы. Отдельные
вестибулярные нарушения у молодых
людей могут проходить через 10-15 лет.
• Обусловлены накоплением АГ в эндолимфе
внутреннего уха (при длительном более 10
дней применения), в концентрациях
значительно превышающих таковые в плазме
крови (стрептомицин, канамицин,
амикацин).
94. ПОБОЧНЫЕ ЭФФЕКТЫ АМИНОГЛИКОЗИДОВ
• Нефротоксическое действие (обратимоенарушение фильтрационной и концентрационной
функции почек, развитие почечной недостаточности).
Обусловлен накоплением АГ в ткани почек.
• Например, гентамицина в корковом слое
содержится в 20 раз, а тобромицина в 7 раз больше,
чем в плазме. Нефротоксическое действие:
гентамицин>амикацин>канамицин>тобрамицин>
стрептомицин> нетилмицин.
• При быстром внутривенном или внутриполостном
введении (дети, пожилые лица) – нервномышечная блокада (снижение высвобождения АЦХ
в нервно-мышечных синапсах и частичная блокада
постсинаптических рецепторов): нарушение дыхания
95. ТЕТРАЦИКЛИНЫ
• Структурная основа - 4 конденсированных 6членных цикла• Продуценты различных видов Streptomyces.
• 1-й препарат данной группы –
хлортетрациклин – 1948 г.
96. ТЕТРАЦИКЛИНЫ
1. Природные:• Тетрациклин
2. Полусинтетические
Метациклин
Доксициклин
Миноциклин
97. ТЕТРАЦИКЛИНЫ
Связываются с рецепторами 30Sсубъединицы бактериальной рибосомы,
блокируя связывание аминоцил-тРНК с
акцепторным участком рибосомальноматричного комплекса
За счет пассивной диффузии и
энергозависимого транспорта проникают
внутрь клеток человека (действуют на
внутриклеточных микробов)
Эффект: Бактериостатический
98. Средства первой линии
1. Особо опасные инфекции (холера, чума,сибирская язва, бруцеллез, туляремия)
2. Риккетсиозы (сыпной тиф, пятнистая
лихорадка скалистых гор, лихорадка Ку)
3. Боррелиозы (возвратный тиф, лаймская
болезнь)
4. Хламидиоз и хламидиозные артриты
4.
Микоплазменные инфекции
99. ФАРМАКОКИНЕТИКА ТЕТРАЦИКЛИНОВ
• Биодоступность тетрациклина 50% исущественно снижается пищей, содержащие
молочные продукты. Т1/2 =8 ч
• Биодоступность доксициклина, миноциклина
=75 -90% и не зависит от приема пищи. Т1/2 =
24 ч
• Создают высокие концентрации): легкие,
печень, почки, синовиальная жидкость,
предстательная железа. Плохо проникают
через ГЭБ.
100. Побочные эффекты тетрациклинов
• Диспептические нарушения: анорексиятошнота, рвота, диарея (раздражающее
действие)
• При длительном применение- повреждение
слизистой ЖКТ (стоматит, глоссит,
эрозивный гастрит, энтероколит)
• Транзиторное повышение активности
печеночных трансаминаз (тетрациклин)
• Образование прочных соединений с Са в
костях и зубах детей – задержка роста
костей и формирования зубов, нарушение
развития и окраски зубной эмали.
(накапливаются в зубной и костной ткани)
101. Побочные эффекты тетрациклинов
• Подавление сапрофитной микрофлорыкандидомикоз,суперинфекция
стафилококками (стафилококковый
энтероколит и пневмония)
• Фотосенсибилизация
• Гемолитическая анемия, тромбоцитопения,
нейтропения
• Аллергические реакции
102. МАКРОЛИДЫ
• Основа химической структуры –макроциклическое лактонное кольцо. В
зависимости от количества атомов углерода
в кольце выделяют 14, 15 И 16 ЧЛЕННЫЕ
МАКРОЛИДЫ
• Эритромицин – обнаружен в 1952 г. в
продуктах метаболизма Streptomyces
erythreus, выделен из проб почвы, взятой на
Филлипинах
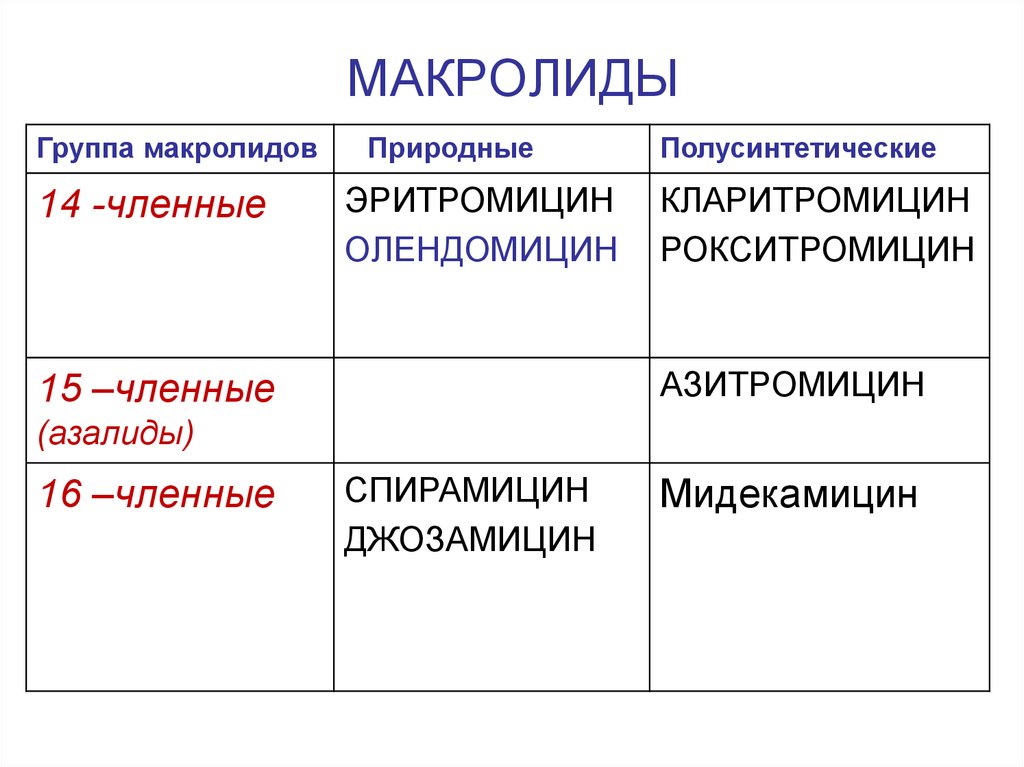
103. МАКРОЛИДЫ
Группа макролидов14 -членные
Природные
ЭРИТРОМИЦИН
ОЛЕНДОМИЦИН
Полусинтетические
КЛАРИТРОМИЦИН
РОКСИТРОМИЦИН
АЗИТРОМИЦИН
15 –членные
(азалиды)
16 –членные
СПИРАМИЦИН
ДЖОЗАМИЦИН
Мидекамицин
104.
АНТИБАКТЕРИАЛЬНАЯ АКТИВНОСТЬМеханизм действия
Нарушение синтеза белка рибосомами микробной клетки.
Макролиды связываются с каталитическим центром
рибосомальной 50S-субъединицы, ингибируют реакции
транслокации и транспептидации (образование пептидных
связей) > торможение синтеза белка на рибосомах >
угнетение роста бактерий.
Эффект
Бактериостатическое действие, но в высоких концентрациях
способны действовать бактерицидно на β-гемолитический
стрептококк группы А, пневмококк, возбудителя коклюша и
дифтерии (высокие концентрации, низкая микробная
обсемененность).
105. МАКРОЛИДЫ
– Для макролидов характерен постантибиотический эффект,т.е.
персистирующее
ингибирование
жизнидеятельности бактерий после их
кратковременного контакта с
антибиотиком: результат необратимых
изменений в рибосомах, следствием
которых является стойкий блок процесса
транслокации.
106. МАКРОЛИДЫ
– Оказывают также иммуномодулирующее ипротивовоспалительное действие.
Способны регулировать такие функции
нейтрофилов как фагоцитоз, хемотаксис,
киллинг.
– 14-членные макролиды ингибируют
окислительный «взрыв», уменьшая
образование агрессивных кислородных
радикалов, способных повреждать не
только бактериальные, но и собственные
клетки
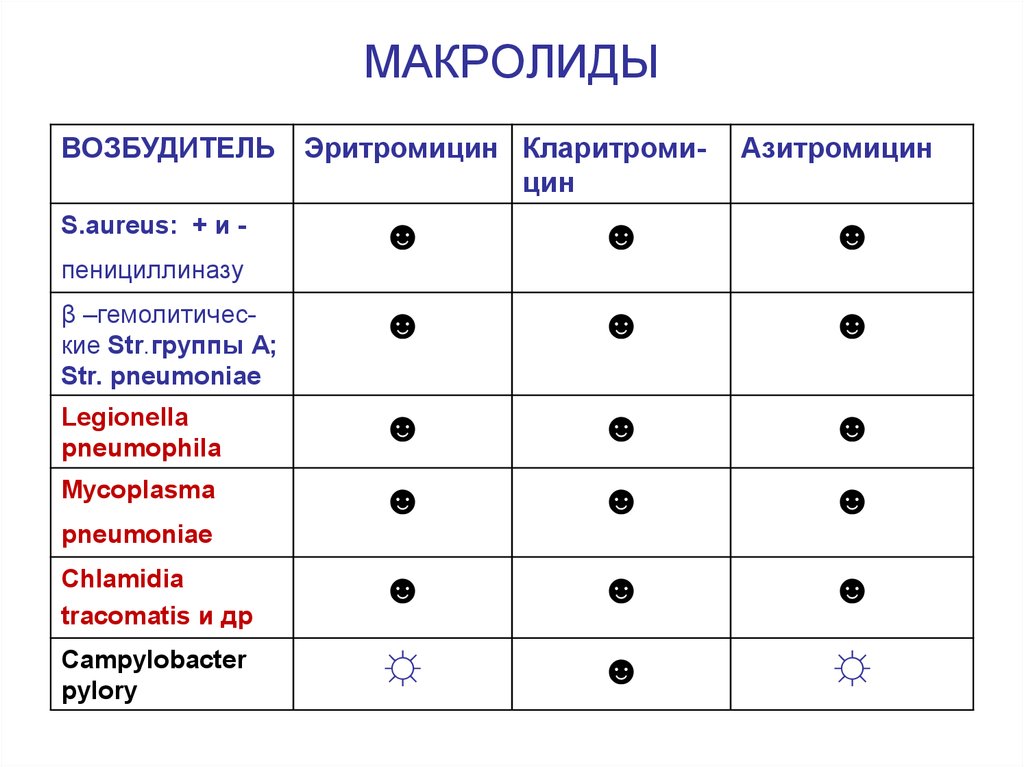
107. МАКРОЛИДЫ
ВОЗБУДИТЕЛЬ Эритромицин КларитромицинS.aureus: + и -
Азитромицин
☻
☻
☻
β –гемолитические Str.группы А;
Str. pneumoniae
☻
☻
☻
Legionella
pneumophila
☻
☻
☻
Mycoplasma
☻
☻
☻
Chlamidia
tracomatis и др
☻
☻
☻
Campylobacter
pylory
☼
☻
☼
пенициллиназу
pneumoniae
108. ФАРМАКОКИНЕТИКА МАКРОЛИДОВ
• Хорошо проникают в ткани: миндалины,среднее ухо, придаточные пазухи носа
легкие, бронхолегочный секрет, лимфатические узлы, органы малого таза, включая
предстательную железу.
• По способности проходить гисто-гематические барьеры (кроме ГЭБ) превосходят
другие АБ (бета-лактамы, аминогликозиды)
Концентрация в в ряде органов в 1.5-3 раза
и более выше, чем в плазме крови
109. ФАРМАКОКИНЕТИКА МАКРОЛИДОВ
• Эффективное проникновение черезклеточные мембраны. Особенно это
относится к фагоцитам, которые накапливают
в себе АБ и выступают для него в качестве
транспортной системы.
• Наиболее высокая внутриклеточная
концентрация характерна для азитромицина:
в альвеолярных макрофагах и моноцитах
периферической крови его концентрация в
50-70 раз больше, чем в сыворотке крови
110. ПРИМЕНЕНИЕ МАКРОЛИДОВ
• Инфекции дыхательных путей и ЛОР-отранов(фарингит, синусит, тонзиллит, бронхит,
внебольничная пневмония, включая легионелезную и
микоплазменную пневмонии
• Инфекционные заболевания кожи и мягких тканей,
вызываемая стафилококками (рожистое воспаление,
пиодермия, фурункулез и т.п.)
• Заболевания, передающиеся половым путем (
гонорея, хламидиоз, инфекции, вызванные
уреаплазмой, сифилис –кроме нейросифилиса)
• Заболевания ЖКТ, ассоциированные с H.pilory
111. ПОБОЧНЫЕ ЭФФЕКТЫ МАКРОЛИДОВ
• Одна из наиболее безопасных групп АБ• Диспептические нарушения (тошнота, боли в
животе, диарея): эритромицин > рокситромицин >кларитромицин> азитромицин
(прокинетический эффект ч/з мотилиновые
рецепторы)
• Транзиторное повышение активности
печеночных трансаминаз, холестатический
гепатит (при длительном применении)
• Аллергические реакции редко (0.5% пациентов)
• При в/в введении- флебиты; кларитромицин в
высоких дозах- обратимое нарушение слуха,
головная боль, головокружение.
112. Хлорамфеникол
• Вырабатывается Streptomyces venezuelae• Выделен в 1947 г. из проб почвы, взятой в
Венесуэле
• В 1948 г. стал доступен для широкого
применения
• К 1950 г. – доказаны возможность вызывать
тяжелые (смертельные) нарушения
кроветворения
• Ограничения клинического применения
(невозможно лечение более безопасными
АБ: резистентность, аллергические
реакции)
113. АБ группы ЛЕВОМИЦЕТИНА (хлорамфеникола)
• Левомицетин основание для приемавнутрь
• Левомицетина сукцинат для в/в и в/м
введения
• Синтомицин –смесь L и D- изомеров для
местного применения.
В РФ зарегистрировано ряд
комбинированных левомицетин содержащих
препаратов для местного применения:
синтомицина линимент и т.д.
114. ЛЕВОМИЦЕТИН
• Оказывает бактериостатическое действие,угнетая синтез белка рибосомами
• Связывается с пептидил- трансферазным
центром рибосомальной 50 S-cубъединицы (в
месте отличном от макролидов) и вызывает
отщепление комплекса пептидил – тРНК
рибосомы.
(бактериоцидный на Haemophilus типа b,
пневмококки, N. meningitidis )
115. ЛЕВОМИЦЕТИН
• Пневмококки (кроме пенициллинрезистентных), менингококки, Haemophilusinfluenzae (в том числе ампициллинрезистертные штаммы), менингококки,
риккетсии (лихорадка Ку, пятнистая
лихорадка скалистых гор, сыпной тиф),
сальмонеллы (генерализованный формы,
брюшной тиф)
• Антианаэробная активность: клостридии,
анаэробные кокки (пептококки ) и бактероиды,
включая Bacteroides fragilis, Fusobacterium.
вызывающие тяжелые инфекции брюшной
полости и абсцессы головного мозга (редко,
есть более безопасные и не менее эффективные АБ)
116. Показания
АБСОЛЮТНЫЕ• Бактериальный менингит (Haemophilus типа b,
пневмококки, N. meningitis ) у пациентов с
иммунодефицитом
• Абсцесс мозга
• Системный сальмонеллез ( тифозная лихорадка)
– 92% штаммов сальмонелл чувствительны
ОТНОСИТЕЛЬНЫЕ
• Риккетсиозы
• Дизентирия, бруцеллез, туляремия
• При анафилактической реакции на беталактамные антибиотики
• При терминальной почечной недостаточности
(90% метаболизма в печени с образованием
неактивного водорастворимого метаболита)
117. ЛЕВОМИЦЕТИН
• Наибольшая опасность –угнетение
кроветворения вплоть до апластической
анемии с необратимым течением (отсюда
рекомендации –не применять у детей до 12
лет).
• Нейротоксическое действие (спутанность
сознания, зрительные и слуховые
галлюцинации- 3-5% ; очень редко- неврит
зрительного нерва)
• Диспептические нарушения (при приеме
внутрь)
• Дисбактериоз, суперинфекция
• Аллергические реакции- сравнительно редко.
118. ЛЕВОМИЦЕТИН
• У детей первых 4-х недель жизни – толькопо жизненным показаниям – летальный у 4060% детей так называемый «серый синдром»
(серая окраска кожи) – следствие
токсического действия неметаболизированного левомицетина:
• токсические концентрации – тяжелая
гипоксия тканей и метаболический ацидоз с
последующим развитием коллапса,
нарушением дыхания
119. ЛИНКОЗАМИДЫ
• Линкомицин (природный антибиотик,выделенный из Streptomyces lincolnensis)
• Клиндамицин*
• * – полусинтетический хлорсодержащее производное
линкомицина. Отличается лучшими антибактериальными и
фармакокинетическими свойствами (лучше всасывается из
ЖКТ).
120. ЛИНКОЗАМИДЫ
• Оказывают бактериостатическое действие• Угнетают белковый синтез на 50S-субъединице бактериальной рибосомы.
• Блокируют образование полисомальных
функциональных комплексов и трансляцию
связанных с т-РНК аминокислот. Рецепторы
на 50S-субъединице (действие линкозамидов) близки к макролидным, что приводит к
конкуренции между этими группами АБ:
антагонизм при совместном применении и
перекрестная резистентность
121. ЛИНКОЗАМИДЫ
• Спектр противомикробной активности:грамположительные кокки: стафилококки,в
том числе продуцирующих пенициллиназу,
PRSA, некоторые внебольничные штамма
MRSA, стрептококки; анаэробы:
спорообразующие (Clostridium perfringens), и
неспоробразующие (пептококки,
фузобактерии, бактероиды, включая
большинство штаммов B. fragilis).
• Противомикробная активность клиндацицина
в отношении анаэробов в 4-8 раз превышает
активность линкомицина, в отношении
остальной флоры – у 2-5 раз
122. ЛИНКОЗАМИДЫ
• Хорошо проникают в различные ткани исреды организма, особенно в костную ткань
(40% от концентрации в крови). Плохо
проникают в СМЖ.
• Частично метаболизируются в печени,
вступая в печеночно-кишечную циркуляцию.
Время сохранения терапевтической
концентрации в крови 5-6 часов (кратность
приема взрослым обычно 3- 4 раза в сутки).
123. Нежелательные явления
• Со стороны пищеварительной системы: боль вживоте, тошнота, псевдомембранозный
энтероколит
• Со стороны органов кроветворения: лейкопения,
нейтропения, агранулоцитоз, тромбоцитопения.
• Со стороны ССС: при быстром в/в введении снижение АД, вплоть до коллапса.
• Аллергические реакции: редко.
124. Итоговая характеристика группы
• Бактериостатическое действие• Узкий спектр антибактериальной
активности: Гр(+) кокки и анаэробы
• Высокие концентрации в костях и суставах
• Плохое проникновение через ГЭБ
• Перекрестная устойчивость к обоим
препаратам
• Относительно частое развитие
псевдомембранозного колита
125. ПОЛИМИКСИНЫ
• ПОЛИМИКСИН В, Е (предназначены дляпарентерального введения:
• ПОЛИМИКСИН М (для приема внутрь, местно)
Открыты в 1947 г., циклические полипептиды,
синтезируемые спорообразующей палочкой Bacillus
polymixa.
• Механизм действия данного класса АБ
полипептидной структуры обусловлен их
способностью связываться
с
фосфолипидными компонентами мембран
бактериальных клеток. Они действуют
бактерицидно как катионные детергенты,
вызывая деструкцию клеточных мембран.
126. Спектр противомикробной активности
• Pseudomonas spp.Klebsiella spp.
Enterobacter spp.
Haemophilus
Yersinia
E. Coli
Shigella spp.
Salmonella spp.
Препараты резерва при лечении
инфекций, вызванных синегнойной
палочкой (при устойчивости к ЦФ,
карбапенемам, аминогликозидам,
фторхинолонам)
Вторичная резистентность развивается медленно
127. Устойчивость P.aeruginosa к антибиотикам (%) в 2010 г.
Полимиксин
ПИП/ТАЗО
Меропенем
Имипенем
Цефепим
Ципрофлоксацин
- 0%
- 15%
- 31%
- 48%
- 58%
- 75%
(С.В. Яковлев, 2010)
128. ПОЛИМИКСИНЫ
• Высокая нефро- и нейротоксичность.• При приеме внутрь, а также местно (кожа,
глаза, уши практически не всысывается)
129. Циклические липопептиды
• Даптомицин - выделен в 1985 году из почвенногомикроорганизма Streptomyces roseosporus (патент 1997 г.: США
– с 2003 г., Европа – с 2006 г., РФ – 2009 г.)
• Первый представитель новой группы АБ группы
циклических липопептидов
ПРОБЛЕМЫ: Появление Гр(+) резистентной флоры
130. Механизм действия даптомицина
• Молекула представляет собой циклическийлипопептид, состоящий из 13 аминокислотных
остатков, имеющий гидрофильное ядро и
гидрофобный «хвост». Последний посредством
кальций-зависимого механизма необратимо
связывается с клеточной мембраной грам(+)
бактерий.
1. Кальций зависимое связывание липофильного
«хвоста» с цитоплазматической мембраной
2. Олигомеризация и формирование ионных каналов
3. Выход ионов калия из клетки, приводящее к
деполяризации мембраны и гибели микробной
клетки
131. Спектр противосикробной активности
• Быстро проявляющееся бактерицидное действиев отношении широкого спектра грам(+)
возбудителей, включая MRSA, S.aureus
с промежуточной чувствительностью к ванкомицину,
ванкомицинорезистентный S.aureus и
ванкомицинорезистентные энтерококки.
• Осложненные инфекции кожи и мягких тканей у
взрослых;
• Бактериемия, вызванная Staphylococcus aureus,
включая установленный или предполагаемый
инфекционный эндокардит у взрослых.
132. Безопасность
• Гиперчувствительность (отдельные спонтанныесообщения), включая легочную эозинофилию, везикулезнобуллезную сыпь с вовлечением слизистых оболочек и
ощущением отёка ротоглотки, анафилаксия;
• Постинфузионные реакции, включающие тахикардию,
свистящее дыхание, лихорадку, озноб, системную гиперемию,
головокружение, обморок; металлический привкус во рту.
• Повышение активности трансаминаз, исчезающее после
прекращении терапии препаратом.
• Рабдомиолиз отмечался у пациентов с ранее существовавшей
почечной недостаточностью или при одновременном
применении препарата с лекарственными препаратами,
вызывающими рабдомиолиз



























































































































 medicine
medicine








