Similar presentations:
Биоэнергетические функции митохондрий
1. Владимиров Юрий Андреевич
Заведующий кафедрой биофизикиРоссийского Медицинского Университета
Биоэнергетические
функции
митохондрий
Москва 2002
2. Биоэнергетические функции митохондрий
Две главные биоэнергетическиефункции митохондрий
1. Окислительное фосфорилирование
– Дыхательная цепь
– Хемоосмотическая теория
окислительного фосфорилирования
2. Транспорт ионов
– Накопление ионов кальция
– Набухание митохондрий
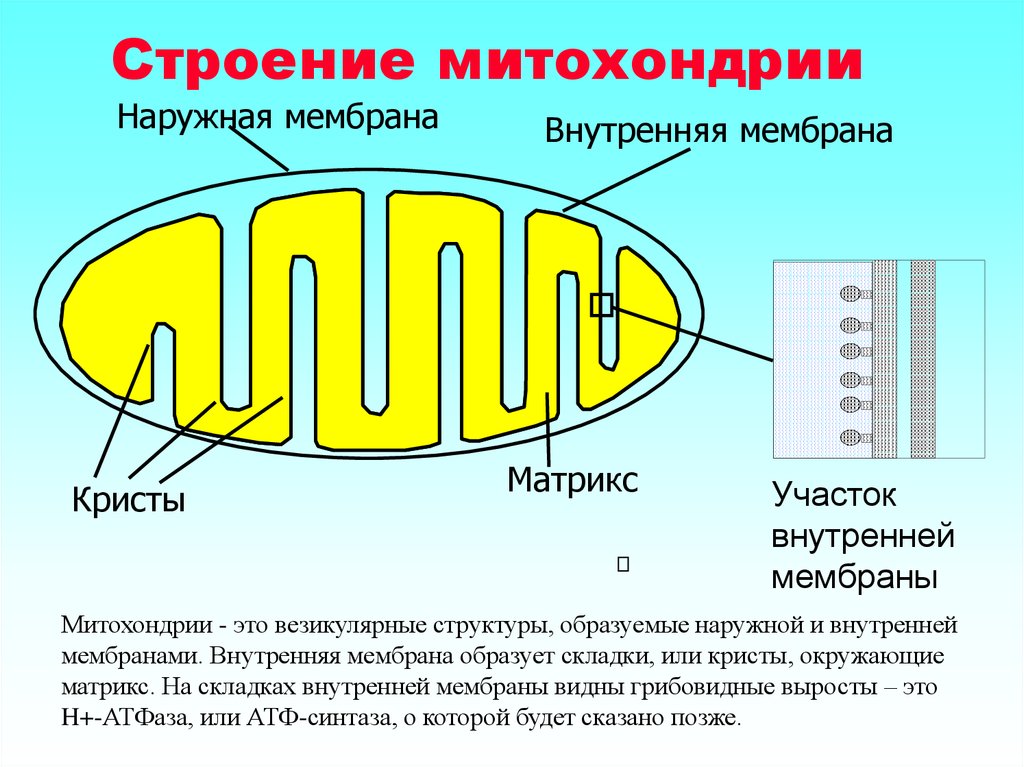
3. Строение митохондрии
Наружная мембранаКристы
Внутренняя мембрана
Матрикс
Участок
внутренней
мембраны
Митохондрии - это везикулярные структуры, образуемые наружной и внутренней
мембранами. Внутренняя мембрана образует складки, или кристы, окружающие
матрикс. На складках внутренней мембраны видны грибовидные выросты – это
H+-АТФаза, или АТФ-синтаза, о которой будет сказано позже.
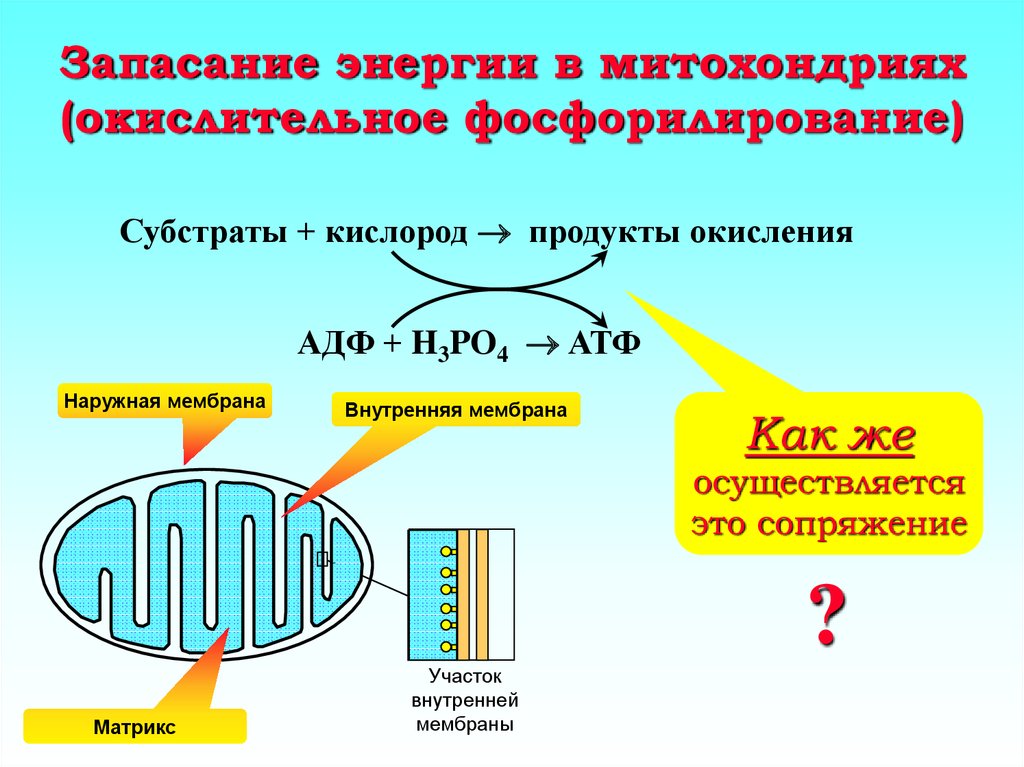
4. Запасание энергии в митохондриях (окислительное фосфорилирование)
Субстраты + кислород продукты окисленияАДФ + H3PO4 АТФ
Наружная мембрана
Внутренняя мембрана
Как же
осуществляется
это сопряжение
?
Матрикс
Участок
внутренней
мембраны
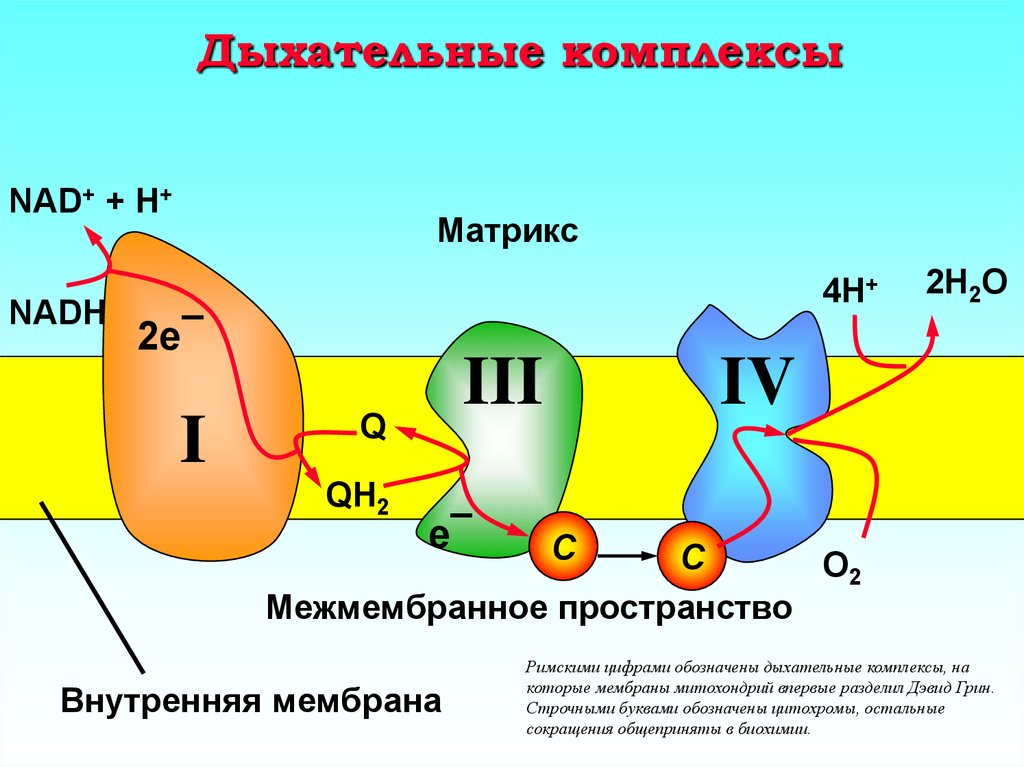
5. Дыхательные комплексы
NAD+ + H+NADH
Матрикс
4H+
2e¯
I
III
II
Q
QH2
e¯
2H2O
IV
C
C
O2
Межмембранное пространство
Внутренняя мембрана
Римскими цифрами обозначены дыхательные комплексы, на
которые мембраны митохондрий впервые разделил Дэвид Грин.
Строчными буквами обозначены цитохромы, остальные
сокращения общеприняты в биохимии.
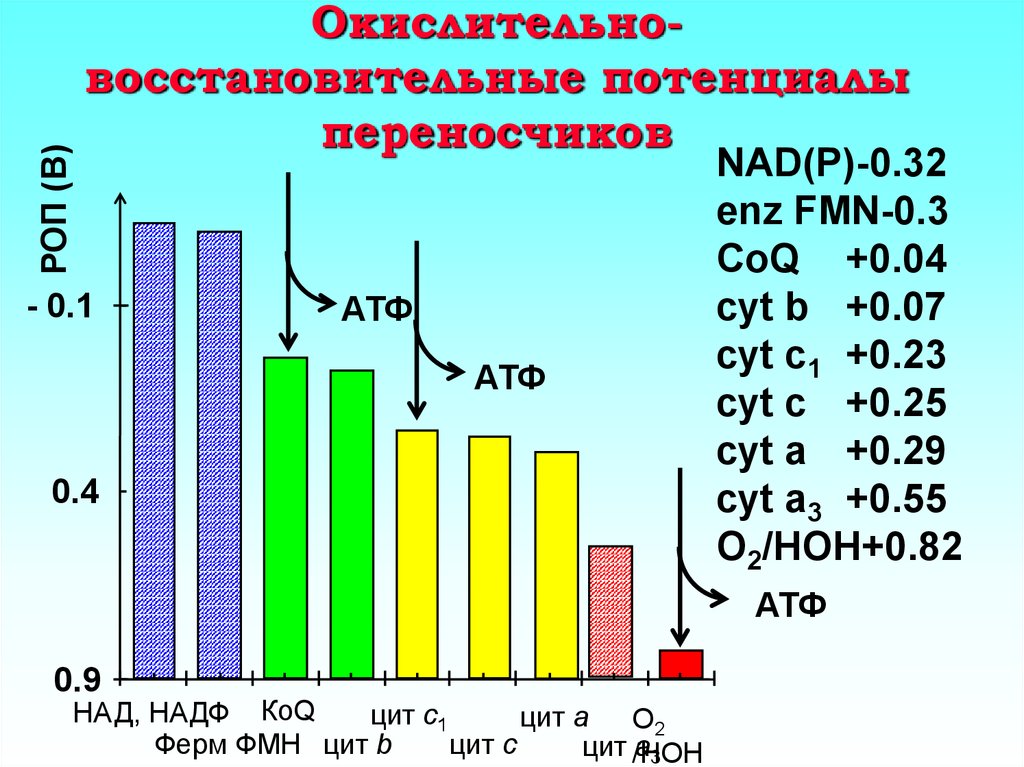
6. Окислительно-восстановительные потенциалы переносчиков
РОП (В)Окислительновосстановительные потенциалы
переносчиков
- 0.1
АТФ
АТФ
0.4
NAD(P)-0.32
enz FMN-0.3
CoQ +0.04
cyt b +0.07
cyt c1 +0.23
cyt c +0.25
cyt a +0.29
cyt a3 +0.55
O2/HOH+0.82
АТФ
0.9
НАД, НАДФ КоQ
цит c1
цит a
O2
Ферм ФМН цит b
цит c
цит /HOH
a3
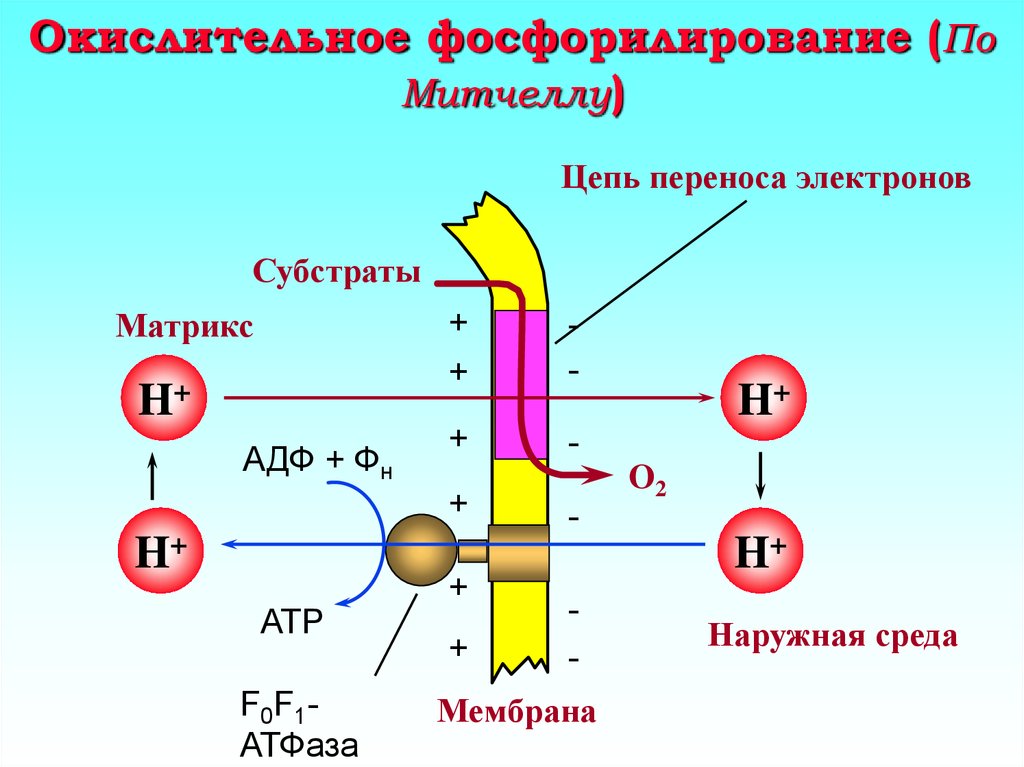
7. Окислительное фосфорилирование (По Митчеллу)
Цепь переноса электроновСубстраты
Матрикс
H+
АДФ + Фн
+
+
-
+
-
+
H+
+
ATP
F0F1АТФаза
+
H+
O2
-
-
Мембрана
H+
Наружная среда
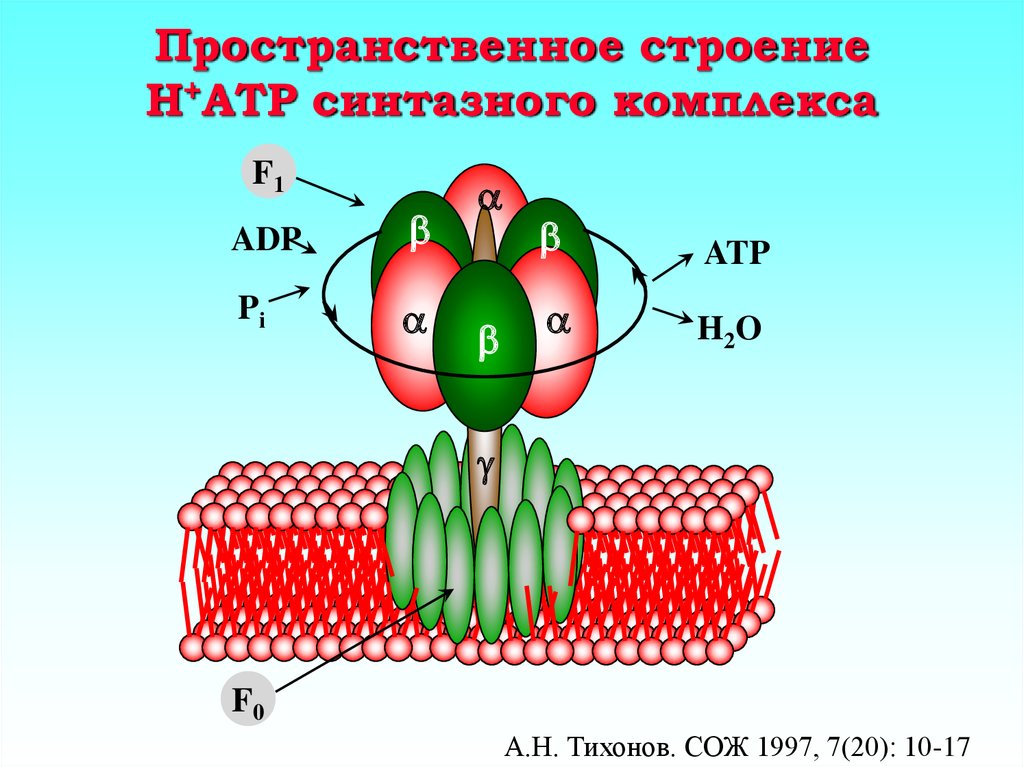
8. Пространственное строение H+ATP синтазного комплекса
F1ADP
b
Pi
a
a
b
b
ATP
a
H2O
g
F0
А.Н. Тихонов. СОЖ 1997, 7(20): 10-17
9. Транспорт кальция и фосфата в митохондрии
2+Ca
H3PO4
10. Протон-движущая сила (PMF)
Энергия одного моля иона в данной среде называется электрохимическимпотенциалом. Разность электрохимических потенциалов протона между двумя
водными фазами внутри и вне митохондрий описывается уравнением:
H
[H ] o
RT ln
F
[H ]i
Где R – газовая постоянная, T – абсолютная температура, [H+]o и [H+]i – концентрации
ионов водорода вне и внутри матрикса, соответственно, F – число Фарадея, разность потенциалов между окружающей средой и матриксом.
Петер Митчелл в качестве единицы энергии использовал электрон-вольты, в
результате чего уравнение (1) несколько трансформируется:
PMF =
H
F
RT [H ] o
ln
F
[H ]i
11. Вклад в PMF DpH и Dj
Вклад в PMF pH иСуммарная энергия окислительно-восстановительной реакции,
превращенная в разность электрохимических потенциалов
ионов водорода, была названа П. Митчеллом протондвижущей силой (PMF - proton motive force), по аналогии с
электродвижущей силой в гальванической батарее.
Заменив натуральный логарифм десятичным, легко найти
величину протон-движущей силы, зная разность pH ( pH) и
разность потенциалов ( ) между средой и матриксом при
комнатной температуре; выраженная в милливольтах она будет
равна:
PMF (мВ) = 60 (мВ) pH +
В митохондриях основной вклад в эту сумму вносит
мембранный потенциал, который в присутствии субстрата
и кислорода составляет около 170-180 мВ.
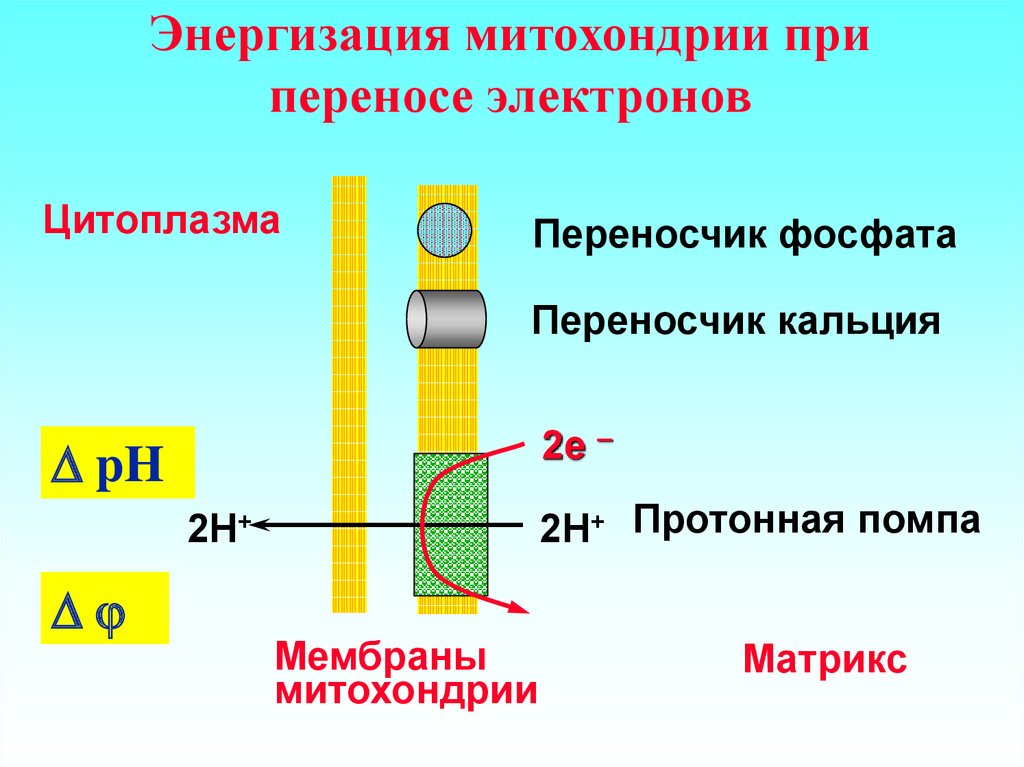
12. Энергизация митохондрии при переносе электронов
ЦитоплазмаПереносчик фосфата
Переносчик кальция
2e –
pH
2H+ Протонная помпа
2H+
Мембраны
митохондрии
Матрикс
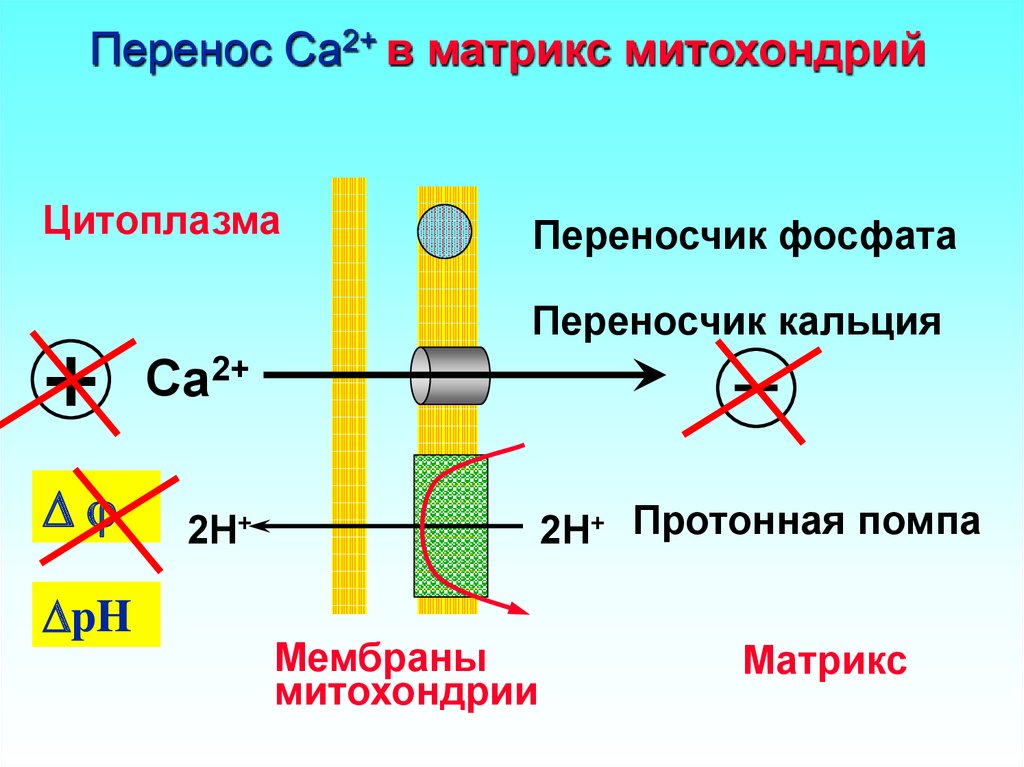
13. Перенос Ca2+ в матрикс митохондрий
ЦитоплазмаПереносчик фосфата
Переносчик кальция
+
pH
Ca2+
2H+ Протонная помпа
2H+
Мембраны
митохондрии
Матрикс
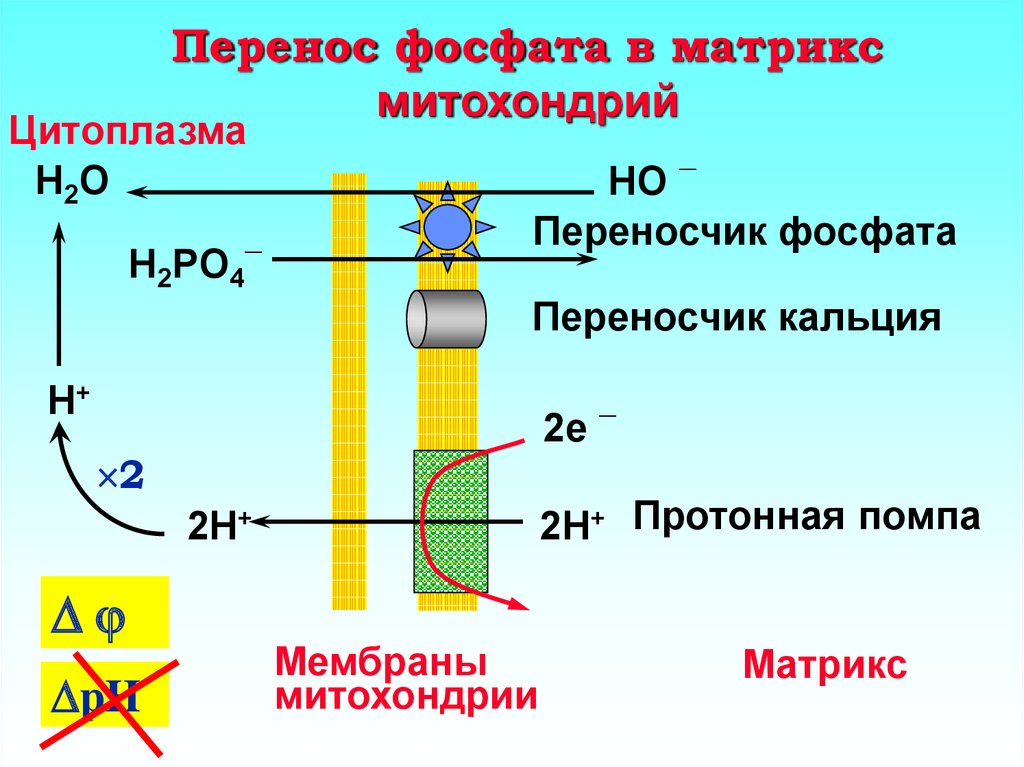
14. Перенос фосфата в матрикс митохондрий
ЦитоплазмаH2O
H2PO4¯
HO ¯
Переносчик фосфата
Переносчик кальция
H+
2e ¯
2
2H+ Протонная помпа
2H+
pH
Мембраны
митохондрии
Матрикс
15. Действие Ca2+ и Pi
Электрохимический потенциал протонаH
[H ] o
RT ln
F
[H ]i
+ Pi
+
2+
Ca
16. Дыхание митохондрий в разных функциональных состояниях
O2субстраты
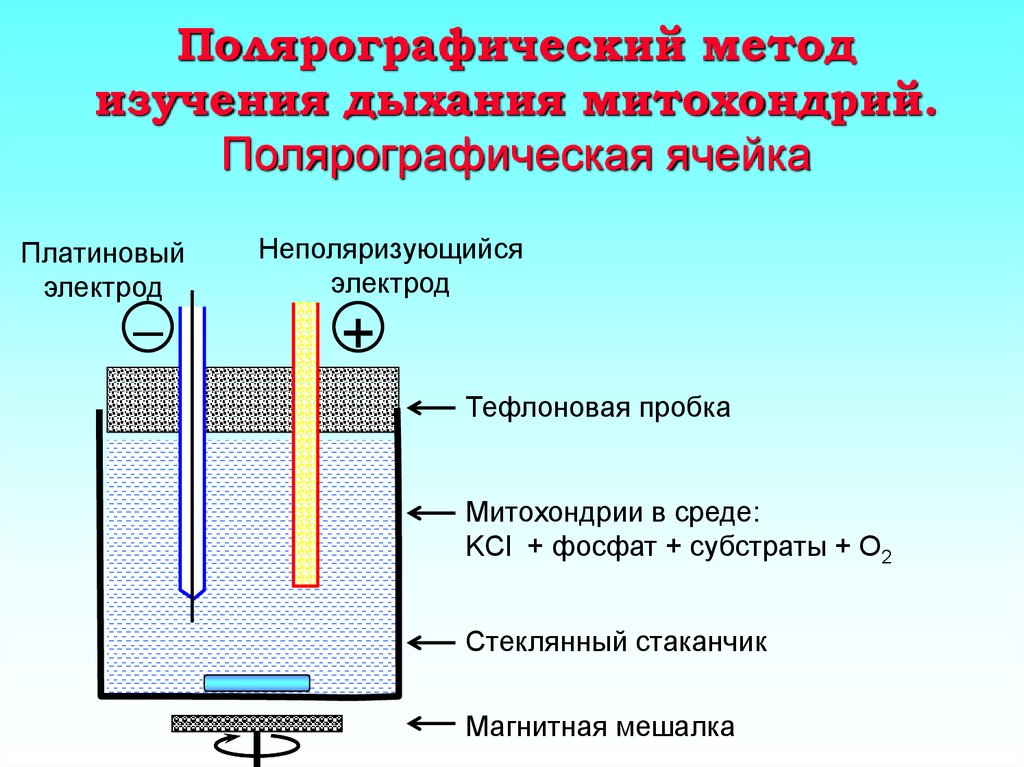
17. Полярографический метод изучения дыхания митохондрий. Полярографическая ячейка
Платиновыйэлектрод
–
Неполяризующийся
электрод
+
Тефлоновая пробка
Митохондрии в среде:
KCl + фосфат + субстраты + O2
Стеклянный стаканчик
Магнитная мешалка
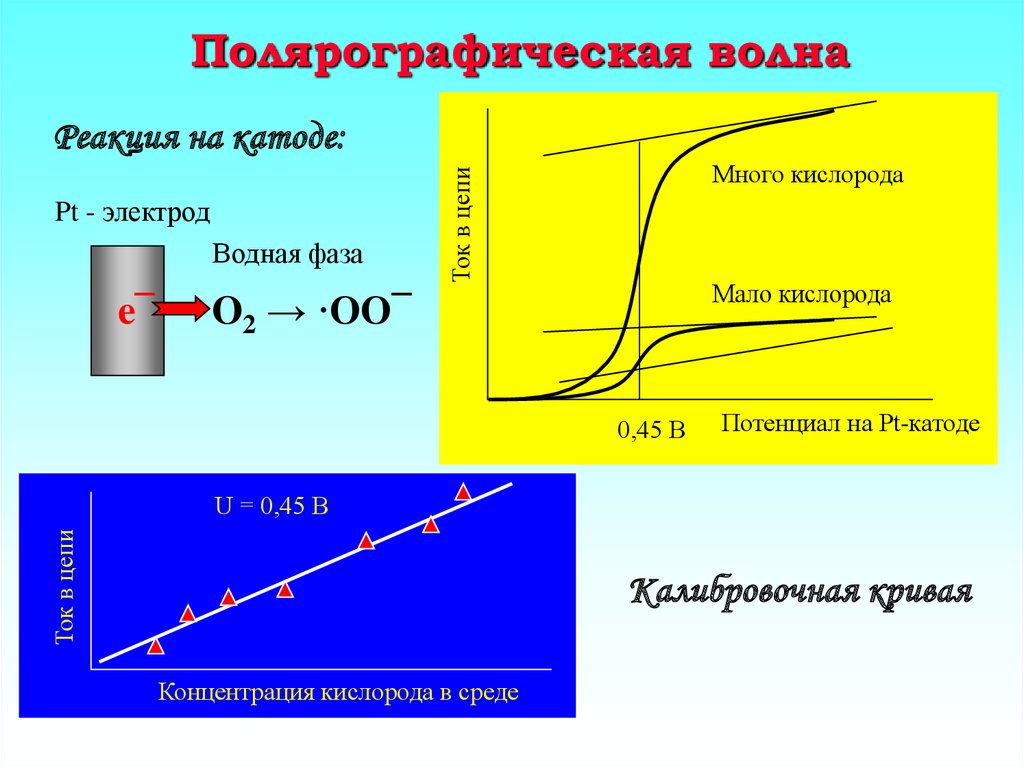
18. Полярографическая волна
Реакция на катоде:Водная фаза
e¯
Ток в цепи
Pt - электрод
Много кислорода
Мало кислорода
O2 → ·OO¯
0,45 В
Потенциал на Pt-катоде
Ток в цепи
U = 0,45 В
Калибровочная кривая
Концентрация кислорода в среде
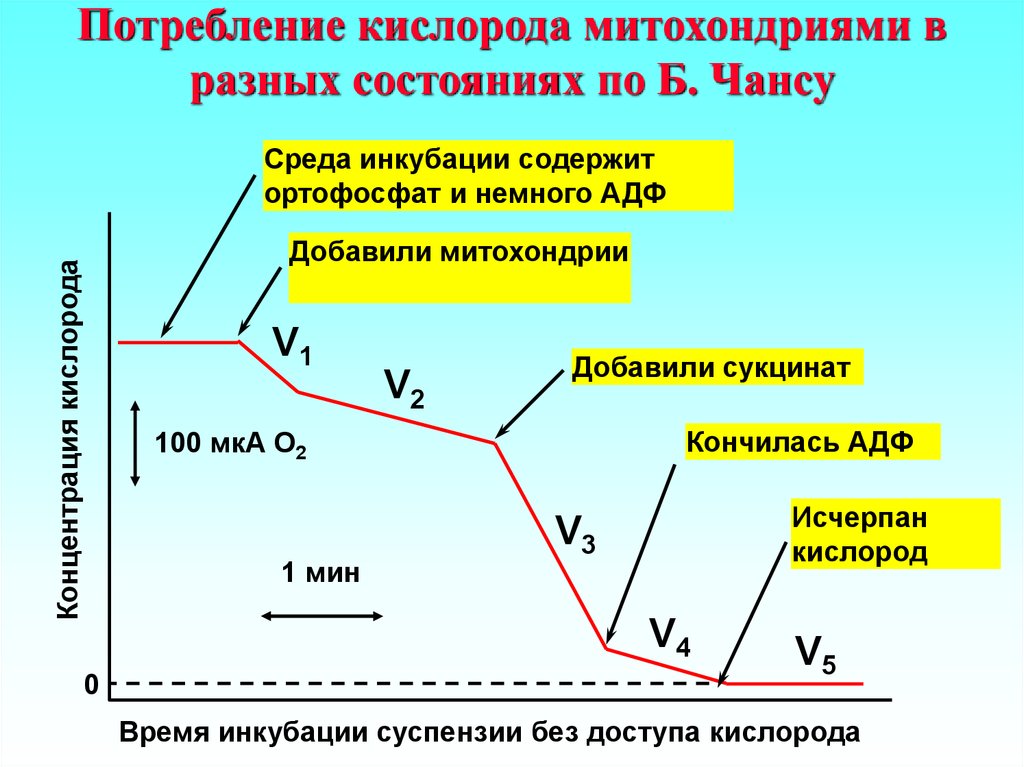
19. Потребление кислорода митохондриями в разных состояниях по Б. Чансу
Среда инкубации содержитортофосфат и немного АДФ
Концентрация кислорода
Добавили митохондрии
V1
V2
Добавили сукцинат
Кончилась АДФ
100 мкА О2
1 мин
Исчерпан
кислород
V3
V4
0
V5
Время инкубации суспензии без доступа кислорода
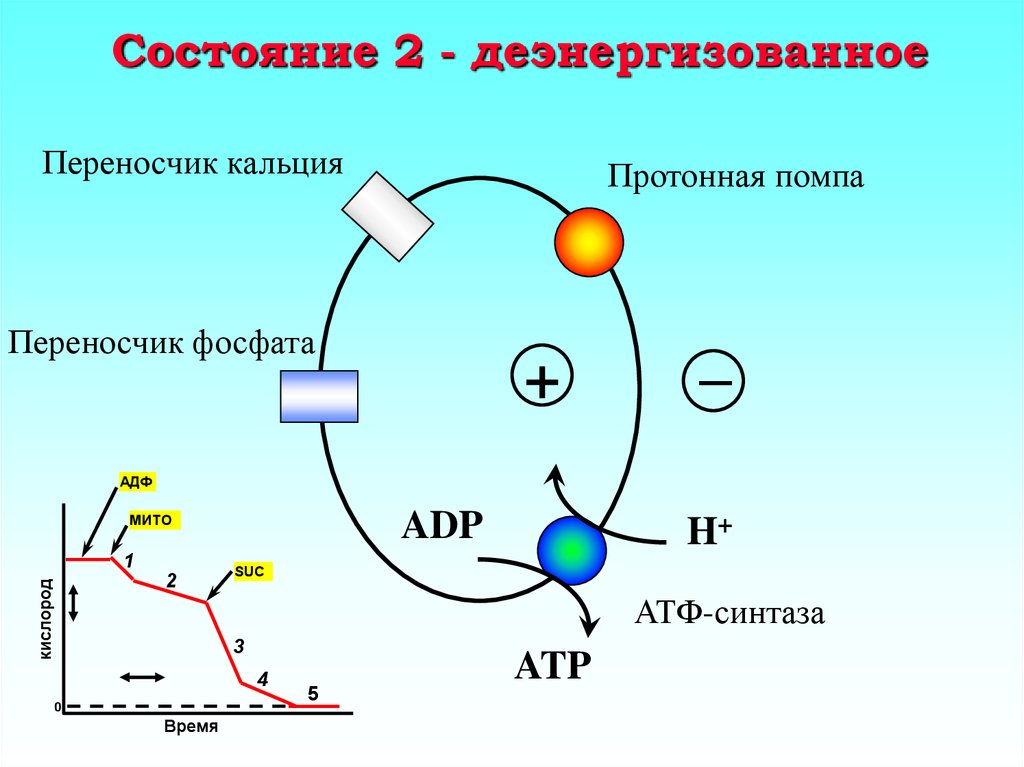
20. Состояние 2 - деэнергизованное
Переносчик кальцияПротонная помпа
Переносчик фосфата
+
–
АДФ
ADP
МИТО
кислород
1
2
H+
SUC
АТФ-синтаза
3
4
0
Время
5
ATP
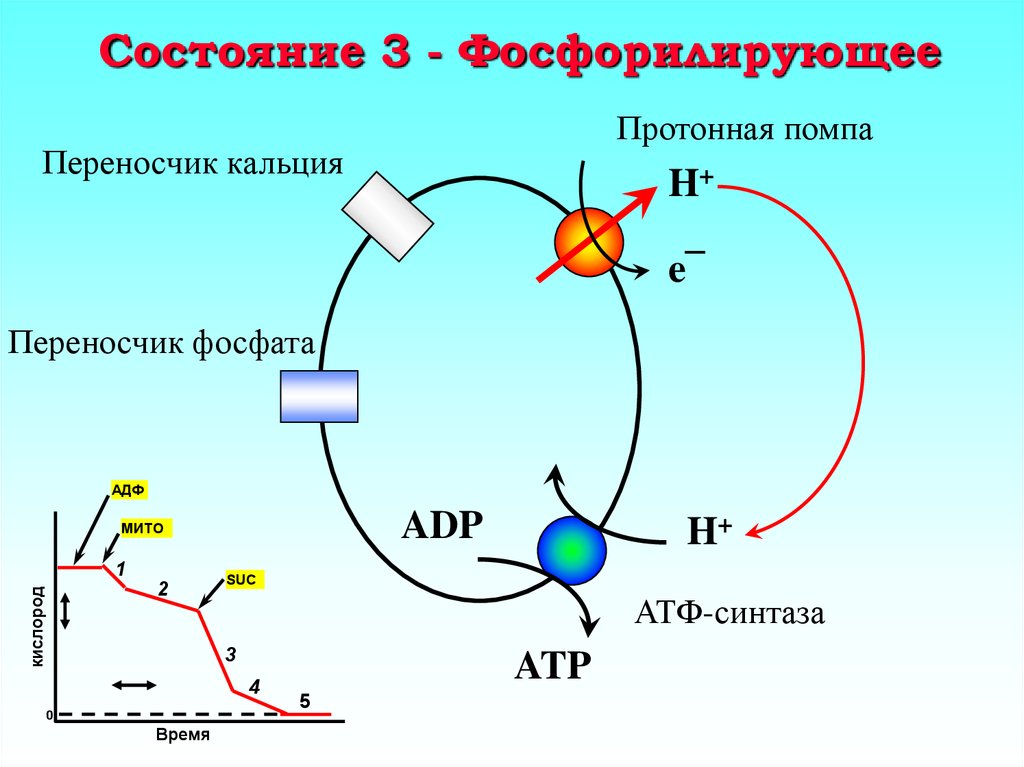
21. Состояние 3 - Фосфорилирующее
Протонная помпаПереносчик кальция
H+
e¯
Переносчик фосфата
АДФ
ADP
МИТО
кислород
1
2
SUC
АТФ-синтаза
3
4
0
Время
H+
ATP
5
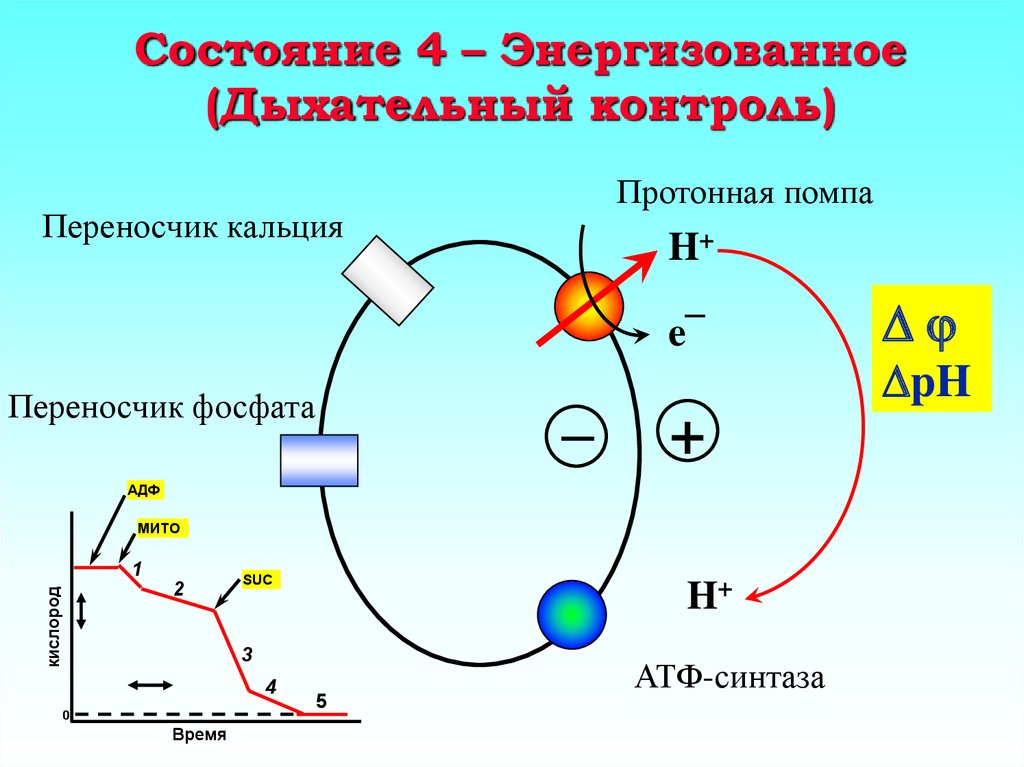
22. Состояние 4 – Энергизованное (Дыхательный контроль)
Протонная помпаПереносчик кальция
H+
e¯
Переносчик фосфата
–
+
АДФ
МИТО
кислород
1
2
SUC
H+
3
4
0
Время
5
АТФ-синтаза
pH
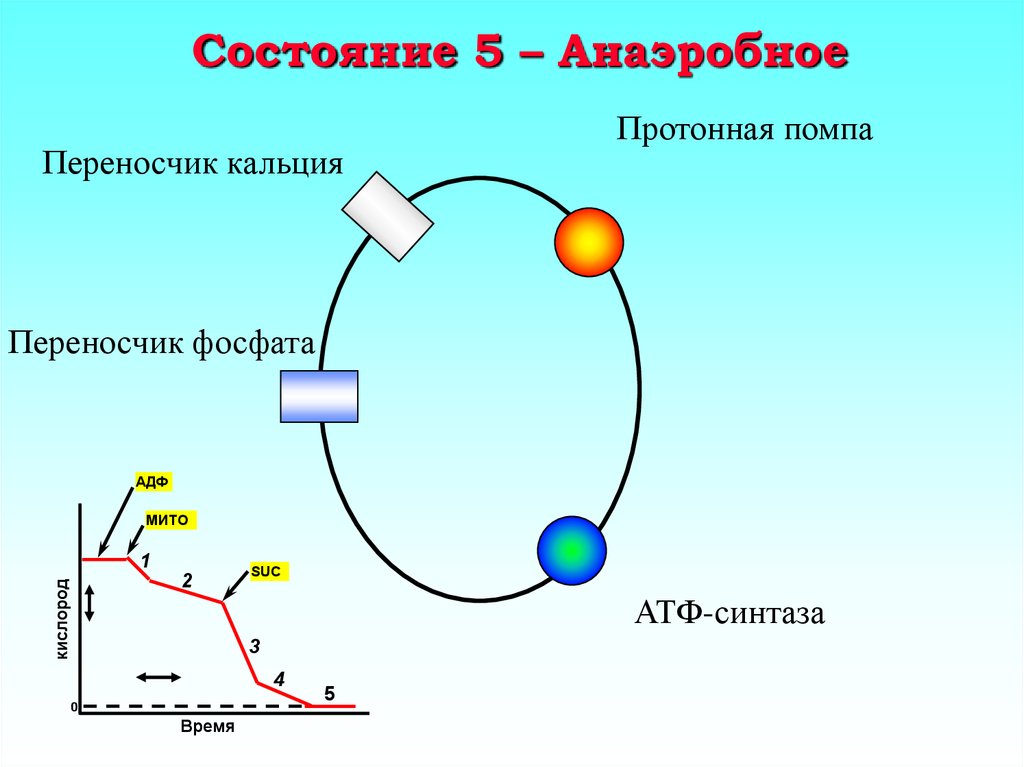
23. Состояние 5 – Анаэробное
Переносчик кальцияПротонная помпа
Переносчик фосфата
АДФ
МИТО
кислород
1
2
SUC
АТФ-синтаза
3
4
0
Время
5
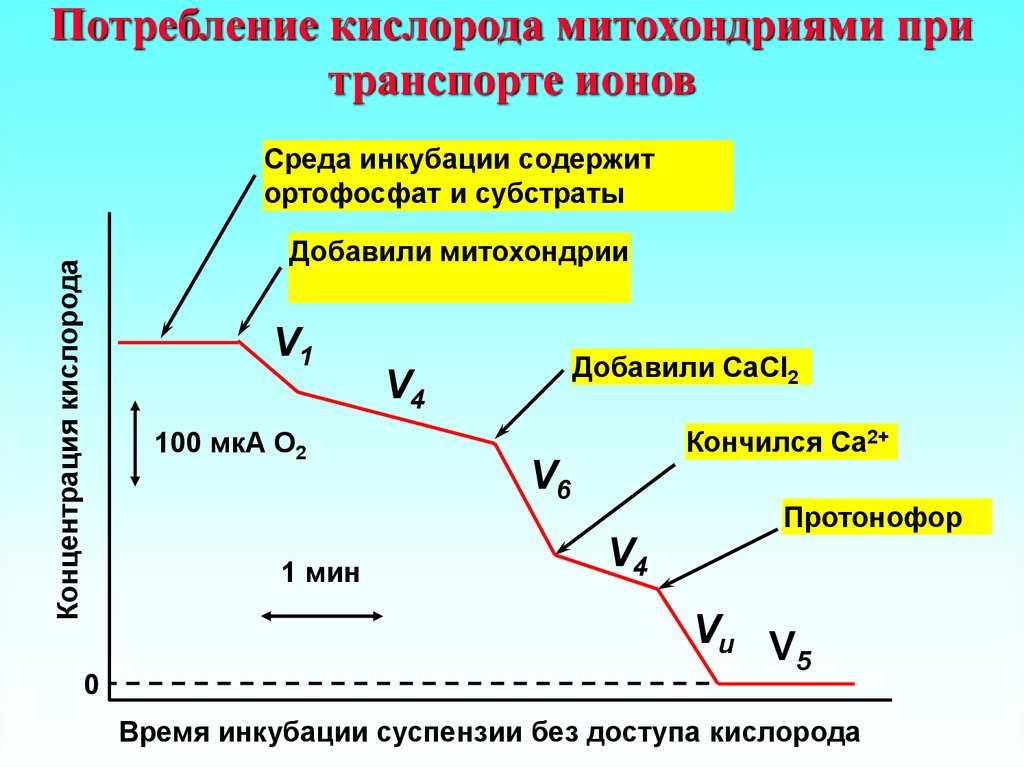
24. Потребление кислорода митохондриями при транспорте ионов
Среда инкубации содержитортофосфат и субстраты
Концентрация кислорода
Добавили митохондрии
V1
100 мкА О2
1 мин
0
Добавили CaCl2
V4
Кончился Ca2+
V6
Протонофор
V4
Vu V
5
Время инкубации суспензии без доступа кислорода
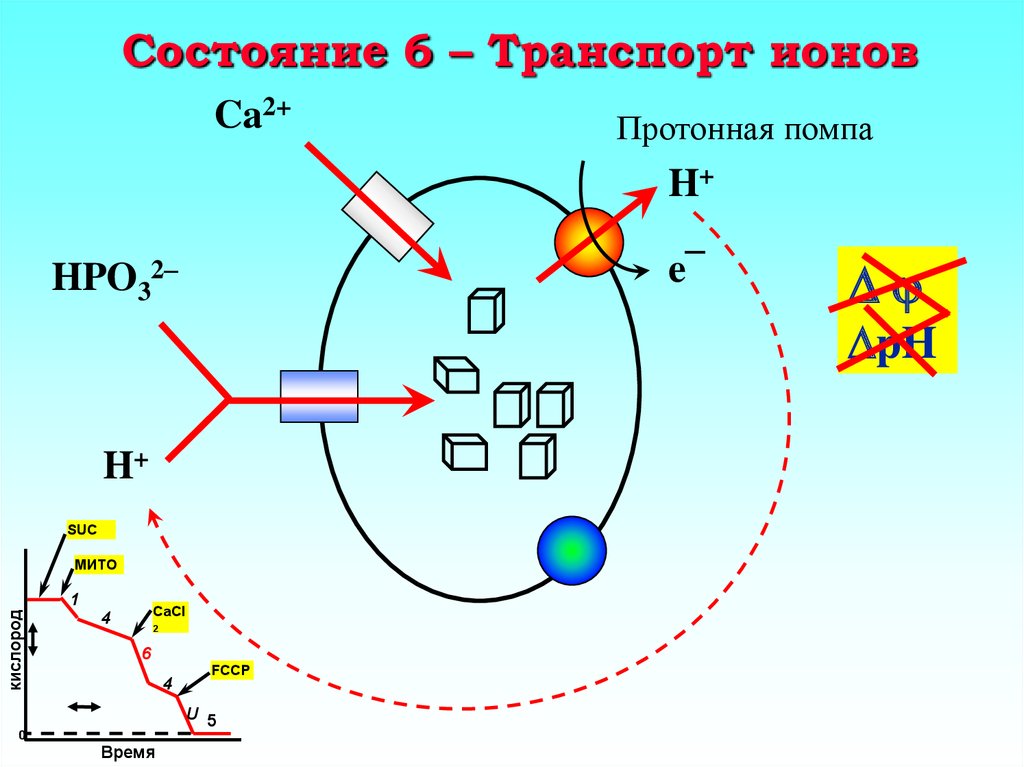
25. Состояние 6 – Транспорт ионов
Ca2+Протонная помпа
H+
e¯
HPO32–
pH
H+
SUC
МИТО
кислород
1
CaCl
4
2
6
4
FCCP
U 5
0
Время
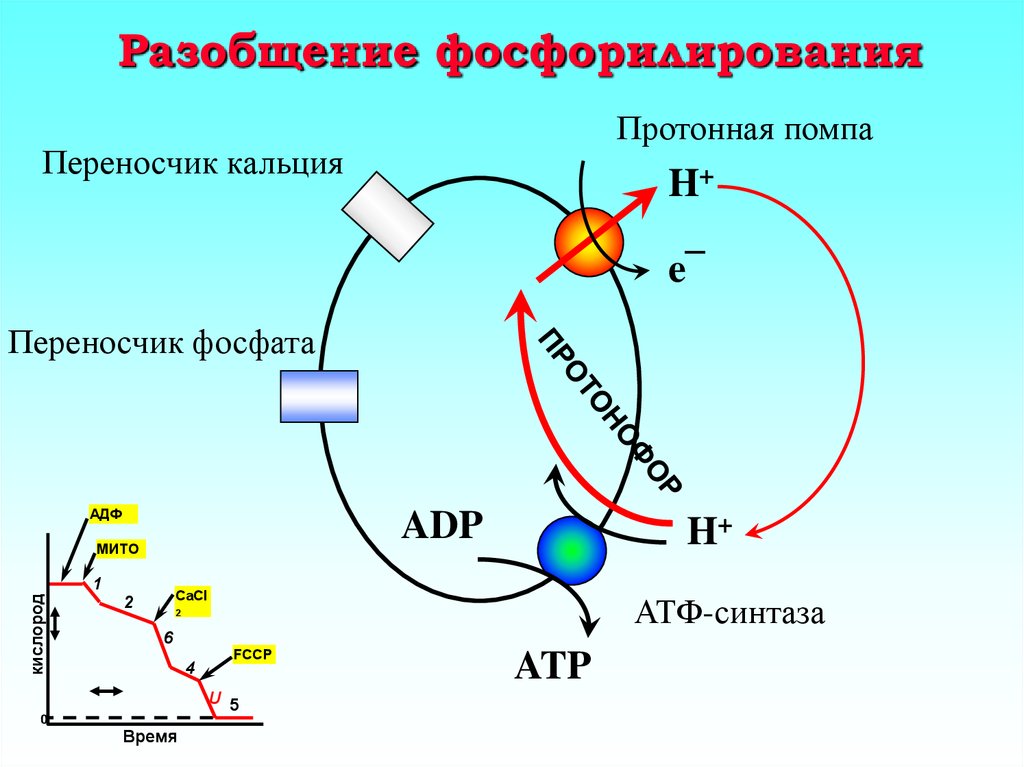
26. Разобщение фосфорилирования
Протонная помпаПереносчик кальция
H+
e¯
Переносчик фосфата
АДФ
ADP
МИТО
кислород
1
H+
CaCl
2
АТФ-синтаза
2
6
4
FCCP
U 5
0
Время
ATP
27. Состояние U - Разобщенное
Переносчик кальцияПротонная помпа
H+
e¯
Переносчик фосфата
АДФ
H+
МИТО
кислород
1
CaCl2
2
АТФ-синтаза
6
4
FCCP
U 5
0
Время
28. Характеристика функциональных состояний
Состояние2
3
4
5
6
U
Состав среды
инкубации
Название
состояния
Потенциал
на мембране
Состояние
переносчиков
электрона
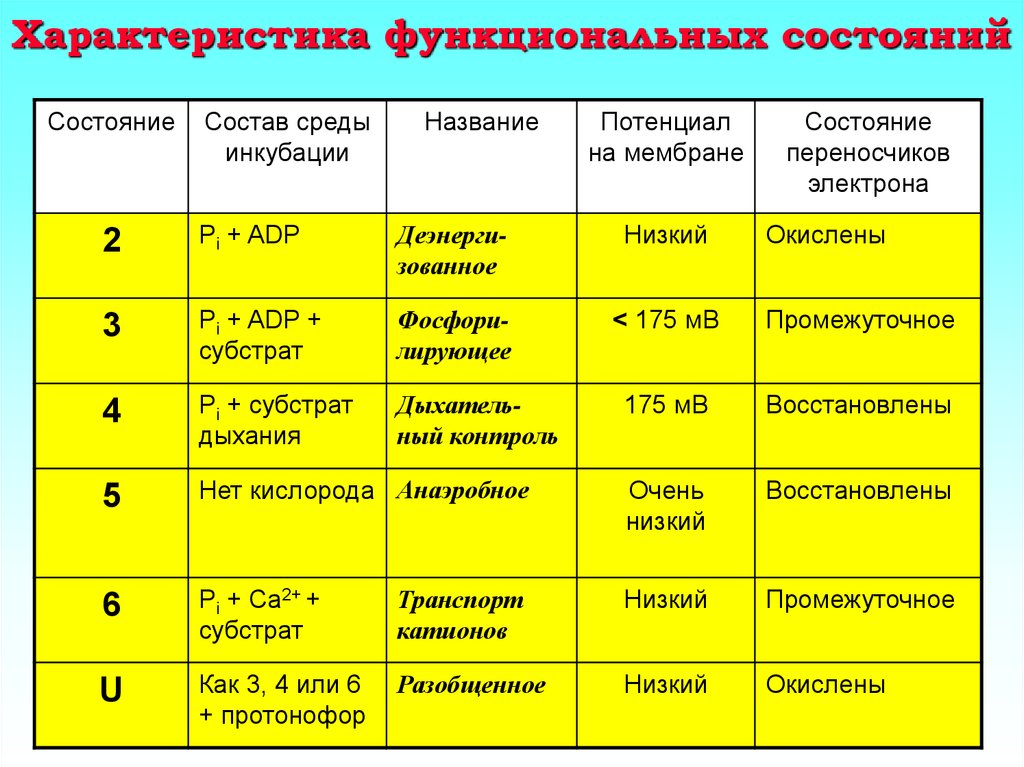
29. Характеристика функциональных состояний
СостояниеСостав среды
инкубации
Название
Потенциал
на мембране
Состояние
переносчиков
электрона
2
Pi + ADP
Деэнергизованное
Низкий
Окислены
3
Pi + ADP +
субстрат
Фосфорилирующее
< 175 мВ
Промежуточное
4
Pi + субстрат
дыхания
Дыхательный контроль
175 мВ
Восстановлены
5
Нет кислорода Анаэробное
Очень
низкий
Восстановлены
6
Pi + Ca2+ +
субстрат
Транспорт
катионов
Низкий
Промежуточное
U
Как 3, 4 или 6
+ протонофор
Разобщенное
Низкий
Окислены
30. Как по скорости дыхания митохондрий в разных состояниях можно судить о месте повреждения?
Состояние2
3
4
5
6
U
Нарушен
перенос
электронов
Повреждена
мембрана
Нарушен
транспорт
фосфата
Нарушен АТФАДФ обмен
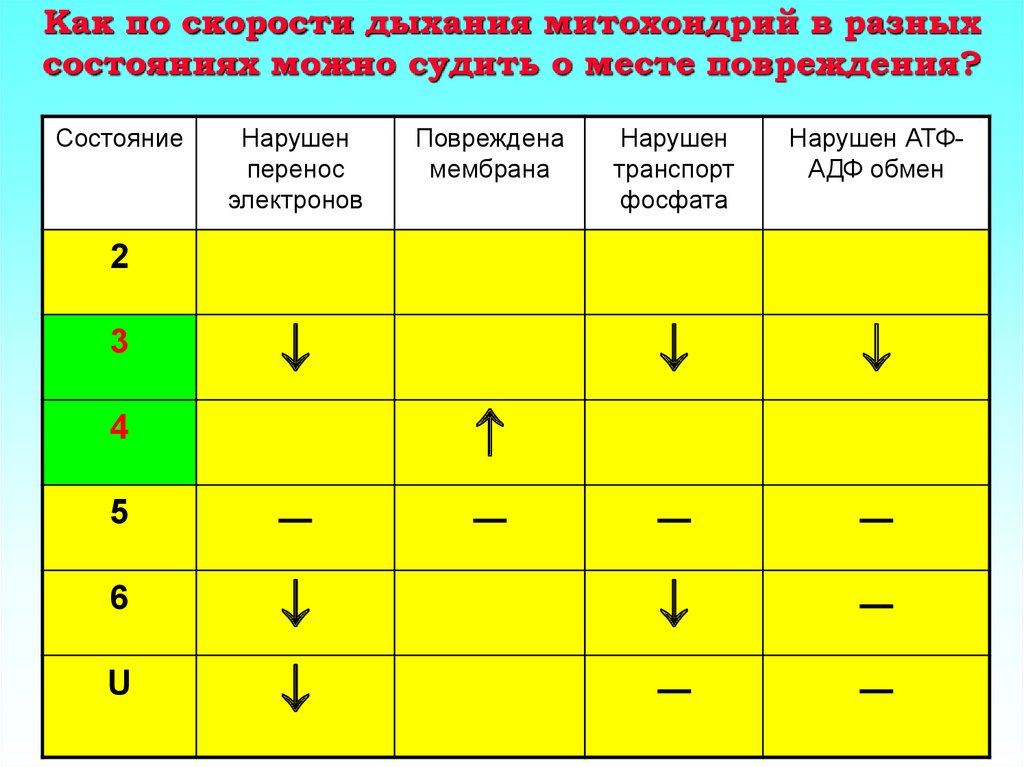
31. Как по скорости дыхания митохондрий в разных состояниях можно судить о месте повреждения?
СостояниеНарушен
перенос
электронов
Повреждена
мембрана
Нарушен
транспорт
фосфата
Нарушен АТФАДФ обмен
─
─
2
3
4
5
─
─
6
─
U
─
─
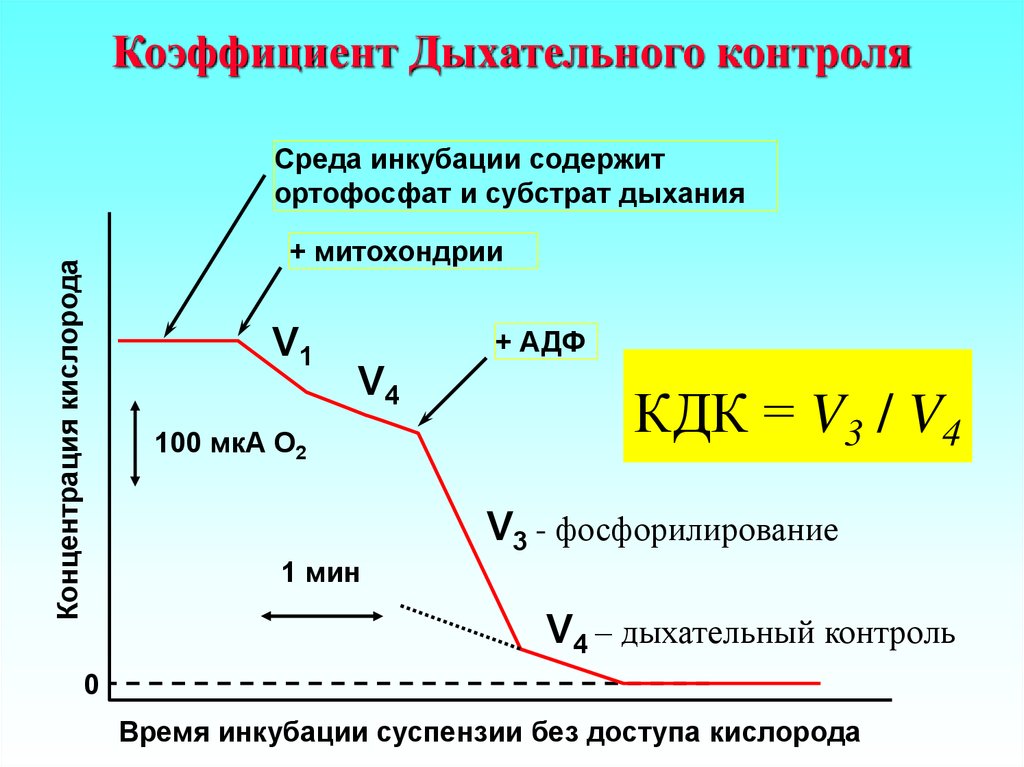
32. Коэффициент Дыхательного контроля
Среда инкубации содержитортофосфат и субстрат дыхания
Концентрация кислорода
+ митохондрии
V1
+ АДФ
V4
100 мкА О2
КДК = V3 / V4
V3 - фосфорилирование
1 мин
V4 – дыхательный контроль
0
Время инкубации суспензии без доступа кислорода
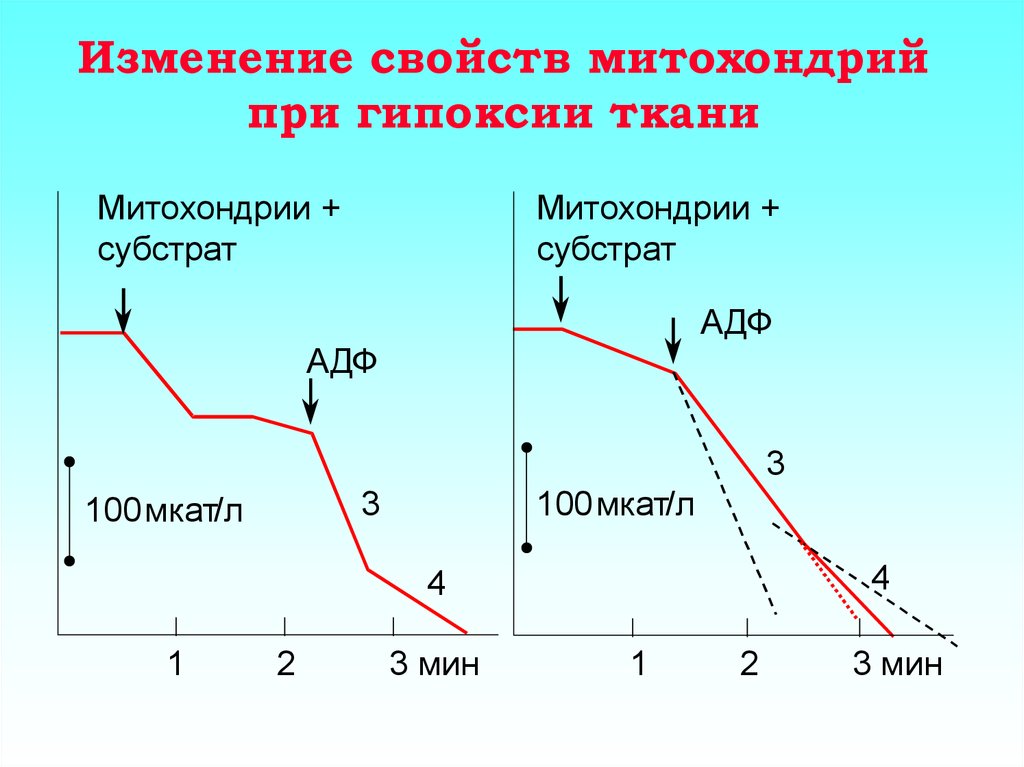
33. Изменение свойств митохондрий при гипоксии ткани
Митохондрии +субстрат
Митохондрии +
субстрат
АДФ
АДФ
3
100 мкат/л
100 мкат/л
3
4
4
1
2
3 мин
1
2
3 мин
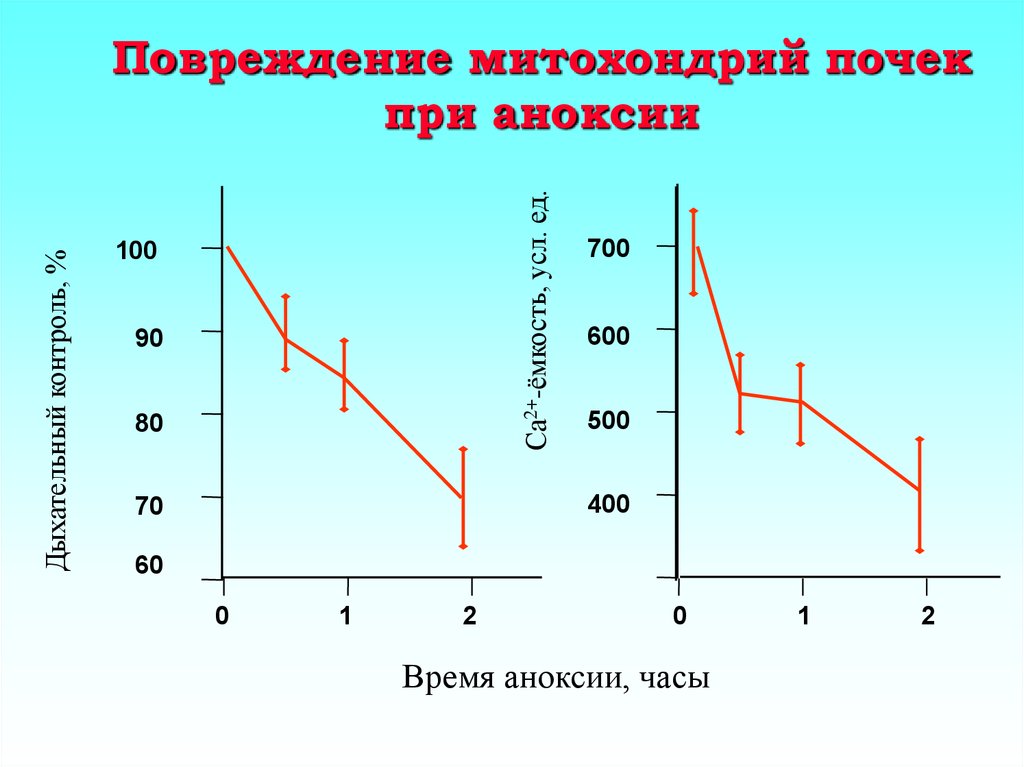
34. Повреждение митохондрий почек при аноксии
Са2+-ёмкость, усл. ед.Дыхательный контроль, %
Повреждение митохондрий почек
при аноксии
100
90
80
700
600
500
400
70
60
0
1
2
0
Время аноксии, часы
1
2






 biology
biology physics
physics








