Similar presentations:
Острые лейкозы у детей
1.
2. Острые лейкозы у детей
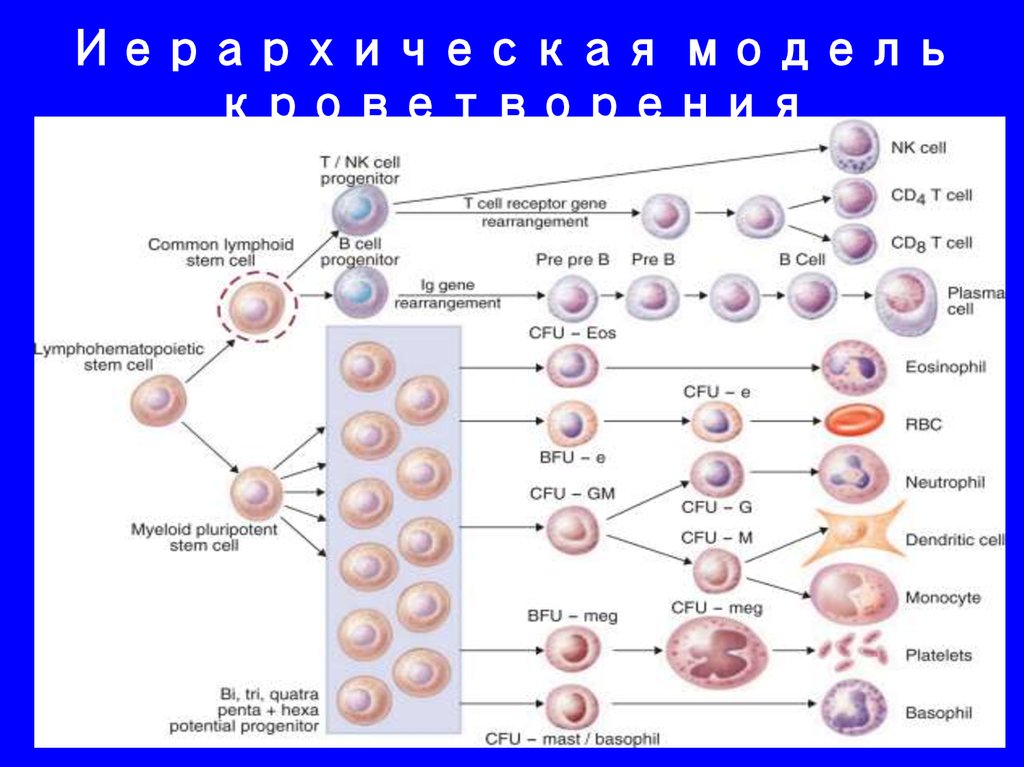
3. Иерархическая модель кроветворения
4. Лейкозы у детей
• 30% всех злокачественных опухолейдетского возраста
• встречаемость около 3250 новых случаев
в год (в возрасте <20 лет) (США)
• относительное распределение по возрасту
• 17% на первом году жизни
• 46% в возрасте от 2 до 3 лет
• 9% в возрасте 19 лет
5. Острые лейкозы у детей история
• первый случай ОЛ -1827 год• описание и термин «лейкемия» -1845 г.,
Рудольф Вирхов
• первый известный случай излечения -1930 г.,
клиника Негели., Швейцария: облучение,
мышьяк
• первые цитостатики :
1948г. метотрексат, 1960 г. 6-МП
• 1962г. - первая программа терапии ОЛЛ –
Дон Пинкель, St.Jude Children Hospital
НИИ детской гематологии
6. Острый лимфобластный лейкоз
• Группа клинически гетерогенныхзаболеваний из клеток-лимфоидных
предшественников
7. Иерархическая модель кроветворения
8. Острый лимфобластный лейкоз
• Слабость, лихорадка, боли в костях,суставах, кровоточивость со
слизистой полости рта, кожный
геморрагический синдром,
• Лимфаденопатия, увеличение печени
и селезенки
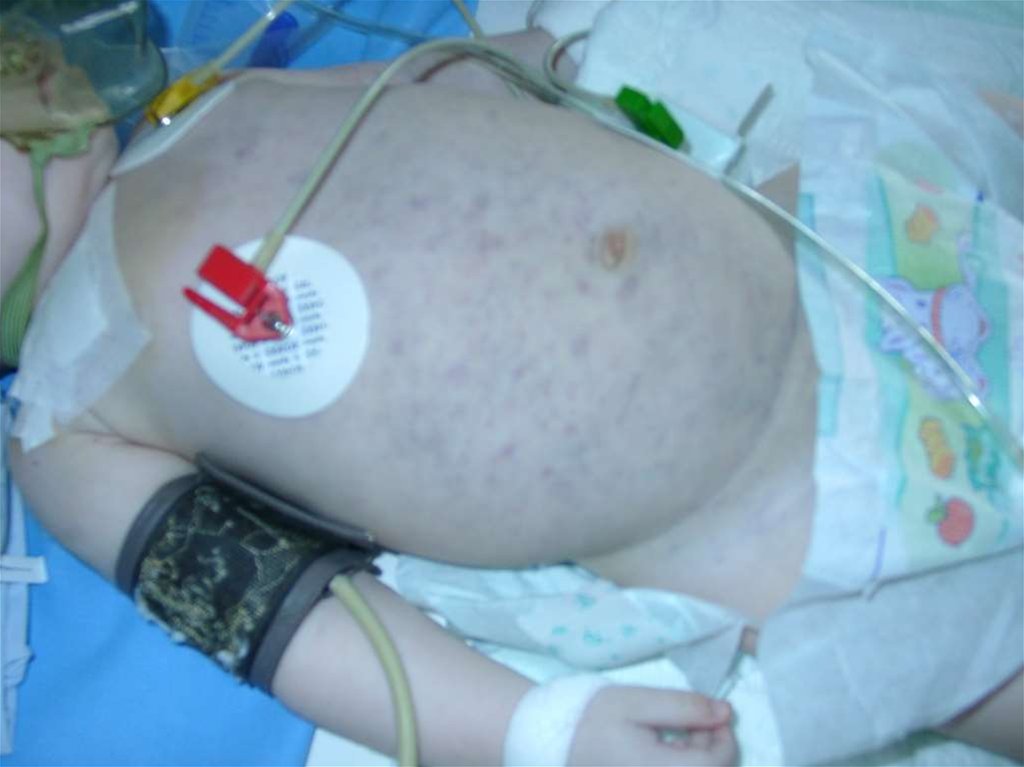
9. Острый лимфобластный лейкоз
• Увеличение почек• Увеличение лимфоузлов средостения,
тимуса
• Лейкемиды на коже
10.
11.
12. Диагностика
• ОАК: гипорегенаторная анемия,тромбоцитопения, ускорение СОЭ
• Миелограмма
• Спинномозговая пункция
• УЗИ брюшной полости
• Рентгенография грудной клетки
• Биохимия крови
• ЭКГ, Эхо-КГ
13. Острые лимфобластные лейкозы у детей диагностика
Основа диагноза - исследованиесубстрата опухоли: костномозговая пункция
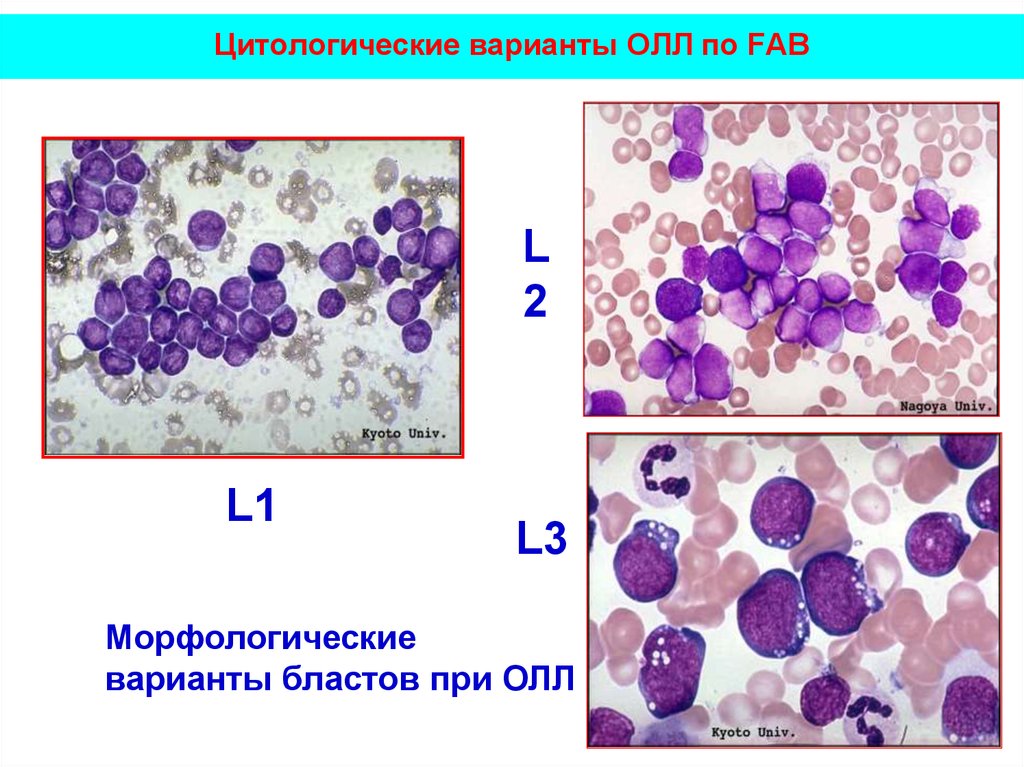
• морфологическое и цитохимические исследования:
L1, L2, L3
МПО/липиды негативны, ЩИК реакция, судан
черный положительна
• иммунофенотипирование:
лимфоидная линия дифференцировки
СD3, СD2, СD7, СD22, СD19, СD79ОЛЛ Т- или В-линии
определение варианта Т1-1V, В1-1V
НИИ детской гематологии
14. Цитологические варианты ОЛЛ по FAB
L2
L1
L3
Морфологические
варианты бластов при ОЛЛ
15. Острые лимфобластные лейкозы у детей, диагностика
ОЛЛ В-линииСД 19+ и/или СД79а+, большинство НLА-ДR+
• про-В-(В I)
- нет экспрессии др. маркеров
• сommon (B II)
- CD 10+
• пре-В-(В III)
- цитоплазмат. Ig M+
• зрелый В- (В 1У) – мембранный IgM, Цитоплазматические легкие цепи
k илиʎ
16. Острые лимфобластные лейкозы у детей диагностика
ОЛЛ Т-линииСД 3+ цит. или мембранный
большинство ТдТ+, НLА-DR-, СД34-, не важны в диагностике
• про-Т- (ТI)
- СД 7+
• пре-Т- (ТII)
- СД2+ и\или СД5+, СД8+
• кортикальный Т-(Т-III) -СД 1а+
• зрелый Т-(Т IУ)
- СД3мембр.+, СД1а альфа\бета+ Т-(а) - анти-ТСR альфа\бета +
гамма\дельта+Т-(б)-анти-ТСR гамма\дельта +
17. Острые лимфобластные лейкозы у детей классификация ВОЗ, 2001
• ОЛЛ из В-клеток предшественниц цитогенетические подгруппы:t (9;22)(q34;q11); BCR-ABL
t (11 q23)/ MLL реаранжировка
t (1;19)(q23;p13), E2A/BBX1
t(12;21)(p12;q22), ETV/CBF
• ОЛЛ из Т-клеток предшественниц
• ОЛЛ из клеток Бёркитта
18. Прогностические факторы, влияющие на исход ОЛЛ
Фактор рискаБлагоприятный
Неблагоприятный
Возраст
Старше 1 года и младше Младше 1 года и старше
9
9
Пол
Женский
Мужской
Лейкоцитоз при
диагнозе
Менее 50000
Более 50000
Ответ на 8 день
Нет бластов в
переферии
Есть бласты в крови
Иммунофенотип
В-клеточный
Т-клеточный
19. Острые лимфобластные лейкозы у детей лечение
• 1948 первая успешная индукция ремиссииОЛЛ у ребенка (S.Farber, L.K.Diamond )
• 1967 разработка базовых принципов
полихимиотерапии ОЛЛ у детей (D.Pinkel)
• 1972 введение комбинированной
профилактики нейролейкемии (St.Jude CRH)
• 1970 образование группы БФМ
формирование кооперативных групп и
создание национальных протоколов
лечения ОЛЛ у детей.
20. Острые лимфобластные лейкозы у детей лечение
Базовые принципы ПХТ в лечении ОЛЛ (D.Pinkel,D.Simone, США)
• индукция ремиссии винкристином и преднизолоном
• курсы консолидации и реиндукции
• поддерживающая терапии 6-МП и метотрексатом
• комбинированная профилактика нейролейкемии
/ эндолюмбальные введения и краниальное
облучение/
21. Острые лимфобластные лейкозы у детей лечение
Прогресс в лечении ОЛЛ стал возможным в связи с :
определением биологической гетерогенности и
введением системы цитоиммунологической
классификации ОЛЛ
разработкой системы прогностических факторов и
разделением больных на группы риска
совершенствованием профилактики нейролейкемии
введением интенсивных высокодозовых режимов ПХТ
интенсивным развитием принципов сопроводительной
терапии
22. Протокол ALL-BFM 90
II *No RT
SRG
PRED-GR
RF < 0.8
I
HD-MTX
Поддерж.терапия
18 Gy
MRG
PRED-GR
RF 0.8
Weeks 0
HD-MTX
I
10 12
20 22
II
28 30
52
Интенсивная двухфазная индукция ремиссии - 8 препаратов
высокие дозы метотрексата и циклофосфана
интенсивная двухфазная консолидация
краниальное облучение для 60% больных
кумулятивная доза антрациклинов - 240 мг/м2
высокая токсичность в первые годы применения в России
78/104
23. Острые лимфобластные лейкозы у детей результаты лечения по протоколу БФМ 90м в 9 клиниках РФ, 1990-1996: общая выживаемость
Всего больных 736, живы 572 (ОВ = 0,75 0,02)24. Острые лимфобластные лейкозы у детей проблемы лечения в Советском Союзе (80-е гг)
• отсутствие правильно организованныхклинических подразделений
• отсутствие стандартизованного лечения
• недостаток опыта в проведении
интенсивных протоколов терапии
• неадекватная сопроводительная терапия
по всем компонентам
• недостаточные возможности
верификации диагноза
25. Острые лимфобластные лейкозы у детей первый отечественный протокол
Принципиальные требования• лечение пациентов максимально внестационарно
• уменьшение потребности в интенсивных сопроводительных
мероприятиях
• уменьшение трансфузионной потребности
• отказ от применения высокодозной интенсивной
химиотерапии
• отказ от краниального облучения у большинства больных
НИИ детской гематологии
26. Острые лейкозы у детей
первые 100 лет - абсолютная фатальностьпоследние 50 лет -торжество комбинированной
полихимио/лучевой терапии + начало использования
методов иммунотерапии, включая ТГСК
будущее - расшифровка молекулярных основ
патогенеза, разработка геннообоснованной терапии и
совершенствование методов иммунотерапии
27. Острый миелолейкоз у детей
28.
ОМЛ у детейГруппа разнородных по
• патогенезу
• клиническому течению и
• ответу на цитотоксическую терапию
заболеваний
в основе которых лежит пролиферация
• малигнизированных
• более или менее ранних
миелоидных предшественников
29.
ОМЛ у детейЭпидемиология
7-8 / 1 000 000 в год
20% от всех лейкемий
6% от всех опухолей у детей
Взрослые 12 - 20/ 1 000 000 в год
Пожилые
40-60/ 1 000 000 в год
30. ОМЛ у детей предрасполагающие причины
• С-м Дауна (trisomy 21)• Синдромы костномозговой недостаточности:
аутосомно-рецессивные
Анемия Фанкони
• С-м Блума
• С-м Костманна
• АДБ
• МДС
31. ОМЛ у детей предрасполагающие причины
• Ионизирующаярадиация
• лекарства
– алкиляторы
• циклофосфан
• ифосфамид
• мелфалан
– Epipodophyllotoxins
• этопозид
– бензолы
32. Иерархическая модель кроветворения
33. ОМЛ у детей FAB - классификация 1985
М0 – недифференцированныйМ1 - миелобластный без дозревания
М2- миелобластный с дозреванием
М3 – промиелоцитарный
М4 – миеломонобластный
М5 -монобластный
М5а монобласты > 80%
М5в монобласты <80% промоноциты >10%
М6 –эритромиелоз
М7 -мегакариоцитарный
34. Клиника
Лихорадка
Геморрагический синдром
Анемия
Гепатоспленомегалия
Поражение ЦНС
35.
ОМЛ у детейКлинические особенности субвариантов
• М2 - склонность к формированию хлором
• М3 - лейкопения, коагулопатия
• М4 - уровень ремиссий 90-100%,
>30% риск ЦНС рецидива
• М5 - склонность к лейкостазам
• M6- часто подострое развитие, желтуха
• М7 – лихорадка ,«сухие» пункции,
спленомегалия
36.
ОМЛ у детейДиагностика
Необходимые тесты
• Миелограмма
• Цитохимическое исследование
МПО или судан черный
Неспецефическая эстераза
Иммунофенотипирование
• Цитогенетическое исследование
• Молекулярное исследование
37. Лечение
• Эрадикация лейкемического клона споследующим востановлением
нормального гемопоэза
• Индукция ремиссии
• Постиндукционная терапия
• Поддерживающая терапия
• Трансплантация костного мозга
38.
СиндромДауна
39. Лейкозы у детей с с-мом Дауна
частота ОЛ у детей с Синдромом Дауна выше в20 раз
возраст – от 0 до 4 лет, медиана 1,8 лет
ОМЛ, 80-90% - М7 вариант (острый
мегакариобластный лейкоз)
также – М0 и М6, не бывает М3, редко М1/М2
часто в периоде новорожденности – ТМПС
(транзиторный миелопролиферативный синдром)
40. Лейкозы у детей с с-мом Дауна
ТМПСДети 1-го месяца жизни, высокий лейкоцитоз
с миелоидными бластными клетками
часто гепатоспленомегалия
Спонтанные ремиссии в течение 1-2 мес.
Не лечить! Динамический контроль
Как правило – позже (в возрасте 1-2 лет)
развивается ОМКБЛ
41.
ОМЛ у больных с синдромом ДаунаЧасто - на 1-м году
транзиторный миелопролиферативный синдром
(транзиторный аномальный гемопоэз)
• по гематологическим признакам
мегакариобластный лейкоз
• проходит самостоятельно
~80% ОМЛ при с-ме Дауна - мегакариобластные
42.
Нейтропении удетей
43. Иерархическая модель кроветворения
44. Лейкоциты
ЛимфоцитыБелые клетки
крови (лейкоциты)
Моноциты
Гранулоциты
Т-клетки - клеточный
иммунитет
В-клетки –
гуморальный
ммунитет
NK-натуральные
киллеры
Базофилы
Являются медиаторами
воспаления и аллергических
реакций
Нейтрофилы
Фагоцитоз
Презентация
антигенов
Синтез цитокинов
Эозинофилы
Являются медиаторами
воспаления и аллергических
реакций
45. Нейтрофилы
Нейтрофилы составляют первую линию защиты отбактериальных инфекций
• За сутки у здорового
человека ≈ 1011нейтрофилов
Распеределение пула
нейтрофилов:
• Периферическая кровь
-5,8 х 109/л )
• Ткани
10%-15%
• Костный мозг
80%
5% (1,9
46. Нейтропения
• Нейтропения - уменьшение нейтрофиловпериферической крови ниже 1500/мкл
• у детей в возрасте от 2 недель до 1 года нижней
границей нормы является 1000/мкл
По степени выраженности:
• 1000-1500/мкл
- легкая степень
• 500-1000/мкл
- средняя степень
• менее 500
- тяжелая степень
• менее 200
- агранулоцитоз
По продолжительности
• острые
до 3 мес
• хронические
более 3 мес.
47. Риск развития инфекций
Опасный пороггранулоциты < 1000/мкл
Высокий риск
гранулоциты < 500 /мкл
Очень высокий риск
гранулоциты < 100/мкл
Экстремальный риск (бактериемия > 20%)
гранулоциты < 100/мкл в течение > 10-14
дней
48. Нейтропении
Причины• Нарушение продукции нейтрофилов в к/м или миграции их
в периферическое русло (наследственные нейтропении,
синдром нейтропении при АА)
• Нарушение соотношения сосудистого и тканевого пула
нейтрофилов (перераспределительные нейтропении)
• Деструкция нейтрофилов в крови и органах фагоцитами
(имунные нейтропении, гемофагоцитарные синдромы,
инфекции и др.)
Возможны сочетания этологических факторов
49. Нейтропении
• Врожденные нейтропении• Приобретенные нейтропении
• Хроническая идиопатическая
нейтропения
50. Врожденные нейтропении
Первичные наследственные нейтропении• тяжелая врожденная нейтропения с аутосомно-рециссивным типом
наследования (синдром Костмана)
• Циклическая нейтропени
• На фоне врожденных заболеваний (синдромы нейтропении)
• Врожденные метаболические болезни, (гликогеноз тип 1в,
метиламиноацидурия, - Синдром Барта, - Синдром Швахмана – Даймонда)
• Первичные иммунодефициты, сопровождающиеся нейтропенией (гипер-IgM синдром, - агаммаглобулинемия, - ретикулярная дисгенезия,
синдром Чедиака –Хигаши)
• WHIM синдром (warts, hypoimmunoglobulinemia, myelokatexis)
(миелокахексия)
• Врожденные АА (врожденный дискератоз, анемия Фанкони)
51. Приобретенные нейтропении
1.Имунные:-первичная аутоиммунная
-вторичная аутоимунная
-аллоимунная нейтропения новорожденных
2. Вторичные (симптоматические) нейтропении
-инфекционные (ВИЧ, ЦМВ, парвавирус 19, Helicobacter pillory и др.
вирусные и бактериальные инфекции)
-лекарственно индуцированные
-вследствие терапии цитостатиками
- при заболеваниях крови (острые лейкозы, МДС, апластическая анемия)
- при аутоиммуных заболеваниях (СКВ, ревматоидный артрит)
- при трансплантации костного мозга, стволовых клеток, почки.
-как следствие гиперспленизма (портальная гипертензия, болезнь Гоше,
новообразования, инфекции).
-неэффективный гранулоцитопоэз (дефицит витамина В12, фолиевой
кислоты, меди).
52. 1. Клинический анализ периферической крови с подсчетом тромбоцитов 1-2 раза в неделю в течение 1-3 месяцев. 2. Исследование титра антигранулоц
Обязательные методы обследования детей снейтропенией
1. Клинический анализ периферической крови с
подсчетом тромбоцитов 1-2 раза в неделю в течение 1-3
месяцев.
2. Исследование титра антигранулоцитарных антител
(АГАТ) в сыворотке крови больного (цитотоксические и
лейкоагглютинирующие тесты), определение АГАТ к
цитоплазме и поверхностным антигенам нейтрофила с
помощью диагностического набора специфических
антител.
3. Определение количества сывороточных
иммуноглобулинов.
4. Цитологическое исследование пунктата костного мозга
с тяжелыми и среднетяжелыми формами.
53. Синдром Костмана
• Синдром Костмана– развивается в результатенарушение созревания нейтрофилов в костном мозге
на уровне про- и миелоцитов («с высоким обрывом
созревания)
• Тип наследования - аутосомно-рецессивный
(бывают спорадические случаи и доминантный тип)
• Встречается 1-2 на 1000000 населения
• При синдроме Костмана у большинства пациентов
выявляется гомозиготная мутация генов HAX1 и
ELA2
54. Циклическая нейтропения
Заболевание имеет аутосомнодоминантный характер наследования иливозникает спорадически. В основе его
лежит мутация гена ELA2
Причем даже у фенотипически здоровых
членов семьи больного циклической
нейтропенией также может быть
выявлена данная мутация.
55. Циклическая нейтропения
• Периодичность составляет от 14 до 36 дней, у70% больных - 21 день.
• Эпизоды нейтропении обычно продолжаются
от 3 до 10 дней, после чего количество
нейтрофилов возвращается к нормальным или
субнормальным показателям.
• В период нейтропении возрастает количество
моноцитов.
56. Циклическая нейтропения
• Согласно европейскому протоколу, диагнозциклической нейтропении устанавливается по
анализам крови, взятым с частотой 3 раза в неделю
в течение последовательных 6 недель.
• Фиксируются цикличные изменения уровня
нейтрофилов, моноцитов, эозинофилов,
лимфоцитов, тромбоцитов и ретикулоцитов в
периферической крови.
• Во время нейтропенической фазы у пациентов
возникают регулярные приступы лихорадки,
появляются язвы во рту, бактериальные инфекции.
• Вне криза состояние нормализуется.
• Антинейтрофильные антитела не выявляются.
57. Х-сцепленная нейтропения (XLN)
• Заболевание вызвано мутацией в гене, кодирующембелок WASP, участвующем в построении
цитоскелета гемопоэтических клеток.
• В литературе описано несколько случаев Хсцепленной нейтропении. У двух из этих больных
была выявлена мутация гена WASP – гена,
пораженного у больных с синдромом ВискоттаОлдрича. Интересно, что, несмотря на мутации того
же гена, у больных с XLN не отмечается
тромбоцитопении и других признаков синдрома
Вискотта-Олдрича. Предполагается, что мутация
при XLN ведет к постоянной активации белка
WASP. Однако непосредственно патогенез
нейтропении неизвестен.
58. Синдром Швахмана-Даймонда
• Заболевание, для которого характерныэкзокринная недостаточность
поджелудочной железы, карликовость,
метафизарная дисплазия и нейтропения.
59. Синдром Швахмана-Даймонда
• Синдром Швахмана-Даймонда вызван мутацией генаSBDS, расположенного на 7q11.Ген кодирует белок с
невыясненной функцией. Заболевание наследуется
аутосомно-рецессивно.
• В основе патогенеза лежит внутриутробная задержка
развития ацинарных клеток поджелудочной железы,
следствием чего является резко сниженная
экзокринная панкреатическая функция. В отличие от
муковисцидоза, секреция анионов не нарушена.
• Причина скелетных и гематологических нарушений
не известна. У половины больных с синдромом
Швахмана-Даймонда отмечается панцитопения, у
остальных – разная степень нейтропении, анемии и
тромбоцитопении. Независимо от числа нейтрофилов,
отмечается дефект их хемотаксиса. В основе
цитопений, вероятно, лежит дефект
колониеобразования, выявляемый in vitro.
60. Синдром Швахмана-Даймонда
• Первыми признаками синдрома Швахмана-Даймонда,проявляющимися в первые месяцы жизни, являются диарея,
задержка роста, потеря веса и выраженная сухость кожи,
сопровождаемая экземой, и жирный стул.
• У пациентов старше 6 месяцев отмечаются рецидивирующие
бактериальные инфекции, нередко геморрагический синдром,
задержка психомоторного развития.
• Внешне часто обращает на себя внимание большой живот,
обусловленный гипотонией и гепатомегалией. Кроме
низкорослости, у больных отмечаются следующие скелетные
аномалии: клиндактилия, синдактилия, деформация Coxa vara,
вальгусная деформация коленных и локтевых суставов, аномалии
зубов.
• Умственное развитие у этих больных как правило не страдает
61. Гипер IgM синдром
• Гипер-IgM синдром – полигенное заболевание изгруппы первичных иммунодефицитов. Это редкое
заболевание характеризуется повторными
инфекциями, ассоциированными с низким уровнем
сывороточных IgG и IgA и нормальным или
увеличенным IgM.
• Нейтропения особенна характерна для Х-сцепленной
формы – у более 50% больных отмечена нейтропения.
• Причиной данной формы гипер-IgM синдрома
является мутация гена CD40 лиганда.
• Лечение – ТГСК, при невозможности ТГСК внутривенные иммуноглобулины и симптоматическая
терапия, включая ростовые факторы.
62. Приобретенные нейтропении
• Наиболее частая причина приобретенныхнейтропений – инфекции. Практически любая
вирусная и некоторые бактериальные
инфекции могут сопровождаться снижением
нейтрофилов в периферической крови.
• Нейтропения в этих случаях обычно
купируется самостоятельно по мере
выздоровления от заболевания.
63. Иммунные нейтропении
• Частота встречаемости составляет 1:100000,т.е. иммунные нейтропении встречаются
примерно в 10 раз чаще, чем врожденные.
• Возникают они в результате повышенной
деструкции нейтрофилов под воздействием
ауто- или алло- антинейтрофильных антител.
• В свою очередь, аутоиммунные нейтропении
разделяются на
– первичные
– вторичные
64. Первичная аутоиммунная нейтропения
Патофизиология.Из-за наличия специфических антиагранулоцитарных антител
происходит усиленный фагоцитоз макрофагами покрытых
антителами нейтрофилов в кровяном русле и тканях, что
приводит к развитию нейтропении. Антигранулоцитарные
антитела обычно являются IgG антителами и направлены против
специфических нейтрофильных антигенов HNA1а`и HNA2в .
Клиника.
Аутоиммунная нейтропения чаще всего встречается у детей первых
5-15 месяцев. Нейтропения часто нетяжелая, количество
нейтрофилов как правило колеблется 500-1000 клеток в мкл , к
инфекционным проявлениям относятся острый средний отит,
гастроэнтерит, тонзиллит и кожные инфекции, которые, как
правило, нетяжелы и спонтанная ремиссия обычно наблюдается в
возрасте 4-5 лет. Тяжелые инфекции - пневмония, сепсис,
менингит - встречаются в 12% случаев.
65. Первичная аутоиммунная нейтропения
Диагностика.В клиническом анализе крови снижение АКН может сочетаться с
моноцитозом и эозинофилией, уровень гемоглобина и количество
тромбоцитов нормальные.
Важным критерием диагностики является обнаружение специфических
антинейтрофильных антител, которые, однако, не всегда можно
идентифицировать вследствие особой специфичности данного
исследования.
При затруднениях в постановке диагноза тест на определение
антинейтрофильных антител рекомендуется повторить 3 и более раза.
Косвенно иммунный характер нейтропении подтверждается при
относительно благоприятном течении заболевания, отсутствии ’’обрыва
созревания’’ на уровне промиелоцита в миелограмме, возникновении
спонтанной ремиссии без применения Г-КСФ.
Исследование костного мозга проводится прежде всего с целью исключить
другое заболевание крови.
Определение уровня сывороточных иммуноглобулинов необходимо для
исключения первичного иммунодефицитного состояния
66. Неонатальная аллоиммунная нейтропения
• Патофизиология схожа с патологией, обусловленной Rhконфликтом. Возникает в результате антигеннойнесовместимости нейтрофилов плода и матери.
• Нейтропения обычно возникает в периоде
новорожденности или в первые месяцы жизни.
• Диагноз базируется на обнаружении специфических IgG,
направленных против гранулоцитарных антигенов,
унаследованных от отца.
• Как при аутоимунной, так и при аллоимунной
нейтропении частота и тяжесть возникновения
бактериальных инфекций значительно ниже, чем при
наследственных нейтропениях.
• Аллоиммунная нейтропения обычно не требует лечения,
несмотря на значительное снижение АКН в анализах
крови, купируется спонтанно по мере естественного
катаболизма специфических антинейтрофильных антител.
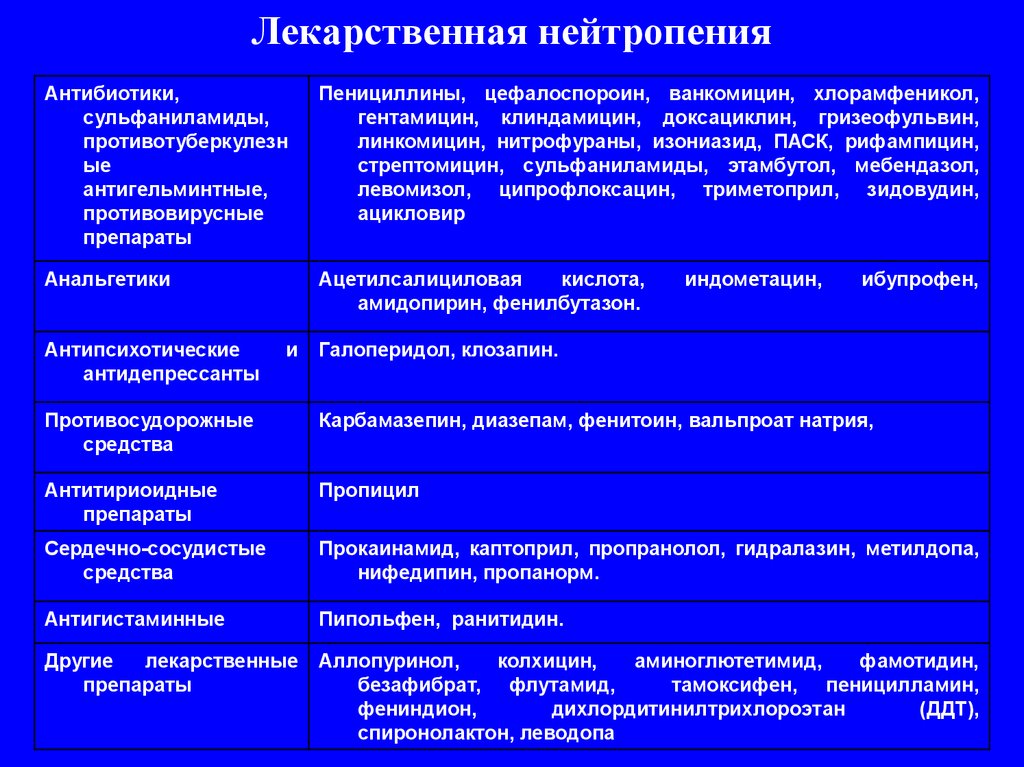
67. Лекарственная нейтропения
Антибиотики,сульфаниламиды,
противотуберкулезн
ые
антигельминтные,
противовирусные
препараты
Пенициллины, цефалоспороин, ванкомицин, хлорамфеникол,
гентамицин, клиндамицин, доксациклин, гризеофульвин,
линкомицин, нитрофураны, изониазид, ПАСК, рифампицин,
стрептомицин, сульфаниламиды, этамбутол, мебендазол,
левомизол, ципрофлоксацин, триметоприл, зидовудин,
ацикловир
Анальгетики
Ацетилсалициловая
кислота,
амидопирин, фенилбутазон.
Антипсихотические
антидепрессанты
и
индометацин,
ибупрофен,
Галоперидол, клозапин.
Противосудорожные
средства
Карбамазепин, диазепам, фенитоин, вальпроат натрия,
Антитириоидные
препараты
Пропицил
Сердечно-сосудистые
средства
Прокаинамид, каптоприл, пропранолол, гидралазин, метилдопа,
нифедипин, пропанорм.
Антигистаминные
Пипольфен, ранитидин.
Другие
лекарственные
препараты
Аллопуринол,
колхицин,
аминоглютетимид,
фамотидин,
безафибрат, флутамид,
тамоксифен, пеницилламин,
фениндион,
дихлордитинилтрихлороэтан
(ДДТ),
спиронолактон, леводопа
68. Идиопатическая нейтропения
• Диагноз идиопатической нейтропенииустанавливается при исключении всех
других вышеперечисленных причин
нейтропенических состояний, патогенез
ее не известен.
• К этой же группе относят выделяемую
многими авторами в отельную
категорию «доброкачесвенную
нейтропению детского возраста»
69. Инфекции у больных с нейтропенией
Особенности инфекций• Слабый локальный воспалительный ответ
• Небольшое число локализаций (пневмонии,
целлюлиты, периодонтиты, синуситы)
• Склонность к фульминантному течению
• Самое частое проявление - лихорадка
неясной этиологии
70. Инфекции у больных с нейтропенией
Источники инфекции• Эндогенная флора ЖКТ (большинство)
(бактерии, грибы, VZV, HSV)
• Руки медицинского персонала
(бактерии, Candida, CMV)
• Трансфузионные среды
(вирусы, редко бактерии)
• Воздух (Aspergillus)
• Пища (бактерии, Candida)
• Инвазивные манипуляции
71. Профилактика инфекций у больных с нейтропенией
Неспецифическая профилактика• мытье рук перед каждым контактом с больным
• ежедневная (или чаще) смена белья
• строгая оральная гигиена
полоскания (бета-иодин, хлоргексидин + сода) х 6-8 раз
избегать ранящих продуктов(леденцы,сушки и т.д.)
избегать пластмассовых ложек и вилок
• минимизация инвазивных манипуляций
(ан. крови из пальца, «лишние» пункции и т.д.)
• низкобактериальная пища
тщательная кулинарная обработка
нельзя: лиственные овощи, цитрусовые, копчености,
черный перец, чай в пакетиках
72. Профилактика инфекций у больных с нейтропенией
Селективная деконтаминация кишечникаЦели
• частоты фульминантных грам (-)
бактериемий и грибковых инфекций
• частоты инвазивных инфекций
• частоты всех инфекций и применения п/э
антибиотиков
• сохранение анаэробной флоры, определяющей
колонизационную резистентность
73. Инфекции у больных с нейтропенией
Самые частые возбудители инфекций у больных с
нейтропенией
Грам(+) кокки и бактерии
S. Epidermidis, S. Aureus
Str. Viridans, S. Pneumoniae
E. Faecalis/E.faecium,
Corynebacterium JK
Грам (-) палочки
E. Coli
Klebsiella sp.
Ps. Aeruginosa
Acinetobacter, Citrobacter, St. Maltophilia, Enterobacter
C. Albicans
Aspergillus
C. Krusei, C. glabrata
Грибы
74.
Инфекции у больных с нейтропениейЛихорадка неясной этиологии
Диагностический подход
Клинический осмотр(«септический» вид?)
АД
Оценка возможности неинфекционной
лихорадки
Гемокультуры
Мочевина, креатинин, лактат
СРБ (>3 mg/dl - признак бактериальной
или грибковой инфекции)
75.
Инфекции у больных с нейтропениейЛихорадка неясной этиологии
Цель начальной эмпирической терапии ЛНЭ предотвращение ранней летальности
(т.е. септического шока)
Принципы антибактериальной терапии
Быстрое начало ( в первые 2-3 часа)
Адекватные препараты широкого спектра
активные против бактерий, способных
вызвать СШ
Достаточные дозы
Достаточная длительность
Своевременная оценка и коррекция
Разумные комбинации







































































 medicine
medicine








