Similar presentations:
Второе начало термодинамики
1. Второе начало термодинамики
Лекция 5Второе начало
термодинамики
2. Вопросы к зачёту
13. Определение второго началатермодинамики.
14. Понятие замкнутой системы.
15. Понятие деградации энергии. Примеры.
16. Принцип двойственности систем.
17. Определение энтропии системы. Формула
Больцмана.
18. Свойства замкнутой системы.
3. Вопросы к зачёту
• 19. Открытые системы и их свойства.• 20. Понятие диссипативных структур.
Примеры.
• 21. Понятие самоорганизации. Примеры.
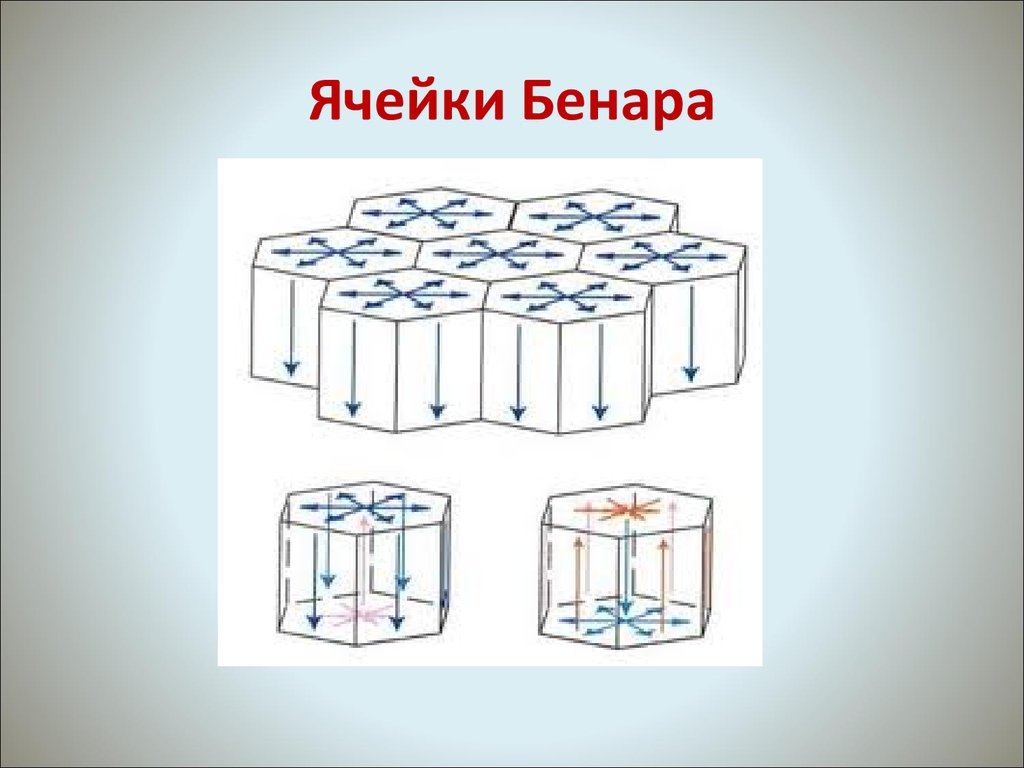
• 22. Как «работают» ячейки Бенара.
• 23. Суть синергетического подхода.
4. Первое начало термодинамики
илизакон сохранения энергии
Q = U + A
5. Формулировка второго начала термодинамики
• Тепло само собой всегда переходит отболее нагретого тела к более
холодному
Или
невозможен самопроизвольный
переход тепла от тела, менее
нагретого, к телу, более нагретому.
6. Замкнутая система
Система не обменивающаяся с внешней средой• ни энергией,
• ни веществом,
• ни информацией.
7. Формулировка второго начала термодинамики
• Второе начало термодинамики запрещает такназываемые вечные двигатели второго рода,
показывая невозможность перехода всей
внутренней энергии системы в полезную
работу.
• Второе начало термодинамики является
постулатом, не доказываемым в рамках
термодинамики. Оно было создано на осно
-ве обобщения опытных фактов и получило
многочисленные экспериментальные
подтверждения.
8. Формулировка второго начала термодинамики
• Постулат Клаузиуса: «Невозможен процесс,единственным результатом которого
являлась бы передача тепла от более
холодного тела к более горячему» (такой
процесс называется процессом Клаузиуса).
• Постулат Томсона: «Невозможен круговой
процесс, единственным результатом
которого было бы производство работы за
счет охлаждения теплового резервуара»
(такой процесс называется процессом
Томсона).
9. Необратимые процессы
• Необратимым называется процесс,который нельзя провести в
противоположном направлении через все
те же самые промежуточные состояния. Все
реальные процессы необратимы. Примеры
необратимых процессов: диффузия,
термодиффузия, теплопроводность, и др.
10. Деградация энергии
• “Высококачественная” световая энергияпревращается в энергию химических связей
тканей растений, которая затем после гибели
растения деградирует в тепловую энергию в
процессе гниения.
• Деградация энергии – переход от
высокоупорядоченной энергии к энергии
хаотического движения (т.е.тепловой энергии)
11. Энтропия
Энтропиия (от греч. ἐντροπία — поворот,превращение) — мера беспорядка
системы или мера хаотической
составляющей любой системы
Рудольф Клаузиус
Энтропия впервые введена Клаузиусом в термодинамике
в 1865 году для определения меры необратимого
рассеивания энергии, меры отклонения реального
процесса от идеального. Она является функцией
состояния и остаётся постоянной в обратимых процессах.
В необратимых процессах энтропия увеличивается.
12. Принцип двойственности систем
• Все системы состоят из двух составляющих:хаотической
и
упорядоченной.
Соотношение этих составляющих меняется
при всех изменениях системы.
13. Энтропи́я
ЭнтропиияЭнтропиия – мера деградации энергии,
мера неупорядоченности,
неопределённости,
нестабильности.
14. Свойства замкнутой системы
• Энергия замкнутой системы остаетсяпостоянной.
• Энтропия замкнутой системы возрастает
15. Формула Больцмана
S = k lnWЛюдвиг Больцман
16. Демон Максвелла
• Демон Максвелла —мысленный эксперимент 1867
года, а также его главный
персонаж — гипотетическое
разумное существо
микроскопического размера,
придуманное
Джеймсом Максвеллом с
целью проиллюстрировать
кажущийся парадокс
Второго начала термодинами
ки
Джеймс Максвелл
.
17. Суть парадокса
• Мысленный эксперимент состоит вследующем: предположим, сосуд с
газом разделён непроницаемой
перегородкой на две части: правую
и левую. В перегородке отверстие с
устройством (так называемый
демон Максвелла), которое позволя
ет пролетать быстрым (горячим)
молекулам газа только из левой
части сосуда в правую, а медленным (холодным) молекулам —
только из правой части сосуда в левую. Тогда, через большой проме
-жуток времени, горячие молекулы
окажутся в правом сосуде, а холод
-ные — в левом.
18. Суть парадокса
• Таким образом, получается, что демонМаксвелла позволяет нагреть правую часть
сосуда и охладить левую без
дополнительного подвода энергии к системе.
Энтропия для системы, состоящей из правой
и левой части сосуда, в начальном состоянии
больше, чем в конечном, что противоречит
термодинамическому принципу неубывания
энтропии в замкнутых системах
19. Демон Максвелла и информация
I a ln NВ информатике используется формула Хартли:
x=log2N.
Получена она в 1928 г. американским инженером Р. Хартли.
Процесс получения информации он формулировал примерно
так: если в заданном множестве, содержащем N равнозначных
элементов, выделен некоторый элемент x, о котором известно
лишь, что он принадлежит этому множеству, то, чтобы найти x,
необходимо получить количество информации, равное log2N.
20.
Наименьшее количество информации 1бит –соответствует выбору одного из двух значений
одной цифры при двоичной записи числа (0
или 1). Т.о. получаем из формулы 1=аLn2 и
тогда а= 1/Ln2
Две цифры – два бита и т.д. I цифр –
соответствует количеству информации в битах,
равному I.
21. Открытые системы
Лекция 6Открытые системы
22.
• Открытые системы – системы,обменивающиеся с окружающей средой
веществом, энергией и информацией.
• Энтропия открытой системы может как
увеличиваться (в случае регресса и
увеличения хаоса), так и уменьшаться (в
случае развития и упорядочения).
23.
• Автотрофы (др.-греч. αὐτός — сам и τροφή — пища) —живые организмы, синтезирующие
органические соединения из неорганических.
• Автотрофы составляют первый ярус в пищевой пирамиде
(первые звенья пищевых цепей). Именно они являются
первичными продуцентами органического вещества в
биосфере, обеспечивая пищей гетеротрофов. Следует
отметить, что иногда резкой границы между автотрофами
и гетеротрофами провести не удается. Например,
одноклеточ- ная эвглена на свету является автотрофом, а в
темноте — гетеротрофом.
24. Диссипативные структуры
• Диссипативная система (или диссипативнаяструктура, от лат. dissipatio — «рассеиваю,
разрушаю») — это открытая система, которая
оперирует вдали от термодинамического
равновесия. Иными словами, это устойчивое
состояние, возникающее в неравновесной среде при
условии диссипации (рассеивания) энергии, которая
поступает извне. Диссипативная система иногда
называется ещё стационарной открытой
системой или неравновесной открытой системой.
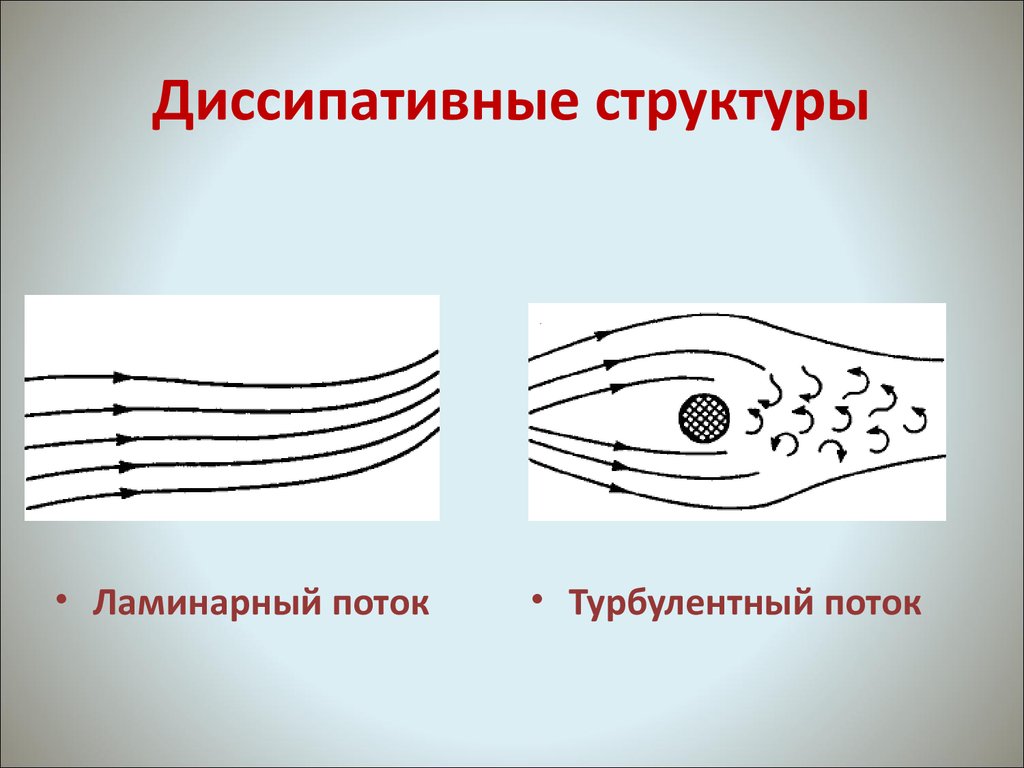
25. Диссипативные структуры
• Ламинарный поток• Турбулентный поток
26. Диссипативные структуры
• Диссипативные структуры в экологии связаны впервую очередь с системами "хищник - жертва"
или "паразит - хозяин" и представляют собой
циклические колебания (временная упорядочен
-ность), которые исследовались Лоткой (1926) и
Вольтеррой (1930). Экспериментально такие
колебания впервые наблюдались в Северной
Америке для популяций зайцев и рысей на
основании данных о числе заготовленных шкурок
27. Диссипативные структуры
28. Ячейки Бенара
29. Ячейки Бенара
30. Ячейки Бенара
31. Ячейки Бенара
32. Ячейки Бенара
33. Реакция Белоусова Жаботинского
34. Необходимые свойства самоорганизующихся систем
• Система должна быть открытой;• Наличие управляющих параметров;
• Наличие внутрисистемных связей.
35. Схема процесса самоорганизации
• внешнее воздействие на систему;• изменение управляющего параметра;
• изменение эффективности прежних или
образование новых внутрисистемных связей;
• образование диссипативных структур,
усложнение системы.
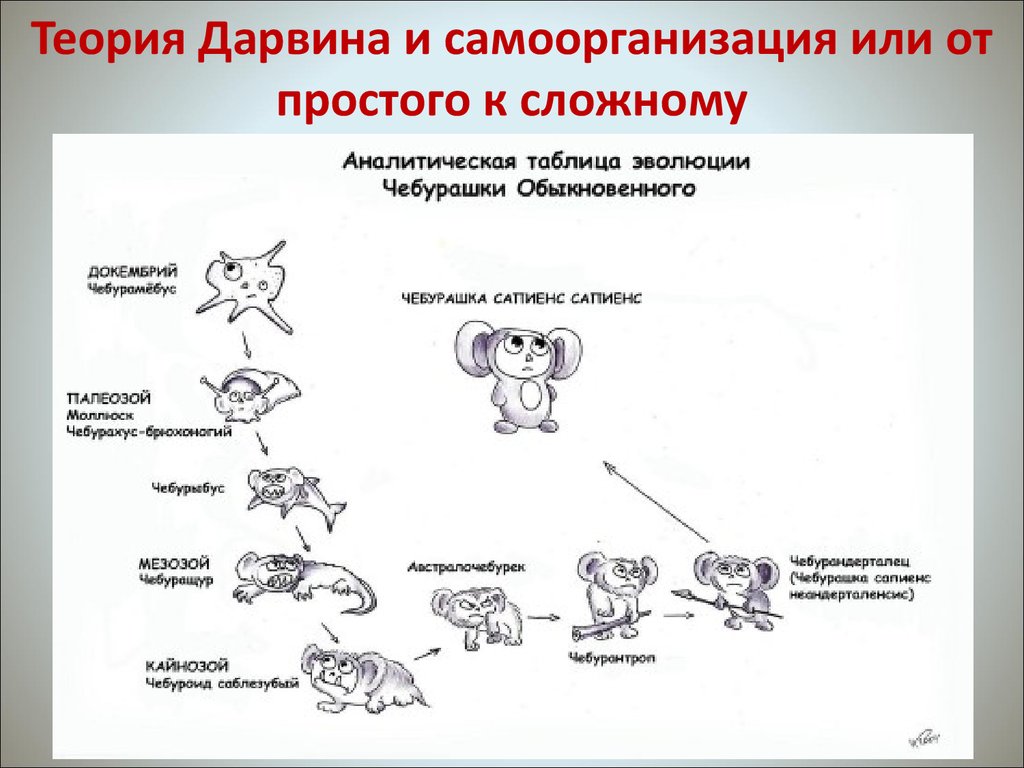
36. Теория Дарвина и самоорганизация или от простого к сложному
37.
Дарвин против Больцмана?Больцман против космоса?
38. Синергетика
• Синергетический подход означаетэквивалентность рассмотрения процессов в
различных открытых системах, из которых
состоит наш мир и проявляющихся как в
живой так и неживой природе, так и в
общественных, психологических и
социальных системах.
39. Хаос и порядок
Порядок из хаосаили
хаос из порядка



































 physics
physics








