Similar presentations:
Свойства щелочей
1.
ХИМИЧЕСКИЕ СВОЙСТВА ЩЕЛОЧЕЙ1.ИЗМЕНЕНИЕ ЦВЕТА В ПРИСУТСТВИИ ИНДИКАТОРОВ
ЛАКМУС
МЕТИЛОРАНЖ
ФЕНОЛФТАЛЕИН
синий
жёлтый
малиновый
2.
2.ЩЁЛОЧЬ + КИСЛОТНЫЙ ОКСИД = СОЛЬ + ВОДА2NaOH + CO2 =
Ca(OH)2 + SO3=
6KOH + P2O5 =
3.
2.ЩЁЛОЧЬ + КИСЛОТНЫЙ ОКСИД = СОЛЬ + ВОДА2NaOH + CO2 =Na2CO3 + H2O
Ca(OH)2 + SO3= CaSO4 + H2O
6KOH + P2O5 =2K3PO4 + 3H2O
4.
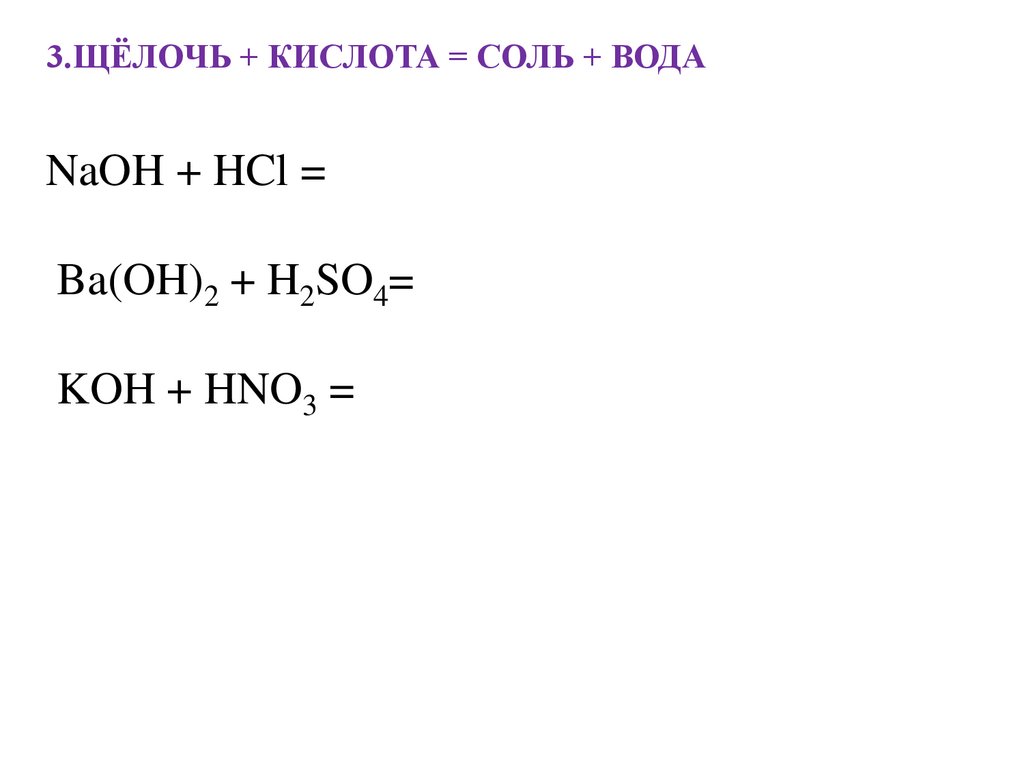
3.ЩЁЛОЧЬ + КИСЛОТА = СОЛЬ + ВОДАNaOH + HCl =
Ba(OH)2 + H2SO4=
KOH + HNO3 =
5.
3.ЩЁЛОЧЬ + КИСЛОТА = СОЛЬ + ВОДАNaOH + HCl = NaCl + H2O
Ba(OH)2 + H2SO4= BaSO4 + 2H2O
KOH + HNO3 =KNO3 + H2O
Взаимодействие щёлочи и кислоты – реакция нейтрализации
6.
4.ЩЁЛОЧЬ + СОЛЬ 1 = ОСНОВАНИЕ + СОЛЬ 2KOH + CuCl2=
NaOH + Mg(NO3)2 =
7.
4.ЩЁЛОЧЬ + СОЛЬ 1 = ОСНОВАНИЕ + СОЛЬ 22KOH + CuCl2=Cu(OH)2 ↓ + 2KCl
2NaOH + Mg(NO3)2 = Mg(OH)2 + 2NaNO3
8.
Ca(OH)2 + NaCl → не взаимодействуют(т.к. необразуется осадок)
КОН + BaSO4 → не взаимодействуют(т.к. соль
нерастворима в воде)
Условие 1. Соль должна быть растворима в воде
Условие 2. В результате взаимодействия в осадок
должна выпасть или соль, или основание.
9.
5.ЩЁЛОЧЬ = ОСНОВНЫЙ ОКСИД + ВОДАЗапомнить!!! Разлагаются только Ca(OH)2и
LiOH
Сa(OH)2 = CaO + H2O
2LiOH = Li2O + H2O
10.
ПОЛУЧЕНИЕЩЕЛОЧЕЙ
11.
1.ЩЕЛОЧНОЙ, ИЛИ ЩЕЛОЧНОЗЕМЕЛЬНЫЙ МЕТАЛЛ +ВОДА = ЩЕЛОЧЬ + ВОДОРОД
2Na + H2O = 2NaOH + H2
Ca + 2H2O = Ca(OH)2 + H2
12.
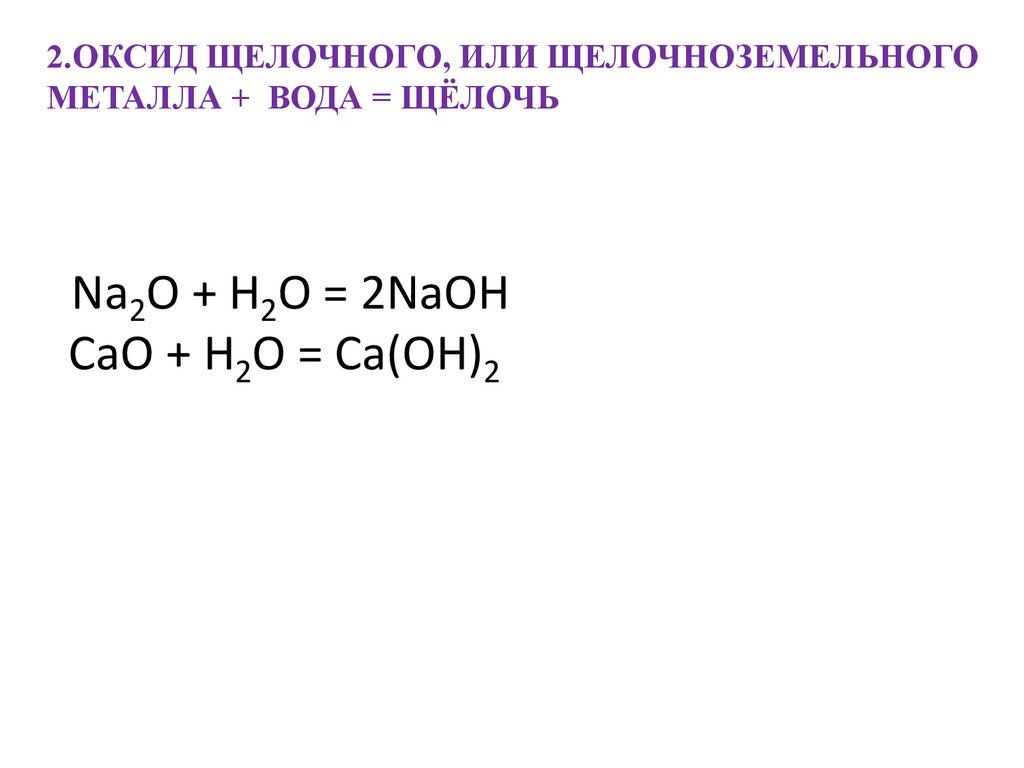
2.ОКСИД ЩЕЛОЧНОГО, ИЛИ ЩЕЛОЧНОЗЕМЕЛЬНОГОМЕТАЛЛА + ВОДА = ЩЁЛОЧЬ
Na2O + H2O = 2NaOH
CaO + H2O = Ca(OH)2
13.
ХИМИЧЕСКИЕ СВОЙСТВАНЕРАСТВОРИМЫХ В ВОДЕ ОСНОВАНИЙ
14.
1.НЕ ИЗМЕНЯЮТ СВОЙ ЦВЕТ В ПРИСУТСТВИИИНДИКАТОРОВ
2.НЕРАСТВОРИМОЕ ОСНОВАНИЕ + КИСЛОТА = СОЛЬ +
ВОДА
Mg(OH)2 + 2HCl =
F e(OH)3 + H2SO4 =
Fe(OH)2 + 2HCl =
15.
1.НЕ ИЗМЕНЯЮТ СВОЙ ЦВЕТ В ПРИСУТСТВИИИНДИКАТОРОВ
2.НЕРАСТВОРИМОЕ ОСНОВАНИЕ + КИСЛОТА = СОЛЬ +
ВОДА
Mg(OH)2 + 2HCl = MgCl2 + 2H2O
F e(OH)3 + H2SO4 = Fe2(SO4)3 + H2O
Fe(OH)2 + 2HCl = FeCl2 + 2H2O
16.
3.НЕРАСТВОРИМОЕ ОСНОВАНИЕ(разложение принагревании) = ОКСИД МЕТАЛЛА + ВОДА
Mg(OH)2 = MgO + H2O
Fe(OH)2 = FeO + H2O
2Al(OH)3 =Al2O3 + 3H2O
17.
ПОЛУЧЕНИЕ НЕРАСТВОРИМЫХ В ВОДЕОСНОВАНИЙ
18.
ЩЁЛОЧЬ + РАСТВОРИМАЯ СОЛЬ = НЕРАСТВОРИМОЕОСНОВАНИЕ + СОЛЬ
Условия:
1)Соль должна быть взята растворимая в
воде;
2)В результате взаимодействия должен
образоваться осадок.
19.
ЩЁЛОЧЬ + РАСТВОРИМАЯ СОЛЬ = НЕРАСТВОРИМОЕОСНОВАНИЕ + СОЛЬ
2KOH + MgCl2 =
2NaOH + CuSO4 =
20.
ЩЁЛОЧЬ + РАСТВОРИМАЯ СОЛЬ = НЕРАСТВОРИМОЕОСНОВАНИЕ + СОЛЬ
2KOH + MgCl2 = Mg(OH)2↓ + 2KCl
2NaOH + CuSO4 =Cu(OH)2↓ + Na2SO4




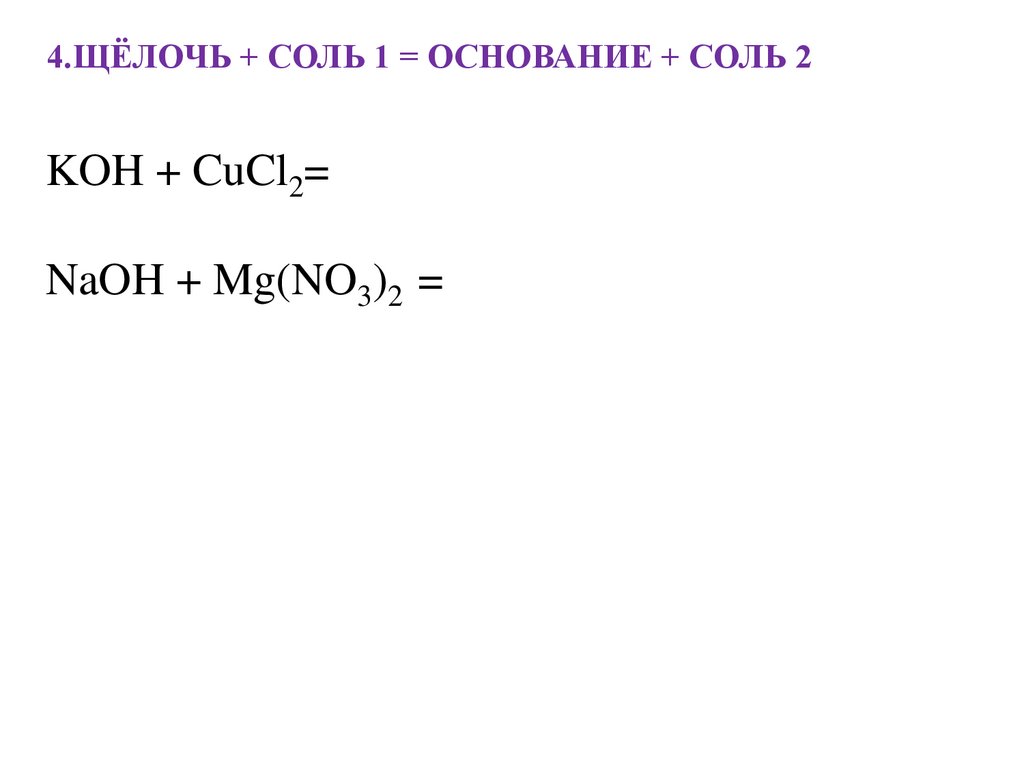













 chemistry
chemistry