Similar presentations:
!!!ЕГЭ_2023_Молек_уров_Химия_клетки
1. Молекулярный уровень Химическая организация клетки
2.
3. Молекулярный уровень: общая характеристика
Молекулярный уровень – начальный,наиболее глубинный уровень
организации живого
Каждый организм состоит из молекул
органических веществ, находящихся в
клетке – это биологические молекулы
Живые организмы состоят из тех же
химических элементов, что и
неживые. В настоящее время известно
более 100 элементов, большая часть их
содержится в живых организмах
Наиболее распространенные в живой
природе: углевод (С), кислород (О),
водород (Н) и азот (N)
Основой всех органических соединений
служит углерод, он вступает в связь с
многими атомами и их группами –
образует цепочки, различные по
химическому составу, длине и форме.
Мономеры – группы атомов,
относительно просто устроенная,
входящая в состав сложных химических
соединений
Полимер – цепь, состоящая из
многочисленных звеньев – мономеров
Биополимеры – полимеры, входящие в
состав живых организмов
Молекула полимера состоит из
тысяч соединенных между собой
мономеров (одинаковых или разных)
Свойства биополимеров зависят от:
строения мономеров
числа мономеров
разнообразия мономеров
Биополимеры универсальны, т.к.
построены по одному плану у всех
живых организмов.
4.
мономермономер
мономер
Мономер - от греч. monos «один»
и meros -«часть», «доля»
Полимер - от греч. polys –
«многочисленный»)
5. Молекулярный уровень: общая характеристика
К биополимерам относятся:
белки
углеводы
нуклеиновые кислоты
Для каждого вида биополимеров
характерны определенное строение
и функции:
Биополимеры -белки, состоят из
мономеров-аминокислот, выполняют
функции: основной структурный
материал, регулируют процессы
Нуклеиновые кислоты состоят из
нуклеотидов, участвуют в передаче
генетической информации
Углеводу состоят из моносахаридов,
главный энергетический материал
живых организмов
Жиры высокомолекулярные
органические соединения –
строительный и энергетический ресурс
организма.
Разнообразные свойства
биополимеров обусловлены
различным сочетанием нескольких
типов мономеров
Специфические свойства
биополимеров проявляются только в
живой клетке
Преемственность между
молекулярным и следующим за ним
клеточным уровнем
обеспечивается тем, что
биологические молекулы – это
материал, из которого образуются
надмолекулярные – клеточные
структуры.
белок
нуклеиновая
кислота
аминокислота
углевод
моносахарид
нуклеотид
К содержанию
6. ХИМИЧЕСКИЙ СОСТАВ КЛЕТКИ. СТРОЕНИЕ КЛЕТКИ.
7.
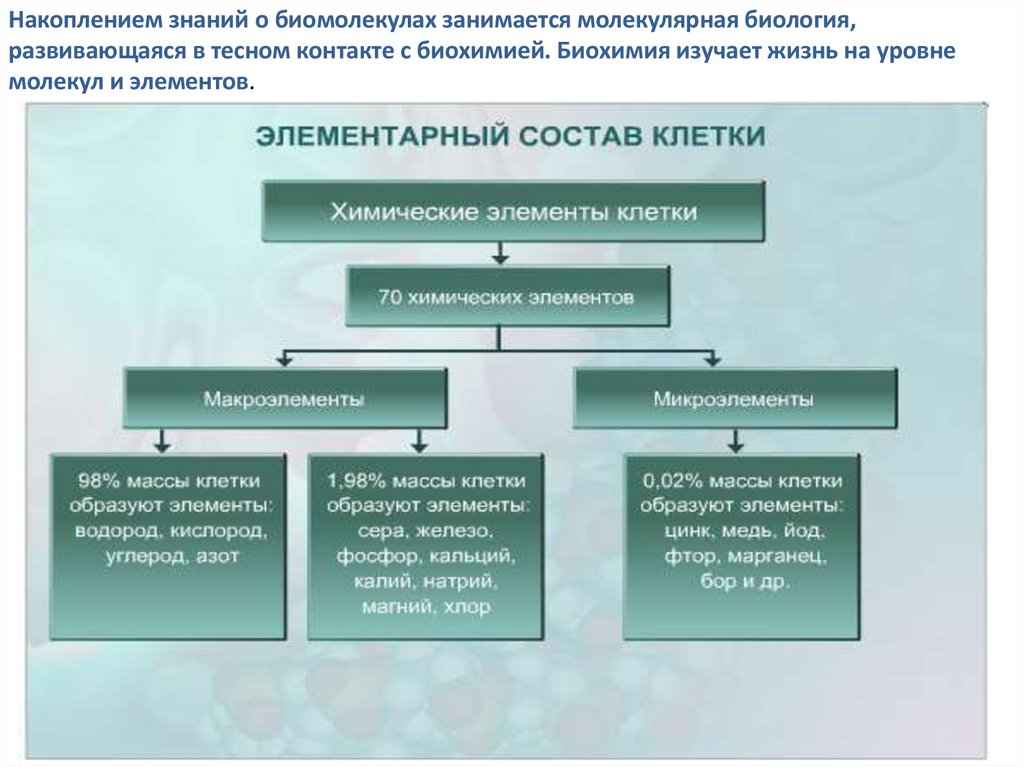
Накоплением знаний о биомолекулах занимается молекулярная биология,развивающаяся в тесном контакте с биохимией. Биохимия изучает жизнь на уровне
молекул и элементов.
8.
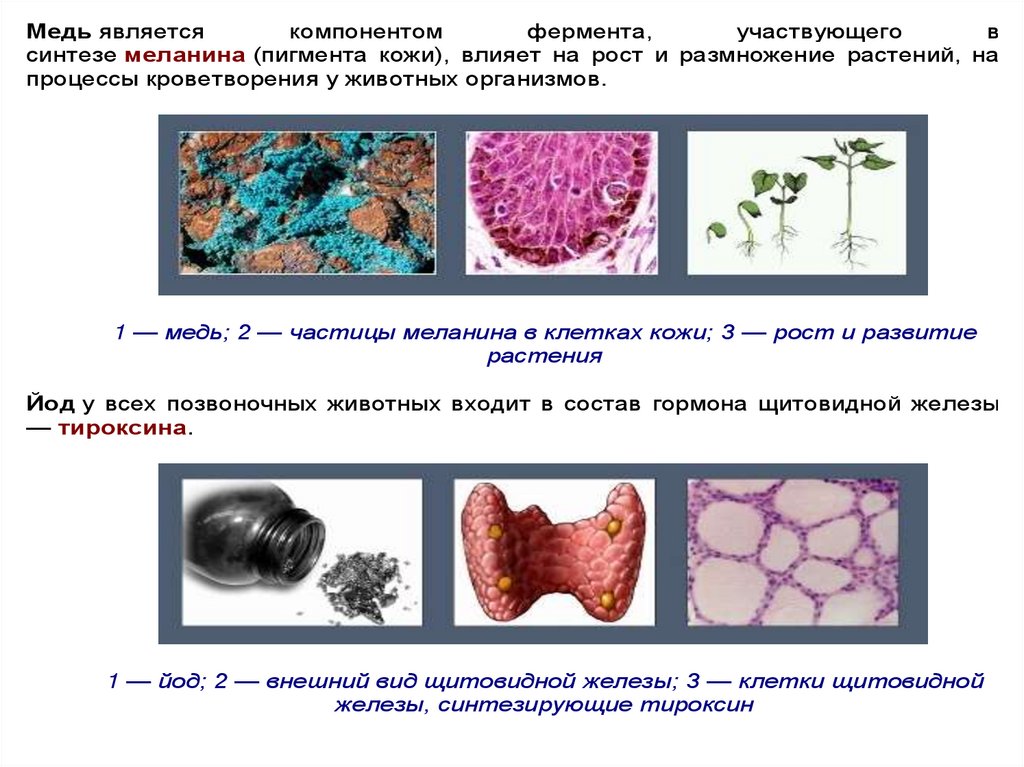
Медь являетсякомпонентом
фермента,
участвующего
в
синтезе меланина (пигмента кожи), влияет на рост и размножение растений, на
процессы кроветворения у животных организмов.
1 — медь; 2 — частицы меланина в клетках кожи; 3 — рост и развитие
растения
Йод у всех позвоночных животных входит в состав гормона щитовидной железы
— тироксина.
1 — йод; 2 — внешний вид щитовидной железы; 3 — клетки щитовидной
железы, синтезирующие тироксин
9.
Бор влияет на ростовые процессы у растений,отмиранию верхушечных почек, цветков и завязей.
его
недостаток
приводит
к
1 — бор в природе; 2 — пространственная структура бора; 3 —
верхушечная почка
Цинк входит в состав гормона поджелудочной железы — инсулина, а также
действует на рост животных и растений.
1 — пространственная структура инсулина; 2 — поджелудочная железа; 3
— рост и развитие животных
В организмы растений и микроорганизмов микроэлементы поступают из почвы и
воды; в организмы животных и человека — с пищей, в составе природных вод и с
воздухом.
10.
Роль микроэлементов в организмеКобальт входит
в
состав
витамина
В12 и
принимает
синтезе гемоглобина, его недостаток приводит к анемии.
участие
в
1 — кобальт в природе; 2 — структурная формула витамина В12; 3 —
эритроциты здорового человека и эритроциты больного анемией
Молибден в составе ферментов участвует в фиксации азота у бактерий и
обеспечивает работу устьичного аппарата у растений.
1 — молибденит (минерал, содержащий молибден); 2 — азотфиксирующие
бактерии; 3 — устьичный аппарат
11. Функции химических элементов в клетке
ЭлементФункция
1) О, Н
Входят в состав воды и биологических веществ
2) С, О, Н, N
входят в состав белков, жиров, липидов, нуклеиновых кислот, полисахаридов.
3) K, Na, Cl
проводят нервные импульсы.
4) Ca
компонент костей, зубов, необходим для мышечного сокращения, компонент
свертывания крови, посредник в механизме действия гормонов.
5) Mg
структурный компонент хлорофилла, поддерживает работу рибосом и
митохондрий
6) Fe
структурный компонент гемоглобина, миоглобина.
7) S
в составе серосодержащих аминокислот, белков.
8) P
в составе нуклеиновых кислот, костной ткани.
9) B
необходим некоторым растениям
10) Mn, Zn, Cu
активаторы ферментов, влияют на процессы тканевого дыхания
11) Co
входит в состав витамина В12
12) F
состав эмали зубов
13) I
состав тироксина
12.
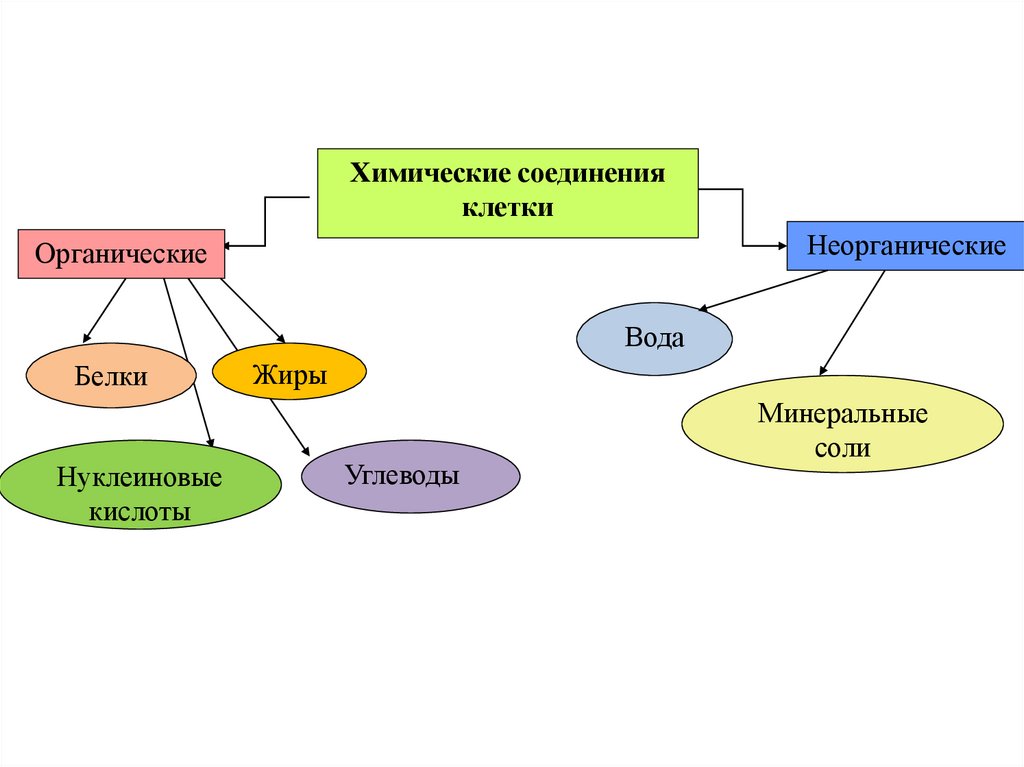
Химические соединенияклетки
Неорганические
Органические
Вода
Белки
Нуклеиновые
кислоты
Жиры
Углеводы
Минеральные
соли
13.
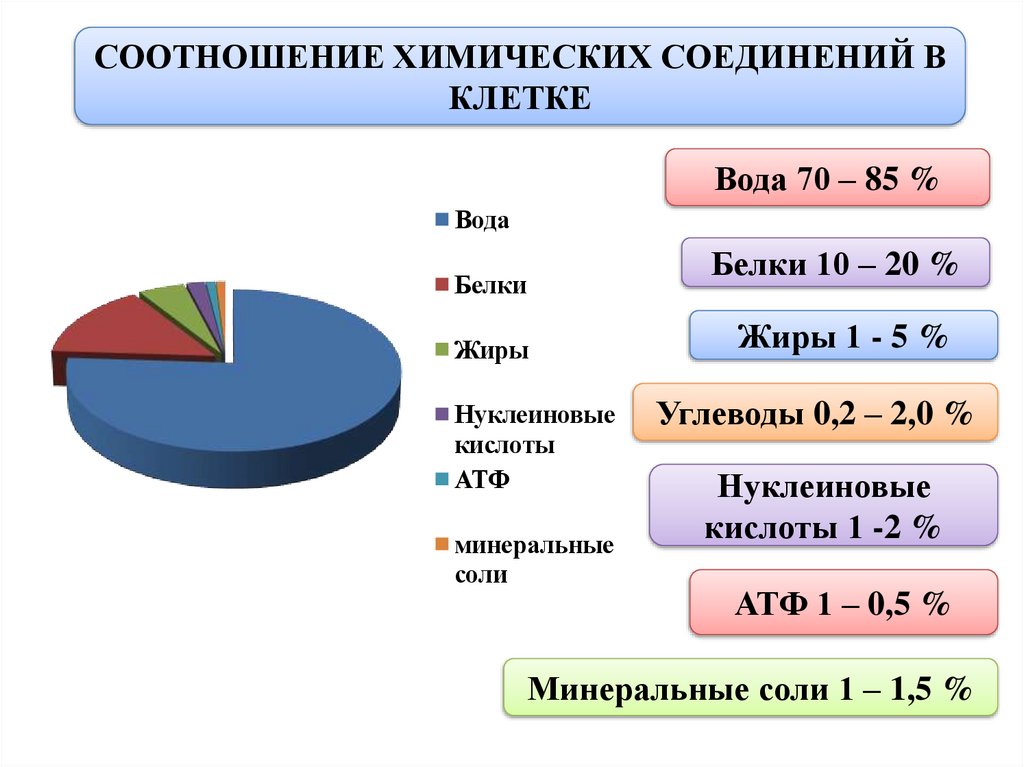
СООТНОШЕНИЕ ХИМИЧЕСКИХ СОЕДИНЕНИЙ ВКЛЕТКЕ
Вода 70 – 85 %
Вода
Белки 10 – 20 %
Белки
Жиры
Нуклеиновые
кислоты
АТФ
минеральные
соли
Жиры 1 - 5 %
Углеводы 0,2 – 2,0 %
Нуклеиновые
кислоты 1 -2 %
АТФ 1 – 0,5 %
Минеральные соли 1 – 1,5 %
14.
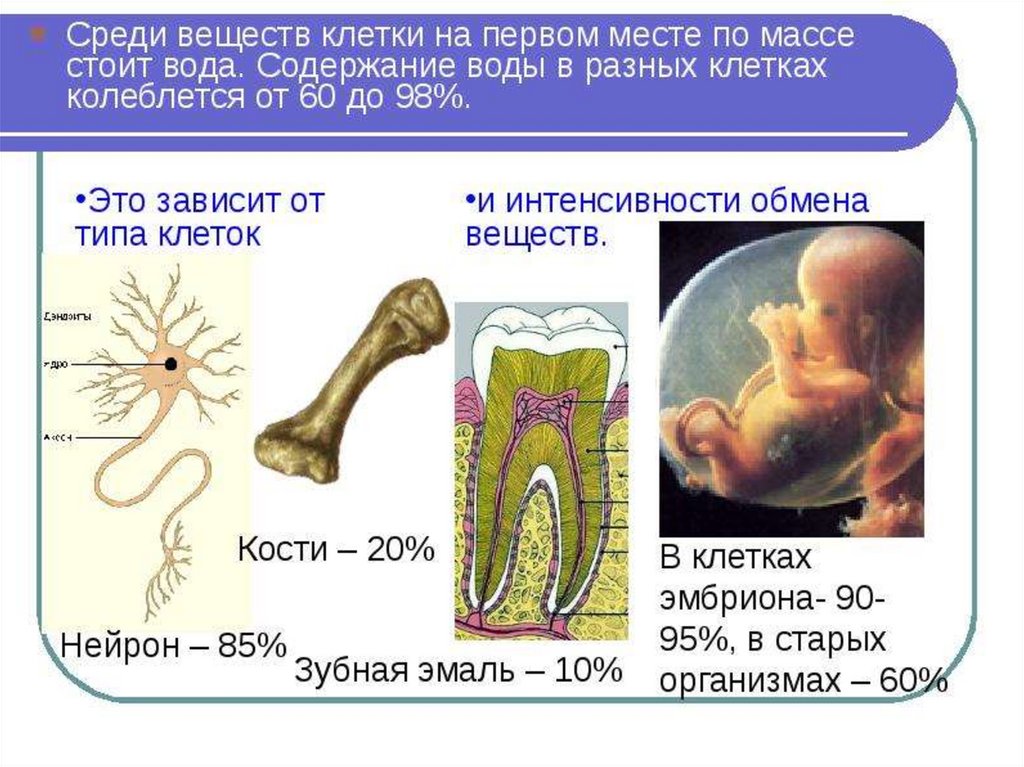
15. Содержание воды в разных клетках организма:
• В молодом организме человека иживотного – 80 % от массы клетки;
• В клетках старого организма – 60 %;
• В головном мозге – 85%;
• В клетках эмали зубов –10 -15 %.
• При потере 20% воды у человека наступает
смерть.
16.
Самое распространенное неорганическое соединение в клеткахживых организмов – вода.
Она поступает в организм из внешней среды; у животных,
кроме того, может образовываться при расщеплении жиров,
белков, углеводов. Вода находится в цитоплазме и её
органеллах, вакуолях, ядре, межклетниках.
Функции воды в клетке:
1. Растворитель
2. Транспорт веществ
3. Создание среды для
химических реакций
4. Участие в образовании
клеточных структур (цитоплазма)
17.
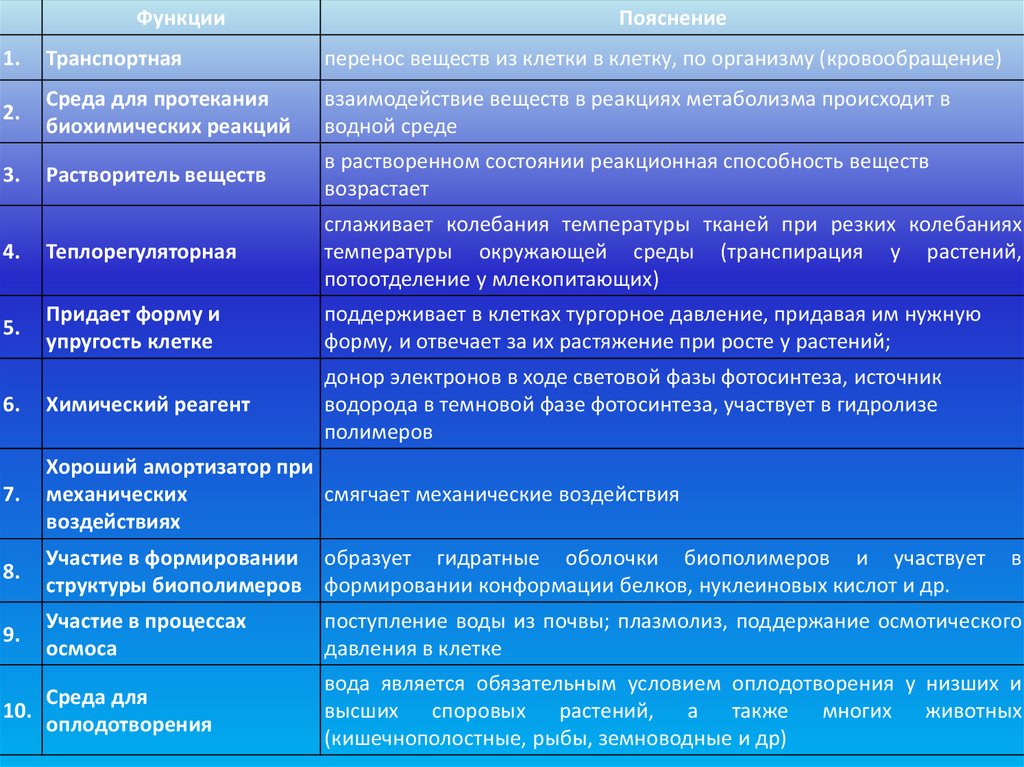
ФункцииПояснение
1.
Транспортная
перенос веществ из клетки в клетку, по организму (кровообращение)
2.
Среда для протекания
биохимических реакций
взаимодействие веществ в реакциях метаболизма происходит в
водной среде
3.
Растворитель веществ
в растворенном состоянии реакционная способность веществ
возрастает
4.
Теплорегуляторная
сглаживает колебания температуры тканей при резких колебаниях
температуры окружающей среды (транспирация у растений,
потоотделение у млекопитающих)
5.
Придает форму и
упругость клетке
поддерживает в клетках тургорное давление, придавая им нужную
форму, и отвечает за их растяжение при росте у растений;
6.
Химический реагент
донор электронов в ходе световой фазы фотосинтеза, источник
водорода в темновой фазе фотосинтеза, участвует в гидролизе
полимеров
7.
Хороший амортизатор при
механических
смягчает механические воздействия
воздействиях
8.
Участие в формировании образует гидратные оболочки биополимеров и участвует
структуры биополимеров формировании конформации белков, нуклеиновых кислот и др.
9.
Участие в процессах
осмоса
Среда для
10.
оплодотворения
в
поступление воды из почвы; плазмолиз, поддержание осмотического
давления в клетке
вода является обязательным условием оплодотворения у низших и
высших споровых растений, а также многих животных
(кишечнополостные, рыбы, земноводные и др)
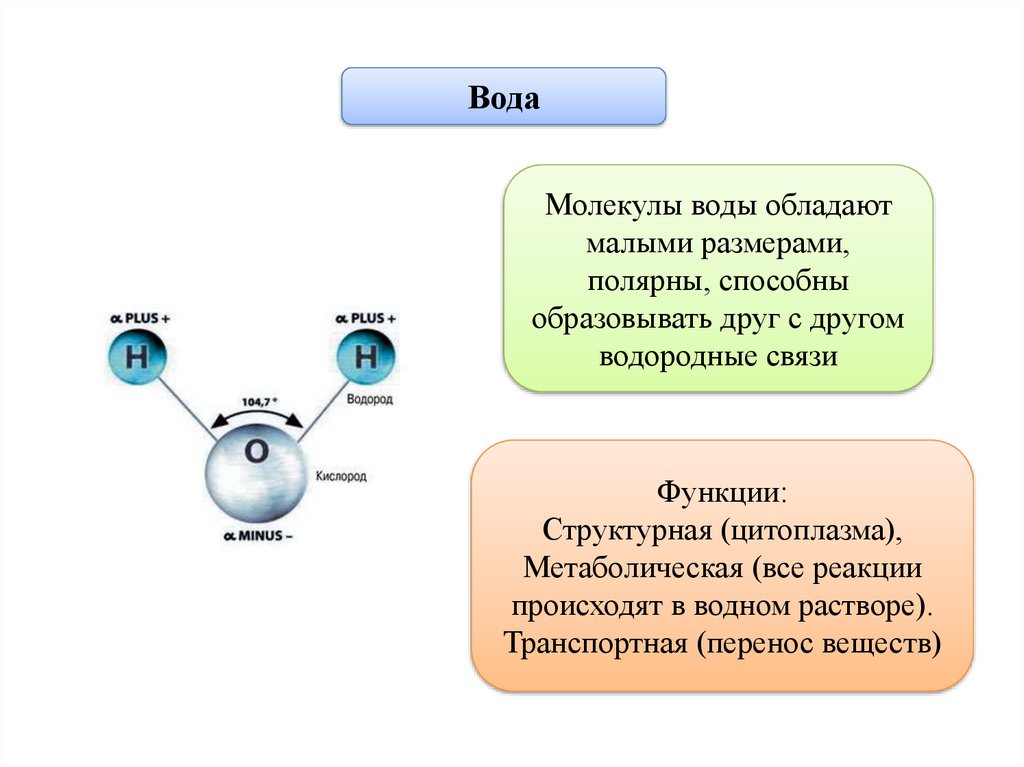
18.
ВодаМолекулы воды обладают
малыми размерами,
полярны, способны
образовывать друг с другом
водородные связи
Функции:
Структурная (цитоплазма),
Метаболическая (все реакции
происходят в водном растворе).
Транспортная (перенос веществ)
19.
20.
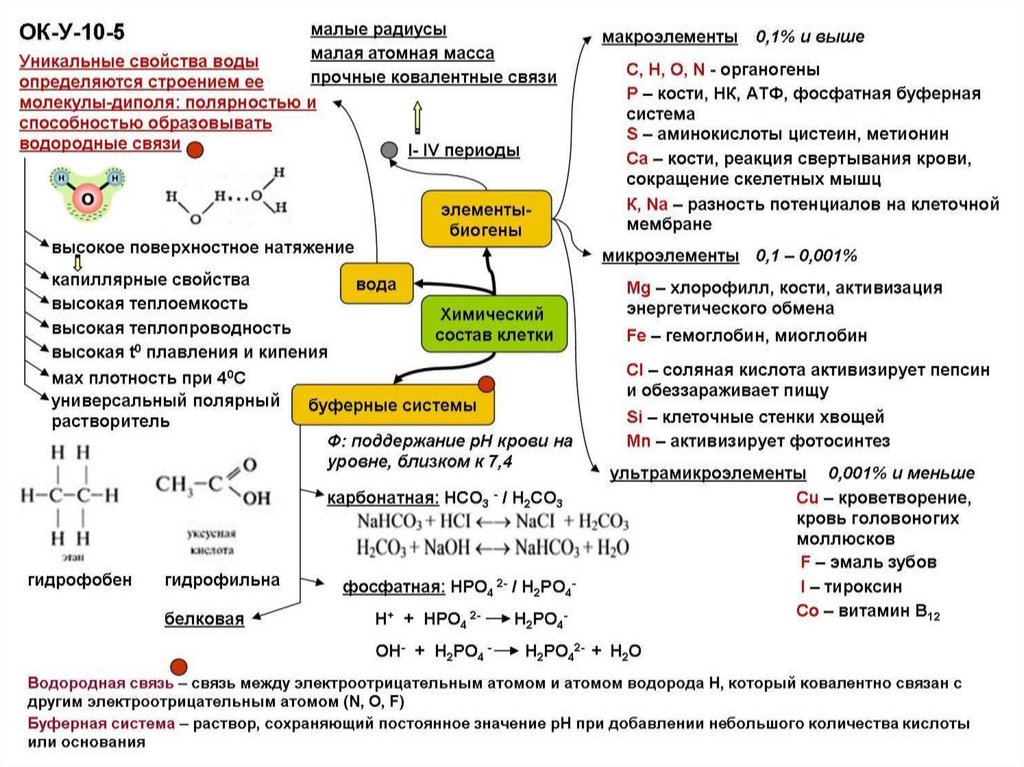
МИНЕРАЛЬНЫЕСОЛИ
Для процессов жизнедеятельности клетки наиболее важны:
катионы: K, Na, Ca, Mg
анионы: Cl, H2PO4, HCO3
ОБЕСПЕЧИВАЮТ:
- Поддержание постоянства внутренней среды;
- Кислотно-щелочное равновесие;
- Влияют на активность ферментов;
- Входят в состав тканей и органов;
- Участвуют в реакциях.
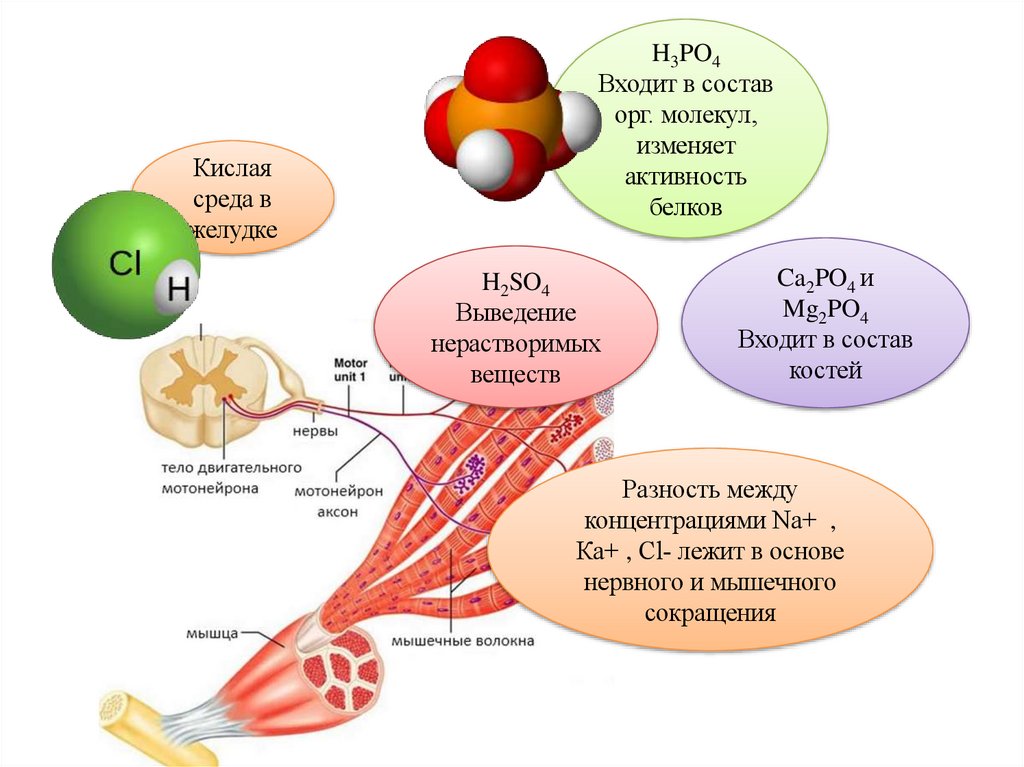
21.
Кислаясреда в
желудке
H3PO4
Входит в состав
орг. молекул,
изменяет
активность
белков
H2SO4
Выведение
нерастворимых
веществ
Ca2PO4 и
Mg2PO4
Входит в состав
костей
Разность между
концентрациями Nа+ ,
Ка+ , Сl‐ лежит в основе
нервного и мышечного
сокращения
22.
Минеральные соли составляют 1–1,5% общеймассы клетки
1. Создают кислую или щелочную реакцию
среды
2. Ca2+ входит в состав костей и зубов, участвует в
свёртывании крови
3. K+ и Na+ обеспечивают раздражимость клеток
4. Cl– входит в состав желудочного сока
5. Mg2+ содержится в хлорофилле
6. I – компонент тироксина (гормона
щитовидной железы)
7. Fe2+ входит в состав гемоглобина
8. Cu, Mn, B участвуют в кроветворении,
фотосинтезе, влияют на рост растений
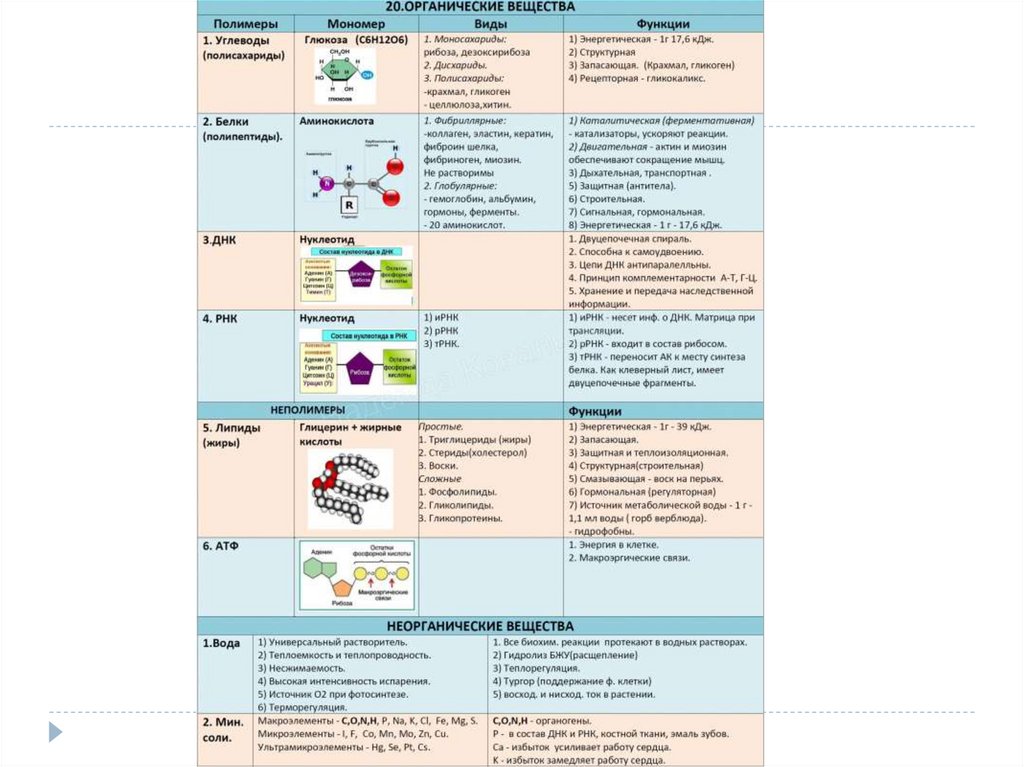
23. Органические вещества клетки
24.
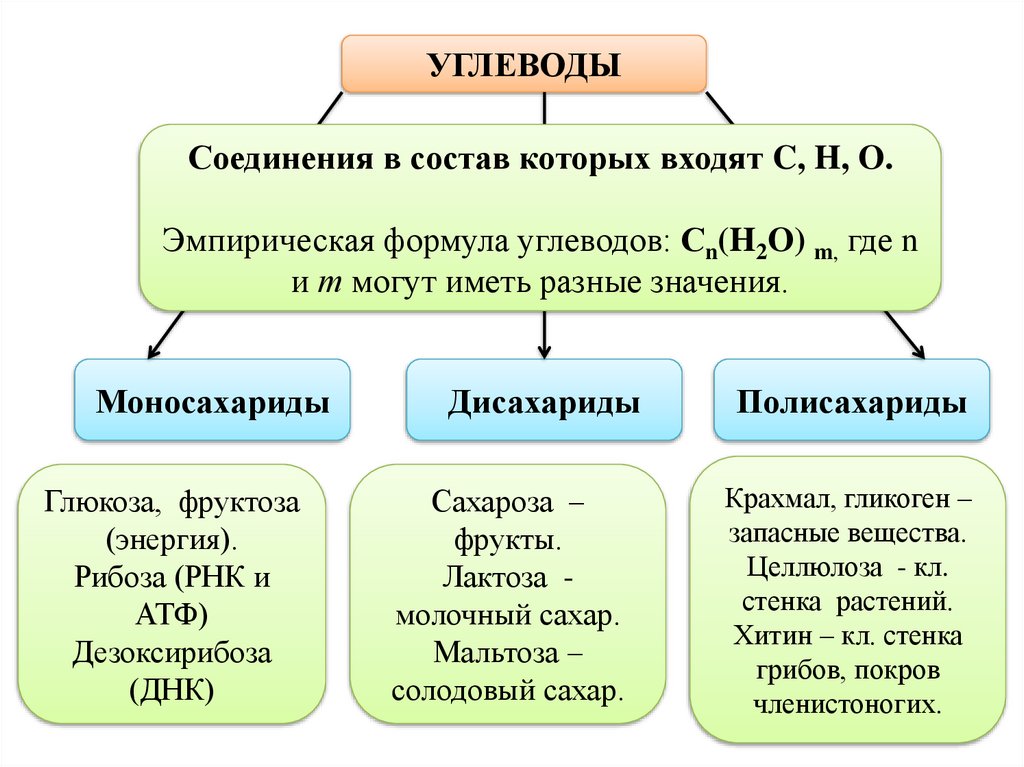
УГЛЕВОДЫСоединения в состав которых входят C, H, O.
Эмпирическая формула углеводов: Сn(H2O) m, где n
и т могут иметь разные значения.
Моносахариды
Глюкоза, фруктоза
(энергия).
Рибоза (РНК и
АТФ)
Дезоксирибоза
(ДНК)
Дисахариды
Полисахариды
Сахароза –
фрукты.
Лактоза молочный сахар.
Мальтоза –
солодовый сахар.
Крахмал, гликоген –
запасные вещества.
Целлюлоза - кл.
стенка растений.
Хитин – кл. стенка
грибов, покров
членистоногих.
25.
26.
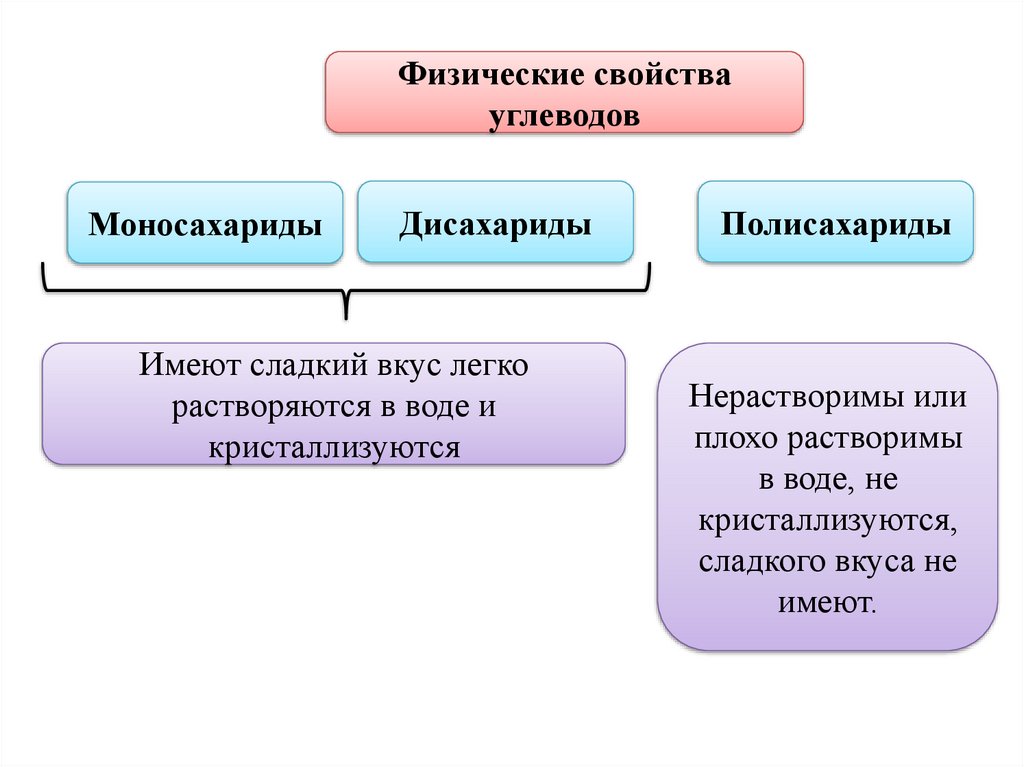
Физические свойствауглеводов
Моносахариды
Дисахариды
Имеют сладкий вкус легко
растворяются в воде и
кристаллизуются
Полисахариды
Нерастворимы или
плохо растворимы
в воде, не
кристаллизуются,
сладкого вкуса не
имеют.
27.
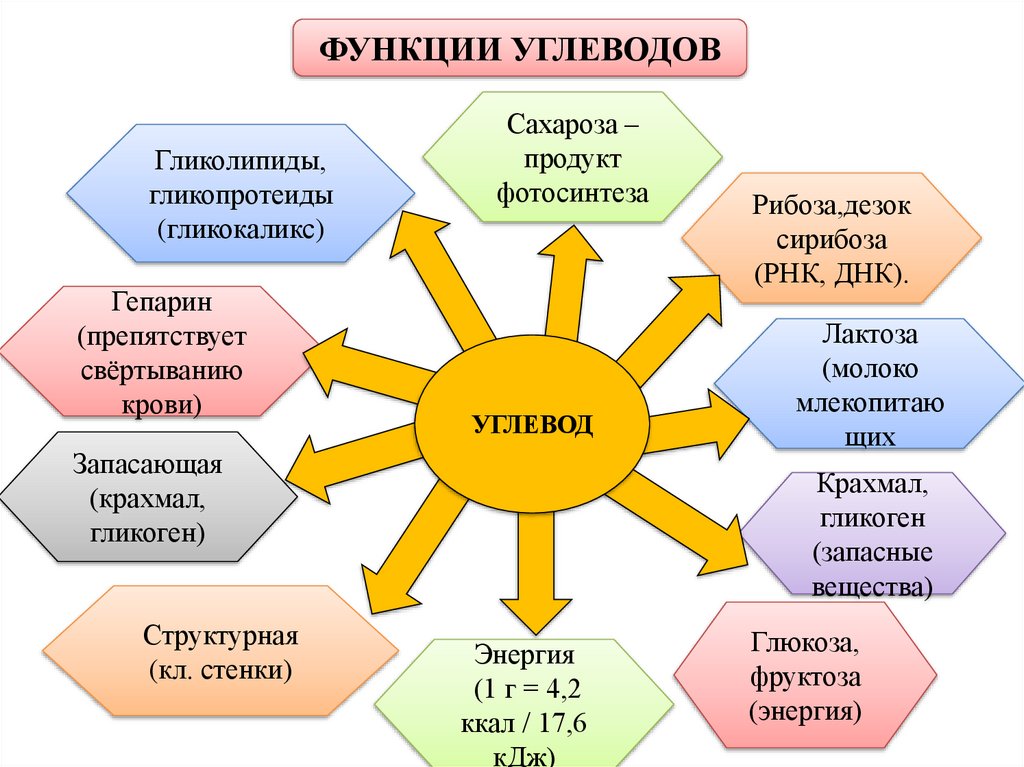
ФУНКЦИИ УГЛЕВОДОВГликолипиды,
гликопротеиды
(гликокаликс)
Гепарин
(препятствует
свёртыванию
крови)
Сахароза –
продукт
фотосинтеза
УГЛЕВОД
Запасающая
(крахмал,
гликоген)
Структурная
(кл. стенки)
Рибоза,дезок
сирибоза
(РНК, ДНК).
Лактоза
(молоко
млекопитаю
щих
Крахмал,
гликоген
(запасные
вещества)
Энергия
(1 г = 4,2
ккал / 17,6
кДж)
Глюкоза,
фруктоза
(энергия)
28. Углеводы (сахариды)
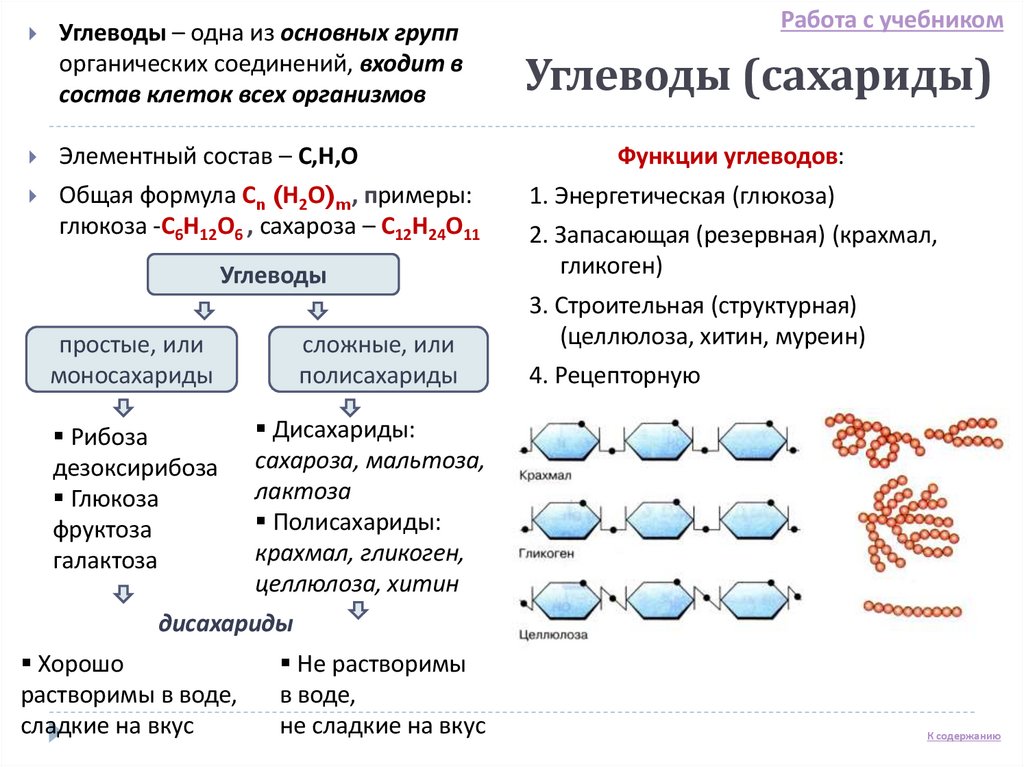
Углеводы – одна из основных группорганических соединений, входит в
состав клеток всех организмов
Элементный состав – С,Н,О
Общая формула Сn (Н2О)m, примеры:
глюкоза -С6Н12О6 , сахароза – С12Н24О11
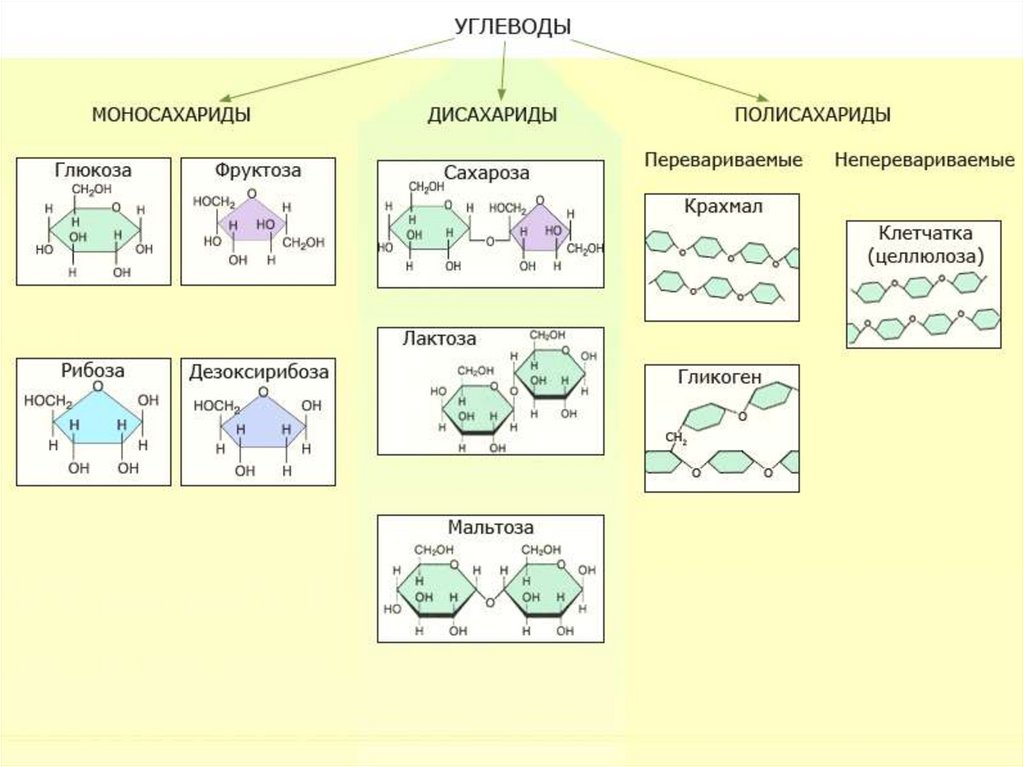
Углеводы
простые, или
моносахариды
сложные, или
полисахариды
Рибоза
дезоксирибоза
Глюкоза
фруктоза
галактоза
Дисахариды:
сахароза, мальтоза,
лактоза
Полисахариды:
крахмал, гликоген,
целлюлоза, хитин
Работа с учебником
Углеводы (сахариды)
Функции углеводов:
1. Энергетическая (глюкоза)
2. Запасающая (резервная) (крахмал,
гликоген)
3. Строительная (структурная)
(целлюлоза, хитин, муреин)
4. Рецепторную
дисахариды
Хорошо
растворимы в воде,
сладкие на вкус
Не растворимы
в воде,
не сладкие на вкус
К содержанию
29.
30. Функции углеводов:
• Энергетическая – основной источникэнергии для организма (сахароза, глюкоза)
60% энергии организм получает при
распаде углеводов. При расщеплении 1 г
углеводов выделяется 17,6 кДж энергии.
• Запасающая функция (полисахариды:
крахмал, гликоген)
• Структурная
• Рецепторная
31.
32.
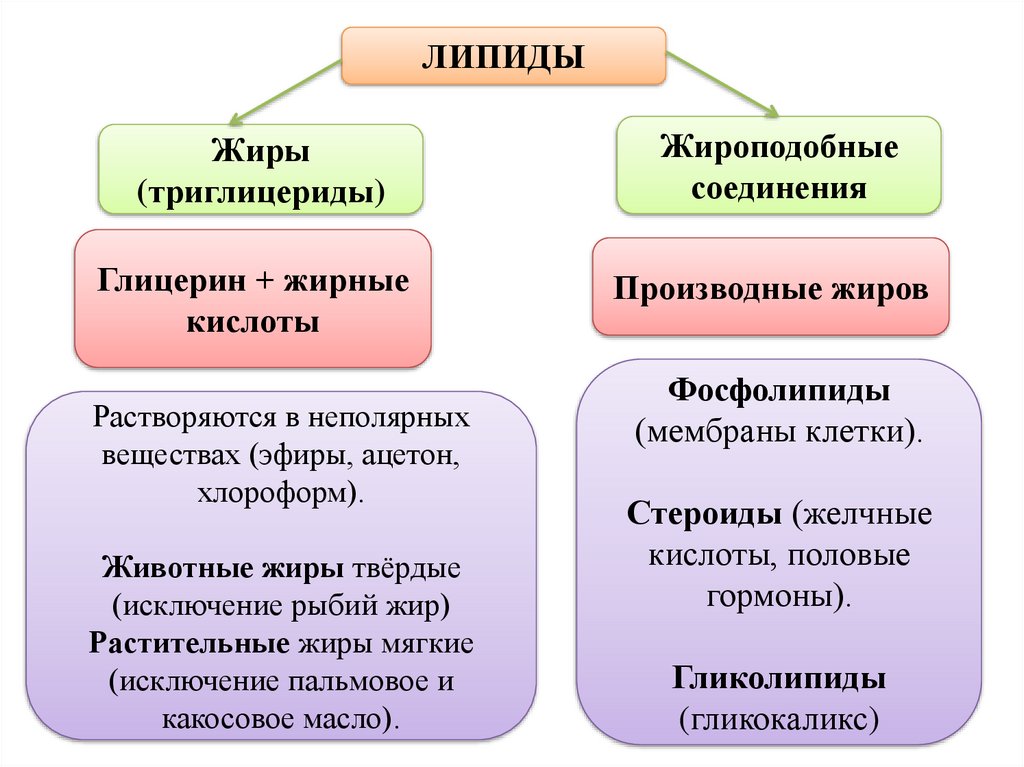
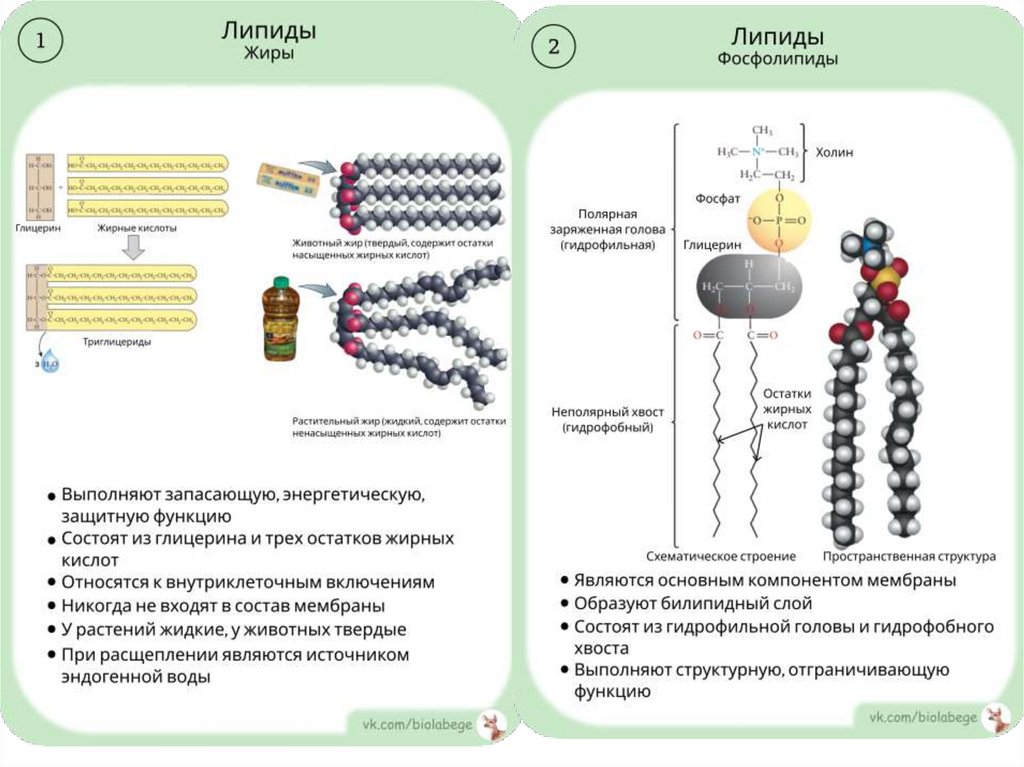
ЛИПИДЫЖиры
(триглицериды)
Жироподобные
соединения
Глицерин + жирные
кислоты
Производные жиров
Растворяются в неполярных
веществах (эфиры, ацетон,
хлороформ).
Животные жиры твёрдые
(исключение рыбий жир)
Растительные жиры мягкие
(исключение пальмовое и
какосовое масло).
Фосфолипиды
(мембраны клетки).
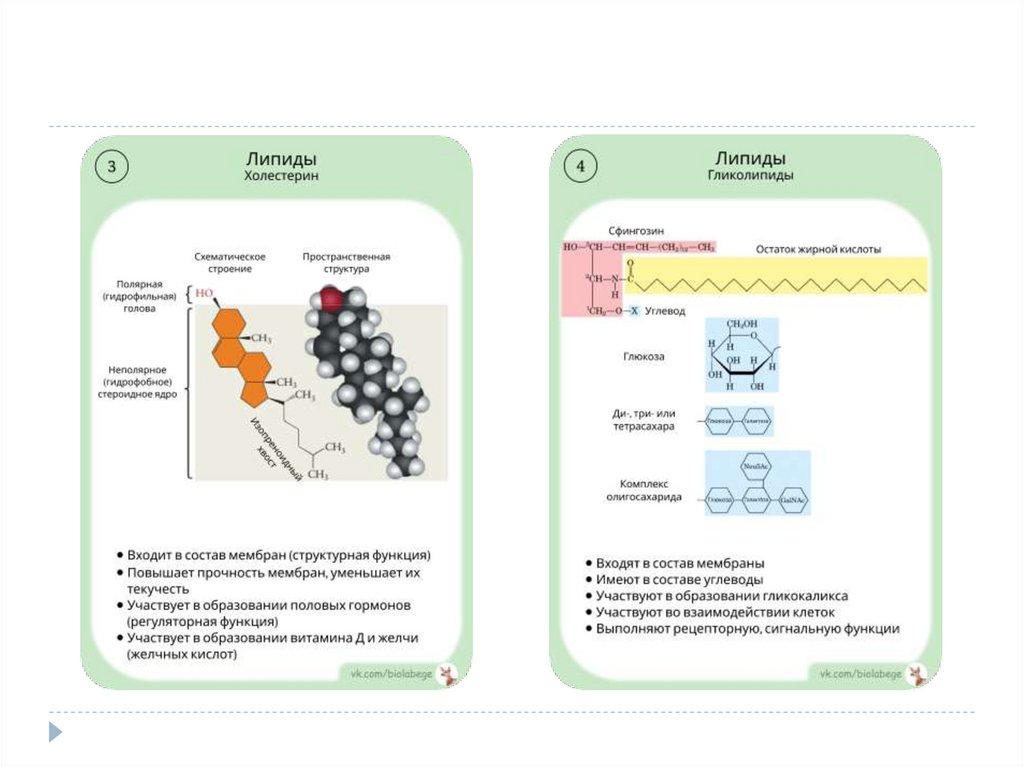
Стероиды (желчные
кислоты, половые
гормоны).
Гликолипиды
(гликокаликс)
33.
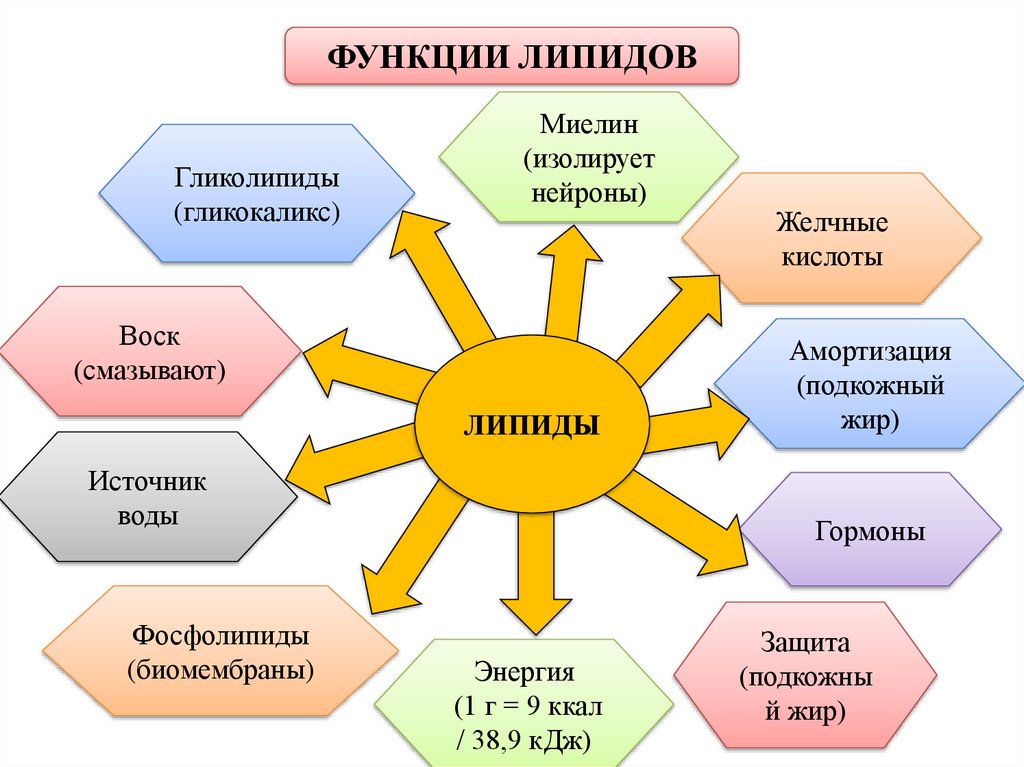
ФУНКЦИИ ЛИПИДОВГликолипиды
(гликокаликс)
Миелин
(изолирует
нейроны)
Воск
(смазывают)
ЛИПИДЫ
Источник
воды
Фосфолипиды
(биомембраны)
Желчные
кислоты
Амортизация
(подкожный
жир)
Гормоны
Энергия
(1 г = 9 ккал
/ 38,9 кДж)
Защита
(подкожны
й жир)
34. Липиды
Липиды – обширная группажироподобных веществ,
нерастворимых в воде
Большинство липидов состоит из
высокомолекулярных жирных кислот
и трехатомного спирта глицерина
Жиры – наиболее простые и
широко распространенные
липиды
Элементный состав – С,Н,О
Функции липидов:
1. энергетическая
В клетках содержится от 2-3% до 50-90%
2. запасающая (жиры)
Содержатся во всех без исключения
клетках
3. источник воды
4. защитная (теплоизоляционная)
5. способствует плавучести
6. строительная
7. регуляторная (гормоны).
К содержанию
35.
36.
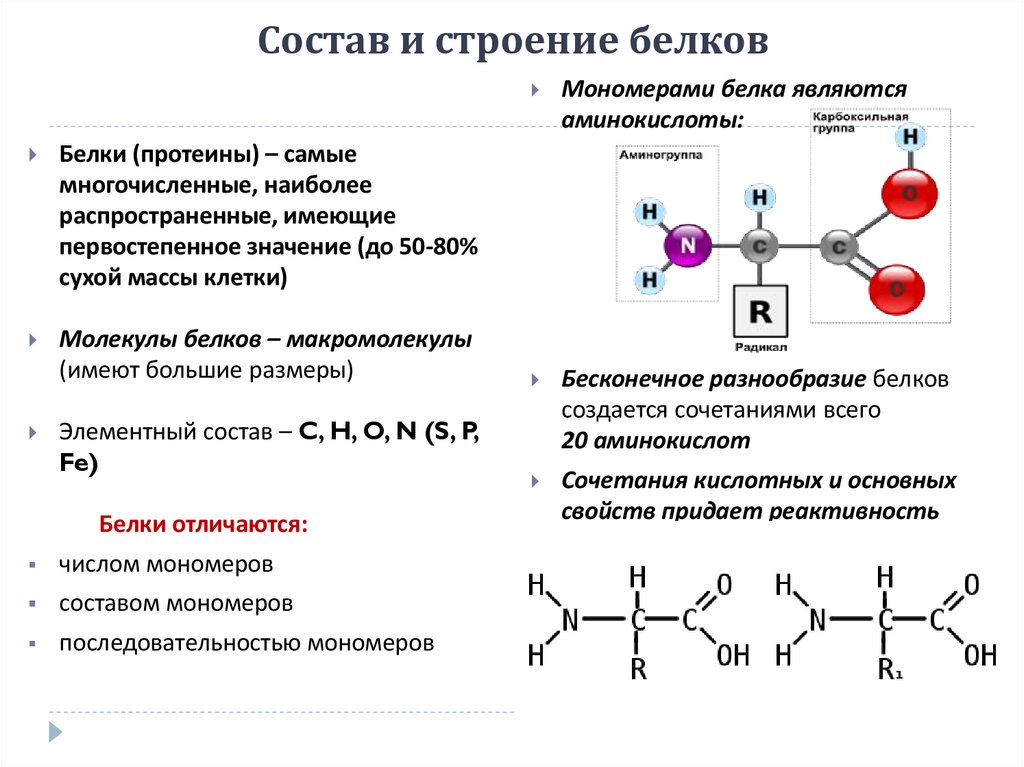
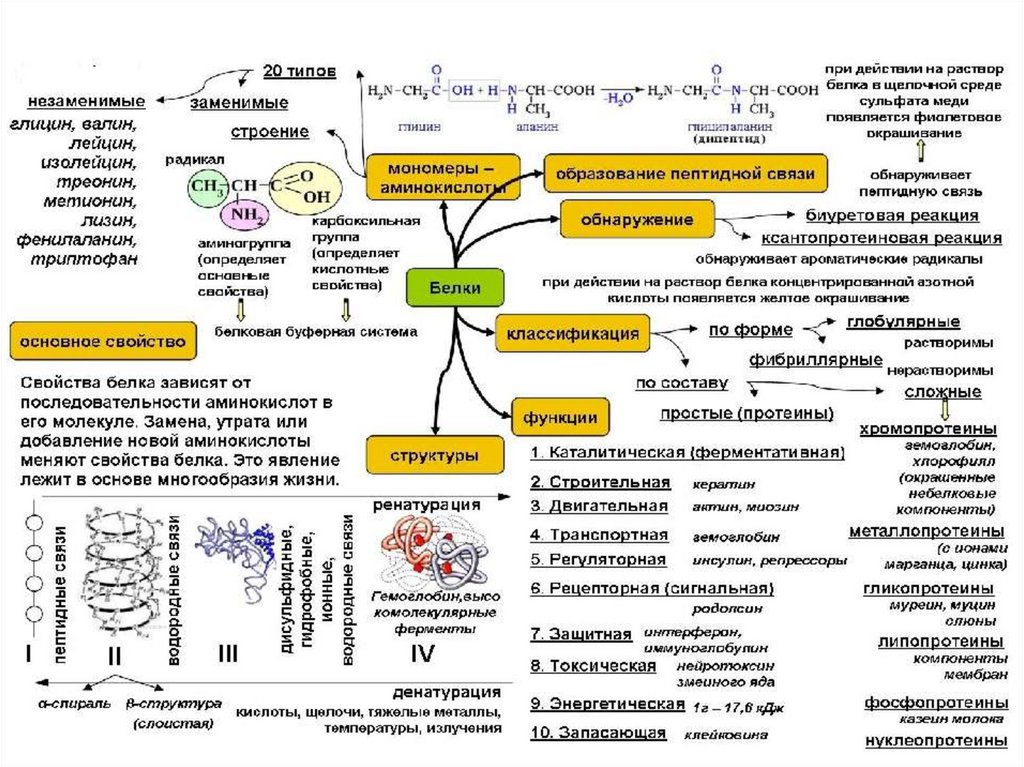
37. Состав и строение белков
Белки (протеины) – самыемногочисленные, наиболее
распространенные, имеющие
первостепенное значение (до 50-80%
сухой массы клетки)
Молекулы белков – макромолекулы
(имеют большие размеры)
Элементный состав – C, H, O, N (S, P,
Fe)
Белки отличаются:
числом мономеров
составом мономеров
последовательностью мономеров
Мономерами белка являются
аминокислоты:
Бесконечное разнообразие белков
создается сочетаниями всего
20 аминокислот
Сочетания кислотных и основных
свойств придает реактивность
38.
В природеизвестно более
150 различных
аминокислот, но в
построении
белков живых
организмов
участвуют только
20
Глицин
Аланин
Валин
Лейцин
Изолейцин
Серин
Треонин
Аспарагиновая
Глутаминовая
Аспарагин
Глутамин
Лизин
Аргинин
Цистеин
Метионин
Фенилаланин
Тирозин
Триптофан
Гистидин
Пролин
гли
ала
вал
лей
иле
сер
тре
асп
глу
асн
глн
лиз
арг
цис
мет
фен
тир
трп
гис
про
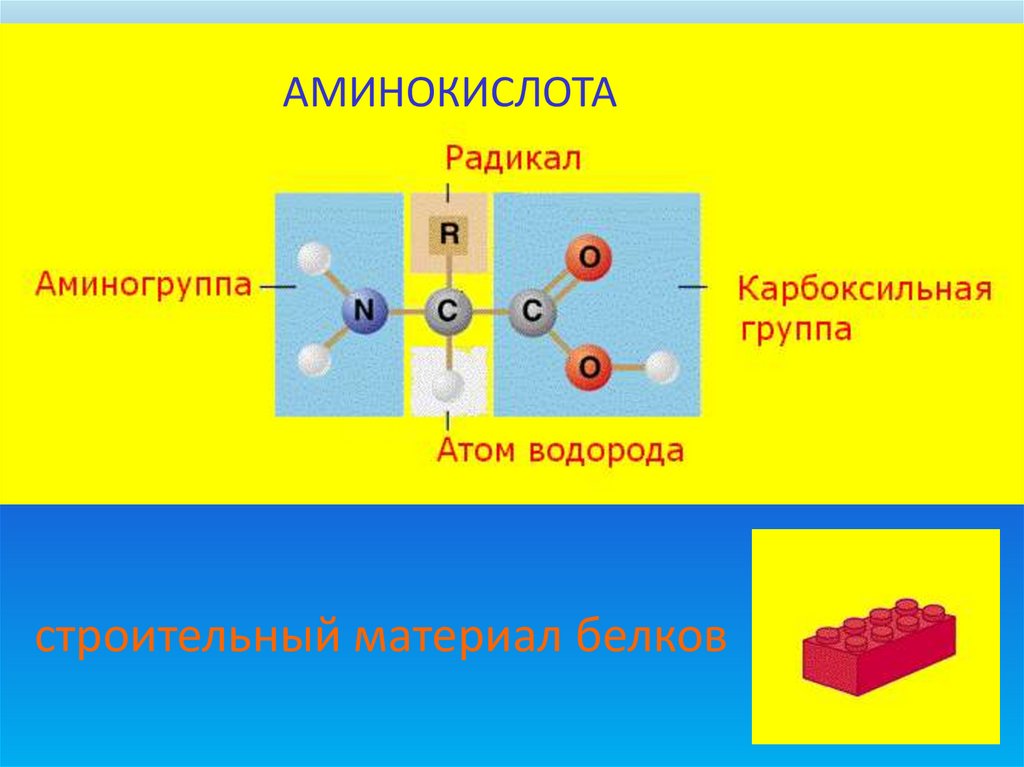
39.
АМИНОКИСЛОТАстроительный материал белков
40.
41.
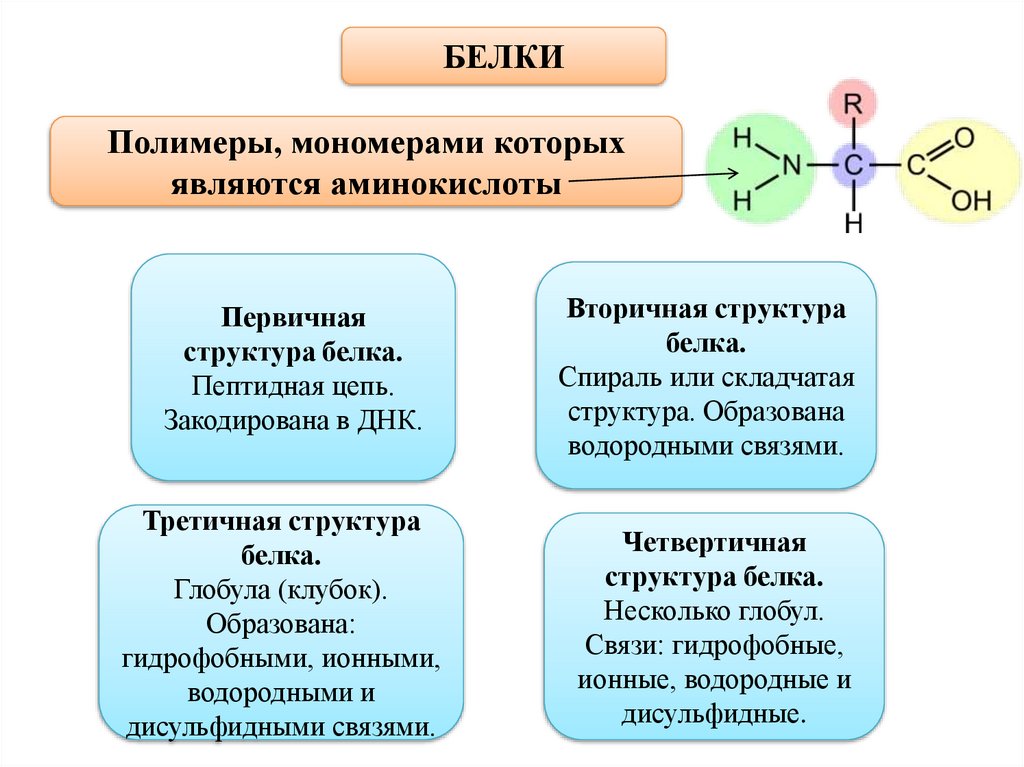
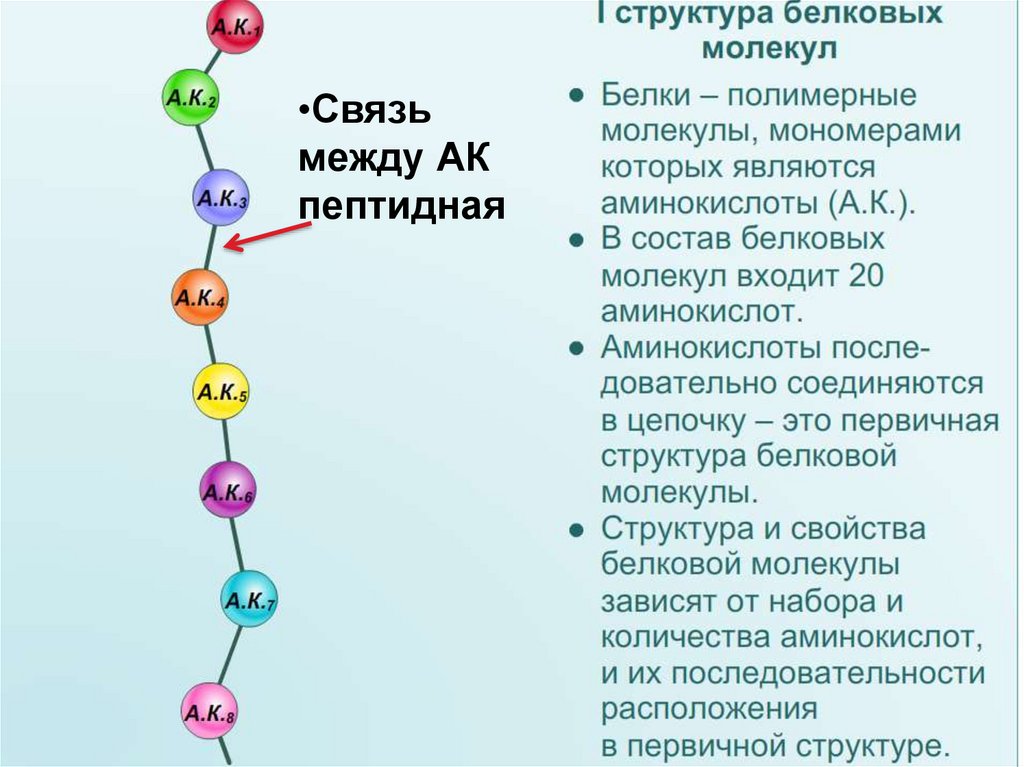
БЕЛКИПолимеры, мономерами которых
являются аминокислоты
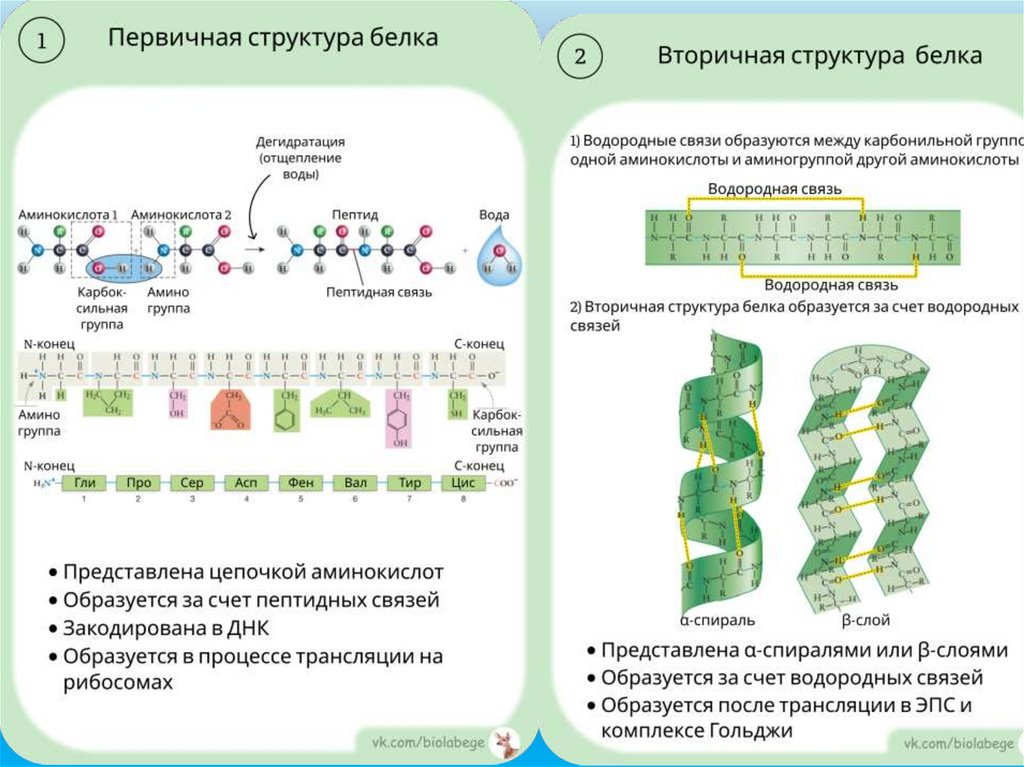
Первичная
структура белка.
Пептидная цепь.
Закодирована в ДНК.
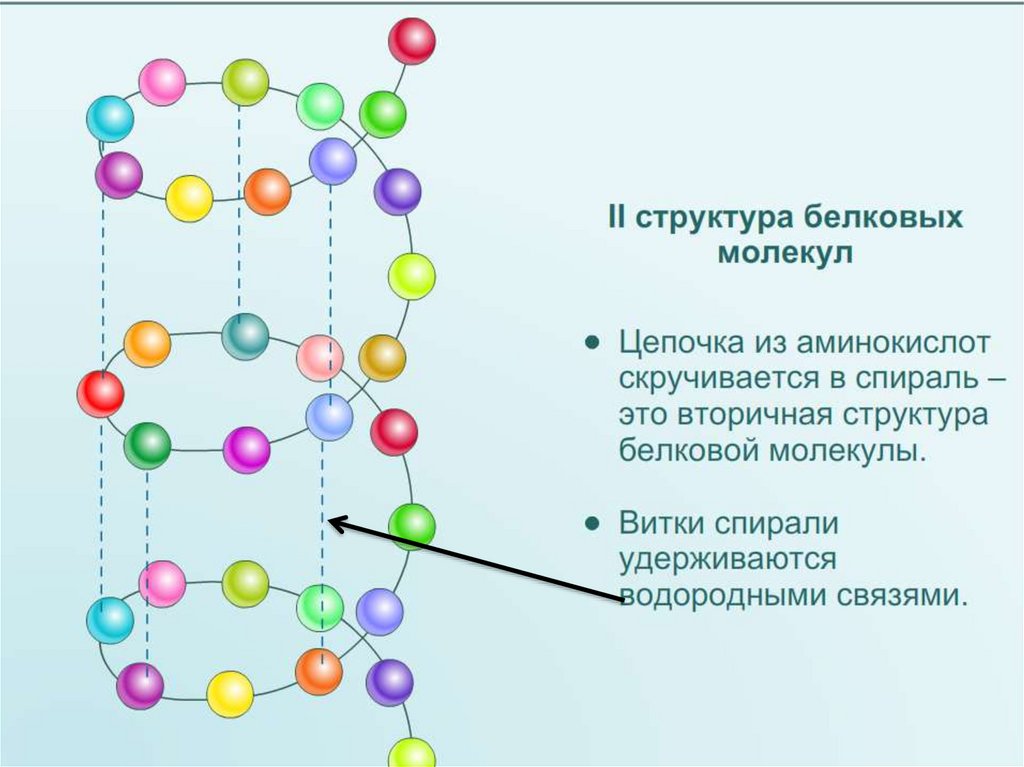
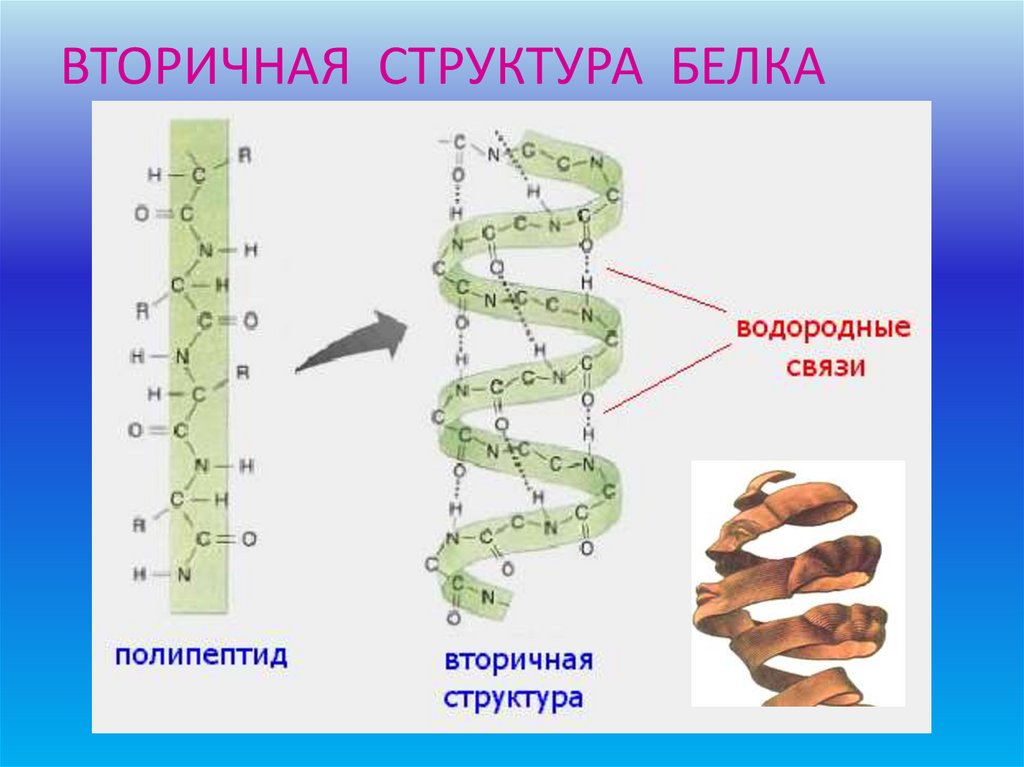
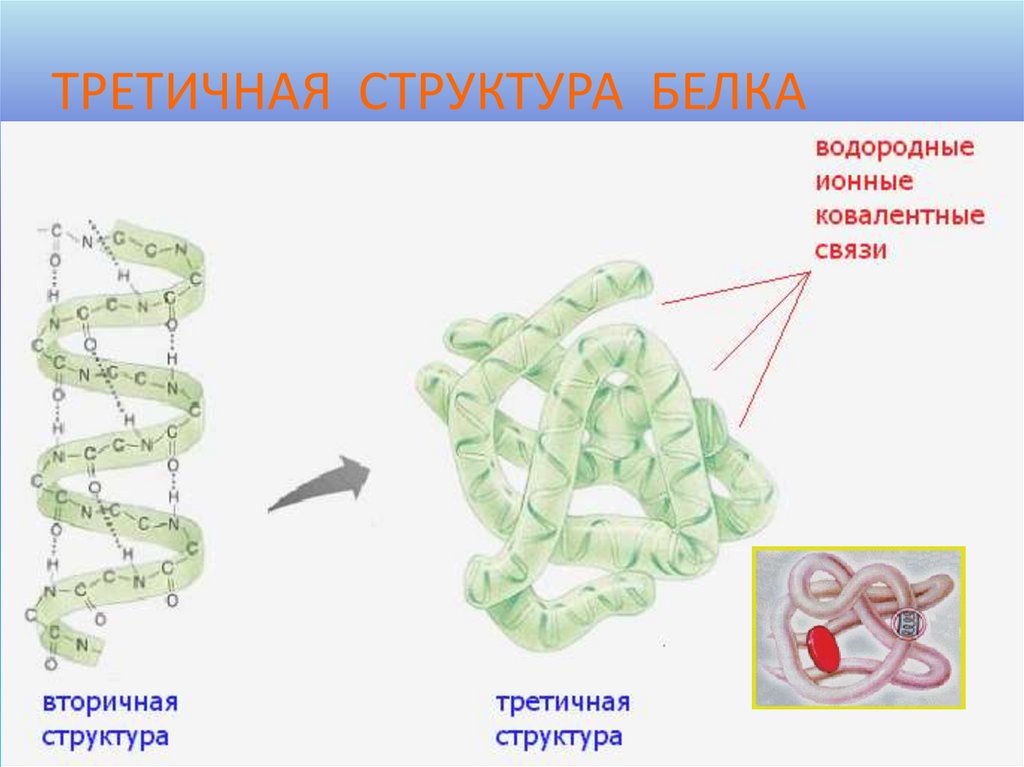
Вторичная структура
белка.
Спираль или складчатая
структура. Образована
водородными связями.
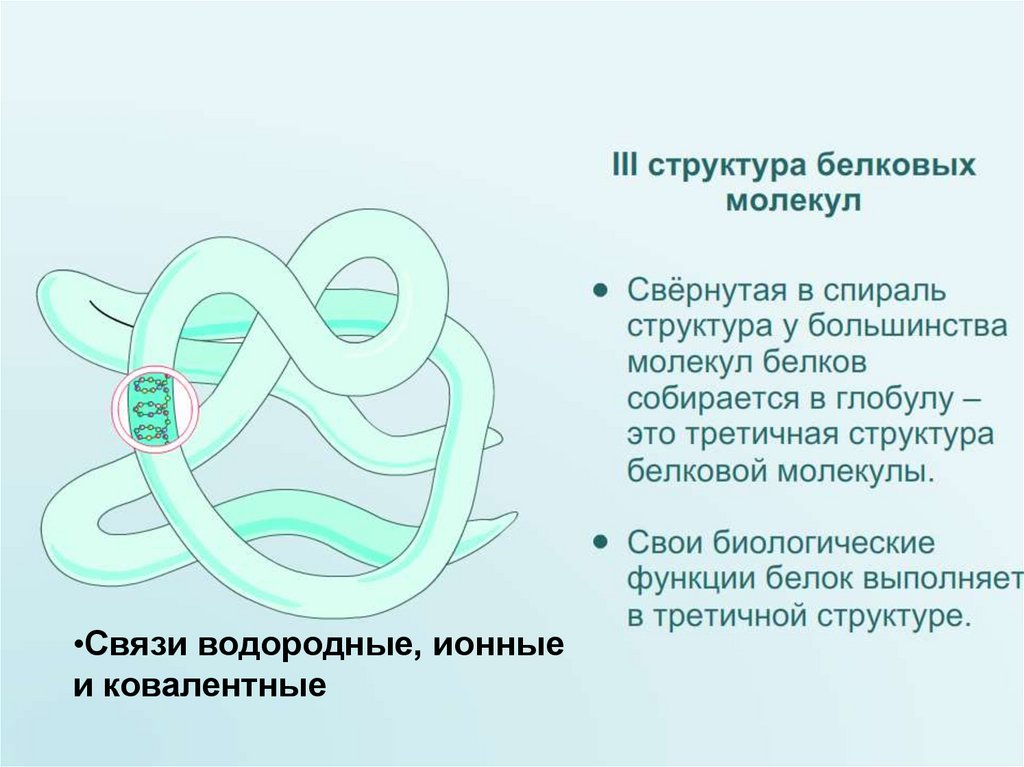
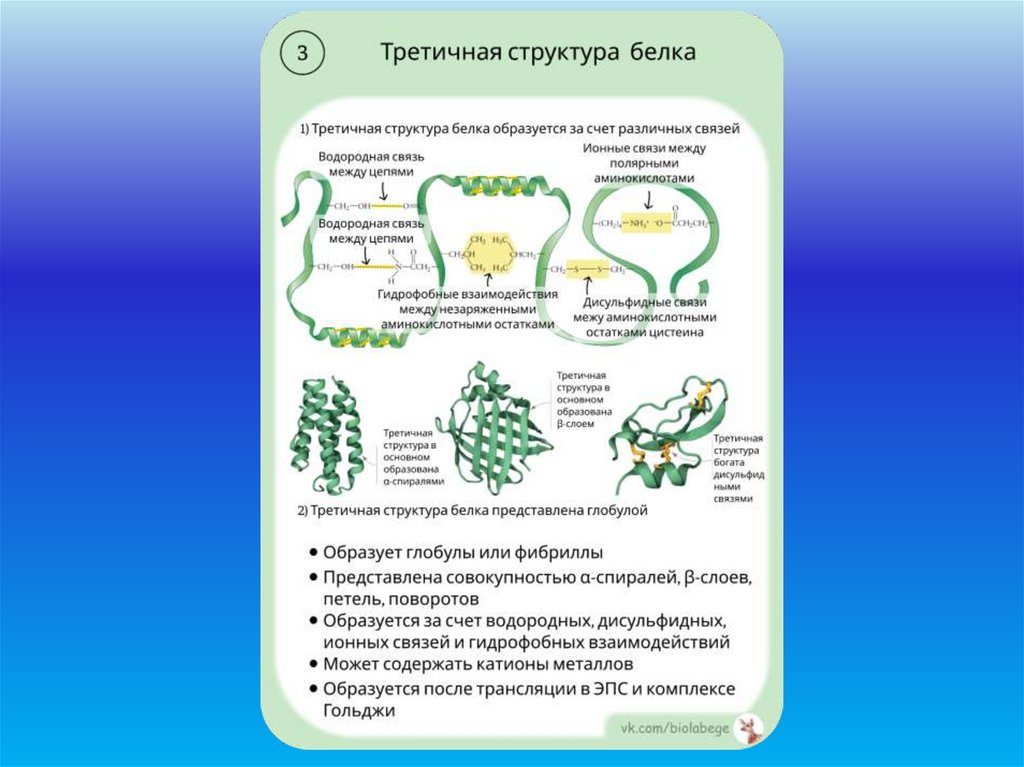
Третичная структура
белка.
Глобула (клубок).
Образована:
гидрофобными, ионными,
водородными и
дисульфидными связями.
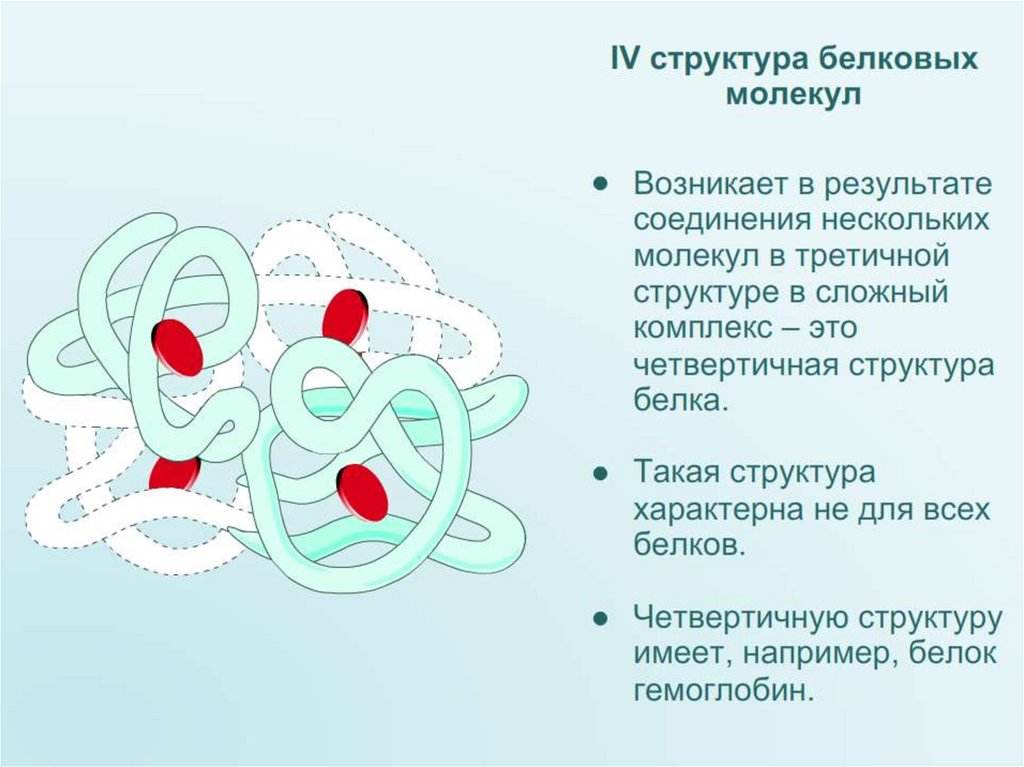
Четвертичная
структура белка.
Несколько глобул.
Связи: гидрофобные,
ионные, водородные и
дисульфидные.
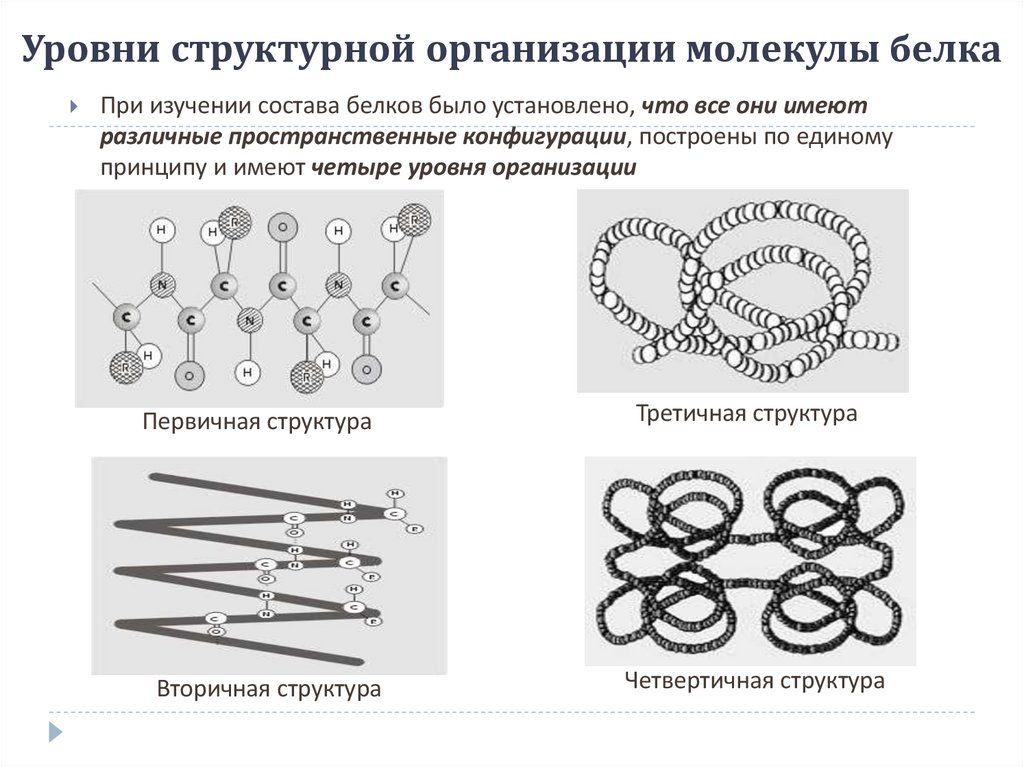
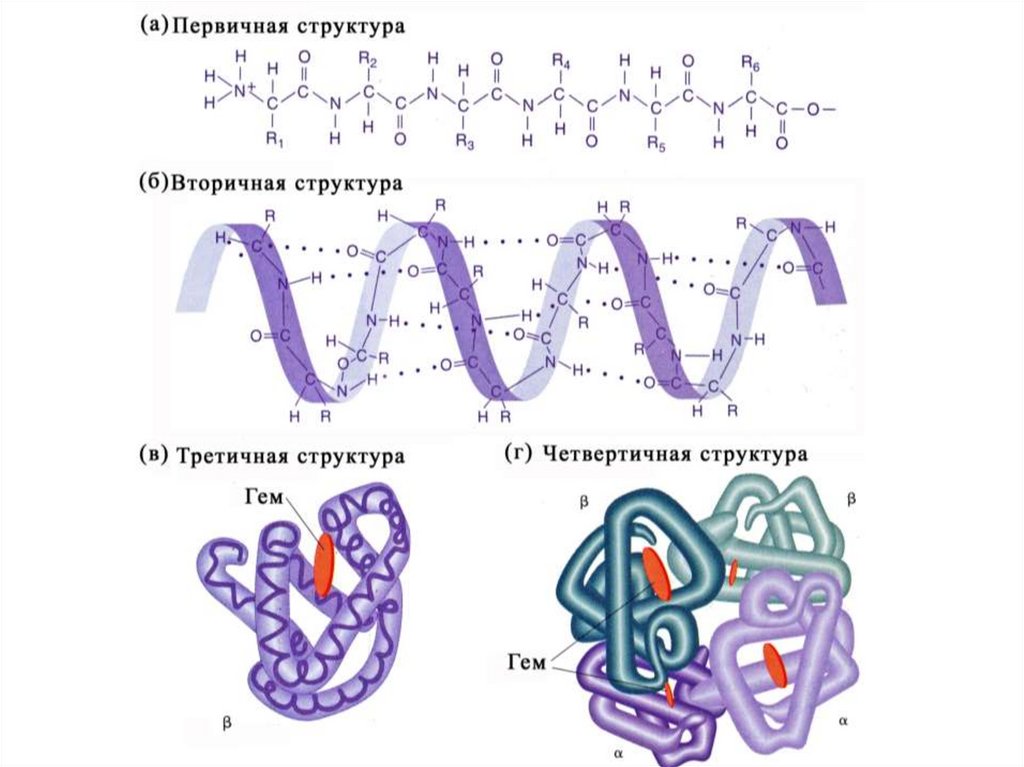
42. Уровни структурной организации молекулы белка
При изучении состава белков было установлено, что все они имеютразличные пространственные конфигурации, построены по единому
принципу и имеют четыре уровня организации
Первичная структура
Третичная структура
Вторичная структура
Четвертичная структура
43.
44.
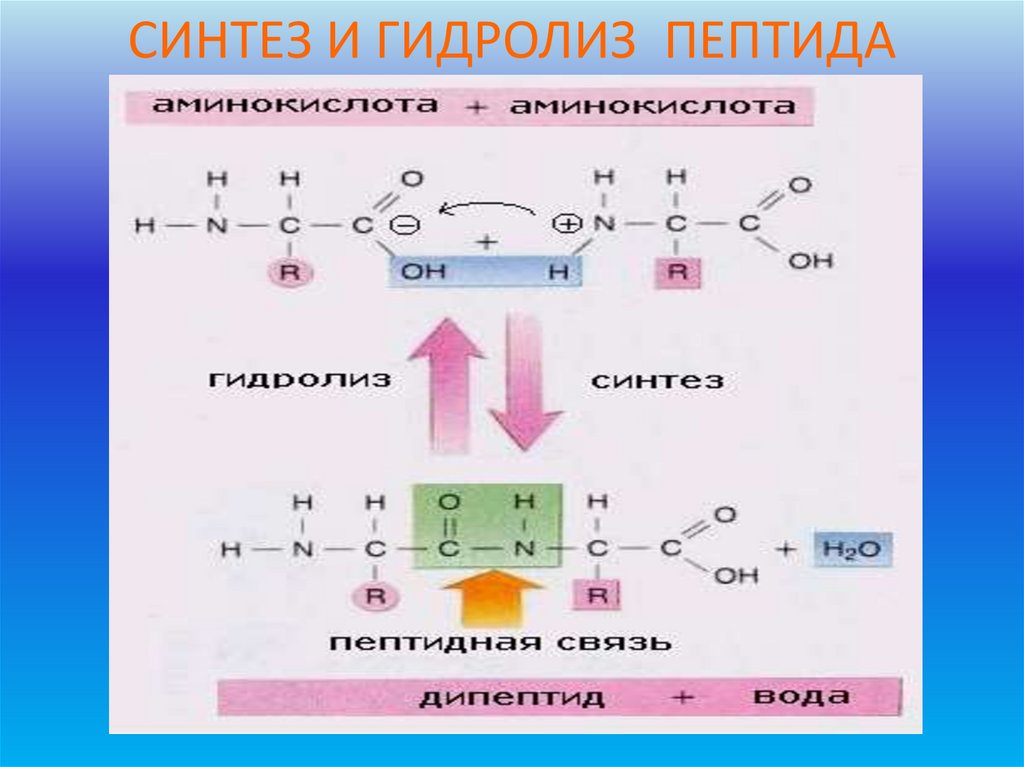
•Связьмежду АК
пептидная
45.
46.
47.
ВТОРИЧНАЯ СТРУКТУРА БЕЛКА48.
•Связи водородные, ионныеи ковалентные
49.
ТРЕТИЧНАЯ СТРУКТУРА БЕЛКА50.
51.
52.
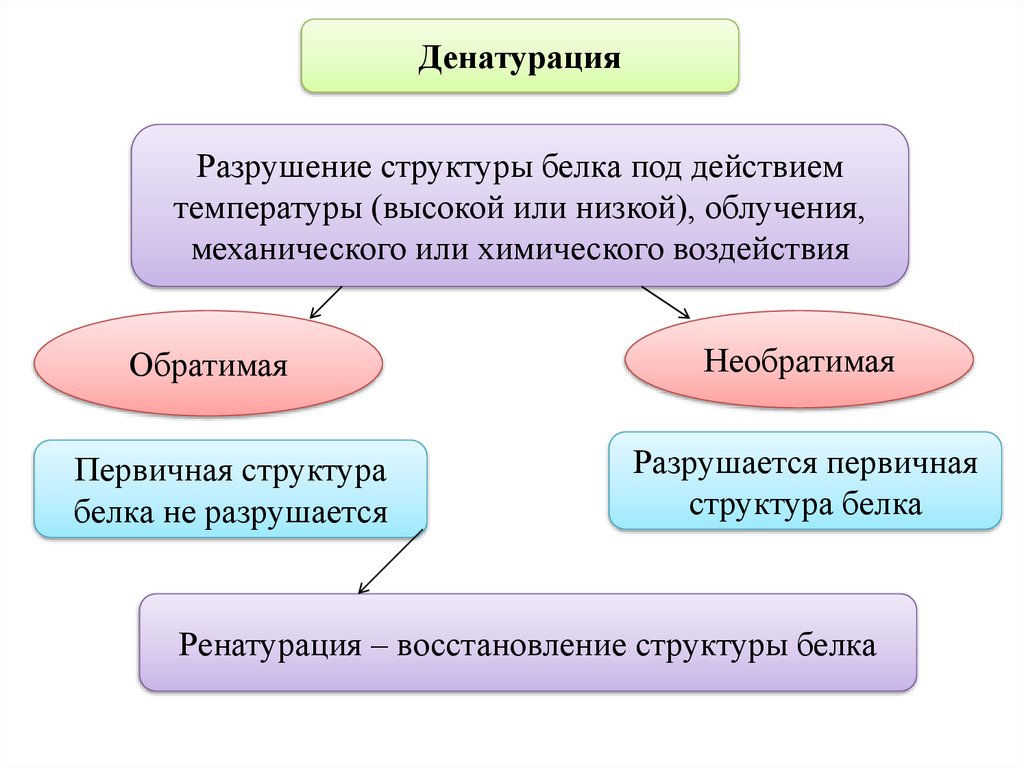
ДенатурацияРазрушение структуры белка под действием
температуры (высокой или низкой), облучения,
механического или химического воздействия
Обратимая
Необратимая
Первичная структура
белка не разрушается
Разрушается первичная
структура белка
Ренатурация – восстановление структуры белка
53.
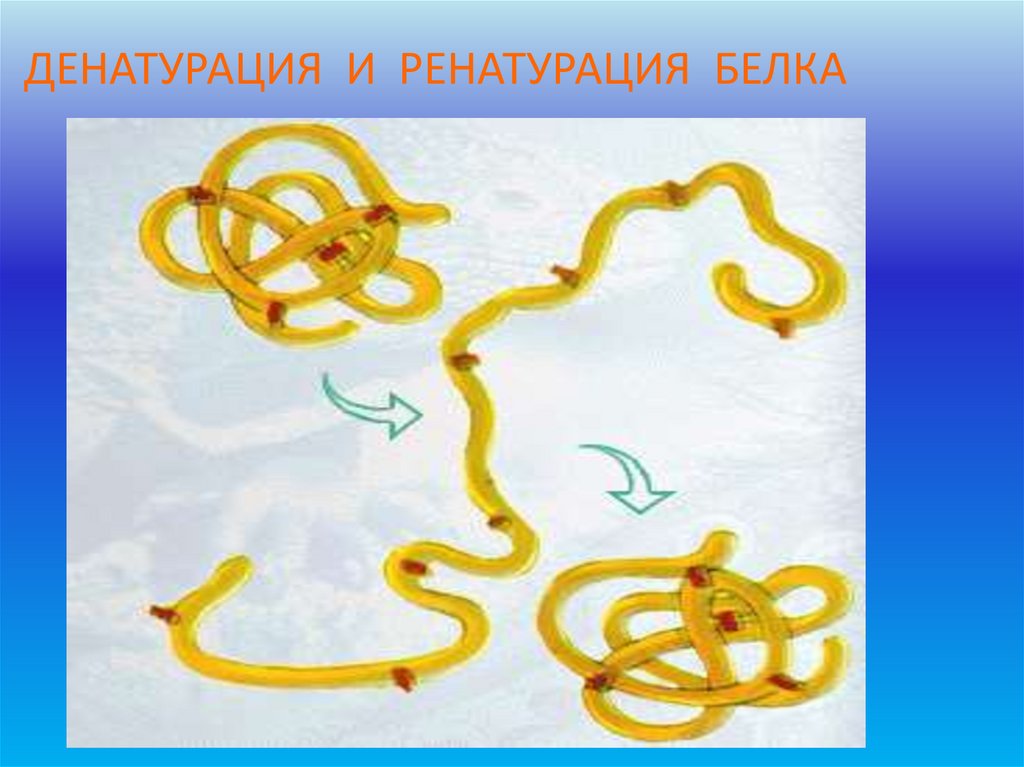
ДЕНАТУРАЦИЯ И РЕНАТУРАЦИЯ БЕЛКА54. Денатурация белков
Денатурация белков - это потеря белкамисвоих естественных свойств (растворимости)
вследствие нарушения пространственной
структуры их молекул
Денатурация происходит под
воздействием:
температуры
химических веществ
лучистой энергии и др.
Разрушаются химические связи начиная
с четвертичной структуры → третичная →
вторичная → первичная → аминокислоты
Этот процесс частично обратим, если
разрушение прошло до первичной структуры
Первичная структура определяет
особенности строения макромолекулы
белка.
Необратимая
денатурация
белка яйца
По составу белки делятся:
Простые
белки
Состоят только
из аминокислот
К содержанию
Сложные
белки
В состав входят
углеводы
(гликопротеины),
жиры
(липопротеины),
нуклеиновые
кислоты
(нуклеопротеины)
55.
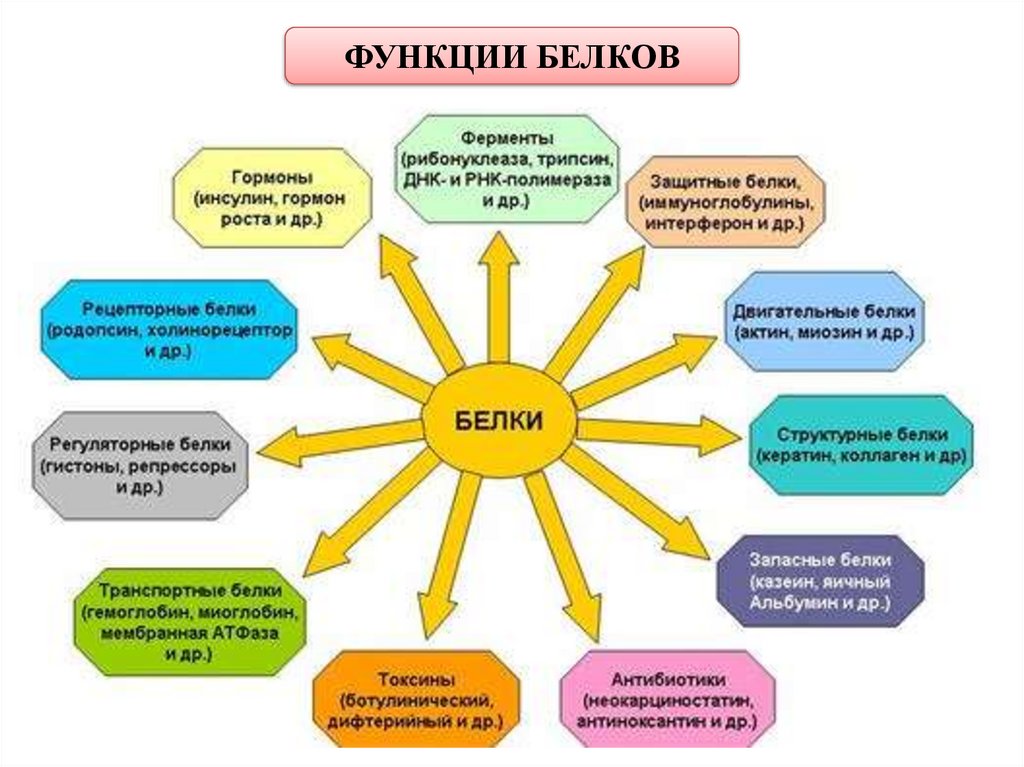
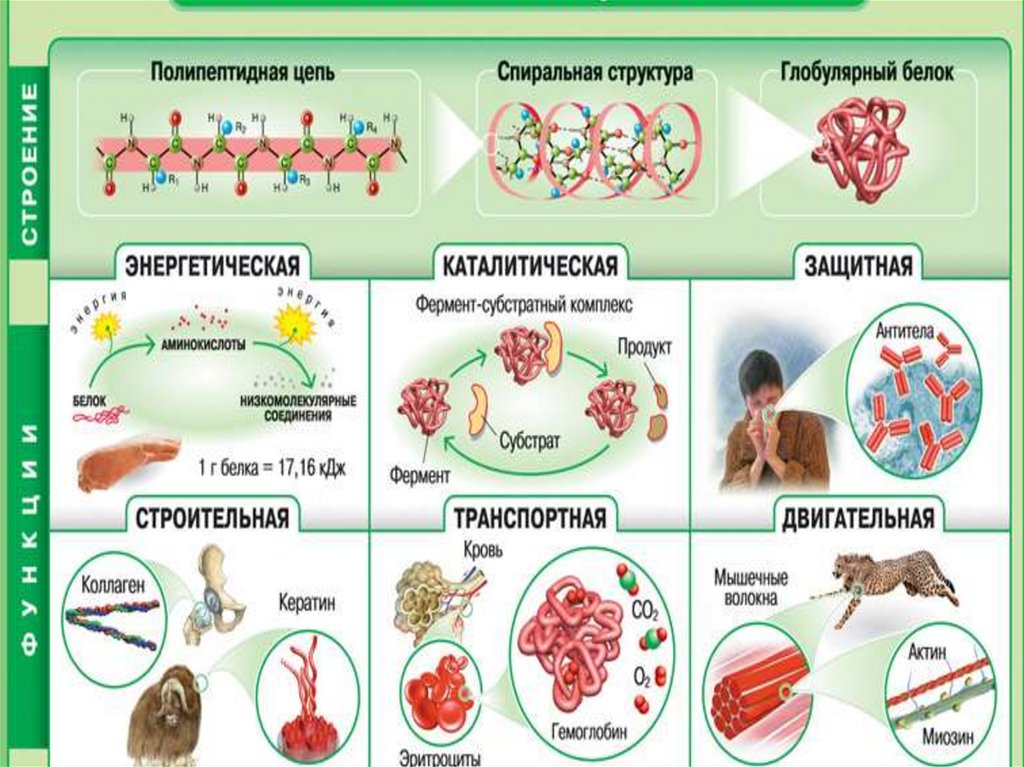
ФУНКЦИИ БЕЛКОВ56.
57.
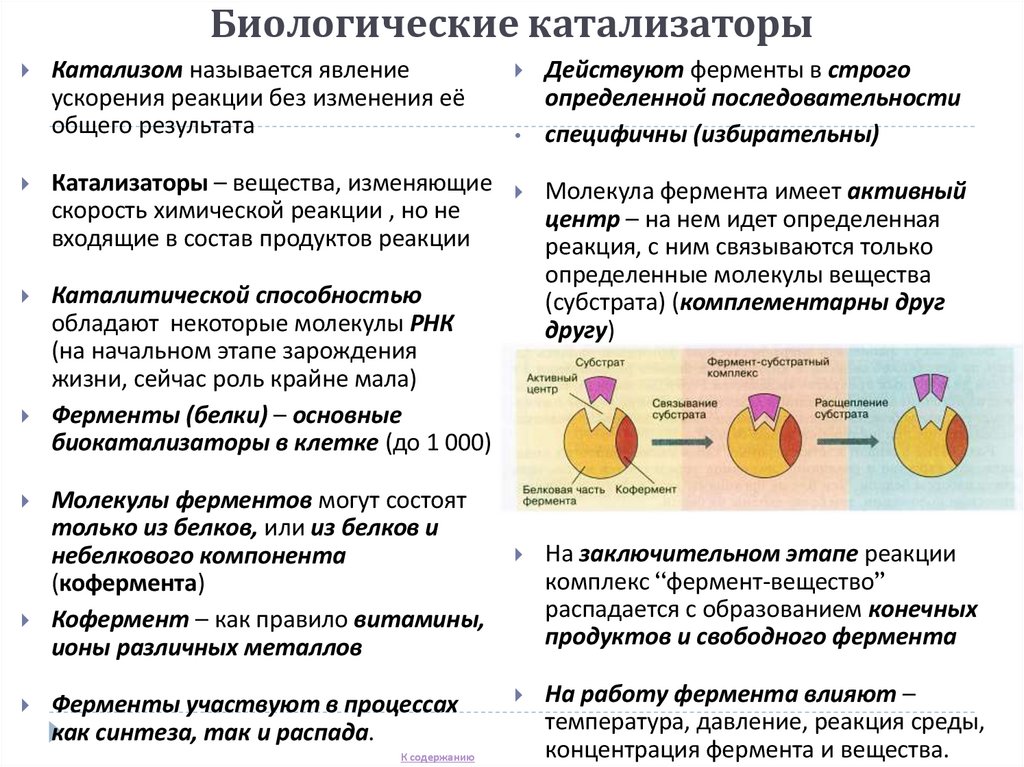
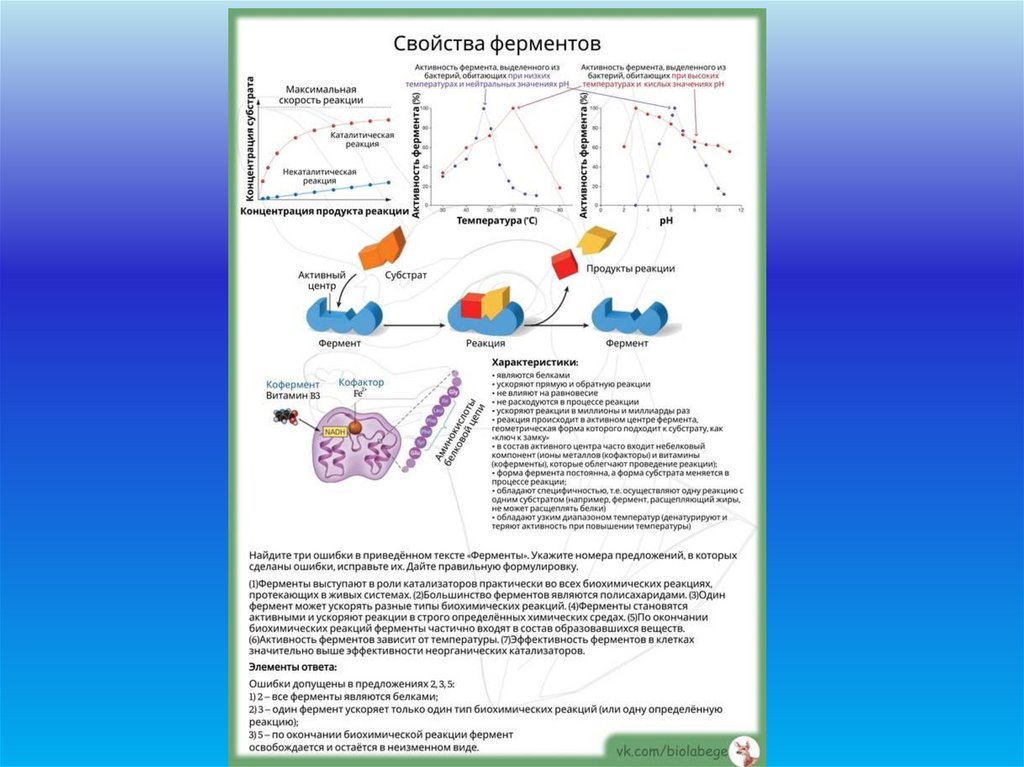
58. Биологические катализаторы
Катализом называется явлениеускорения реакции без изменения её
общего результата
Катализаторы – вещества, изменяющие
скорость химической реакции , но не
входящие в состав продуктов реакции
Каталитической способностью
обладают некоторые молекулы РНК
(на начальном этапе зарождения
жизни, сейчас роль крайне мала)
Ферменты (белки) – основные
биокатализаторы в клетке (до 1 000)
Молекула фермента имеет активный
центр – на нем идет определенная
реакция, с ним связываются только
определенные молекулы вещества
(субстрата) (комплементарны друг
другу)
На заключительном этапе реакции
комплекс “фермент-вещество”
распадается с образованием конечных
продуктов и свободного фермента
На работу фермента влияют –
температура, давление, реакция среды,
концентрация фермента и вещества.
Молекулы ферментов могут состоят
только из белков, или из белков и
небелкового компонента
(кофермента)
Кофермент – как правило витамины,
ионы различных металлов
Ферменты участвуют в процессах
как синтеза, так и распада.
К содержанию
Действуют ферменты в строго
определенной последовательности
специфичны (избирательны)
59.
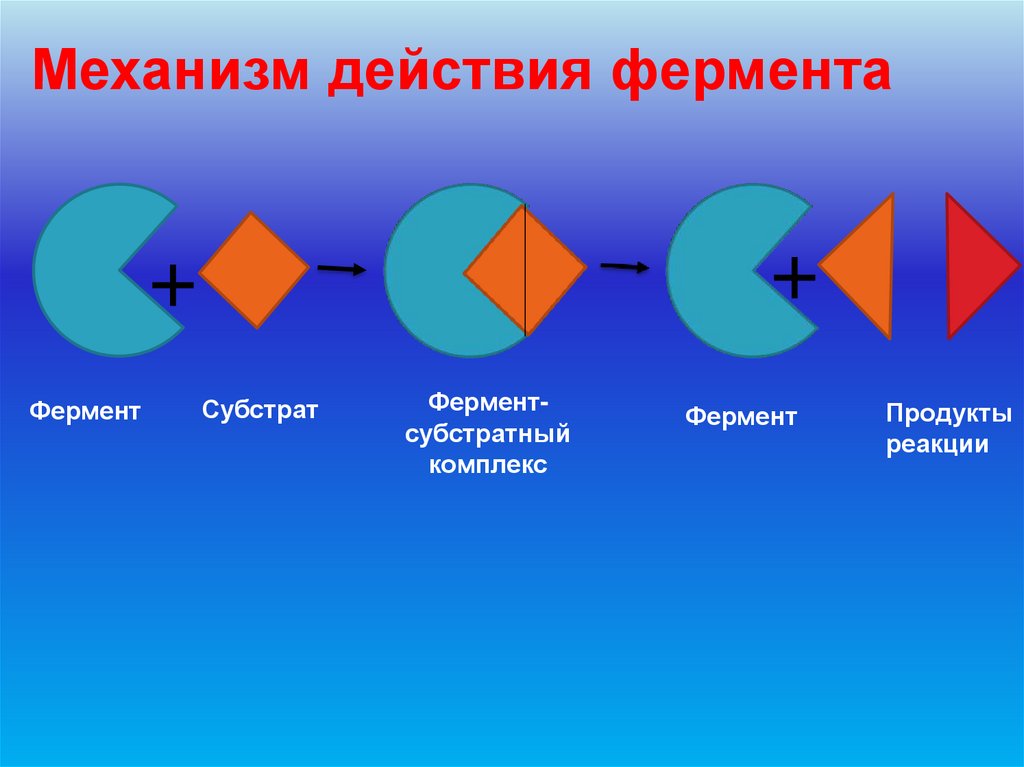
Механизм действия фермента+
+
Фермент
Субстрат
Ферментсубстратный
комплекс
Фермент
Продукты
реакции
60.
61.
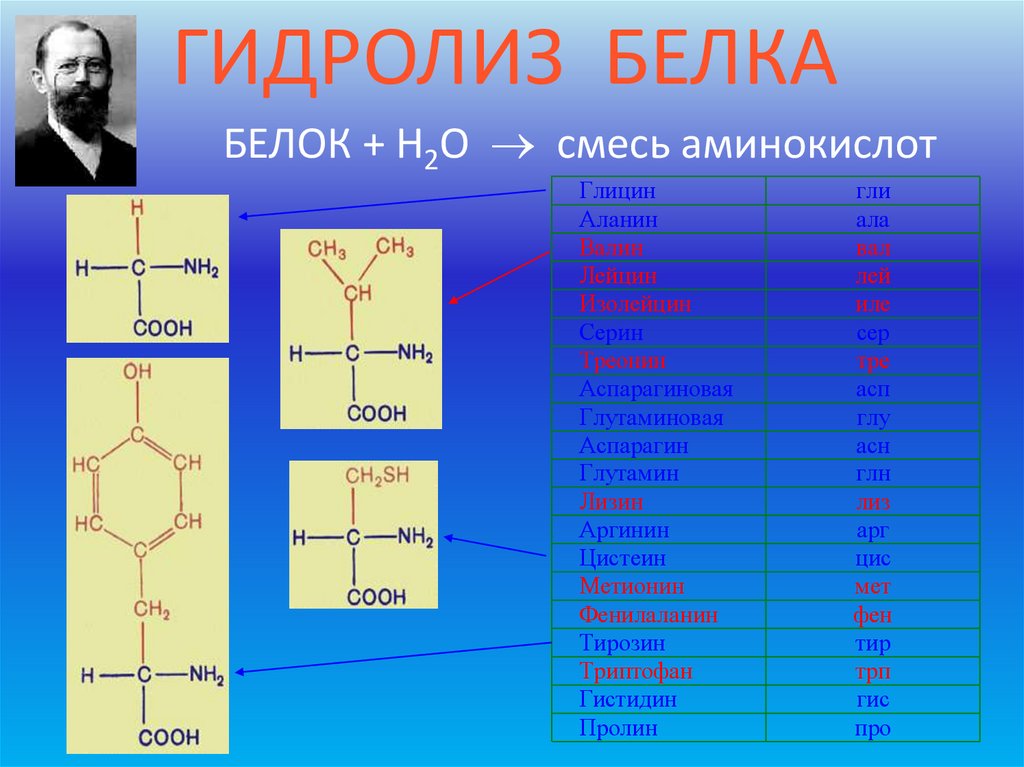
ГИДРОЛИЗ БЕЛКАБЕЛОК + H2O смесь аминокислот
Глицин
Аланин
Валин
Лейцин
Изолейцин
Серин
Треонин
Аспарагиновая
Глутаминовая
Аспарагин
Глутамин
Лизин
Аргинин
Цистеин
Метионин
Фенилаланин
Тирозин
Триптофан
Гистидин
Пролин
гли
ала
вал
лей
иле
сер
тре
асп
глу
асн
глн
лиз
арг
цис
мет
фен
тир
трп
гис
про
62.
СИНТЕЗ И ГИДРОЛИЗ ПЕПТИДА63.
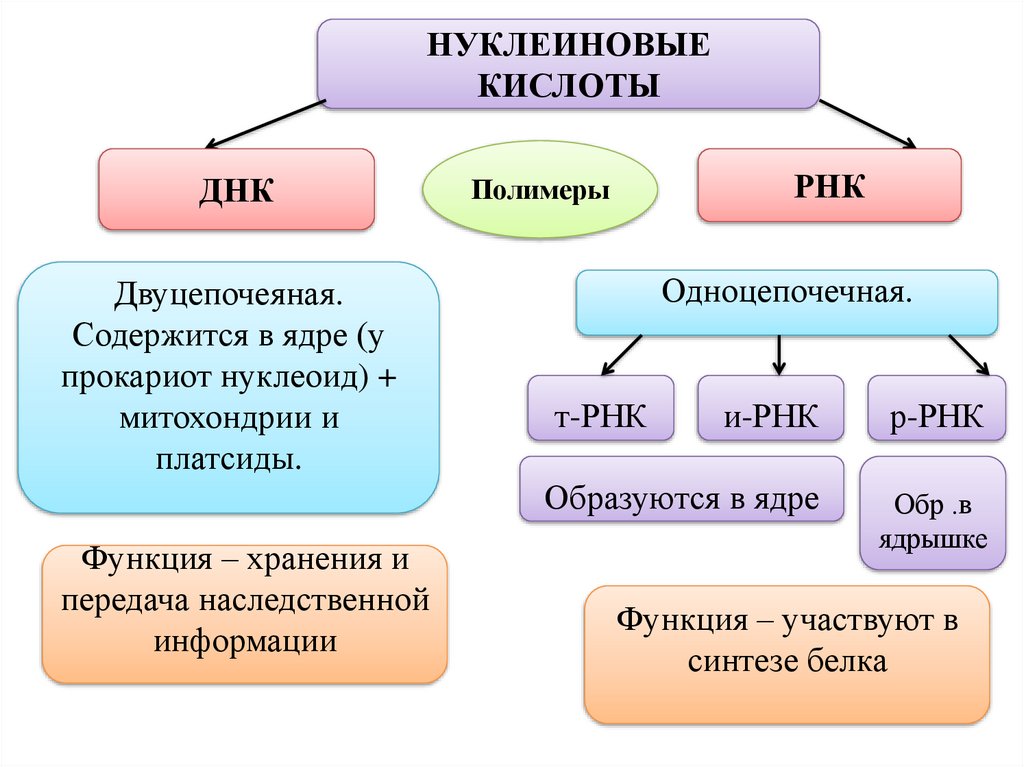
НУКЛЕИНОВЫЕКИСЛОТЫ
ДНК
Двуцепочеяная.
Содержится в ядре (у
прокариот нуклеоид) +
митохондрии и
платсиды.
Функция – хранения и
передача наследственной
информации
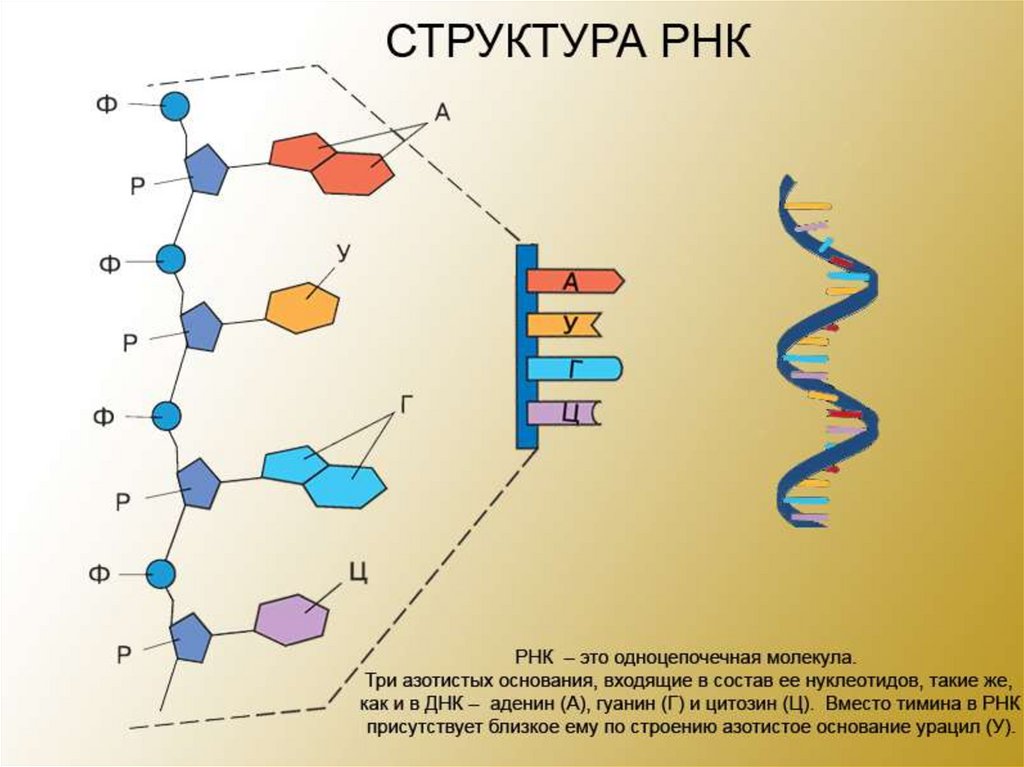
РНК
Полимеры
Одноцепочечная.
т-РНК
и-РНК
р-РНК
Образуются в ядре
Обр .в
ядрышке
Функция – участвуют в
синтезе белка
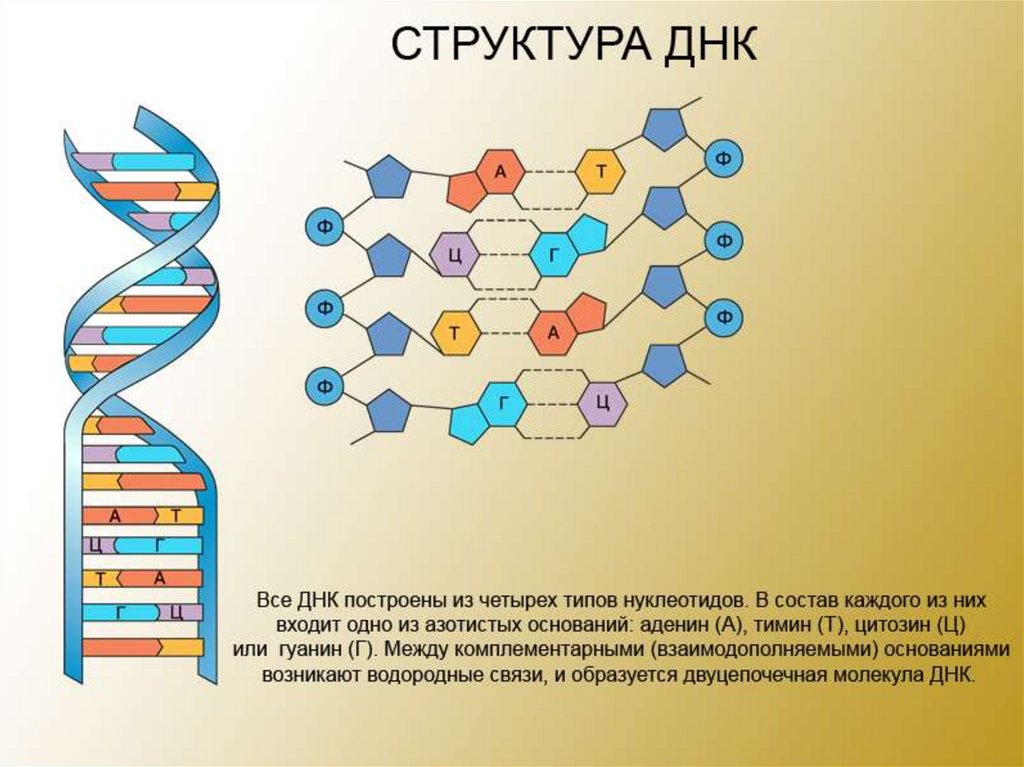
64. Модель ДНК
1953 г. – созданиемодели ДНК
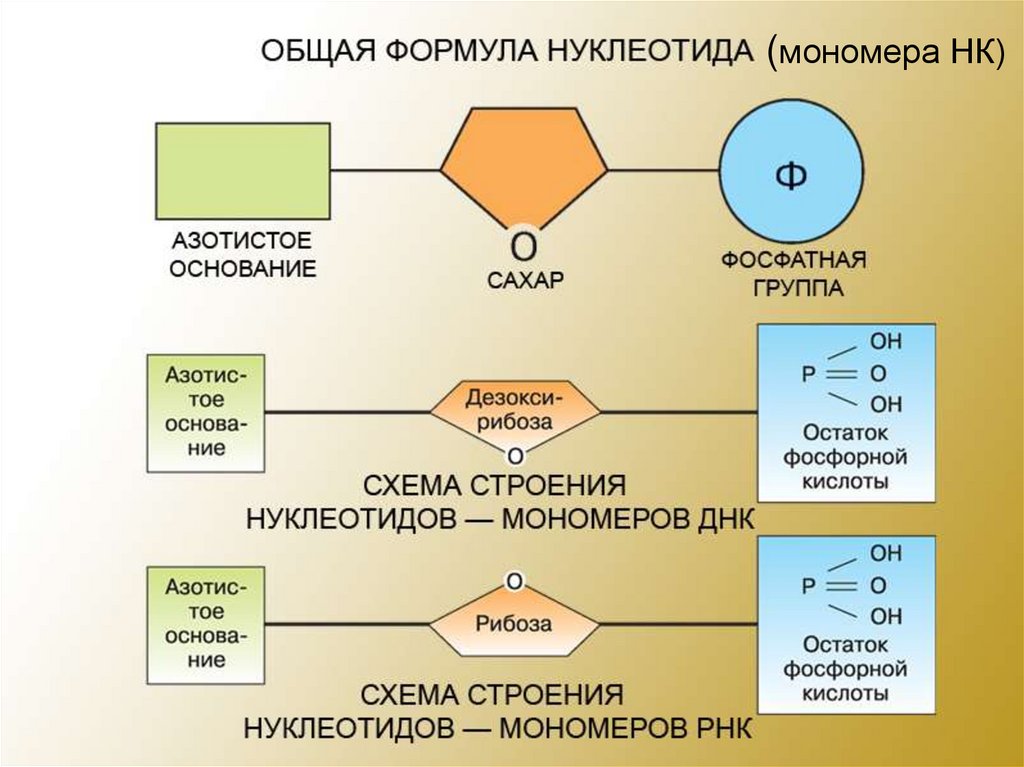
65.
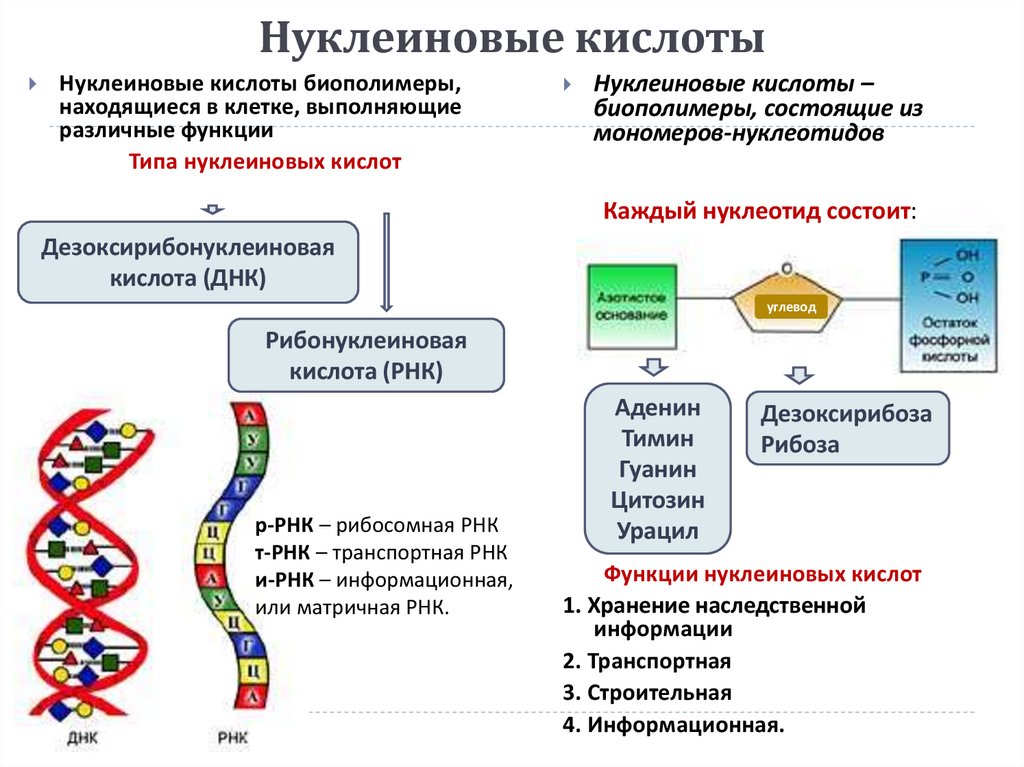
(мономера НК)66. Нуклеиновые кислоты
Нуклеиновые кислоты биополимеры,находящиеся в клетке, выполняющие
различные функции
Типа нуклеиновых кислот
Нуклеиновые кислоты –
биополимеры, состоящие из
мономеров-нуклеотидов
Каждый нуклеотид состоит:
Дезоксирибонуклеиновая
кислота (ДНК)
углевод
Рибонуклеиновая
кислота (РНК)
р-РНК – рибосомная РНК
т-РНК – транспортная РНК
и-РНК – информационная,
или матричная РНК.
Аденин
Тимин
Гуанин
Цитозин
Урацил
Дезоксирибоза
Рибоза
Функции нуклеиновых кислот
1. Хранение наследственной
информации
2. Транспортная
3. Строительная
4. Информационная.
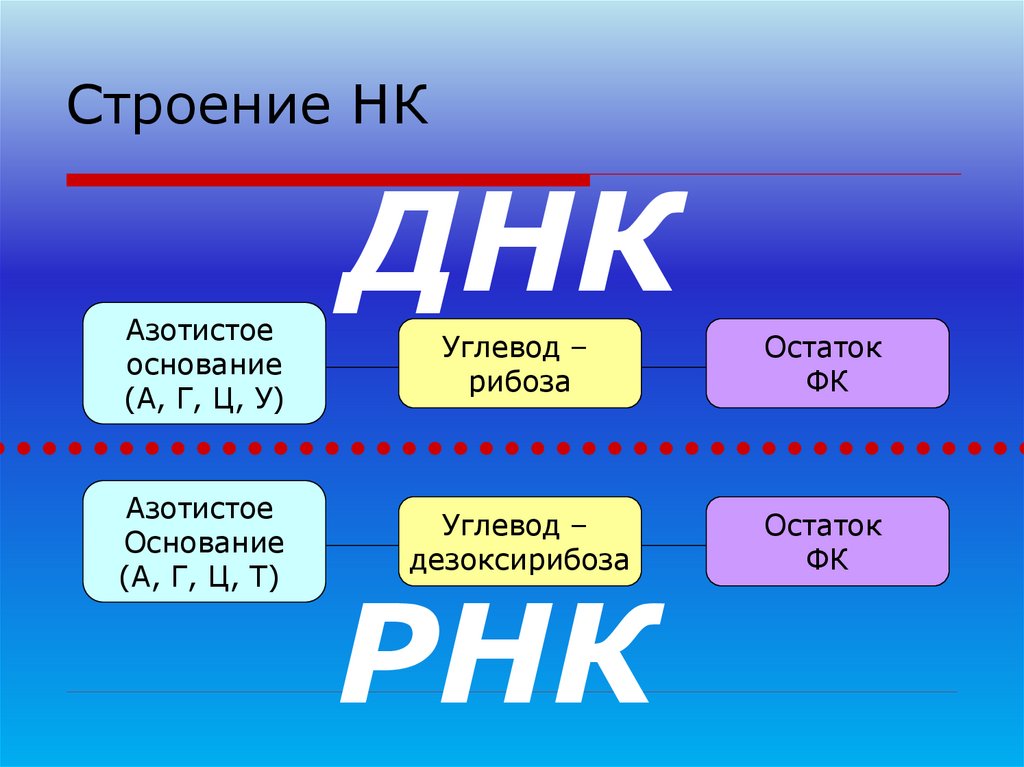
67. Строение НК
Азотистоеоснование
(А, Г, Ц, У)
Азотистое
Основание
(А, Г, Ц, Т)
ДНК
Углевод –
рибоза
Остаток
ФК
Углевод –
дезоксирибоза
Остаток
ФК
РНК
68.
Азотистые основанияДНК
РНК
Аденин
Гуанин
Цитозин
Тимин
Аденин
Гуанин
Цитозин
Урацил
69.
Нуклеиновые кислоты бывают двух типов:ДНК
РНК
Дезоксирибоза в
качестве углевода
Рибоза в качестве
углевода
Только тимин и нет
урацила
Урацил вместо тимина
Содержится в ядре
Очень крупная
(миллионы
нуклеотидов)
Содержится не только
в ядре, но и в
цитоплазме
По размерам редко
превышает пару
тысяч нуклеотидов
70. Виды РНК
В клетке имеется несколько видов РНК. Все они участвуютв синтезе белка.
Транспортные РНК (т-РНК) - это самые
маленькие по размерам РНК. Они связывают АК
и транспортируют их к месту синтеза белка.
Информационные РНК (и-РНК) - они в 10 раз
больше тРНК. Их функция состоит в переносе
информации о структуре белка от ДНК к месту
синтеза белка.
Рибосомные РНК (р-РНК) - имеют
наибольшие размеры молекулы, входят в
состав рибосом.
71.
72.
73. Комплиментарность
Комплиментарность пространственная взаимодополняемостьмолекул или их частей, приводящая к
образованию водородных связей.
Комплиментарные структуры подходят
друг к другу как «ключ с замком»
(А+Т)+(Г+Ц)=100%
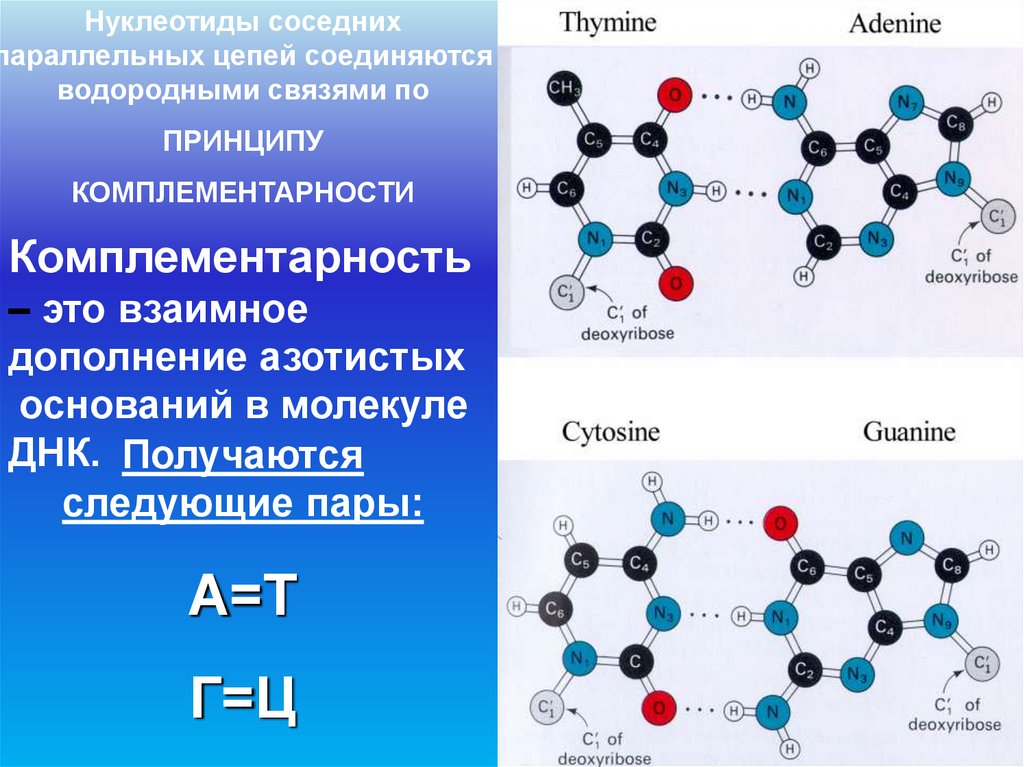
74.
Нуклеотиды соседнихпараллельных цепей соединяются
водородными связями по
ПРИНЦИПУ
КОМПЛЕМЕНТАРНОСТИ
Комплементарность
– это взаимное
дополнение азотистых
оснований в молекуле
ДНК. Получаются
следующие пары:
А=Т
Г=Ц
75.
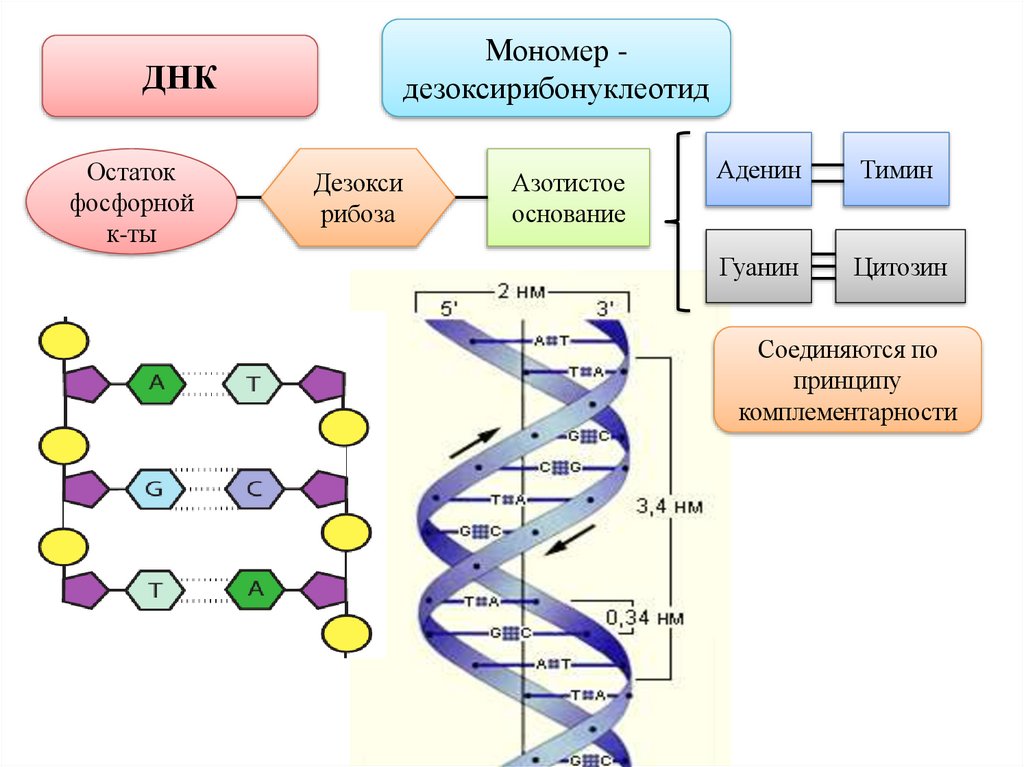
Мономер дезоксирибонуклеотидДНК
Остаток
фосфорной
к-ты
Дезокси
рибоза
Азотистое
основание
Аденин
Тимин
Гуанин
Цитозин
Соединяются по
принципу
комплементарности
76. Участок двуспиральной молекулы ДНК: на один виток приходится 10 пар нуклеотидов.
Участокдвуспиральн
ой молекулы
ДНК: на один
виток
приходится
10 пар
нуклеотидов
.
77.
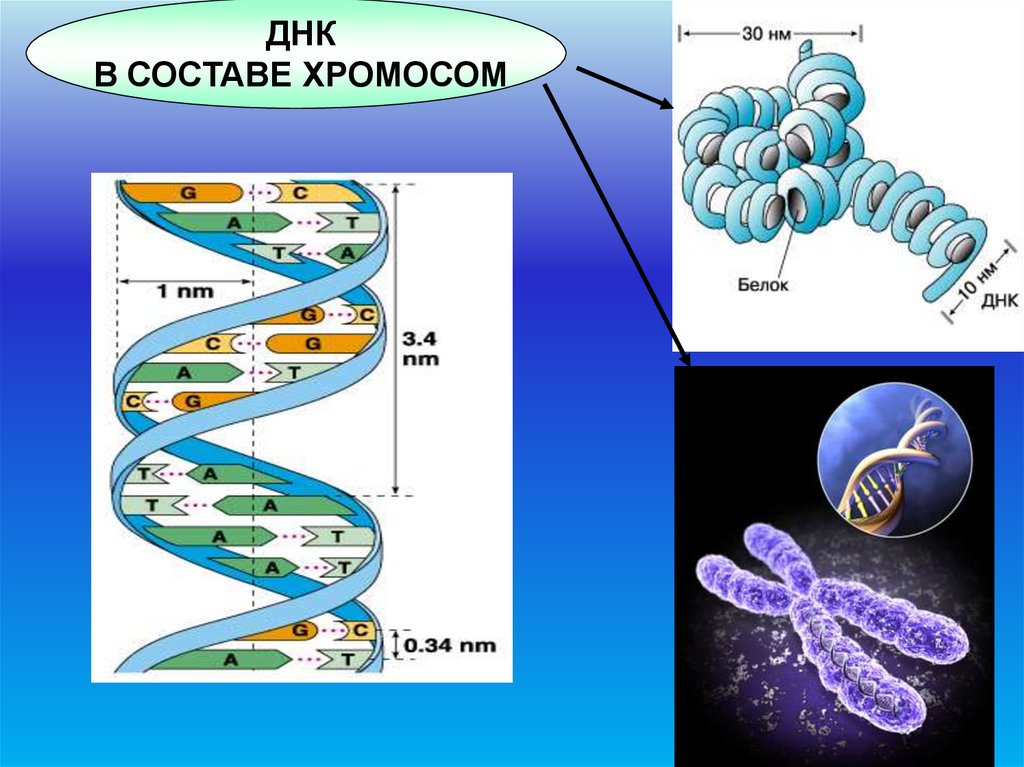
ДНКВ СОСТАВЕ ХРОМОСОМ
77
78.
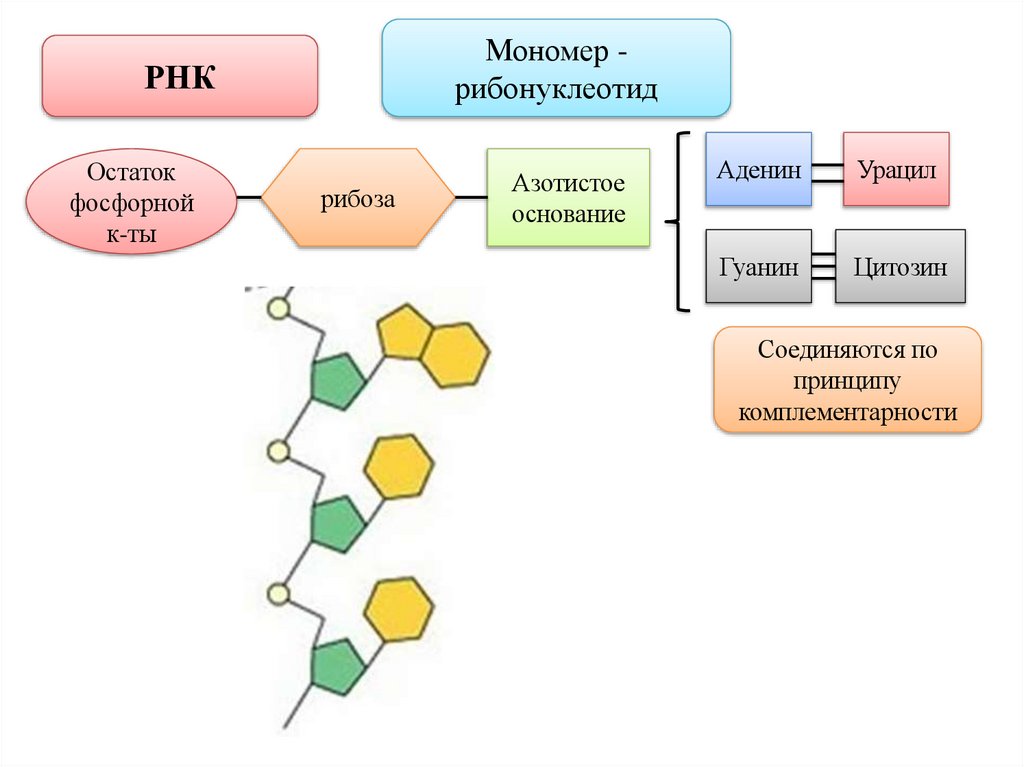
Мономер рибонуклеотидРНК
Остаток
фосфорной
к-ты
рибоза
Азотистое
основание
Аденин
Урацил
Гуанин
Цитозин
Соединяются по
принципу
комплементарности
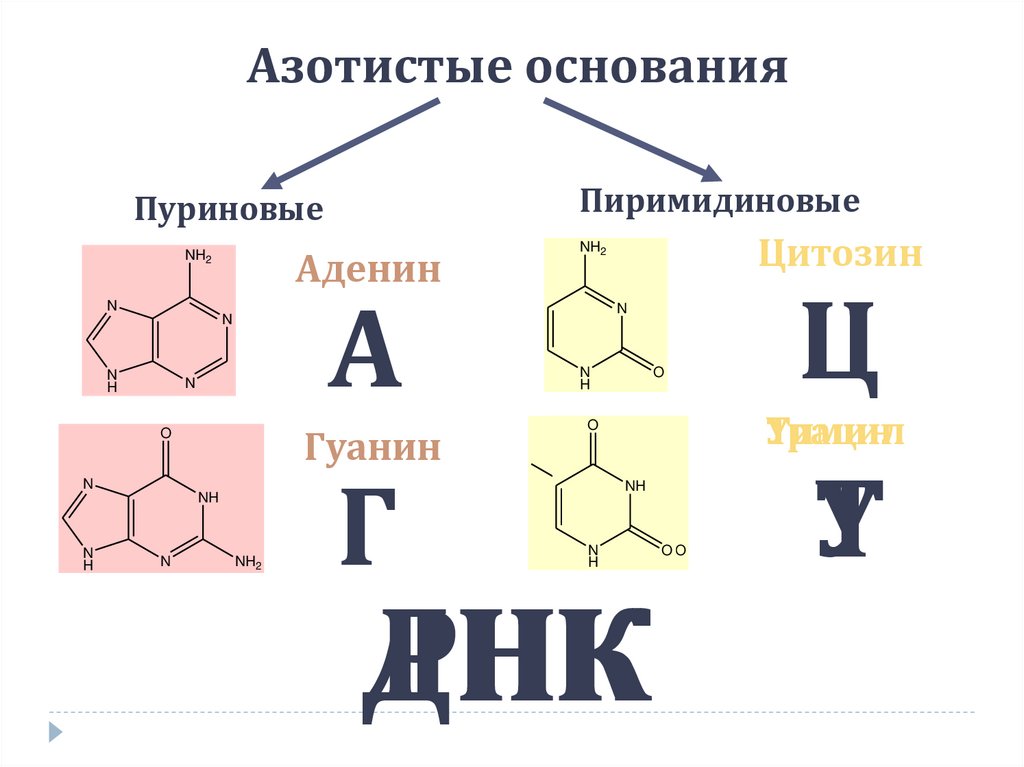
79.
Азотистые основанияПиримидиновые
Пуриновые
Аденин
NH2
N
А
N
N
H
N
Гуанин
O
N
N
H
NH
N
NH2
Г
Цитозин
NH2
N
N
H
O
Урацил
Тимин
OO
NH
NH
NN
HH
Ц
ДНК
РНК
OO
У
Т
80.
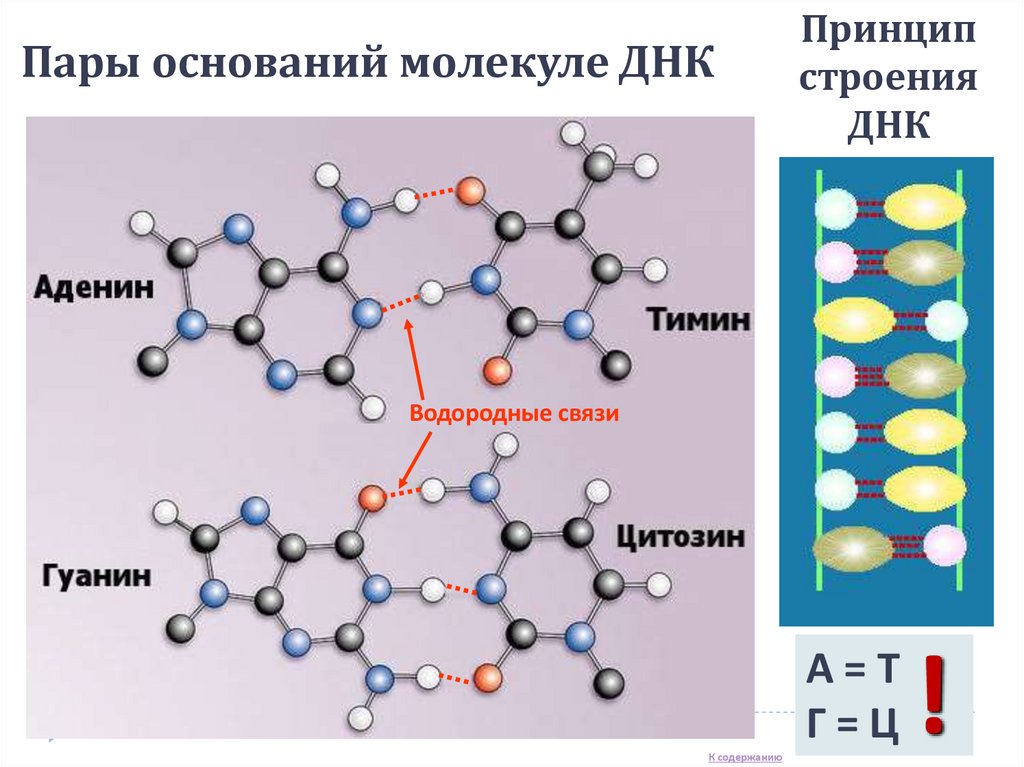
Пары оснований молекуле ДНКПринцип
строения
ДНК
Водородные связи
А=Т
Г=Ц
К содержанию
!
81.
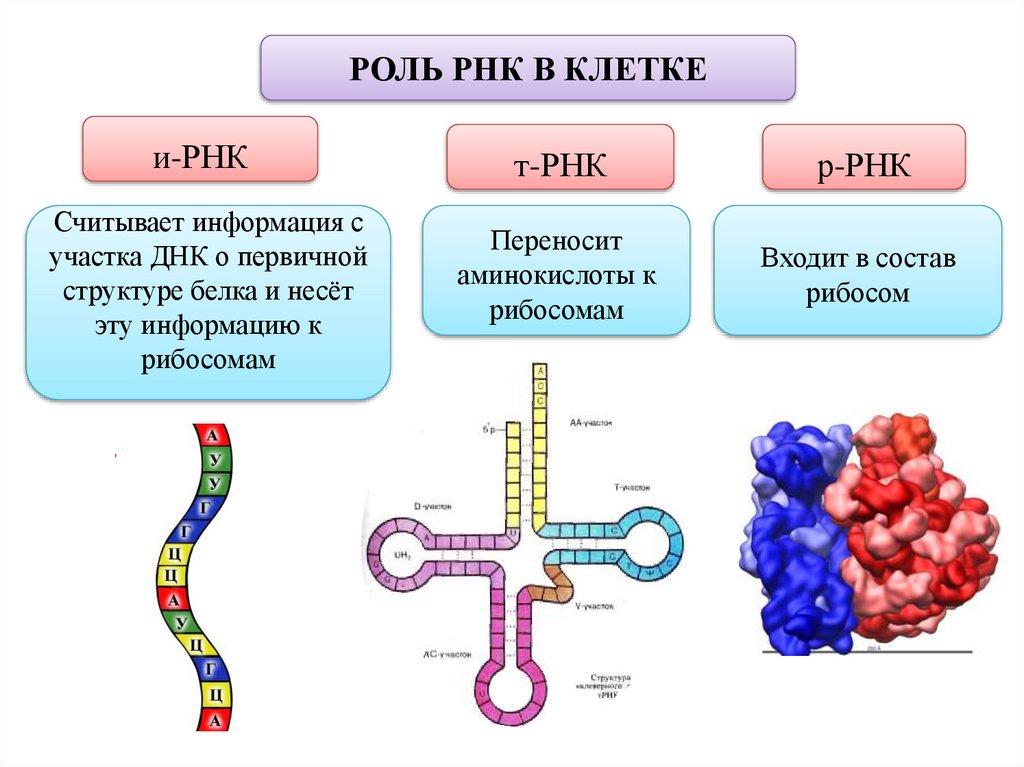
РОЛЬ РНК В КЛЕТКЕи-РНК
Считывает информация с
участка ДНК о первичной
структуре белка и несёт
эту информацию к
рибосомам
т-РНК
р-РНК
Переносит
аминокислоты к
рибосомам
Входит в состав
рибосом
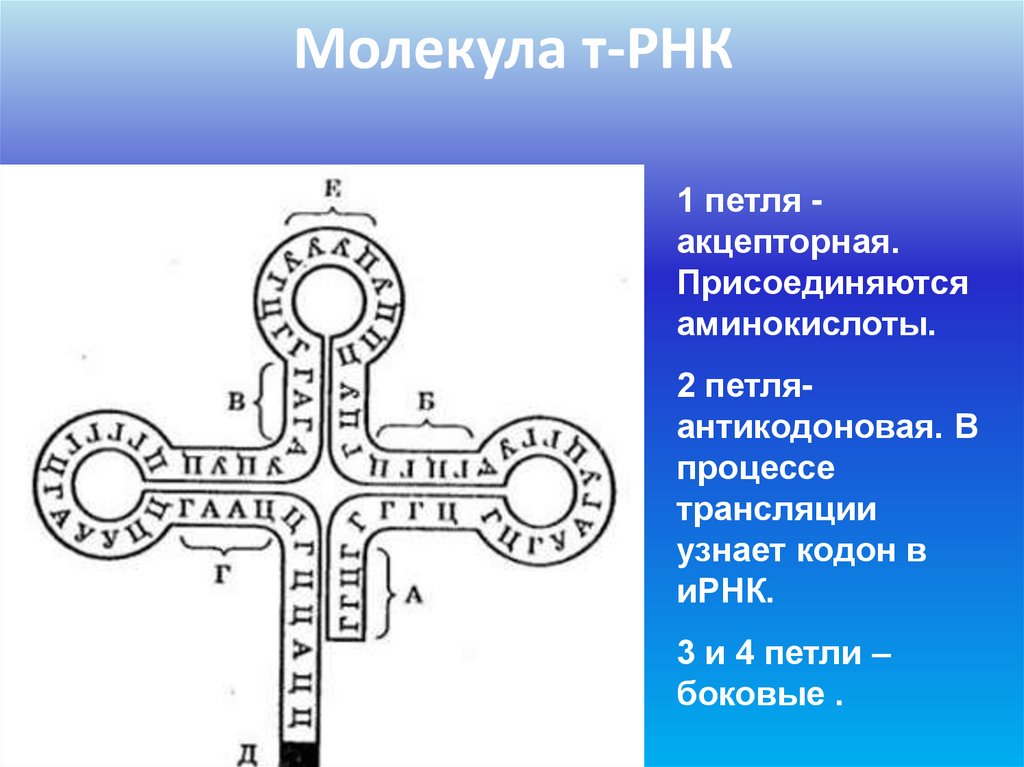
82. Молекула т-РНК
1 петля акцепторная.Присоединяются
аминокислоты.
2 петляантикодоновая. В
процессе
трансляции
узнает кодон в
иРНК.
3 и 4 петли –
боковые .
83.
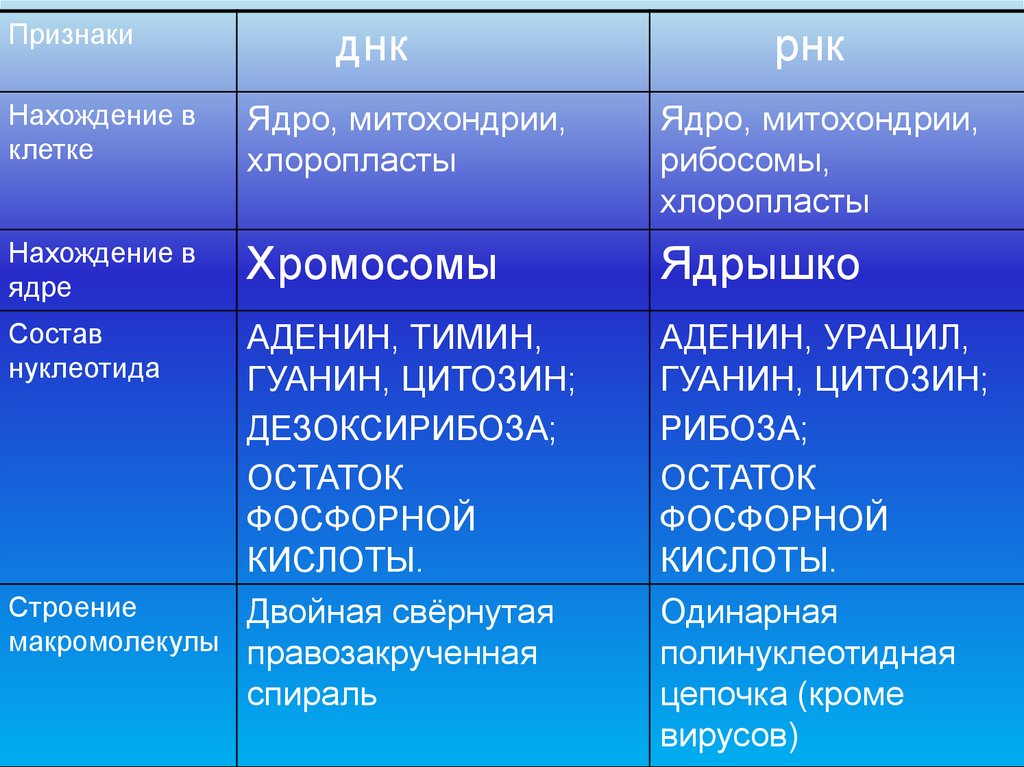
Признакиднк
рнк
Нахождение в
клетке
Ядро, митохондрии,
хлоропласты
Ядро, митохондрии,
рибосомы,
хлоропласты
Нахождение в
ядре
Хромосомы
Ядрышко
Состав
нуклеотида
АДЕНИН, ТИМИН,
ГУАНИН, ЦИТОЗИН;
ДЕЗОКСИРИБОЗА;
ОСТАТОК
ФОСФОРНОЙ
КИСЛОТЫ.
АДЕНИН, УРАЦИЛ,
ГУАНИН, ЦИТОЗИН;
РИБОЗА;
ОСТАТОК
ФОСФОРНОЙ
КИСЛОТЫ.
Строение
Двойная свёрнутая
макромолекулы правозакрученная
спираль
Одинарная
полинуклеотидная
цепочка (кроме
вирусов)
84.
СвойстваСпособна к
самоудвоению по
принципу
комплементарности:
А-Т; Т-А; Г-Ц; Ц-Г.
Стабильна.
Не способна к
самоудвоению.
Лабильна.
Функции
Химическая основа
гена. Хранение и
передача
наследственной
информации о
структуре белков.
иРНК(мРНК)определ
яет порядок
расположения
аминокислоты в
белке;
тРНК –подносит
аминокислоты к
месту синтеза белка
–рибосомам;
рРНК- определяет
структуру рибосом.
85.
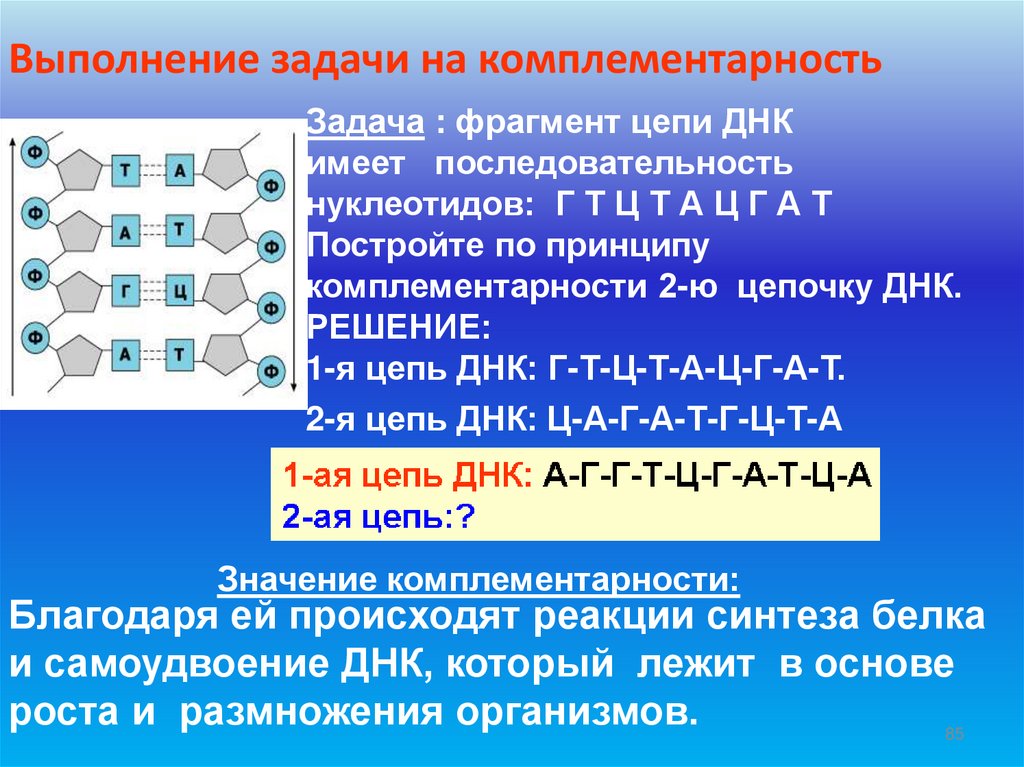
Выполнение задачи на комплементарностьЗадача : фрагмент цепи ДНК
имеет последовательность
нуклеотидов: Г Т Ц Т А Ц Г А Т
Постройте по принципу
комплементарности 2-ю цепочку ДНК.
РЕШЕНИЕ:
1-я цепь ДНК: Г-Т-Ц-Т-А-Ц-Г-А-Т.
2-я цепь ДНК: Ц-А-Г-А-Т-Г-Ц-Т-А
Значение комплементарности:
Благодаря ей происходят реакции синтеза белка
и самоудвоение ДНК, который лежит в основе
роста и размножения организмов.
85
86.
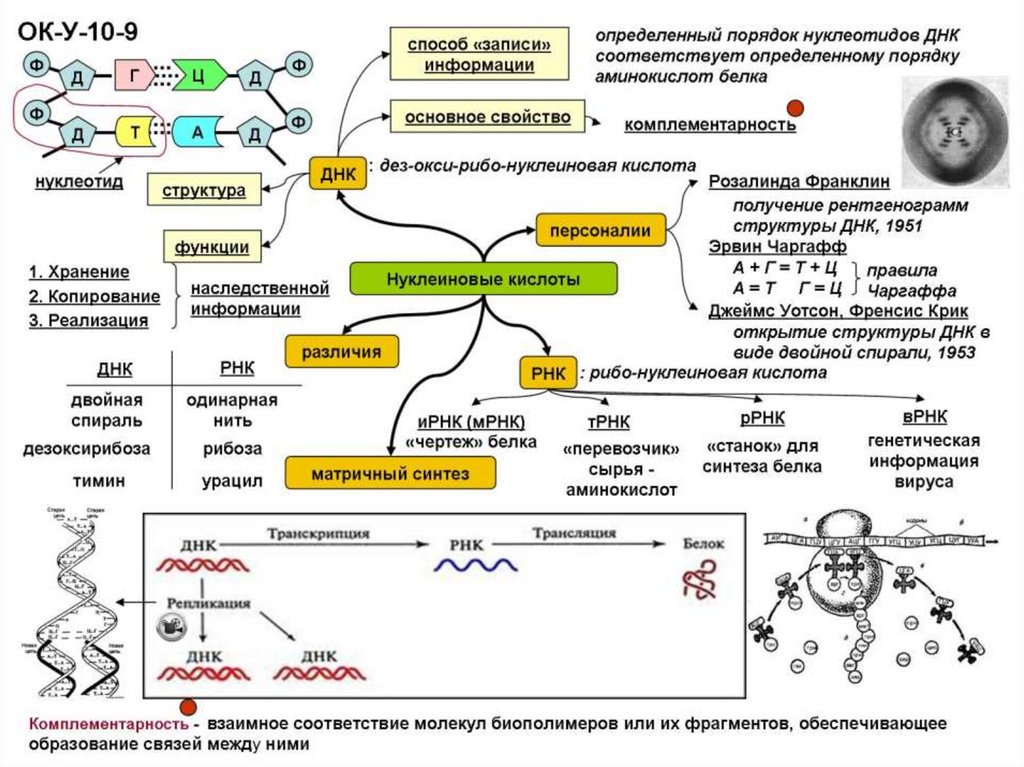
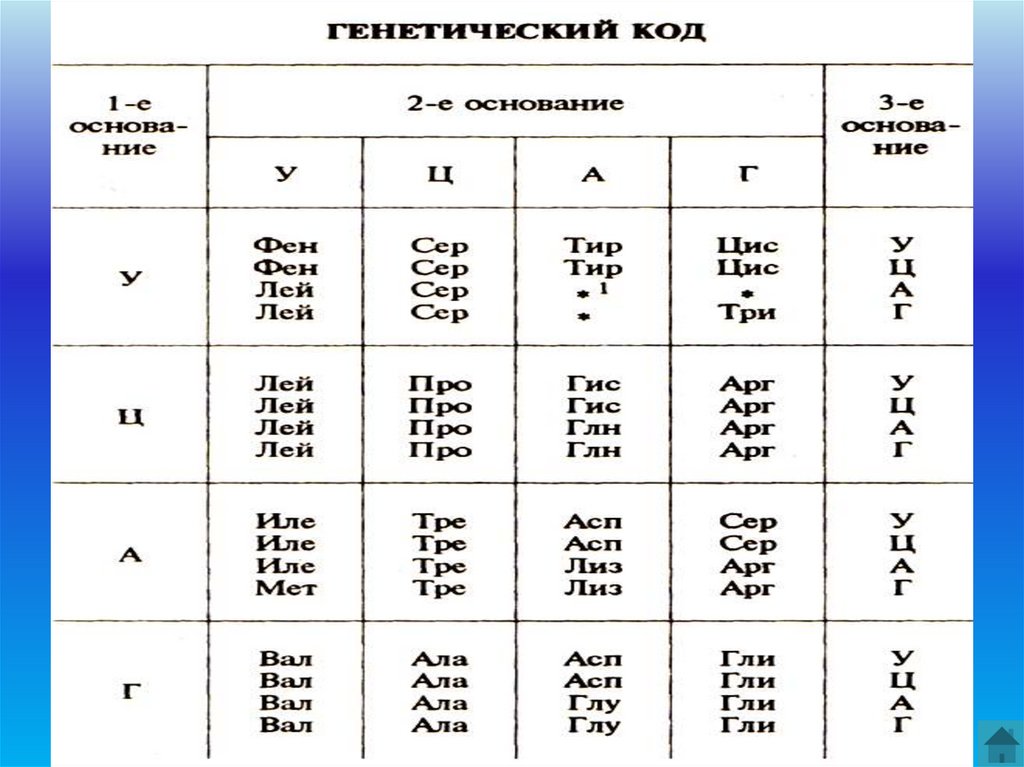
87. Генетический код
Наследственная информация записана вмолекулах НК в виде последовательности
нуклеотидов. Определенные участки
молекулы ДНК и РНК (у вирусов и фагов)
содержат информацию о первичной
структуре одного белка и называются
генами.
1 ген = 1 молекула белка
Поэтому наследственную информацию,
которую содержат ДНК называют
генетической.
88.
Одна аминокислотазакодирована тремя
нуклеотидами (один
кодон).
АЦТ
АГЦ
ГАТ
Триплет, кодон
ген
АК1
Пример: АК триптофан
закодирована в РНК
УГГ, в ДНК - АЦЦ.
АК2
белок
АК3
89.
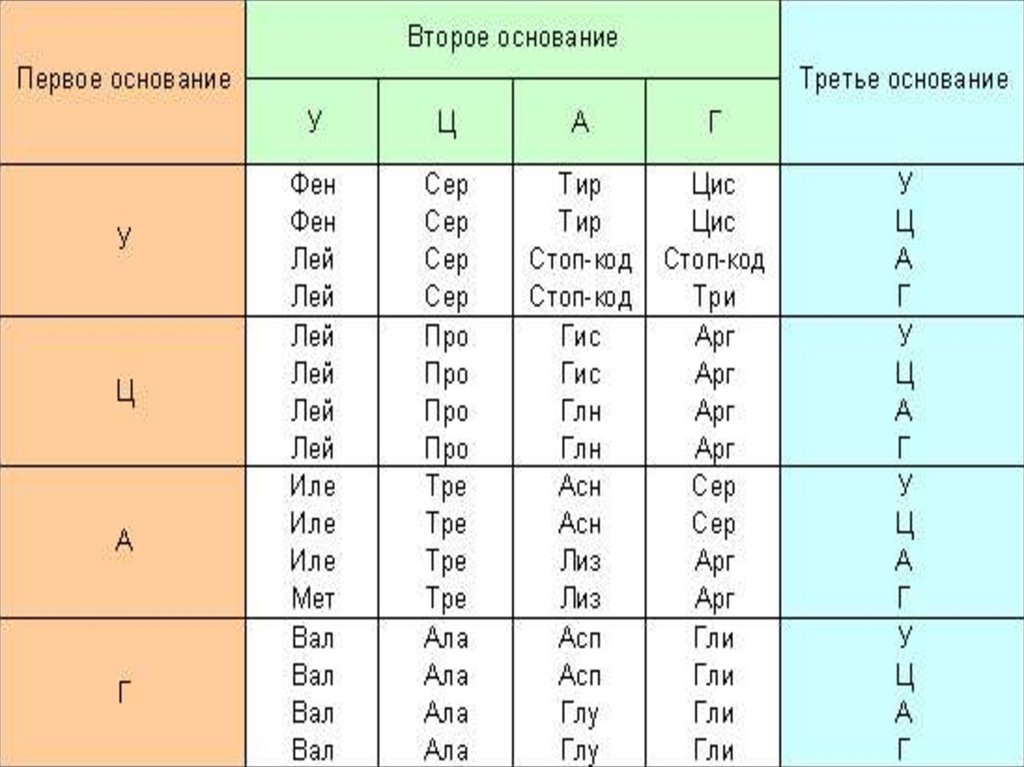
Имеется 64 кодона:А
Т
Ц
Г
43
61 кодон кодирует 20
(21) аминокислот, три
кодона являются
знаками препинания:
кодоны-терминаторы
УАА, УАГ, УГА (в РНК).
90. Свойства генетического кода:
УниверсальностьДискретность (кодовые
триплеты считываются с
молекулы РНК целиком)
Специфичность (кодон кодирует
только АК)
Избыточность кода (несколько)
91.
92.
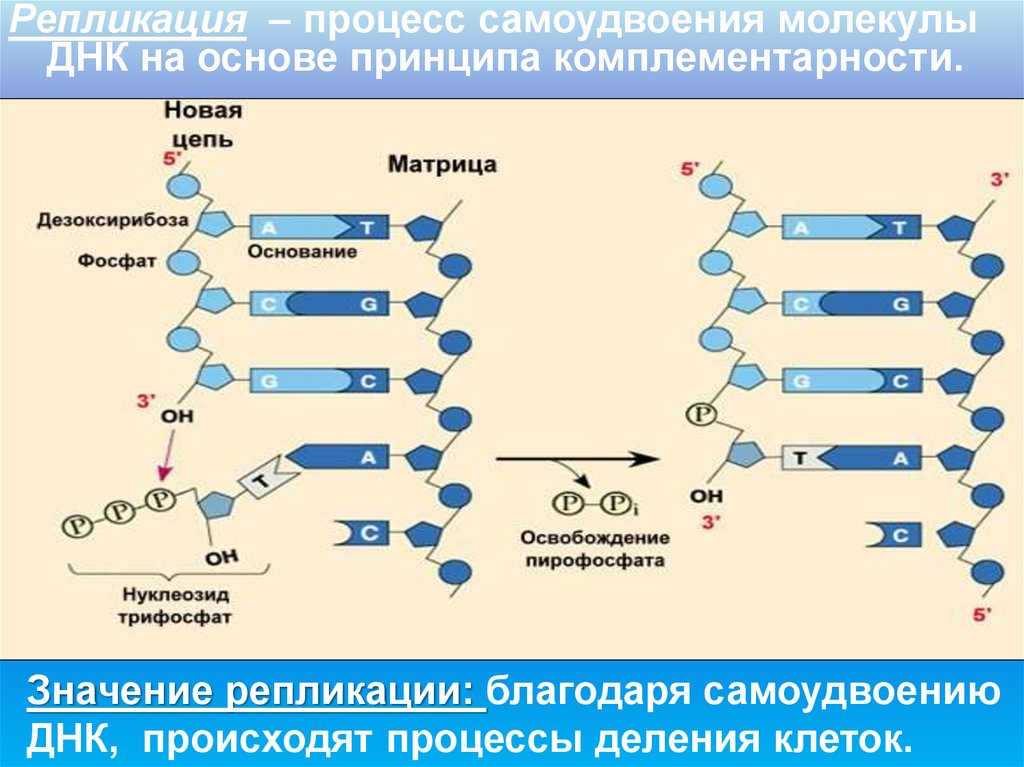
Репликация – процесс самоудвоения молекулыДНК на основе принципа комплементарности.
Значение репликации: благодаря самоудвоению
ДНК, происходят процессы деления клеток.
93.
В процессе репликации требуется,чтобы обеспечивалась
комплементарность нуклеотидов. Это
придуманный природой способ
избежать ошибок при синтезе двойной
спирали ДНК, а также РНК и белков.
Азотистые основания нуклеотидов
могут соединяться друг с другом
только в определённых сочетаниях
(аденин с тимином, гуанин – с
цитозином).
http://files.school-collection.edu.ru/dlrstore/08fc4dd0-78b8-8896-9a96ea9a76644104/00135958510902377.htm
94.
ЗадачаДано:
А-А-Г-Т-Ц-Т-А-Ц-Г-Т-А-Т
1.Нарисуйте схему структуры
двухцепочечной ДНК
2.Каким свойством ДНК вы
руководствовались?
3.Какова длина (в нм) этого фрагмента
ДНК? (Каждый нуклеотид занимает
0,34нм по длине цепи ДНК)
4.Сколько в % содержится нуклеотидов
(по отдельности) в этой ДНК?
95.
Молекула ДНК всегдадвухцепочечная, поэтому ее длина
равна длине одной цепи, а каждый
нуклеотид в ней занимает 0,34нм.
Следовательно, 12
нуклеотидов в цепи
12 * 0,34нм = 4,08нм
96.
Всего в 2 цепях 24нуклеотида, из них А=8, т.к.
А=Т, то Т=8
А=Т=8=8*100%/24=33,4%
(А и Т по 33,4%)
Г=4, т.к. Г=Ц, то Ц=4.
Г=Ц=4=4*100%/24=16,6%
(Г и Ц по 16,6%)
97.
В молекуле ДНК обнаружено 880гуаниновых нуклеотидов, которые
составляют 22% от общего
количества нуклеотидов этого
ДНК. Определите :
1)Сколько содержится других
нуклеотидов (по отдельности) в
этой молекуле ДНК?
2)Какова длина ДНК?
98.
На основе принципакомплементарности
(А+Т) +(Г+Ц)=100%
1)Определяем количество цитозина
Г=Ц=880, или 22%
2) На долю тимина и аденозина
приходится
100% - (22%+22%) = 56%
Т=Ц=56%/2=28%
99.
3) Найдем количество тимина и цитозина22% - 880 нуклеотидов
28% - ?
Т=А=(28%*880)/22%=1120 нуклеотидов
4) Всего нуклеотидов
2*880 + 2*1120 = 4000
5) Для определения длины ДНК узнаем,
сколько нуклеотидов содержится в 1
цепи:
4000/2=2000
6) Вычисляем длину 1 цепи ДНК
2000*0,34нм=680нм
Такова длина и всей молекулы ДНК.
100.
1.Дано: А=600=12,5%2.Дано: Ц= 300= 15%
Найти:
1)Количество нуклеотидов и
в%
2)Длину всего ДНК
101.
102.
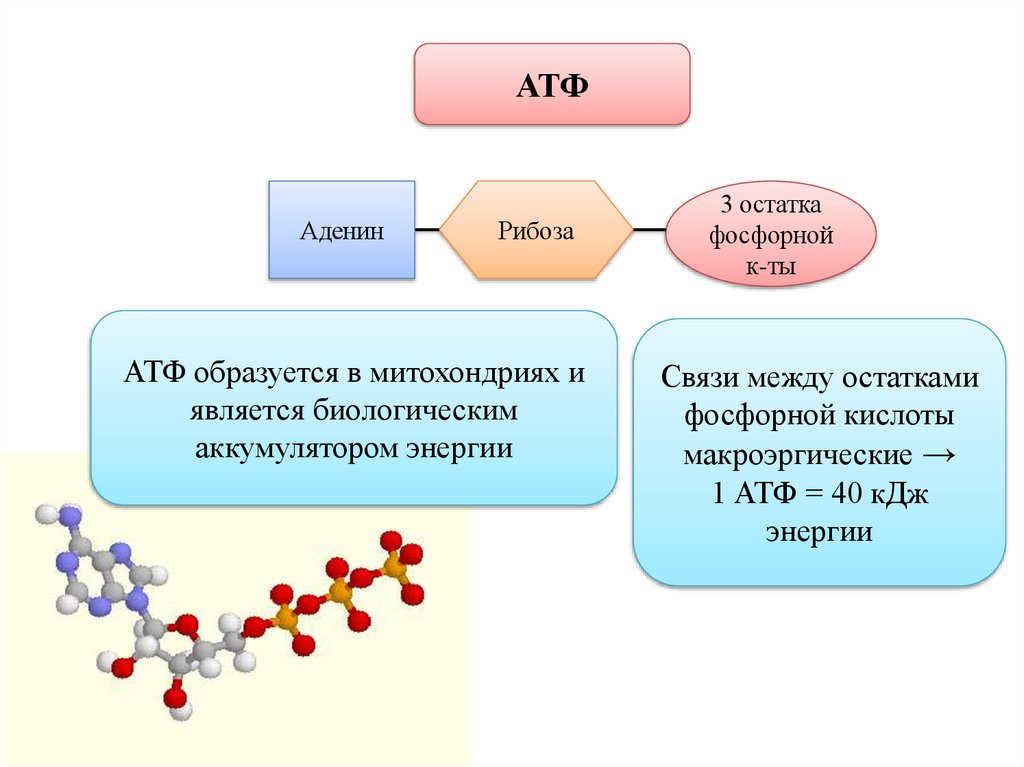
АТФАденин
Рибоза
АТФ образуется в митохондриях и
является биологическим
аккумулятором энергии
3 остатка
фосфорной
к-ты
Связи между остатками
фосфорной кислоты
макроэргические →
1 АТФ = 40 кДж
энергии
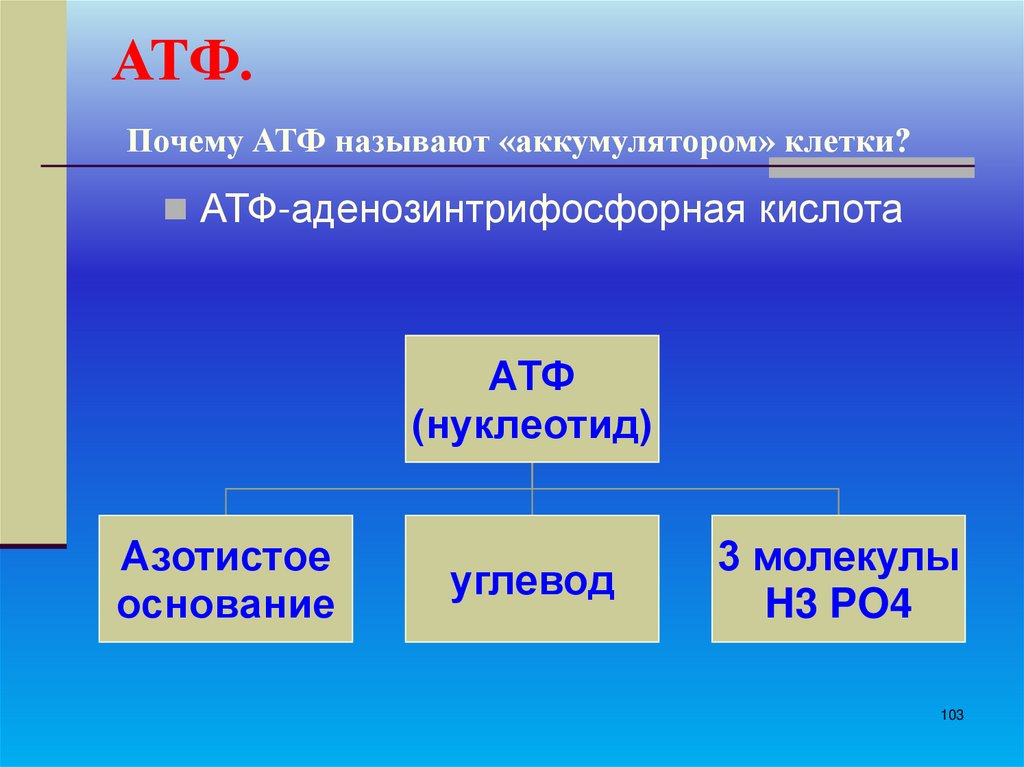
103. АТФ. Почему АТФ называют «аккумулятором» клетки?
АТФ-аденозинтрифосфорная кислотаАТФ
(нуклеотид)
Азотистое
основание
углевод
3 молекулы
H3 PO4
103
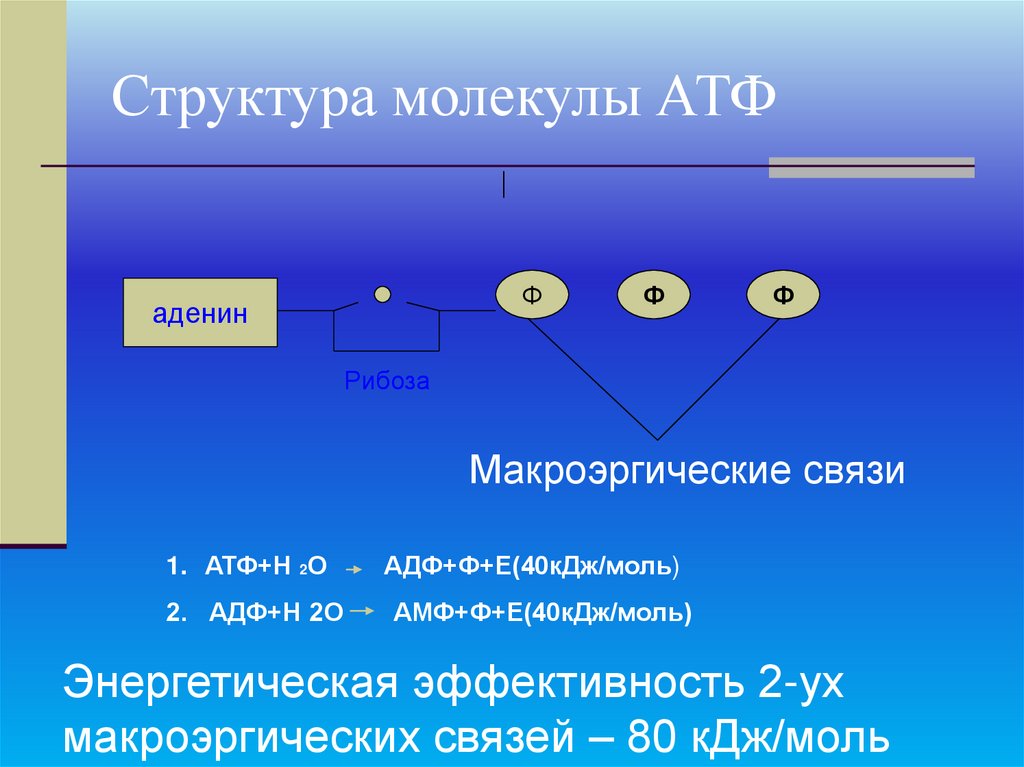
104. Структура молекулы АТФ
Фаденин
Ф
Ф
Рибоза
Макроэргические связи
1. АТФ+Н 2О
АДФ+Ф+Е(40кДж/моль)
2. АДФ+Н 2О
АМФ+Ф+Е(40кДж/моль)
Энергетическая эффективность 2-ух
макроэргических связей – 80 кДж/моль
105.
• АТФ Образуется в митохондрияхклеток животных и хлоропластах
растений.
• Энергия АТФ используется на
движение, биосинтез, деление и т.д.
• Средняя продолжительность
жизни 1 молекулы АТФ менее 1мин,
т.к. она расщепляется и
восстанавливается 2400раз в сутки.
106. АТФ и другие органические соединения
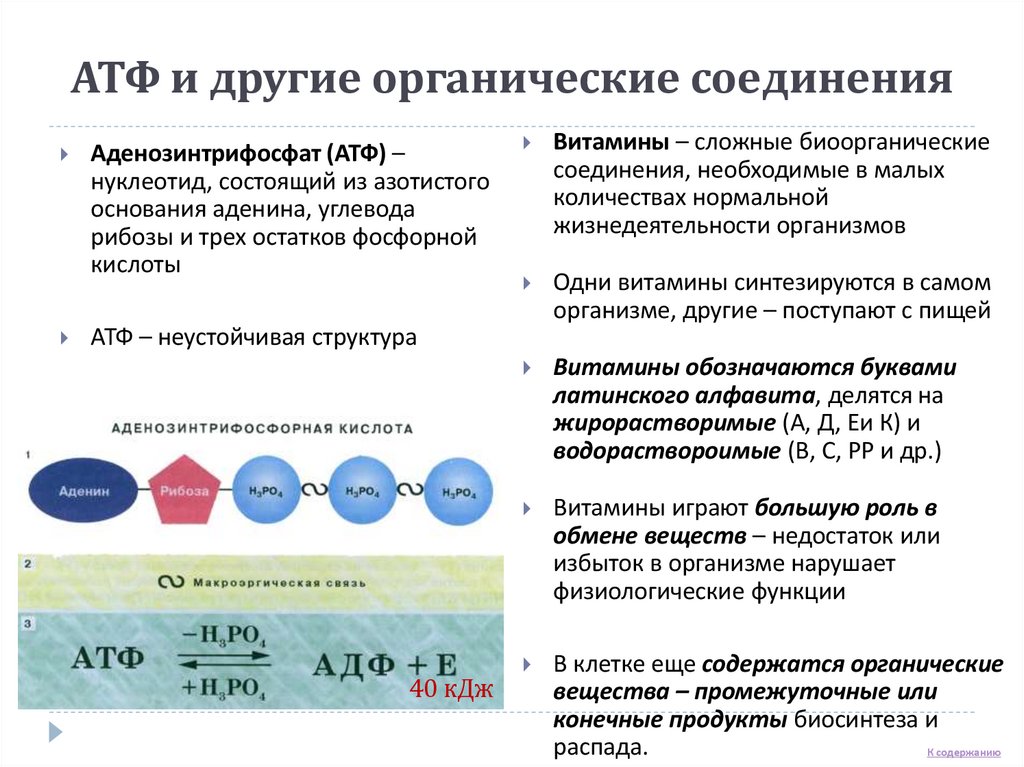
Аденозинтрифосфат (АТФ) –нуклеотид, состоящий из азотистого
основания аденина, углевода
рибозы и трех остатков фосфорной
кислоты
Витамины – сложные биоорганические
соединения, необходимые в малых
количествах нормальной
жизнедеятельности организмов
Одни витамины синтезируются в самом
организме, другие – поступают с пищей
Витамины обозначаются буквами
латинского алфавита, делятся на
жирорастворимые (А, Д, Еи К) и
водораствороимые (В, С, РР и др.)
Витамины играют большую роль в
обмене веществ – недостаток или
избыток в организме нарушает
физиологические функции
В клетке еще содержатся органические
вещества – промежуточные или
конечные продукты биосинтеза и
распада.
К содержанию
АТФ – неустойчивая структура
40 кДж
107. Вирусы
Вирусы – неклеточные организмы,простейшая форма жизни на нашей
планете, занимающая промежуточное
положение между неживой и живой
материей
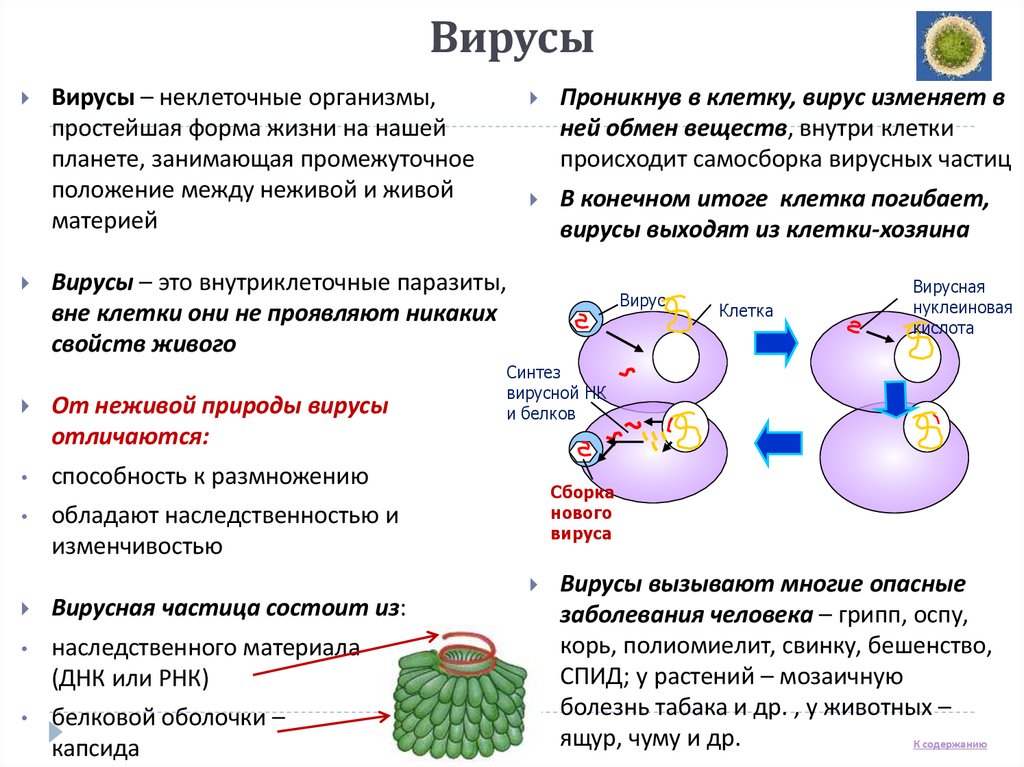
Проникнув в клетку, вирус изменяет в
ней обмен веществ, внутри клетки
происходит самосборка вирусных частиц
В конечном итоге клетка погибает,
вирусы выходят из клетки-хозяина
Вирусы – это внутриклеточные паразиты,
вне клетки они не проявляют никаких
свойств живого
От неживой природы вирусы
отличаются:
способность к размножению
обладают наследственностью и
изменчивостью
Вирус
Синтез
вирусной НК
и белков
Сборка
нового
вируса
Вирусная частица состоит из:
наследственного материала
(ДНК или РНК)
белковой оболочки –
капсида
Клетка
Вирусная
нуклеиновая
кислота
Вирусы вызывают многие опасные
заболевания человека – грипп, оспу,
корь, полиомиелит, свинку, бешенство,
СПИД; у растений – мозаичную
болезнь табака и др. , у животных –
ящур, чуму и др.
К содержанию





































 biology
biology








