Similar presentations:
22. Азот, соединения азота
1.
Азот,соединения азота
2.
Д. РезерфордК. Шееле
В 1772 г.
в экспериментах
по сжиганию веществ
обнаружили газ,
не поддерживающий
дыхание и горение.
А. Лавуазье
В 1787 г. установил
наличие в воздухе газа,
не поддерживающего
дыхания и горения.
Он дал название
этому газу «азот»,
означающее
«безжизненный».
В 1790 г. дал азоту
другое название –
нитрогениум –
«рождающий селитру».
Ж. Шапталь
3.
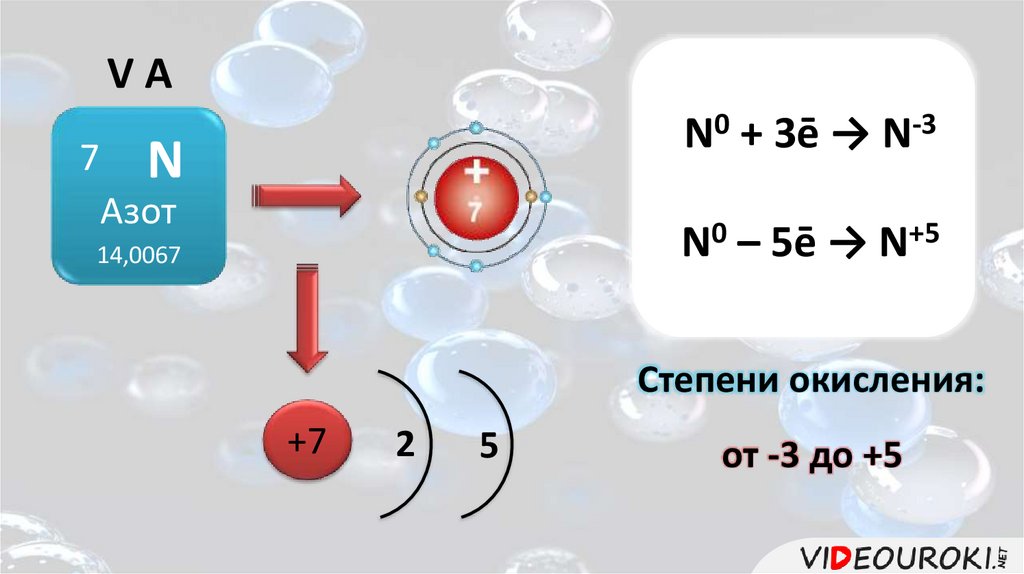
VA7
N0 + 3ē → N-3
N
Азот
N0 – 5ē → N+5
14,0067
Степени окисления:
+7
2
5
от -3 до +5
4.
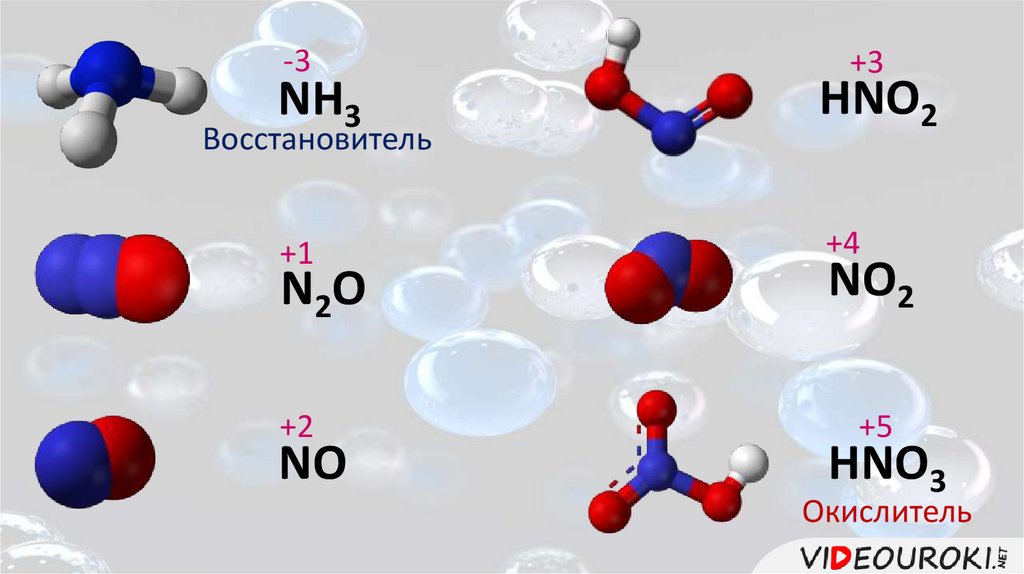
-3+3
NH3
HNO2
+1
+4
Восстановитель
N2O
+2
NO
NO2
+5
HNO3
Окислитель
5.
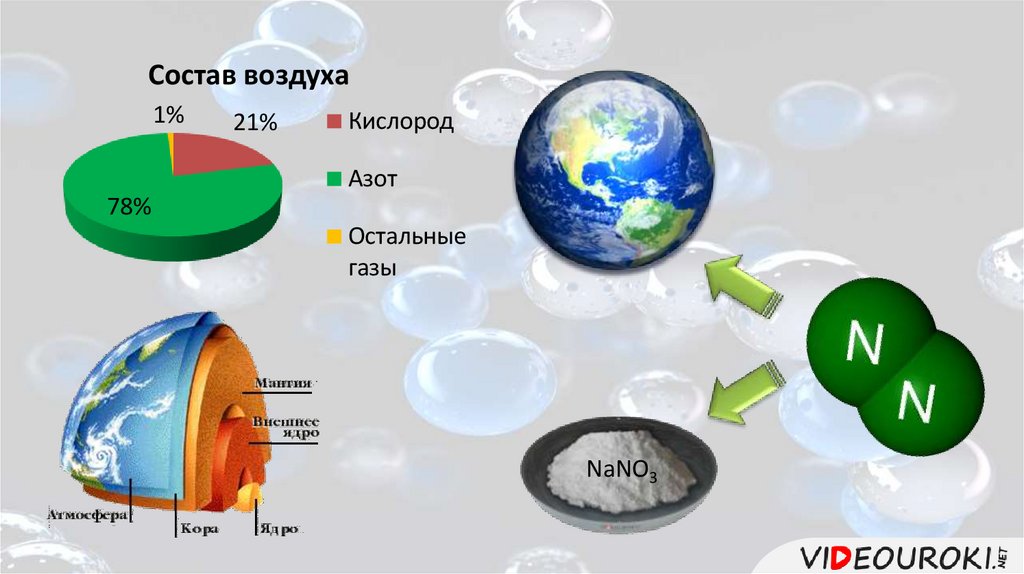
Состав воздуха1%
21%
Кислород
Азот
78%
Остальные
газы
NaNO3
6.
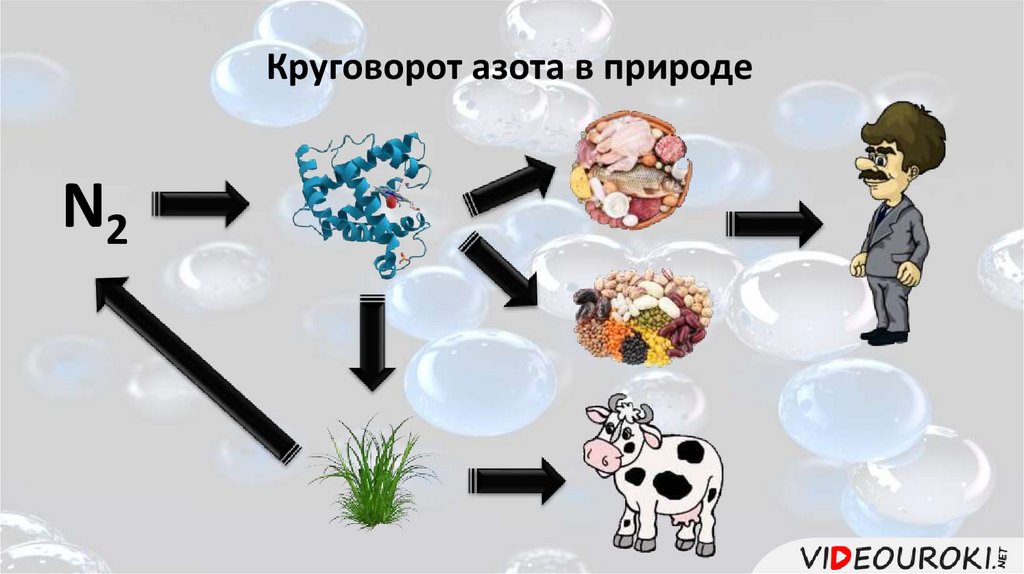
Круговорот азота в природеN2
7.
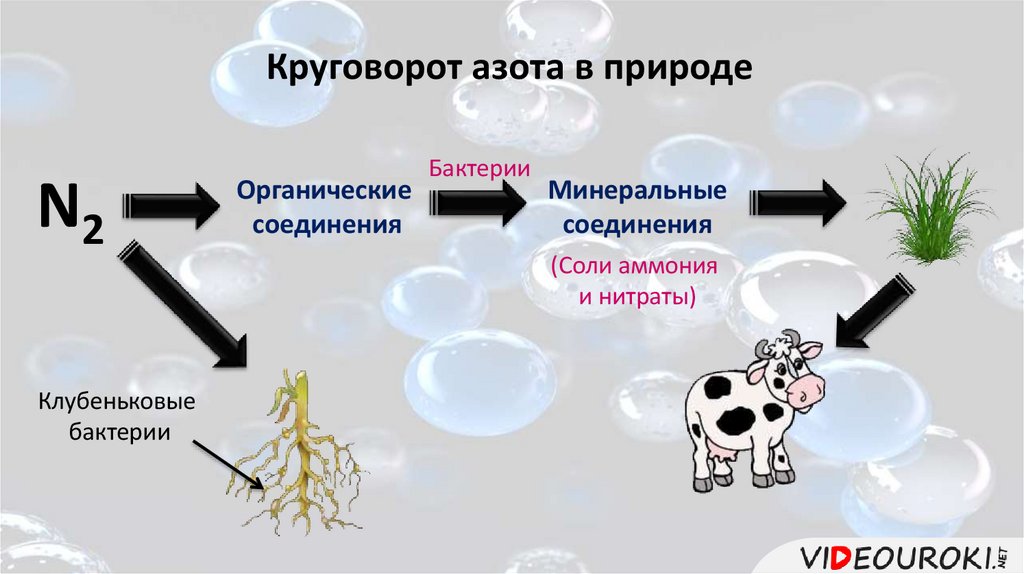
Круговорот азота в природеN2
Клубеньковые
бактерии
Органические
соединения
Бактерии
Минеральные
соединения
(Соли аммония
и нитраты)
8.
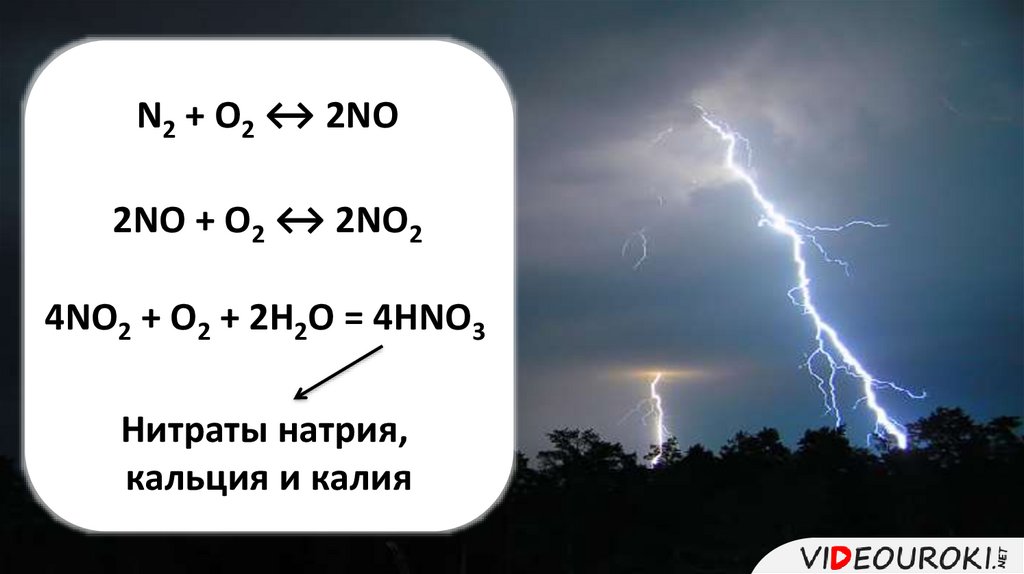
N2 + O2 ↔ 2NO2NO + O2 ↔ 2NO2
4NO2 + O2 + 2H2O = 4HNO3
Нитраты натрия,
кальция и калия
9.
N2●
●
N N N N
●
●
●
―
―
―
Азот – малоактивное
вещество.
Азот является бесцветным газом, не имеет запаха и вкуса.
Не сжижается при обычной температуре.
Азот плохо растворим в воде.
Температура плавления азота -210 0С, а температура кипения
-196 0С.
10.
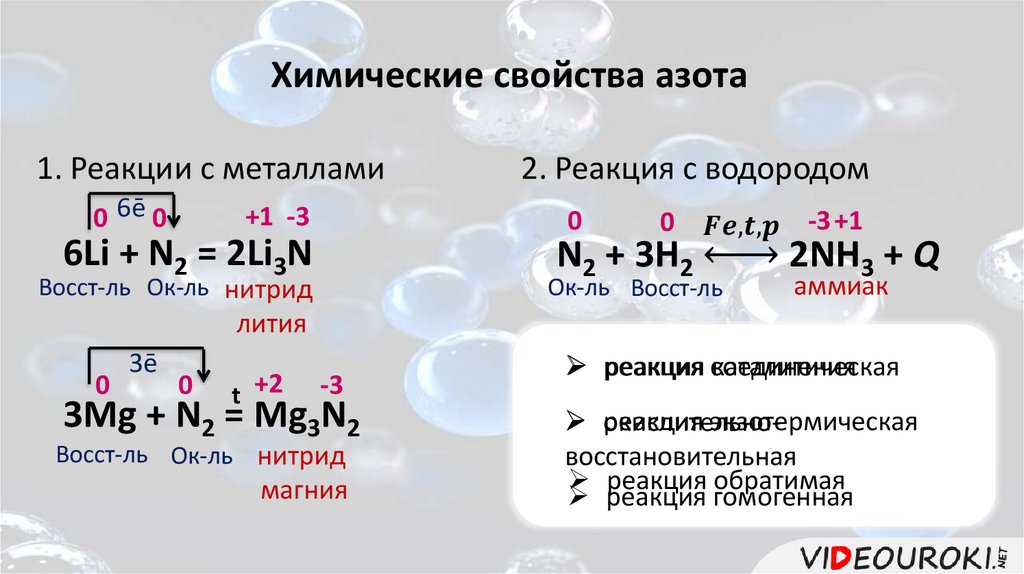
Химические свойства азота1. Реакции с металлами
0 6ē 0
+1 -3
2. Реакция с водородом
0
6Li + N2 = 2Li3N
0






 chemistry
chemistry








