Similar presentations:
Урок 36.Кислород (испр)
1.
В чем горят дрова и газ,Фосфор, водород, алмаз?
Дышит чем любой из нас
Каждый миг, и каждый час?
Без чего мертва природа?
Правильно, без
2.
« Кислород - это вещество, вокругкоторого вращается земная химия»
Й.Я. Берцелиус
3. Тема урока: Воздух и его состав. Кислород
20.12.20253
4. ЦЕЛЬ УРОКА:
расширить знания о кислороде,как химическом элементе и
простом веществе
https://resh.edu.ru/subject/lesson/2447/main/
20.12.2025
4
5.
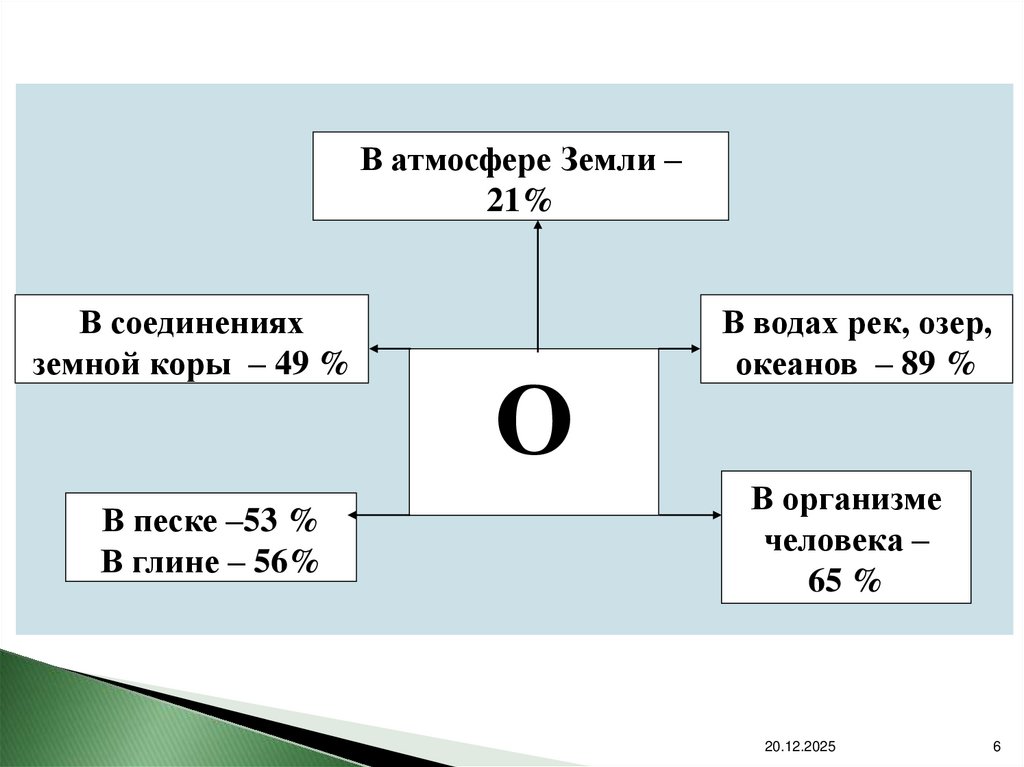
Кислород в природе20.12.2025
5
6.
В атмосфере Земли –21%
В соединениях
земной коры – 49 %
В песке –53 %
В глине – 56%
О
В водах рек, озер,
океанов – 89 %
В организме
человека –
65 %
20.12.2025
6
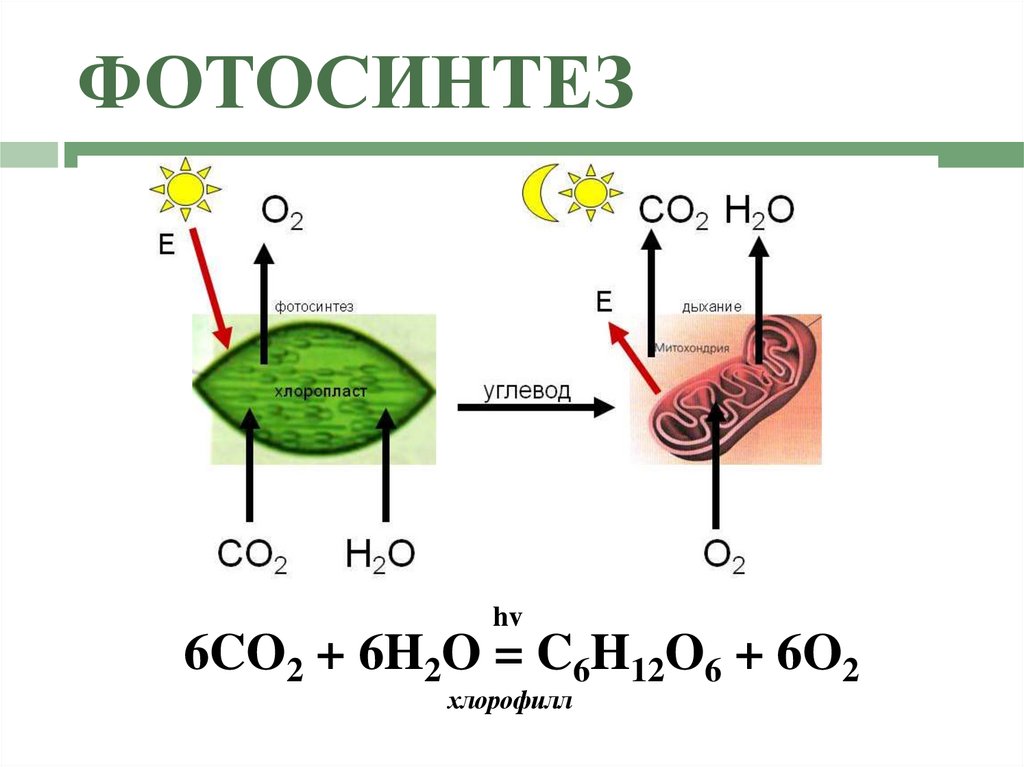
7. ФОТОСИНТЕЗ
hv6CO2 + 6H2O = C6H12O6 + 6O2
хлорофилл
8.
СОСТАВ ВОЗДУХАЛаборатория Лавуазье
9.
СОСТАВ ВОЗДУХА20.12.2025
9
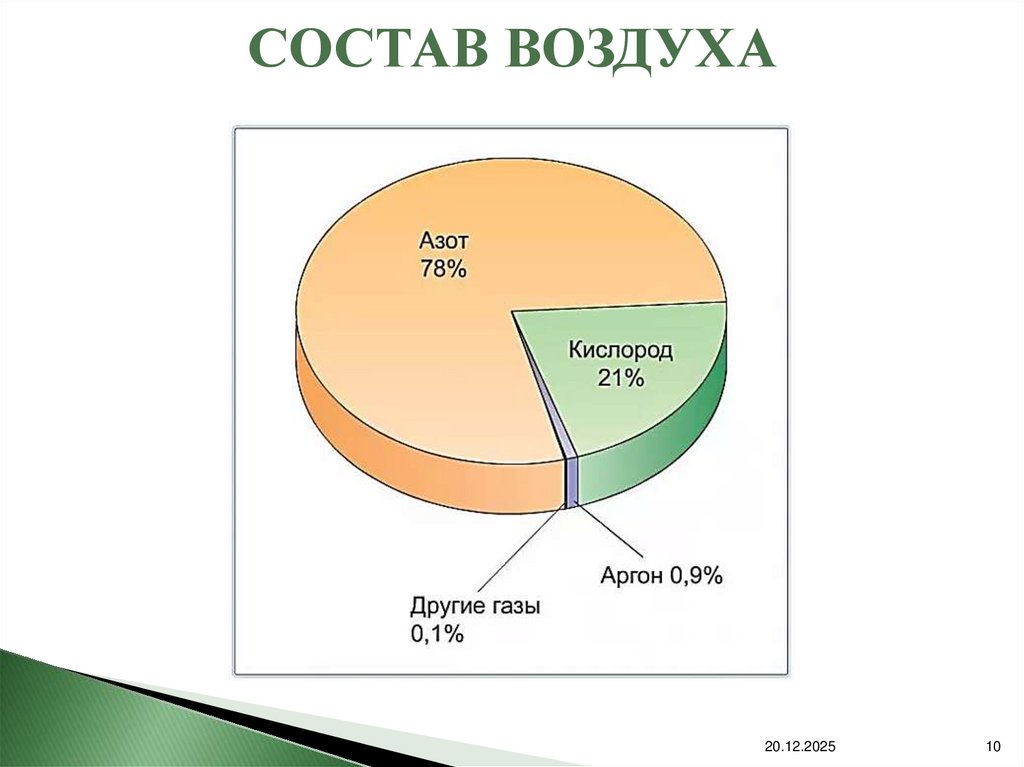
10.
СОСТАВ ВОЗДУХА20.12.2025
10
11.
ОБЪЕМНОЙ ДОЛЕЙ КОМПОНЕНТА ГАЗОВОЙ СМЕСИназывают отношение объема данного газа к общему объему
смеси:
20.12.2025
11
12.
Кислород как химический элементПлан характеристика химического элемента:
1)Символ
2)Порядковый номер
3)Положение в ПСХЭ
4)Химическая природа
5)Относительная атомная масса
6)Валентность
20.12.2025
12
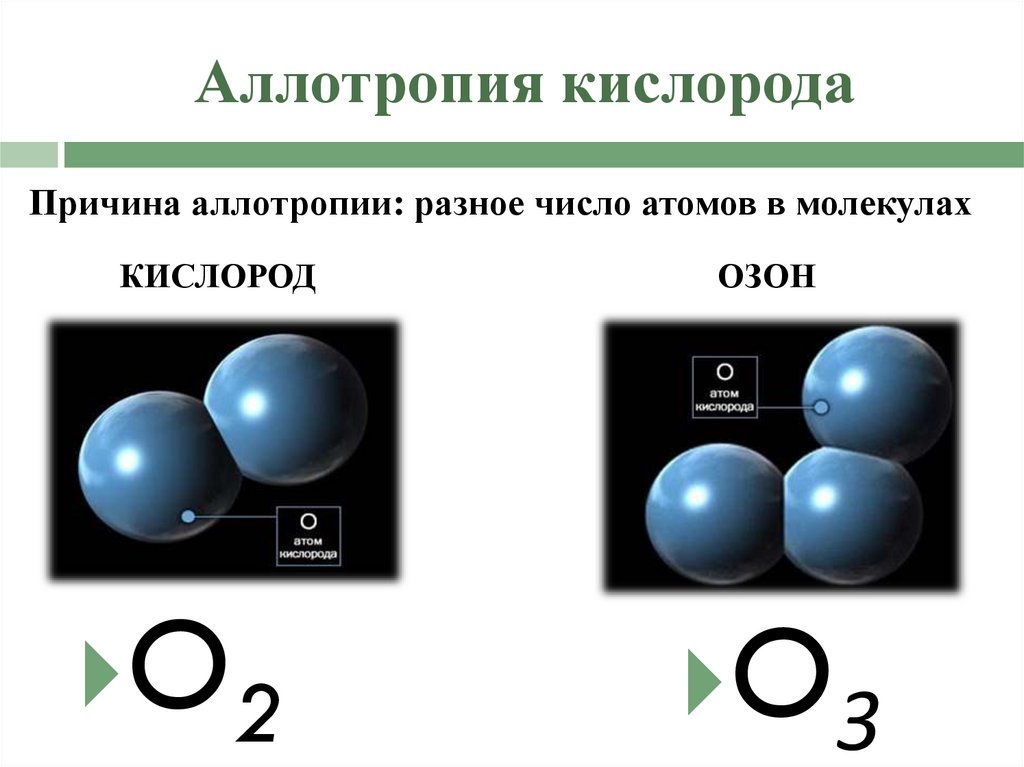
13. Аллотропия кислорода
Причина аллотропии: разное число атомов в молекулахКИСЛОРОД
O2
ОЗОН
O3
14.
Кислород как простое веществоМолекулярная формула
O2
Структурная формула
20.12.2025
14
15.
O2Физические свойства кислорода
Газ - без цвета, вкуса и запаха;
в 100V H2O растворяется 3V O2 (н.у.)
t кип= -183 С
t пл = -219 C
ρ = 1, 429 г/л (при 0 оС и 1 атм)
D по воздуху = 1,1
20.12.2025
15
16. Получение кислорода
В промышленности:1)перегонка жидкого воздуха
2)электролиз воды
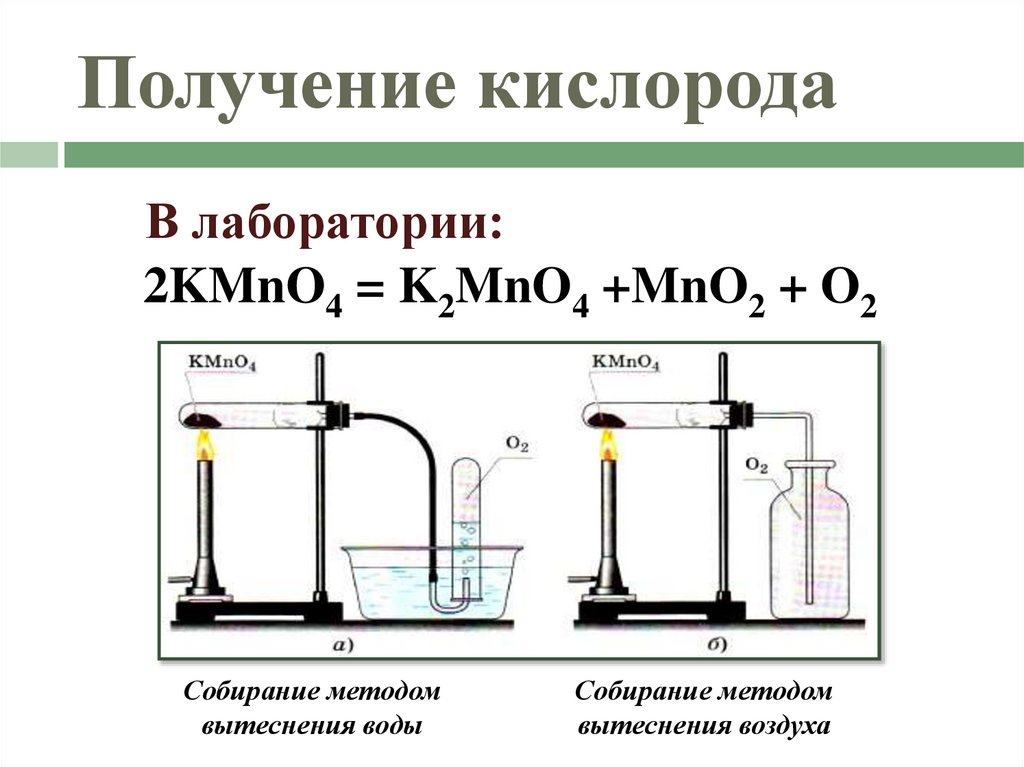
17. Получение кислорода
В лаборатории:2KMnO4 = K2MnO4 +MnO2 + O2
Собирание методом
вытеснения воды
Собирание методом
вытеснения воздуха
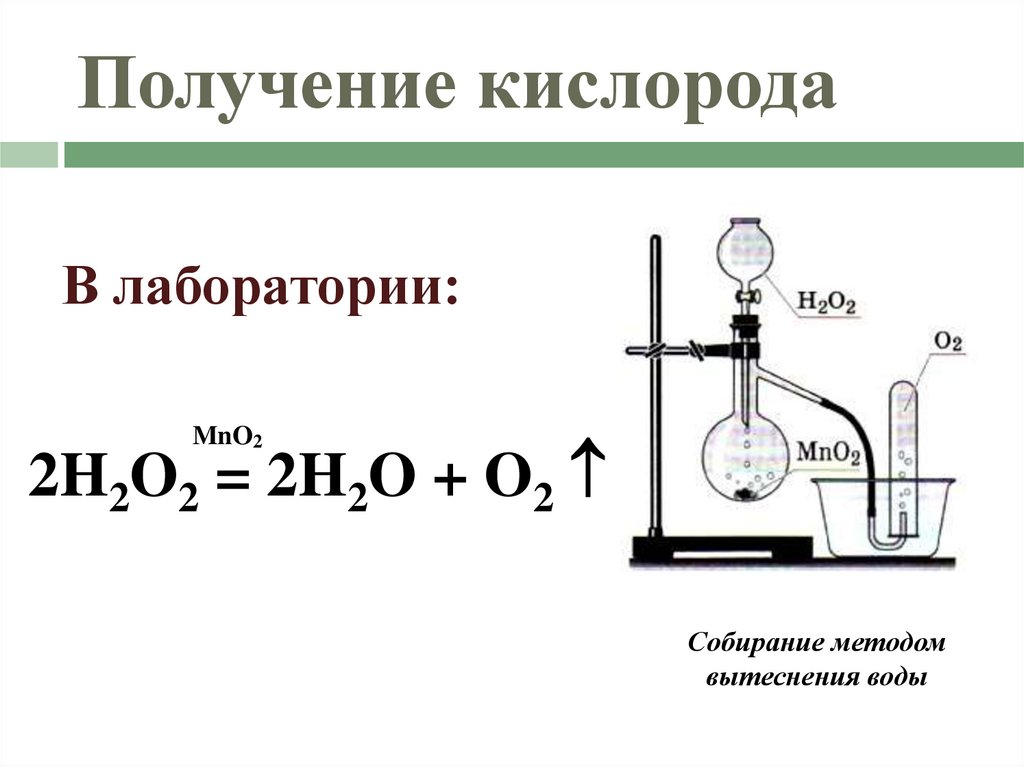
18. Получение кислорода
В лаборатории:MnO2
2H2O2 = 2H2O + O2
Собирание методом
вытеснения воды
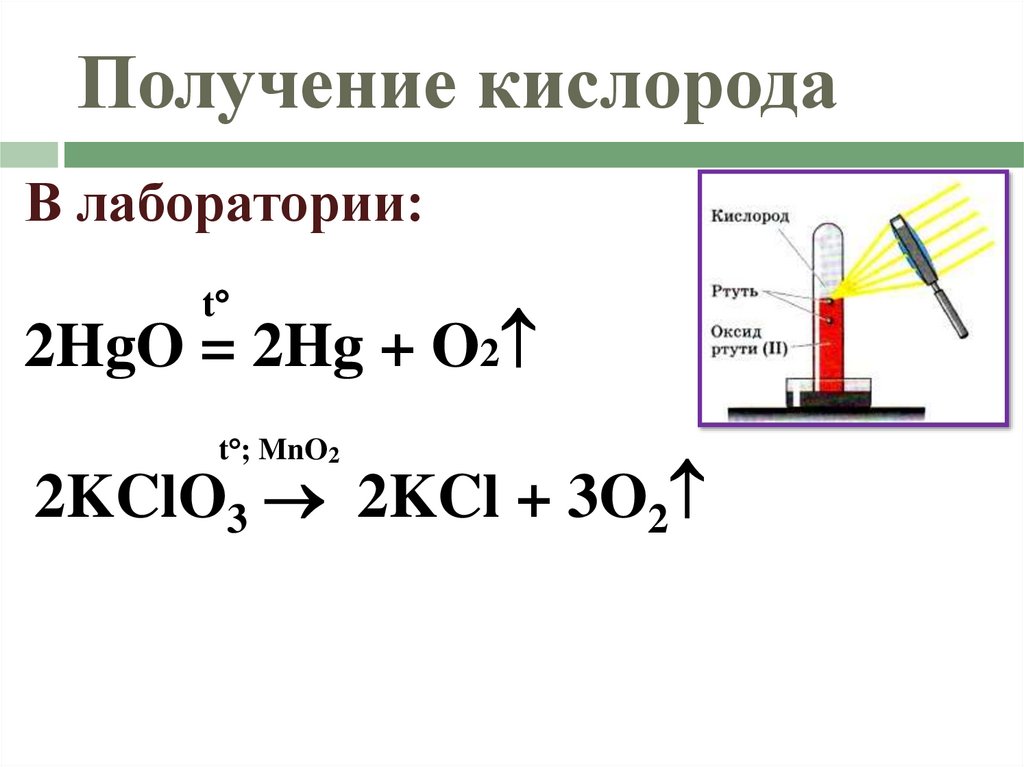
19. Получение кислорода
В лаборатории:t
2HgO = 2Hg + O2
t ; MnO2
2KClO3 2KCl + 3O2
20. Получение кислорода
2Na2O2 + 2CO2 = 2Na2CO3 + O2↑21. Получение озона
Во время грозы (в природе)В лаборатории с помощью озонатора
3O2 2O3
22.
O3Физические свойства озона
Газ синего цвета, с резким запахом
Растворимость в воде выше чем у O2
t кип= -112 С
t пл = -193 C
ρ = 2, 144 г/л (при 0 оС и 1 атм)
D по воздуху = 1,66
20.12.2025
22
23. Распознавание озона
24. Распознавание озона
2KI + H2O + O3 = 2KOH + I2 + O225. Химические свойства кислорода
Взаимодействие с простыми веществами1. Взаимодействует с металлами (кроме золота и платины)
Ме + O2 = МеО (оксид металла)
2. Взаимодействует с неметаллами (кроме галогенов - VII-A
группа)
НеМе + O2 = НеМеО (оксид неметалла)
26.
27.
28.
29.
https://ya.ru/video/preview/1320018591989497009330.
31.
Li + O2 =P + O2 =
2500C
Ca + O2 =
3000C
Cu + O2 =
S + O2 =
7000C
C + O2 =
32. Взаимодействие с простыми веществами
Г2 + O2 =Au + O2 =
Pt + O2 =
Инертные газы+ O2 =
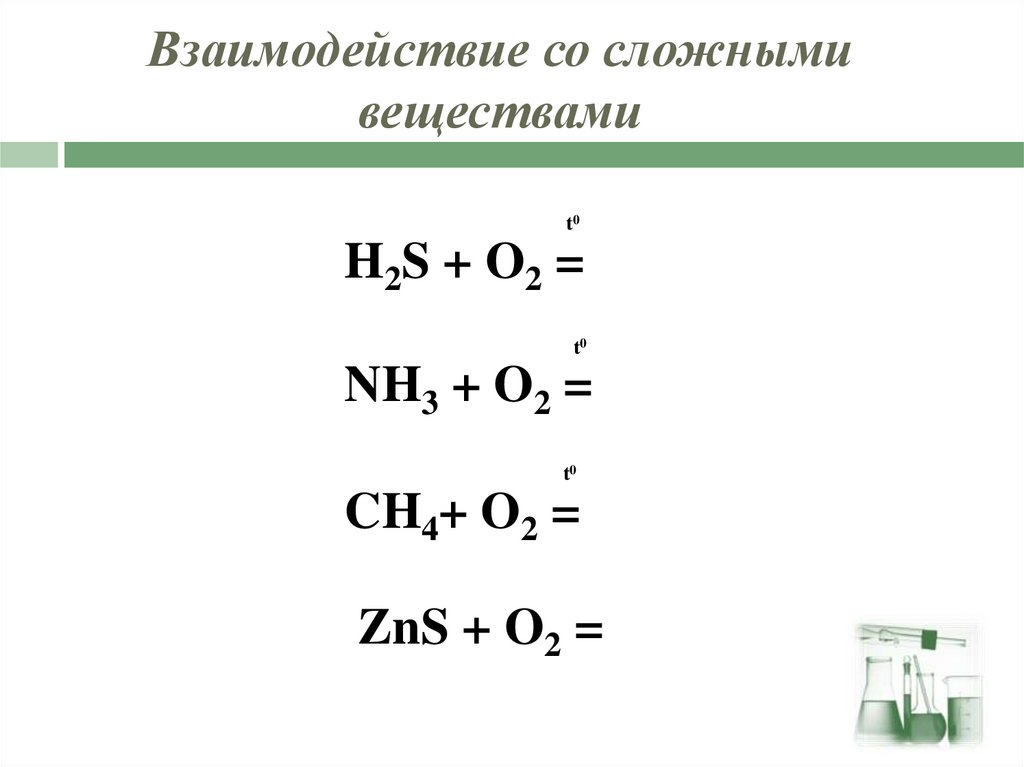
33. Взаимодействие со сложными веществами
t0H2S + O2 =
t0
NH3 + O2 =
t0
CH4+ O2 =
ZnS + O2 =
34. Взаимодействие со сложными веществами
Под действием O2, низшиесоответствующие высшие оксиды
2NO + O2 = 2NO2
t0
2SO2 + O2 = 2SO3
t0
2CO + O2 = 2CO2
оксиды
переходят
в
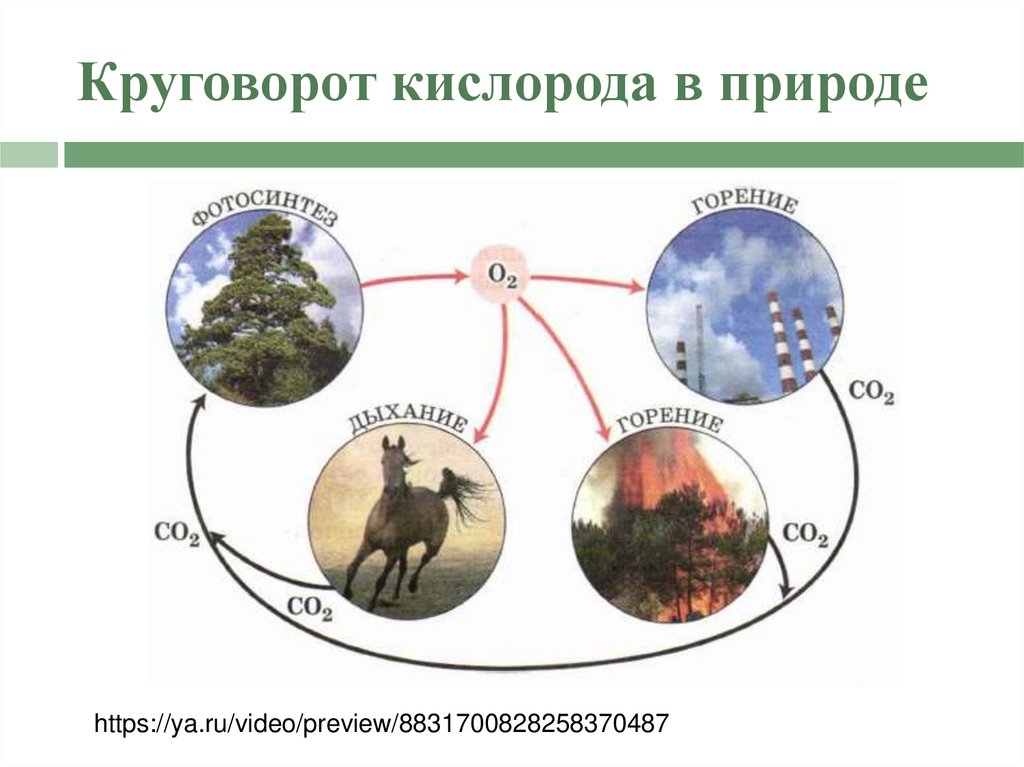
35. Круговорот кислорода в природе
https://ya.ru/video/preview/883170082825837048736. Задание на самоподготовку
§12,13 – учитьУпр.7, стр.62
Упр. 6 стр 67
20.12.2025
36



























 chemistry
chemistry








