Similar presentations:
47ebe229447d4ba195af90093ad406a9
1. СПИРТЫ: состав, строение, классификация, изомерия, номенклатура, физические свойства.
СПИРТЫ: состав,СПИРТЫ: состав, строение,
строение,
классификация, изомерия,
классификация,
изомерия,
номенклатура, физические свойства.
номенклатура, физические
свойства.
2.
Цели урока:1.Сформировать представление о
классификации спиртов.
2.Познакомиться с отдельными
представителями спиртов, их строение,
физическими свойствами,
номенклатурой, изомерией,
рассмотреть влияние спиртов на живые
организмы.
3.Рассмотреть влияние водородной
связи на физические свойства спиртов
3.
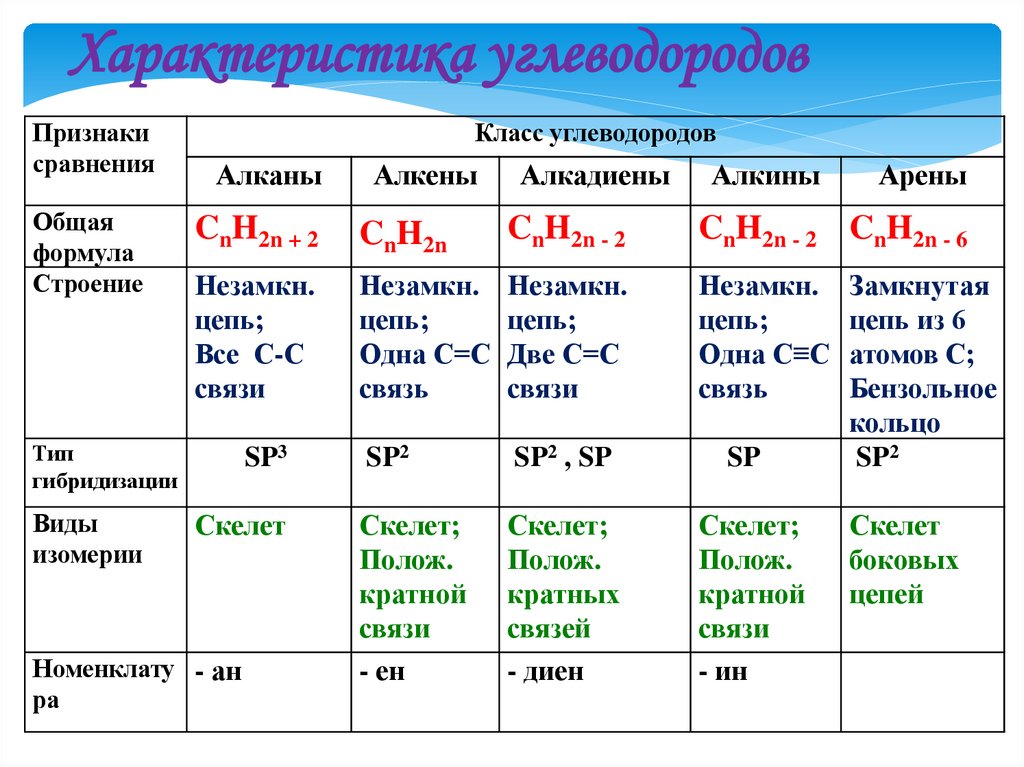
Характеристика углеводородовПризнаки
сравнения
Общая
формула
Строение
Класс углеводородов
Алканы
Алкены
Алкадиены
Алкины
CnH2n + 2
CnH2n
CnH2n - 2
CnH2n - 2 CnH2n - 6
Незамкн.
цепь;
Все С-С
связи
Незамкн. Незамкн.
цепь;
цепь;
Одна С=С Две С=С
связь
связи
Тип
гибридизации
Виды
изомерии
SP3
Скелет
Номенклату - ан
ра
Арены
SP2
SP2 , SP
Незамкн. Замкнутая
цепь;
цепь из 6
Одна С≡С атомов С;
связь
Бензольное
кольцо
SP
SP2
Скелет;
Полож.
кратной
связи
- ен
Скелет;
Полож.
кратных
связей
- диен
Скелет;
Полож.
кратной
связи
- ин
Скелет
боковых
цепей
4.
Исторические данные.В 11 веке алхимики обнаружили, что при нагревании вина, образуются пары летучего вещества,
которые при охлаждении конденсируются в бесцветную жидкость со жгучим вкусом.
В 13 веке этанол стали использовать в медицине под названиями “мать”, “государыня”, “царица
всех лекарств”.
Чистый спирт начали получать в 6-7 веках арабы и назвали его « аль коголь», что означает
одурманивающий.
Впервые в XV веке слово алкоголь применил к этанолу знаменитый немецкий врач,
естествоиспытатель Теофраст Парацельс.
Только в 1780 году (18 век) А.Лавуазье установил, что в состав этилового спирта входят углерод,
водород, кислород, а молекулярную формулу С2Н6О определил в 1833 году Берцеллус.
5.
Основные вопросы урока1. Какие вещества называются спиртами?
2. По каким признакам классифицируют спирты?
3. Какие виды изомерии характерны для спиртов?
4. Номенклатура спиртов?
5. Физические свойства характерные для спиртов
6. Где нашли применение спирты?
6. Спирты (алканолы) – это органические вещества, в молекулах которых алкильный радикал связан с гидроксильной группой. R – OH
Группа -ОН обусловливаетсвойства спиртов, поэтому
данную группу атомов называют
функциональной группой
7.
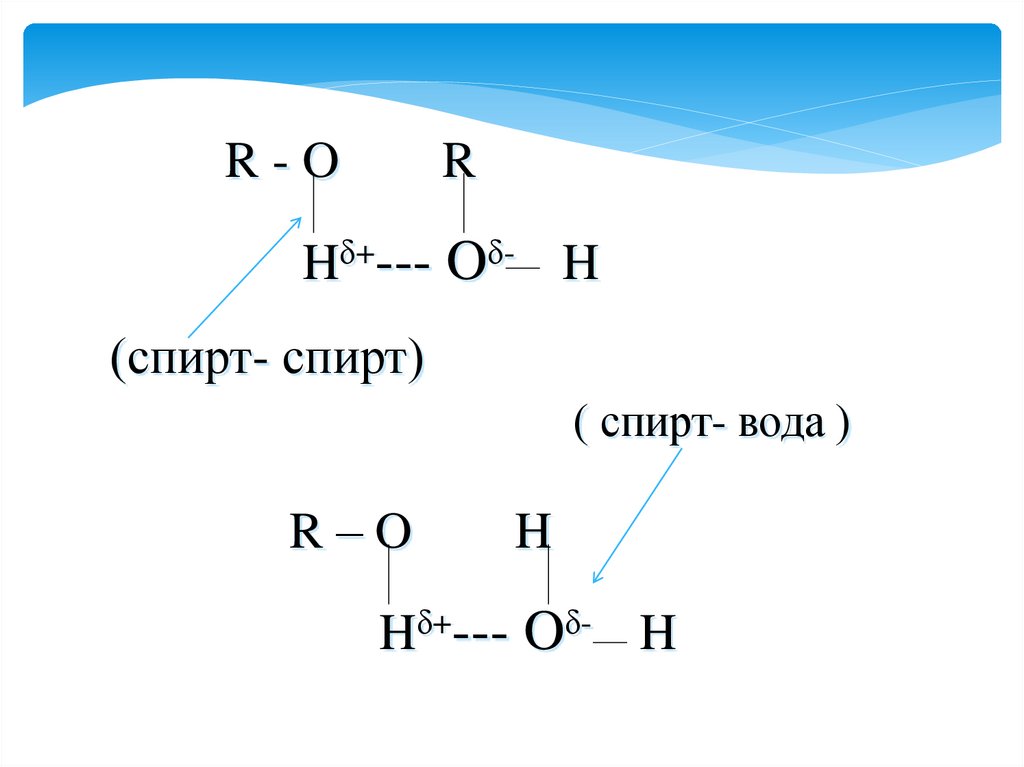
R-OR
Hδ+--- Oδ- H
(спирт- спирт)
( спирт- вода )
R–O
H
Hδ+--- Oδ- H
8.
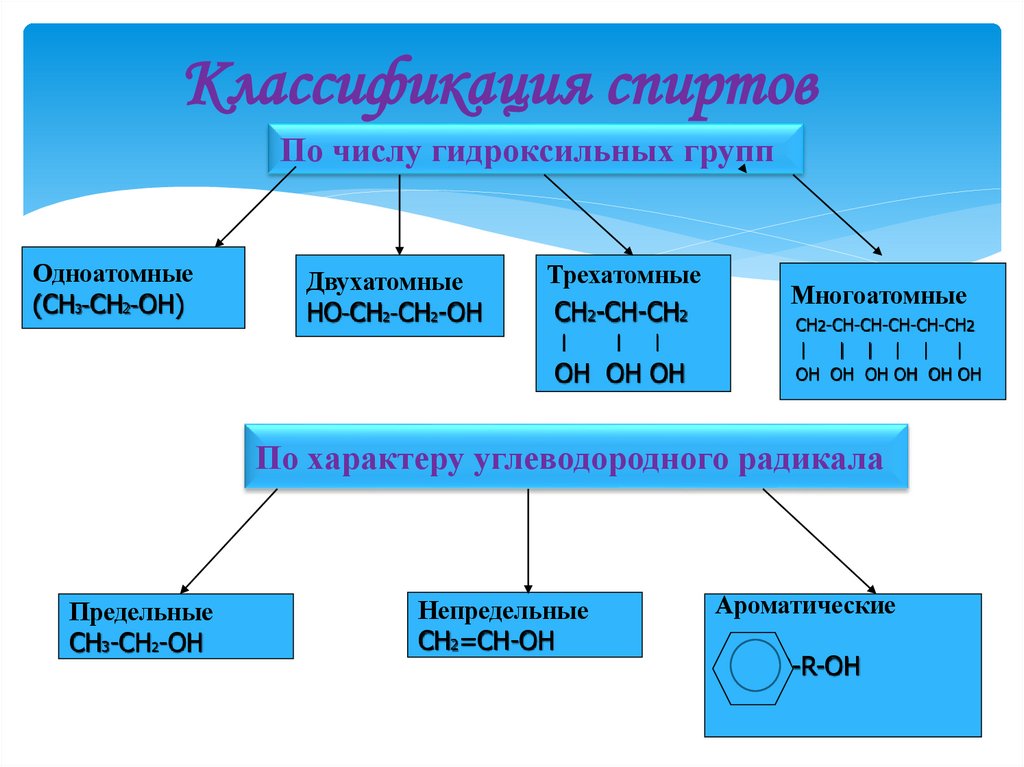
Классификация спиртовПо числу гидроксильных групп
Одноатомные
(СН3-CH2-ОН)
Двухатомные
НО-СН2-СН2-ОН
Трехатомные
СН2-СН-СН2
|
|
|
ОН ОН ОН
Многоатомные
СН2-СН-СН-CH-CH-СН2
|
| | | |
|
ОН ОН ОН ОН OH OH
По характеру углеводородного радикала
Предельные
СН3-СН2-ОН
Непредельные
СН2=СН-ОН
Ароматические
-СН2-О-R-OН
9.
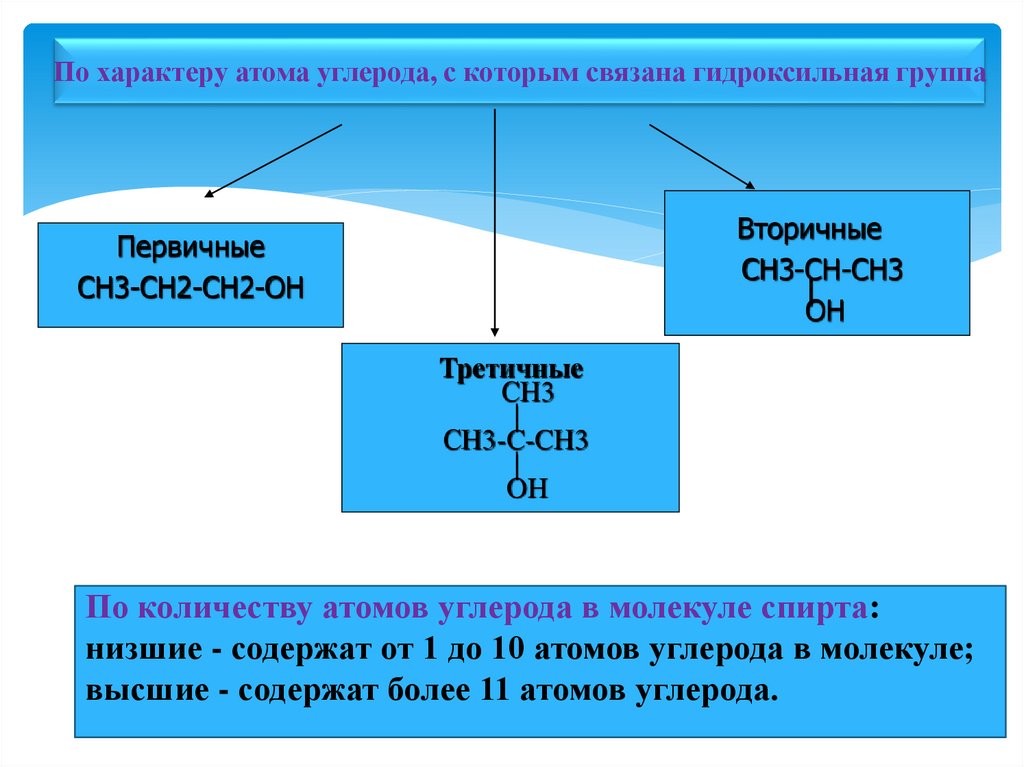
По характеру атома углерода, с которым связана гидроксильная группаВторичные
СН3-СН-СН3
|
ОН
Первичные
СН3-СН2-СН2-ОН
Третичные
СН3
|
СН3-C-CН3
|
ОН
По количеству атомов углерода в молекуле спирта:
низшие - содержат от 1 до 10 атомов углерода в молекуле;
высшие - содержат более 11 атомов углерода.
10. Предельные одноатомные спирты CnH2n+1OH – общая формула алканолов Номенклатура спиртов
1.При образовании названия спиртов кназванию углеводорода,
соответствующего спирту, добавляют
суффикс – ОЛ.
2.Цифрами после суффикса указывают
положение ОН- группы в главной цепи, а
префиксами ДИ-, ТРИ-, ТЕТРА- и т. д. –
их число.
11.
напримерНО – CH2 – CH₂ – OH - ЭТАНДИОЛ- 1,2.
1
CH₃ OH – метанол (метиловый спирт)
2
1
CH₃ – CH₂ – OH – этанол (этиловый спирт)
3
2
1
CH₃ – CH₂ – CH₂ - OH – пропанол – 1
12.
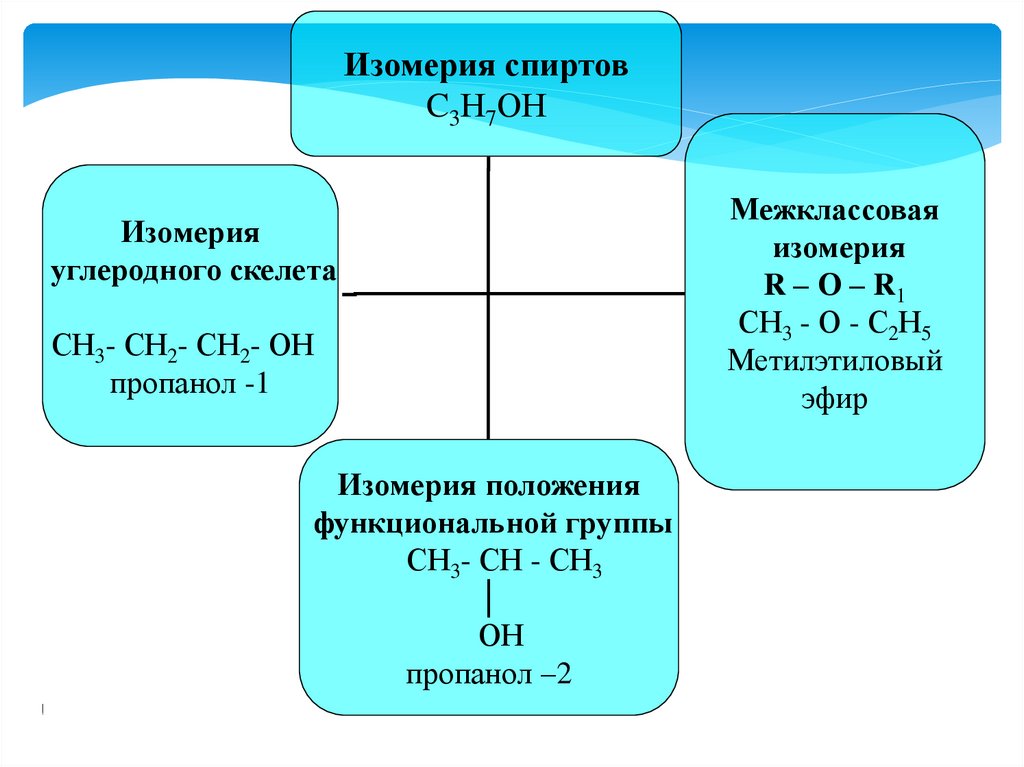
Изомерия спиртовC3Н7ОН
Изомерия
углеродного скелета
СН3- СН2- СН2- ОН
пропанол -1
Изомерия положения
функциональной группы
СН3- СН - СН3
│
ОН
пропанол –2
Межклассовая
изомерия
R – О – R1
СН3 - О - С2Н5
Метилэтиловый
эфир
13.
Виды изомерии спиртов-изомерия положения ОН- группы, (начиная с С3)
CH3-CH2-CH2-OH
CH3-CHOH-CH3
пропанол-1
-углеродного скелета,
CH3-CH2-CH2-CH2-OH
и
пропанол-2 ;
(начиная с С4 );
бутанол-1
CH3-CH-CH2-OH 2-метилпропанол-1
|
CH3
-межклассовая изомерия с простыми эфирами,
(начиная с С2 )
СН3-CH2–OH
и
CH3–O–CH3
14. Физические свойства.
Температура кипения спиртов выше температуры кипениясоответствующих углеводородов.
Среди спиртов нет газов.
С увеличением относительной молекулярной
массы
спиртов повышаются их температуры кипения,
уменьшается растворимость в воде.
Это объясняется наличием межмолекулярной водородной
связи, которая может образовываться как между
молекулами спиртов, так и между молекулами спиртов и
воды.
Это влияет на физические свойства спиртов: повышает
температуру кипения, снижает летучесть, способствует
хорошей растворимости в воде, не позволяет перегонкой
получить 100% спирт из его водного раствора.
1. Запах
С1 - С3 - «спиртовой» запах
С4 - С6 - «сивушный» запах
С11 - запаха нет
Агрегатное состояние:
С1- С11- жидкости
С12 - С…- твердые
вещества
15. Этиловый спирт пагубно влияет на клетки головного мозга
СПАСИБО ЗАУРОК










 chemistry
chemistry








