Similar presentations:
9. БИОБЕЗОПАСНОСТЬ МИКРОБИОЛОГИЧЕСКИХ ЛАБОРАТОРИЙ ФАРМАЦЕВТИЧЕСКИЙ АСПЕКТ
1. БИОБЕЗОПАСНОСТЬ МИКРОБИОЛОГИЧЕСКИХ ЛАБОРАТОРИЙ: ФАРМАЦЕВТИЧЕСКИЙ АСПЕКТ
Лекция 9Организация безопасной работы с
микроорганизмами I-IV групп
патогенности
1
2. План лекции
1. Микробиологическая лаборатория нафармацевтическом предприятии
2. Организация и оборудование лаборатории
3. Специфические и нежелательные
микроорганизмы на фармацевтическом
производстве
4. Микроорганизмы-индикаторы
2
3. 1 Микробиологическая лаборатория на фармацевтическом предприятии
• Микробиологическая лаборатория на фармацевтическомпредприятии обеспечивает:
– контроль санитарно-гигиенического состояния производства,
– основного и вспомогательного сырья,
– производственного процесса и готовой продукции,
• которые проводятся в соответствии с программой
производственного контроля.
Программа производственного контроля – документ
предприятия-изготовителя, определяющий порядок и
периодичность контроля санитарно-гигиенического
состояния производства лекарственных средств, сырья,
производственного процесса и готового продукта.
3
4. Значительную часть требований к качеству фармацевтической продукции и к условиям производства контролирует микробиолог
• стерильность,• микробное обсеменение сырья и нестерильных лекарственных
средств,
• соблюдение правил производственной гигиены,
предусмотренных GMP.
• Микробиологическая лаборатория обеспечивает контроль
качества, осуществляя микробиологический мониторинг всех
этапов производственного процесса:
– – входной контроль сырья,
– – контроль хранения и упаковки,
– – контроль процесса производства,
– – контроль готового продукта (приемо-сдаточный контроль),
– – контроль утилизации.
4
5. Основной микробиологический мониторинг включает отслеживание контаминации:
• – воздуха – активным методом (при помощи прибора) ипассивным (седиментационный метод);
• – оборудования чистых помещений – метод отпечатков на
агаровую среду, метод взятия мазков с поверхности;
• – работников – метод отпечатков;
• – упаковочного материала;
• – химических субстанций, применяемых для
производства лекарственных препаратов;
• – лекарственного растительного сырья;
• – воды очищенной и воды инъекционной;– готовых
лекарственных препаратов.
5
6. На асептических производствах также контролируется:
• – стерильность первичной упаковки;• – микробиологическая нагрузка инъекционного препарата
перед фильтрацией;
• – cтерильность дезсредств;
• – эффективность методов стерилизации;
• – описание мер, которые должны быть приняты при
превышении лимитов
Используются три схемы организации контроля качества –
усиленный, нормальный и ослабленный контроль.
6
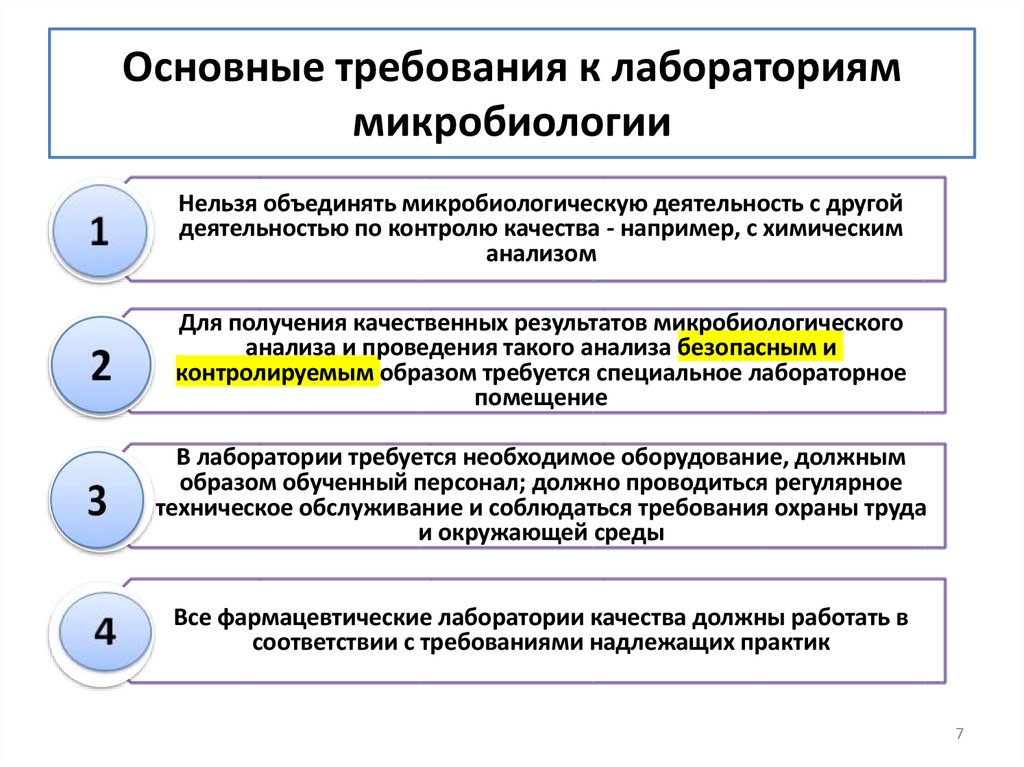
7. Основные требования к лабораториям микробиологии
Нельзя объединять микробиологическую деятельность с другойдеятельностью по контролю качества - например, с химическим
анализом
Для получения качественных результатов микробиологического
анализа и проведения такого анализа безопасным и
контролируемым образом требуется специальное лабораторное
помещение
В лаборатории требуется необходимое оборудование, должным
образом обученный персонал; должно проводиться регулярное
техническое обслуживание и соблюдаться требования охраны труда
и окружающей среды
Все фармацевтические лаборатории качества должны работать в
соответствии с требованиями надлежащих практик
7
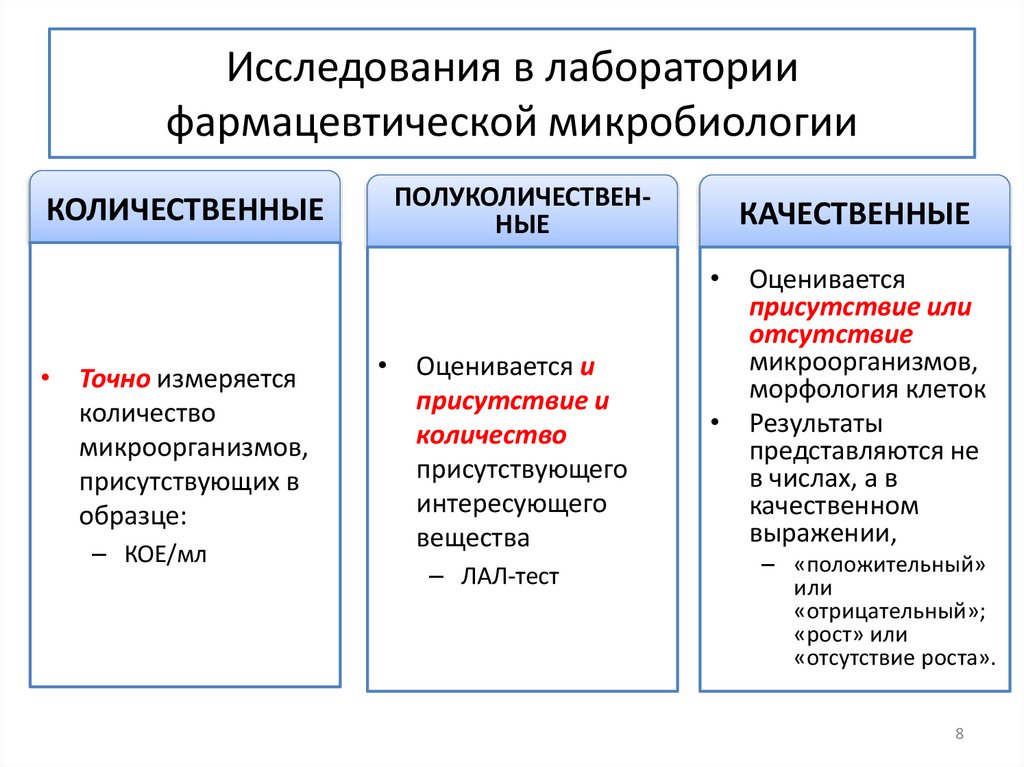
8. Исследования в лаборатории фармацевтической микробиологии
КОЛИЧЕСТВЕННЫЕ• Точно измеряется
количество
микроорганизмов,
присутствующих в
образце:
– КОЕ/мл
ПОЛУКОЛИЧЕСТВЕННЫЕ
КАЧЕСТВЕННЫЕ
• Оценивается и
присутствие и
количество
присутствующего
интересующего
вещества
• Оценивается
присутствие или
отсутствие
микроорганизмов,
морфология клеток
• Результаты
представляются не
в числах, а в
качественном
выражении,
– ЛАЛ-тест
– «положительный»
или
«отрицательный»;
«рост» или
«отсутствие роста».
8
9. Основные функции заведующего микробиологической лабораторией на фармацевтическом производстве
Заведующий микробиологическойследующие функции:
лаборатории
должен
выполнять
1) установление политики и процедур в области качества (включая
необходимые стандартные операционные процедуры (СОП);
2) обеспечение документирования всех политик, процессов, процедур и
инструкций;
3) Обеспечение того, что весь персонал понимает документы, инструкции, а
также свои обязанности и ответственность. Это требует эффективной
системы обучения и оценки знаний;
4) предоставление персоналу соответствующих полномочий и ресурсов для
выполнения своих обязанностей. Это относится к ученым-биологам и
микробиологам с высшим образованием.
Заведующий микробиологической лабораторией должен иметь
достаточный опыт и квалификацию в области микробиологии.
9
10. Основные составляющие эффективного управления лабораторией
• Строгий тайм-менеджмент• Иерархия кадров
• Наставничество
• Персонал – самый важный ресурс лаборатории!
• Логичная разработка должностных инструкций
– они должны отражать все необходимые для
работы навыки.
Рабочий процесс лаборатории – сумма всех операций,
необходимых для проведения анализа.
Анализ начинается с отбора пробы и заканчивается отчетностью
10
11. Стандартные операционные процедуры (СОП)
Все процедуры и анализы, производимые в лаборатории, должны
быть зафиксированы в СОП – стандартных операционных процедурах.
СОП должны содержать пошаговые письменные инструкции для
каждой процедуры, выполняемой в лаборатории.
Эффективная СОП должна быть:
подробной, ясной и краткой – такой, чтобы персонал, обычно не
выполняющий данную процедуру, мог сделать это, следуя СОП. Все
необходимые детали (например, требования к температуре инкубации и
точные инструкции по времени) должны быть прописаны в СОП;
легкой для понимания новыми сотрудниками или обучающимися;
актуальной и уместной;
рассмотрена и утверждена руководством лаборатории.
11
12. Менеджмент проб
Менеджмент проб - одна из важнейших составляющих системыменеджмента качества, и контроль образцов является одной из
ключевых составляющих управления лабораторией
Например, СОП по процедурам контроля образцов должна
содержать:
1) описание того, какие образцы следует хранить;
2) срок годности;
3) местонахождение;
4) условия хранения;
5) система организации хранения;
6) порядок транспортировки образцов: часто образцы собираются за
пределами лаборатории и их необходимо транспортировать для
последующей обработки и анализа.
12
13. Наиболее важными аспектами исследований являются микроорганизмы и питательные среды
• Микробиология требует использования живыхконтрольных микроорганизмов для проверки
надлежащей работы индикаторов, различных
реагентов и питательных сред.
• Тест-штаммы необходимо бережно поддерживать в
виде исходных и рабочих культур.
– Качественной питательной средой в
микробиологической лаборатории считается такая
среда, которая подходит для получения оптимальных и
надежных результатов исследований.
13
14. Требования к обучению персонала микробиологической лаборатории на фармацевтическом предприятии
Обучение — это процесс получения и развития знаний,навыков и моделей поведения в соответствии с
определенными требованиями
• Обучение должно устранять выявленные пробелы в
конкретных знаниях и умениях, касающихся задач, которые
должен выполнять сотрудник, как указано в должностных
инструкциях
• Проверка квалификации — это наиболее часто используемый
тип оценки качества обучения
– персонал получает некоторую пробу, в которой затем
пытается определить уровень эндотоксинов; Такая проверка
может происходить 2-4 раза в год.
14
15. Безопасность в микробиологической лаборатории
Руководитель лаборатории должен обеспечить наличиенеобходимого оборудования, такого как:
1) средства индивидуальной защиты (защитные очки, лабораторный
халат, перчатки);
2) огнетушители и противопожарные одеяла;
3) хранилища для легковоспламеняющихся и токсичных химикатов;
4) станции промывки глаз и аварийный душ;
5) материалы и оборудование для утилизации отходов;
6) аптечка первой помощи.
15
16. Безопасность в микробиологической лаборатории
• Все химические вещества
должны быть маркированы с
указанием их общепринятых
названий, концентрации и
уровня опасности.
Все
отходы,
удаляемые
из
лаборатории, должны быть надежно
упакованы. Отходы должны быть
обеззаражены
на
месте
или
вывезены
специализированной
компанией
для
сжигания.
Обеззараживание
отходов
биологической опасности 3 и 4
всегда следует проводить на месте.
•Коррозионные, токсичные и
высокореактивные
химикаты
должны храниться в хорошо
вентилируемом помещении, а
химические вещества, которые
могут
воспламениться
при
комнатной
температуре,
должны
храниться
в
специальном
противопожарном шкафу.
Работу с микроорганизмами
следует проводить в боксах
микробиологической
безопасности (соответствующих
классу биологической опасности
микроорганизма).
16
17. Безопасность в микробиологической лаборатории
• В соответствии с СанПиН 2.1.3684-21– отходы от деятельности, использующей генноинженерномодифицированные организмы в медицинских целях,
– отходы от производства лекарств и медизделий,
– хранения биомедицинских клеточных продуктов,
– отходы от использования возбудителей инфекционных заболеваний
1-2 групп патогенности;
– отходы из микробиологических, клинико-диагностических
лабораторий, фармацевтических и иммунобиологических
производств, работающих с микроорганизмами 1-2 групп
патогенности,
– биологические отходы вивариев,
– живые вакцины, непригодные к использованию,
• относятся к классу опасности В.
17
18. Безопасность в микробиологической лаборатории
• Большинство лабораторий имеет два физических уровнязащиты:
– первичный барьер (защитное оборудование), который будет
сдерживать опасность в источнике, и
– вторичный барьер (сама лаборатория)
• Весь воздух, покидающий боксы безопасности, должен
проходить через HEPA-фильтры.
• В лабораториях поддерживается более низкое давление, чем в
прилегающих помещениях (отрицательное давление), чтобы
предотвратить распространение контаминации по зданию
• Работы с опасными микроорганизмами следует проводить в
боксе микробиологической безопасности
18
19. Группы патогенности микроорганизмов
IV группа – наименее опасные патогены. Пример:Pseudomonas aeruginosa, Mycoplasma spp., Salmonella spp.,
Staphylococcus spp; вирус кори, краснухи, паротита,
аденовирусы; грибы рода Mucor, Trichosporon, Rhizopus.
III группа: Clostridium botulinum, C. tetani; Mycobacterium spp.,
Salmonella typhi, Escherichia coli; вирусы гриппа A, B, C; герпеса
простого, гепатита А и Е, вирус Эпштейн-Барра; Candida
albicans.
II группа: Bacillus anthracis, Brucella spp., Vibrio cholerae;
вирусы ВИЧ, гепатита B и С, бешенства, коронавирус SARS;
возбудители прионных болезней; Chlamydia trachomatis.
I группа: Yersinia pestis
19
20. Система управления лабораторной информацией (LIMS)
В значительной степени бумажную систему ведения документациилаборатории заменила электронная система – LIMS.
в
LIMS (Laboratory Information Management System) — это программная
система, которая позволяет автоматизировать управление лабораторией.
LIMS позволяет проводить:
1) получение и регистрацию образца и связанных с ним данных;
2) назначение, планирование и отслеживание пробы и связанной с ней
аналитической рабочей нагрузки;
3) контроль качества пробы, используемого оборудования и инвентаря;
4) хранение данных, связанных с анализом пробы;
5) проверку, утверждение и компиляцию выборочных данных для
отчетности и дальнейшего анализа.
20
21. 2. Организация и оборудование лаборатории
В структуру лаборатории входят– лабораторные комнаты и боксы для работы в
асептических условиях;
– автоклавная – специально оборудованное
помещение для стерилизации питательных сред,
посуды, обеззараживания отработанного
материала;
– моечная, оборудованная для мытья посуды;
– виварий – помещение, предназначенное для
содержания лабораторных животных.
21
22. Общие требования к микробиологическим лабораториям
• Микробиологические лаборатории должны находиться в отдельномздании или в изолированной части здания.
• Лаборатория должна иметь, как минимум, два входа.
• Все помещения должны иметь естественное и искусственное
освещение, температура воздуха должна поддерживаться в пределах
18–21 оС.
• Стены в должны быть облицованы глазурованной плиткой или
выкрашены масляной краской светлых тонов на высоту 1,5 метра.
• Полы в лабораторных помещениях покрываются линолеумом или
гладкой плиткой. Полы не должны быть скользкими.
• Ширина основных проходов в помещениях к рабочим местам должна
быть не менее 1,5 метра.
• В лаборатории должны быть особым образом проведены
электричество, вентиляция, водопровод и отопление.
• В системе водоснабжения предусматривается раздельная подача
воды для бытовых нужд и для лабораторных исследований.
22
23. Общие требования к микробиологическим лабораториям
«Чистая» зона«Заразная» зона
Работы с ПБА не проводятся
(препараторская,
стерилизационная,
помещение для хранения
дезсредств)
Проводятся работы с ПБА
и осуществляется их
хранение
(боксированные помещения
для микробиологических
исследований)
Требуется обязательное оснащение микробиологической
лаборатории:
1.
Горячим и холодным водоснабжением, канализацией,
системой сбора и удаления отходов, средствами связи и
системой поддержания микроклимата.
2.
Пожарной и аварийной сигнализацией.
23
24.
Ламинарные боксы-укрытия• Создают абактериальную среду
внутри бокса для защиты
продукта от воздействия
окружающей среды.
• Не защищают оператора от
вредного воздействия
продукта. Пример: ПЦР-бокс.
Боксы биологической безопасности
(ламинарные боксы)
• Конструкция, используемая для
физической изоляции
(удержания и контролируемого
удаления из рабочей зоны)
микроорганизмов с целью
предотвращения возможности
заражения персонала и
контаминации воздуха рабочей
зоны и окружающей среды.
24
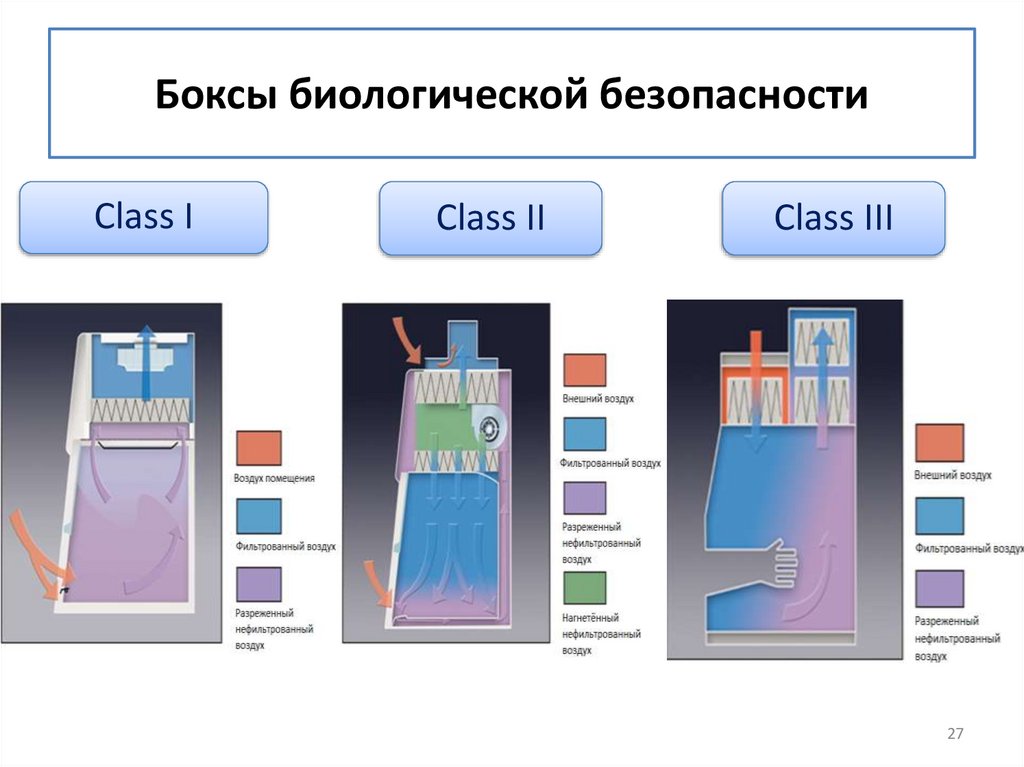
25. Устройство ламинарного бокса 1 класса защиты
• Ламинары класса Iоборудованы:
– притяжной вентиляцией
нестерильного воздуха из
помещения
– и выходом этого воздуха в
то же помещение после
фильтрации (защита от
микробных аэрозолей)
– и в строгом смысле слова
не пригодны для
стерильной работы.
25
26. Устройство ламинарного бокса 2 класса защиты
• Ламинары с защитой класса IIобразуют внутри бокса поток
стерильного воздуха, забор
которого происходит из
помещения, и который
стерилизуется, проходя через
бактериальные фильтры.
• Конструкция позволяет также
проводить стерильные посевы
микроорганизмов в струе
стерильного воздуха, прошедшего
через бактериальные фильтры и
распределенного внутри ламинара
в виде ламинарного потока (без
завихрений)
26
27. Боксы биологической безопасности
Class IClass II
Class III
27
28. 3 Специфические и нежелательные микроорганизмы на фармацевтическом производстве
• Специфические МО описаны:– в гармонизированной фармакопее Европейская Фармакопея
2.6.13 и USP <62»
– ОФС 1.2.4.002.15 «Микробиологическая чистота» Государственной
Фармакопеи.
• Эти НД указывают требования к наличию и отсутствию
данных «специфических» МО в нестерильных
лекарственных препаратах.
• Современные подходы к оценке риска требуют от
микробиолога определения более широкого списка МО,
на которые стоит обратить внимание на конкретном
производстве
28
29. «Нежелательных» микроорганизмы на производстве можно разделить на 2 группы:
• конкретныеиндикаторные
«специфические»
микроорганизмы, для
которых необходимо
тестирование согласно
фармакопей
• микроорганизмы,
определенные
фармацевтической
организацией как
нежелательные в
отношении
конкретного продукта
на их собственном
производстве
29
30. 4 Микроорганизмы-индикаторы
• Для нестерильных продуктов существует обязательноетребование об отсутствии определенных
микроорганизмов.
• Эти микроорганизмы включают патогены, такие как
Salmonella, и индикаторы фекального загрязнения, такие
как Escherichia coli.
• Эти микроорганизмы напрямую представляют риск, или
могут указывать на присутствие других микроорганизмов
из аналогичных источников, которые представляют
особый риск для пациентов с ослабленным иммунитетом
30
31. Полный список специфических микроорганизмов, описанных в гармонизированной фармакопее (USP <62 и Ph. Eur. 2.6.13, совпадает с
Полный список специфических микроорганизмов,описанных в гармонизированной фармакопее
(USP <62 и Ph. Eur. 2.6.13, совпадает с ГФ РФ):
Желчеустойчивые грамотрицательные бактерии;
Escherichia coli;
Salmonella;
Pseudomonas aeruginosa;
Staphylococcus aureus;
Clostridia;
Candida albicans
31
32. Желчеустойчивые грамотрицательные бактерии
• Желчеустойчивые грамотрицательные бактерии лучшевсего определять как те микроорганизмы, которые в
определенных условиях демонстрируют рост на
фиолетово-красной желчно-глюкозной агаровой среде
– К ним относятся Г- бактерии, которые растут в присутствии солей
желчных кислот, не ферментируют лактозу, ферментриуют
глюкозу
• Примеры:
– Salmonella, E. coli, Yersinia pestis, Klebsiella и Shigella Proteus,
Enterobacter, Serratia и Citrobacter
Бульон Мосселя (1 г образца) → чашки с краснофиолетовым агаром с желчью и глюкозой
32
33. Escherichia coli
• E. coli - это грамотрицательная, факультативно анаэробнаяпалочковидная бактерия из рода Escherichia, которая
обычно встречается в нижнем отделе кишечника
теплокровных организмов.
• Большинство штаммов Е. coli безвредны, но некоторые
серотипы могут вызывать серьезные пищевые отравления
и иногда являются причиной отзыва пищевой и
фармацевтической продукции при обнаружении
контаминации этим организмом.
В фармакопейном тесте для проверки наличия E. coli
используют среду МакКонки
33
34. Salmonella
• Сальмонеллы - это род палочковидных грамотрицательныхбактерий.
• Существует только два вида Salmonella:
– Salmonella bongori и Salmonella enterica, в которых насчитывается
около шести подвидов и бесчисленное количество сероваров.
• Их можно разделить на две группы - тифоидные и
нетифоидные серовары.
– Нетифоидные серовары встречаются чаще и обычно вызывают
самоограничивающееся желудочно-кишечное заболевание.
– Тифоидные серовары включают Salmonella typhi и Salmonella paratyphi
А, которые встречаются только у людей и не встречаются у других
животных.
Фармакопейный тест на сальмонеллы включает
использование жидкой среды Раппапорта-Вассилиадиса
или XLD-агара (ксилозо-лизинового дезоксихолатного). 34
35. P. aeruginosa
• P. aeruginosa это грамотрицательная аэробнаякоккобациллярная бактерия с униполярной подвижностью.
• Это условно-патогенный микроорганизм человека, часто
связанный с загрязнением водных систем.
– Р. aeruginosa обычно поражает легочные и мочевыводящие пути,
ожоги, раны, и вызывает инфекции крови.
• просто идентифицировать: Р. aeruginosa секретирует различные
пигменты, включая пиоцианин (сине- зеленый), пиовердин
(желто-зеленый флуоресцентный) и пиорубин (краснокоричневый).
Согласно фармакопее, рекомендуемая среда
цетримидный агар
35
36. S. aureus
• S. aureus - это грамположительные кокки, которые частовстречаются в дыхательных путях и на коже человека.
• Хотя S. aureus не всегда патогенен, он является частой
причиной кожных инфекций (например, фурункулов),
респираторных заболеваний (например, синусита) и
пищевых отравлений.
• Связанные с заболеванием штаммы часто способствуют
развитию инфекций, продуцируя сильнодействующие
белковые токсины.
В фармакопее рекомендуемой средой является
маннит-солевой агар
36
37. Клостридии
• Clostridium это палочковидные грамположительныебактерии, образующие эндоспоры.
• Есть ряд видов, которые могут вызывать заболевания у
людей, в том числе Clostridium botulinum, Clostridium
difficile и Clostridium tetani.
• Все патогенные виды клостридий продуцируют белковые
экзотоксины (такие как ботулинический и столбнячный
токсины), которые играют ключевую роль в патогенезе
заболеваний.
В фармакопейном методе анализа указана усиленная
дифференциально- диагностическая среда для Clostridia,
затем следует колумбийский агар.
37
38. C. albicans
• C. albicans диплоидный грибок, который растет как в формедрожжевых клеток, так и в форме нитчатых гифов.
• Это возбудитель оппортунистических инфекций полости рта и
слизистых половых органов у людей.
• С. albicans является комменсалом и компонентом нормальной
кишечной микрофлоры, состоящей из микроорганизмов,
обитающих во рту и желудочно-кишечном тракте человека.
• Грибок представляет опасность для хозяина с ослабленным
иммунитетом.
В фармакопейном методе анализа для выделения
используются среда Сабуро с декстрозой.
38