Similar presentations:
1177956
1.
Тема: Тепловой эффект химическойреакции, термохимические уравнения,
экзо- и эндотермические реакции.
Изучите презентацию,
запишите краткий конспект в тетрадь
2.
Закон сохраненияэнергии
Энергия не возникает из
ничего и не исчезает
бесследно, а только
переходит из одной
формы в другую.
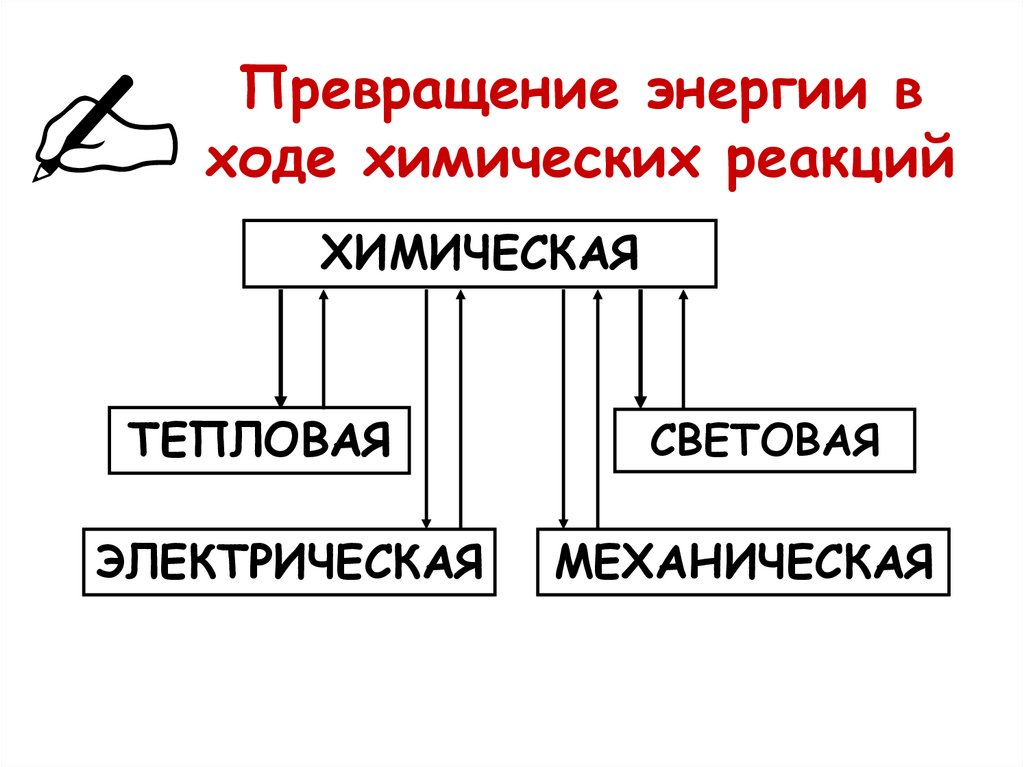
3. Превращение энергии в ходе химических реакций
ХИМИЧЕСКАЯТЕПЛОВАЯ
ЭЛЕКТРИЧЕСКАЯ
СВЕТОВАЯ
МЕХАНИЧЕСКАЯ
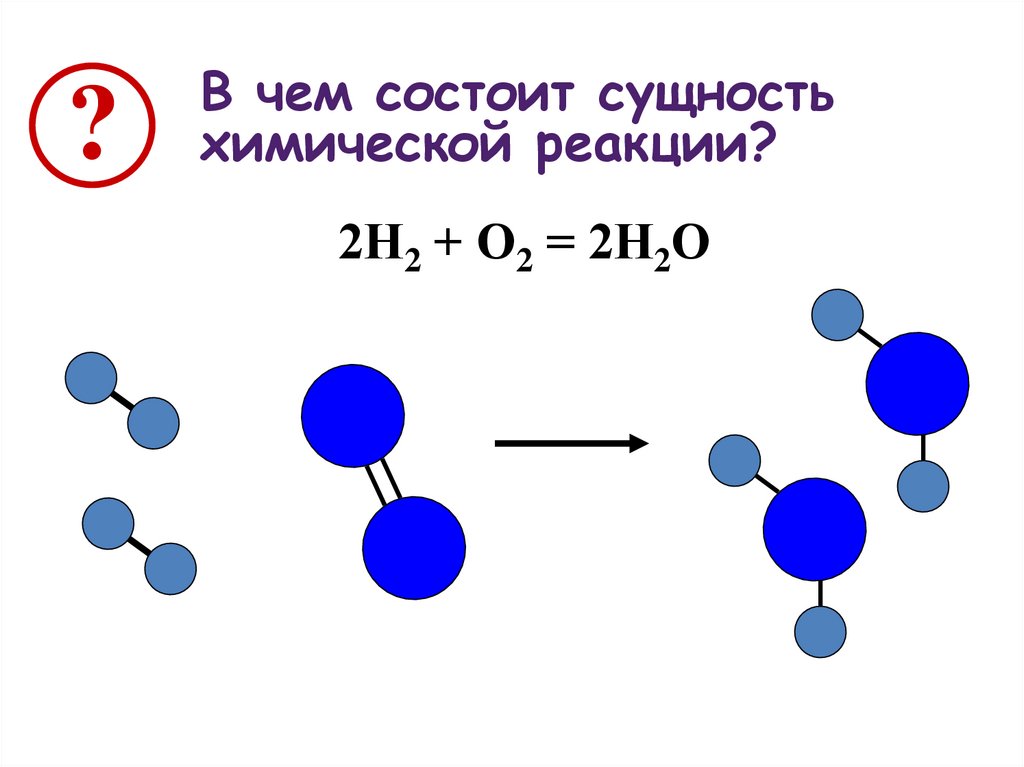
4.
?В чем состоит сущность
химической реакции?
2Н2 + О2 = 2Н2О
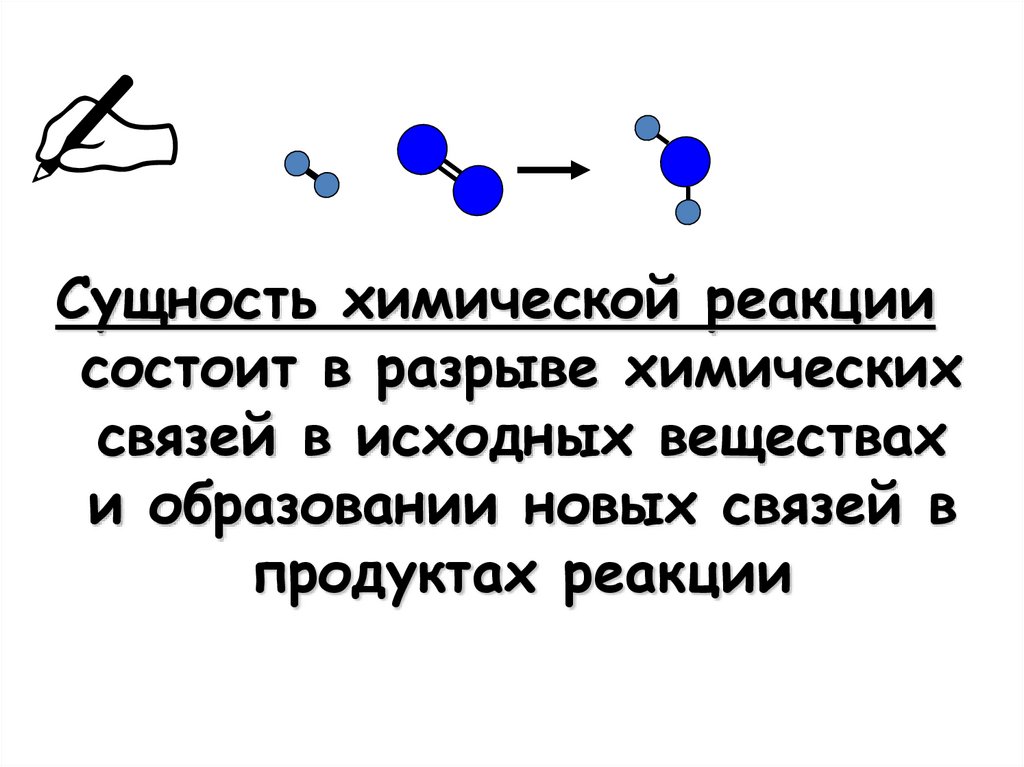
5.
Сущность химической реакциисостоит в разрыве химических
связей в исходных веществах
и образовании новых связей в
продуктах реакции
6.
?Связаны ли процессы
разрыва и образования
химических связей
с процессами изменения
энергии?
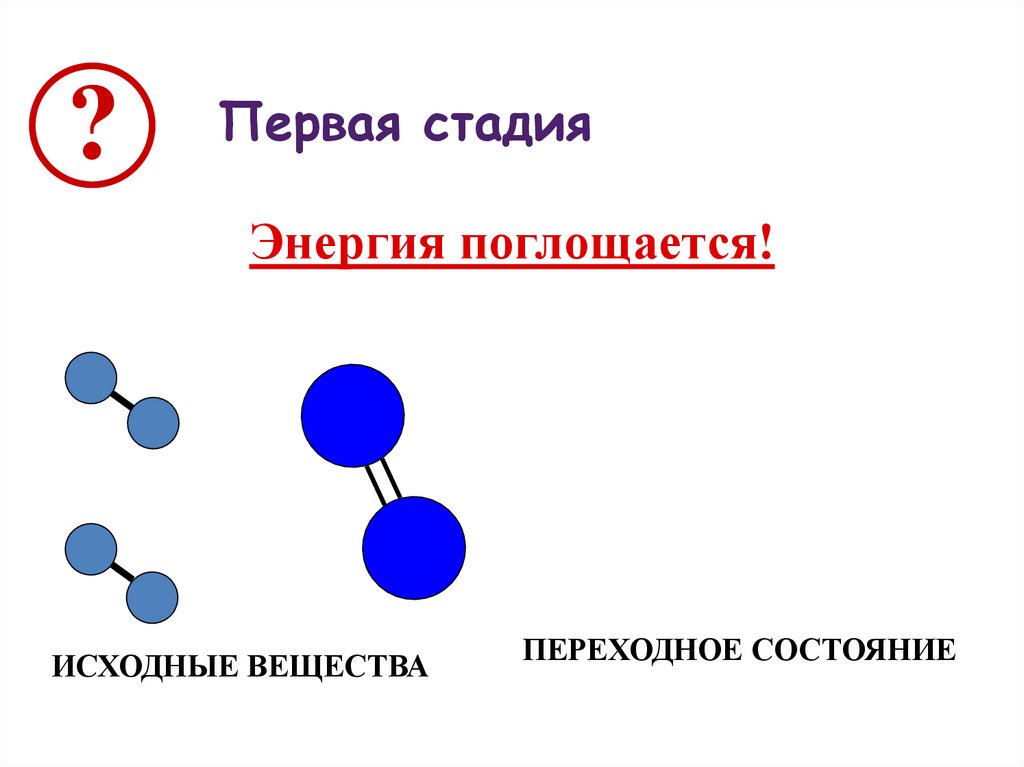
7.
?Первая стадия
Энергия поглощается!
ИСХОДНЫЕ ВЕЩЕСТВА
ПЕРЕХОДНОЕ СОСТОЯНИЕ
8.
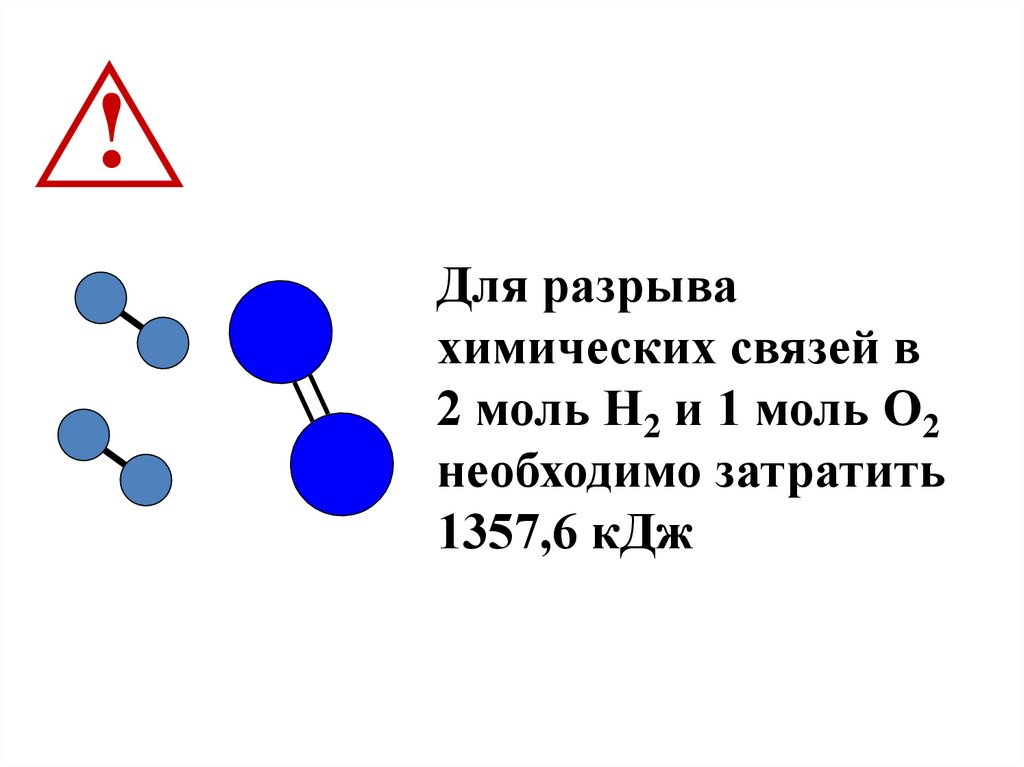
!Для разрыва
химических связей в
2 моль Н2 и 1 моль О2
необходимо затратить
1357,6 кДж
9.
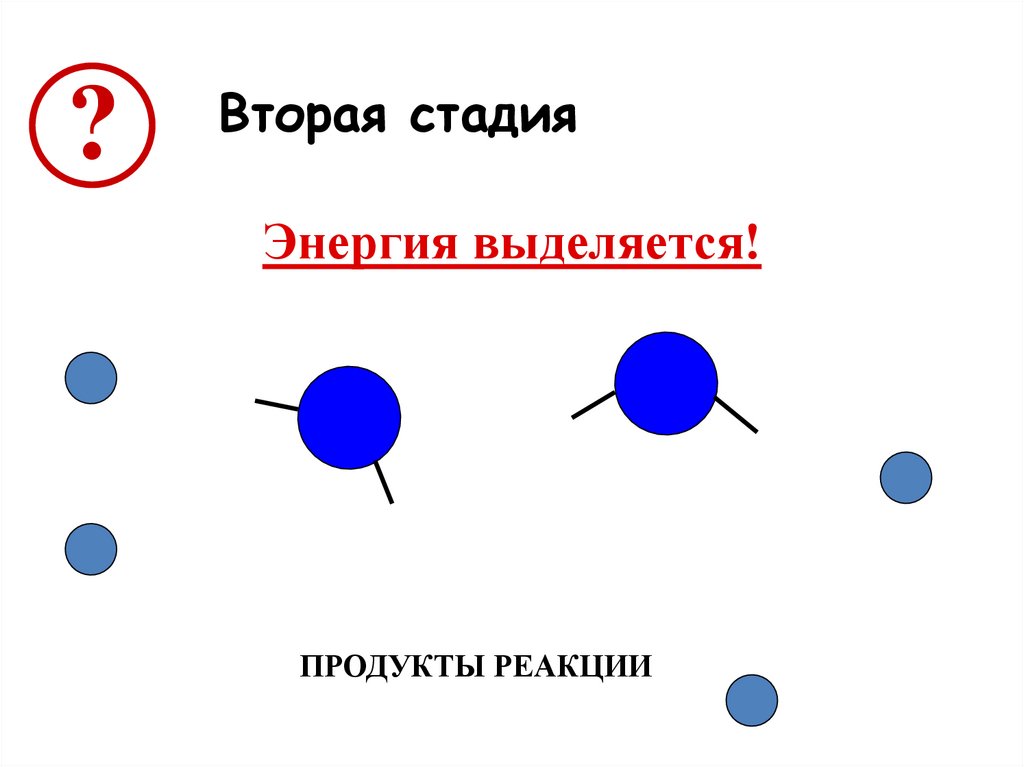
?Вторая стадия
Энергия выделяется!
ПРОДУКТЫ РЕАКЦИИ
10.
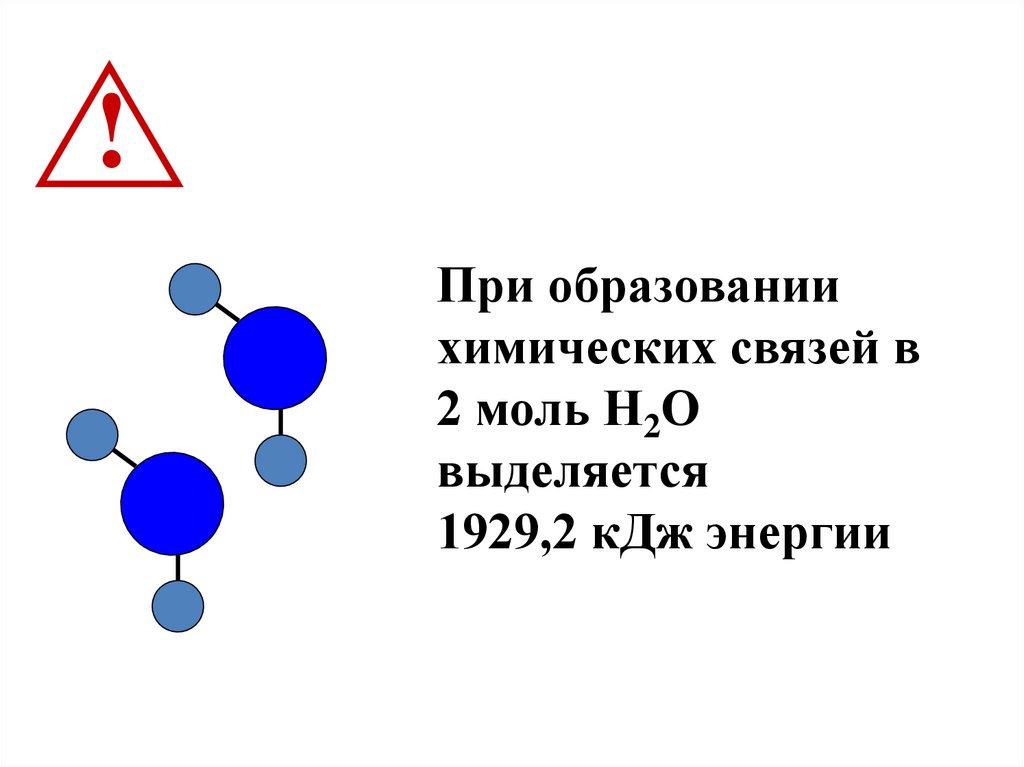
!При образовании
химических связей в
2 моль Н2О
выделяется
1929,2 кДж энергии
11. Любая химическая реакция заключается в разрыве одних химических связей и образовании других!
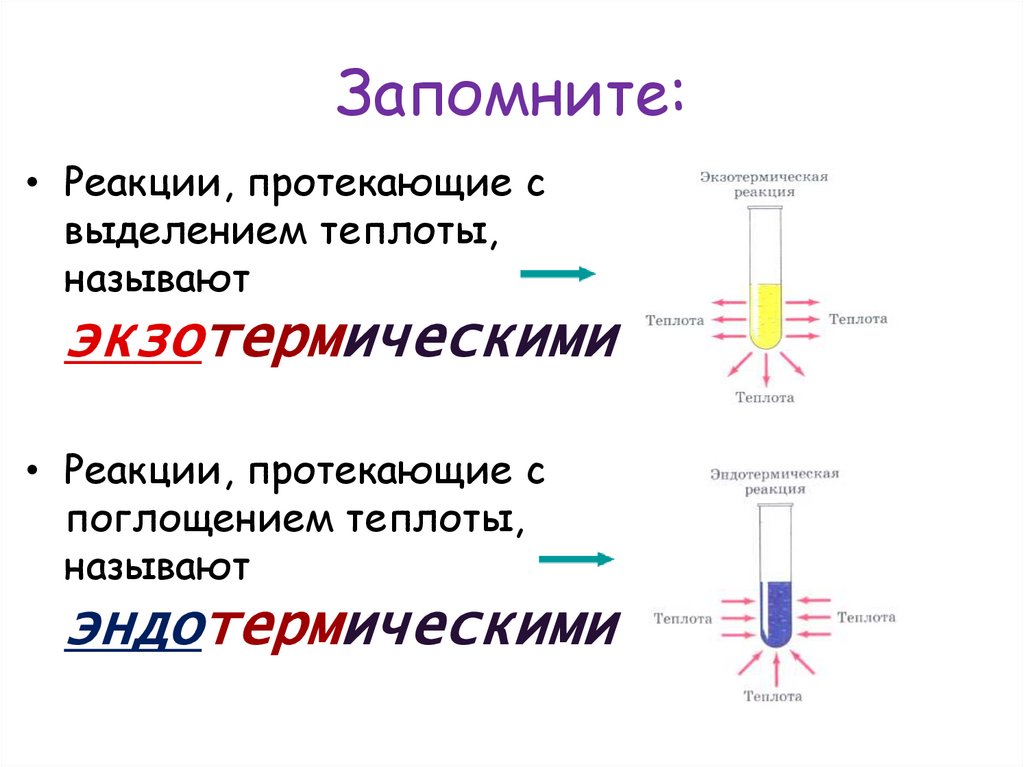
12. Запомните:
• Реакции, протекающие свыделением теплоты,
называют
экзотермическими
• Реакции, протекающие с
поглощением теплоты,
называют
эндотермическими
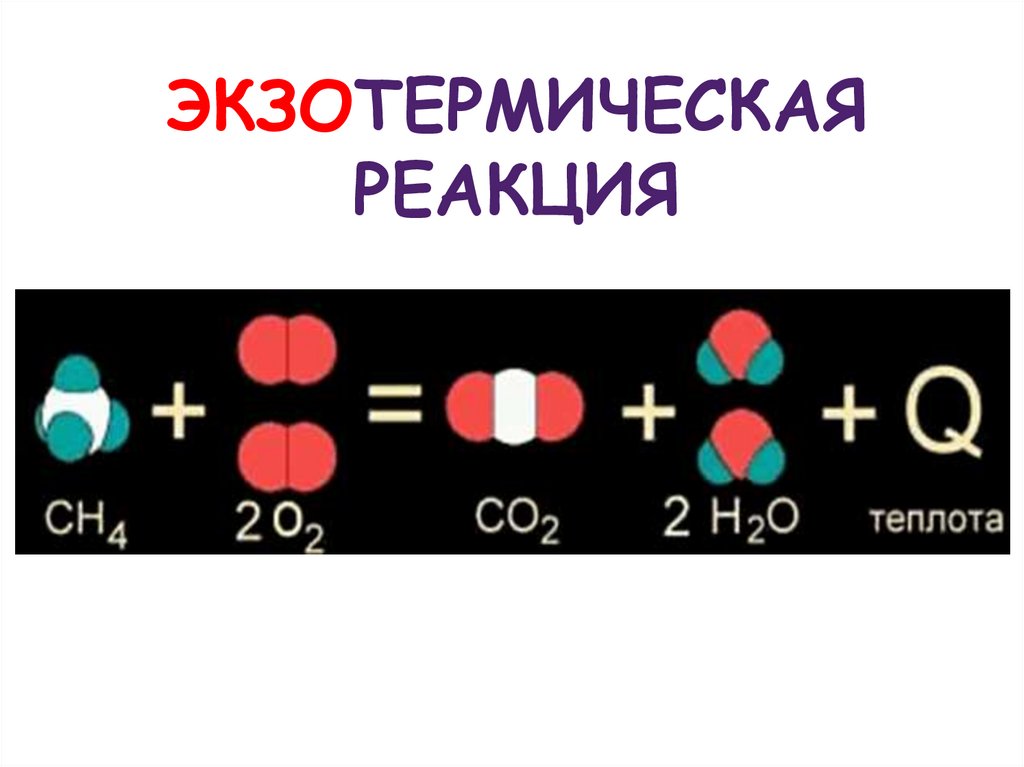
13. ЭКЗОТЕРМИЧЕСКАЯ РЕАКЦИЯ
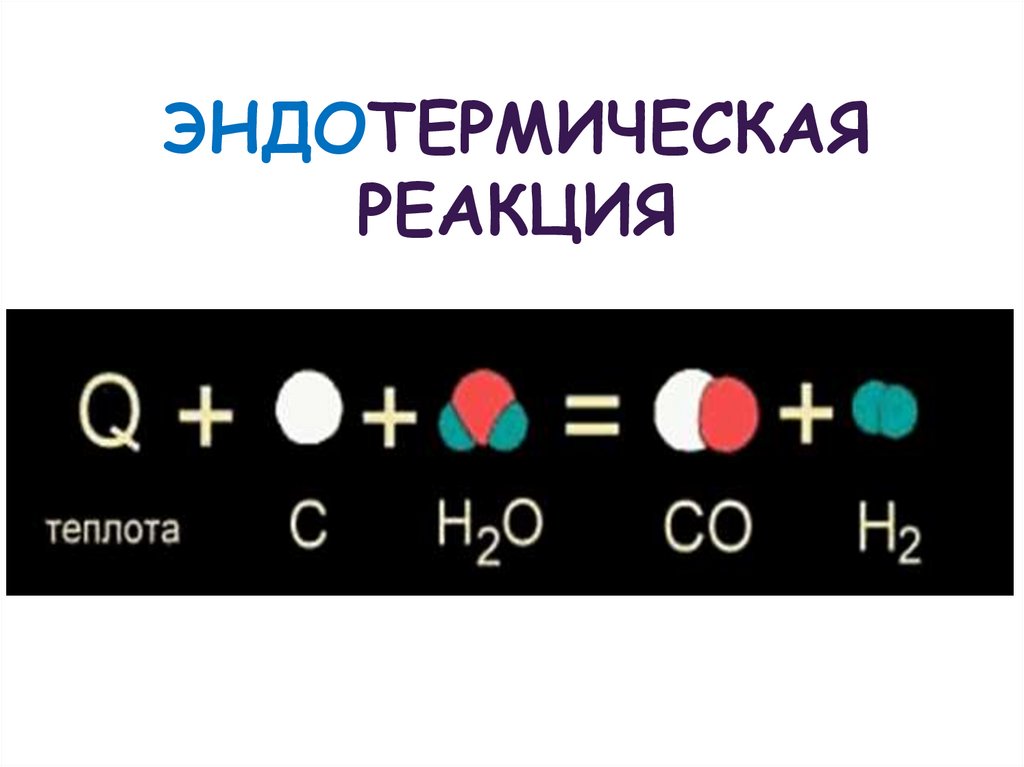
14. ЭНДОТЕРМИЧЕСКАЯ РЕАКЦИЯ
15. Любая химическая реакция сопровождается выделением или поглощением ЭНЕРГИИ!
16. Все реакции сопровождаются тепловыми эффектами.
,17. Тепловой эффект химической реакции Q- это количество теплоты, которое выделяется или поглощается при химических реакциях Дж;
кДж18. С(тв.) + О2(г.) СО2(г.) + 402,24кДж 2HgO(тв.)2Hg(ж.)+O2(г.) - 180 кДж
С(тв.) + О2(г.) СО2(г.) + 402,24кДж2HgO(тв.) 2Hg(ж.)+O2(г.) - 180
кДж
19. Химические уравнения, в которых указывается тепловой эффект, называются ТЕРМОХИМИЧЕСКИМИ
20.
Задания для закрепления• Повторить конспект
• Выполнить задания
1)Из следующего перечня формул веществ выписать только формулы оксидов.NaCl,
Al2O3, HN O3, KOH, P2 O5, CH4, H2SO4, CO2, Cu (OH)2, Cl2O7,
2)Определить валентность элементов по формулам оксидов:
N2O, NO, N2O3, NO2, N2O5, SO3
3)Составить формулы оксидов: магния (II), железа (III), серы (IV), бора (III), хрома
(VI).
4) Продолжить уравнения реакций
а) Zn + O2→
б) Al + O2→
в) H2S + O2→










 chemistry
chemistry








