Similar presentations:
Презентация ПЗ на тему ЦТК ЦПЭ (1)
1.
Аэробное дихотомическоеокисление глюкозы , этапы
(цикл трикарбоновых кислот).
Биологическое окисление (ЦПЭ)
2. Вопросы для самоподготовки
1. Тканевое дыхание (определение). Этапы тканевого дыхания и роль.2. Этапы аэробного дихотомического окисления глюкозы.
3. В каком органоиде клетки локализованы ферменты ЦТК и тканевого дыхания?
4. Какие реакции ЦТК являются энергопоставляющими и почему? Приведите примеры.
5. Биологическая роль ЦТК.
6. Какие вещества являются ингибиторами ЦТК? Приведите примеры, укажите тип
ингибирования.
7. Макроэрг (определение). Примеры макроэргов.
8. Что такое цепь терминального окисления (определение), каков смысл ее работы?
9. Строение НАД+, ФАД, цитохромов и их функциональная роль системе тканевого дыхания.
10. Состав компонентов дыхательной цепи, особенности их строения, роль.
11. Укажите звенья в цепи терминального окисления, сопряженные с синтезом АТФ.
12. Хемиосмотическая теория Митчелла, ее положения и сущность. Как происходит
образование АТФ в дыхательной цепи? Как называется тип образования АТФ в дыхательной
цепи?
13. Коэффициент эффективности тканевого дыхания Р/О, чему он может быть равен в
интактной клетке?
14. Разобщение окисления и фосфорилирования, факторы его вызывающие. Биологическая
роль. Механизм действия разобщителей.
15. Примеры ингибиторов дыхательной цепи. Механизм действия ингибиторов.
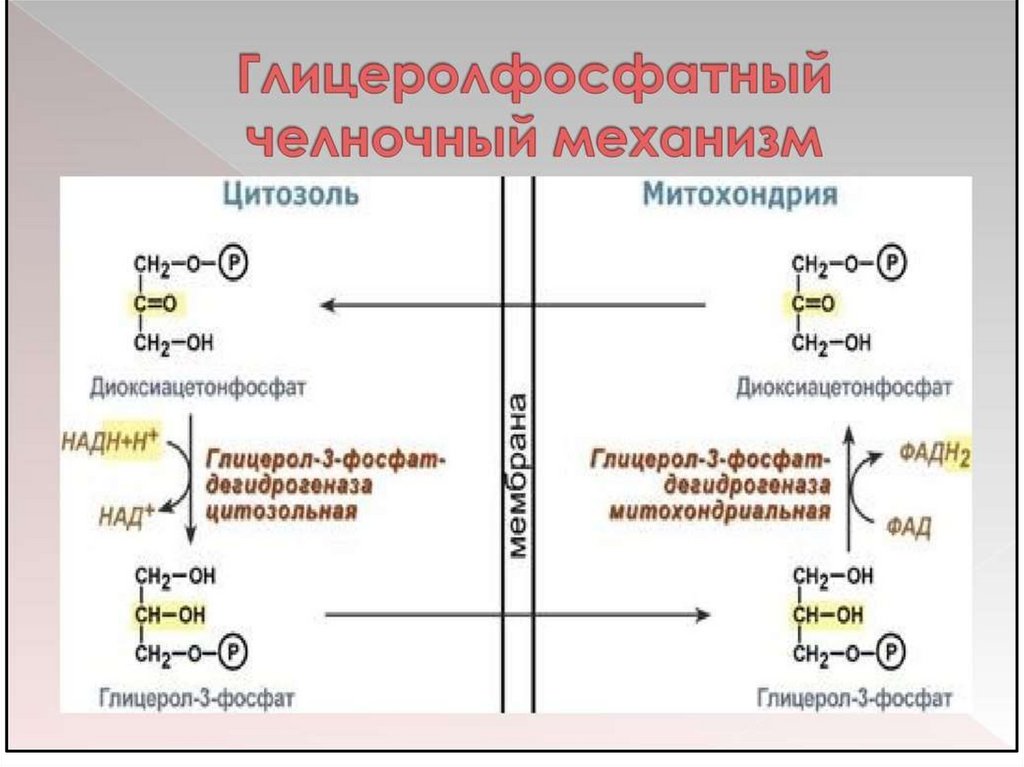
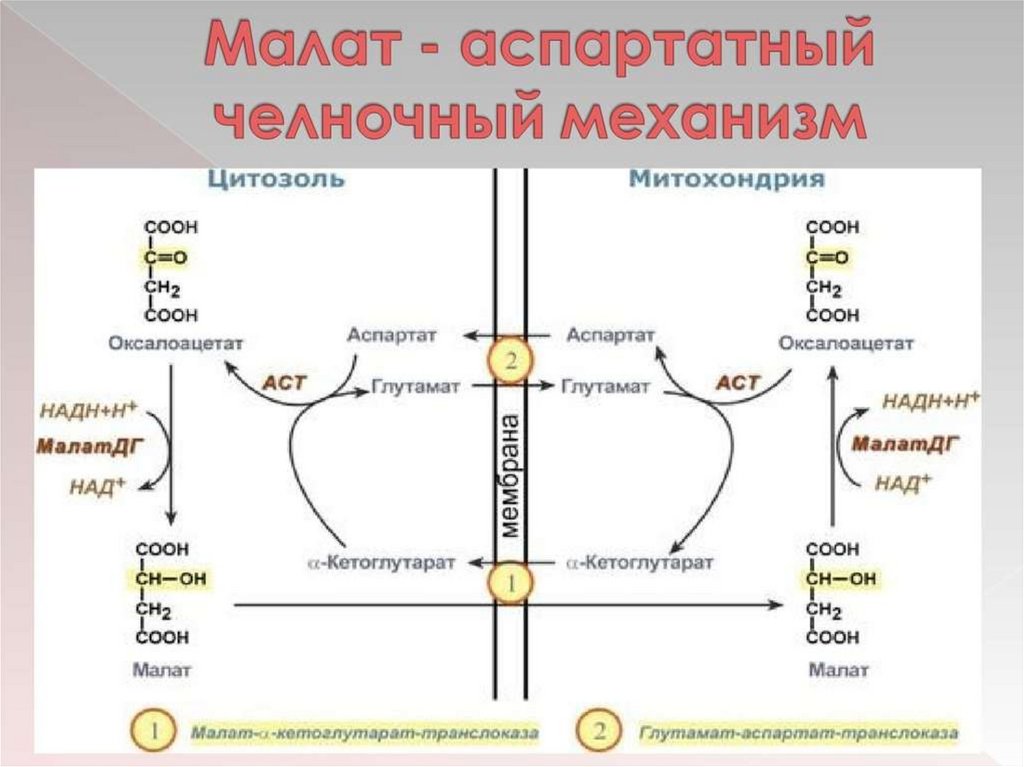
16. Челночные механизмы переноса водорода из цитоплазмы в митохондрии
(глицеролфосфатный, малатаспартатный).
17. Энергетический выход окисления глюкозы в аэробных условиях.
3. Рекомендуемая литература
Основная
Биохимия: учебник для вузов / под ред. Е.С. Северина. –
М.: ГЭОТАР-МЕД, 2015. – С. 262-293
Дополнительная
Березов Т.Т. Биологическая химия / Т.Т. Березов, Б.Ф.
Коровкин. - М.: Медицина, 1998. - С. 305-315, 345- 352
Электронные ресурсы:
Биохимия [Электронный ресурс]: учебник / под ред. Е.
С. Северина. - 5-е изд., испр. и доп. - М.: ГЭОТАРМедиа, 2015. - http://www.studmedlib.ru / book /
Биологическая химия с упражнениями и задачами
[Электронный ресурс] / под ред. С.Е. Северина - М.:
ГЭОТАР-Медиа, 2014. - http://www.studmedlib.ru / book /
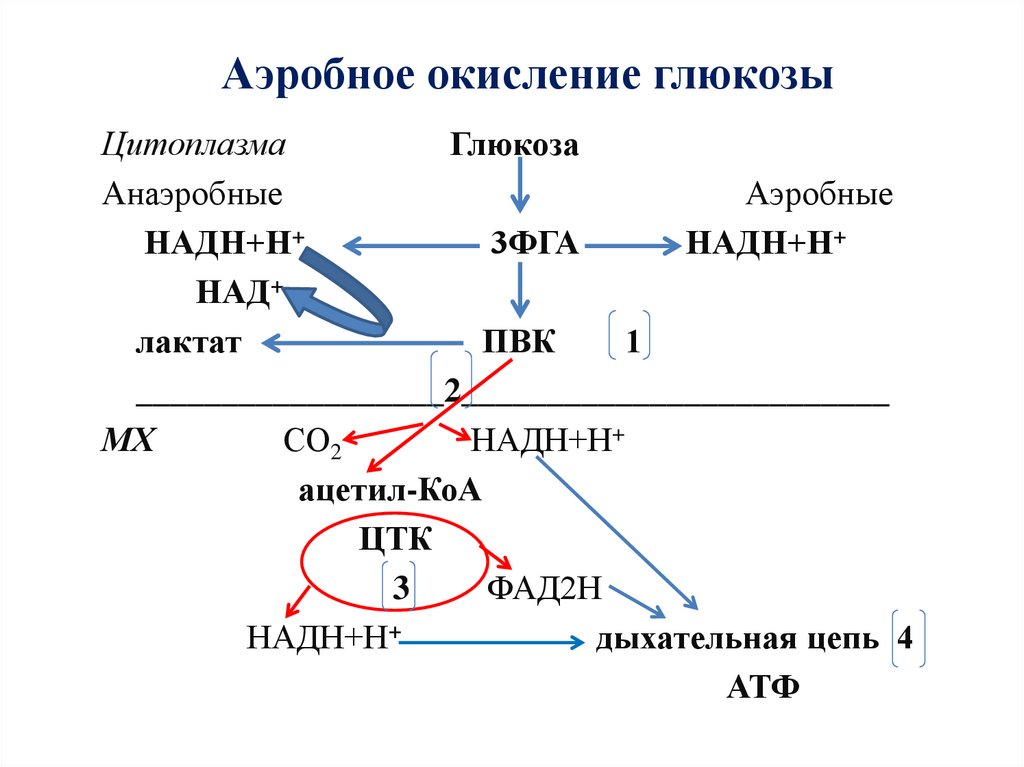
4. Аэробное окисление глюкозы
ЦитоплазмаГлюкоза
Анаэробные
Аэробные
НАДН+Н+
3ФГА
НАДН+Н+
НАД+
лактат
ПВК
1
__________________2_________________________
МХ
СО2
НАДН+Н+
ацетил-КоА
ЦТК
3
ФАД2Н
НАДН+Н+
дыхательная цепь 4
АТФ
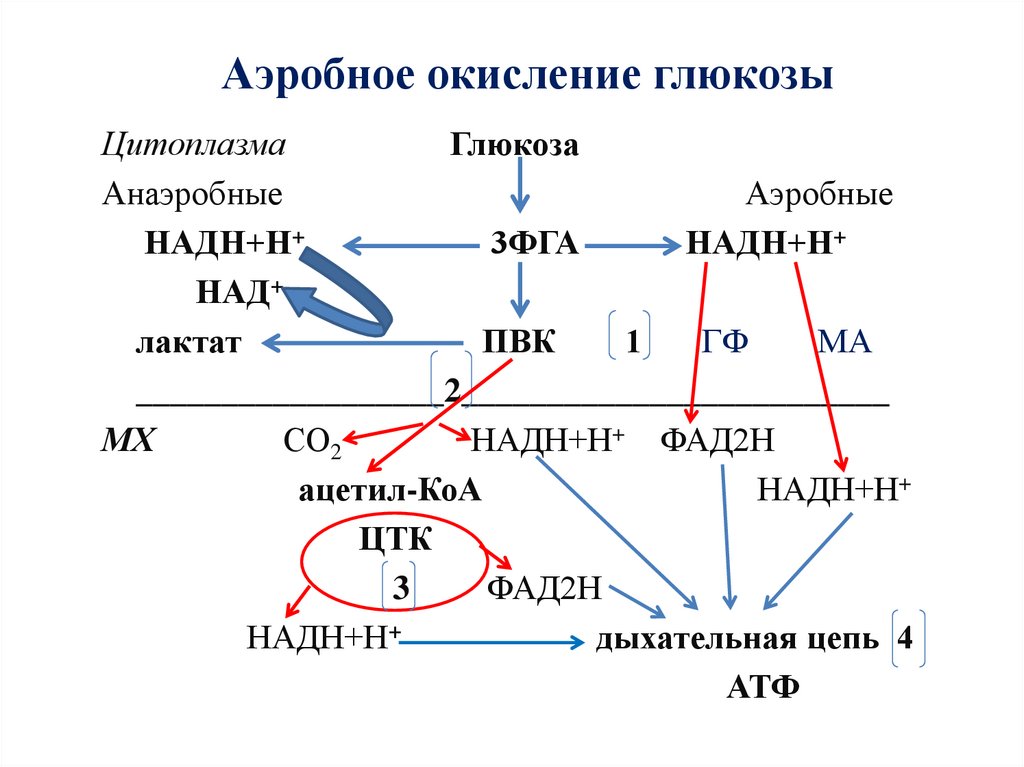
5. Аэробное окисление глюкозы
ЦитоплазмаГлюкоза
Анаэробные
Аэробные
НАДН+Н+
3ФГА
НАДН+Н+
НАД+
лактат
ПВК
1
ГФ
МА
__________________2_________________________
МХ
СО2
НАДН+Н+ ФАД2Н
ацетил-КоА
НАДН+Н+
ЦТК
3
ФАД2Н
НАДН+Н+
дыхательная цепь 4
АТФ
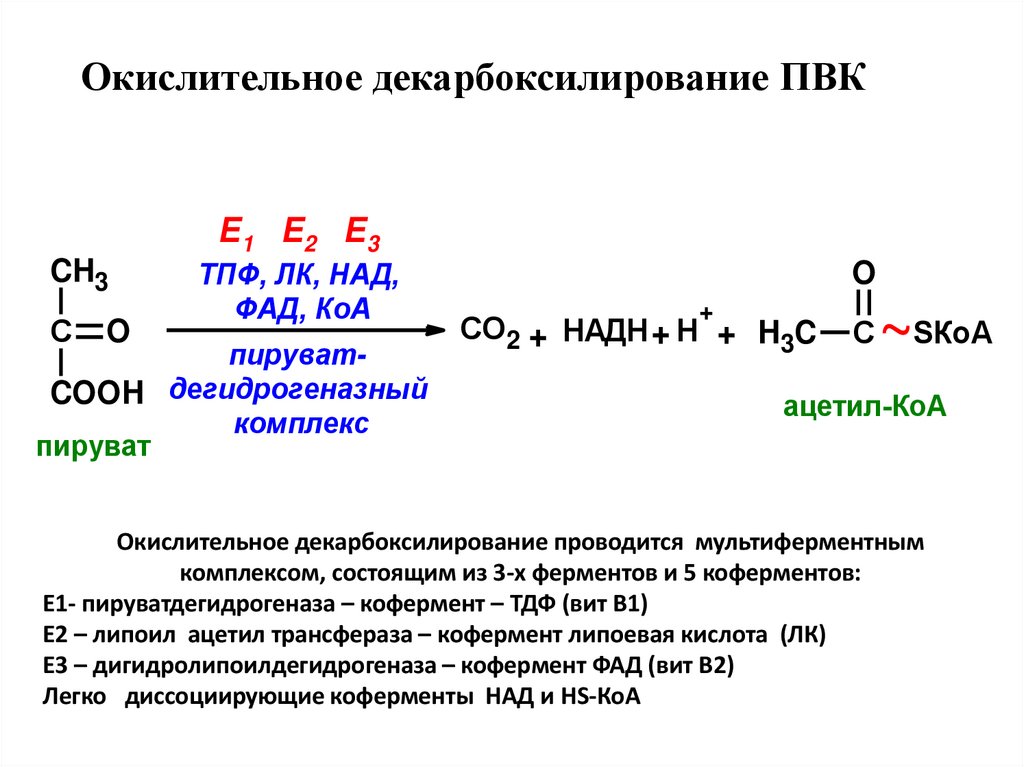
6. Окислительное декарбоксилирование ПВК
Е1 Е2 Е 3CH3
С
O
ТПФ, ЛК, НАД,
ФАД, КоА
пируватCOOH дегидрогеназный
комплекс
пируват
O
+
СО2 + НАДН + Н + H3C
С
~SКоА
ацетил-КоА
Окислительное декарбоксилирование проводится мультиферментным
комплексом, состоящим из 3-х ферментов и 5 коферментов:
Е1- пируватдегидрогеназа – кофермент – ТДФ (вит В1)
Е2 – липоил ацетил трансфераза – кофермент липоевая кислота (ЛК)
Е3 – дигидролипоилдегидрогеназа – кофермент ФАД (вит В2)
Легко диссоциирующие коферменты НАД и HS-КоА
7.
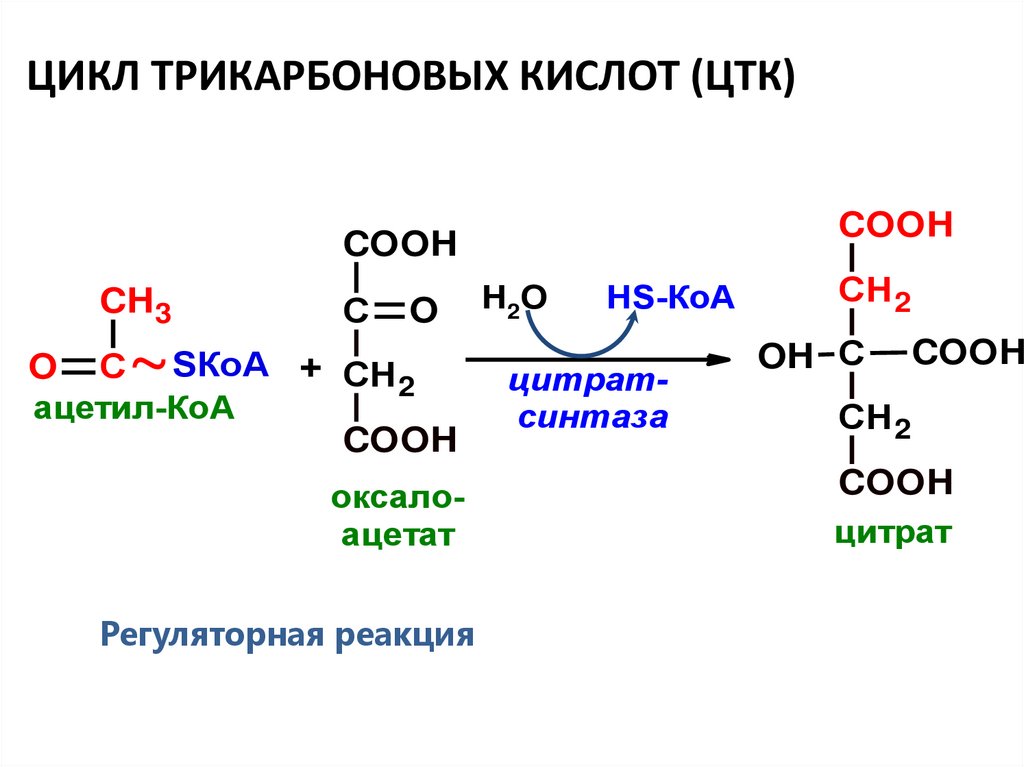
ЦИКЛ ТРИКАРБОНОВЫХ КИСЛОТ (ЦТК)COOH
COOH
CH3
С
O
~
ацетил-КоА
O
С
SКоА + СН
2
COOH
оксалоацетат
Регуляторная реакция
Н2О
НS-КоА
цитратсинтаза
СН 2
OH С
COOH
СН 2
COOH
цитрат
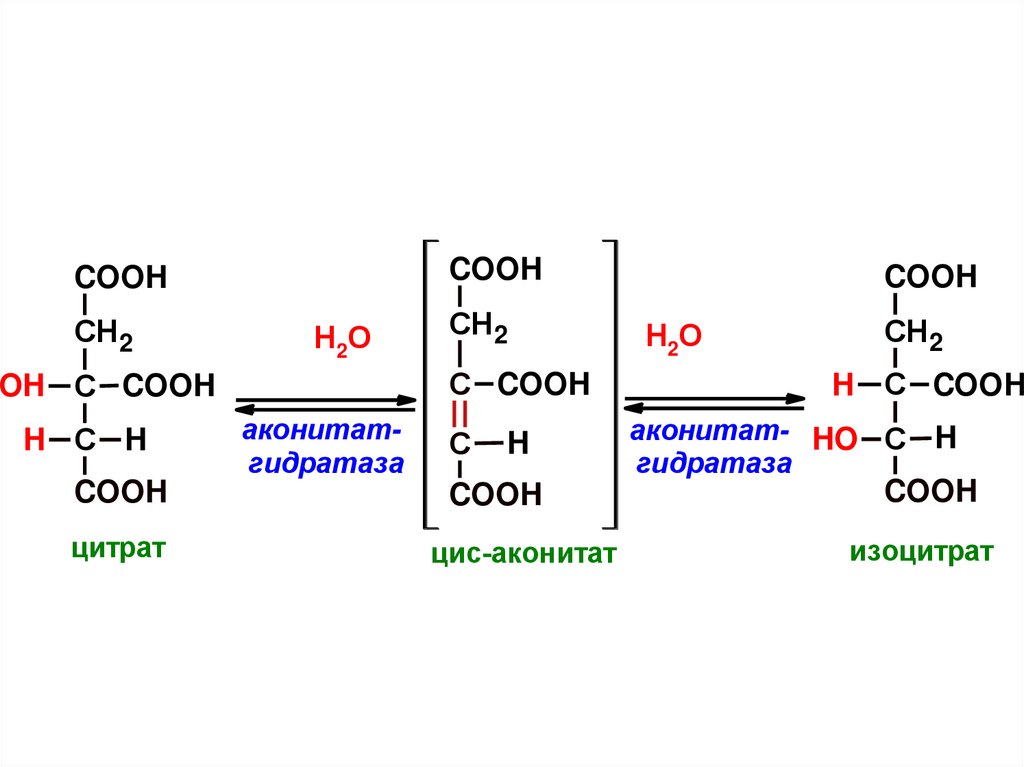
8.
COOHCOOH
СН 2
Н2О
С COOH
OH С COOH
H С H
СН 2
аконитатгидратаза
С
H
COOH
COOH
цитрат
цис-аконитат
COOH
Н2О
СН 2
H С COOH
аконитат- HO С H
гидратаза
COOH
изоцитрат
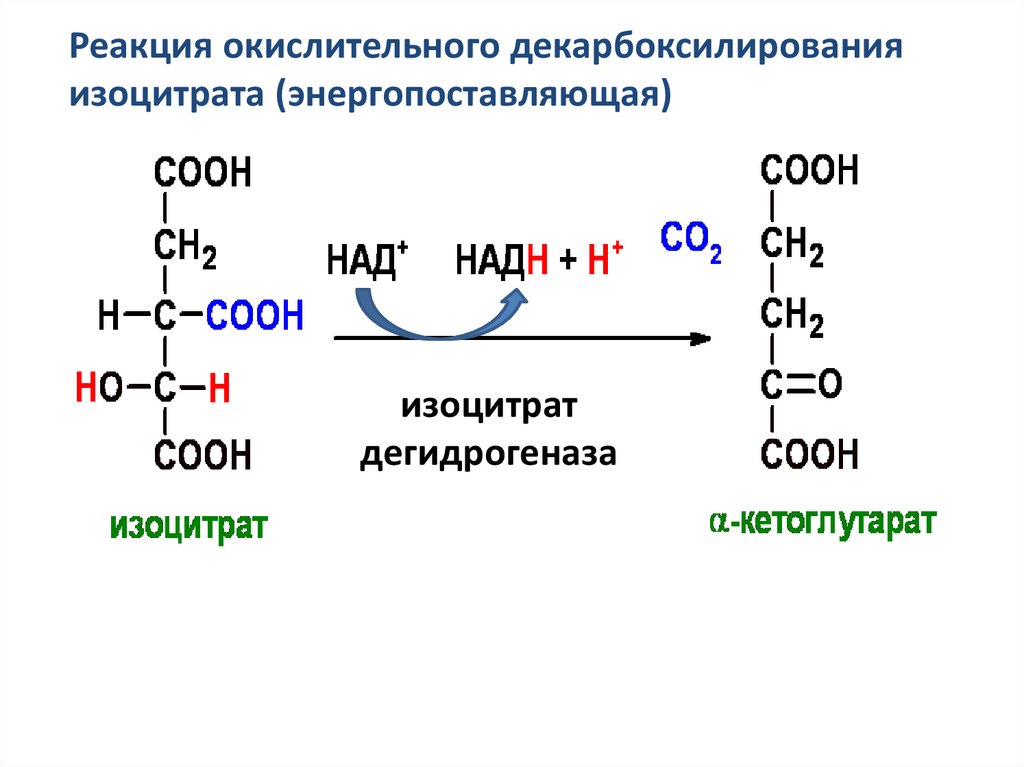
9.
Реакция окислительного декарбоксилированияизоцитрата (энергопоставляющая)
изоцитрат
дегидрогеназа
10.
COOHСН2
KоА
НАД+
СН2
С O
COOH
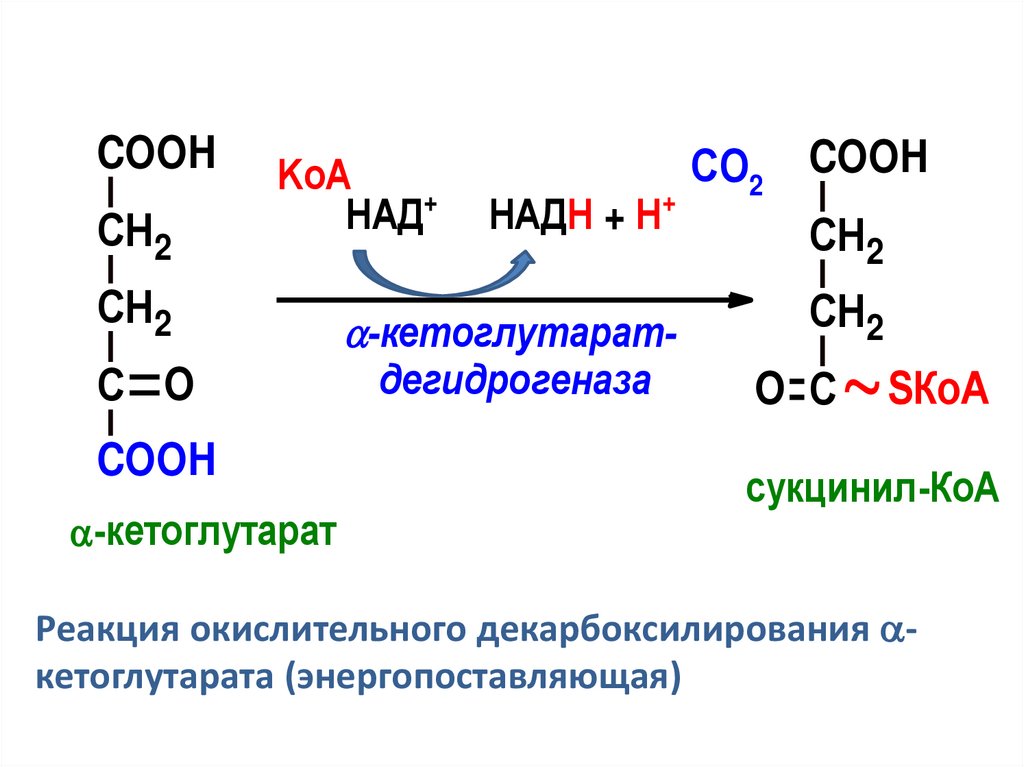
-кетоглутарат
НАДН + Н+
-кетоглутаратдегидрогеназа
СО2
COOH
СН2
СН2
O С
~SКоА
сукцинил-КоА
Реакция окислительного декарбоксилирования кетоглутарата (энергопоставляющая)
11.
COOHСН2
СН2
COOH
ФАД
ФАДН2
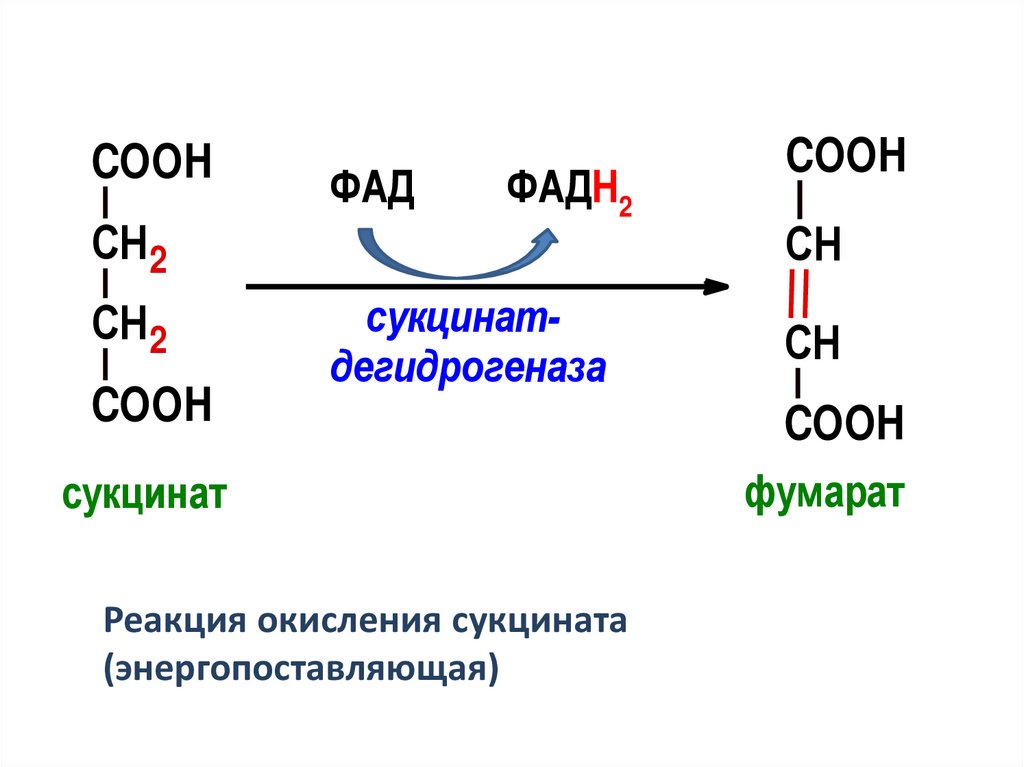
сукцинатдегидрогеназа
сукцинат
Реакция окисления сукцината
(энергопоставляющая)
COOH
СН
СН
COOH
фумарат
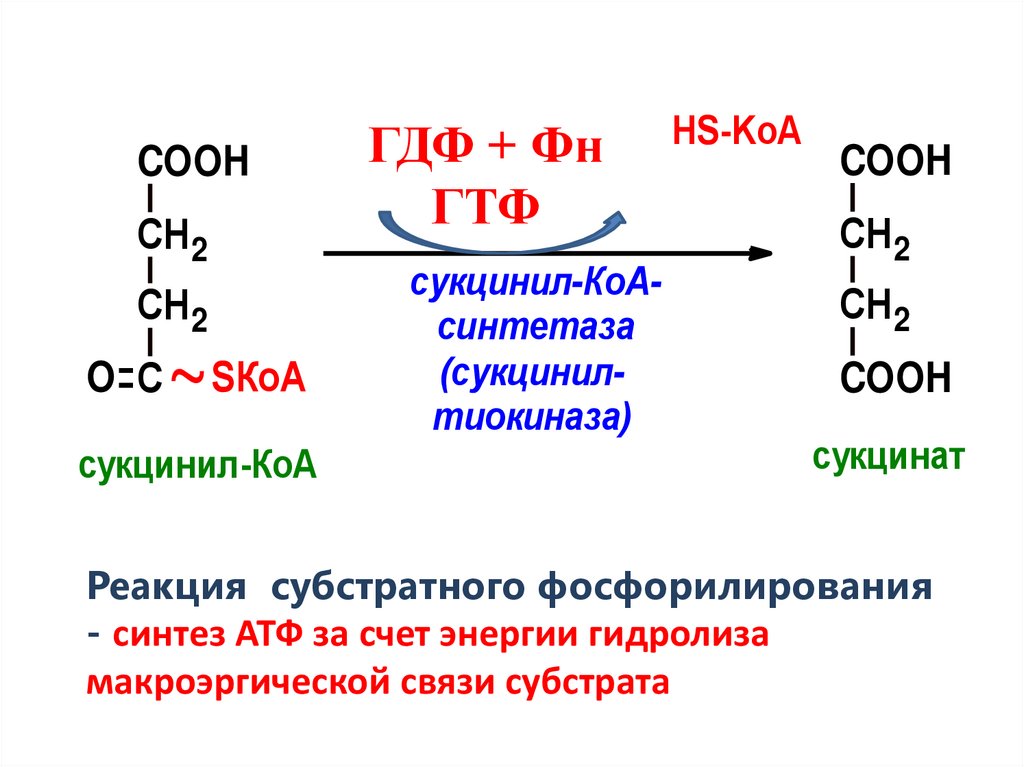
12.
COOHСН 2
СН 2
O С
~SКоА
сукцинил-КоА
ГДФ + Фн НS-KоА COOH
АДФ + НР АТФ
ГТФ
СН
сукцинил-КоАсинтетаза
(сукцинилтиокиназа)
2
СН 2
COOH
сукцинат
Реакция субстратного фосфорилирования
- синтез АТФ за счет энергии гидролиза
макроэргической связи субстрата
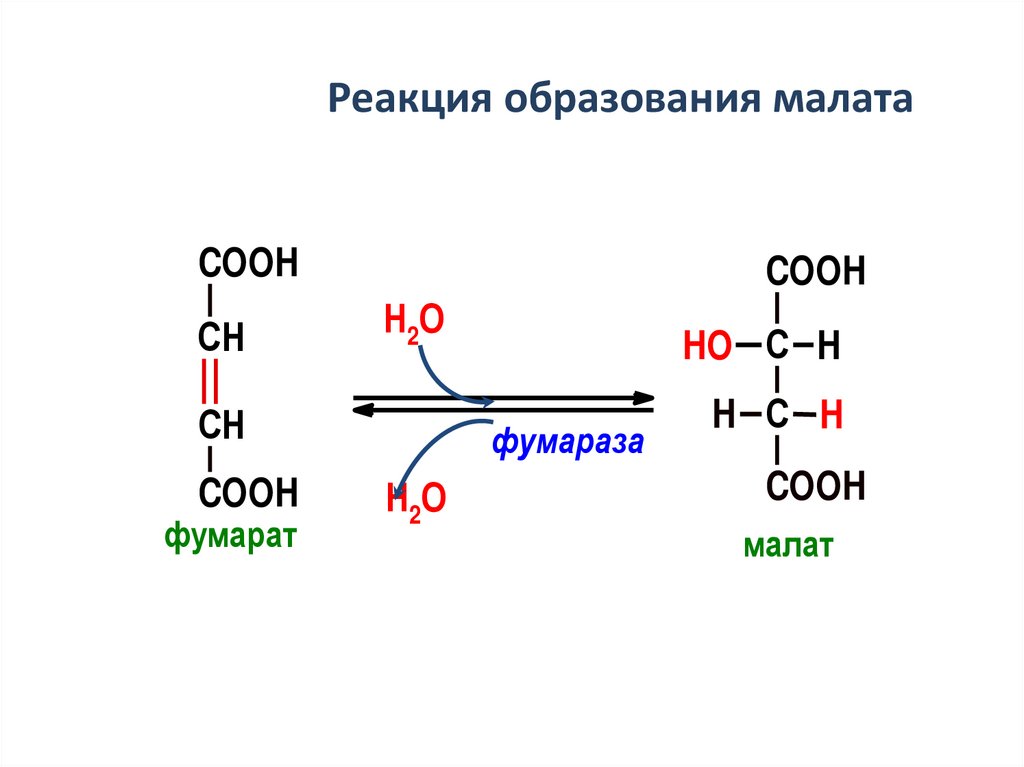
13.
Реакция образования малатаCOOH
СН
COOH
Н2О
СН
COOH
фумарат
HO С H
фумараза
Н2О
H С H
COOH
малат
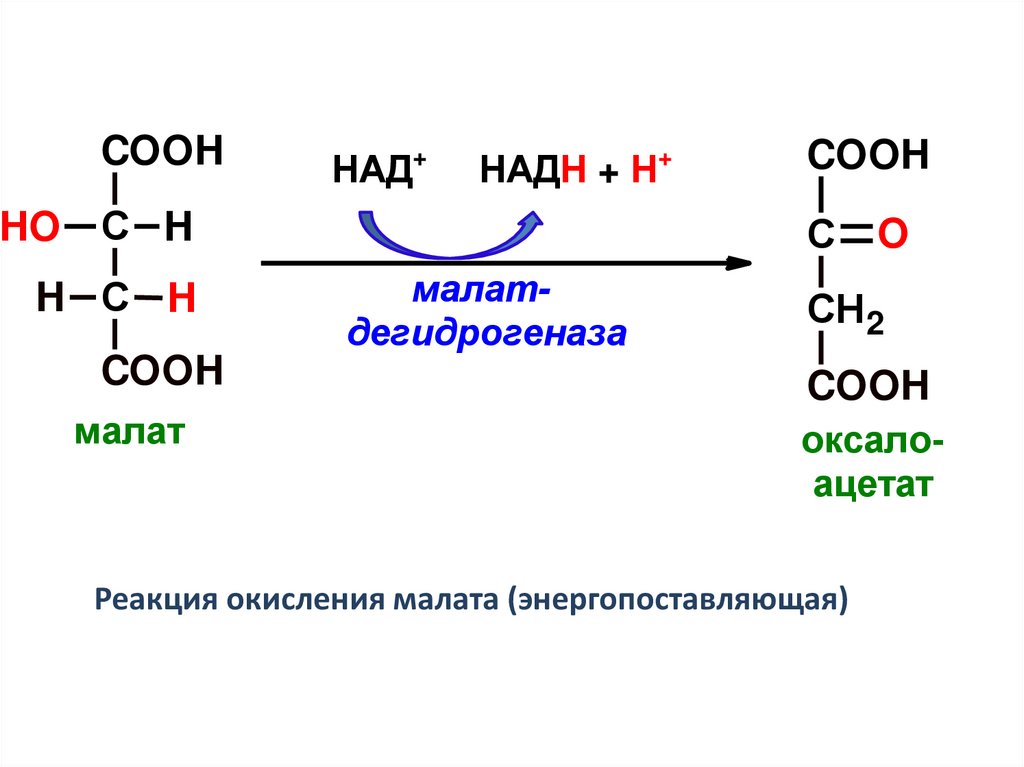
14.
COOHНАД+
НАДН + Н+
HO С H
H С H
COOH
малат
COOH
С
малатдегидрогеназа
O
СН 2
COOH
оксалоацетат
Реакция окисления малата (энергопоставляющая)
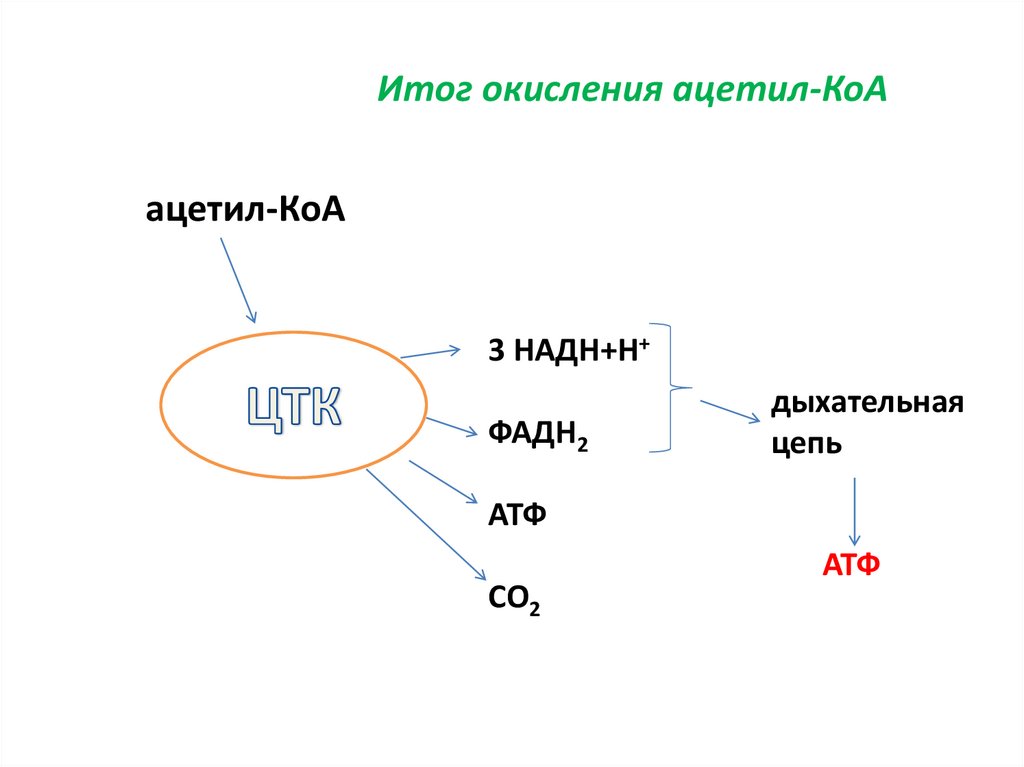
15.
Итог окисления ацетил-КоАацетил-КоА
3 НАДН+Н+
ФАДН2
дыхательная
цепь
АТФ
СО2
АТФ
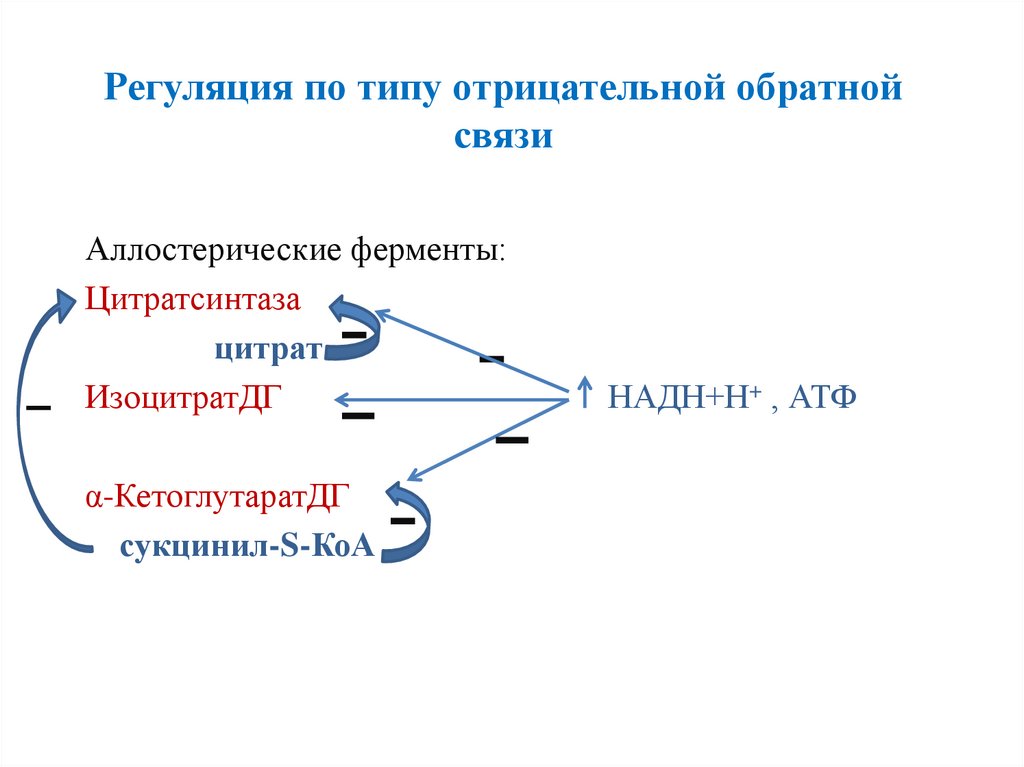
16. Регуляция по типу отрицательной обратной связи
Аллостерические ферменты:Цитратсинтаза
цитрат
ИзоцитратДГ
α-КетоглутаратДГ
сукцинил-S-КоА
НАДН+Н+ , АТФ
17.
Роль ЦТК1. Энергетическая – восстановленные коферменты
(3 НАДН+Н и 1 ФАД2Н) поступают в ЦПЭ, где
образуется основное количество АТФ посредством
окислительного фосфорилирования + 1 АТФ
образовалась непосредственно в ЦТК
2. Объединяет углеводный, липидный и белковый
обмены за счет наличия общих метаболитов:
ацетил-КоА, оксалоацетата, α-кетоглутарата, фумарата
3. Пластическая – метаболиты ЦТК могут
использоваться для реакций синтеза: оксалоацетат –
для синтеза аспартата, α-кетоглутарат – для синтеза
глутамата, сукцинил-КоА для синтеза гема, ацетил-КоА
переносится в цитоплазму и используется для синтеза
липидов
18.
Ингибиторы ЦТК1. Тиоловые яды – ингибиторы дегидрогеназ,
содержащих SH- группы в активном центре
2. Ингибирование по типу летального синтеза – при
попадании в организм фторацетата из него
синтезируется фторцитрат – необратимый ингибитор
аконитатгидратазы
3. Обратимое конкурентное ингибирование
сукцинатдегидрогеназы малонатом
4. Метаболические аллостерические регуляторы –
высокая концентрация АТФ, НАДН+Н, подавляют
активность дегидрогеназ и цитратсинтазы по
механизму отрицательной обратной связи.
19.
Биологическое окисление или тканевоедыхание – окисление органических
соединений, сопровождающееся
потреблением О2 для образования АТФ с
выделением СО2 и воды.
20.
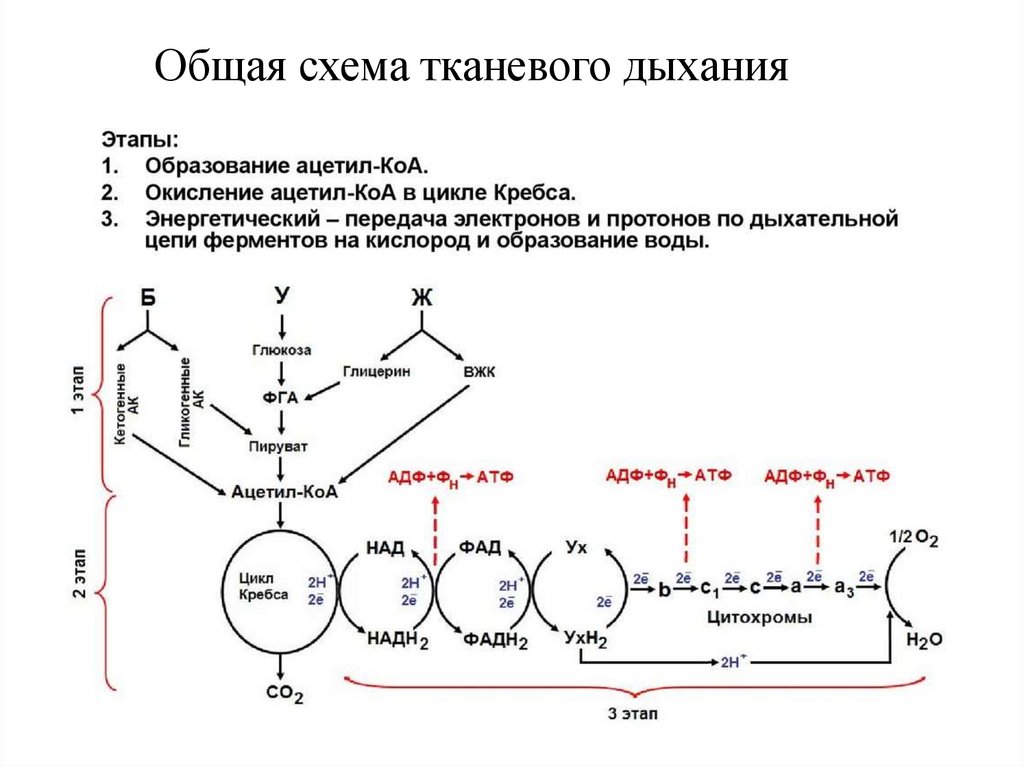
Общая схема тканевого дыхания21.
● Синтез АТФ происходит в реакцияхфосфорилирования, но самостоятельно протекать не
может, а только с использованием свободной энергии
(полезной энергии)
● АДФ + ФН → АТФ (∆G> -30,5 кДж/моль)
● Макроэргическое соединение – соединение,
стандартная свободная энергия гидролиза которого
равна -30,5 кДж/моль или более «-»
22.
Типы образования АТФ23.
Субстратноефосфорилирование
Окислительное
фосфорилирование
Синтез АТФ за счет энергии
гидролиза макроэргической связи
субстрата:
1,3-дифосфоглицерат (∆G - 54
кДж/моль)
фосфоенолпируват (∆G - 62
кДж/моль)
креатинфосфат (∆G - 43 кДж/моль)
глюкозо-6-фосфат (∆G - 14
кДж/моль)
Более энергетически
выгодное
Синтез АТФ происходит за
счет энергии переноса ℮ в
дыхательной цепи путем
сопряжения процессов
окисления и
фосфорилирования
24.
Субстратное фосфорилирование25.
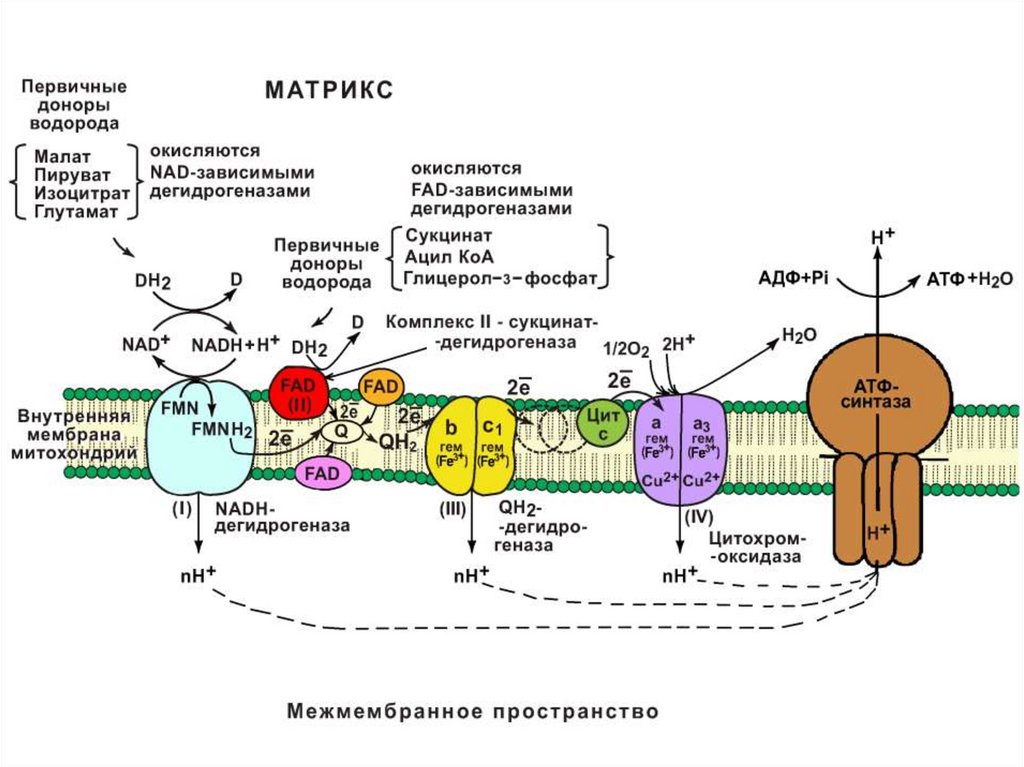
Строение дыхательной цепи● Дыхательная цепь - это каскад окислительновосстановительных ферментов, расположенных во внутренней
мембране митохондрий, участвующих в переносе ℮ от
восстановленных коферментов на О2 (℮- транспортная цепь).
● Все компоненты ДЦ расположены в соответствии со своим
окислительно-восстановительным потенциалом (это
способность принимать и отдавать ℮).
● Первым компонентом является НАДН и он принимает ℮ и
Н+ от субстратов с помощью НАД-зав. ДГ и выполняет
коллекторную функцию.
26.
27.
● ФП1 – флавопротеин 1− НАДН-дегидрогеназа принимает 2℮ ,2Н+; флавинзависимая ДГ имеет простетическую группу ФМН
и железосерный комплекс, в которых Fe связано с атомом серы
через SH-группы цистеина (негемовое Fe).
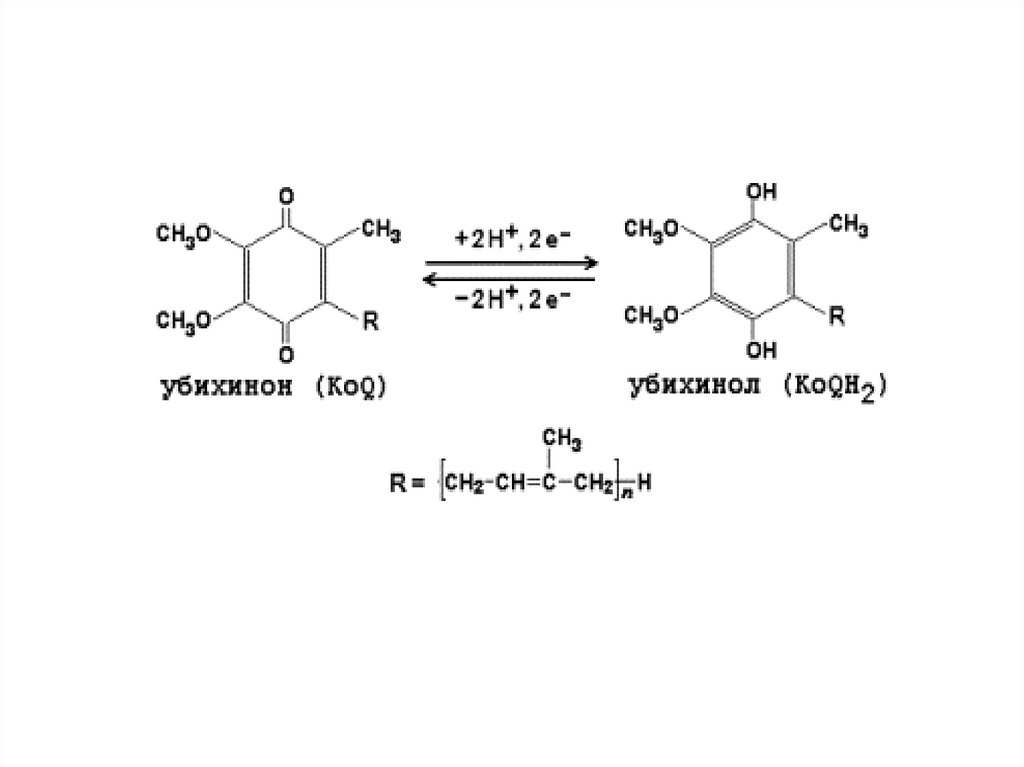
● Следующий переносчик ℮ – убихинон или Q10
жирорастворимый хинон содержащий 10 остатков изопрена
(синтезируется в организме, но с возрастом его синтез
снижается). Убихинон выполняет коллекторную функцию и
принимает ℮ и Н+ от ФАД – зависимых ДГ и превращается в
востановленную форму - убихинол
● Убихинол передает ℮ на систему цитохромов, а 2Н+ протона
перекачивает из матрикса митохондрий (перенос каждой пары
℮ 2℮ сопровождается выкачиванием 4Н+).
28.
29.
● Цитохромы – сложные белки, содержащиепростетическую группу гем, которая принимает и
отдает ℮ (гемовое Fe2+). Fe3+гем → Fe2+гем
● Последний цитохром аа3 наз. Цитохромоксидаза,
передает ℮ на О2.
● Цит. аа3 содержит 2 молекулы гема и 2 атома Cu+.
℮
℮
● Fe3+гем → Fe2+гем
Cu2+ → Cu+
● Все ферменты ДЦ расположены в соответствии со
своим ок-восс. потенциалом – (т.е. способностью
принимать и отдавать ℮). Электроны движутся от
электро «-» потенциала к О2 (электро «+»
потенциалом).
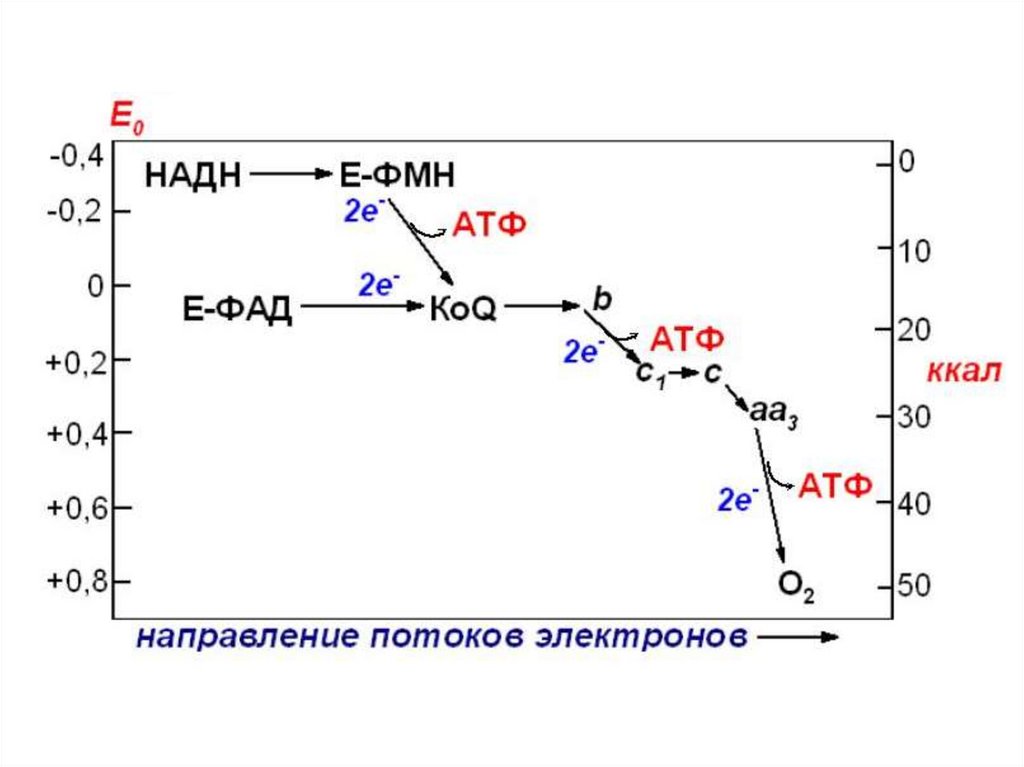
30.
31.
● На участках перепада ок.-в. потенциала придвижении ℮ выделяется полезная свободная
энергия, которая на 55% рассеивается в виде тепла,
а 45% используется на синтез АТФ. Эти участки ДЦ
называются участками сопряжения окисления и
фосфорлирования и тип образования АТФ
называется окислительным фосфорилированием.
● Энергетический выход
● В полной цепи при окислении НАДН − 3 АТФ
● В короткой цепи при окислении ФАД2Н – 2 АТФ
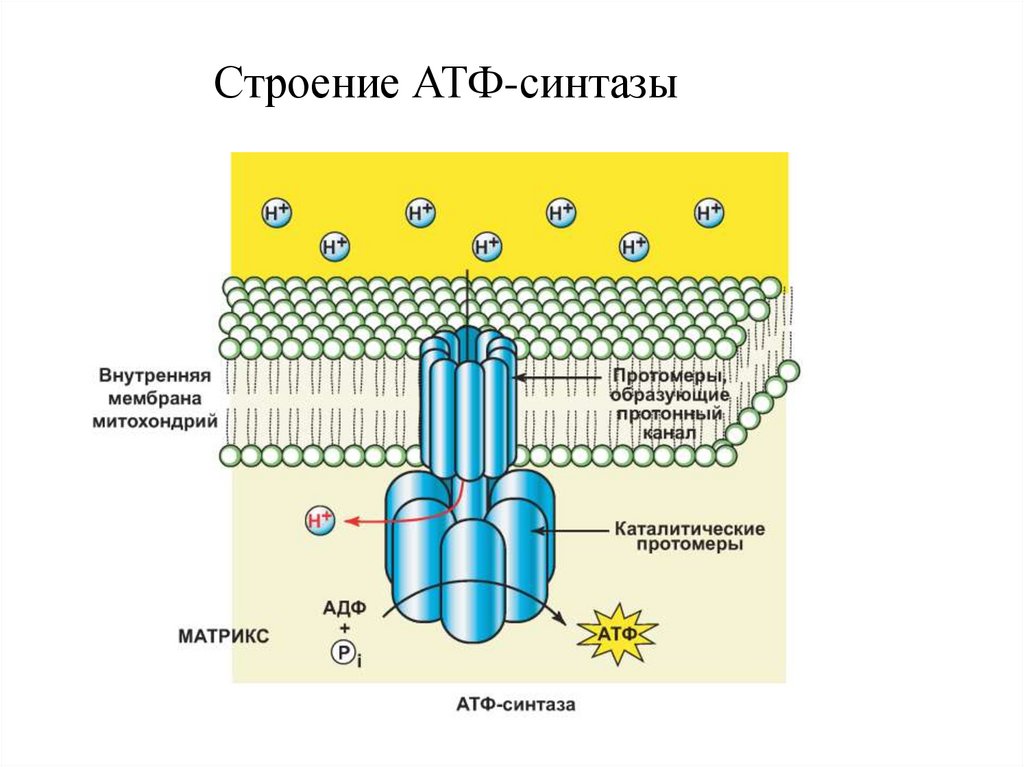
32.
Строение АТФ-синтазы33.
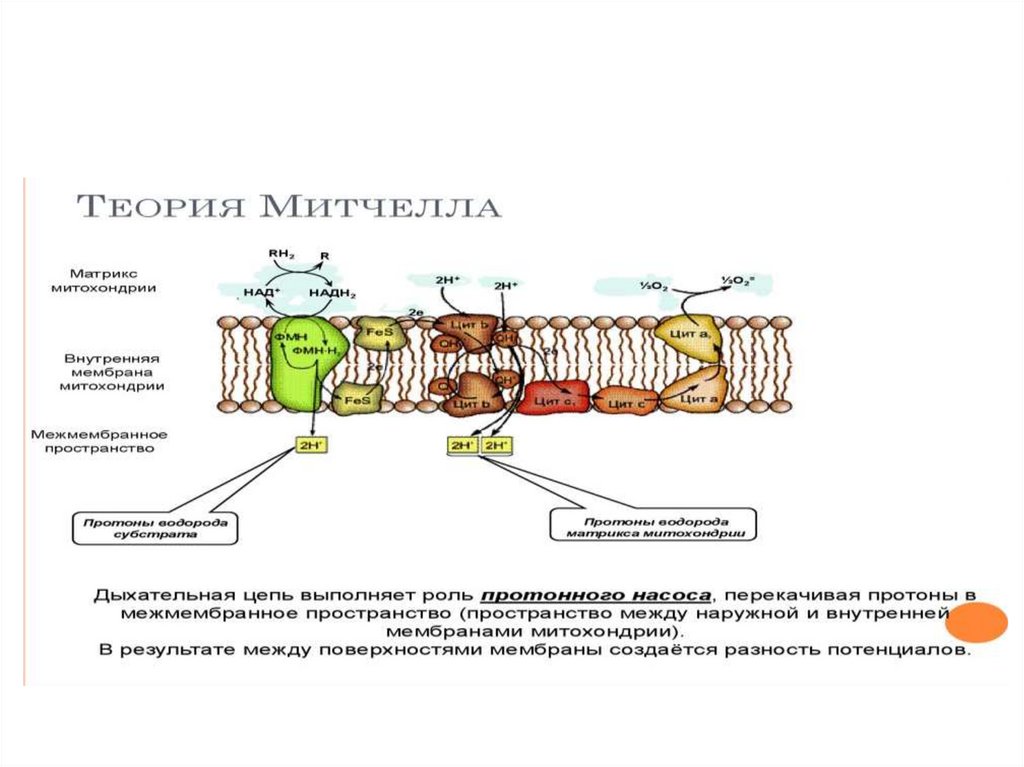
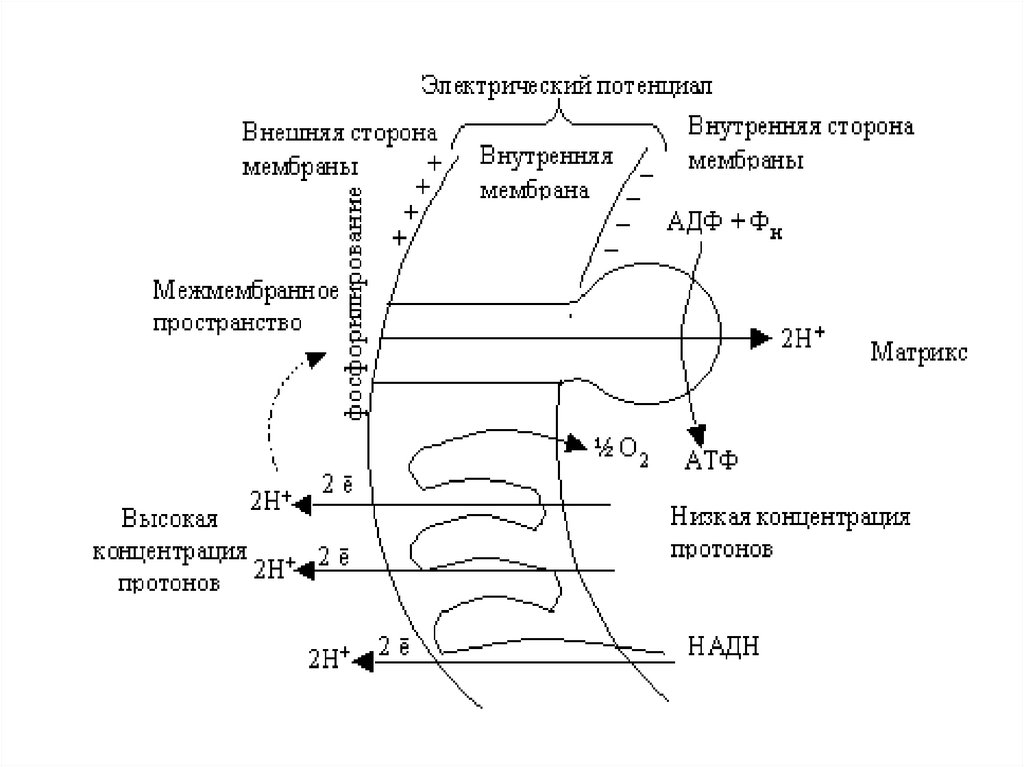
Хемиосмотическая теория МитчеллаСопряжение окисления и фосфорилирования
(Нобелевская премия в 1978 г.)
● Мембрана мх должна быть интактной, целостной.
● Мембрана мх д.б. непроницаемой для Н+ и
катионов.
● На мембране образуется электрохимический
потенциал, необходимый для работы АТФ-синтетазы
● В процессе синтеза АТФ имеет место сопряжение
окисления и фосфорилирования.
34.
35.
36.
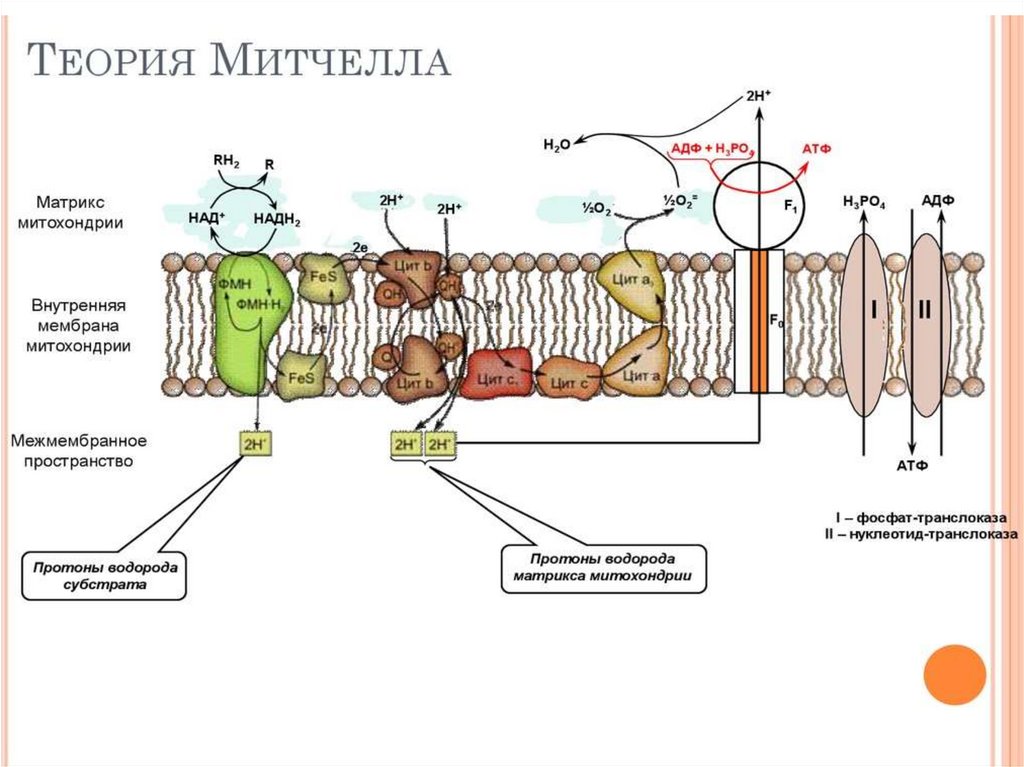
37.
● Перенос 2℮ по ДЦ на О2 сопровождается выкачиванием2Н+ протонов из матрикса в межмембранное пространство,
возникает трансмембранный потенциал - это разность
заряда и рН среды ( μН+). Протоны проходят через АТФ −
синтазу (протонный канал) и одновременно с образованием
АТФ образуется вода 1/2О2+2Н+ → Н2О.
● АТФ − синтаза использует полезную энергию и
катализирует реакцию фосфорилирования
АДФ +Фн → АТФ.
● Это осуществляется путем сопряжения окисления и
фосфорилирования. Если мембрана повреждена Н+
проходят в матрикс мх, минуя АТФ-синтазу, μН+
потенциал падает АТФ не образуется эффект называется
разобщением окисления и фосфорилирования
38.
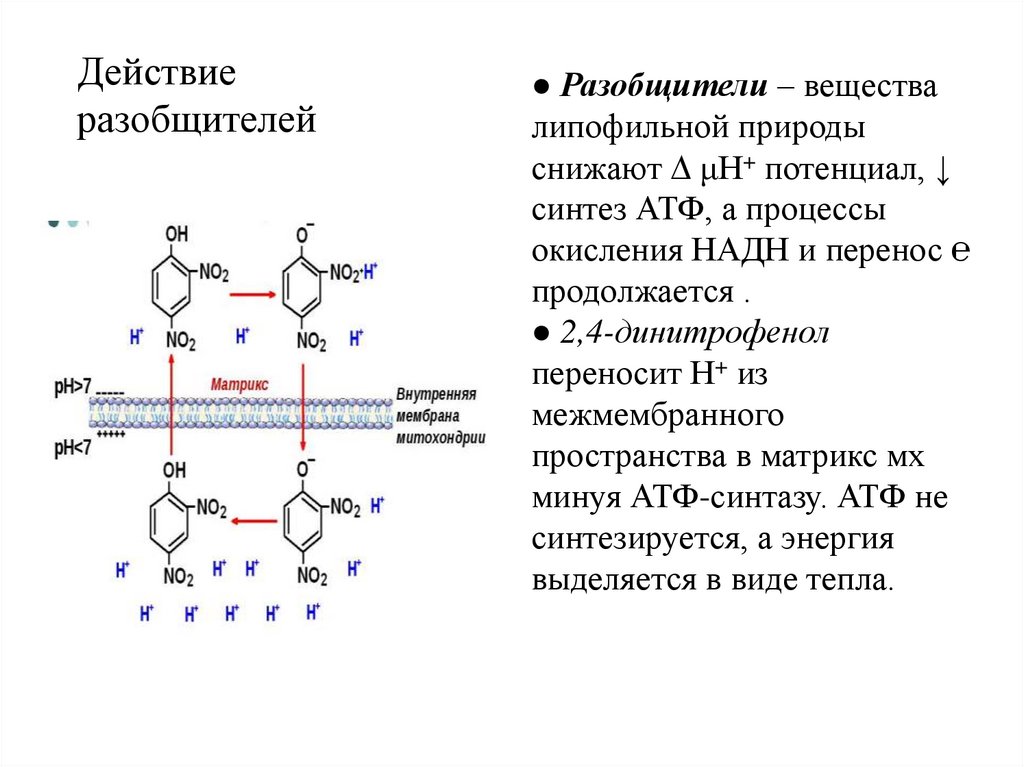
Действиеразобщителей
● Разобщители – вещества
липофильной природы
снижают μН+ потенциал, ↓
синтез АТФ, а процессы
окисления НАДН и перенос ℮
продолжается .
● 2,4-динитрофенол
переносит Н+ из
межмембранного
пространства в матрикс мх
минуя АТФ-синтазу. АТФ не
синтезируется, а энергия
выделяется в виде тепла.
39.
40.
Разобщители дыхательной цепи● Ионофоры переносят катионы, снижают μН+
и синтез АТФ.
● Дикумарол (Са2+), грамицидин (Са2+),
валиномицин (К+), нигерицин (К+)
● Активные формы кислорода нарушают
проницаемость мембраны и вызывают эффект
разобщения.
℮
℮
● 1/2 О2 → О2•− → Н2О2
41.
Разобщение дыхания и окислительногофосфорилирования
42.
Факторы, повышающие эффективностьработы ДЦ
● Глицерофосфолипиды как структурный
компонент клеточной мембраны мх.
● КоQ и препараты убихинола
●Антиоксиданты витамины Е, С, А и др.
43.
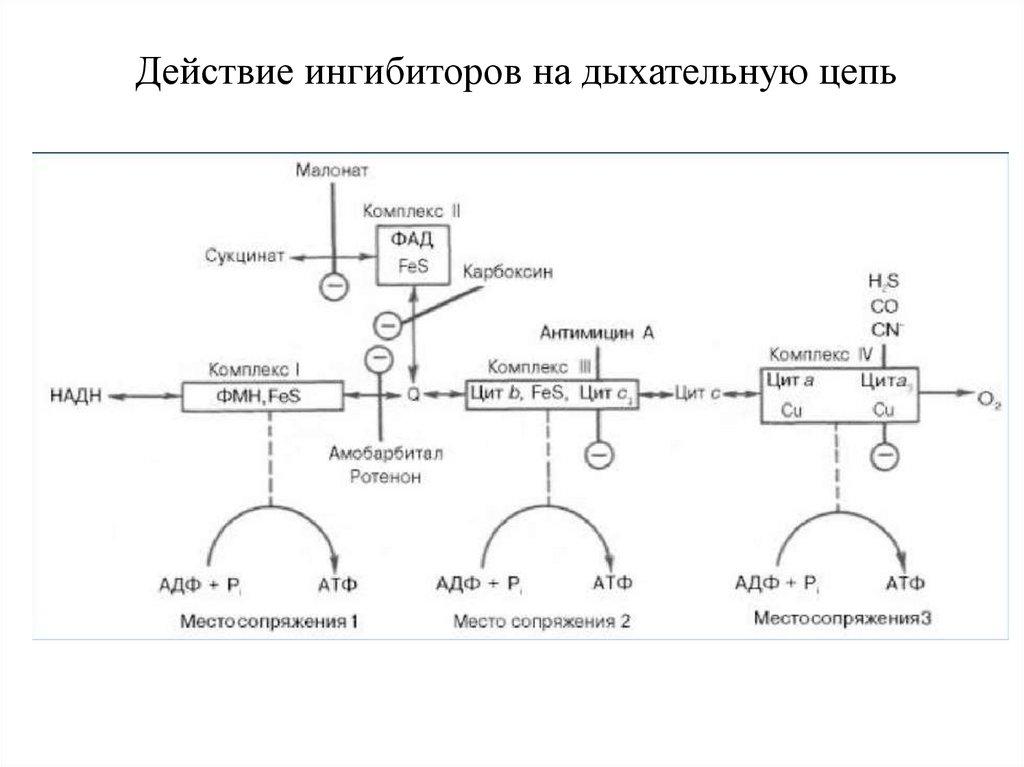
Ингибиторы дыхательной цепиИнгибиторы действуют на точки сопряжения окисления и
фосфорилирования
● ФМН – [ Fe-S ] — барбитураты (амитал), ротенон
(токсичное в-во некоторых водорослей), ацетальдегид
(метаболизм алкоголя)
Блокируют перенос ℮ на О2 и синтез АТФ. В данной
ситуации возможно запустить короткую дыхательную цепь
с использованием сукцината.
● цит b → цит с1 — антибиотик антимицин А
Наиболее опасное действие ингибиторов
●цит аа3 — CN- , СО, Н2S блокируется перенос ℮ на О2,
снижается выработка АТФ, возникает гипоксия вплоть до
летального исхода.
44.
Действие ингибиторов на дыхательную цепь45.
46.
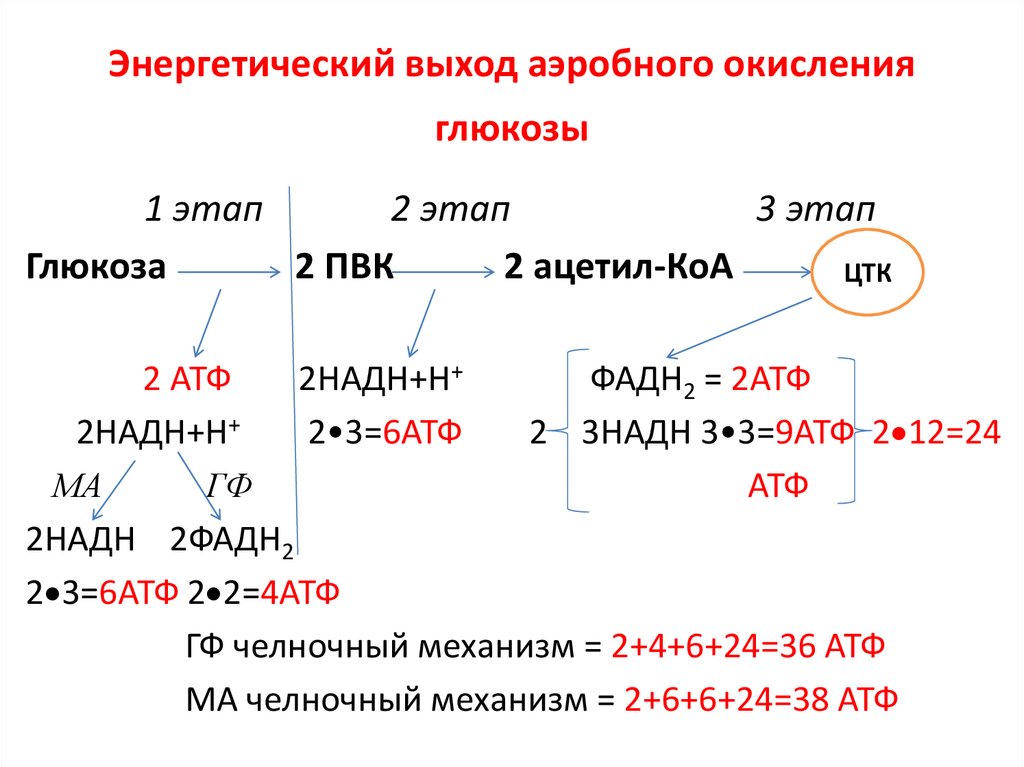
47. Энергетический выход аэробного окисления глюкозы
1 этап2 этап
3 этап
Глюкоза
2 ПВК
2 ацетил-КоА
ЦТК
ЦТК
2 АТФ
2НАДН+Н+
МА
ГФ
2НАДН+Н+
2•3=6АТФ
ФАДН2 = 2АТФ
2 3НАДН 3•3=9АТФ 2 12=24
АТФ
2НАДН 2ФАДН2
2 3=6АТФ 2 2=4АТФ
ГФ челночный механизм = 2+4+6+24=36 АТФ
МА челночный механизм = 2+6+6+24=38 АТФ





















 biology
biology








