Similar presentations:
https___school.mos.ru_ej_attachments_files_219_513_625_original_21%20%D0%A3%D0%A0%D0%9E%D0%9A.%209%20%D0%BA%D0%BB.%20%D0%A1%D0%9A%D0%9E%D0%A0%D0%9E%D0%A1%D0%A2%D0%AC%20%D0%A5%D0%98%D0%9C%20%D0%A0%D0%95%D0%90%D0% (1)
1.
2.
3.
4.
5.
6.
7.
8.
9.
Некоторые понятия химической кинетики.Химическая кинетика – раздел химии, изучаю-
щий скорость и механизмы химических реакций.
Гомогенные реакции – реакции, протекающие в
однородной среде (в растворе или газовой фазе)
во всем объеме реакционной смеси.
Гетерогенные реакции – реакции в неоднородных
системах, как правило, благодаря участию
твердого вещества. Реакция в таких системах
протекает на границе раздела фаз.
10. Что такое химические реакции?
*• Химические реакции – превращения одних веществ в
другие, отличающиеся по составу и (или)
строению. При химических реакциях обязательно
происходит изменение веществ, при котором
рвутся старые и образуются новые связи между
атомами.
Признаки химических реакций:
1) Выделяется газ; 2) Выпадет осадок;
3) Изменяется окраска веществ;
4) Выделяется или поглощается тепло, свет.
11.
Как оценить скорость реакции?*Скорость
гомогенной
реакции
определяется как
изменение
концентрации
одного из
веществ в
единицу времени:
C моль
V
(
)
t л * с
*Скорость
гетерогенной
реакции
определяется как
изменение
количества
вещества в единицу
времени на единице
поверхности:
n моль
V
(
)
2
t * S с * м
S — площадь поверхности соприкосновения веществ .
12. Факторы, влияющие на скорость химической реакции.
Природа реагирующих веществТемпература
Концентрация реагирующих веществ
Наличие катализатора (ингибитора)
Площадь поверхности
соприкосновения веществ
13.
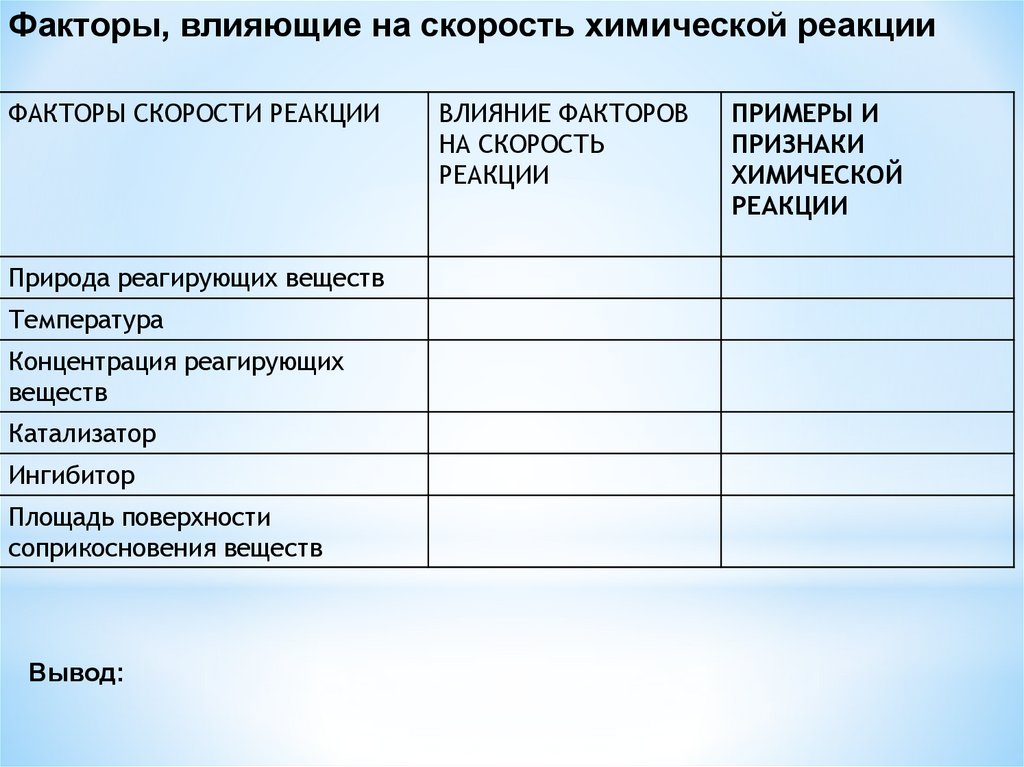
Факторы, влияющие на скорость химической реакцииФАКТОРЫ СКОРОСТИ
РЕАКЦИИ
ВЛИЯНИЕ ФАКТОРОВ
НА СКОРОСТЬ
РЕАКЦИИ
ПРИМЕРЫ И ПРИЗНАКИ
ХИМИЧЕСКОЙ
РЕАКЦИИ
14. Природа реагирующих веществ
**В каком случае реакция пойдет с бОльшей
скоростью:
Zn + HCl или
Zn + CH3COOH
В случае c HCl реакция пойдет быстрее, т.к.
соляная кислота – сильная, а уксусная – слабая.
Mg + HCl
или
Fe + HCl
В случае c Mg реакция пойдет быстрее, т.к.
магний более активный металл, чем железо.
15. Температура
*При повышении температуры в большинстве случаев
скорость химической реакции значительно увеличивается.
В прошлом веке голландский химик Я. Х. Вант-Гофф
сформулировал правило:
Повышение температуры на каждые 10 °С приводит к
увеличению скорости реакции в 2–4 раза (эту величину
называют температурным коэффициентом
реакции).
,
16. Концентрация реагирующих веществ
Для реакций с участием газообразных веществповышение давления в системе или уменьшение объема
равносильно повышению концентрации
реагирующих веществ.
2SO2 + О2 2 SO3 + Q
Пример: Если в реакции
давление в системе увеличить в 2 раза, то
скорость реакции возрастет в 8 раз.
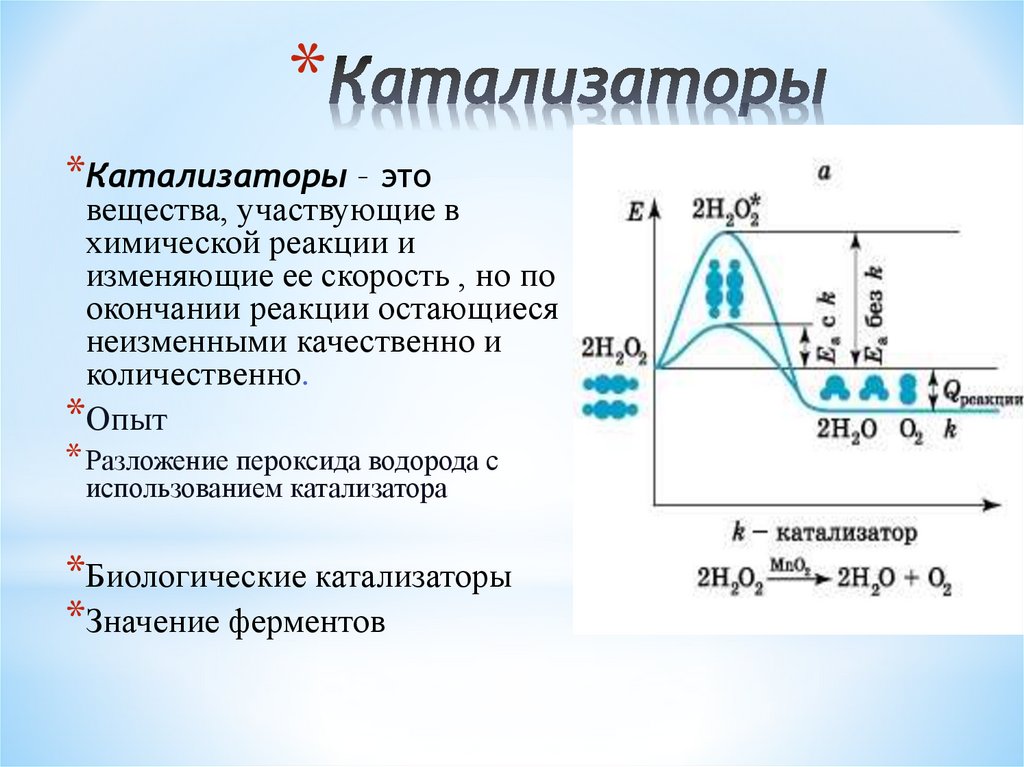
17. Катализаторы
**Катализаторы – это
вещества, участвующие в
химической реакции и
изменяющие ее скорость , но по
окончании реакции остающиеся
неизменными качественно и
количественно.
*Опыт
* Разложение пероксида водорода с
использованием катализатора
*Биологические катализаторы
*Значение ферментов
18. Катализаторы
*Ферменты – биологически активные катализаторы.
Используются в производстве детского питания, сыров,
хлебопечении, виноделии и пивоварении.
Нежелательные реакции необходимо замедлять. Для этого
используют вещества – ингибиторы.
19. Площадь соприкосновения реагирующих веществ
В производстве серной кислотыпри обжиге пирита
(серного колчедана)
4FeS2 + 11O2 = 2Fe2O3 + 8SO2
для увеличении поверхности
соприкосновения твердого
компонента с воздухом используют
принцип «кипящего слоя».
20.
Факторы, влияющие на скорость химической реакцииФАКТОРЫ СКОРОСТИ РЕАКЦИИ
Природа реагирующих веществ
Температура
Концентрация реагирующих
веществ
Катализатор
Ингибитор
Площадь поверхности
соприкосновения веществ
Вывод:
ВЛИЯНИЕ ФАКТОРОВ
НА СКОРОСТЬ
РЕАКЦИИ
ПРИМЕРЫ И
ПРИЗНАКИ
ХИМИЧЕСКОЙ
РЕАКЦИИ

















 chemistry
chemistry








