Similar presentations:
Влияние ионизирующих излучений на здоровье человека. Лекция 16
1. 06.04.2022
ЛЕКЦИЯ 16Влияние ионизирующих излучений на
здоровье человека
Байтимирова Марина Олеговна
2. Биологическое действие ионизирующих излучений
БИОЛОГИЧЕСКОЕ ДЕЙСТВИЕИОНИЗИРУЮЩИХ ИЗЛУЧЕНИЙ
Основной радиобиологический парадокс по определению
Н.В.Тимофеева-Ресовского, состоит в значительной диспропорции
между количеством поглощенной энергии ионизирующей радиации и
величиной вызванного ею биологического эффекта.
Смертельная для человека поглощенная доза - 10 Гр энергетически
эквивалентна приблизительно 170 кал
(количество тепловой энергии, которое передается человеку от выпитого стакана горячего
чая, вызывая повышение температуры тела всего на 0,001 °С).
Ионизирующие излучения обладают высокой биологической
активностью. Вызывают ионизацию любых химических соединений
биосубстратов и этим индуцировать длительно протекающие реакции
в живых тканях.
Результатом биологического действия радиации является, как
правило, нарушение нормальных биохимических процессов с
последующими функциональными и морфологическими
изменениями в клетках и тканях.
2
3. Развитие радиобиологических эффектов во времени
РАЗВИТИЕ РАДИОБИОЛОГИЧЕСКИХ ЭФФЕКТОВ ВО ВРЕМЕНИДлительность
процесса (сек)
10-15
Поглощение энергии
Возбуждение/ионизация
10-12
Исходные треки частиц
Формирование радикалов
10
-9
Диффузия, химические реакции
10-6
Первичное повреждение ДНК
10-3
1мс
100
1с
Разрывы ДНК/базовое повреждение
Процессы репарации
Фиксация повреждения
Гибель клеток
103
1ч
Мутации/трансформации/аберрации
1день
10
6
Физические взаимодействия: первичные процессы
поглощения энергии излучения атомами и молекулами
биологического объекта, в результате они могут
претерпевать возбуждение, ионизацию или диссоциацию
Физико-химические взаимодействия. Наиболее
типичные реакции и изменения: реакции окисления,
восстановления, деструкции (расщепление крупных
молекул, отщепление активных групп, разрывы цепей);
реакции димеризации (удвоенной молекулы в результате
реакции присоединения), полимеризации и другие
усложнения молекул; внутримолекулярные изменения.
Биологическая стадия. Действие ионизирующей
радиации на живые организмы может приводить к
нарушениям биологической организации на всех ее
уровнях, от молекулярного и клеточного до
организменного и популяционного.
Пролиферация поврежденных клеток
1год
Промоция/завершение
109
10лет
Тератогенез
Рак
Наследственные дефекты
Медицинские эффекты
являются следствием поглощения физической
энергии излучения и последующего индуцирования
изменений на молекулярном уровне.
3
4.
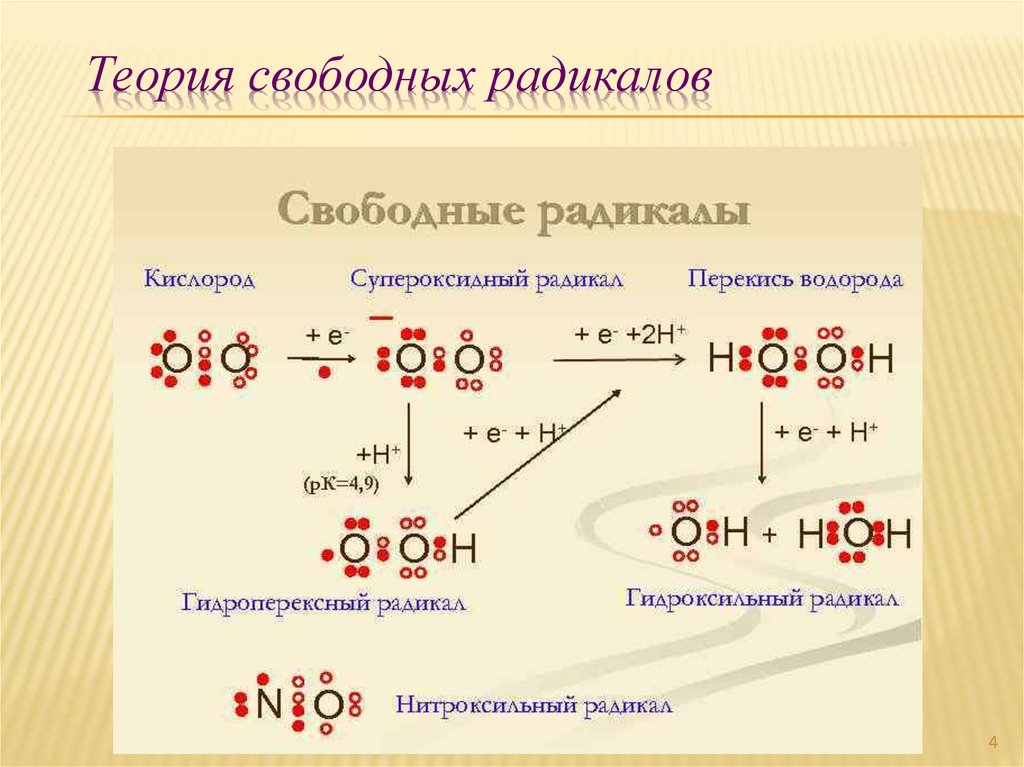
Теория свободных радикалов4
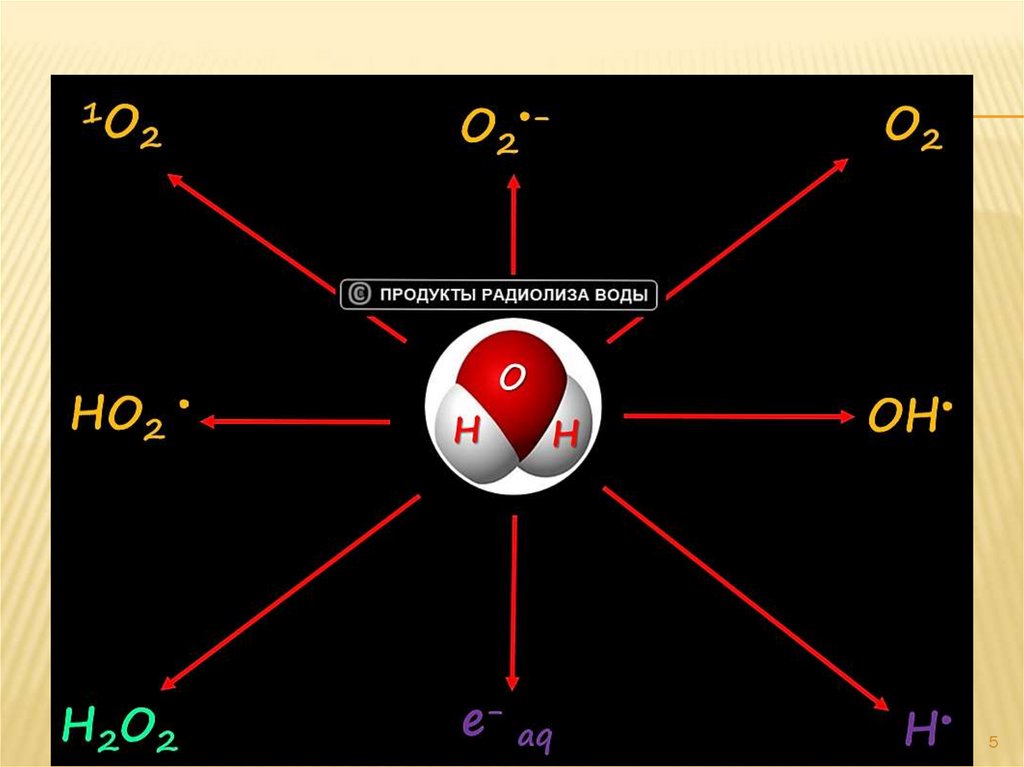
5.
56.
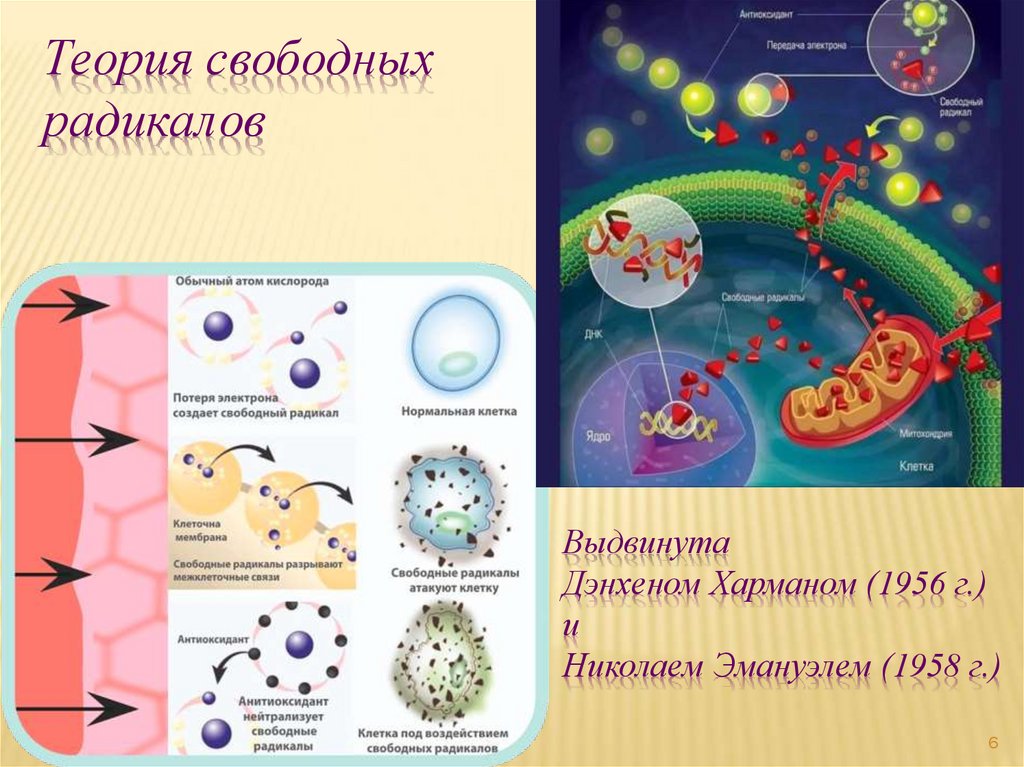
Теория свободныхрадикалов
Выдвинута
Дэнхеном Харманом (1956 г.)
и
Николаем Эмануэлем (1958 г.)
6
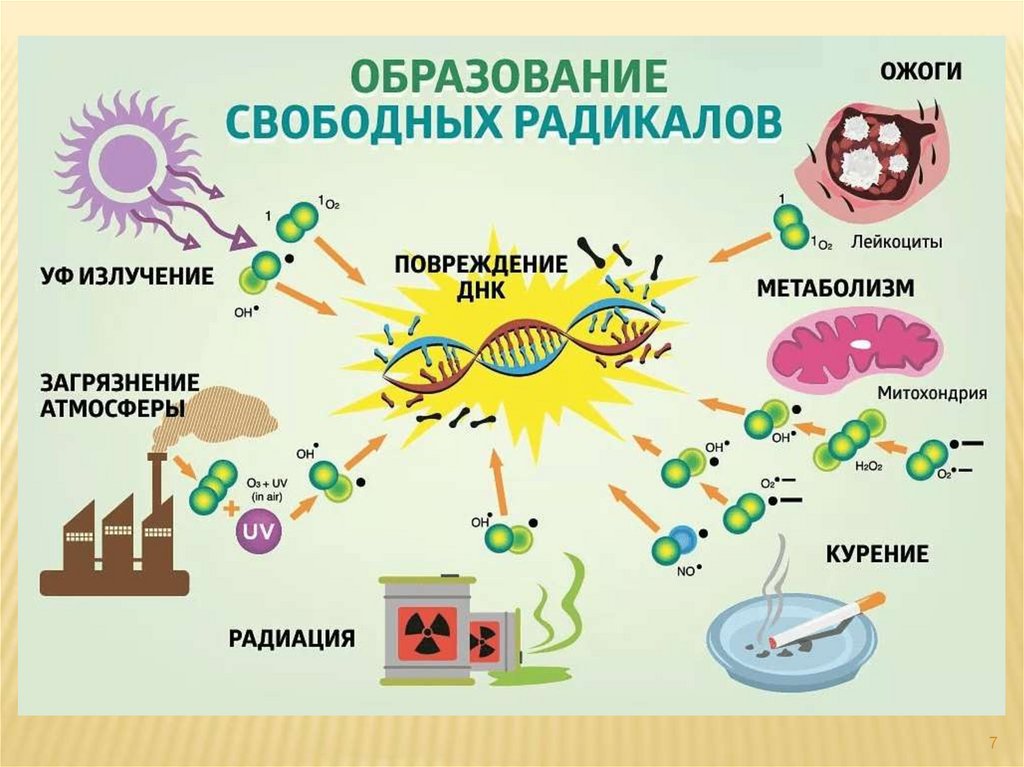
7.
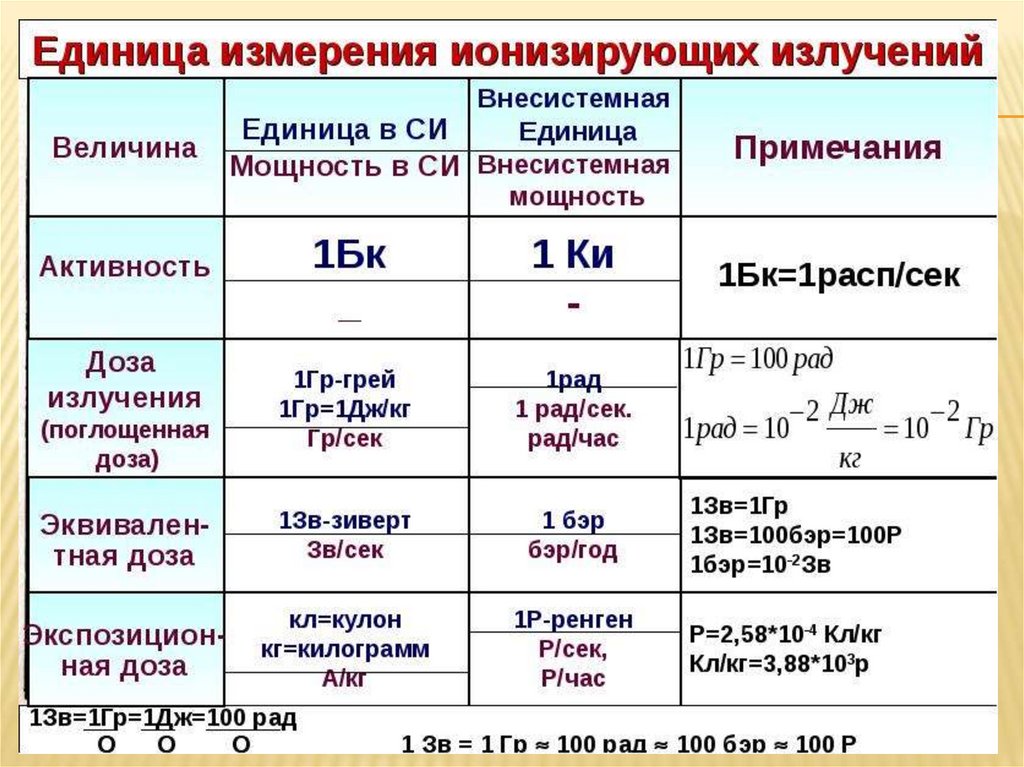
78. Дозы облучения
Поглощённая доза (D) – это энергия ионизирующегоизлучения, поглощённая облучаемым телом (веществом
организма), в пересчёте на единицу массы:
de
D
dm
Согласно международной системе единиц СИ измеряется в
греях: 1 Гр = 1 Дж/кг.
Эквивалентная доза (H) – поглощённая доза, умноженная
на коэффициент, отражающий способность данного вида
излучения повреждать ткани организма:
H DТ WR
Измеряют в системе единиц СИ в зивертах (Зв).
Эффективная доза (E) – величина, используемая как мера
риска возникновения отдалённых последствий облучения
всего тела человека и отдельных его органов и тканей с
учётом их радиочувствительности: E HT WT
T
8
9. Взвешивающие коэффициенты для излучения WR
Вид излученияДиапазон энергий
WR
Фотоны, электроны
Все энергии
1
Нейтроны
< 10 кэВ
5
10–100 кэВ
10
100 кэВ – 2 МэВ
20
2 – 20 МэВ
10
> 20 МэВ
5
Протоны
> 2 МэВ
5
Альфа-частицы, осколки
деления, тяжёлые ядра
Все энергии
20
9
10.
1011.
1112. Дозы облучения
Поглощённая доза (D) – это энергия ионизирующегоизлучения, поглощённая облучаемым телом (веществом
организма), в пересчёте на единицу массы:
de
D
dm
Согласно международной системе единиц СИ измеряется в
греях: 1 Гр = 1 Дж/кг.
Эквивалентная доза (H) – поглощённая доза, умноженная
на коэффициент, отражающий способность данного вида
излучения повреждать ткани организма:
H DТ WR
Измеряют в системе единиц СИ в зивертах (Зв).
Эффективная доза (E) – величина, используемая как мера
риска возникновения отдалённых последствий облучения
всего тела человека и отдельных его органов и тканей с
учётом их радиочувствительности: E HT WT
T
12
13. Взвешивающие коэффициенты для органов или тканей WT
Орган или тканьWT
Орган или ткань
WT
Гонады
0,2
Грудная железа
0,05
Толстая кишка
0,12
Печень
0,05
Пищевод
0,05
Щитовидная железа
0,05
Костная поверхность
0,01
Красный
мозг
костный
0,12
Лёгкие
0,12
Желудок
0,12
Кожа
0,01
Мочевой пузырь
0,05
Остальное
0,05
13
14.
1415. Радиационная чувствительность организмов
1516. Основные принципы радиационной безопасности
Принцип нормирования. Непревышение допустимыхпределов индивидуальных доз облучения граждан от всех
источников излучения.
Принцип обоснованности. Запрещение всех видов
деятельности по использованию источников излучения, при
которых полученная для человека и общества польза не
превышает риск возможного вреда, причиненного
дополнительным облучением
Принцип оптимизации. Поддержание на возможно низком
уровне с учетом экономических и социальных факторов
индивидуальных доз облучения и числа облучаемых лиц при
использовании любого источника излучения.
16
17. 1. Нормы на облучение персонала впервые введены в 1948 году (приказом по ПО «Маяк»): - 0,1 Р в сутки при штатной работе (1
мЗв/сут).- 30 Р в год при штатной работе (300 мЗв/год).
- 25 Р разово при ликвидации аварии (250 мЗв).
2. По стране допустимые уровни облучения персонала и населения
регламентировались, начиная с 1960 г. «Санитарными правилами
работы с радиоактивными веществами и источниками ионизирующих
излучений СП-333-60», однако изначально они распространялись
только на техногенные источники ИИИ.
3. Впервые ограничения на природное облучение были введены
относительно недавно по рекомендации МКРЗ: в 1987 году в
Основных санитарных правилах работы с радиоактивными
веществами другими источниками ионизирующих излучений (ОСП72/87).
4. Нормы на медицинское облучение впервые установлены в 1996
17
году в НРБ-96.
18. Требования НРБ-99/2009:
ТРЕБОВАНИЯ НРБ-99/2009:1.4. Требования Норм не распространяются на источники излучения, создающие
при любых условиях обращения с ними индивидуальную годовую эффективную дозу
не более 10 мкЗв. Требования Норм не распространяются также на космическое
излучение на поверхности Земли и внутреннее облучение человека, создаваемое
природным калием, на которые практически невозможно влиять.
Нормирование техногенного облучения в контролируемых условях:
Нормируемые
Пределы доз
величины*
Персонал (группа А)**
Эффективная доза 20 мЗв в год в среднем за любые
последовательные 5 лет, но не
более 50 мЗв в год
Население
1 мЗв в год в среднем за
любые последовательные 5
лет, но не более 5 мЗв в год
Эквивалентная
доза за год
в хрусталике
глаза***
150 мЗв
15 мЗв
коже****
500 мЗв
50 мЗв
кистях и стопах
500 мЗв
50 мЗв
19. Требования НРБ-99/2009:
ТРЕБОВАНИЯ НРБ-99/2009:3.1.4. Эффективная доза для персонала не должна превышать за период
трудовой деятельности (50 лет) - 1000 мЗв, а для населения за период жизни (70
лет) - 70 мЗв. Началом периодов считается 1 января 2000 года. – пункт
распространяется только на техногенные источники
4.1. Эффективная доза облучения природными источниками излучения всех
работников, включая персонал, не должна превышать 5 мЗв в год в
производственных условиях (любые профессии и производства).
4.3. Воздействие космических излучений на экипажи самолетов нормируется
как природное облучение в производственных условиях по п.4.1.
5.3.1. Допустимое значение эффективной дозы, обусловленной суммарным
воздействием природных источников излучения, для населения не
устанавливается. Снижение облучения населения достигается путем
установления системы ограничений на облучение населения от отдельных
природных источников излучения.
5.4.4. При проведении обоснованных медицинских рентгенорадиологических
обследований в связи с профессиональной деятельностью или в рамках медикоюридических процедур, а также рентгенорадиологических профилактических
медицинских и научных исследований практически здоровых лиц, не
получающих прямой пользы для своего здоровья от процедур, связанных с
облучением, годовая эффективная доза не должна превышать 1 мЗв.
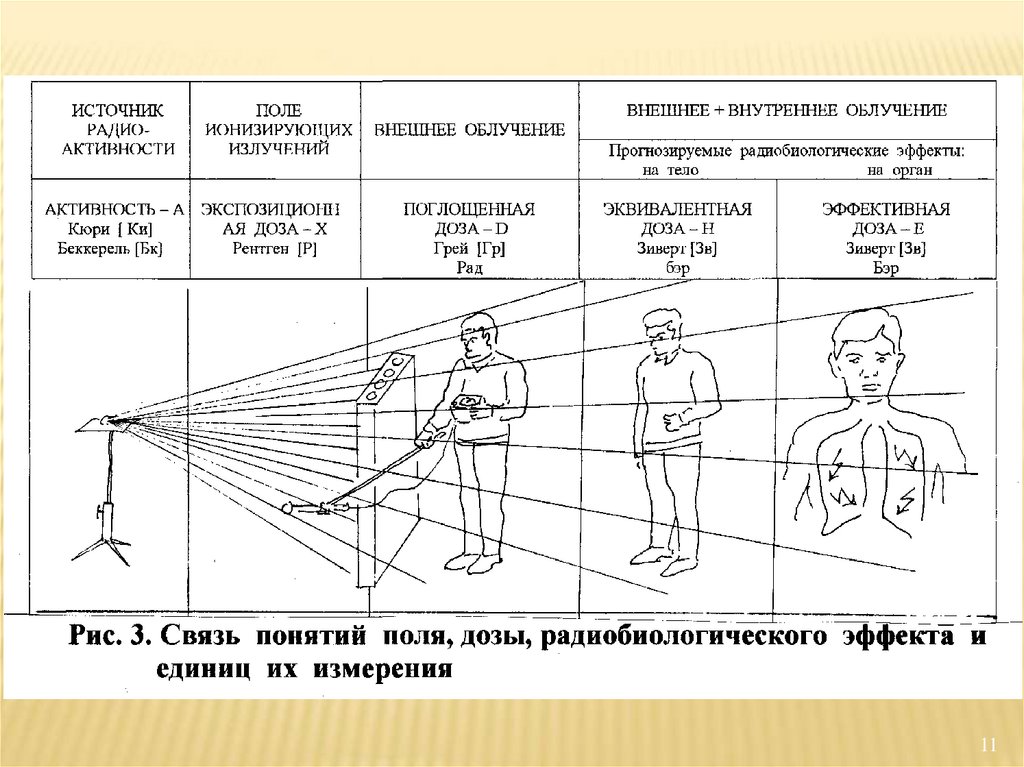
20. Виды облучения
Внешнееоблучение
–
воздействие
на
организм
ионизирующего излучения, приходящего извне (от устройства
или закрытого источника, содержащего радиоактивное
вещество).
Внутреннее облучение – облучение организма, отдельных
органов и тканей ионизирующим излучением, испускаемым
содержащимися
в
них
радионуклидами
(источник
ионизирующего излучения находится внутри организма).
Опасность при внешнем и внутреннем облучении
определяется, прежде всего, видом излучения и его
проникающей способностью.
20
21. Факторы, определяющие степень радиационной опасности при внешнем облучении
Вид излучения. Внешнее облучение α- и β-частицамименее опасно, так как они имеют небольшой пробег в ткани и
не достигают кроветворных и других органов. Опасность
представляют γ- и нейтронное излучение, проникающие в
ткань на большую глубину и разрушающие её.
Расстояние
до источника излучения. Интенсивность
радиации снижается пропорционально квадрату расстояния.
Время облучения. Чем более дробно порции излучения
распределены по времени, тем меньше его поражающее
действие.
Размер облучаемой поверхности. Чем меньше облучаемая
поверхность при той же мощности потока излучения, тем
меньше биологический эффект.
21
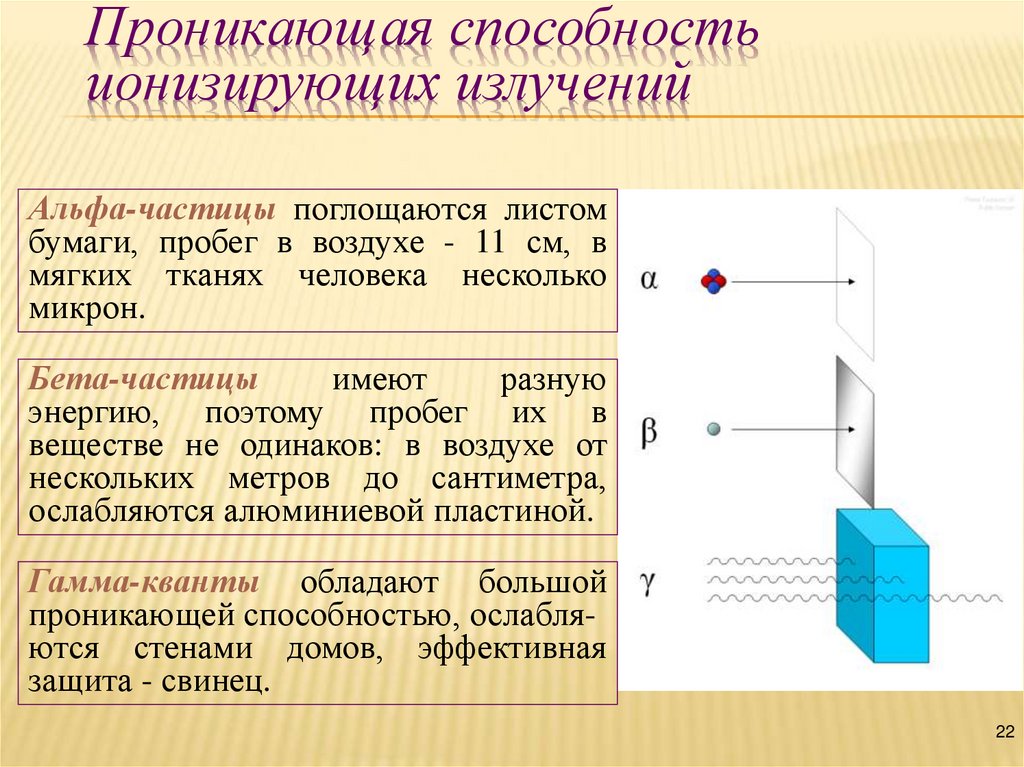
22. Проникающая способность ионизирующих излучений
Альфа-частицы поглощаются листомбумаги, пробег в воздухе - 11 см, в
мягких тканях человека несколько
микрон.
Бета-частицы
имеют
разную
энергию, поэтому пробег их в
веществе не одинаков: в воздухе от
нескольких метров до сантиметра,
ослабляются алюминиевой пластиной.
Гамма-кванты обладают большой
проникающей способностью, ослабляются стенами домов, эффективная
защита - свинец.
22
23. Пример
При облучениифотонами
поглощенной дозой
450 рад
6 см2 =>
При облучении
фотонами
поглощенной дозой
450 рад
Всего тела =>
Поражения не
наблюдается
50% смертельных
случаев
23
24.
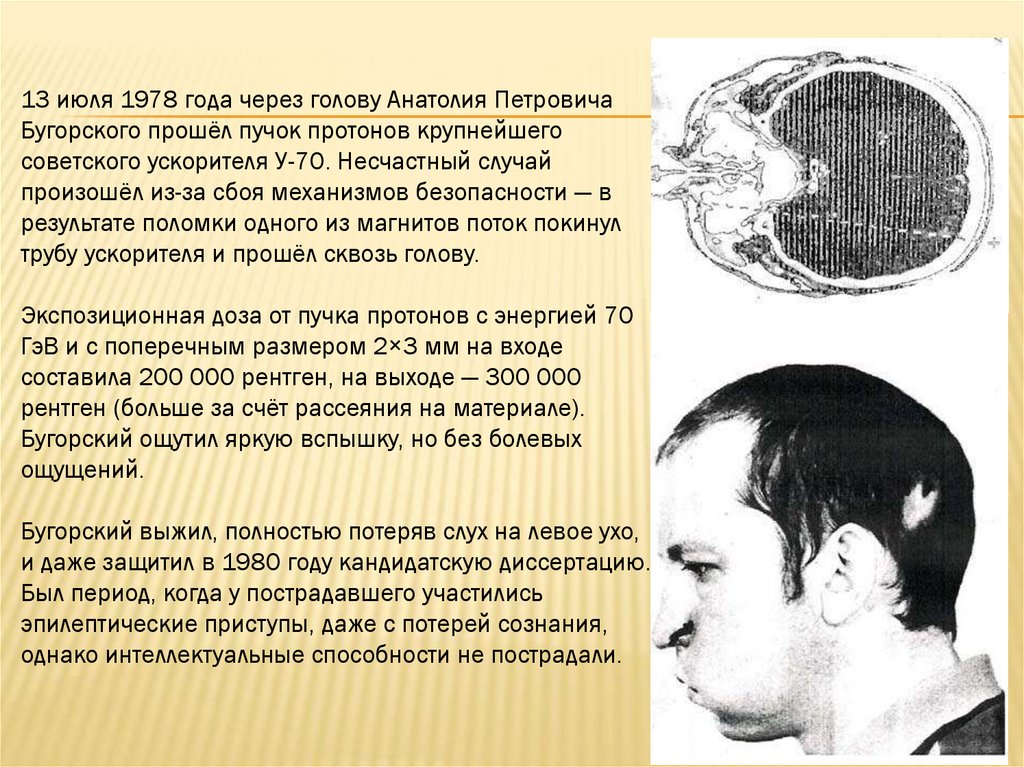
13 июля 1978 года через голову Анатолия ПетровичаБугорского прошёл пучок протонов крупнейшего
советского ускорителя У-70. Несчастный случай
произошёл из-за сбоя механизмов безопасности — в
результате поломки одного из магнитов поток покинул
трубу ускорителя и прошёл сквозь голову.
Экспозиционная доза от пучка протонов с энергией 70
ГэВ и с поперечным размером 2×3 мм на входе
составила 200 000 рентген, на выходе — 300 000
рентген (больше за счёт рассеяния на материале).
Бугорский ощутил яркую вспышку, но без болевых
ощущений.
Бугорский выжил, полностью потеряв слух на левое ухо,
и даже защитил в 1980 году кандидатскую диссертацию.
Был период, когда у пострадавшего участились
эпилептические приступы, даже с потерей сознания,
однако интеллектуальные способности не пострадали.
24
25. Защита от воздействия ионизирующих излучений
При внешнем облучении дозупредпринять следующие действия:
можно
ослабить,
если
• Сократить время воздействия источника ионизирующего
излучения до минимума (защита временем).
• Находиться на возможно большем расстоянии от источника
ионизирующего излучения (защита расстоянием).
• Применять защитные экраны. В качестве защитных
материалов используются свинец, сталь, бетон, вода и т.д.
• В быту следить за облучением при медицинском
обследовании (учитывать количество проводимых процедур) и
правильным выбором строительных материалов.
2
26. Защитные свойства домов и убежищ
специальное убежищеослабляет излучение
практически
полностью
каменный дом
10–50 раз
деревянный дом
4–10
погреба и подвалы деревянных
домов
50–100
кирпичная кладка толщиной:
50 см
10
80 см
100
26
27. Виды облучения
Внешнее облучение – воздействие на организмионизирующего излучения, приходящего извне (от
устройства или закрытого источника, содержащего
радиоактивное вещество).
Внутреннее облучение – облучение организма,
отдельных органов и тканей ионизирующим излучением,
испускаемым содержащимися в них радионуклидами
(источник ионизирующего излучения находится внутри
организма).
Опасность при внешнем и внутреннем облучении
определяется, прежде всего, видом излучения и его
проникающей способностью.
27
28. Факторы, определяющие степень радиационной опасности при внутреннем облучении
Вид излучения. При внутреннем облучении наиболее опаснырадионуклиды, испускающие при распаде α-частицы, так как
они имеют большую ионизирующую способность.
Энергия излучения. Чем энергия излучения
больше повреждающий эффект.
Время пребывания излучателя в организме. Время будет
определяться периодом радиоактивного полураспада и
периодом биологического полувыведения. Чем дольше
радионуклид находится в организме, тем больший вред он
ему нанесёт.
выше,
тем
28
29. Факторы, определяющие степень радиационной опасности при внутреннем облучении
Путьпоступления радиоактивного вещества в организм (при
дыхании, с пищей и водой, через кожу).
Продолжительность
поступления радиоактивного вещества в
организм.
Распределение
радионуклида в организме человека (наличие
критического органа).
Критический орган – это орган, способный избирательно накапливать
тот или иной радионуклид в соответствии с его химическими
свойствами.
131
I, 132I, 125I
Sr, 90Y, 226Ra, 239Pu
Костная система
C, 106Ru, 137Cs, 134Cs
Равномерное распределение
по всем органам и тканям
90
14
Щитовидная железа
29
30. Защита от попадания радионуклидов внутрь организма
Осуществлятьконтроль воды, воздуха, продуктов
питания. Для каждой из перечисленных категорий
существуют
предельно
допустимые
нормы
содержания радионуклидов.
Принять меры по снижению содержания радона в
помещении.
В случае радиационной аварии защитить органы
дыхания, поверхности тела (платки, куртки, сапоги).
При попадании радионуклидов на поверхность кожи
провести дезактивацию водой, хозяйственным
мылом, поверхностно-активными веществами.
Если произошло попадание радионуклида внутрь
организма человека, то принять меры, ускоряющие
их выведение.
30
31. Выведение радионуклидов из организма
Механическое удаление радионуклида (приём рвотныхсредств, промывание желудка и кишечника, обильное питьё,
приём адсорбентов).
Применение
адсорбентов
(веществ
поглощающих
радионуклиды).
Ускорение выведения радионуклидов методом замещения
или комплексообразования. Вытесняют радиоизотопы
подобными им, которые естественно присутствуют в
организме. Соли некоторых органических кислот образуют с
катионами растворимые комплексы, которые легко проходят
через почки.
Применение радиопротекторов. Радиопротекторы вводят
перед предполагаемым облучением (например, перед лучевой
терапией).
Поддержка
защитных и восстановительных сил
организма.
31
32. Эффекты облучения людей
ЭФФЕКТЫ ОБЛУЧЕНИЯ ЛЮДЕЙРадиационные эффекты облучения людей
Соматические
Соматико-стохастические
Генетические
(детерминированные)
(стохастические)
(стохастические)
Острая лучевая
болезнь
Лейкозы
Доминантные
генные мутации
Хроническая
лучевая болезнь
Опухоли
Рецессивные
генные мутации
Локальные
лучевые
поражения
Сокращение
продолжительности жизни
Хромосомные
аберрации
32
33. Возникновение детерминированных эффектов
ВОЗНИКНОВЕНИЕ ДЕТЕРМИНИРОВАННЫХЭФФЕКТОВ
Общее или локальное облучение ткани, вызывающее гибель
некоторой части клеток, которая не может быть
скомпенсирована размножением жизнеспособных клеток.
Происшедшая потеря клеток может вызвать тяжелое и
обнаруживаемое клинически нарушение функции ткани или
органа.
Степень тяжести наблюдаемого эффекта зависит от дозы. Должен
существовать порог, ниже которого потеря клеток слишком
мала, чтобы заметно нарушить функцию ткани или органа.
33
34. Дозы и последствия облучения
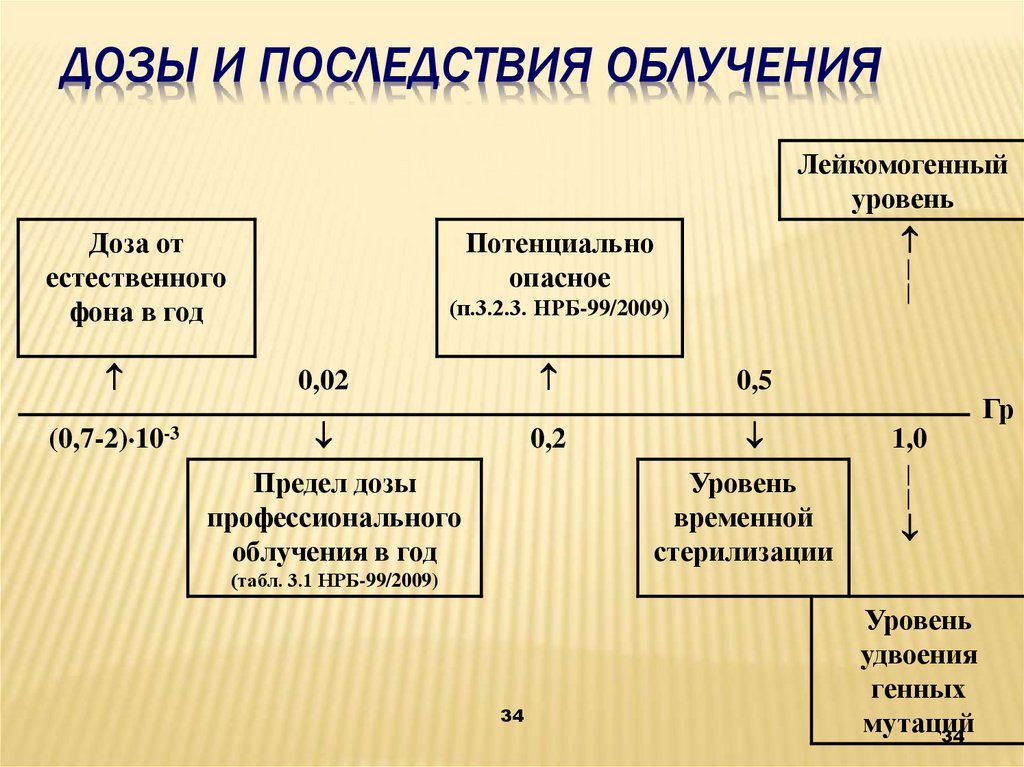
ДОЗЫ И ПОСЛЕДСТВИЯ ОБЛУЧЕНИЯЛейкомогенный
уровень
Доза от
естественного
фона в год
Потенциально
опасное
(п.3.2.3. НРБ-99/2009)
0,02
0,5
(0,7-2) 10-3
0,2
1,0
Уровень
временной
стерилизации
Предел дозы
профессионального
облучения в год
Гр
(табл. 3.1 НРБ-99/2009)
34
Уровень
удвоения
генных
мутаций
34
35. Дозы и последствия облучения
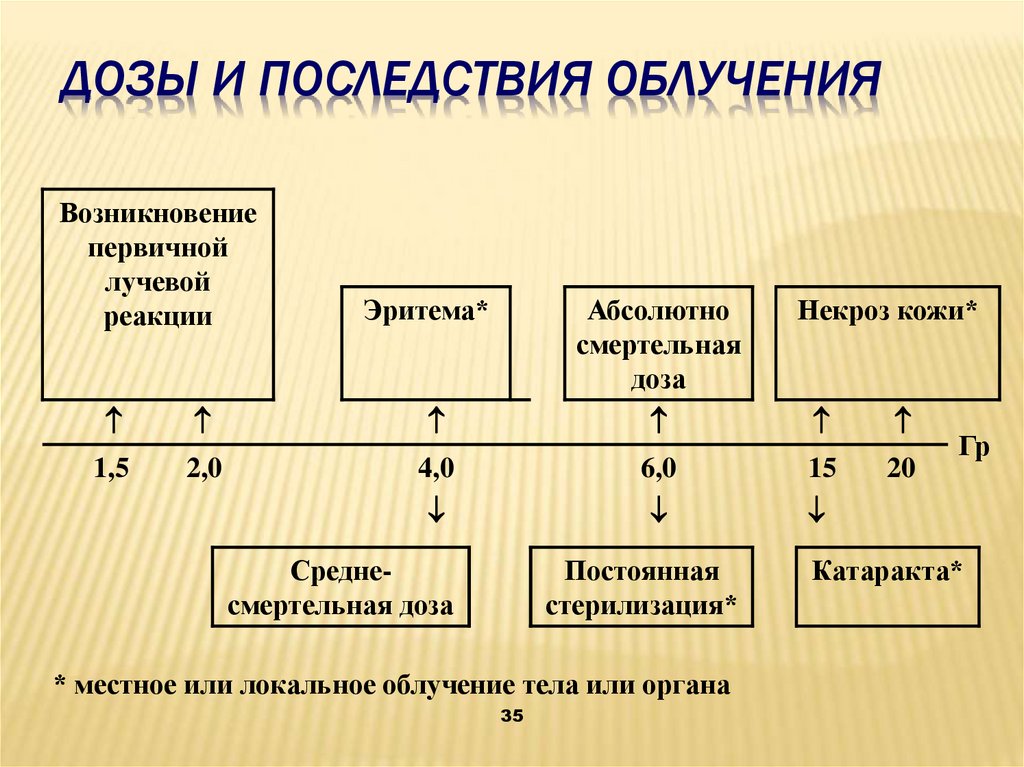
ДОЗЫ И ПОСЛЕДСТВИЯ ОБЛУЧЕНИЯВозникновение
первичной
лучевой
реакции
Эритема*
Абсолютно
смертельная
доза
Некроз кожи*
1,5
2,0
4,0
6,0
15
20
Среднесмертельная доза
Постоянная
стерилизация*
* местное или локальное облучение тела или органа
35
Гр
Катаракта*
36. Последствия облучения людей
Детерминированные:лучевая болезнь;
локальные лучевые поражения.
Стохастические:
сокращение продолжительности жизни;
лейкозы (злокачественные изменения кровообразующих
клеток);
опухоли разных органов и клеток;
наследственные болезни.
Радионуклиды, попавшие внутрь организма человека,
вызывают
различные
последствия,
схожие
с
последствиями от внешнего облучения при равных
поглощённых дозах.
36
37. Формы ОЛБ
ФОРМЫ ОЛБкостномозговая (1-6 Гр) Типичная форма ОЛБ, развивается при
одномоментном/кратковременном облучении дозой 1-6 Гр. Летальность составляет 50 %.
Имеет четыре степени. Характерно поражение кроветворной системы;
переходная форма (6-10 Гр) Переходная форма ОЛБ возникает при дозе облучения в 6-10
Гр. Для неё характерны поражения кроветворной системы и кишечника с характерными
симптомами - диареей и рвотой с обезвоживанием. Летальность составляет 95 %;
кишечная (10-20 Гр) Является результатом одномоментного/кратковременного облучения
дозой 10-20 Гр. Протекает с тяжелым энтеритом, кровотечениями из ЖКТ, диареей,
кровавой рвотой и обезвоживанием, лихорадкой, инфекционно-септическими
осложнениями. Летальность составляет 100 %;
токсемическая (сосудистая) (20-80 Гр) Манифестирует при
одномоментном/кратковременном облучении дозой 20-80 Гр. Характеризуется тяжелой
интоксикацией и гемодинамическими нарушениями. Летальность составляет 100 %;
церебральная (80-120 Гр). По особенностям клинической картины обозначается как
молниеносная или острейшая лучевая болезнь, характеризуется общим поражением
нервной системы с нарушением её жизненно важных функций. Летальность составляет
100 %;
смерть под лучом (более 120 Гр): гибель нервных, мышечных клеток с быстрым
смертельным исходом. Летальность составляет 100 %, однако, таких случаев ещё не
наблюдалось.
37
38. Клинические синдромы ОЛБ
КЛИНИЧЕСКИЕ СИНДРОМЫ ОЛБАгранулоцитоз
Геморрагический синдром
Анемический синдром
Оральный синдром
Кишечный синдром
Поздний радиационный гепатит
Синдром радиационной кахексии
Синдром инфекционных осложнений
Синдром сердечно-сосудистых осложнений
38
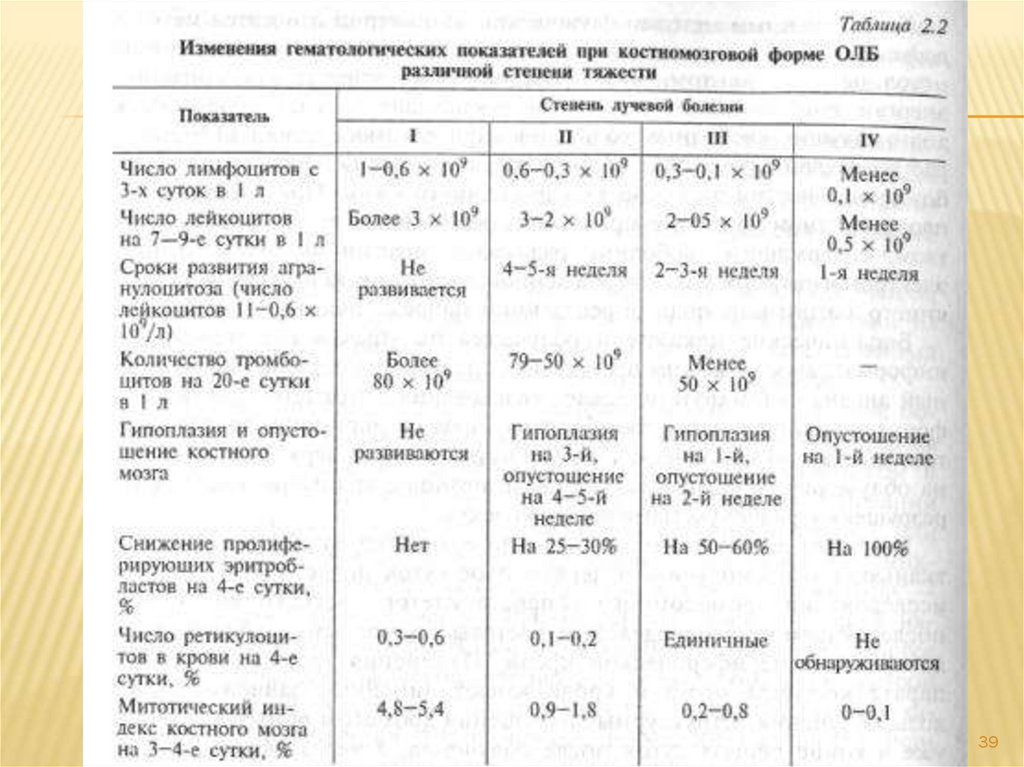
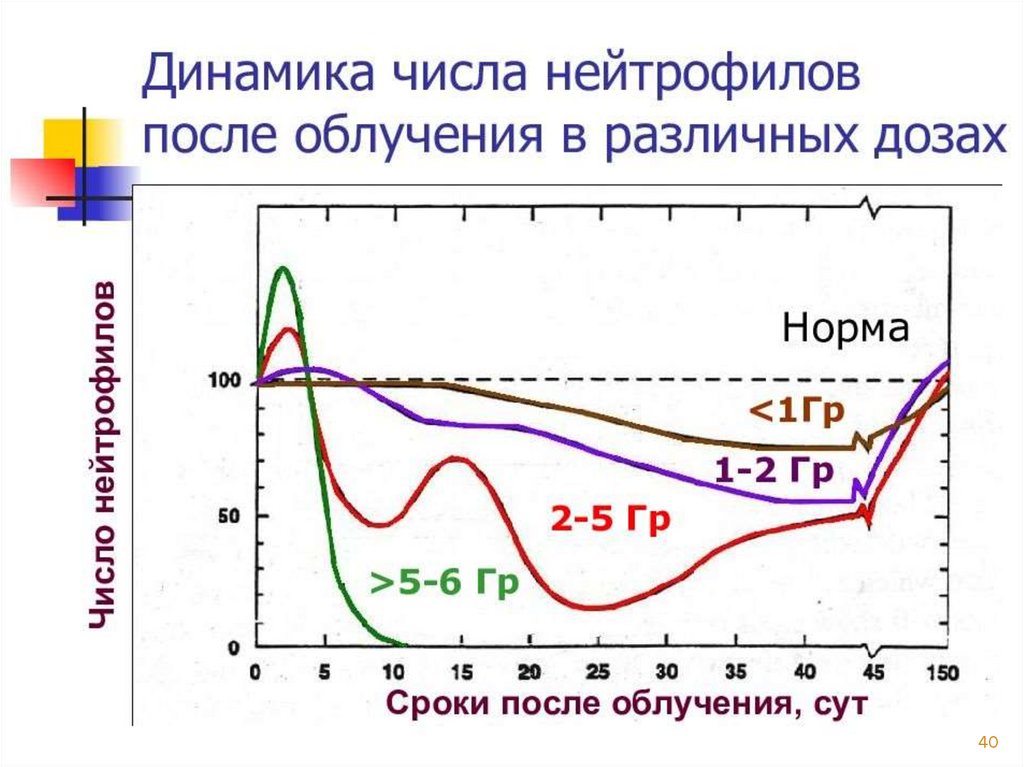
39.
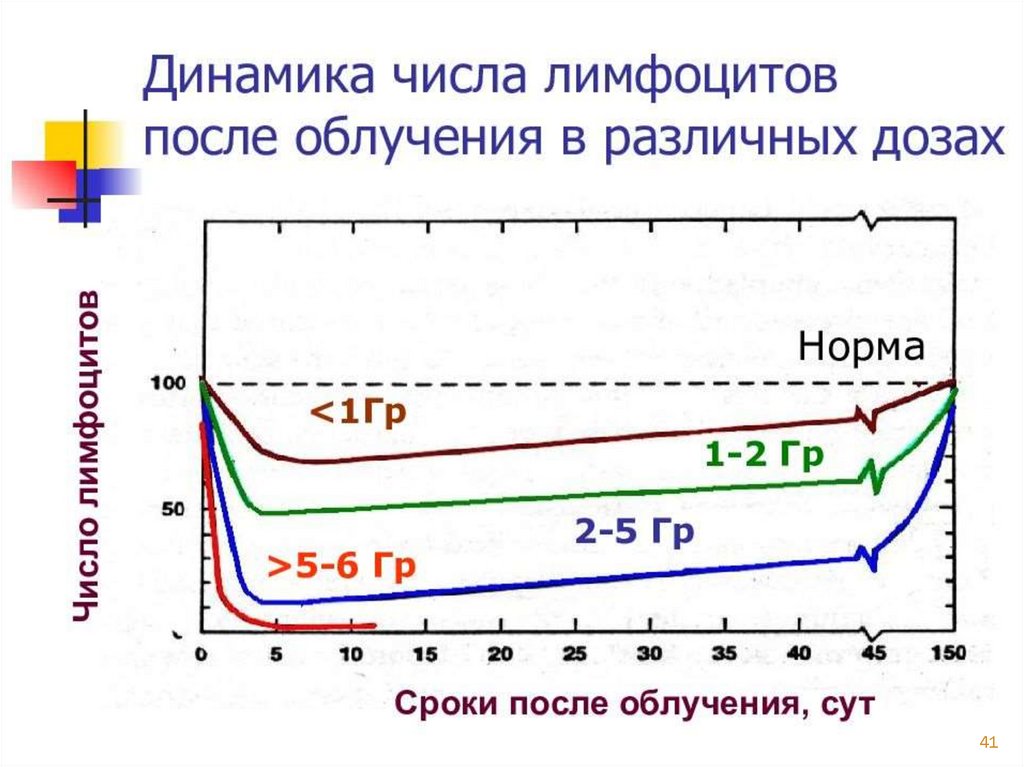
3940.
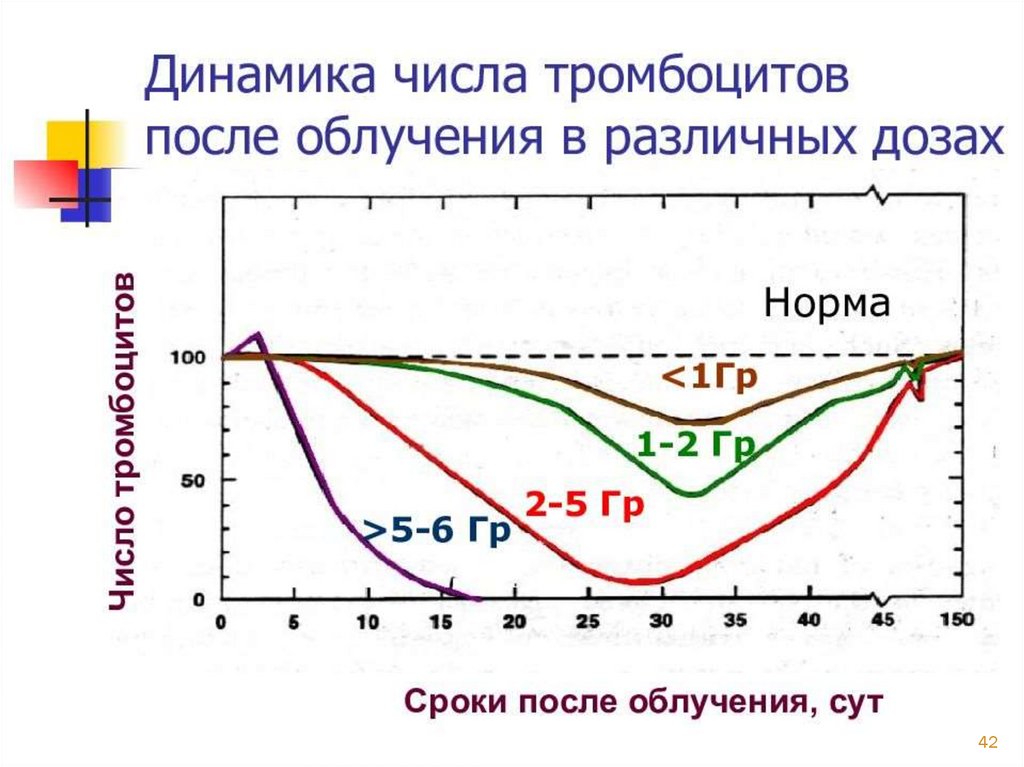
4041.
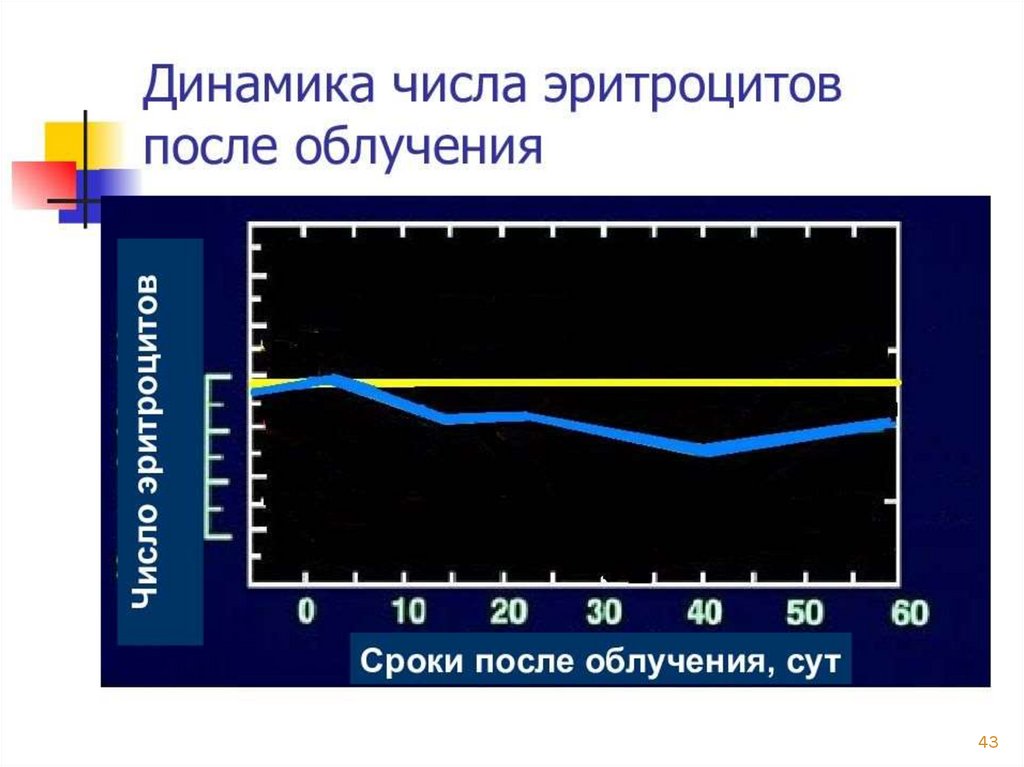
4142.
4243.
4344.
4445.
4546. Парадокс
46Из презентации
Романова С.А.
ПАРАДОКС
Гистоавторадиограммы легких человека
при поступлении в организм 1
микрограмма
(1×10-6
грамма)
плутония (норма и через 1 год после
поступления).
47. Легкие человека (норма)
47Из презентации
Романова С.А.
ЛЕГКИЕ ЧЕЛОВЕКА (НОРМА)
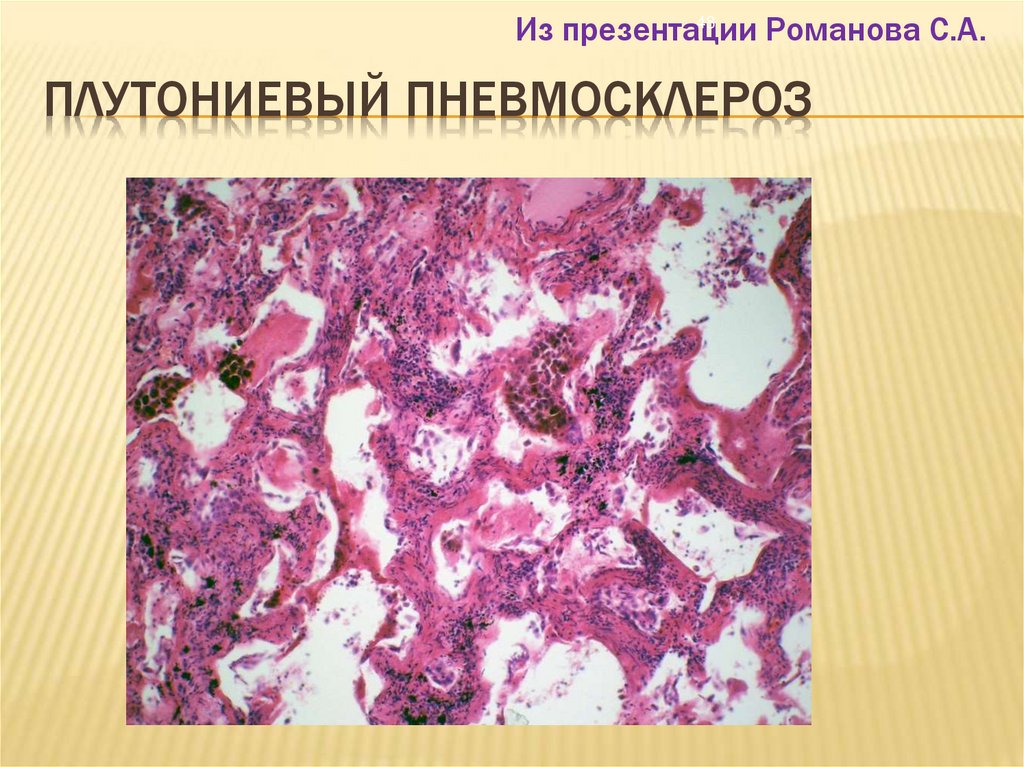
48. Плутониевый пневмосклероз
48Из презентации
Романова С.А.
ПЛУТОНИЕВЫЙ ПНЕВМОСКЛЕРОЗ
49. Общие сведения
Из презентации Романова С.А.ОБЩИЕ СВЕДЕНИЯ
Количество клеток – 1013 штук;
Размер клетки 5-6 микрон (10-6 метра)
В ядре каждой соматической клетки 23 пары
хромосом;
Общая длина всех молекул ДНК в клетке – 2
метра;
49
50. Генетические эффекты
одиночные генные мутации;неправильный
набор хромосом, т. е. слишком
большое или малое их число или наличие
хромосомных аберраций с неправильным
присоединением осколков хромосом после их
разрыва в момент деления клетки;
частые, но небольшие мутации, которые нельзя
идентифицировать по особым отличительным
признакам и наблюдаемым изменениям в
хромосомах.
50
51. Стохастические эффекты
Основные виды стохастических эффектовоблучения:
изменения в соматических клетках,
приводящие к возникновению рака;
генетические мутации, оказывающие
влияние на будущие поколения;
влияние на зародыш и плод, вследствие
облучения матери в период беременности.
51
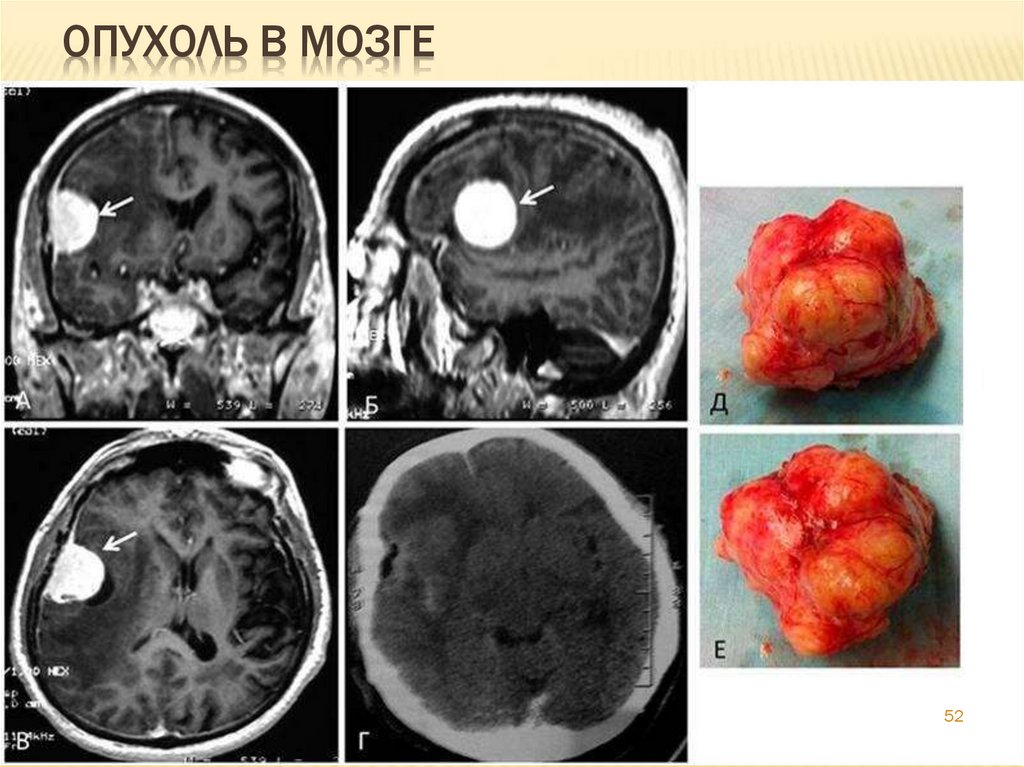
52. Опухоль в мозге
ОПУХОЛЬ В МОЗГЕ52
53. Вероятность онкологических заболеваний
Разовая эквивалентная доза не выше 0,1 Зв –малая, при этом накопленная мощность
эквивалентной дозы за жизнь не должна
превышать 1 Зв.
Понятие «низкий уровень облучения»
обозначает либо малую дозу облучения при
любой мощности дозы, либо низкую мощность
дозы в течение всей жизни, либо то и другое
вместе. С другой стороны, эквивалентные
дозы, превышающие 1 Зв, следует считать
большими, а дозы, заключенные между 0,1 и
1 Зв, – промежуточными.
Таблица - Размер выборки, необходимой
для статистически значимого (с 90%
вероятностью) определения зависимости
доза-эффект в канцерогенезе
Относительная среднестатистическая
вероятность заболевания раком после
получения однократной дозы в 0,01 Гр при
равномерном облучении всего тела.
Уровень доз,
Зв
1
0,1
0,01
Размер выборки, чел.
1000
100 000
10 000 000
Для регистрации эффектов при дозе 10 мЗв с доверительной вероятностью 90%
контингент исследуемых согласно [НКДАР ООН, 1988] должен быть не менее 5
млн. человек
53
54. Оценка риска заболевания лейкозом и раком
ОЦЕНКА РИСКА ЗАБОЛЕВАНИЯЛЕЙКОЗОМ И РАКОМ
Вид злокачественного
заболевания
Лейкоз
Число случаев на 1000
облученных человек/Зв
1,5 - 2,5
Рак щитовидной железы
5 - 15
Рак молочной железы
5 - 20
Всевозможные виды рака в 1 случай смерти/ 100
результате общего облучения облученных человек/Зв
организма
54
55. Оценка генетических эффектов, вызванных облучением
ОЦЕНКА ГЕНЕТИЧЕСКИХ ЭФФЕКТОВ,ВЫЗВАННЫХ ОБЛУЧЕНИЕМ
В настоящее время принято значение удваивающей дозы для
человеческой популяции в 1 Гр.
При воздействии на людей излучений с низкой линейной
потерей энергии (ЛПЭ) при малой мощности дозы
рассчитанное количество генетических заболеваний на 1
Гр оценивается:
для первого поколения в 3000…4700 на миллион
живорожденных, что составляет 0,3...0,5% естественной
частоты генетических нарушений для человеческой
популяции;
для последующих поколений 1850 случаев на 1 млн
живорожденных или 0,17% естественной частоты
генетических нарушений 55
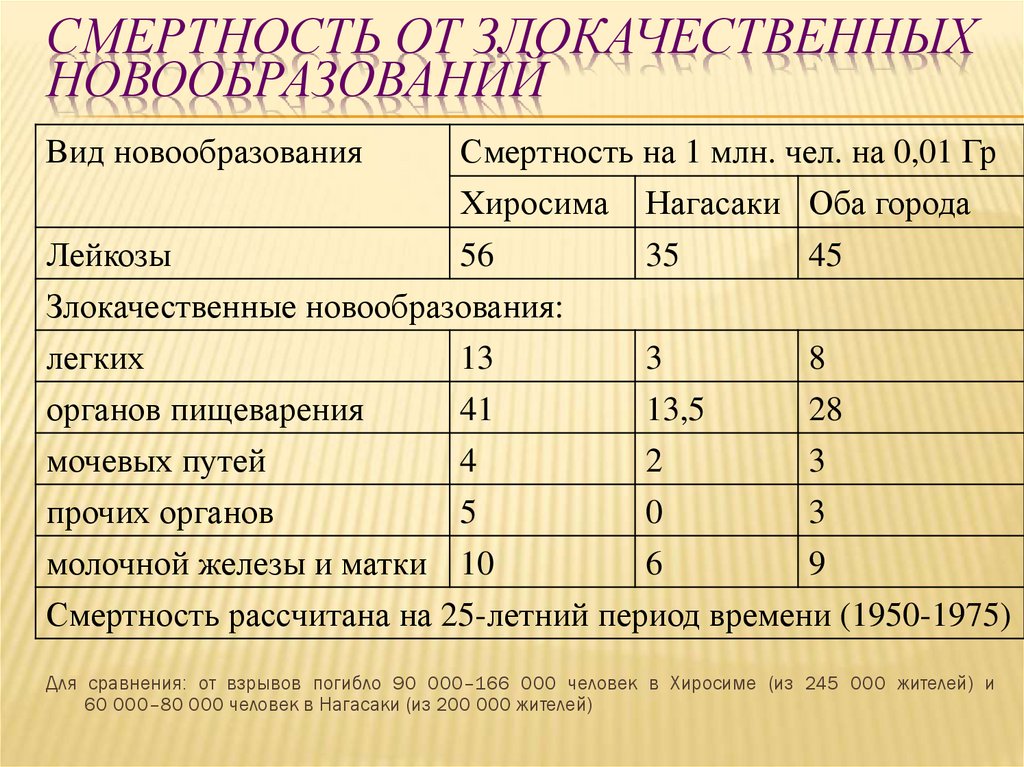
56. Смертность от Злокачественных новообразований
СМЕРТНОСТЬ ОТ ЗЛОКАЧЕСТВЕННЫХНОВООБРАЗОВАНИЙ
Вид новообразования
Смертность на 1 млн. чел. на 0,01 Гр
Хиросима Нагасаки Оба города
Лейкозы
56
Злокачественные новообразования:
легких
13
35
45
3
8
органов пищеварения
мочевых путей
прочих органов
13,5
2
0
28
3
3
41
4
5
молочной железы и матки 10
6
9
Смертность рассчитана на 25-летний период времени (1950-1975)
Для сравнения: от взрывов погибло 90 000–166 000 человек в Хиросиме (из 245 000 жителей) и
60 000–80 000 человек в Нагасаки (из 200 000 жителей)
57.
Наибольшие дозы бета и гамма-излучениябыли
получены
персоналом станции и
© НОУ ДПО
«ЦИПК
Росатома»
первым прибывшим пожарным в ночь на 26 апреля. У 134 человек с установленной
лучевой болезнью дозы облучения составили 0,8 – 16 Гр. Дозы обусловленные
внутренним облучением, лишь в единичных случаях превышали 1 Гр на щитовидную
железу и, как правило, не более 0,3 Гр на все другие органы. Из 134 человек 28
умерли в остром периоде лучевой болезни и 13 – позднее от различных причин.
Следующую по степени радиационного воздействия группу составляли представители
различных профессий ( около 230 000 человек, в основном, мужчины в возрасте 2045 лет), которые в 1986-87 годах осуществляли работы по ликвидации последствий
аварии на участках 30-ти километровой зоны с наиболее высокими уровнями
радиационного воздействия. Для большинства из этой групп средние дозы общего
облучения составили 40 -80 мЗв, и лишь у 8% дозы превышали 250 мЗв ( до 500 мЗв).
Уровень радиационного воздействия в последующие годы был существенно ниже.
Среди населения, проживающего в районах значительного радиоактивного
загрязнения или с задержкой отселенного из 30 - ти километровой зоны (около 272
000 человек в период с 1986 по 1991 год) только менее 1% получили дозы облучения,
превышающие 15 сГр. Результаты медико-биологических исследований позволяют
предположить, что опасность отдаленных онкологических последствий (за
исключением опухолей щитовидной железы) в данном случае может составить
единицы процентов от естественного уровня таких заболеваний. Вообще прогнозы,
сделанные отечественными учеными медиками в этой области почти 15 лет после
аварии полностью подтверждается.
58.
© НОУ ДПО «ЦИПК Росатома»Радиоактивными выбросами, в первую очередь изотопами йода и цезия, были загрязнены
обширные территории Украины, Белоруссии и России. Следует особо выделить группу,
представленную детьми младенческого возраста, радиационное воздействие на которых было
обусловлено, в основном, интенсивными выпадениями радиоактивного йода в начальные
периоды времени после аварии. Особенности их вскармливания и пищевого рациона,
размеры щитовидной железы и ряд других факторов предопределили облучения этого органа в
широком диапазоне доз – от 0,3 до 1 Гр и даже выше. Следствием стало значительное
учащение (через 2 – 5 лет) случаев рака щитовидной железы на Украине, в Белоруссии и
России (всего до 1800 случаев), что в несколько раз превысило средний уровень
заболеваемости до аварии. Среди детей (на момент аварии) Брянской обл. выявлено 170
раков щитовидной железы, из которых 55 обусловлены радиационным фактором. Однако,
благодаря эффективному выявлению и лечению за все годы из общего числа пациентов
умерли три человека.
Другие последствия (лейкозы, раки отдельных органов помимо щитовидной
железы), которые можно непосредственно связать с облучением, за истекший срок
(20 лет) не обнаружены ни у детского , ни у взрослого населения. По данным
Российского государственного медико-дозиметрического регистра (РГДМР) среди
ликвидаторов России (около 285 000 человек) выявлено 145 лейкозов, из которых
50 обусловлены радиацией, и 55 случаев рака щитовидной железы, из которых 12
обусловлены радиацией. Основные тенденции в заболеваемости как населения,
так и участников ликвидации последствий аварии, соответствуют аналогичным (в
соответствующих возрастных группах) для всего населения.
59. Нарушения развития эмбриона и плода, вызванные облучением матери во время беременности
Сроки беременностиПоследствия
Предымплантационный Смерть зародыша
(до 9 дней)
Влияние на те структуры, которые
должны развиваться в момент
Органогенез
вредной экспозиции. Грубые
(с 9 дн. до 6 недель)
аномалии плода, задержка роста и
развития организма.
Плодный период
Врожденные дефекты, задержка
(после 6 недель)
развития при дозе > 0,01-0,2 Зв
Воздействие ионизирующих излучений должно быть
исключено. Допустимо только по жизненным показаниям
59
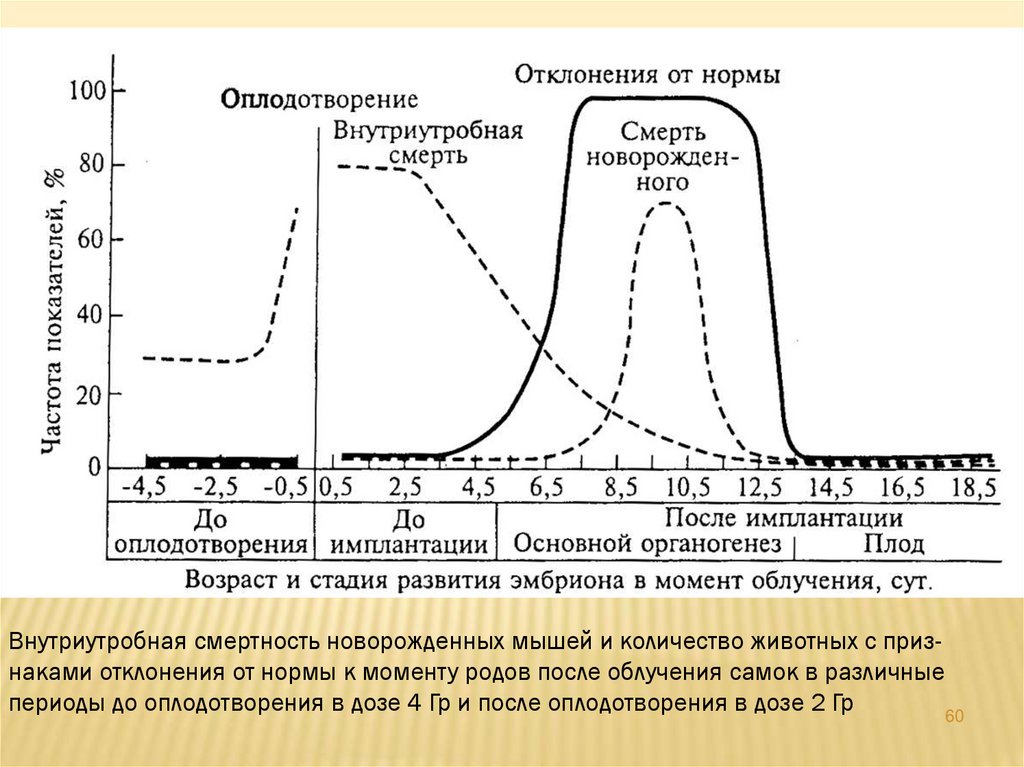
60.
Внутриутробная смертность новорожденных мышей и количество животных с признаками отклонения от нормы к моменту родов после облучения самок в различныепериоды до оплодотворения в дозе 4 Гр и после оплодотворения в дозе 2 Гр
60
61.
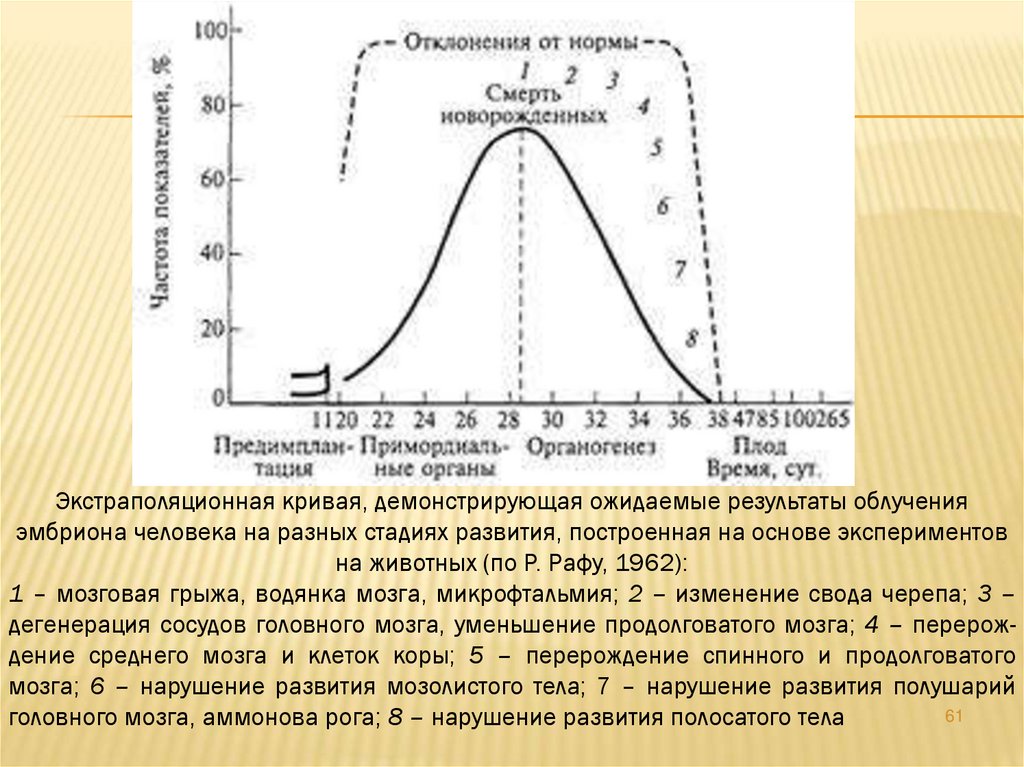
Экстраполяционная кривая, демонстрирующая ожидаемые результаты облученияэмбриона человека на разных стадиях развития, построенная на основе экспериментов
на животных (по Р. Рафу, 1962):
1 – мозговая грыжа, водянка мозга, микрофтальмия; 2 – изменение свода черепа; 3 –
дегенерация сосудов головного мозга, уменьшение продолговатого мозга; 4 – перерождение среднего мозга и клеток коры; 5 – перерождение спинного и продолговатого
мозга; 6 – нарушение развития мозолистого тела; 7 – нарушение развития полушарий
61
головного мозга, аммонова рога; 8 – нарушение развития полосатого тела
62.
Поглощенная доза, сГр
25
10-50
15
10
3-10
До 10
Последствия облучения
Временная (на 2-6 мес.) стерильность женщин при разовом облучении.
Гибель от рака 1 человека из 100 при суммарном облучении за 70 лет (Danby, 1993)
После 15 генераций клеточные популяции «помнят» об облучении и отвечают на внешние стимулы иначе, чем
контрольные (Пелевина и др., 1996)
Начало угнетения сперматогенеза у человека.
Развитие умственной отсталости при разовом внешнем облучении в утробе в период 8-15 недель после зачатия (Рябухин,
2000).
Клинически значимое подавление кроветворения в красном костном мозге человека при разовом внешнем облучении
(Колышкин, Рыбальский, 1995).
Снижение числа сперматозоидов у человека на период до 1 года при разовом внешнем облучении; возникновение
уродств у новорожденных (Москалев, Стрельцова, 1978).
Увеличение риска смерти от лейкемии на 22% при суммарном облучении за 70 лет (JARC…, 1994).
Увеличение частоты аберраций хромосом в лимфоцитах, дицентриков и кольцевых хромосом (Lloyd et al., 1988; PolfRuling et al., 1983; цит. по: Рябухин, 2000)
Увеличение числа хромосомных аберраций в лимфоцитах (Севанькаев, 1991)
9
Учащение случаев возникновения рака щитовидной железы (Ron et. al., 1989; цит. по: Рябухин, 2000)
5
Поражение вилочковой железы человека (Neta, 1992; цит. по: Рябухин, 2000)
Смертность от солидных раков в группе, получивших дозы 6-15 сГр выше, чем в группе, получившей 0-5 сГр.
Появление врожденных пороков развития у человека (Мельников, 2001; по: Miller, 1976).
4
3-5
1,6
1
0,2
Повышение смертности от разных раков при суммарном внешнем облучении за 30 лет, сравнительно с необлученным
персоналом (Radiation..., 1991).
Вдвое большее число неблагоприятных исходов беременности, чем в контроле (Ижевский, 2001).
Дополнительные случаи лейкемии у человека (Carter, 1993)
Улавливаемые существующими методами изменения биохимических процессов в клетке (Бурлакова и др., 1996;
Spitkovsky, 1993).
Ускорение полового созревания девочек - появление менструаций (Москалев, Стрельцова, 1978).
Увеличение числа мертворождений (Москалев, Стрельцова, 1978).
Повышение частоты аберраций в лимфоцитах при использовании йода-131 с диагностическими целями (Яковлева, 1984;
по: Москалев, Стрельцова, 1978).
50-350 наследственных аномалий в первом поколении на 1 млн новорожденных (Шевченко, 1989).
Сокращение продолжительности жизни на 1-30 суток (Ушаков, Карпов, 1997).
Поражения головного мозга новорожденных при облучении в утробе (Schull et. al, 1991)
Увеличение смертности от всех раков на каждые 10 мЗв, полученные после 45 лет, через 10 лет - на 4,98%; через 20 лет
- на 7,3% (Richardson, Wing, 1999).
Порог вероятности возникновения уродств у новорожденного при облучении области живота матери (Principles..., 1993)
0,005-0,0007Величина аппроксимирующих минимально действующих доз (Зайнуллин, 1998).
62
63. Подходы к нормированию воздействия ионизирующих излучений на живую природу
Антропоцентрический подход.Биоцентрический
подход: понятие радиационной
безопасности распространяется на отдельные особи
других видов (кроме человека).
Экоцентрический
подход: понятие радиационной
безопасности распространяется и на биотическую
(человек и другие живые организмы), и на абиотическую
компоненты экосистем. Экологическое нормирование
должно базироваться на принципах коэволюции,
биотической регуляции устойчивости биосферы и
контроле потоков веществ, являющихся компонентами
биогеохимических циклов.
63
64. В основу действующих концепций нормирования радиационного фактора МКРЗ положен антропоцентрический принцип ограничения дозы:
«Нормы контроля окружающей среды, необходимыедля защиты человека в той мере, которая в данное
время признается желательной, обеспечат
безопасность и других биологических видов, хотя
случайно их отдельным особям может быть
причинен вред, но не до такой степени, которая
представляла бы опасность для всего вида или
нарушала бы баланс между видами».
64
65. Оценка Риска
Ключевым в этой методологии является положение, что вредныевоздействия факторов окружающей среды на конкретную
популяцию вызывают неблагоприятные последствия, частоту и
проявление которых можно характеризовать риском.
Риск определяется как мера количественного измерения
опасности, включающая количественные показатели ущерба от
воздействия того или иного опасного фактора и вероятности
(частоты) возникновения рассматриваемого опасного фактора.
В настоящее время используются следующие подходы к
нормированию радиационного фактора:
1) концепция нулевого риска;
2) беспороговая концепция;
3) концепция приемлемого риска.
65
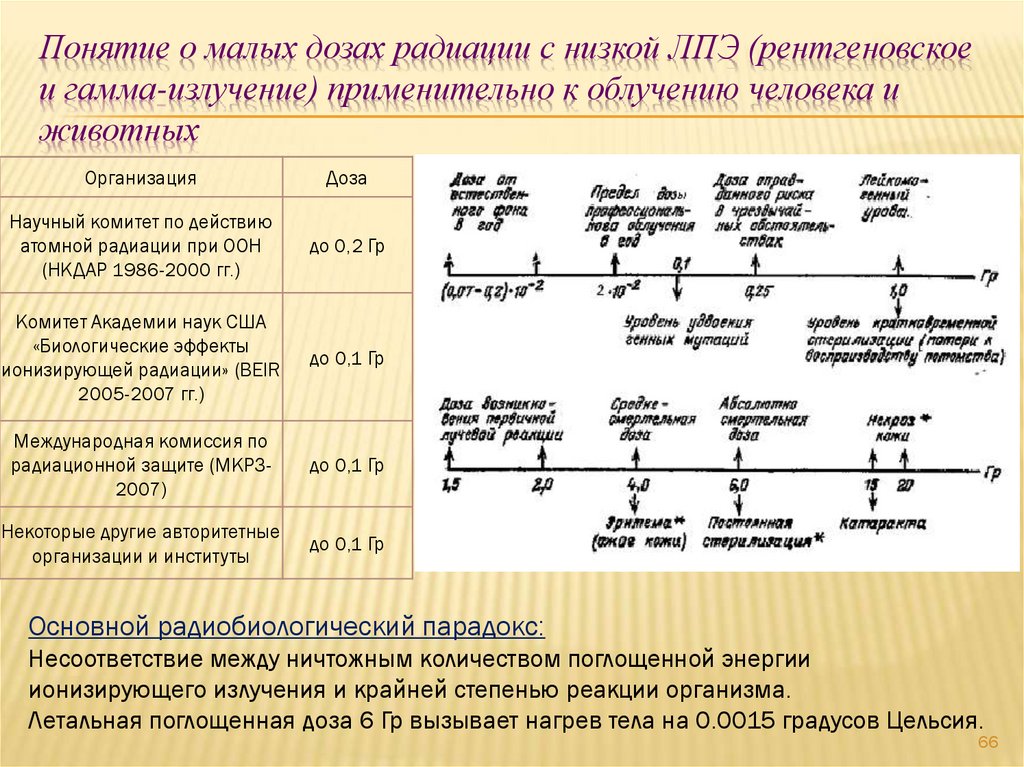
66. Понятие о малых дозах радиации с низкой ЛПЭ (рентгеновское и гамма-излучение) применительно к облучению человека и животных
ОрганизацияДоза
Научный комитет по действию
атомной радиации при ООН
(НКДАР 1986-2000 гг.)
до 0,2 Гр
Комитет Академии наук США
«Биологические эффекты
ионизирующей радиации» (BEIR
2005-2007 гг.)
до 0,1 Гр
Международная комиссия по
радиационной защите (МКРЗ2007)
до 0,1 Гр
Некоторые другие авторитетные
организации и институты
до 0,1 Гр
Основной радиобиологический парадокс:
Несоответствие между ничтожным количеством поглощенной энергии
ионизирующего излучения и крайней степенью реакции организма.
Летальная поглощенная доза 6 Гр вызывает нагрев тела на 0.0015 градусов Цельсия.
66
67. Концепция нулевого риска
Суть концепции нулевого риска в отношении радиации состоитв том, что ее воздействие на организм человека имеет
пороговый характер, т. е. проявление воздействия радиации
наблюдается только при дозах, превышающих некоторое
предельно допустимое значение. Как отмечалось выше,
детерминированные соматические поражения имеют
пороговый характер в зависимости от дозы облучения, поэтому
установление в нормах радиационной безопасности предельно
допустимой дозы облучения для персонала, работающего с
источниками ионизирующего излучения, ниже этой пороговой
величины полностью исключает возможность соматических
поражений при работе в полях излучений, удовлетворяющих
требованиям НРБ.
67
68. Обоснование пороговой концепции
1.2.
3.
4.
Жизнь на Земле возникла и эволюционирует в условиях
постоянного действия ИИ в «малых» дозах. В процессе облучения
бесчисленных поколений растений, животных, человека не
накоплен груз, несовместимый с жизнью.
В регионах с повышенным естественным радиационным фоном
(ЕРФ) не выявлено изменений состояния здоровья местного
населения по сравнению с населением, проживающим в регионах
со средне земным уровнем ЕРФ.
При облучении организм не ведет себя пассивно. Первоначальные
эффекты не обязательно транслируются на более высокие уровни.
По данным эпидемиологических наблюдений, не зарегистрировано
убедительных доказательств увеличения числа злокачественных
новообразований и генетических нарушений у облученных в
«малых» дозах.
68
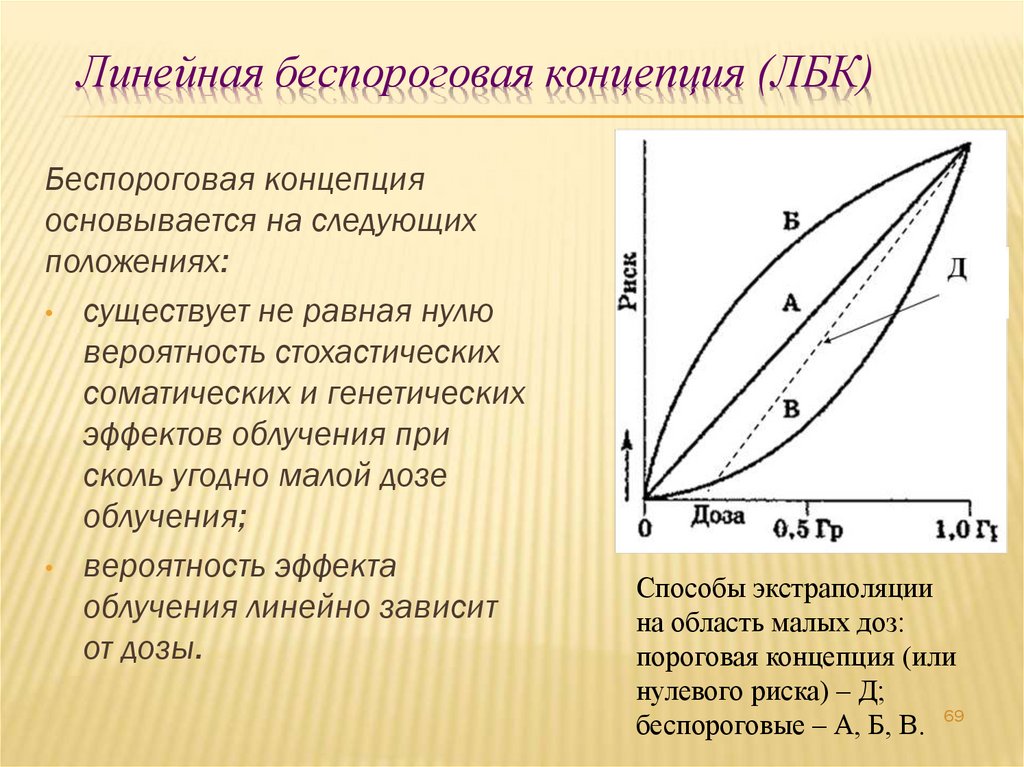
69. Линейная беспороговая концепция (ЛБК)
Беспороговая концепцияосновывается на следующих
положениях:
• существует не равная нулю
вероятность стохастических
соматических и генетических
эффектов облучения при
сколь угодно малой дозе
облучения;
• вероятность эффекта
облучения линейно зависит
от дозы.
Способы экстраполяции
на область малых доз:
пороговая концепция (или
нулевого риска) – Д;
беспороговые – А, Б, В. 69
70. Обоснование ЛБК
1.2.
3.
Особенности
биологического
действия
ИИ,
заключающиеся в процессах ионизации и возбуждения
атомов и молекул с последующим образованием
перекисей и радикалов, отмечаются при любой дозе
облучения. Количество изменений зависит только от дозы
облучения, т.е. от поглощенной энергии.
Моноклоновость большинства новообразований, т.е.
развитие
опухоли
из
одной
или
нескольких
неопластически измененных клеток.
Развитие клонов клеток до фазы прогрессии опухоли
может протекать при неизмененном иммунологическом и
гормональном статусе организма.
70
71. Радиационный гормезис
Гормезис – обозначение инверсионной биологической,физиологической или биохимической реакции организма на
«малые» дозы какого-либо воздействия, противоположной той,
которая развивается на более высокие дозы.
Позитивный эффект «малых» доз известен как радиационный
гормезис. Данная теория предполагает наличие диапазона доз,
оказывающих благоприятное действие на различные
проявления жизнедеятельности. При этом утверждается, что
кривая доза – эффект в ее самой начальной части может
отклоняться от линейной зависимости. Уровни доз, вызывающие
положительные радиационные эффекты, могут значительно
отличаться для данного вида организма, его различных тканей,
определенного процесса и могут колебаться у млекопитающих
от 0,1 до 1,5 Гр.
71
72. Радиоадаптивный ответ
Радиоадаптивный ответ Еще одним указанием нахарактеризуется четкой существование радиационного
дозовой зависимостью – гормезиса служат эксперименты,
он инициируется дозой
10-50 мГр, и проверяется свидетельствующие о том, что под
эффект адаптации дозой влиянием «малых» доз ИИ
естественная продолжительность жизни
100-1500 мГр. Иначе
животных увеличивается на 10–12% по
говоря, клетка,
получившая дозу 10-50
сравнению с адекватным контролем.
мГр, приобретает
Гамма-облучение в «малых» дозах
устойчивость к
стимулирует прорастание семян,
последующему
вызывает увеличение вегетативной
повреждающему
массы растений. «Малые» дозы
воздействию в дозе,
которая на 1-2 порядка активируют иммунную систему у разных
видов животных и ключевые
выше инициирующей.
мембраносвязанные ферменты,
активируют репарационные системы.
72
73. Основные пределы доз согласно НРБ-99/2009
Нормируемыевеличины
Эффективная доза
Персонал (группа А)
20 мЗв в год
Население
1 мЗв в год
в среднем за любые в среднем за любые
последовательные 5 лет, но последовательные 5 лет, но
не более 50 мЗв в год
не более 5 мЗв в год
Эквивалентная
доза за год в:
хрусталике глаза
150 мЗв
15 мЗв
коже
500 мЗв
50 мЗв
кистях и стопах
500 мЗв
50 мЗв
73
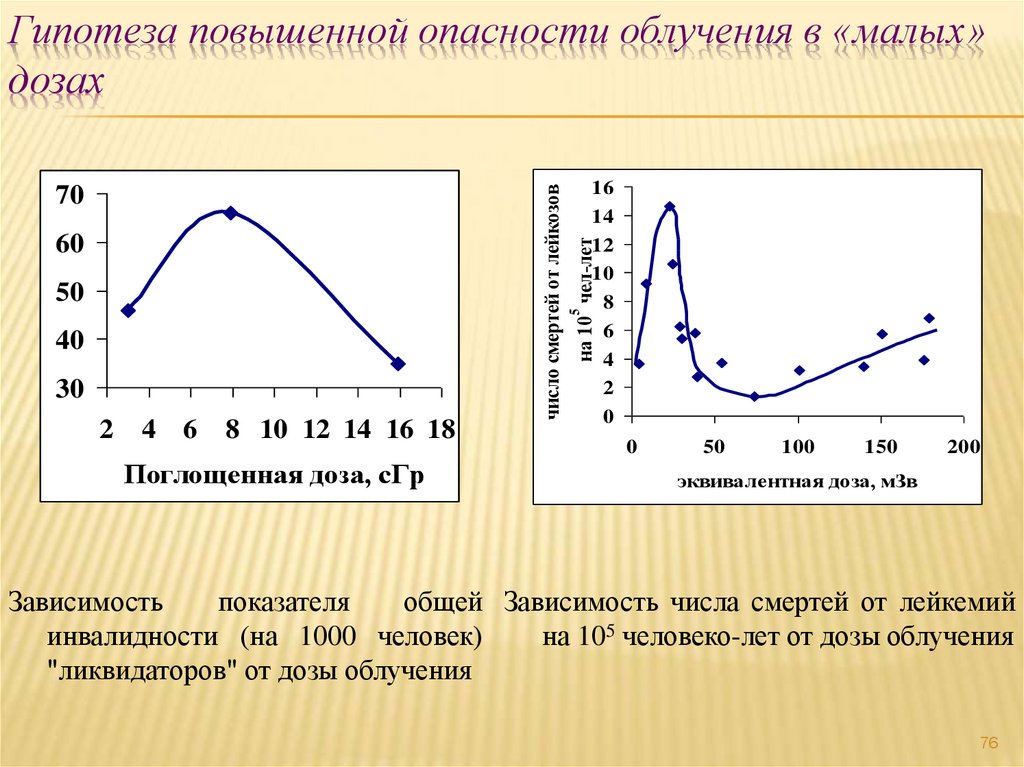
74. Гипотеза повышенной опасности облучения в «малых» дозах
Согласно гипотезе, об усилении эффекта облучения со снижениемдозы, в области «малых» доз на единицу дозы риск значительно
выше, чем при «больших» дозах. Существуют исследования,
показывающие, что канцерогенная опасность при «малых» дозах
облучения в 20–30 раз выше значений, представляемых НКДАР
и МКРЗ. Причиной этого считается, что «малые» дозы очень
опасны, поскольку у организмов нет системы защиты от них и,
более того, они провоцируют у человека самые разные
заболевания, в том числе сердечно-сосудистой и нервной
системы, которые обычно не связывают с прямым действием
радиации.
Исследованиями доказано, что облучение в малых дозах
вызывает многочисленные структурные перестройки в клетках,
приводя к изменению их функциональной активности. Более того,
когда мы воздействуем на клеточную мембрану, облучая весь
организм, практически одинаковые изменения происходят и при
очень больших, и при очень малых дозах. То есть малыми дозами
радиации можно, например, убить клетку так же, как и большими,
если речь идет не о разовом, а длительном воздействии.
74
75. Гипотеза повышенной опасности облучения в «малых» дозах
Например, если при 100 рентгенах организм может что-то восстановить, то ужпри 1 рентгене обязательно ликвидирует повреждения. Но 99 процентов
неприятностей, которые можно «снять» при высокой дозе и мощности, остаются
при малых. Можно получить 100 рентген за один раз, а можно растянуть эту
дозу на длительное время. И в этом случае 100 рентген единовременно - это
хуже. Доза в 15 рентген - и сразу, и частями - даст примерно одинаковые
последствия. А вот 1 рентген, полученный за раз, может нанести меньший
вред, чем та же доза, растянутая на несколько приемов, скажем, в течение
месяца.
Выживает тот, у кого все-таки получается адаптироваться.
слабое облучение действует опосредованно, запуская механизмы геномной
регуляции. Например, можно спровоцировать апоптоз - запрограммированную
гибель клетки. Тогда высокие дозы радиации приводят к гибели,
непосредственно повреждая молекулу ДНК, а малые - через экспрессию гена и
появление белков, которые и запустят механизм запрограммированной
гибели. Кстати, тот же апоптоз для организма в целом может быть очень
положительным явлением, например, когда самоуничтожается раковая клетка.
75
76. Гипотеза повышенной опасности облучения в «малых» дозах
5040
30
2
4 6
8 10 12 14 16 18
Поглощенная доза, сГр
5
60
16
14
12
10
8
6
4
2
0
на 10 чел-лет
70
число смертей от лейкозов
Гипотеза повышенной опасности облучения в «малых»
дозах
0
50
100
150
200
эквивалентная доза, мЗв
Зависимость
показателя
общей Зависимость числа смертей от лейкемий
инвалидности (на 1000 человек)
на 105 человеко-лет от дозы облучения
"ликвидаторов" от дозы облучения
76
77. Гипотеза повышенной опасности облучения в «малых» дозах
1. Смертельные случаи от лейкозов при облучении в малых дозахмогут быть по величинам сопоставимы со смертностью от лейкозов
для доз облучения в десятки раз более высоких.
2.
Для низких доз облучения (до 10 сЗв) имеется область доз, где
наблюдается уменьшение эффекта с увеличением дозы, доходящее
до смены знака эффекта - до уменьшения смертей от лейкозов
ниже уровня контроля.
3.
Различная зависимость эффекта от дозы в области малых и
высоких доз облучения позволяет думать о разных механизмах,
лежащих в основе увеличения смертности от лейкозов при малых и
высоких дозах облучения. Одним из объяснений может быть
указанное выше соображение о разных функциях облучения в
канцерогенезе, а именно - для низких доз облучения главное промотирующая функция облучения, для высоких - индуцирующая
или же разное соотношение между системами восстановления и
повреждения при низких и высоких дозах.
77





















































 life safety
life safety








