Similar presentations:
Идеальный календарь профилактических прививок: актуальные возможности вакцинопрофилактики детей и подростков
1. Идеальный календарь профилактических прививок: актуальные возможности вакцинопрофилактики детей и подростков
Научно-практическая конференцияИдеальный календарь профилактических прививок: актуальные
возможности вакцинопрофилактики детей и подростков
03.06.2025
Щекино, Болдина, 1. Щекинская районная больница
Идеальный календарь профилактических
прививок: актуальные возможности
вакцинопрофилактики детей и подростков
Юдакова Ольга Викторовна,
главный внештатный специалист эпидемиолог департамента
здравоохранения министерства здравоохранения Тульской области
MAT-RU-2502106_v1.0_06-2025
Материал подготовлен в рамках осуществления научной деятельности при поддержке компании АО «Санофи Россия». Упоминание международных непатентованных наименований / торговых
наименований препаратов приведено в данной презентации исключительно в научных целях и не направлено на продвижение, привлечение внимания или акцентирование преимуществ какоголибо препарата или производителя. Информация предназначена исключительно для медицинских работников.
2.
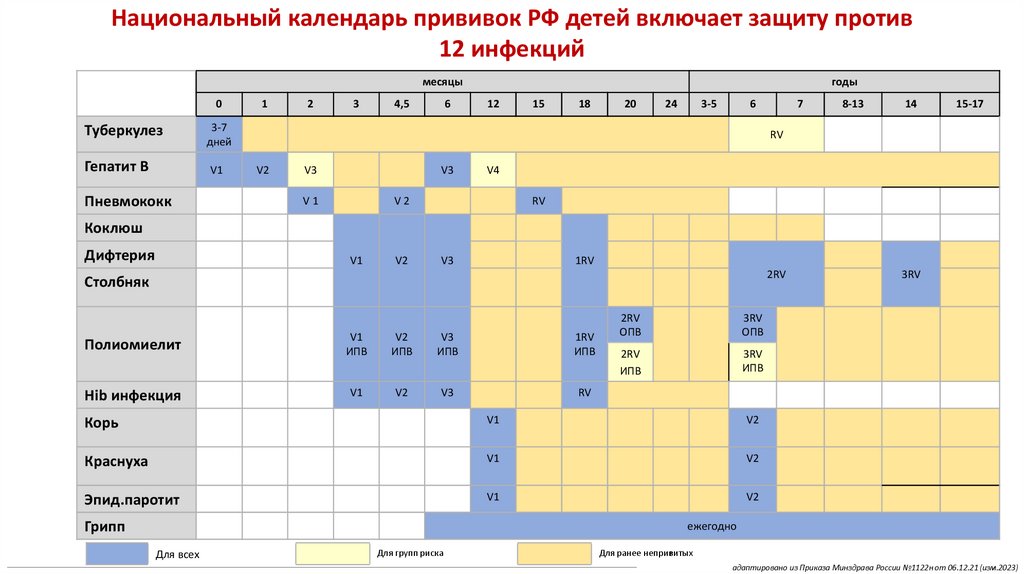
Национальный календарь прививок РФ детей включает защиту против12 инфекций
месяцы
0
Туберкулез
3-7
дней
Гепатит В
V1
Пневмококк
1
2
3
4,5
6
годы
12
15
18
20
24
3-5
6
7
8-13
14
15-17
RV
V2
V3
V3
V1
V4
V2
RV
Коклюш
Дифтерия
V1
V2
V3
1RV
2RV
Столбняк
Полиомиелит
V1
ИПВ
V2
ИПВ
V3
ИПВ
1RV
ИПВ
Hib инфекция
V1
V2
V3
RV
2RV
ОПВ
3RV
ОПВ
2RV
ИПВ
3RV
ИПВ
Корь
V1
V2
Краснуха
V1
V2
Эпид.паротит
V1
V2
Грипп
3RV
ежегодно
Для всех
Для групп риска
Для ранее непривитых
адаптировано из Приказа Минздрава России №1122н от 06.12.21 (изм.2023)
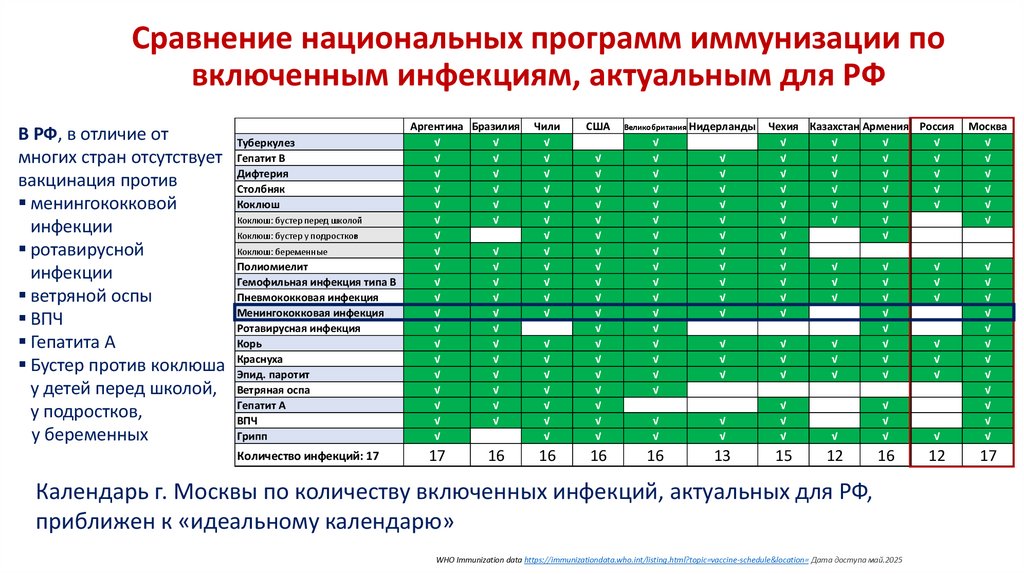
3. Сравнение национальных программ иммунизации по включенным инфекциям, актуальным для РФ
В РФ, в отличие отТуберкулез
многих стран отсутствует Гепатит В
Дифтерия
вакцинация против
Столбняк
Коклюш
менингококковой
Коклюш: бустер перед школой
инфекции
Коклюш: бустер у подростков
Коклюш: беременные
ротавирусной
Полиомиелит
инфекции
Гемофильная инфекция типа В
Пневмококковая инфекция
ветряной оспы
Менингококковая инфекция
ВПЧ
Ротавирусная инфекция
Корь
Гепатита А
Бустер против коклюша Краснуха
Эпид. паротит
у детей перед школой, Ветряная оспа
Гепатит А
у подростков,
ВПЧ
Грипп
у беременных
Количество инфекций: 17
Аргентина Бразилия
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
17
16
Чили
√
√
√
√
√
√
√
√
√
√
√
√
США
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
16
16
Великобритания Нидерланды
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
Чехия Казахстан Армения Россия
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
16
13
15
Москва
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
12
16
12
17
Календарь г. Москвы по количеству включенных инфекций, актуальных для РФ,
приближен к «идеальному календарю»
WHO Immunization data https://immunizationdata.who.int/listing.html?topic=vaccine-schedule&location= Дата доступа май.2025
4.
Региональный календарь Тульской области (2017)(с изм. от 21.01.2022г. № 43-осн)
Вакцинация против ветряной оспы:
-Дети 24 месяцев (не болевшие и не привитые ранее при оформлении в детское
дошкольное учреждение);
-Дети с 12 мес. до 18 лет, находившиеся в тесном контакте с больным ветряной оспой
(не болевшие и не привитые ранее);
-Лица, подлежащие призыву на военную службу;
-Взрослые старше 18 лет, находившиеся в тесном контакте с больным ветряной оспой
(не болевшие и не привитые ранее)
Вакцинация против ротавирусной инфекции:
Дети до 8 мес.
(в 2, 3 и 4,5 мес.)
Вторая ревакцинация против коклюша
(комбинированной вакциной с уменьшенным содержанием дифтерийных и столбнячных
антигенов, и содержанием ацеллюлярного коклюшного компонента) – дети в 6 – 7 лет
Данные из личного архива Юдаковой О.В., 2024
5.
Вакцинация против вируса папилломы человека:до 2022 г. – девочки с 12-ти лет
с 2022г. - Дети с 9 лет (в том числе из социально неблагополучных слоев населения региона (школы-интернаты,
детские дома)
Вакцинация против менингококковой инфекции:
- лица, подлежащие призыву на военную службу;
- дети от 2 до 5 лет;
- контактные в очагах генерализованной формы менингококковой инфекции, включая медицинских работников;
- паломники
Вакцинация против пневмококковой инфекции:
- лица, подлежащие призыву на военную службу;
- лица старше 50 лет, страдающие хроническими заболеваниями;
- лица старше 60 лет, проживающие в социальных учреждениях
Вакцинация против природно-очаговых инфекций:
туляремии – лица, проживающие на эндемичных территориях;
сибирской язвы, лептоспироза и бешенства – лица, имеющие профессиональный риск заражения
Данные из личного архива Юдаковой О.В., 2024
6. Вакцинопрофилактика должна учитывать вызовы нового времени
Широкое применение вакцинации независимо от возраста, сучётом особенностей состояния здоровья, профессионального риска,
образа жизни, территориальных характеристик
Информационно-разъяснительная
работа
с
населением
и
профессиональное обучение специалистов различного профиля
вопросам вакцинопрофилактики
Важное внимание успешной коммуникации с населением
Юдакова О.В, из личного архива
7.
78. Проблемы на пути достижения Идеального календаря прививок
• Невыполнение действующего НКПП• Недостаточный уровень знаний медицинских
специалистов
• Низкий уровень информированности населения
вопросам вакцинации
• Низкий уровень приверженности населения
• Экономические и политические проблемы в ходе
реализации Стратегии иммунопрофилактики
• Ограничение назначения и использования
вакцинации в группах риска и широких возрастных
группах
• Неправильное толкование
противопоказаний
• Нарушения оформления
документов о вакцинации
• Нарушения вакцинального
статуса после пандемии………..
Юдакова О.В, из личного архива
9. Идеальный календарь иммунизации детей и подростков Рекомендации Союза педиатров России
• оптимальный календарь детских прививок• разрабатывался для родителей, желающих защитить своих детей от серьезных
инфекций и их тяжелых осложнений;
• включает прививки против 18 наиболее актуальных инфекций:
• к уже существующим в НКПП 12 вакцинам добавлена иммунизация:
РСВИ
ротавирусной инфекции,
ветряной оспы,
менингококковой инфекции,
вирусного гепатита А,
папилломавирусной инфекции,
клещевого энцефалита (для регионов, где актуально)
ревакцинации против коклюша
Идеальный календарь иммунизации Союза педиатров России. https://www.pediatr-russia.ru/information/vaktsinatsiya/kalendar-vaktsinatsii/ доступ май 2025
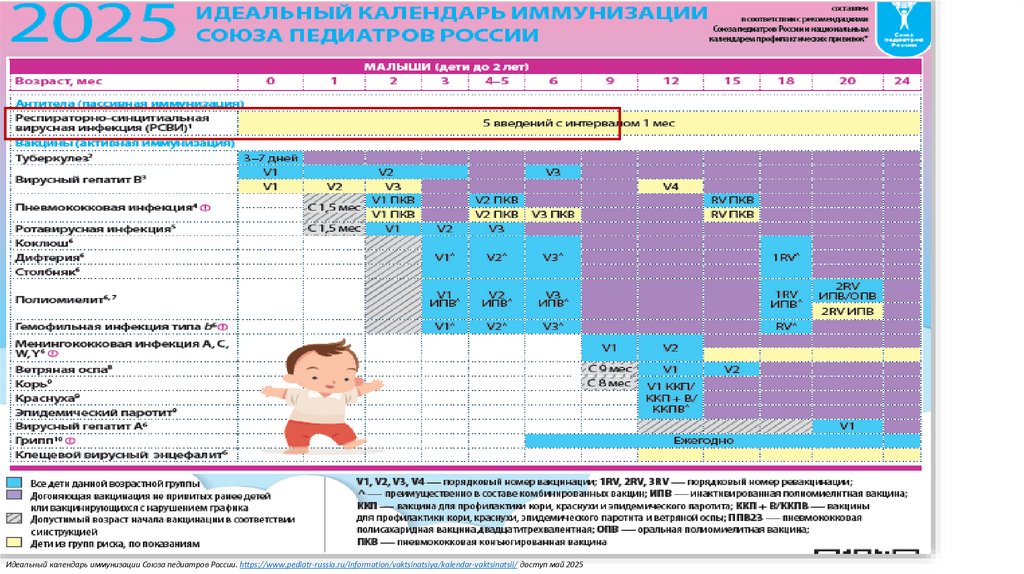
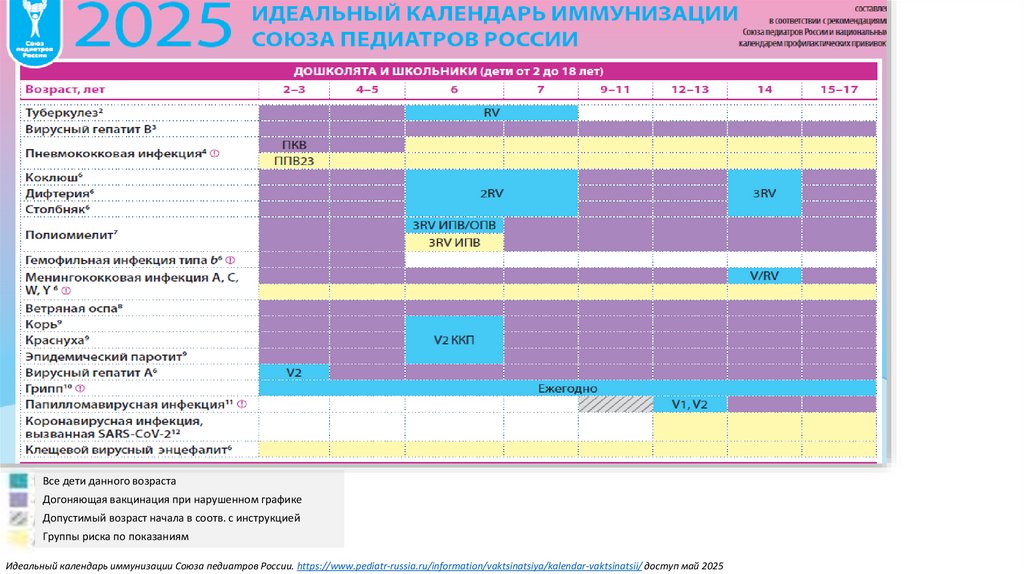
10.
Идеальный календарь иммунизации Союза педиатров России. https://www.pediatr-russia.ru/information/vaktsinatsiya/kalendar-vaktsinatsii/ доступ май 202511.
Все дети данного возрастаДогоняющая вакцинация при нарушенном графике
Допустимый возраст начала в соотв. с инструкцией
Группы риска по показаниям
Идеальный календарь иммунизации Союза педиатров России. https://www.pediatr-russia.ru/information/vaktsinatsiya/kalendar-vaktsinatsii/ доступ май 2025
12.
1. Внесение изменений в НКПП:- Вакцинация против Hib всех младенцев
-
Вакцинация ИПВ всей когорты младенцев
V1-V3-1RV в составе комбинированных
вакцин
-
Ревакцинация общей когорты ОПВ в 20
мес, в 6 и 14 лет
-
Ревакцинация групп риска ИПВ в 6 и 14 лет
2. Внесение изменений в календарь профилактических прививок по эпидемическим показаниям:
- Расширение контингентов для вакцинации против менингококковой инфекции
- Включение ревакцинации
комбинированных вакцин
против
коклюша
определенным
категориям
- Расширение контингентов для вакцинации против ветряной оспы
- Расширение контингентов для вакцинации против пневмококковой инфекции
- Включение вакцинации против ВПЧ детям обоего пола в 11-12 лет
• Совершенствование национального календаря профилактических прививок. Резолюция Независимого Экспертного совета в сфере иммунопрофилактики.
Педиатрическая фармакология. 2021;18(1):85-87.
• Юдакова О.В из личного архива
граждан
c
использованием
13.
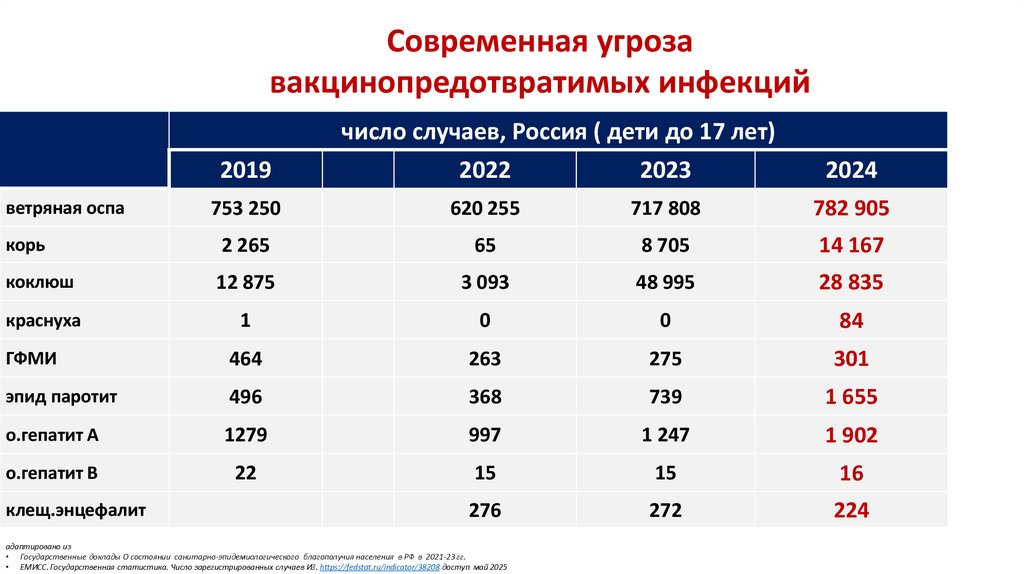
Современная угрозавакцинопредотвратимых инфекций
2019
число случаев, Россия ( дети до 17 лет)
2022
2023
2024
ветряная оспа
753 250
620 255
717 808
782 905
корь
2 265
65
8 705
14 167
коклюш
12 875
3 093
48 995
28 835
краснуха
1
0
0
84
ГФМИ
464
263
275
301
эпид паротит
496
368
739
1 655
о.гепатит А
1279
997
1 247
1 902
о.гепатит В
22
15
15
16
276
272
224
клещ.энцефалит
адаптировано из
• Государственные доклады О состоянии санитарно-эпидемиологического благополучия населения в РФ в 2021-23 гг.
• ЕМИСС. Государственная статистика. Число зарегистрированных случаев ИЗ. https://fedstat.ru/indicator/38208 доступ май 2025
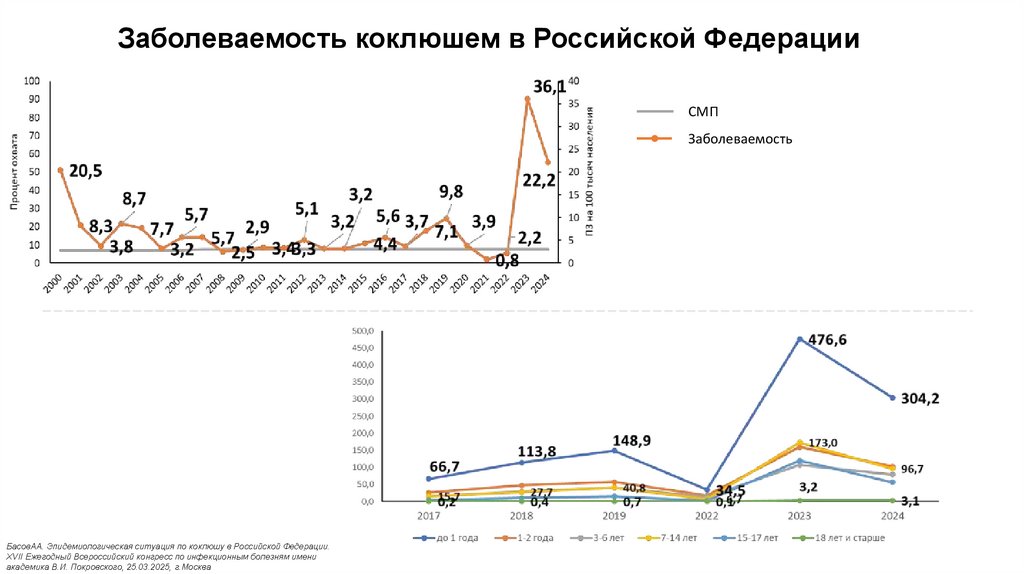
14. Заболеваемость коклюшем в Российской Федерации
СМПЗаболеваемость
БасовАА. Эпидемиологическая ситуация по коклюшу в Российской Федерации.
XVII Ежегодный Всероссийский конгресс по инфекционным болезням имени
академика В.И. Покровского, 25.03.2025, г.Москва
15.
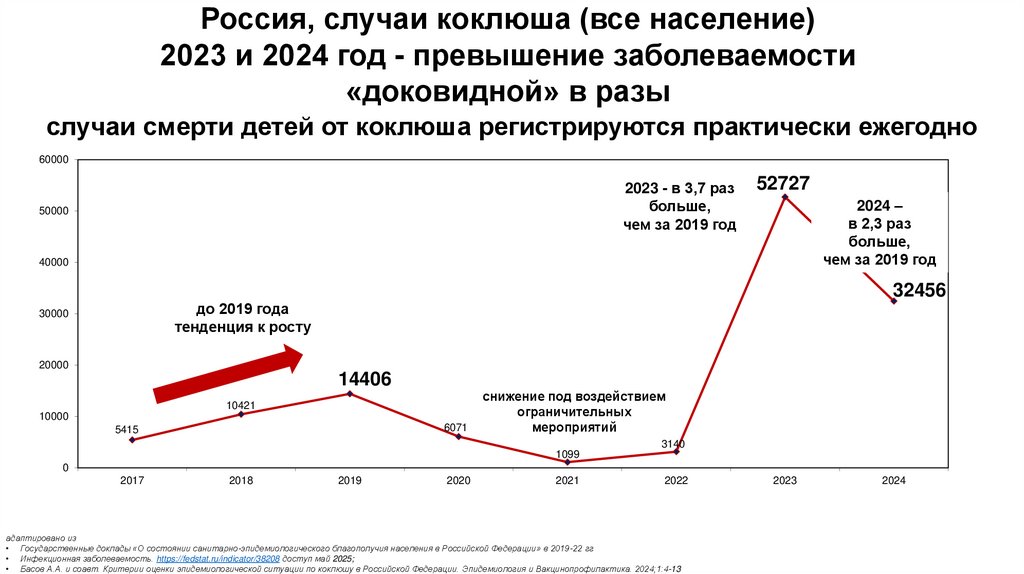
Россия, случаи коклюша (все население)2023 и 2024 год - превышение заболеваемости
«доковидной» в разы
случаи смерти детей от коклюша регистрируются практически ежегодно
60000
2023 - в 3,7 раз
больше,
чем за 2019 год
50000
52727
2024 –
в 2,3 раз
больше,
чем за 2019 год
40000
32456
до 2019 года
тенденция к росту
30000
20000
14406
10421
10000
6071
5415
снижение под воздействием
ограничительных
мероприятий
3140
1099
0
2017
2018
2019
2020
2021
2022
адаптировано из
• Государственные доклады «О состоянии санитарно-эпидемиологического благополучия населения в Российской Федерации» в 2019-22 гг
• Инфекционная заболеваемость. https://fedstat.ru/indicator/38208 доступ май 2025;
• Басов А.А. и соавт. Критерии оценки эпидемиологической ситуации по коклюшу в Российской Федерации. Эпидемиология и Вакцинопрофилактика. 2024;1:4-13
2023
2024
16. Основные причины роста заболеваемости коклюшем
1. Защитный иммунитет после вакцинации и послеперенесенного заболевания уменьшается со временем
2. Неполная регистрация случаев коклюша у школьников
старших классов и взрослых
3. Увеличение доли восприимчивых к коклюшу лиц в период
ограничительных мероприятий для профилактики ковид-19
(«иммунный долг»)
4. Увеличение количества расшифрованных случаев коклюша
благодаря повсеместному внедрению ПЦР-диагностики
Басов А. А. и соавт. Критерии оценки эпидемиологической ситуации коклюша в Российской Федерации. Эпидемиология и Вакцинопрофилактика. 2024;1:4-13
БасовАА. Эпидемиологическая ситуация по коклюшу в Российской Федерации. XVII Ежегодный Всероссийский конгресс по инфекционным болезням имени академика В.И. Покровского,
25.03.2025, г.Москва
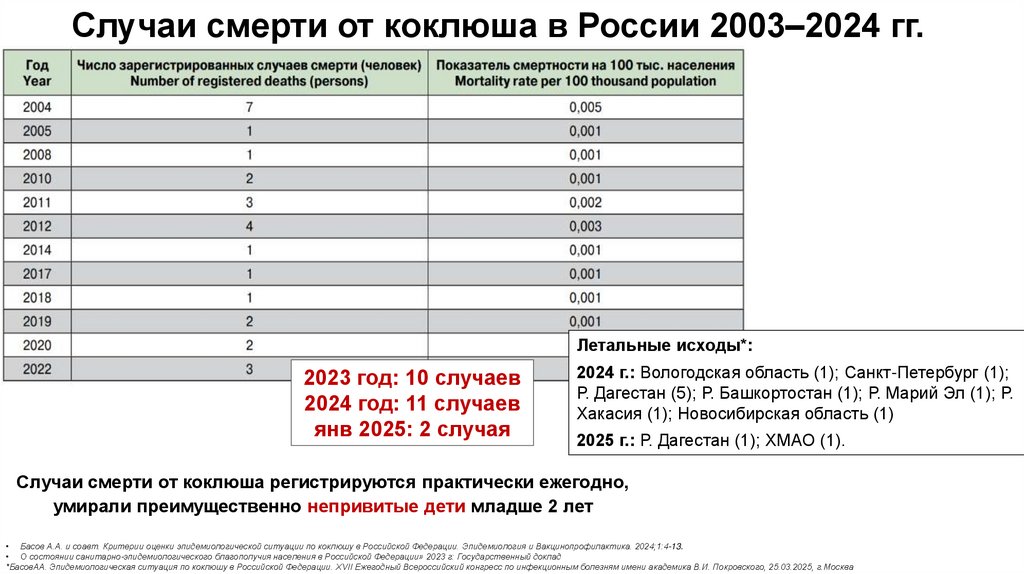
17. Случаи смерти от коклюша в России 2003–2024 гг.
Летальные исходы*:2023 год: 10 случаев
2024 год: 11 случаев
янв 2025: 2 случая
2024 г.: Вологодская область (1); Санкт-Петербург (1);
Р. Дагестан (5); Р. Башкортостан (1); Р. Марий Эл (1); Р.
Хакасия (1); Новосибирская область (1)
2025 г.: Р. Дагестан (1); ХМАО (1).
Случаи смерти от коклюша регистрируются практически ежегодно,
умирали преимущественно непривитые дети младше 2 лет
• Басов А.А. и соавт. Критерии оценки эпидемиологической ситуации по коклюшу в Российской Федерации. Эпидемиология и Вакцинопрофилактика. 2024;1:4-13.
• О состоянии санитарно-эпидемиологического благополучия населения в Российской Федерации» 2023 г: Государственный доклад
*БасовАА. Эпидемиологическая ситуация по коклюшу в Российской Федерации. XVII Ежегодный Всероссийский конгресс по инфекционным болезням имени академика В.И. Покровского, 25.03.2025, г.Москва
18. Коклюш тяжелее всего протекает у детей <12 мес.
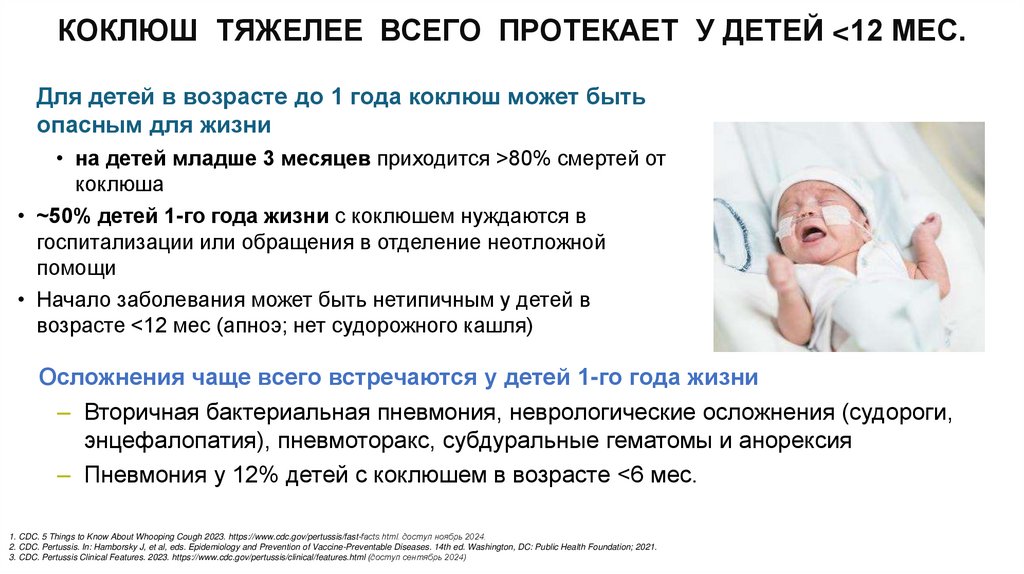
КОКЛЮШ ТЯЖЕЛЕЕ ВСЕГО ПРОТЕКАЕТ У ДЕТЕЙ <12 МЕС.Для детей в возрасте до 1 года коклюш может быть
опасным для жизни
• на детей младше 3 месяцев приходится >80% смертей от
коклюша
• ~50% детей 1-го года жизни с коклюшем нуждаются в
госпитализации или обращения в отделение неотложной
помощи
• Начало заболевания может быть нетипичным у детей в
возрасте <12 мес (апноэ; нет судорожного кашля)
Осложнения чаще всего встречаются у детей 1-го года жизни
– Вторичная бактериальная пневмония, неврологические осложнения (судороги,
энцефалопатия), пневмоторакс, субдуральные гематомы и анорексия
– Пневмония у 12% детей с коклюшем в возрасте <6 мес.
1. CDC. 5 Things to Know About Whooping Cough 2023. https://www.cdc.gov/pertussis/fast-facts.html. доступ ноябрь 2024.
2. CDC. Pertussis. In: Hamborsky J, et al, eds. Epidemiology and Prevention of Vaccine-Preventable Diseases. 14th ed. Washington, DC: Public Health Foundation; 2021.
3. CDC. Pertussis Clinical Features. 2023. https://www.cdc.gov/pertussis/clinical/features.html (доступ сентябрь 2024)
19.
Осложнения коклюша. Младенцы и детиЛегочные, неврологические и нарушения питания
• Наиболее частые - легочные осложнения. У подавляющего большинства
перенесших коклюш - ателектазы различной степени выраженности или
бронхопневмонии
• Острая коклюшная энцефалопатия - обычно на пароксизмальной стадии,
судороги в результате гипоксии или внутричерепного кровоизлияния, связанных с
приступами кашля
• Пищевые нарушения - дефицит питательных веществ в результате
повторяющейся рвоты
• Нетяжелые осложнения коклюша - субконъюнктивальные кровоизлияния,
носовые кровотечения как последствия приступообразного кашля, отечность лица,
язвочки на уздечке языка из-за высовывания во время приступа.
• Часто возникает гнойный средний отит, вызываемый обычными бактериями
верхних дыхательных путей, не B.pertussis.
Вакцины против коклюша: документ по позиции ВОЗ – август 2015 г. Еженедельный эпидемиологический бюллетень. 2015;35:433-460
Pertussis Vaccines in Plotkin’s Vaccines ed8th © 2023 Elsevier Inc. All rights reserved. ISBN 978-0-323-79058-1
20.
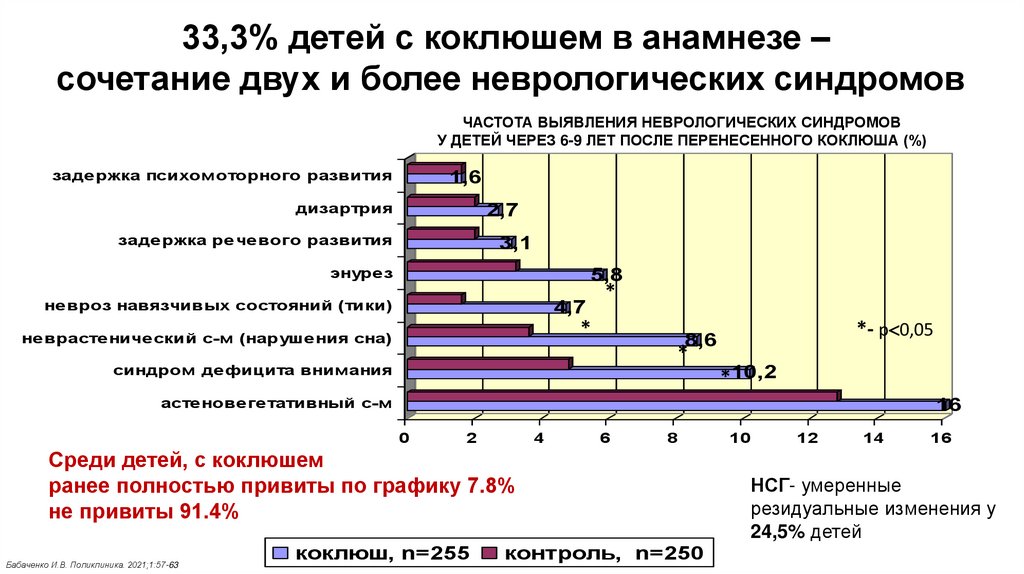
33,3% детей с коклюшем в анамнезе –сочетание двух и более неврологических синдромов
ЧАСТОТА ВЫЯВЛЕНИЯ НЕВРОЛОГИЧЕСКИХ СИНДРОМОВ
У ДЕТЕЙ ЧЕРЕЗ 6-9 ЛЕТ ПОСЛЕ ПЕРЕНЕСЕННОГО КОКЛЮША (%)
1,6
заде ржка психомоторного развития
2,7
дизартрия
заде ржка ре че вого развития
3,1
5,8
энуре з
не вроз навязчивых состояний (тики)
4,7
не врасте ниче ский с-м (наруше ния сна)
*
*
*- р 0,05
8,6
*
синдром де фицита внимания
*10,2
16
асте нове ге тативный с-м
0
2
4
6
8
Среди детей, с коклюшем
ранее полностью привиты по графику 7.8%
не привиты 91.4%
Бабаченко И.В. Поликлиника. 2021;1:57-63
коклюш, n=255
контроль, n=250
10
12
14
16
НСГ- умеренные
резидуальные изменения у
24,5% детей
21. Частота выявления неврологических синдромов у детей через 6-9 лет после перенесенного коклюша (%)
Осложнения коклюша. Подростки и взрослые• средний отит
• пневмония
• недержание мочи
• перелом ребра
• сильная потеря веса
• проблемы со сном и работоспособностью
(ночной кашель)
• мигрень, обмороки при кашле, потеря
памяти
• расслоение сонной артерии
• случаи смерти от коклюша у подростков и
взрослых редки, но регистрируются
• Коклюш у подростков и
взрослых не всегда просто
«легкий кашель»
• - кашель ≥3 недель, может
длиться ≥9 недель
• - в среднем 14 дней нарушенного
сна
• - взрослые могут пропустить в
среднем 7 дней работы
• - подростки могут пропустить в
среднем 5 дней учебы
Вакцины против коклюша: документ по позиции ВОЗ – август 2015 г. Еженедельный эпидемиологический бюллетень. 2015;35:433-460
Pertussis Vaccines in Plotkin’s Vaccines ed8th © 2023 Elsevier Inc. All rights reserved. ISBN 978-0-323-79058-1
De Serres G, Shadmani R, Duval B, Boulianne N, Déry P, Douville Fradet M, Rochette L, Halperin SA. Morbidity of pertussis in adolescents and adults. J Infect Dis. 2000 Jul;182(1):174-9.
22.
У ЛЮДЕЙ С ХОБЛ ИЛИ БРОНХИАЛЬНОЙ АСТМОЙЧАЩЕ РАЗВИВАЕТСЯ ТЯЖЕЛЫЙ КОКЛЮШ
Когорта людей с БА 960 494 пациента, в сравнении с 3 841 976 человек в общей численности населения (данные США 2007-2019 гг)
ХОБЛ
и
бронхиальная астма
Коклюш
Риск развития коклюша выше по сравнению с населением в целом
• у пациентов с бронхиальной астмой в 3,57 раза (95% ДИ 3,25-3,92)
• у пациентов с ХОБЛ в 1,83 раза (95% ДИ 1,57-2,12).
Риск развития коклюша с осложнениями выше по сравнению с
населением в целом
• у пациентов с бронхиальной астмой в 4,12 раза (95% ДИ 3,16-5,38)
• у пациентов с ХОБЛ в 2,82 раза (95% ДИ 2,14-3,27).
Naeger S, Pool V, Macina D. Increased Burden of Pertussis Among Adolescents and Adults With Asthma or COPD in the United States, 2007 to 2019.
Chest. 2024;6:1352-1361
23.
ЗАБОЛЕВАЕМОСТЬ КОКЛЮШЕМ СМЕЩАЕТСЯ В СТОРОНУДЕТЕЙ СТАРШЕГО ВОЗРАСТА, ПОДРОСТКОВ И ВЗРОСЛЫХ
Распределение коклюша по возрастам в странах с высоким охватом
вакцинацией сместилось в сторону детей старшего возраста, подростков и
взрослых1-3
• обусловлено постепенным ослаблением естественного и поствакцинального
иммунитета и улучшением диагностики1
Коклюш в возрастах, не охватываемых стандартной детской вакцинацией,
- серьезная проблема общественного здравоохранения4
• подростки и взрослые - важные источники инфекции для младенцев3
• 54% случаев коклюша, зарегистрированных в США в 2016 г., отмечены у лиц
в возрасте 11 лет и старше5
Большинство из них - пациенты от 11 до 19 лет
~8% взрослых >20 лет с коклюшем были госпитализированы
1. Tan T, et al. Pediatr Infect Dis J. 2005;24(5):S10-S18.
2. Schellekens J, et al. Pediatr Infect Dis J. 2005;24(5):S19-S24.
3. WHO. Wkly Epidemiol Record. 2015;90(35):433-460.
4. Kilgore PE, et al. Clin Microbiol Rev. 2016;29(3):449-486.
5. CDC. 2017 provisional pertussis surveillance report. https://www.cdc.gov/pertussis/downloads/pertuss-surv-report-2017.pdf. Дата доступа май 2025 г
24.
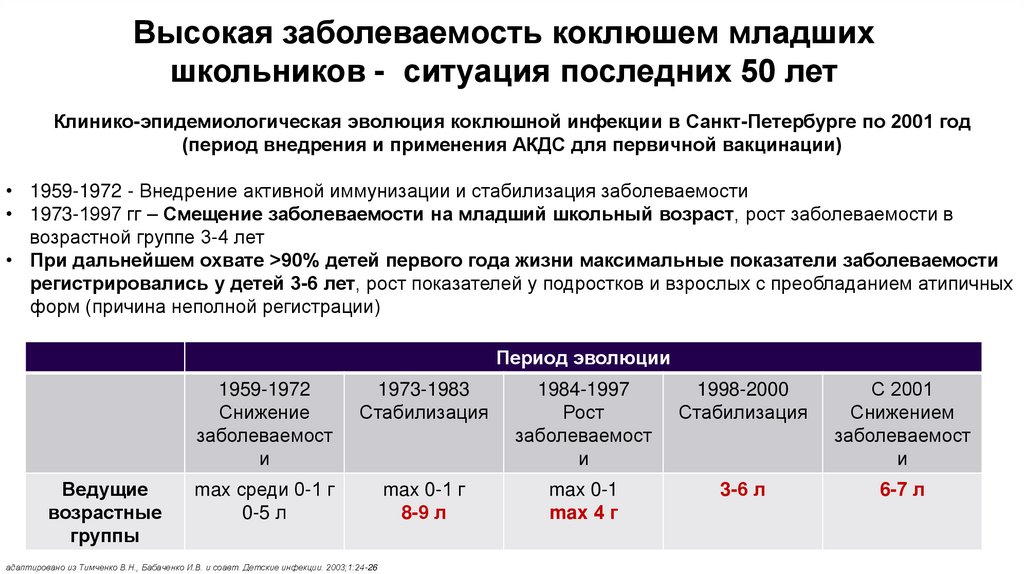
Высокая заболеваемость коклюшем младшихшкольников - ситуация последних 50 лет
Клинико-эпидемиологическая эволюция коклюшной инфекции в Санкт-Петербурге по 2001 год
(период внедрения и применения АКДС для первичной вакцинации)
• 1959-1972 - Внедрение активной иммунизации и стабилизация заболеваемости
• 1973-1997 гг – Смещение заболеваемости на младший школьный возраст, рост заболеваемости в
возрастной группе 3-4 лет
• При дальнейшем охвате >90% детей первого года жизни максимальные показатели заболеваемости
регистрировались у детей 3-6 лет, рост показателей у подростков и взрослых с преобладанием атипичных
форм (причина неполной регистрации)
Период эволюции
Ведущие
возрастные
группы
1959-1972
Снижение
заболеваемост
и
1973-1983
Стабилизация
1984-1997
Рост
заболеваемост
и
1998-2000
Стабилизация
С 2001
Снижением
заболеваемост
и
max среди 0-1 г
0-5 л
max 0-1 г
8-9 л
max 0-1
max 4 г
3-6 л
6-7 л
адаптировано из Тимченко В.Н., Бабаченко И.В. и соавт. Детские инфекции. 2003;1:24-26
25.
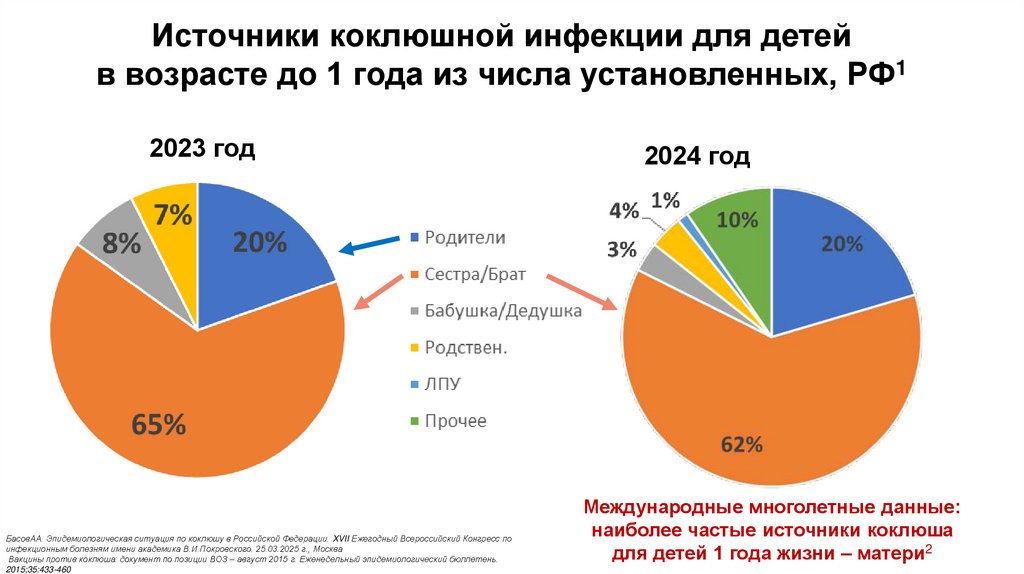
Источники коклюшной инфекции для детейв возрасте до 1 года из числа установленных, РФ1
2023 год
БасовАА. Эпидемиологическая ситуация по коклюшу в Российской Федерации. XVII Ежегодный Всероссийский Конгресс по
инфекционным болезням имени академика В.И.Покровского. 25.03.2025 г., Москва
Вакцины против коклюша: документ по позиции ВОЗ – август 2015 г. Еженедельный эпидемиологический бюллетень.
2015;35:433-460
2024 год
Международные многолетные данные:
наиболее частые источники коклюша
для детей 1 года жизни – матери2
26.
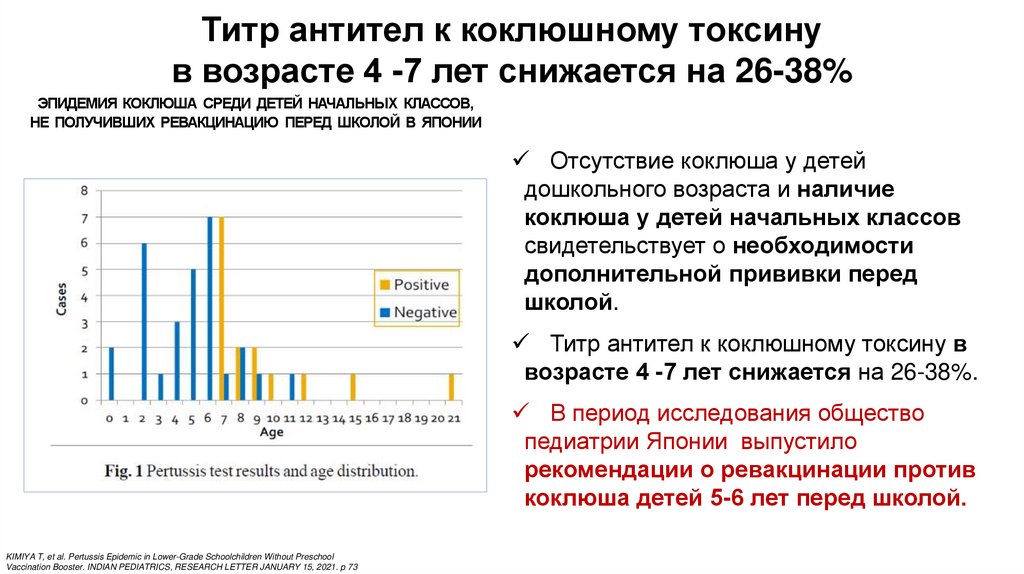
Титр антител к коклюшному токсинув возрасте 4 -7 лет снижается на 26-38%
ЭПИДЕМИЯ КОКЛЮША СРЕДИ ДЕТЕЙ НАЧАЛЬНЫХ КЛАССОВ,
НЕ ПОЛУЧИВШИХ РЕВАКЦИНАЦИЮ ПЕРЕД ШКОЛОЙ В ЯПОНИИ
Отсутствие коклюша у детей
дошкольного возраста и наличие
коклюша у детей начальных классов
свидетельствует о необходимости
дополнительной прививки перед
школой.
Титр антител к коклюшному токсину в
возрасте 4 -7 лет снижается на 26-38%.
В период исследования общество
педиатрии Японии выпустило
рекомендации о ревакцинации против
коклюша детей 5-6 лет перед школой.
KIMIYA T, et al. Pertussis Epidemic in Lower-Grade Schoolchildren Without Preschool
Vaccination Booster. INDIAN PEDIATRICS, RESEARCH LETTER JANUARY 15, 2021. p 73
27. эпидемия коклюша среди детей начальных классов, не получивших ревакцинацию перед школой в Японии
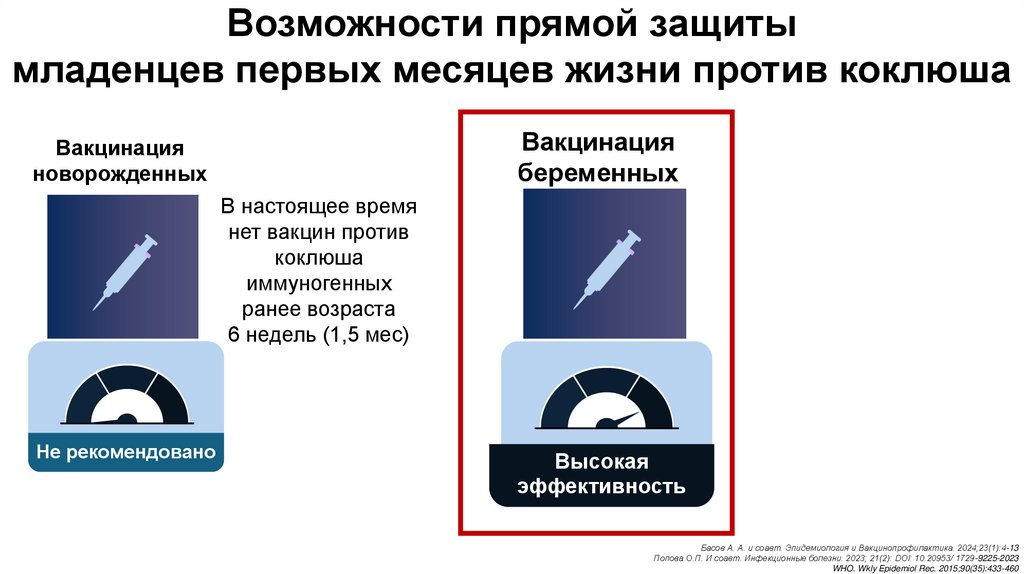
Возможности прямой защитымладенцев первых месяцев жизни против коклюша
Вакцинация
беременных
Вакцинация
новорожденных
В настоящее время
нет вакцин против
коклюша
иммуногенных
ранее возраста
6 недель (1,5 мес)
Не рекомендовано
Высокая
эффективность
Басов А. А. и соавт. Эпидемиология и Вакцинопрофилактика.
28 2024;23(1):4-13
Попова О.П. И соавт. Инфекционные болезни. 2023; 21(2): DOI: 10.20953/ 1729-9225-2023
WHO. Wkly Epidemiol Rec. 2015;90(35):433-460
28.
Клинические рекомендацииНормальная беременность, 2023
5.3. Вакцинация на предгравидарном этапе и
во время беременности
29.
ИНФОРМАЦИОННОЕ ПИСЬМОглавного детского инфекциониста ФМБА и Минздрава России
О необходимости улучшения диагностики и совершенствования вакцинопрофилактики
коклюша
от 30.01.2024 №01-21/97
Поэтапное внедрение возрастных ревакцинаций
против коклюша:
Сайт НИИДИ http://niidi.ru/dotAsset/4eae3d65-001a-4cf7-88bb31975ea3d476.pdf. Дата доступа май 2025 г
дети до 14 лет, в первую очередь из многодетных семей
и проживающих в закрытых учреждениях
пациенты с бронхолегочной патологией и
иммунодефицитными состояниями
взрослые- сотрудники медицинских и образовательных
учреждений
взрослые, где в семьях есть новорожденные и дети до 1
года
пожилые старше 60 лет
беременные женщины
30.
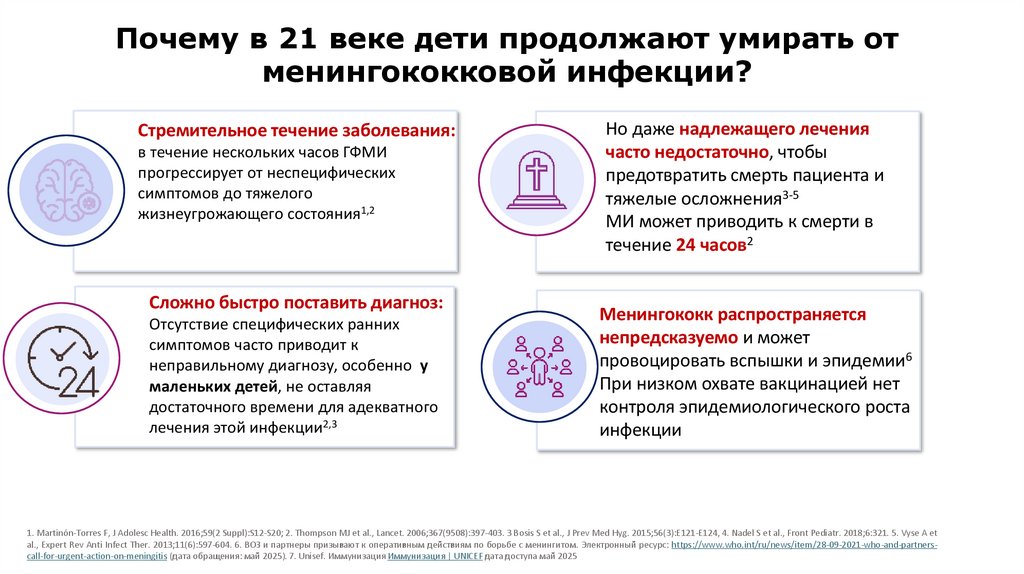
Почему в 21 веке дети продолжают умирать отменингококковой инфекции?
Стремительное течение заболевания:
в течение нескольких часов ГФМИ
прогрессирует от неспецифических
.
симптомов до тяжелого
жизнеугрожающего состояния1,2
Сложно быстро поставить диагноз:
Отсутствие специфических ранних
симптомов часто приводит к
неправильному диагнозу, особенно у
маленьких детей, не оставляя
достаточного времени для адекватного
лечения этой инфекции2,3
Но даже надлежащего лечения
часто недостаточно, чтобы
предотвратить смерть пациента и
тяжелые осложнения3-5
МИ может приводить к смерти в
течение 24 часов2
Менингококк распространяется
непредсказуемо и может
провоцировать вспышки и эпидемии6
При низком охвате вакцинацией нет
контроля эпидемиологического роста
инфекции
1. Martinón-Torres F, J Adolesc Health. 2016;59(2 Suppl):S12-S20; 2. Thompson MJ et al., Lancet. 2006;367(9508):397-403. 3 Bosis S et al., J Prev Med Hyg. 2015;56(3):E121-E124, 4. Nadel S et al., Front Pediatr. 2018;6:321. 5. Vyse A et
al., Expert Rev Anti Infect Ther. 2013;11(6):597-604. 6. ВОЗ и партнеры призывают к оперативным действиям по борьбе с менингитом. Электронный ресурс: https://www.who.int/ru/news/item/28-09-2021-who-and-partnerscall-for-urgent-action-on-meningitis (дата обращения: май 2025). 7. Unisef. Иммунизация Иммунизация | UNICEF дата доступа май 2025
31.
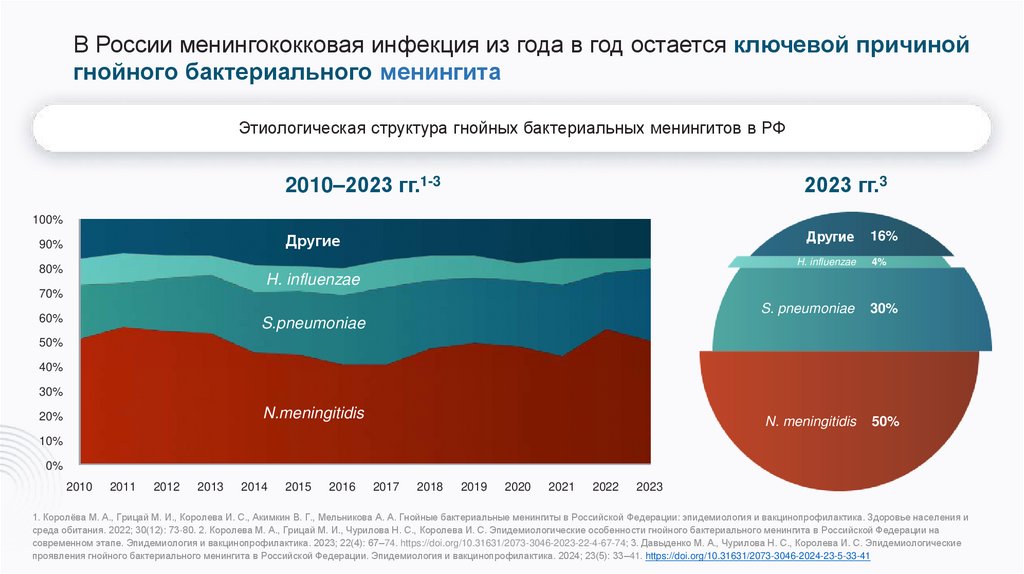
В России менингококковая инфекция из года в год остается ключевой причинойгнойного бактериального менингита
Этиологическая структура гнойных бактериальных менингитов в РФ
2010–2023 гг.1-3
2023 гг.3
Другие
Другие
16%
H. influenzae
4%
100%
90%
80%
H. influenzae
70%
60%
S. pneumoniae
30%
N. meningitidis
50%
S.pneumoniae
50%
40%
30%
N.meningitidis
20%
10%
0%
2010
2011
2012
2013
2014
2015
2016
2017
2018
2019
2020
2021
2022
2023
1. Королёва М. А., Грицай М. И., Королева И. С., Акимкин В. Г., Мельникова А. А. Гнойные бактериальные менингиты в Российской Федерации: эпидемиология и вакцинопрофилактика. Здоровье населения и
среда обитания. 2022; 30(12): 73-80. 2. Королева М. А., Грицай М. И., Чурилова Н. С., Королева И. С. Эпидемиологические особенности гнойного бактериального менингита в Российской Федерации на
современном этапе. Эпидемиология и вакцинопрофилактика. 2023; 22(4): 67–74. https://doi.org/10.31631/2073-3046-2023-22-4-67-74; 3. Давыденко М. А., Чурилова Н. С., Королева И. С. Эпидемиологические
проявления гнойного бактериального менингита в Российской Федерации. Эпидемиология и вакцинопрофилактика. 2024; 23(5): 33–41. https://doi.org/10.31631/2073-3046-2024-23-5-33-41
32.
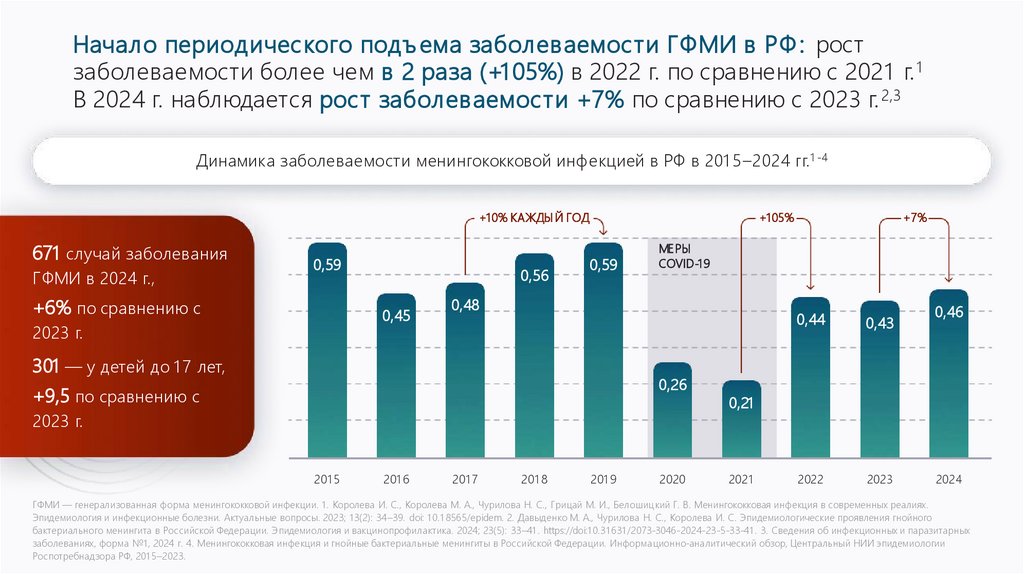
Начало периодического подъ ема заболеваемос ти ГФМИ в РФ : ростзаболеваемости более чем в 2 раза (+1 05%) в 2022 г. по сравнению с 2021 г. 1
В 2024 г. наблюдается рост заболеваемости +7% по сравнению с 2023 г. 2,3
Динамика заболеваемости менингококковой инфекцией в РФ в 201 5–2024 гг.1 -4
+10% КАЖДЫ Й ГОД
671 случай заболевания
ГФМИ в 2024 г.,
0,59
+6% по сравнению с
0,56
0,45
2023 г.
+105%
0,59
МЕРЫ
COVID-1 9
0,48
301 — у детей до 1 7 лет,
0,26
+9,5 по сравнению с
2023 г.
201 5
201 6
201 7
201 8
201 9
+7%
2020
0,44
0,43
2022
2023
0,46
0,21
2021
2024
ГФМИ — генерализованная форма менингококковой инфекции. 1 . Королева И. С., Королева М. А., Чурилова Н. С., Грицай М. И., Белошицкий Г. В. Менингококковая инфекция в современных реалиях.
Эпидемиология и инфекционные болезни. Актуальные вопросы. 2023; 13(2): 34–39. doi: 1 0.1 8565/epidem. 2. Давыденко М. А., Чурилова Н. С., Королева И. С. Эпидемиологические проявления гнойного
бактериального менингита в Российской Федерации. Эпидемиология и вакцинопрофилактика. 2024; 23(5): 33–41 . https://doi:1 0.31 631 /2073-3046-2024-23-5-33-41 . 3. Сведения об инфекционных и паразитарных
заболеваниях, форма №1, 2024 г. 4. Менингококковая инфекция и гнойные бактериальные менингиты в Российской Федерации. Информационно-аналитический обзор, Центральный НИИ эпидемиологии
Роспотребнадзора РФ, 201 5–2023.
33.
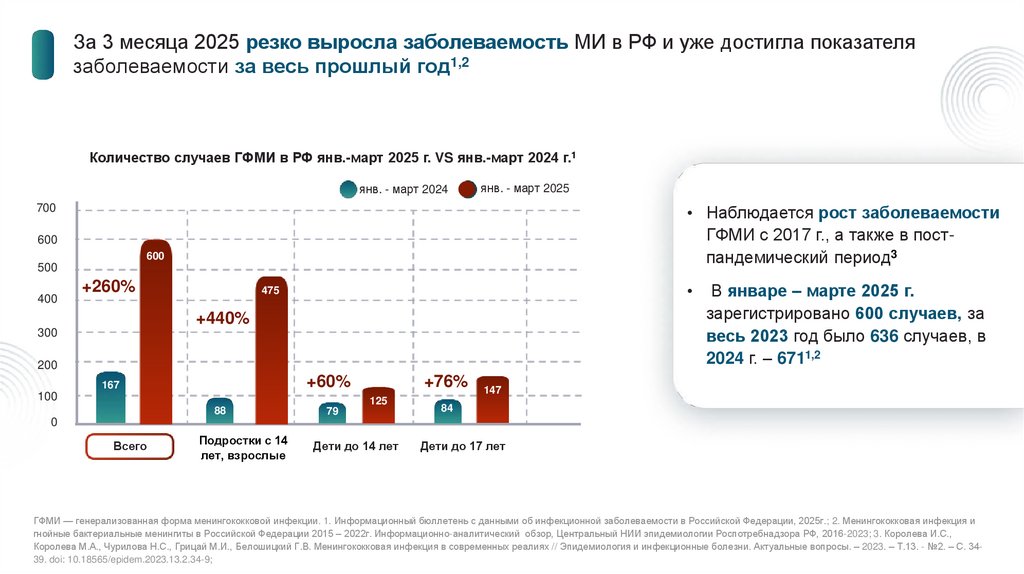
За 3 месяца 2025 резко выросла заболеваемость МИ в РФ и уже достигла показателязаболеваемости за весь прошлый год1,2
Количество случаев ГФМИ в РФ янв.-март 2025 г. VS янв.-март 2024 г.1
янв. - март 2024
янв. - март 2025
• Наблюдается рост заболеваемости
ГФМИ с 2017 г., а также в постпандемический период3
700
600
600
500
400
+260%
2,07
475
+440%
300
200
1,41
1,41
+60%
167
100
88
0
Всего
Подростки с 14
лет, взрослые
0,79
+76%
125
0,55
Дети до 14 лет
В январе – марте 2025 г.
зарегистрировано 600 случаев, за
весь 2023 год было 636 случаев, в
2024 г. – 6711,2
147
84
Дети до 17 лет
ГФМИ — генерализованная форма менингококковой инфекции. 1. Информационный бюллетень с данными об инфекционной заболеваемости в Российской Федерации, 2025г.; 2. Менингококковая инфекция и
гнойные бактериальные менингиты в Российской Федерации 2015 – 2022г. Информационно-аналитический обзор, Центральный НИИ эпидемиологии Роспотребнадзора РФ, 2016-2023; 3. Королева И.С.,
Королева М.А., Чурилова Н.С., Грицай М.И., Белошицкий Г.В. Менингококковая инфекция в современных реалиях // Эпидемиология и инфекционные болезни. Актуальные вопросы. – 2023. – Т.13. - №2. – С. 3439. doi: 10.18565/epidem.2023.13.2.34-9;
34.
В СМИ регулярно публикуются трагические случаи смерти отменингита/менингококковой инфекции среди детей
Почему в больнице Полевского умер
школьник - 13 июня 2024 - Е1.ру (e1.ru)
Российский школьник умер, за
сутки сгорев от неизвестной
болезни - МК (mk.ru)
Полуторагодовалый ребёнок умер
от менингококка во Владивостоке
| АиФ Владивосток (aif.ru)
Воспитанник детского сада в Инте заболел
менингитом | АиФ Коми (aif.ru)
У жителя Инты
подозревают
генерализованную
менингококковую
инфекцию | АиФ Коми
(aif.ru)
Тюменские медики спасли грудного ребенка
от последствий менингококковой инфекции
| 10.05.2024 | Тюмень - БезФормата
(bezformata.com)
Тюменские врачи спасли грудного ребенка от
опасной инфекции | АиФ Тюмень (aif.ru)
В Коми выявили второй очаг
инфекционного менингита
(tass.ru)
Данные Юдаковой О.В
35. В СМИ регулярно публикуются трагические случаи смерти от менингита/менингококковой инфекции среди детей
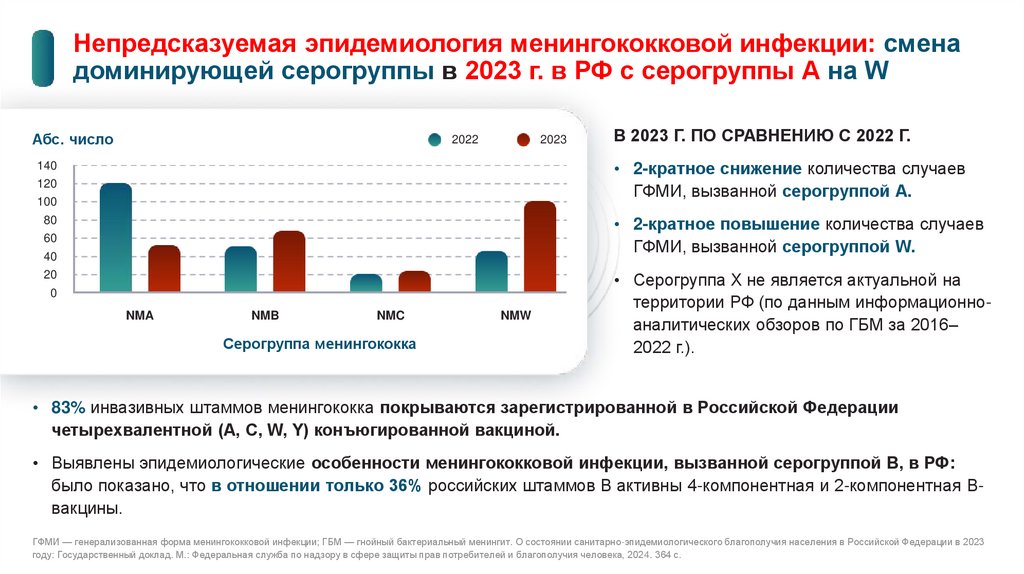
Непредсказуемая эпидемиология менингококковой инфекции: сменадоминирующей серогруппы в 2023 г. в РФ с серогруппы А на W
Абс. число
2022
2023
В 2023 Г. ПО СРАВНЕНИЮ С 2022 Г.
• 2-кратное снижение количества случаев
ГФМИ, вызванной серогруппой А.
140
120
100
• 2-кратное повышение количества случаев
ГФМИ, вызванной серогруппой W.
80
60
40
20
0
NMA
NMB
NMC
Серогруппа менингококка
NMW
• Серогруппа Х не является актуальной на
территории РФ (по данным информационноаналитических обзоров по ГБМ за 2016–
2022 г.).
• 83% инвазивных штаммов менингококка покрываются зарегистрированной в Российской Федерации
четырехвалентной (A, C, W, Y) конъюгированной вакциной.
• Выявлены эпидемиологические особенности менингококковой инфекции, вызванной серогруппой В, в РФ:
было показано, что в отношении только 36% российских штаммов В активны 4-компонентная и 2-компонентная Ввакцины.
ГФМИ — генерализованная форма менингококковой инфекции; ГБМ — гнойный бактериальный менингит. О состоянии санитарно-эпидемиологического благополучия населения в Российской Федерации в 2023
году: Государственный доклад. М.: Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека, 2024. 364 с.
36.
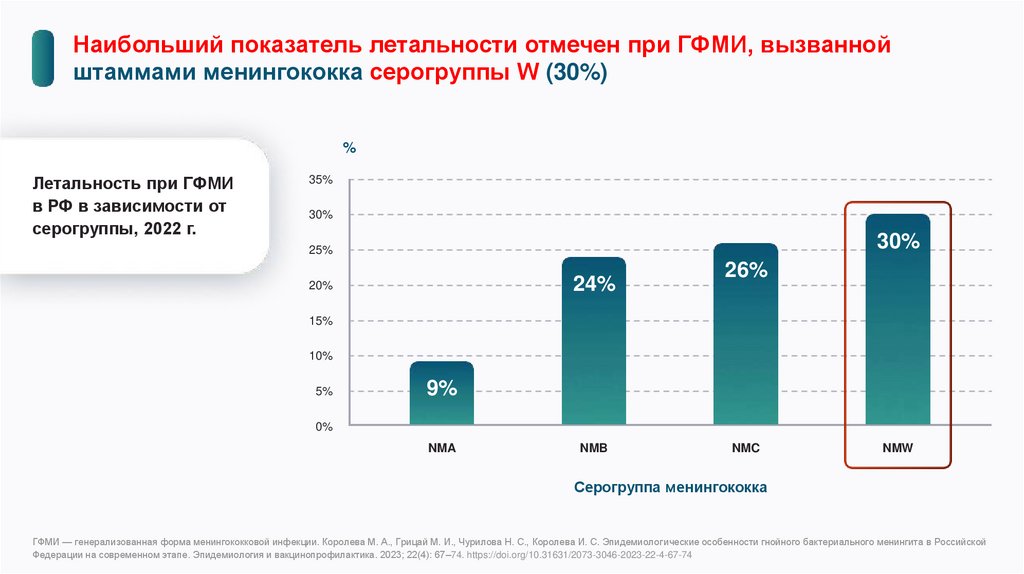
Наибольший показатель летальности отмечен при ГФМИ, вызваннойштаммами менингококка серогруппы W (30%)
%
Летальность при ГФМИ
в РФ в зависимости от
серогруппы, 2022 г.
35%
30%
30%
25%
24%
20%
26%
15%
10%
5%
9%
0%
NMA
NMB
NMC
NMW
Серогруппа менингококка
ГФМИ — генерализованная форма менингококковой инфекции. Королева М. А., Грицай М. И., Чурилова Н. С., Королева И. С. Эпидемиологические особенности гнойного бактериального менингита в Российской
Федерации на современном этапе. Эпидемиология и вакцинопрофилактика. 2023; 22(4): 67–74. https://doi.org/10.31631/2073-3046-2023-22-4-67-74
37.
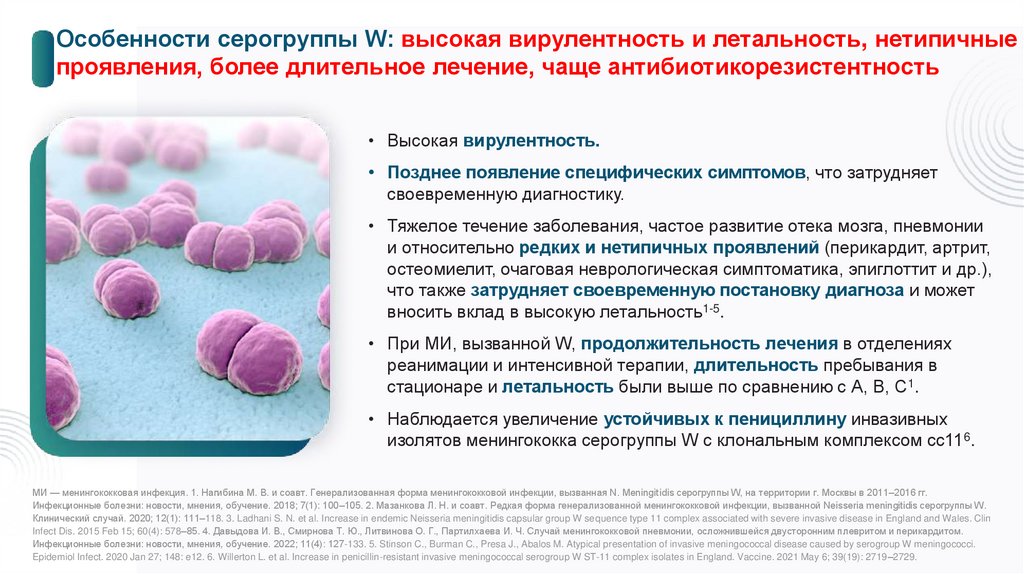
Особенности серогруппы W: высокая вирулентность и летальность, нетипичныепроявления, более длительное лечение, чаще антибиотикорезистентность
• Высокая вирулентность.
• Позднее появление специфических симптомов, что затрудняет
своевременную диагностику.
• Тяжелое течение заболевания, частое развитие отека мозга, пневмонии
и относительно редких и нетипичных проявлений (перикардит, артрит,
остеомиелит, очаговая неврологическая симптоматика, эпиглоттит и др.),
что также затрудняет своевременную постановку диагноза и может
вносить вклад в высокую летальность1-5.
• При МИ, вызванной W, продолжительность лечения в отделениях
реанимации и интенсивной терапии, длительность пребывания в
стационаре и летальность были выше по сравнению с А, B, C1.
• Наблюдается увеличение устойчивых к пенициллину инвазивных
изолятов менингококка серогруппы W с клональным комплексом cc116.
МИ — менингококковая инфекция. 1. Нагибина М. В. и соавт. Генерализованная форма менингококковой инфекции, вызванная N. Meningitidis серогруппы W, на территории г. Москвы в 2011–2016 гг.
Инфекционные болезни: новости, мнения, обучение. 2018; 7(1): 100–105. 2. Мазанкова Л. Н. и соавт. Редкая форма генерализованной менингококковой инфекции, вызванной Neisseria meningitidis серогруппы W.
Клинический случай. 2020; 12(1): 111–118. 3. Ladhani S. N. et al. Increase in endemic Neisseria meningitidis capsular group W sequence type 11 complex associated with severe invasive disease in England and Wales. Clin
Infect Dis. 2015 Feb 15; 60(4): 578–85. 4. Давыдова И. В., Смирнова Т. Ю., Литвинова О. Г., Партилхаева И. Ч. Случай менингококковой пневмонии, осложнившейся двусторонним плевритом и перикардитом.
Инфекционные болезни: новости, мнения, обучение. 2022; 11(4): 127-133. 5. Stinson C., Burman C., Presa J., Abalos M. Atypical presentation of invasive meningococcal disease caused by serogroup W meningococci.
Epidemiol Infect. 2020 Jan 27; 148: e12. 6. Willerton L. et al. Increase in penicillin-resistant invasive meningococcal serogroup W ST-11 complex isolates in England. Vaccine. 2021 May 6; 39(19): 2719–2729.
38.
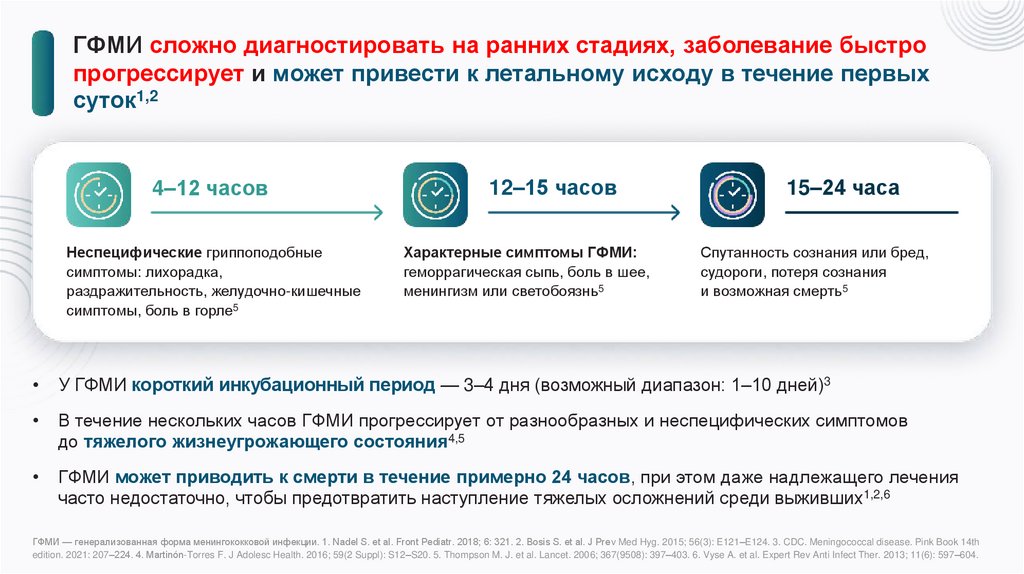
ГФМИ сложно диагностировать на ранних стадиях, заболевание быстропрогрессирует и может привести к летальному исходу в течение первых
суток1,2
4–12 часов
Неспецифические гриппоподобные
симптомы: лихорадка,
раздражительность, желудочно-кишечные
симптомы, боль в горле5
12–15 часов
Характерные симптомы ГФМИ:
геморрагическая сыпь, боль в шее,
менингизм или светобоязнь5
15–24 часа
Спутанность сознания или бред,
судороги, потеря сознания
и возможная смерть5
У ГФМИ короткий инкубационный период — 3–4 дня (возможный диапазон: 1–10 дней)3
В течение нескольких часов ГФМИ прогрессирует от разнообразных и неспецифических симптомов
до тяжелого жизнеугрожающего состояния4,5
ГФМИ может приводить к смерти в течение примерно 24 часов, при этом даже надлежащего лечения
часто недостаточно, чтобы предотвратить наступление тяжелых осложнений среди выживших1,2,6
ГФМИ — генерализованная форма менингококковой инфекции. 1. Nadel S. et al. Front Pediatr. 2018; 6: 321. 2. Bosis S. et al. J Prev Med Hyg. 2015; 56(3): E121–E124. 3. CDC. Meningococcal disease. Pink Book 14th
edition. 2021: 207–224. 4. Martinón-Torres F. J Adolesc Health. 2016; 59(2 Suppl): S12–S20. 5. Thompson M. J. et al. Lancet. 2006; 367(9508): 397–403. 6. Vyse A. et al. Expert Rev Anti Infect Ther. 2013; 11(6): 597–604.
39.
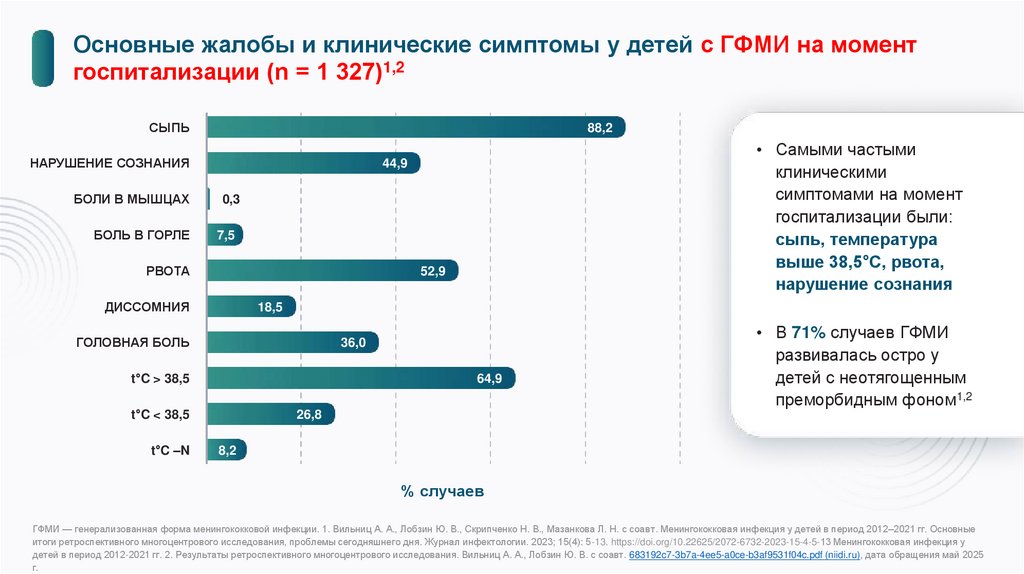
Основные жалобы и клинические симптомы у детей с ГФМИ на моментгоспитализации (n = 1 327)1,2
СЫПЬ
88,2
НАРУШЕНИЕ СОЗНАНИЯ
БОЛИ В МЫШЦАХ
0,3
БОЛЬ В ГОРЛЕ
7,5
РВОТА
52,9
ДИССОМНИЯ
18,5
ГОЛОВНАЯ БОЛЬ
36,0
t°C > 38,5
64,9
t°C < 38,5
t°C –N
• Самыми частыми
клиническими
симптомами на момент
госпитализации были:
сыпь, температура
выше 38,5°С, рвота,
нарушение сознания
44,9
• В 71% случаев ГФМИ
развивалась остро у
детей с неотягощенным
преморбидным фоном1,2
26,8
8,2
% случаев
ГФМИ — генерализованная форма менингококковой инфекции. 1. Вильниц А. А., Лобзин Ю. В., Скрипченко Н. В., Мазанкова Л. Н. с соавт. Менингококковая инфекция у детей в период 2012–2021 гг. Основные
итоги ретроспективного многоцентрового исследования, проблемы сегодняшнего дня. Журнал инфектологии. 2023; 15(4): 5-13. https://doi.org/10.22625/2072-6732-2023-15-4-5-13 Менингококковая инфекция у
детей в период 2012-2021 гг. 2. Результаты ретроспективного многоцентрового исследования. Вильниц А. А., Лобзин Ю. В. с соавт. 683192c7-3b7a-4ee5-a0ce-b3af9531f04c.pdf (niidi.ru), дата обращения май 2025
г.
40.
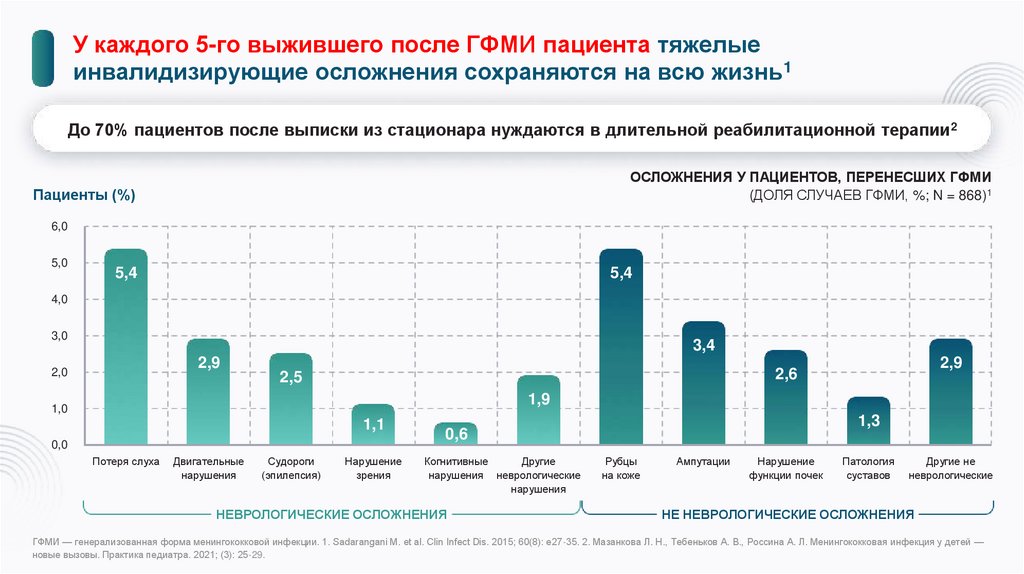
У каждого 5-го выжившего после ГФМИ пациента тяжелыеинвалидизирующие осложнения сохраняются на всю жизнь1
До 70% пациентов после выписки из стационара нуждаются в длительной реабилитационной терапии2
ОСЛОЖНЕНИЯ У ПАЦИЕНТОВ, ПЕРЕНЕСШИХ ГФМИ
(ДОЛЯ СЛУЧАЕВ ГФМИ, %; N = 868)1
Пациенты (%)
6,0
5,0
5,4
5,4
4,0
3,0
3,4
2,9
2,0
2,9
2,6
2,5
1,9
1,0
1,1
0,0
Потеря слуха
Двигательные
нарушения
Судороги
(эпилепсия)
Нарушение
зрения
1,3
0,6
Когнитивные
Другие
нарушения неврологические
нарушения
НЕВРОЛОГИЧЕСКИЕ ОСЛОЖНЕНИЯ
Рубцы
на коже
Ампутации
Нарушение
функции почек
Патология
суставов
Другие не
неврологические
НЕ НЕВРОЛОГИЧЕСКИЕ ОСЛОЖНЕНИЯ
ГФМИ — генерализованная форма менингококковой инфекции. 1. Sadarangani M. et al. Clin Infect Dis. 2015; 60(8): e27-35. 2. Мазанкова Л. Н., Тебеньков А. В., Россина А. Л. Менингококковая инфекция у детей —
новые вызовы. Практика педиатра. 2021; (3): 25-29.
41.
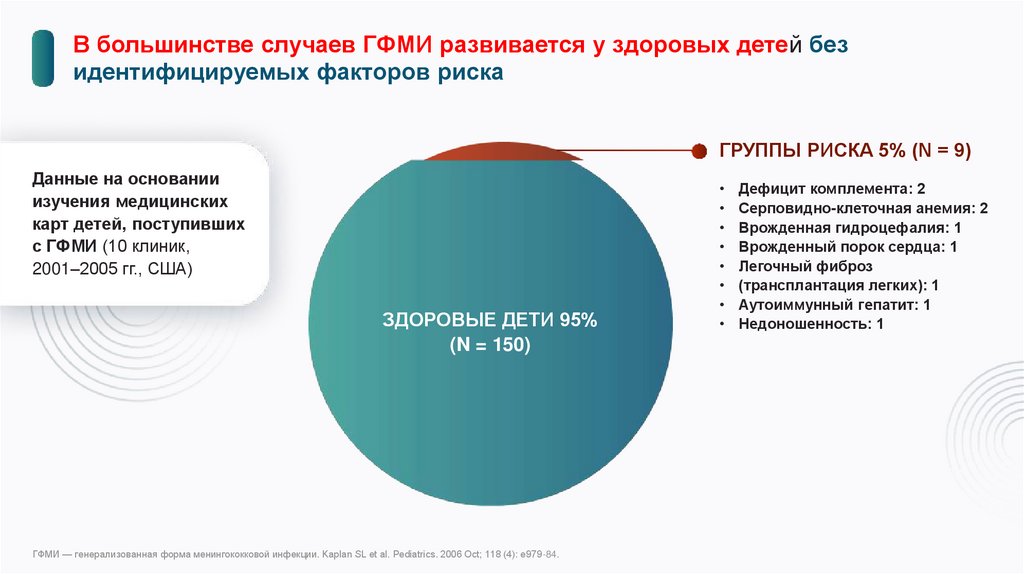
В большинстве случаев ГФМИ развивается у здоровых детей безидентифицируемых факторов риска
ГРУППЫ РИСКА 5% (N = 9)
Данные на основании
изучения медицинских
карт детей, поступивших
с ГФМИ (10 клиник,
2001–2005 гг., США)
ЗДОРОВЫЕ ДЕТИ 95%
(N = 150)
ГФМИ — генерализованная форма менингококковой инфекции. Kaplan SL et al. Pediatrics. 2006 Oct; 118 (4): e979-84.
Дефицит комплемента: 2
Серповидно-клеточная анемия: 2
Врожденная гидроцефалия: 1
Врожденный порок сердца: 1
Легочный фиброз
(трансплантация легких): 1
Аутоиммунный гепатит: 1
Недоношенность: 1
42.
ГФМИ приводит к значительным экономическим и социальнымпоследствиям
• Лечение ГФМИ связано со значительными расходами на
лечение1 из-за длительной госпитализации и тяжелых, часто
необратимых последствий перенесенной инфекции2,3
₽
• Последствия ГФМИ связаны с высокими непрямыми
расходами вследствие необходимости реабилитации и
коррекции долгосрочных осложнений1,4
• ГФМИ влечет за собой значительные общественные
экономические издержки, связанные с длительным
лечением выживших пациентов и контролем вспышек1,2
ГФМИ — генерализованная форма менингококковой инфекции. 1. Martinón-Torres F. J Adolesc Health. 2016; 59(2 Suppl): S12-S20. 2. Wright C. et al. Paediatr Drugs. 2013; 15(1): 49-58. 3. Bénard S. et al. J Infect Public
Health. 2016; 9(3): 339-347. 4. Davis K. L. et al. Hum Vaccin. 2011; 7(1): 96-101.
43.
Заболеванию подвержены лица любого возраста, но в 3–4 раза чащестрадают дети. Дети до 5 лет — основная возрастная группа риска ГФМИ1,2
• У детей до 5 лет регистрируется самый высокий показатель заболеваемости ГФМИ, который
превысил в ~7 раз средний показатель заболеваемости в 2023 г.2
• Среди детей до 5 лет выделяются дети первого года жизни, уровень заболеваемости
которых в ~2–5 раз выше по сравнению с детьми до 5 лет и в 10 раз выше по сравнению со
старшими возрастными категориями1.
• Также группа детей до 5 лет вносит значительный вклад в формирование смертности при
ГФМИ, показатель смертности в которой в 2023 г. превысил средний показатель смертности
в 6 раз2.
• Дети, переболевшие ГФМИ, сталкиваются с осложнениями и снижением качества жизни
чаще, чем взрослые3.
ГФМИ — генерализованная форма менингококковой инфекции. 1. Королева И. С. с соавт. Менингококковая инфекция в Москве: десятилетнее наблюдение (2014–2023 гг.). Эпидемиол. инфекц. болезни. Актуал.
вопр. 2024; 14(3): 30–6, DOI: 10.18565/epidem.2024.14.3.30–6. 2. Менингококковая инфекция и гнойные бактериальные менингиты в Российской Федерации 2023. Информационно-аналитический обзор.
Центральный НИИ эпидемиологии Роспотребнадзора РФ, 2024. 3. Olbrich et al. Infect Dis Ther 2018; 7(4): 421–438.
44.
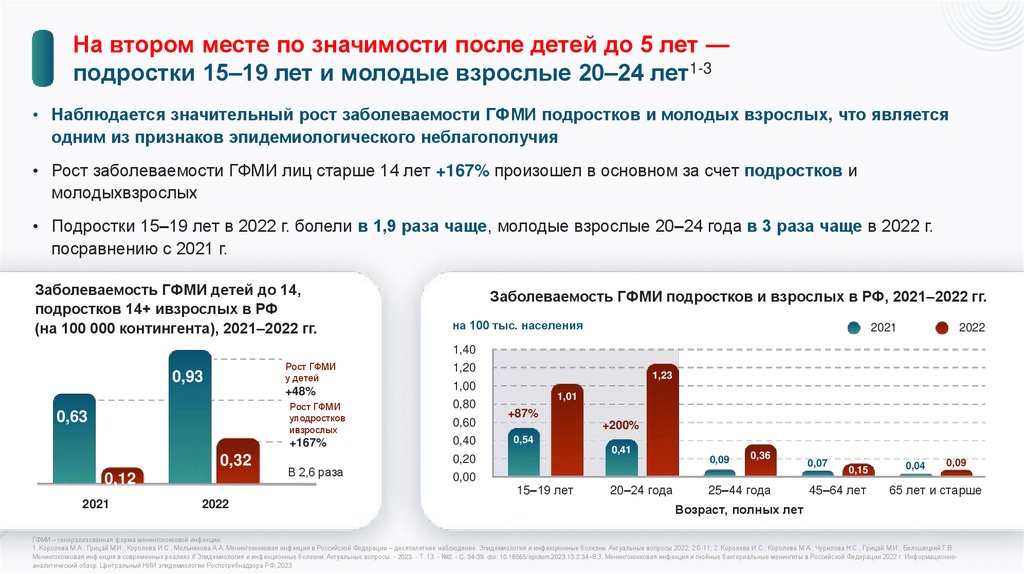
На втором месте по значимости после детей до 5 лет —подростки 15–19 лет и молодые взрослые 20–24 лет1-3
• Наблюдается значительный рост заболеваемости ГФМИ подростков и молодых взрослых, что является
одним из признаков эпидемиологического неблагополучия
• Рост заболеваемости ГФМИ лиц старше 14 лет +167% произошел в основном за счет подростков и
молодыхвзрослых
• Подростки 15–19 лет в 2022 г. болели в 1,9 раза чаще, молодые взрослые 20–24 года в 3 раза чаще в 2022 г.
посравнению с 2021 г.
Заболеваемость ГФМИ детей до 14,
подростков 14+ ивзрослых в РФ
(на 100 000 контингента), 2021–2022 гг.
Заболеваемость ГФМИ подростков и взрослых в РФ, 2021–2022 гг.
на 100 тыс. населения
2021
2022
1,40
Рост ГФМИ
у детей
0,93
+48%
Рост ГФМИ
уподростков
ивзрослых
0,63
+167%
0,32
0,12
2021
2022
1,20
1,23
1,00
0,80
0,60
0,40
1,01
+87%
+200%
0,54
0,41
0,20
В 2,6 раза
0,00
0,09
15–19 лет
20–24 года
0,36
25–44 года
0,07
0,15
45–64 лет
0,04
0,09
65 лет и старше
Возраст, полных лет
ГФМИ – генерализованная форма менингококковой инфекции.
1. Королева М.А., Грицай М.И., Королева И.С., Мельникова А.А. Менингококковая инфекция в Российской Федерации – десятилетнее наблюдение. Эпидемиология и инфекционные болезни. Актуальные вопросы 2022; 2:6-11; 2. Королева И.С., Королева М.А., Чурилова Н.С., Грицай М.И., Белошицкий Г.В.
Менингококковая инфекция в современных реалиях // Эпидемиология и инфекционные болезни. Актуальные вопросы. - 2023. - Т. 13. - №2. - C. 34-39. doi: 10.18565/epidem.2023.13.2.34–9;3. Менингококковая инфекция и гнойные бактериальные менингиты в Российской Федерации 2022 г. Информационноаналитический обзор. Центральный НИИ эпидемиологии Роспотребнадзора РФ, 2023
45.
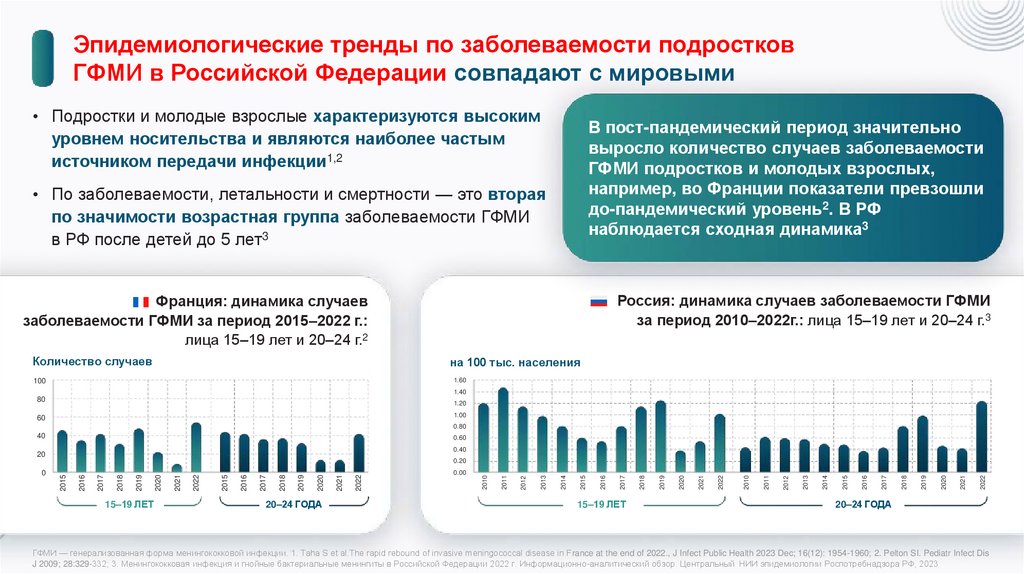
Эпидемиологические тренды по заболеваемости подростковГФМИ в Российской Федерации совпадают с мировыми
• Подростки и молодые взрослые характеризуются высоким
уровнем носительства и являются наиболее частым
источником передачи инфекции1,2
В пост-пандемический период значительно
выросло количество случаев заболеваемости
ГФМИ подростков и молодых взрослых,
например, во Франции показатели превзошли
до-пандемический уровень2. В РФ
наблюдается сходная динамика3
• По заболеваемости, летальности и смертности — это вторая
по значимости возрастная группа заболеваемости ГФМИ
в РФ после детей до 5 лет3
Россия: динамика случаев заболеваемости ГФМИ
за период 2010–2022г.: лица 15–19 лет и 20–24 г.3
Франция: динамика случаев
заболеваемости ГФМИ за период 2015–2022 г.:
лица 15–19 лет и 20–24 г.2
Количество случаев
на 100 тыс. населения
100
1.60
1.40
80
1.20
1.00
60
0.80
40
0.60
0.40
20
15–19 ЛЕТ
20–24 ГОДА
15–19 ЛЕТ
2022
2021
2020
2019
2018
2017
2016
2015
2014
2013
2012
2011
2010
2022
2021
2020
2019
2018
2017
2016
2015
2014
2013
2012
2011
0.00
2010
2022
2021
2020
2019
2018
2017
2016
2015
2022
2021
2020
2019
2018
2017
2016
2015
0.20
0
20–24 ГОДА
ГФМИ — генерализованная форма менингококковой инфекции. 1. Taha S et al.The rapid rebound of invasive meningococcal disease in France at the end of 2022., J Infect Public Health 2023 Dec; 16(12): 1954-1960; 2. Pelton SI. Pediatr Infect Dis
J 2009; 28:329-332; 3. Менингококковая инфекция и гнойные бактериальные менингиты в Российской Федерации 2022 г. Информационно-аналитический обзор. Центральный НИИ эпидемиологии Роспотребнадзора РФ, 2023
46.
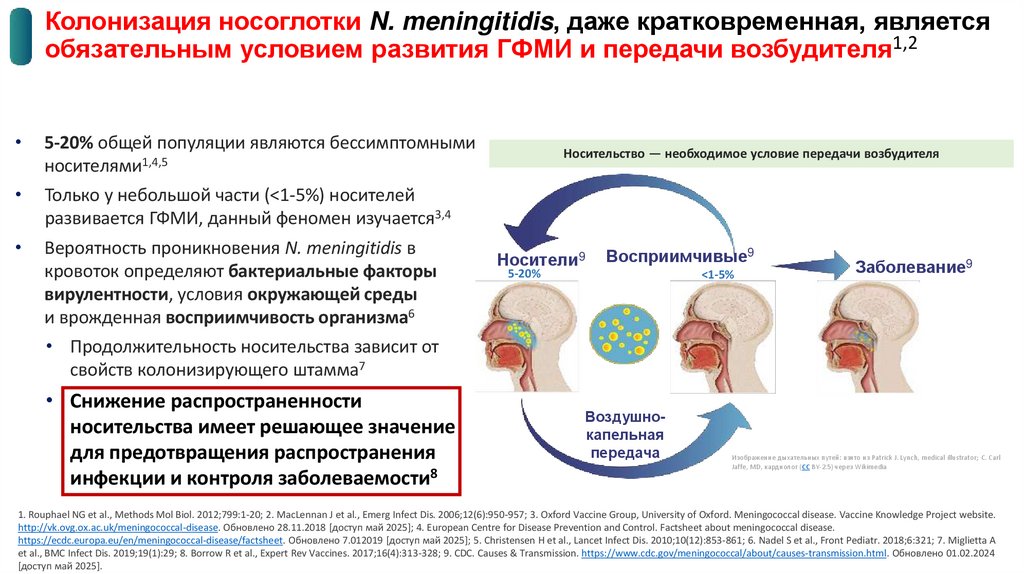
Колонизация носоглотки N. meningitidis, даже кратковременная, являетсяобязательным условием развития ГФМИ и передачи возбудителя1,2
5-20% общей популяции являются бессимптомными
носителями1,4,5
Только у небольшой части (<1-5%) носителей
развивается ГФМИ, данный феномен изучается3,4
Вероятность проникновения N. meningitidis в
кровоток определяют бактериальные факторы
вирулентности, условия окружающей среды
и врожденная восприимчивость организма6
Носительство — необходимое условие передачи возбудителя
Носители9
Восприимчивые9
5-20%
<1-5%
Заболевание9
• Продолжительность носительства зависит от
свойств колонизирующего штамма7
• Снижение распространенности
носительства имеет решающее значение
для предотвращения распространения
инфекции и контроля заболеваемости8
Воздушнокапельная
передача
Изображение дыхательных путей: взято из Patrick J. Lynch, medical illustrator; C. Carl
Jaffe, MD, кардиолог (CC BY-2.5) через Wikimedia
1. Rouphael NG et al., Methods Mol Biol. 2012;799:1-20; 2. MacLennan J et al., Emerg Infect Dis. 2006;12(6):950-957; 3. Oxford Vaccine Group, University of Oxford. Meningococcal disease. Vaccine Knowledge Project website.
http://vk.ovg.ox.ac.uk/meningococcal-disease. Обновлено 28.11.2018 [доступ май 2025]; 4. European Centre for Disease Prevention and Control. Factsheet about meningococcal disease.
https://ecdc.europa.eu/en/meningococcal-disease/factsheet. Обновлено 7.012019 [доступ май 2025]; 5. Christensen H et al., Lancet Infect Dis. 2010;10(12):853-861; 6. Nadel S et al., Front Pediatr. 2018;6:321; 7. Miglietta A
et al., BMC Infect Dis. 2019;19(1):29; 8. Borrow R et al., Expert Rev Vaccines. 2017;16(4):313-328; 9. CDC. Causes & Transmission. https://www.cdc.gov/meningococcal/about/causes-transmission.html. Обновлено 01.02.2024
[доступ май 2025].
47.
Проживание в общежитии – фактор, увеличивающий риск развития ИМИу студентов
на 100 тыс.
Среднегодовая заболеваемость студентов в 43 университетах Великобритании в
зависимости от доли студентов, проживающих в общежитии (от ежегодного набора)
20
18
16
14
12
10
8
6
4
2
0
ОР=2,6
15,3
Университеты с высокой долей проживающих
в общежитиях*
5,9
* Высокая доля, >10% от ежегодного набора студентов; низкая доля, <10% от ежегодного набора студентов.
ИМИ – инвазивная менингококковая инфекция
ОР – относительный риск; указаны 95%ДИ
Neal KR et al. Epidemiol Infect 1999; 122:351-357
Университеты с низкой долей проживающих в
общежитиях*
48. Проживание в общежитии – фактор, увеличивающий риск развития ИМИ у студентов
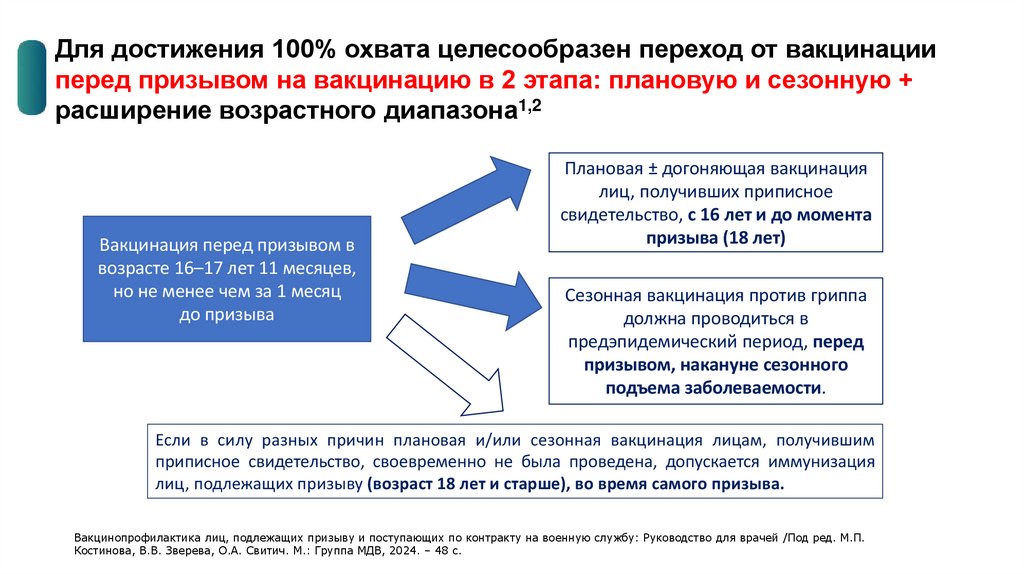
Для достижения 100% охвата целесообразен переход от вакцинацииперед призывом на вакцинацию в 2 этапа: плановую и сезонную +
расширение возрастного диапазона1,2
Вакцинация перед призывом в
возрасте 16–17 лет 11 месяцев,
но не менее чем за 1 месяц
до призыва
Плановая ± догоняющая вакцинация
лиц, получивших приписное
свидетельство, с 16 лет и до момента
призыва (18 лет)
Сезонная вакцинация против гриппа
должна проводиться в
предэпидемический период, перед
призывом, накануне сезонного
подъема заболеваемости.
Если в силу разных причин плановая и/или сезонная вакцинация лицам, получившим
приписное свидетельство, своевременно не была проведена, допускается иммунизация
лиц, подлежащих призыву (возраст 18 лет и старше), во время самого призыва.
Вакцинопрофилактика лиц, подлежащих призыву и поступающих по контракту на военную службу: Руководство для врачей /Под ред. М.П.
Костинова, В.В. Зверева, О.А. Свитич. М.: Группа МДВ, 2024. – 48 с.
49. Для достижения 100% охвата целесообразен переход от вакцинации перед призывом на вакцинацию в 2 этапа: плановую и сезонную +
Вакцинации против МИ в межэпидемический период в плановом порядкеподлежат лица из групп высокого риска инфицирования
В СООТВЕТСТВИИ С СП 3.3686-21 В ЧАСТИ «ПРОФИЛАКТИКА МЕНИНГОКОККОВОЙ ИНФЕКЦИИ»
ВЫДЕЛЯЮТ СЛЕДУЮЩИЕ ГРУППЫ РИСКА ИНФИЦИРОВАНИЯ И ЗАБОЛЕВАНИЯ МИ
Возрастные группы
Дети до 5 лет (в связи с высокой заболеваемостью
в даннойвозрастной группе)
Подростки в возрасте 13–17 лет (в связи с повышенным
уровнем носительства возбудителя в данной возрастной
группе)
Лица старше 60 лет
Лица, отъезжающие в эндемичные
по менингококковойинфекции районы
Лица, проживающие
в услов иях скученности
Воспитанники и персонал учреждений стационарного
социального обслуживания с
круглосуточнымпребыванием (дома ребенка, детские
дома, интернаты)
Лица, проживающие в общежитиях
Проф ессионал ь ны е группы
Призывники
Медицинские работники структурных подразделений,
оказывающих специализированную медицинскую помощь
по профилю “инфекционные болезни”
Медицинские работники и сотрудники лабораторий,
работающих с живой культурой менингококка
Участники массовых международных
спортивных икультурных мероприятий
Вакцинация против менингококковой инфекции проводится разрешенными на территории
Российской Федерации вакцинами в соответствии с инструкциями по их применению.
При проведении вакцинации используются вакцины с наибольшим набором актуальных
МИ — менингококковая инфекция.
Адаптировано из: СанПин 3.3686-21 (раздел XXXIX
для страны серогрупп возбудителя, позволяющие обеспечить максимальную
Профилактика менингококковой
эффективность иммунизации и формирование популяционного иммунитета
инфекции) от 28.01.2021, вступившие
всилу 01.09.2021.
50.
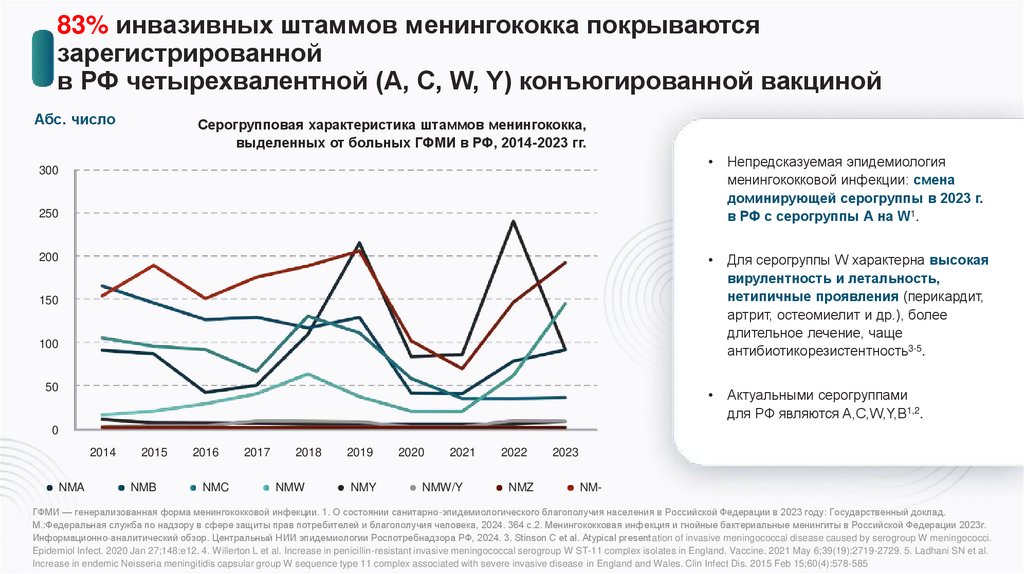
83% инвазивных штаммов менингококка покрываютсязарегистрированной
в РФ четырехвалентной (A, C, W, Y) конъюгированной вакциной
Абс. число
Серогрупповая характеристика штаммов менингококка,
выделенных от больных ГФМИ в РФ, 2014-2023 гг.
300
Непредсказуемая эпидемиология
менингококковой инфекции: смена
доминирующей серогруппы в 2023 г.
в РФ с серогруппы А на W1.
Для серогруппы W характерна высокая
вирулентность и летальность,
нетипичные проявления (перикардит,
артрит, остеомиелит и др.), более
длительное лечение, чаще
антибиотикорезистентность3-5.
Актуальными серогруппами
для РФ являются A,C,W,Y,B1,2.
250
200
150
100
50
0
2014
NMA
2015
NMB
2016
NMC
2017
2018
NMW
2019
NMY
2020
2021
NMW/Y
2022
NMZ
2023
NM-
ГФМИ — генерализованная форма менингококковой инфекции. 1. О состоянии санитарно-эпидемиологического благополучия населения в Российской Федерации в 2023 году: Государственный доклад.
М.:Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека, 2024. 364 с.2. Менингококковая инфекция и гнойные бактериальные менингиты в Российской Федерации 2023г.
Информационно-аналитический обзор. Центральный НИИ эпидемиологии Роспотребнадзора РФ, 2024. 3. Stinson C et al. Atypical presentation of invasive meningococcal disease caused by serogroup W meningococci.
Epidemiol Infect. 2020 Jan 27;148:e12. 4. Willerton L et al. Increase in penicillin-resistant invasive meningococcal serogroup W ST-11 complex isolates in England. Vaccine. 2021 May 6;39(19):2719-2729. 5. Ladhani SN et al.
Increase in endemic Neisseria meningitidis capsular group W sequence type 11 complex associated with severe invasive disease in England and Wales. Clin Infect Dis. 2015 Feb 15;60(4):578-585
51.
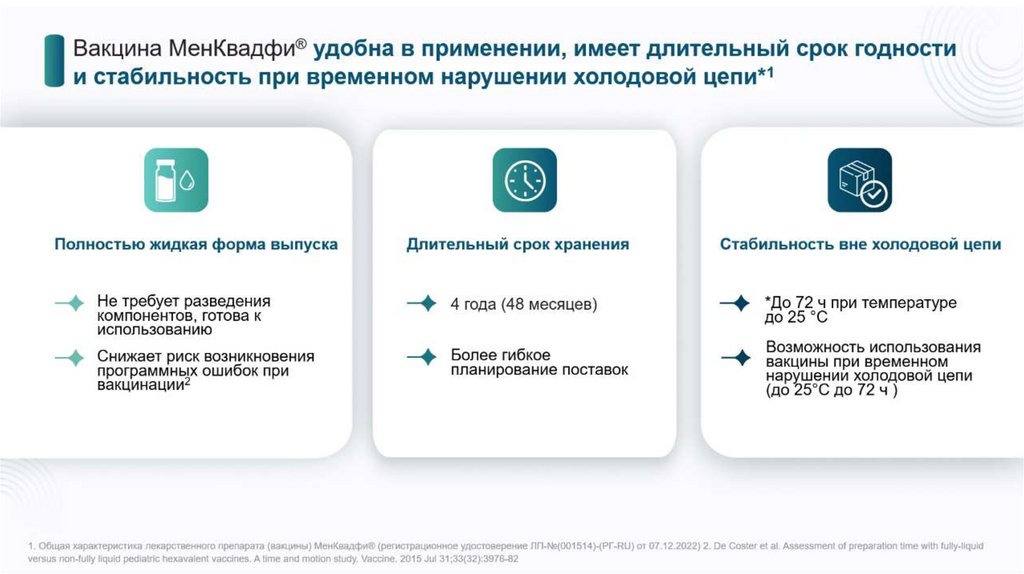
Вакцина МенКвадфи® применяется с 6 недель и без ограничения верхнейграницы применения1
Дети с 6
недель
Дети с 12
месяцев
Дети до 5 лет
Подростки
Взрослые
(группы риска: паломники,
ЛЖВ, мед. работники)
Пожилые
МенКвадфи®
С 6 недель до 6 мес.:
С 6 месяцев до 12 мес.:
С 12 месяцев:
3 дозы с интервалом не
менее 2 мес. + ревакцинация
1 доза на втором году жизни
(с 12 мес.)
1 доза на первом году жизни
+ ревакцинация 1 доза на
втором году жизни (с 12
мес.)
1 доза
Применение вакицны МенКвадфи® в РФ позволяет расширить возможности по вакцинопрофилактике
менингококковой инфекции против серогрупп A, C, W, Y у детей, начиная с 6 недель, подростков и
взрослых1
1. Общая характеристика лекарственного препарата (вакцины) МенКвадфи® (регистрационное удостоверение ЛП-№(001514)-(РГ-RU) от 07.12.2022)
52.
03.06.202553
53.
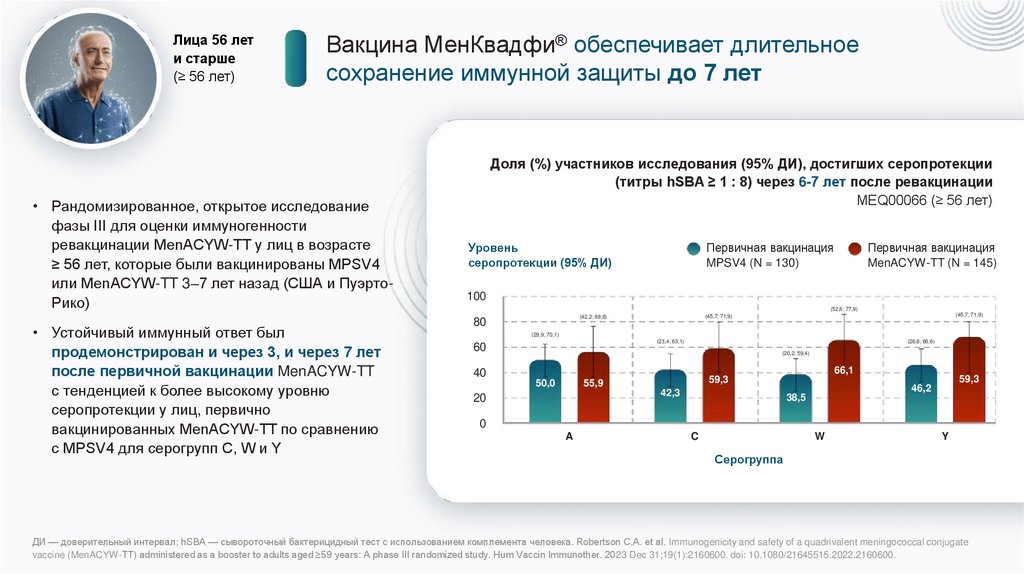
Лица 56 лети старше
(≥ 56 лет)
Вакцина МенКвадфи® обеспечивает длительное
сохранение иммунной защиты до 7 лет
• Рандомизированное, открытое исследование
фазы III для оценки иммуногенности
ревакцинации MenACYW-TT у лиц в возрасте
≥ 56 лет, которые были вакцинированы MPSV4
или MenACYW-TT 3–7 лет назад (США и ПуэртоРико)
• Устойчивый иммунный ответ был
продемонстрирован и через 3, и через 7 лет
после первичной вакцинации MenACYW-TT
с тенденцией к более высокому уровню
серопротекции у лиц, первично
вакцинированных MenACYW-TT по сравнению
с MPSV4 для серогрупп C, W и Y
Доля (%) участников исследования (95% ДИ), достигших серопротекции
(титры hSBA ≥ 1 : 8) через 6-7 лет после ревакцинации
MEQ00066 (≥ 56 лет)
Уровень
серопротекции (95% ДИ)
Первичная вакцинация
MPSV4 (N = 130)
Первичная вакцинация
MenACYW-TT (N = 145)
100
(52,6; 77,9)
(45,7; 71,9)
(45,7; 71,9)
(42,2; 68,8)
80
(29,9; 70,1)
(23,4; 63,1)
60
(26,6; 66,6)
(20,2; 59,4)
40
50,0
42,3
20
66,1
59,3
55,9
59,3
46,2
38,5
0
A
C
W
Y
Серогруппа
ДИ — доверительный интервал; hSBA — сывороточный бактерицидный тест с использованием комплемента человека. Robertson C.A. et al. Immunogenicity and safety of a quadrivalent meningococcal conjugate
vaccine (MenACYW-TT) administered as a booster to adults aged ≥59 years: A phase III randomized study. Hum Vaccin Immunother. 2023 Dec 31;19(1):2160600. doi: 10.1080/21645515.2022.2160600.
54.
Детимладшего
возраста
(12–23
месяца)
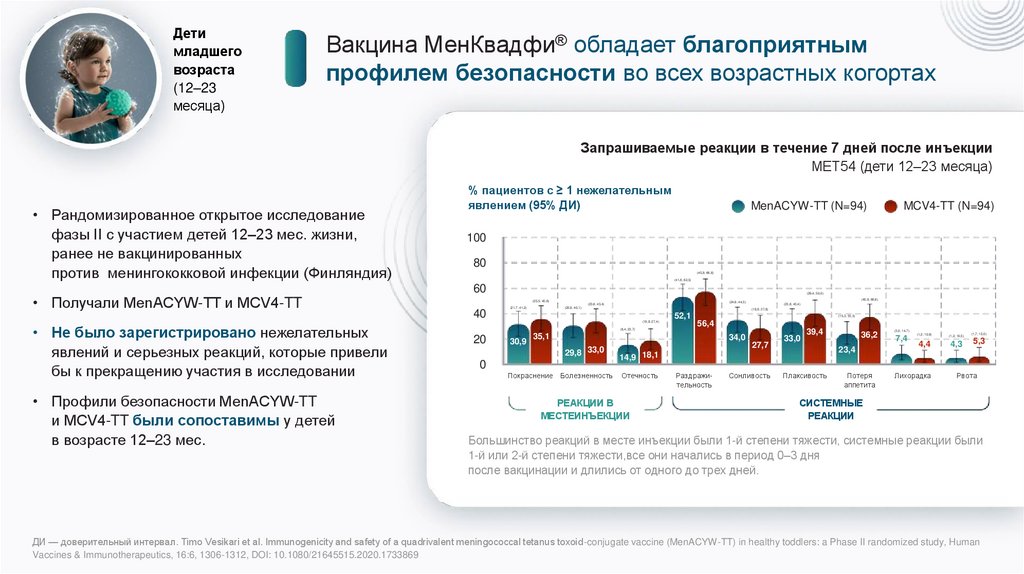
Вакцина МенКвадфи® обладает благоприятным
профилем безопасности во всех возрастных когортах
Запрашиваемые реакции в течение 7 дней после инъекции
MET54 (дети 12–23 месяца)
• Рандомизированное открытое исследование
фазы II с участием детей 12–23 мес. жизни,
ранее не вакцинированных
против менингококковой инфекции (Финляндия)
• Получали MenACYW-TT и MCV4-TT
% пациентов с ≥ 1 нежелательным
явлением (95% ДИ)
• Профили безопасности MenACYW-TT
и MCV4-TT были сопоставимы у детей
в возрасте 12–23 мес.
MCV4-TT (N=94)
100
80
(45,8; 66,6)
(41,6; 62,5)
60
(29,4; 50,0)
(25,5; 45,6)
40
(45,8; 66,6)
(24,6; 44,5)
(23,6; 43,4)
(21,7; 41,2)
(20,8; 40,1)
(23,6; 43,4)
(18,9; 37,8)
52,1
(10,9; 27,4)
• Не было зарегистрировано нежелательных
явлений и серьезных реакций, которые привели
бы к прекращению участия в исследовании
MenACYW-TT (N=94)
(15,3; 33,3)
56,4
(8,4; 23,7)
20
30,9
35,1
34,0
29,8 33,0
0
Покраснение Болезненность
27,7
33,0
39,4
23,4
14,9 18,1
Отечность
РЕАКЦИИ В
МЕСТЕИНЪЕКЦИИ
Раздражительность
Сонливость
36,2
Плаксивость
Потеря
аппетита
(3,0; 14,7)
7,4
(1,2; 10,9)
4,4
Лихорадка
(1,2; 10,5)
4,3
(1,7; 12,0)
5,3
Рвота
СИСТЕМНЫЕ
РЕАКЦИИ
Большинство реакций в месте инъекции были 1-й степени тяжести, системные реакции были
1-й или 2-й степени тяжести,все они начались в период 0–3 дня
после вакцинации и длились от одного до трех дней.
ДИ — доверительный интервал. Timo Vesikari et al. Immunogenicity and safety of a quadrivalent meningococcal tetanus toxoid-conjugate vaccine (MenACYW-TT) in healthy toddlers: a Phase II randomized study, Human
Vaccines & Immunotherapeutics, 16:6, 1306-1312, DOI: 10.1080/21645515.2020.1733869
55.
ЗаключениеМенингококковая инфекция остается в фокусе внимания за счет высоких показателей летальности
и смертности, особенно детей первых лет жизни1,2.
Заболеть может человек любого возраста, но чаще болеют и погибают дети до 5 лет3. Вторая возрастная
группа риска — подростки и молодые взрослые, третья — лица пожилого возраста и другие группы
риска2.
Эпидемиология менингококковой инфекции также непредсказуема: в 2023 году произошла смена
доминирующего штамма в РФ с серогруппы А на серогруппу W, которая характеризуется более сложным
течением заболевания и более высокой летальностью. Вакцинация должна быть направлена на защиту
против актуальных в стране серогрупп, включая W как доминирующую серогруппу4.
Вакцины Менактра® и МенКвадфи® позволяют расширить возрастной диапазон для охвата наиболее
уязвимых когорт — с 6 недель жизни и без ограничения по возрасту.
НККП — национальный календарь профилактических прививок. 1. Давыденко М. А., Чурилова Н. С., Королева И. С. Эпидемиологические проявления гнойного бактериального менингита в Российской
Федерации. Эпидемиология и Вакцинопрофилактика. 2024;23(5):33-41. https://doi:10.31631/2073-3046-2024-23-5-33-41; 2. Менингококковая инфекция и гнойные бактериальные менингиты в Российской Федерации
2023 г. Информационно-аналитический обзор. Центральный НИИ эпидемиологии Роспотребнадзора РФ, 2024. 3. Достижение целей в области борьбы с менингитом на период до 2030 г.: глобальная дорожная
карта. ВОЗ, 2021 г. http://apps.who.int/iris/bitstream/handle/10665/342010/9789240030145-rus.pdf (дата обращения: май.2025). 4. О состоянии санитарно-эпидемиологического благополучия населения в
Российской Федерации в 2023 году: Государственный доклад. М.: Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека, 2024. 364 с. 5. Общая характеристика
лекарственного препарата (вакцины) МенКвадфи®, регистрационное удостоверение ЛП-№(001514)-(РГ-RU) от 07.12.2022.6. Общая характеристика лекарственного препарата (вакцины)
Менактра®, регистрационное удостоверение ЛП-№(001763)-(РГ-RU) от 02.02.2023






















 medicine
medicine








