Similar presentations:
ЕГЭ по химии в 2025 году
1. ЕГЭ по химии в 2025 году
ЕГЭ ПО ХИМИИВ 2025 ГОДУ
2. Результаты ЕГЭ
РЕЗУЛЬТАТЫ ЕГЭКоличество 100-бальных экзаменационных работ:
2024 год – 13 работ.
Средний балл в 2024 году – 64,43 балла
(по России - 56,55 балла)
Структура КИМа по химии.
Количество заданий – 34.
Время выполнения 210 минут.
Максимальный первичный балл – 56
(36 баллов – 1-ая часть и 20 баллов – 2-ая часть).
3. Состав КИМа
СОСТАВ КИМАКаждый КИМ состоит из 34 заданий.
Часть 1 содержит 28 заданий с кратким ответом, в их
числе:
– 15 заданий базового уровня сложности;
– 13 заданий повышенного уровня сложности.
Часть 2 содержит 6 заданий (№№ 29 - 34) высокого уровня
сложности, то есть это задания с развёрнутым ответом.
Все задания базового уровня сложности предполагают
выбор 2-х или 3-х правильных ответов.
В заданиях №№ 12, 18 вместо выбора двух обязательных
ответов предлагается выбрать неизвестное число верных
ответов.
4. Задание №1
ЗАДАНИЕ №1Для выполнения задания 1 необходимо использовать ряд химических
элементов:
1) F; 2) Mg; 3) Br; 4); 5) H.
Определите два элемента, которым соответствуют ионы, имеющие
столько же s-электронов, как и атом неона.
Процент выполнения по региону– 77,81 %.
Из указанных в ряду элементов выберите три элемента-неметалла.
Расположите выбранные элементы в порядке уменьшения
окислительной способности образуемых ими простых веществ.
Процент выполнения по региону– 69,89 %.
Из числа указанных в ряду элементов выберите два элемента, у
которых разность между значениями их высшей и низшей степеней
окисления не равна 2.
Процент выполнения по региону– 69,10 %.
5. Задание №4
ЗАДАНИЕ №4Из предложенного перечня выберите два вещества немолекулярного
строения, в которых присутствует ковалентная полярная связь.
1) карбонат натрия
2) сульфид натрия
3) оксид кремния (IV)
4) хлорид бария
5) Бромоводород
Процент выполнения по региону– 56,42 %.
6. Задание №5
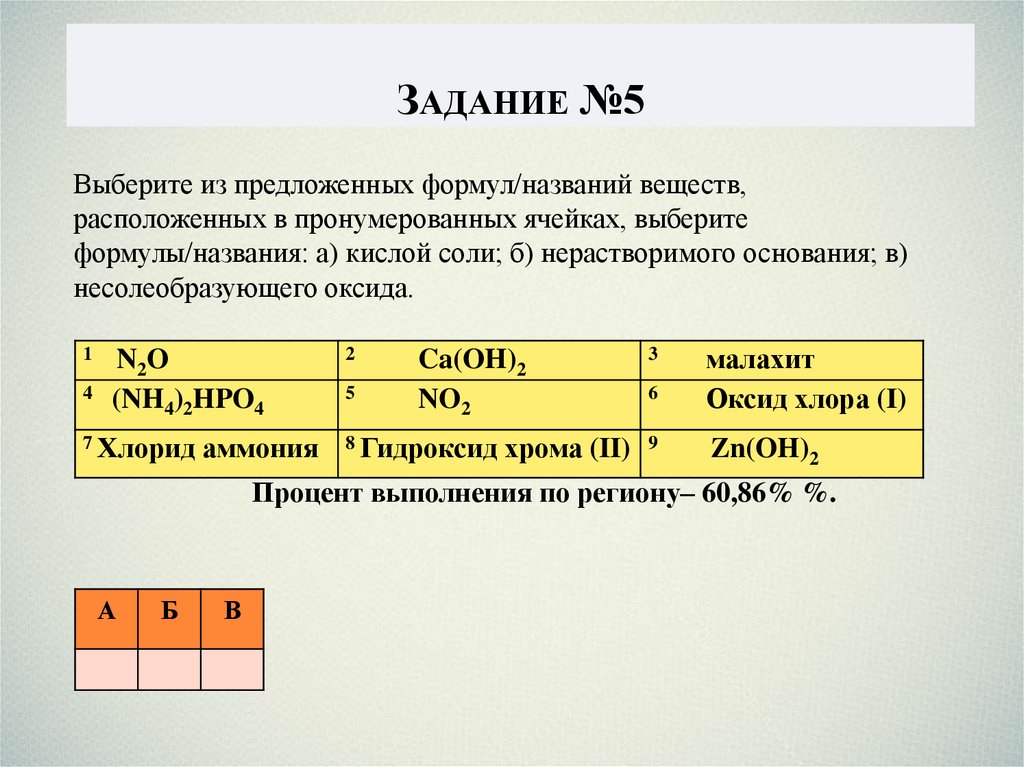
ЗАДАНИЕ №5Выберите из предложенных формул/названий веществ,
расположенных в пронумерованных ячейках, выберите
формулы/названия: а) кислой соли; б) нерастворимого основания; в)
несолеобразующего оксида.
2
3
N2 O
Ca(OH)2
малахит
4 (NH ) HPO
5
6
NO2
Оксид хлора (I)
4 2
4
Запишите в таблицу номер ячейки, в которой расположено вещество.
7 Хлорид аммония 8 Гидроксид хрома (II) 9
Zn(OH)2
1
Процент выполнения по региону– 60,86% %.
А
Б
В
7. Задания №6-7
ЗАДАНИЯ №6-7Даны две пробирки с раствором вещества Х. В одну из них добавили
соляную кислоту, при этом наблюдали выделение газа. В другую пробирку
добавили раствор вещества Y и при этом наблюдали только образование
осадка.
1) иодид магния 2) цинк 3) гидрокарбонат кальция
4) гидроксид натрия 5) ортофосфат бария
Процент выполнения по региону– 66,40 %.
Установите соответствие между веществом и реагентами, с каждым из
которых это вещество может взаимодействовать: к каждой позиции,
обозначенной буквой, подберите соответствующую позицию, обозначенную
цифрой.
Вещество
Реагенты
А) H2SO4(разб)
1) BaCl2, K2S, KOH
Б) ZnSO4(р-р)
2) Br2, HI, H2O
В) Ba
3) Ag3PO4, CaO, CO2
Г) SiO2
4) Na2CO3, NaOH, HF
5) CaCO3, Fe(OH)2, Ag
Процент выполнения по региону– 44,61 %.
8. Задание №8
ЗАДАНИЕ №8Установите соответствие между исходными веществами, вступающими в
реакцию, и преимущественно образующимися продуктами этой реакции:
к каждой позиции, обозначенной буквой, подберите соответствующую
позицию, обозначенную цифрой.
Исходные вещества
Продукты реакции
A) HNO3(конц.) и Ag
1) Cu(NO3)2, NO2 и H2O
Б) HNO3(разб.) и Cu(OH)2
2) AgNO3 и H2O
В) HNO3(разб.) и Cu
3) Cu(NO3)2 и H2O
Г) HNO3(разб.) и Ag2O
4) Cu(NO3)2, NO и H2O
5) AgNO3, NO2 и H2O
6) AgNO3, NH4NO3 и H2O
Процент выполнения по региону– 55,23 %.
9. Задания №9-10
ЗАДАНИЯ №9-10Задана схема превращений веществ:
KOH(тв.), t°
HCl(изб.)
Al
→
X → Y
Определите, какие вещества являются веществами Х и Y.
1) K[Al(OH)4] 2) AlCl3 3) K3[Al(OH)6] 4) KAlO2 5) Al(OH)3
Процент выполнения по региону– 55,63 %.
Установите соответствие между общей формулой класса органических
веществ и веществом, которое принадлежит к этому классу: к каждой
позиции, обозначенной буквой, подберите соответствующую позицию,
обозначенную цифрой.
Общая формула Вещество
A) CnH2n-6
1) изопрен
Б) CnH2n-2
2) толуол
В) CnH2n-4
3) стирол
4) изобутан
Процент выполнения по региону– 75,28 %.
10. Задания №11-12
ЗАДАНИЯ №11-12Из предложенного перечня выберите два вещества, молекулы которых
содержат одну или несколько гидроксильных групп.
1) бензол 2) этилацетат 3) ацетон 4) этиленгликоль 5) фенол
Процент выполнения по региону– 63,55 %.
Из предложенного перечня выберите схемы всех реакций, для
определения продуктов которых следует применить правило
Марковникова.
1 ) СН2=СН-СН3 + H2O → (H+)
2) СН2=СН-СН3 + HBr →
3) СН2=СН-CH2-СН3 + HCl →
4) СН3-СН=CH-СН3 + HCl →
5) СН2=СН-СН3 + H2 → (Pt)
Запишите номера выбранных ответов.
Ответ:____________________________
Процент выполнения по региону– 42 %.
11. Задания №13-14
ЗАДАНИЯ №13-14Из предложенного перечня выберите два вещества, которые не
подвергаются гидролизу.
1) аминоуксусная кислота 2) триэтиламин 3) глицилглицин
4) крахмал 5) тристеарат глицерина
Процент выполнения по региону– 62,28%.
Установите соответствие между схемой реакции и продуктом, который
преимущественно образуется в результате этой реакции: к каждой
позиции, обозначенной буквой, подберите соответствующую позицию,
обозначенную цифрой.
Схема реакции
Продукт реакции
А) C2H5Cl + NaOH(спирт.) →
1) этен
Б) C2H5Cl + NaOH(водн.) →
2) бутен
В) C2H2 + Na →
3) этан
Г) C2H5Cl + Na →
4) н-бутан
5) ацетиленид натрия
6) этанол
Процент выполнения по региону– 59,03 %.
12. Задание №15
ЗАДАНИЕ №15Установите соответствие между схемой реакции и веществом Х,
принимающим участие в этой реакции: к каждой позиции, обозначенной
буквой, подберите соответствующую позицию, обозначенную цифрой.
Схема реакции
Вещество Х
Х
А) СН3ОН → НСНО
1) Cu(OH)2
Х
Б) CH3CH2OH → C2H4
2) CuO
Х
В) CH3CH2OH → CH3CH2OK
3) KOH(р-р)
Х
Г) СН3ОН → СН3ОCH3
4) K2CO3
5) H2SO4(конц.)
6) K
Процент выполнения по региону– 53,72 %.
13. Задания №16-17
ЗАДАНИЯ №16-17Задана следующая схема превращений веществ:
Х → хлорэтан → Y → метилпропан
Определите, какие из указанных веществ являются веществами Х и Y.
1) пропан 2) н-бутан 3) этилен 4) 2-хлорпропан 5) 1,2-дихлорэтан
Процент выполнения по региону– 62.12 %.
Из предложенного перечня выберите все типы реакций, к которым
можно отнести взаимодействие водорода с оксидом меди (II).
1) реакция замещения
2) окислительно-восстановительная реакция
3) обратимая реакция
4) гетерогенная реакция
5) каталитическая реакция
Ответ:_____________________________
Процент выполнения по региону– 46,91 %.
14. Задание №17
ЗАДАНИЕ №1715. Задание №18
ЗАДАНИЕ №18Из предложенного перечня выберите все реакции, которые при
одинаковых температуре и концентрации кислот протекают с
большей скоростью, чем взаимодействие оксида цинка с
раствором уксусной кислоты.
1) взаимодействие оксида цинка с соляной кислотой
2) взаимодействие оксида цинка с раствором масляной кислоты
3) взаимодействие растворов сульфида натрия и уксусной к-ты
4) взаимодействие растворов гидроксида натрия и уксусной к-ты
5) взаимодействие растворов гидроксида бария и азотной к-ты
Ответ:_____________________
Процент выполнения по региону– 59,27 %.
16. Задания №19-20
ЗАДАНИЯ №19-20Установите соответствие между уравнением реакции и свойством атома
азота в этой реакции: к каждой позиции, обозначенной буквой, подберите
соответствующую позицию, обозначенную цифрой.
Уравнение реакции
Свойство атома азота
A) P + 5HNO3 = H3PO4 + 5NO2 + H2O 1) и окислитель, и в-тель
Б) 2NH3 + 3CuO = N2 + 3Cu + 3H2O 2) только окислитель
В) N2O + H2 = N2 + H2O
3) не проявляет ок-в свойств
4) только восстановитель
Процент выполнения по региону– 75,59 %.
Установите соответствие между веществом и продуктами электролиза
водного раствора этого вещества, которые выделились на инертных
электродах: к каждой позиции, обозначенной буквой, подберите
соответствующую позицию, обозначенную цифрой.
Вещество
Продукты электролиза
А) сульфат калия
1) металл и кислород
Б) хлорид алюминия
2) водород и галоген
В) сульфид лития
3) водород и сера
4) водород и кислород
Процент выполнения по региону– 75,28 %.
17. Задание №21
ЗАДАНИЕ №21Для веществ, приведенных в перечне, определите характер среды их
водных растворов.
1) K3PO4 2) H2SO4 3) Pb(NO3)2 4) KClO3
Запишите номера веществ в порядке возрастания рН их водных
растворов, учитывая, что концентрация веществ во всех растворах
(моль/л) одинаковая.
Процент выполнения по региону– 71,79 %.
18. Задание №22
ЗАДАНИЕ №22Установите соответствие между способом взаимодействия на
равновесную систему
[Al(OH)4]-(р-р) + CH3COOH(р-р) ↔ Al(OH)3(тв.) + CH3COO-(р-р) + H2O(ж) + Q
И смещением химического равновесия в результате этого воздействия: к
каждой позиции, обозначенной буквой, подберите соответствующую
позицию, обозначенную цифрой.
Процент выполнения по региону– 56,26 %.
Воздействие на систему
Химическое равновесие
А) добавление уксусной к-лоты
1) смещается в сторону прямой реакции
Б) доб твердого ацетата калия
2) смещается в сторону обратной р-ции
В) доб тв гидроксида алюминия
3) практически не смещается
Г) увеличение давления
19. Задание №23
ЗАДАНИЕ №23В реактор постоянного объёма поместили водород и пары брома. При этом
концентрация паров брома составляла 0,12 моль/л. В результате
протекания обратимой реакции
H2(г) + Br2(г) ↔ 2HBr(г)
В реакционной системе установилось химическое равновесие, при котором
концентрации водорода и бромоводорода составили 0,27 моль/л и 0,18
моль/л соответственно. Определите исходную концентрацию Н2(Х)
равновесную концентрацию Br2 (Y).
1) 0,02 моль/л 2) 0,03 моль/л
3) 0,18 моль/л 4) 0,27 моль/л
5) 0,36 моль/л 6) 0,37 моль/л
Процент выполнения по региону– 84,55 %.
20. Задание №24
ЗАДАНИЕ №24Установите соответствие между веществами и реагентом, с помощью
которого можно различить эти вещества: к каждой позиции, обозначенной
буквой, подберите соответствующую позицию, обозначенную цифрой.
Вещества
Реагент
А) Mg(OH)2 и Zn(OH)2
1) NaCl
Б) NaOH(р-р) и Ba(OH)2(р-р)
2) HNO3
В) Sr(OH)2(р-р) и K3PO4(р-р)
3) CaF2
Г) Ba(OH)2(р-р) и K3PO4(р-р)
4) K2SO4
5) KOH(конц.)
Процент выполнения по региону– 51,03%.
21. Задание №25
ЗАДАНИЕ №25Установите соответствие между мономером и полимером,
образующимся при его полимеризации: к каждой позиции,
обозначенной буквой, подберите соответствующую позицию,
обозначенную цифрой.
Мономер
Полимер
А) хлорэтен
1) натуральный каучук
Б) 2-хлорбутадиен-1,3
2) поливинилхлорид
В) бутадиен-1,3
3) дивиниловый каучук
4) хлоропреновый каучук
Процент выполнения по региону– 55,94%.
22.
Задания №26-28Какую массу 12%-ного раствора нитрата бария надо взять, чтобы при
добавлении 30 г воды получить раствор с массовой долей соли 8%?
(запишите число с точностью до целых). Ответ: _______________ г.
Процент выполнения по региону– 62,76 %.
Горение угля протекает в соответствии с термохимическим
уравнением реакции
С(графит) + О2(г) = СО2(г) + 393,5 кДж.
Вычислите количество вещества кислорода, который необходим для
получения 590 кДж (запишите число с точностью до десятых).
Ответ: _______________ моль.
Процент выполнения по региону– 74,96 %.
Вычислите массу аммиака, полученного с выходом 25% при
взаимодействии 44,8 л (н.у.) азота с избытком водорода. (запишите
число с точностью до целых) Ответ: _______________ г.
Процент выполнения по региону– 47,86%.
23. Задание №29-30
ЗАДАНИЕ №29-30Даны вещества: гидроксид стронция, сульфид меди (II), фосфин,
азотная кислота, перманганат калия, дигидрофосфат натрия.
Из предложенного перечня выберите вещества, окислительновосстановительная реакция между которыми протекает в растворе
только кислоты и выделением газа. В ответе запишите уравнение
только одной из возможных окислительно-восстановительных
реакций с участием выбранных веществ. Составьте электронный
баланс (запишите уравнения процессов окисления и восстановления),
укажите окислитель и восстановитель.
Процент выполнения по региону– 44,73 %.
Из предложенного перечня выберите два вещества, реакция ионного
обмена между которыми приводит к образованию осадка. Запишите
молекулярное, полное и сокращенное ионное уравнения реакции с
участием выбранных веществ.
Процент выполнения по региону– 45,17 %.
24. Задания №31-32
ЗАДАНИЯ №31-32Гидросульфит калия обработали бромоводородной кислотой.
Выделившийся при этом газ смешали с сероводородом. Полученное
твердое вещество растворили в горячей концентрированной азотной
кислоте, при этом наблюдалось интенсивное выделение бурого газа. Газ
при охлаждении пропустили через раствор гидроксида натрия.
Процент выполнения по региону– 47,37 %.
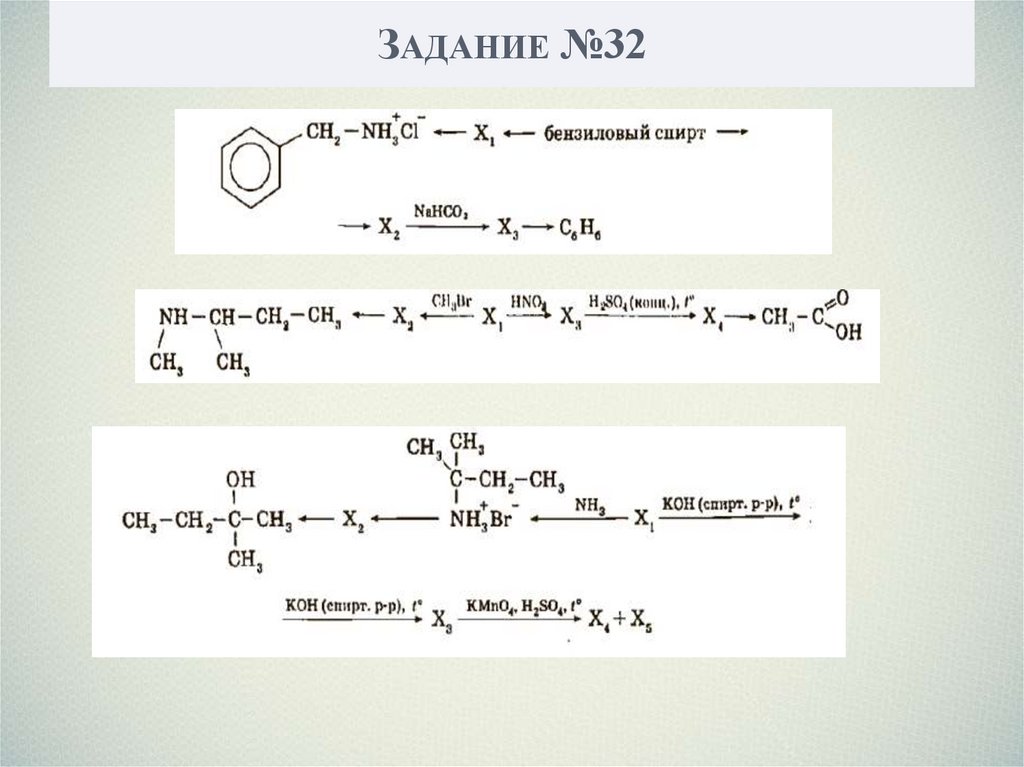
Напишите уравнения реакций, с помощью которых можно осуществить
следующие превращения:
KMnO4(водн.р-р), t°
Cl2, hν
Толуол
→
Х1 → С6Н6 → Х2 → Х3 → С6Н11-С6Н11
Процент выполнения по региону– 47,35 %.
25. Задание №33
ЗАДАНИЕ №33При сгорании 29,2 г органического вещества А образовалось 26,88 л (н.у.)
оксида углерода (IV), 4,48 л (н.у.) азота и 25,2 г воды. Известно, что молекула
вещества А имеет неразветвленный углеродный скелет, содержит три
функциональные группы, при этом азотсодержащие группы максимально
удалены друг от друга. Вещество А способно реагировать как с соляной
кислотой, так и с гидроксидом натрия.
На основании данных условия задачи:
1) приведите необходимые вычисления и установите молекулярную формулу
вещества А;
2) составьте структурную формулу вещества А, которая однозначно отражает
порядок связи атомов в его молекуле;
3) напишите уравнение реакции вещества А с избытком соляной кислоты
(используйте структурные формулы органических веществ).
Процент выполнения по региону– 37,08 %.
26. Задание №34
ЗАДАНИЕ №34К 64 г насыщенного раствора гидроксида натрия добавили
25,7 г фосфида цинка. После окончания реакции к
образовавшемуся раствору прилили 137,2 г 50%-ного
раствора серной кислоты. Вычислите массовую долю
сульфата цинка в конечном растворе. В условиях, при
которых были проведены реакции, растворимость гидроксида
натрия составляет 100 г на 100 г воды, сульфата цинка – 57,7
г на 100 г воды, растворимость сульфата натрия – 28 г на 100
г воды.
Процент выполнения по региону– 11,25 %.






























 chemistry
chemistry








