Similar presentations:
Будова атома. Ядро й електронні оболонки. Склад атомних ядер
1.
12. Цілі уроку
Продовжити знайомство з періодичноюсистемою хімічних елементів
Д.І.Менделєєва;
Розкрити зміст порядкового номера
елемента на основі знань про будову
атома;
Розширити знання про радіоактивність;
Сформувати поняття сучасного
періодичного закону;
Формувати уміння обчислювати кількість
протонів, нейтронів і електронів у атомі.
2
3. Хімічна фортуна
34. Атом
Найменшаелектронейтральна частинка
хімічного елемента, яка несе
усі властивості елемента.
5. Розмір атомів
Атом має дуже малі розміри1 нм = 10-9м
Наприклад, радиус атома
заліза 0,13 нм.
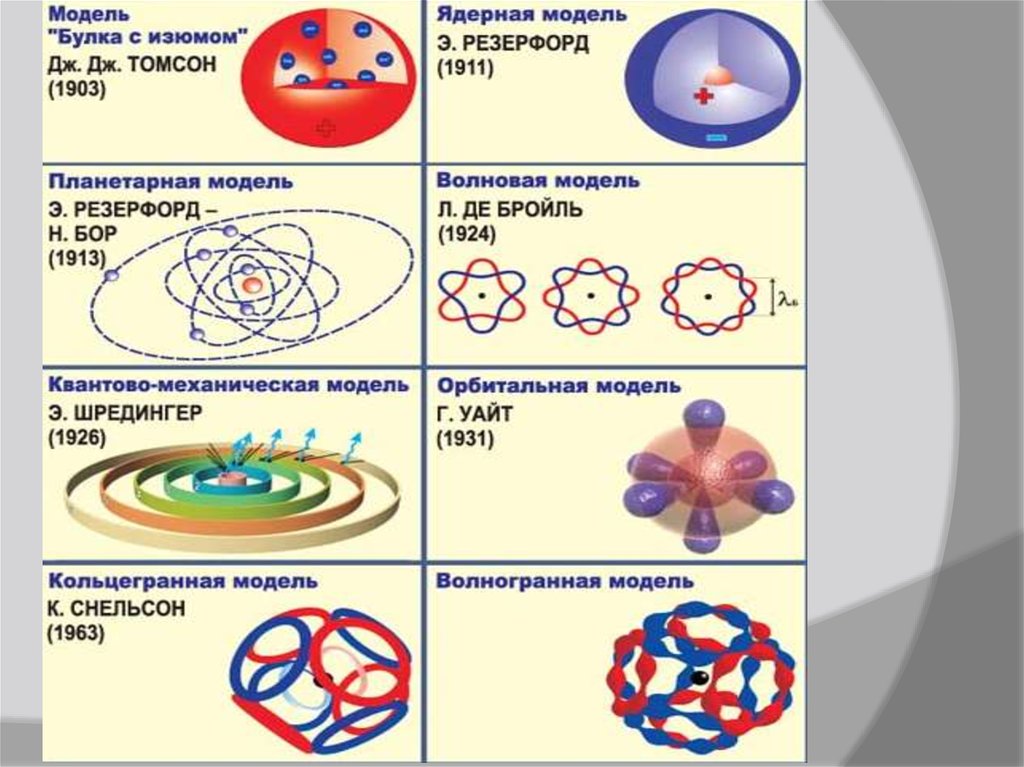
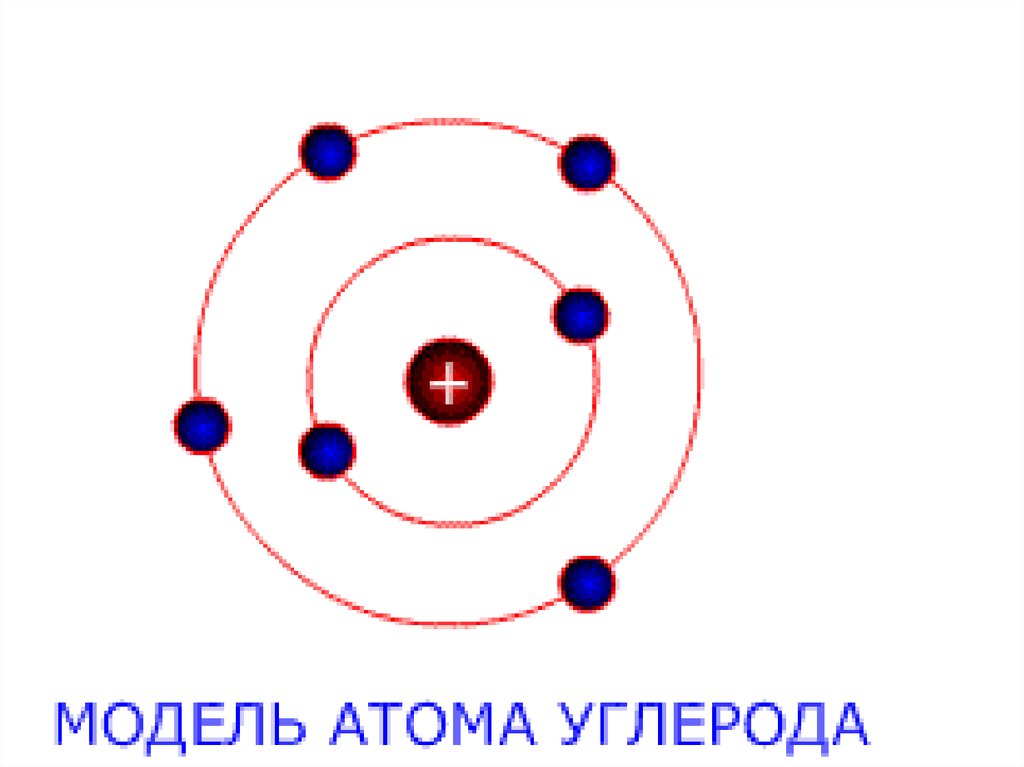
6. Історичні моделі будови атомів
7.
8.
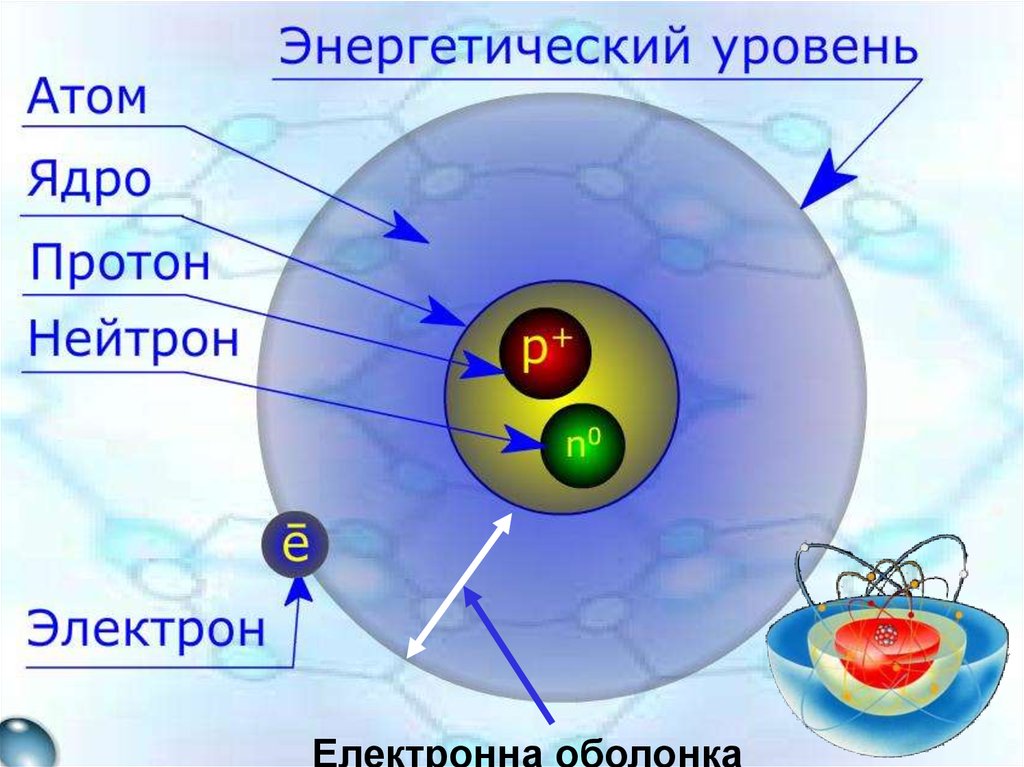
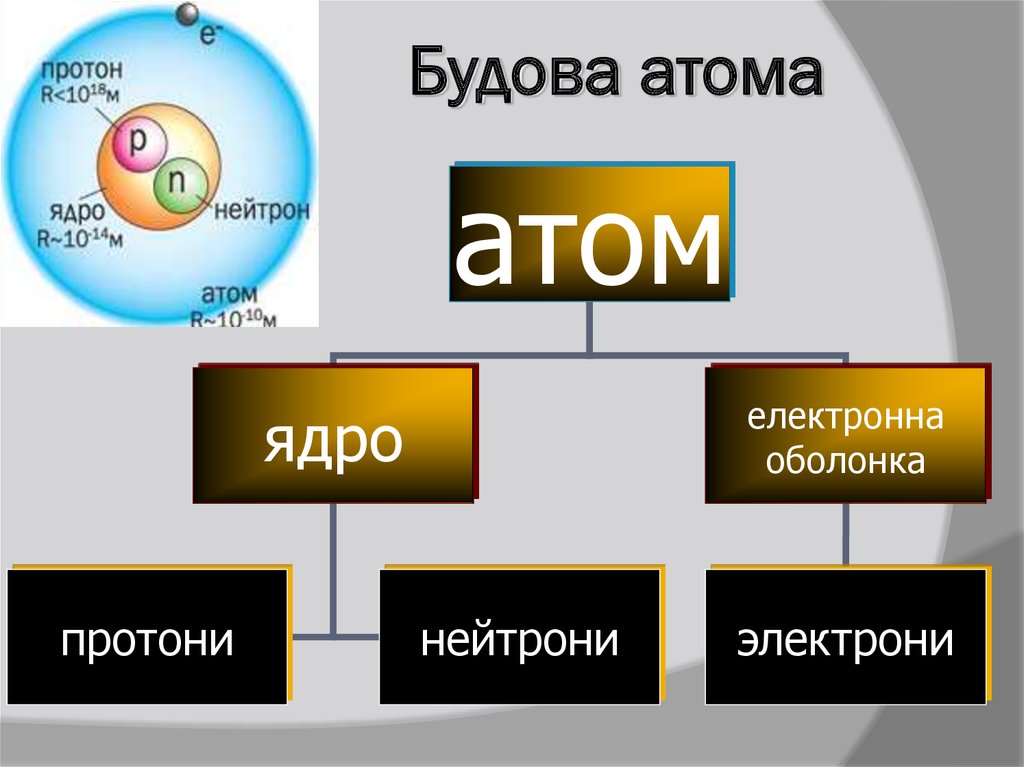
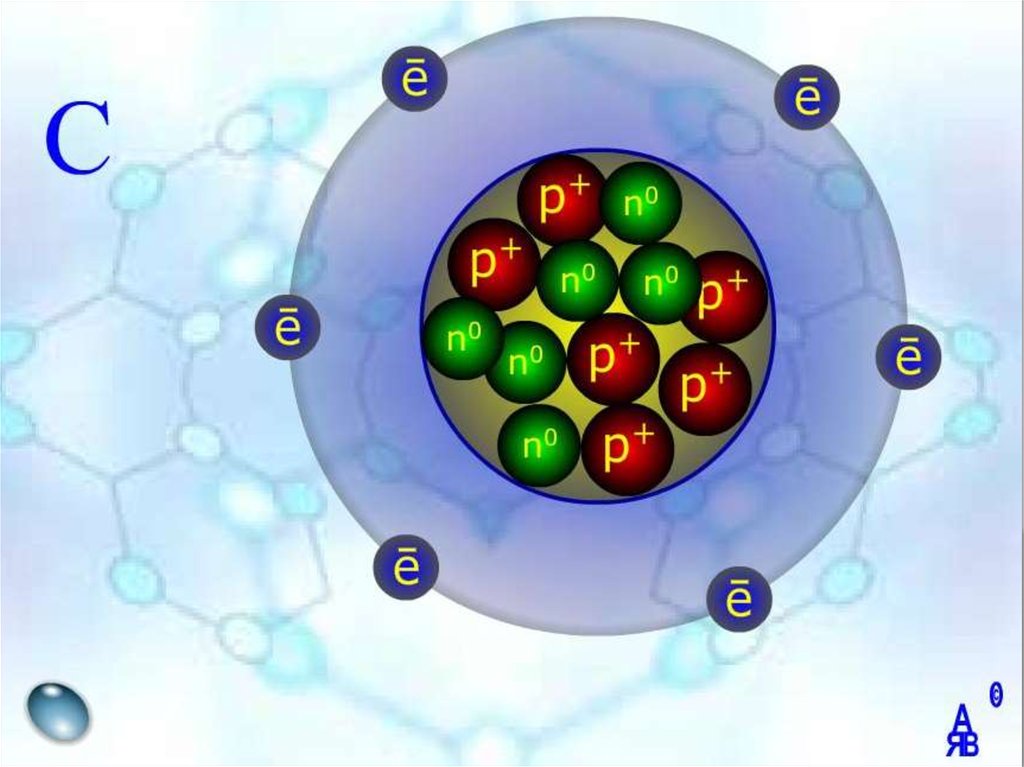
Електронна оболонка9. Будова атома
атомелектронна
оболонка
ядро
протони
нейтрони
электрони
10.
Нейтрон– нейтральна частинка, що не
має електричного заряду
Протон
– позитивно заряджена
частинка
Електрон
– негативно заряджена
частинка
Демидова О.Л.
10
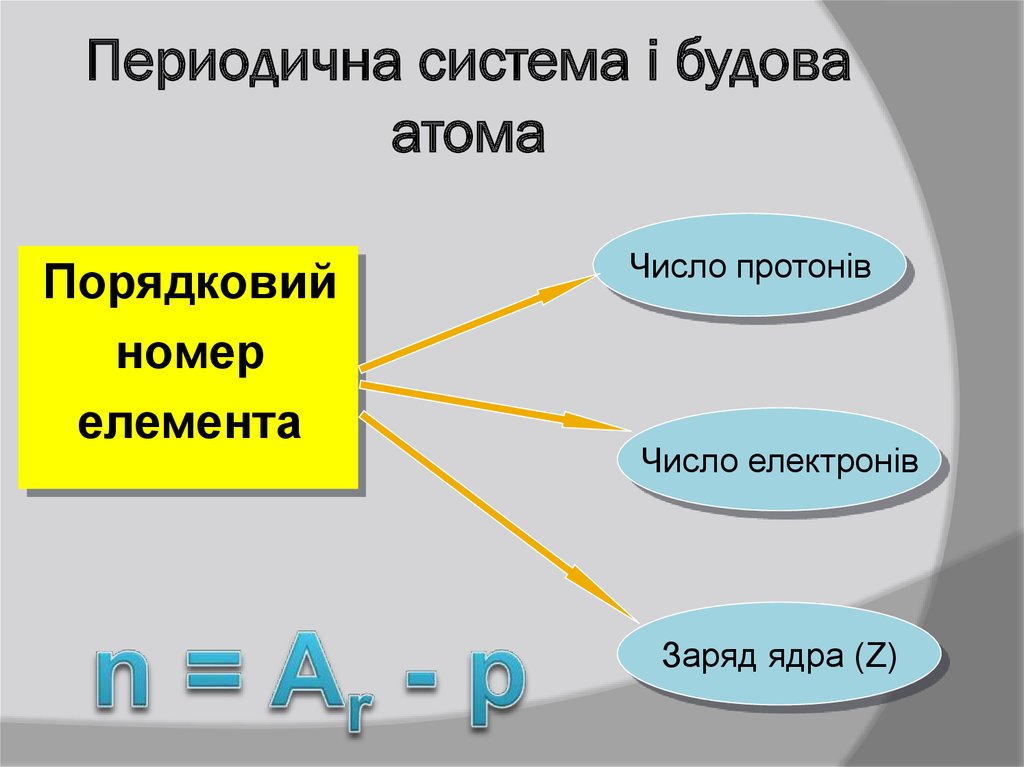
11. Периодична система і будова атома
Порядковийномер
елемента
Число протонів
Число електронів
Заряд ядра (Z)
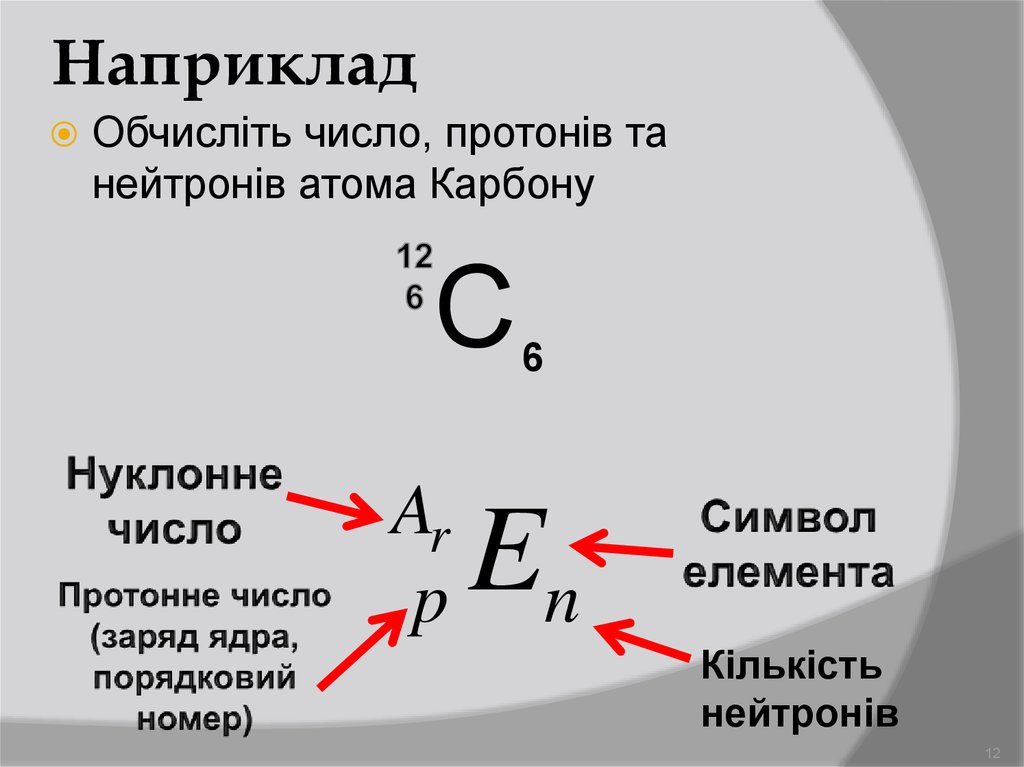
12. Наприклад
Обчисліть число, протонів танейтронів атома Карбону
С
Ar
p
6
En
Кількість
нейтронів
12
13.
14.
15. Основні терміни
– загальна кількістьпротонів і нейтронів
Протонне число – загальне
число протонів
Нуклонне число – загальне
число протонів і нейтронів
Хімічний елемент – вид атомів
із певним протонним числом
Нуклони
Демидова О.Л.
15
16. Домашня робота
Опрацюватипараграф
22;
Вик. пис. впр. № 1-4
ст.123
Демидова О.Л.
16
17.
18. Сторінками історії
А.Беккерель у1896
році виявив, що
матеріали, які містять
Уран, засвідчують у
темряві
фотопластинку,
спричиняють світіння
речовин. Надалі
з’ясувалось, що цю
здатність має не лише
Уран.
Демидова О.Л.
18
19.
П’єр і Марія СклодовськаКюрі відкрили два новірадіоактивні елементи –
Полоній і Радій. І у 1903
році одержали Нобелівську
премію з фізики за відкриття
радіоактивності.
У 1911 році після смерті
чоловіка Марія була
удосконалена Нобелівської
премії у галузі хімії за
відкриття нею Радію.
Демидова О.Л.
19
20. Радіоактивність
Цездатність деяких
елементів випромінювати.
Радіоактивний розпад
• Процес розпадання ядер на
менші ядра, окремі частинки
– α, β, γ.
Демидова О.Л.
20
21.
α-випромінення –випромінювання позитивно
заряджених частинок (ядра
Гелію)
β-випромінення – це
випромінювання негативно
заряджених частинок
(електронів)
γ-випромінення – випромінення
електромагнітних хвиль
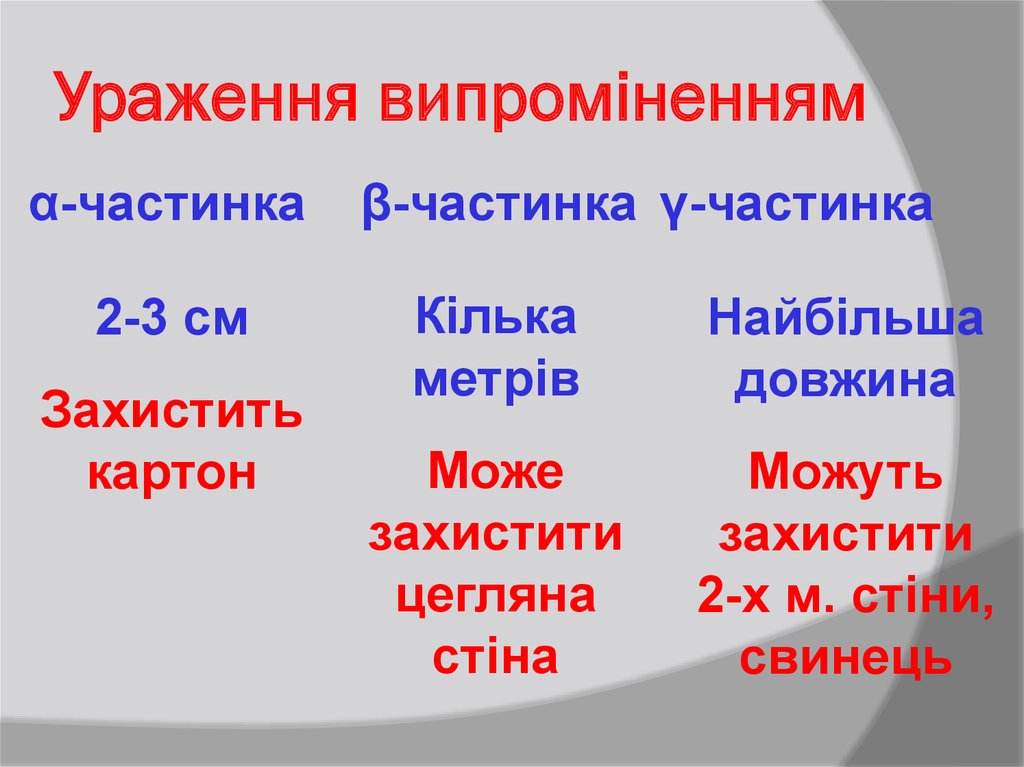
22. Ураження випроміненням
α-частинка2-3 см
Захистить
картон
β-частинка γ-частинка
Кілька
метрів
Найбільша
довжина
Може
захистити
цегляна
стіна
Можуть
захистити
2-х м. стіни,
свинець
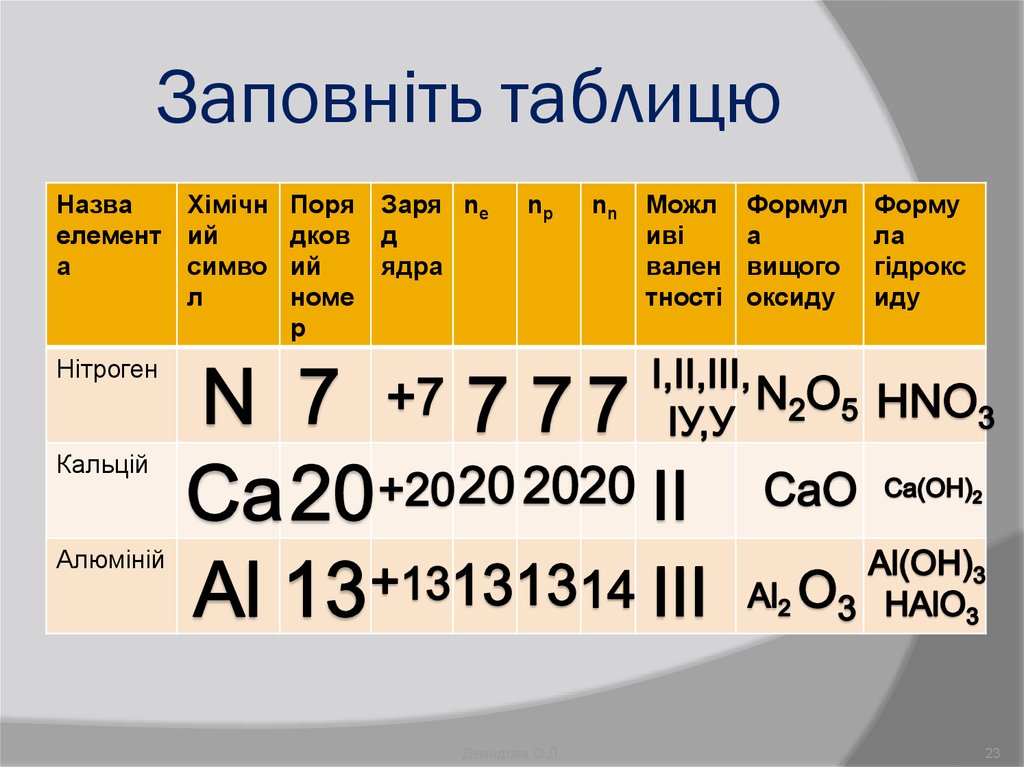
23. Заповніть таблицю
НазваХімічн Поря
елемент ий
дков
а
симво ий
л
номе
р
Заря ne
д
ядра
np
nn
Можл
иві
вален
тності
Формул
а
вищого
оксиду
Форму
ла
гідрокс
иду
Нітроген
Кальцій
Алюміній
Демидова О.Л.
23
24.
Демидова О.Л.24
25. Домашня робота
Опрацюватипараграф
23;
Вик. пис. впр. № 5-7
ст.132
Демидова О.Л.
25
26. Дякую за урок
Допобачення
Демидова О.Л.
26
27.
Назвітьелемент VІ
групи, відносна
молекулярна маса
сполуки з Гідрогеном
якого дорівнює 81
Демидова О.Л.
27
28.
Назвітьелемент V
групи, відносна
молекулярна маса
оксиду якого
дорівнює 142
Демидова О.Л.
28
29.
Порівняйтеметалічні
властивості
елементів: Алюмінію
та Галію, Кальцію та
Барію.
Демидова О.Л.
29
30.
Порівняйтенеметалічні
властивості
елементів: Оксигену
та Карбону, Флуору
та Бору.
Демидова О.Л.
30
31.
Яккласифікують
групи та періоди?
Демидова О.Л.
31
32.
Якзмінюється
валентність у
періодичній
системі хімічних
елементів?
Демидова О.Л.
32
33.
Якзмінюються
неметалічні та
металічні
властивості
елементів у періодах
Демидова О.Л.
33
34.
Розкажітьпро
структуру
періодичної системи
хімічних елементів
Демидова О.Л.
34
35.
Щоназивають
групою?
Демидова О.Л.
35
36.
Щоназивається
періодом?
Демидова О.Л.
36



























 chemistry
chemistry








