Similar presentations:
Железоуглеродистые сплавы
1. Материаловедение
Преподаватель:Зольников А.Е.
2. ЖЕЛЕЗОУГЛЕРОДИСТЫЕ СПЛАВЫ
3.
• Основными конструкционнымиматериалами являются стали и чугуны.
• Стали и чугуны представляют собой сплавы
железа с углеродом.
• Компонентами железоуглеродистых
сплавов являются железо, углерод и
цементит.
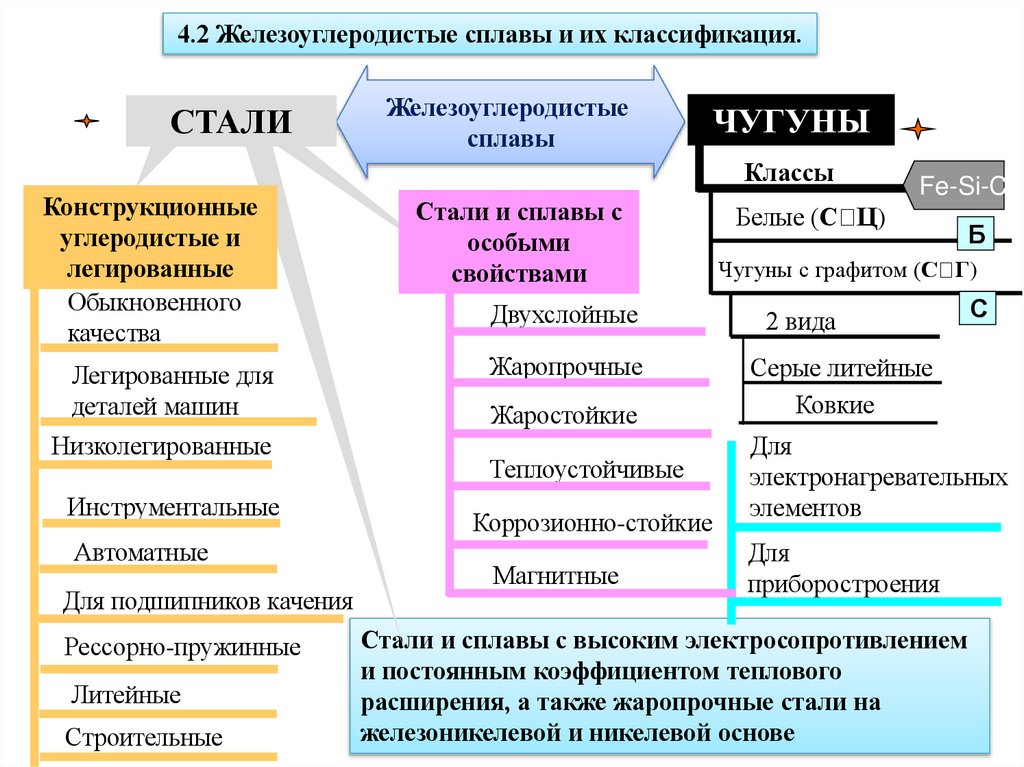
4. 4.2 Железоуглеродистые сплавы и их классификация.
СТАЛИЖелезоуглеродистые
сплавы
ЧУГУНЫ
Классы
Конструкционные
углеродистые и
легированные
Обыкновенного
качества
Легированные для
деталей машин
Низколегированные
Инструментальные
Автоматные
Для подшипников качения
Рессорно-пружинные
Литейные
Строительные
Стали и сплавы с
особыми
свойствами
Fe-Si-C
Белые (С Ц)
Чугуны с графитом (С Г)
Двухслойные
2 вида
Жаропрочные
Серые литейные
Ковкие
Жаростойкие
Теплоустойчивые
Коррозионно-стойкие
Магнитные
Б
С
Для
электронагревательных
элементов
Для
приборостроения
Стали и сплавы с высоким электросопротивлением
и постоянным коэффициентом теплового
расширения, а также жаропрочные стали на
железоникелевой и никелевой основе
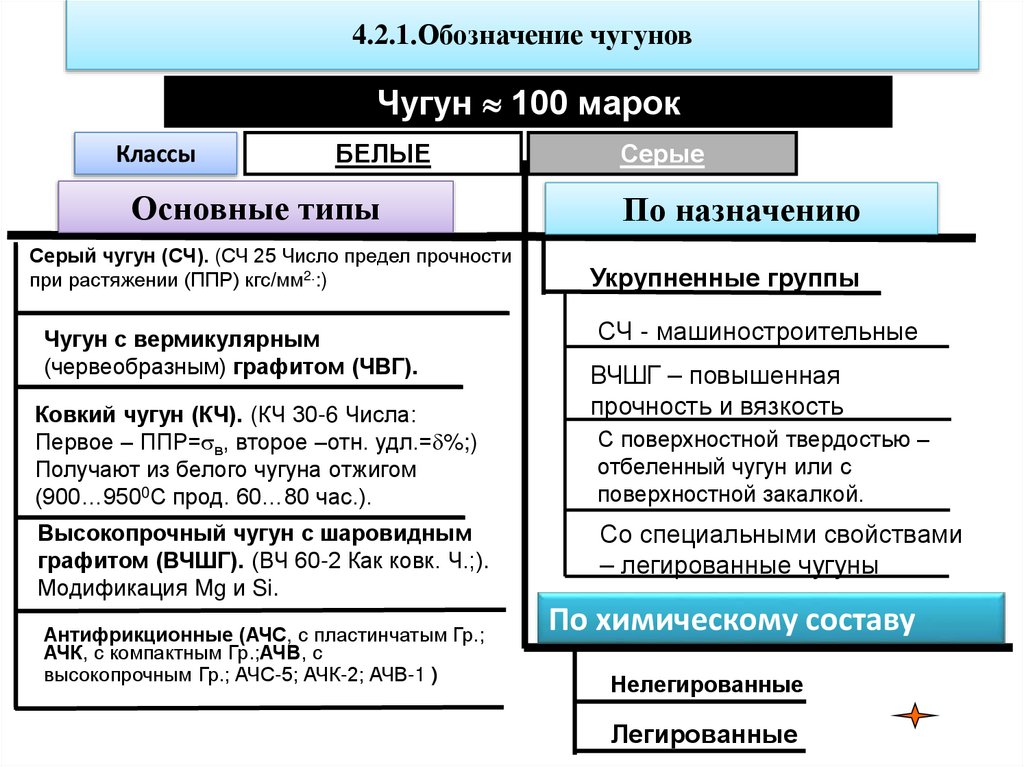
5. 4.2.1.Обозначение чугунов
Чугун 100 марокКлассы
БЕЛЫЕ
Основные типы
Серый чугун (СЧ). (СЧ 25 Число предел прочности
при растяжении (ППР) кгс/мм2.:)
Чугун с вермикулярным
(червеобразным) графитом (ЧВГ).
Ковкий чугун (КЧ). (КЧ 30-6 Числа:
Первое – ППР= в, второе –отн. удл.= %;)
Получают из белого чугуна отжигом
(900…9500С прод. 60…80 час.).
Высокопрочный чугун с шаровидным
графитом (ВЧШГ). (ВЧ 60-2 Как ковк. Ч.;).
Модификация Mg и Si.
Антифрикционные (АЧС, с пластинчатым Гр.;
АЧК, с компактным Гр.;АЧВ, с
высокопрочным Гр.; АЧС-5; АЧК-2; АЧВ-1 )
Серые
По назначению
Укрупненные группы
СЧ - машиностроительные
ВЧШГ – повышенная
прочность и вязкость
С поверхностной твердостью –
отбеленный чугун или с
поверхностной закалкой.
Со специальными свойствами
– легированные чугуны
По химическому составу
Нелегированные
Легированные
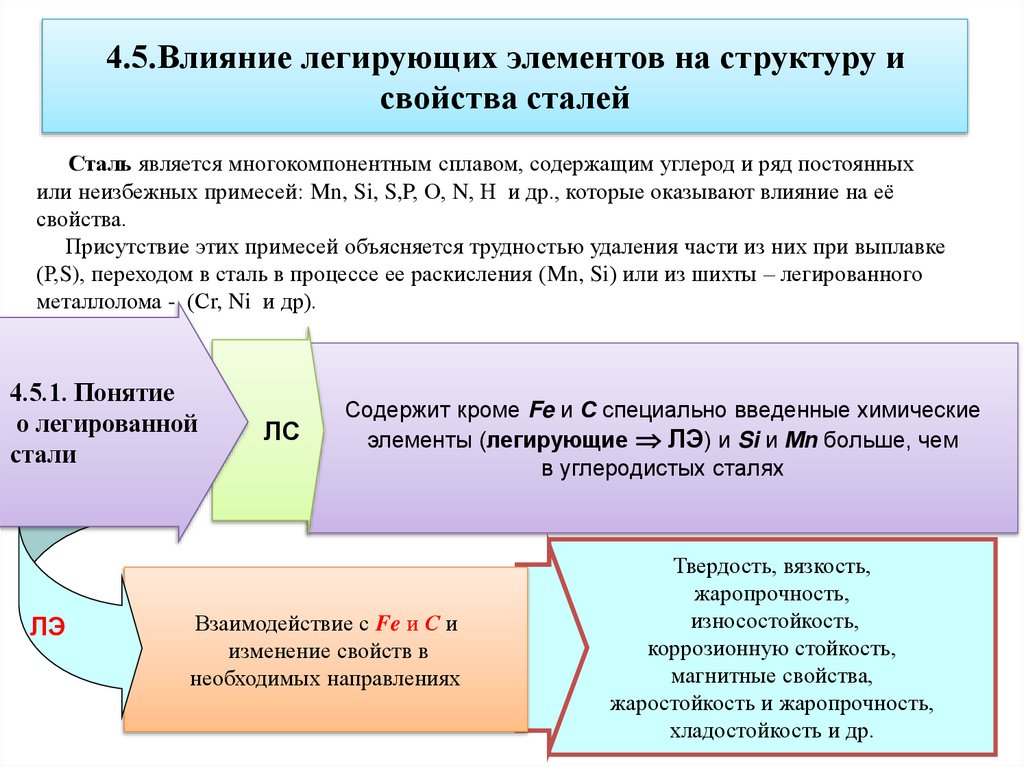
6. 4.5.Влияние легирующих элементов на структуру и свойства сталей
Сталь является многокомпонентным сплавом, содержащим углерод и ряд постоянныхили неизбежных примесей: Mn, Si, S,P, О, N, Н и др., которые оказывают влияние на её
свойства.
Присутствие этих примесей объясняется трудностью удаления части из них при выплавке
(Р,S), переходом в сталь в процессе ее раскисления (Mn, Si) или из шихты – легированного
металлолома - (Сr, Ni и др).
4.5.1. Понятие
о легированной
стали
ЛЭ
ЛС
Содержит кроме Fe и С специально введенные химические
элементы (легирующие ЛЭ) и Si и Мn больше, чем
в углеродистых сталях
Взаимодействие с Fe и С и
изменение свойств в
необходимых направлениях
Твердость, вязкость,
жаропрочность,
износостойкость,
коррозионную стойкость,
магнитные свойства,
жаростойкость и жаропрочность,
хладостойкость и др.
7. 4.5.2 Распределение легирующих элементов в стали
зависит от их свойств в соответствии сих положением впериодической системе (таблице) элементов Д.И.МЕНДЕЛЕЕВА.
Растворяются в Fe и Fe3C
почти все элементы
Образуют самостоятельные карбиды левее Fe Ti,Nb,V, W,Mo,Cr,
Взаимодействие
Mn, и др. Образ. Фазы внедрения МеС (чаще), Ме2С
ЛЭ
Карбиды не образуют правее Fe Ni,Co,Si,Cu и др.
с
Fe и С
Не растворяются в Fe далеко от Fe О,В,S.
Химические соединения с Fe
большинство ЛЭ при большом сод.
Не растворяются в Fe и не образуют химсоединения с
Образуют оксиды
Pb, Ag.
Mn,Si,Al,Ni,Ti,V и др. при раскислении.
8. 4.5.3.Влияние основных легирующих элементов на структуру и свойства сталей
Хром - повышает твердость и прочность, сохраняет вязкость, увеличивает
сопротивляемость стали коррозии.
Никель – повышает прочность, ударную вязкость, коррозионную стойкость,
прокаливаемость стали.
Вольфрам – образует очень твердые карбиды, резко увеличивает твердость и
красностойкость стали.
Ванадий - увеличивает плотность стали, измельчает зерно и повышает твердость и
прочностью.
Кобальт - увеличивает ударную вязкость, жаропрочность и магнитные свойства стали.
Молибден – повышает упругость, прочность, красностойкость, коррозионную
стойкость и окалийностойкость стали.
Медь – усиливает антикоррозионные свойства стали.
Титан – увеличивает прочность стали, повышает обрабатываемость и сопротивление
стали.
Ниобий – повышает сопротивление коррозии.
Алюминий – повышает жаростойкость (совместно с кремнием улучшает коррозионную
стойкость)
Цирконий - позволяет получать мелкозернистую сталь.
9. 4.5.5. Растворение легирующих элементов в стали
Близкие к Fe в табл. МенделееваЛЭ
Кристаллич. решетка ЛЭ подобна Fe
атом ЛЭ атом Fe
Твердые
растворы
замещения
(ТРЗ)
Раство атом ЛЭ - атом Fe РА
римость
Количество ЛЭ
ЛЭ зависит
Валентность
от
Крист.реш. ЛЭ одинакова Fe неограниченная растворимость РА 8%
Ограниченная растворимость 8% РА 15%
Не образуют растворов и не смешиваются (расплав) РА 20%
Растворимость
в Fe и
Fe
Ограниченная (ТРЗ) Cr, Mn, V, Si, Mo, W, Ni, Nb, Al, Zr.
Полная с Fe Ni, Co.
Хорошо растворяются в А Ni, Mr, Cr и др.
Растворы внедрения
атом ЛЭ меньше 63% атом Fe B, C, N, O, H.
Искажение решетки изменение свойств
10. Железо обладает полиморфизмом – способностью изменять свою кристаллическую решетку.
11.
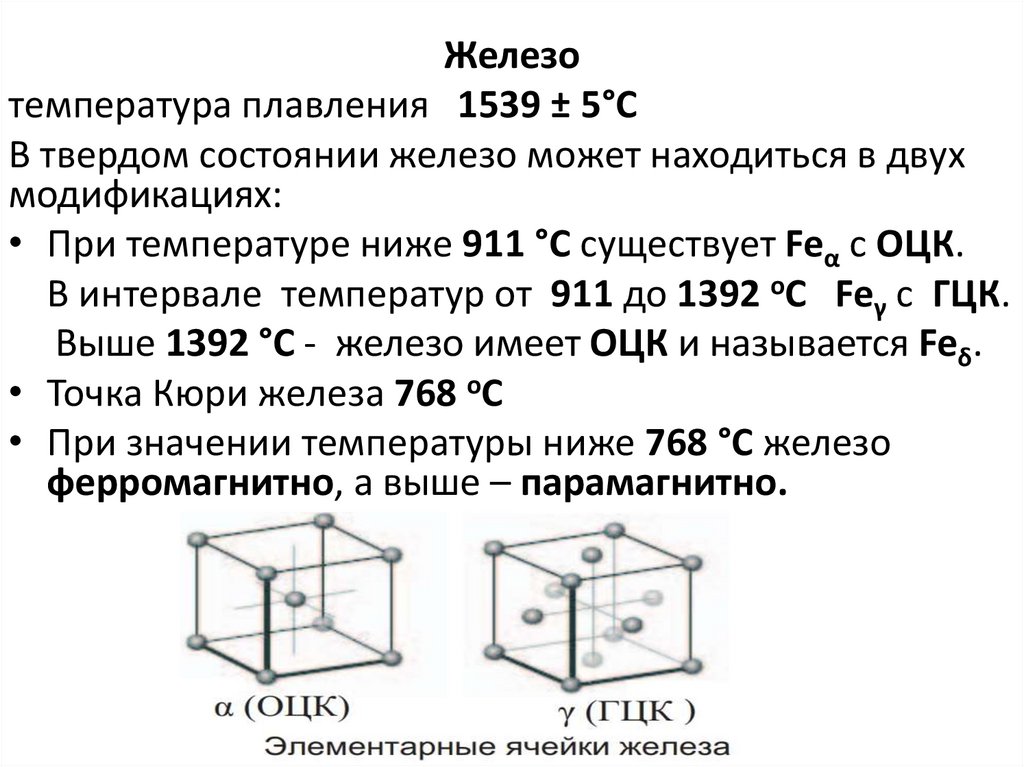
Железотемпература плавления 1539 ± 5°С
В твердом состоянии железо может находиться в двух
модификациях:
• При температуре ниже 911 °С существует Feα с ОЦК.
В интервале температур от 911 до 1392 oС Feγ с ГЦК.
Выше 1392 °С - железо имеет ОЦК и называется Feδ.
• Точка Кюри железа 768 oС
• При значении температуры ниже 768 °С железо
ферромагнитно, а выше – парамагнитно.
12.
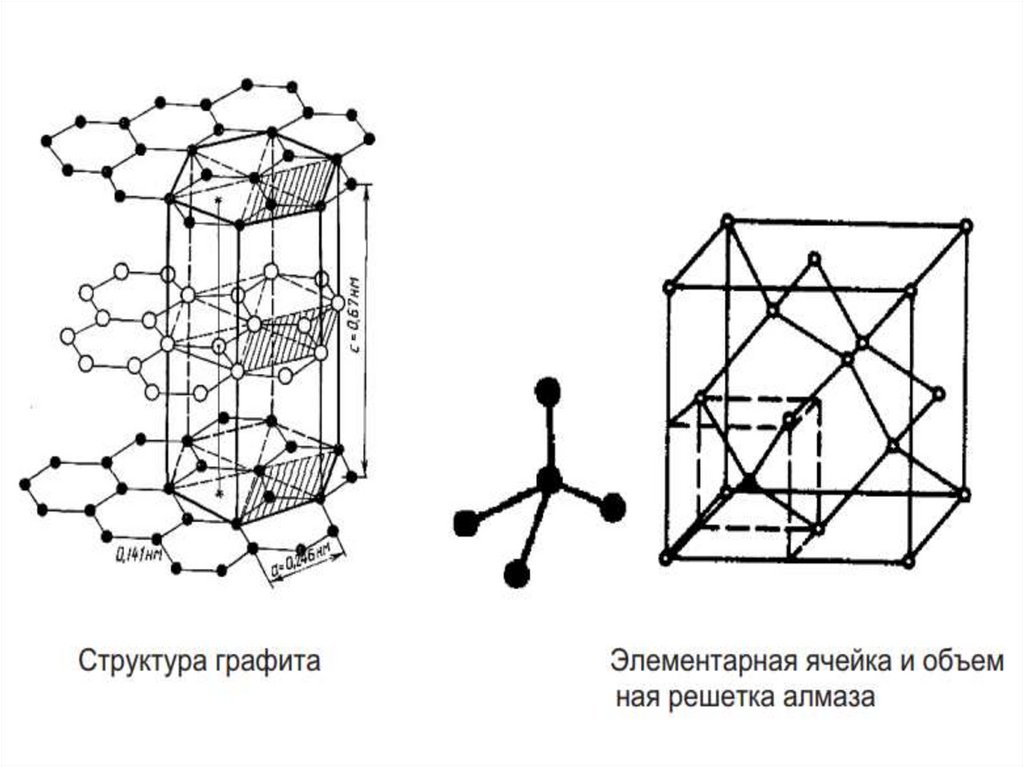
2. Углерод.Неметаллический элемент, обладающий
полиморфизмом.
• Может существовать в форме графита с
гексагональной кристаллической решеткой
(температура плавления 3500 °С)
• Графит имеет слоистое строение, обладает низкой
механической прочностью.
• Углерод в форме алмаза имеет сложную кубическую
решетку (температура плавления 5000 °С).
• Алмаз – чрезвычайно твердый, что объясняется
строением кристаллической решетки с ковалентной
межатомной связью.
13.
14. Взаимодействие железа и углерода в сплаве
• 1. Углерод растворяется в железе в жидком и твердомсостоянии, образуя твердые растворы:
• Твердый раствор внедрения углерода в α – железе –
называют Феррит обозначается Feα (C)
• Феррит имеет переменную предельную
растворимость углерода:
минимальную – 0,006 % при комнатной температуре
(точка Q на диаграмме ),
максимальную – 0,02 % при температуре 727 °С (точка
P на диаграмме).
• Свойства феррита близки к свойствам чистого железа.
Он мягкий и пластичный (130 НВ), магнитный до 768 °С .
15.
• Твердый раствор внедрения углерода в γ-железеназывается Аустенит (А) обозначается Feγ (С)
Углерод занимает место в центре
гранецентрированной кубической ячейки.
• Аустенит имеет переменную предельную
растворимость углерода:
минимальную – 0,8 % при температуре 727 °С (точка S ),
максимальную – 2,14 % при 1147 °С (точка Е).
Аустенит имеет более высокую твердость 200-250 НВ,
пластичный, парамагнитный.
16.
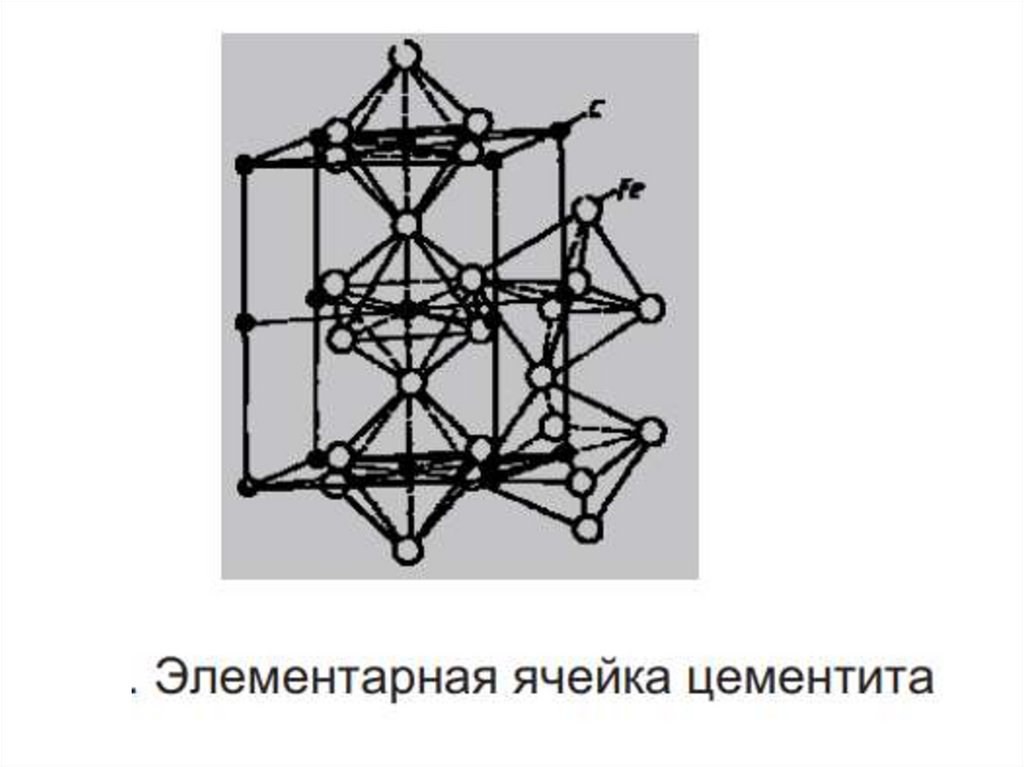
2. Железо и углерод могут образовыватьхимическое соединение Цементит (Fe3C) (карбид
железа), содержит 6,67 % углерода.
Цементит имеет высокую твердость (800 НВ),
практически нулевую пластичность.
• Аллотропных превращений не испытывает.
• Температура плавления Fe3C около 1550 °С .
• При низких температурах цементит слабо
ферромагнитен, магнитные свойства теряет при
температуре около 217 °С.
• Цементит – соединение неустойчивое и при
определенных условиях распадается с
образованием свободного углерода в виде
графита.
17.
18.
• 3. В высокоуглеродистых соединениях углерод можетнаходиться в чистом виде – т.е. в виде графита(серые
чугуны)
В системе Fе – Fе3С могут существовать следующие
фазы:
• жидкая фаза (в жидком состоянии железо хорошо
растворяет углерод в любых пропорциях),
• твердые растворы (феррит, аустенит),
• химическое соединение (цементит)
• свободный углерод в виде графита.
• Кроме того, к структурным составляющим относят
перлит и ледебурит – механические смеси.
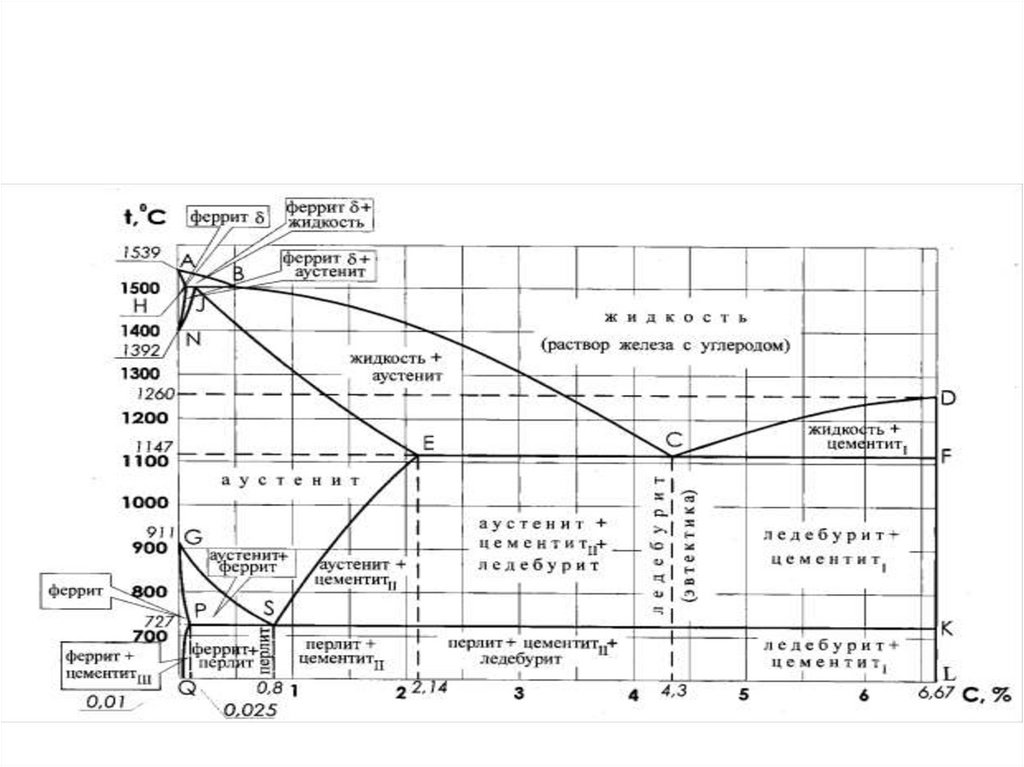
19. Диаграмма состояния железо-углерод (железо – цементит)
• Эта диаграмма представляет собой частьдиаграммы железо-углерод.
• Содержание углерода ограничивается 6,67 %,
таким образом вторым компонентом этой
диаграммы является химическое соединение
– цементит.
20.
• Фазовые и структурные изменения,происходящие при охлаждении или нагреве
железо-углеродистых сплавов связаны с
изменением кристаллической решетки железа
и изменением растворимости в нем углерода.
• При понижении температуры растворимость
углерода в железе уменьшается.
21.
22.
23.
24.
• Ж- жидкость• А – аустенит
• Ф – феррит
• Ц- цементит (первичный, вторичный,
третичный)
• Л-ледебурит
• П-перлит
25.
• Линия АСD – линия ликвидуса. Выше этой линиисплав находится в жидком состоянии
• Линия AECF – линия солидуса. Ниже этой линии
сплав находится в твердом состоянии
• По линии АС – кристаллизуется аустенит
• По линии СD – кристаллизуется цементит,
называемый – первичным
• В точке С – аустенит и цементит кристаллизуются
одновременно, образуя эвтектический сплав,
называемый ледебуритом
26.
• ЛЕДЕБУРИТ (Л) – эвтектическая смесь, котораяобразуется из жидкой фазы (из расплава) с
концентрацией углерода 4,3 % при температуре
1147 °С. В диапазоне температур 1147...727 °С
ледебурит состоит из двух фаз – аустенита и
цементита.
• При температуре ниже 727 °С аустенит внутри
ледебурита превращается в перлит. Таким
образом, ниже 727 °С ледебурит также
представляет механическую смесь, но состоящую
уже из перлита и цементита (а по фазам – из
феррита и цементита). Содержание углерода в
ледебурите всегда постоянно и составляет 4,3 %.
27.
• По линии ES – из аустенита выделяетсявторичный цементит.
• По линии GS – кристаллизуется феррит
• По лини GP – превращение аустенита в феррит
заканчивается.
• При достижении температуры 727 С происходит
эвтектоидное превращение аустенита, т.е.
• PSK – линия эвтектоидного превращения.
По механизму данное превращение похоже на
эвтектическое, но протекает в твердом состоянии.
• При содержании углерода 0,8% образуется
эвтектоидный сплав - перлит.
28.
• ПЕРЛИТ (П) – эвтектоидная смесь,состоящая из двух фаз –феррита и
цементита. Эта структура образуется в
результате распада аустенита с
содержанием углерода 0,8 % при
температуре 727 °С и ниже. Содержание
углерода в перлите для всех
железоуглеродистых сплавов всегда
постоянно и равно 0,8 %.
29.
Цементит. В железоуглеродистых сплавахприсутствуют:
• цементит первичный (ЦI),
• цементит вторичный (ЦII),
• цементит третичный (ЦIII).
• Химические и физические свойства этих фаз
одинаковы.
• ЦI выделяется из жидкой фазы в виде крупных
пластинчатых кристаллов. (DC)
• ЦII выделяется из аустенита и располагается в
виде сетки вокруг зерен аустенита (при
охлаждении – вокруг зерен перлита). (ES)
• ЦIII выделяется из феррита и в виде мелких
включений располагается у границ ферритных
зерен. (PQ)
30.
• Железоуглеродистые сплавы с долейуглерода, не превышающей 2,14 %, называют
сталями.
• В их структуре имеется перлит, но отсутствует
ледебурит.
• По структуре стали в зависимости от
содержания углерода подразделяют на:
техническое железо (С < 0,02 %),
Углеродистые стали(0,02-2,14%):
доэвтектоидные (0,02 < С < 0,8 %),
эвтектоидные (С = 0,8 %)
и заэвтектоидные стали (0,8 < С < 2,14 %).
31.
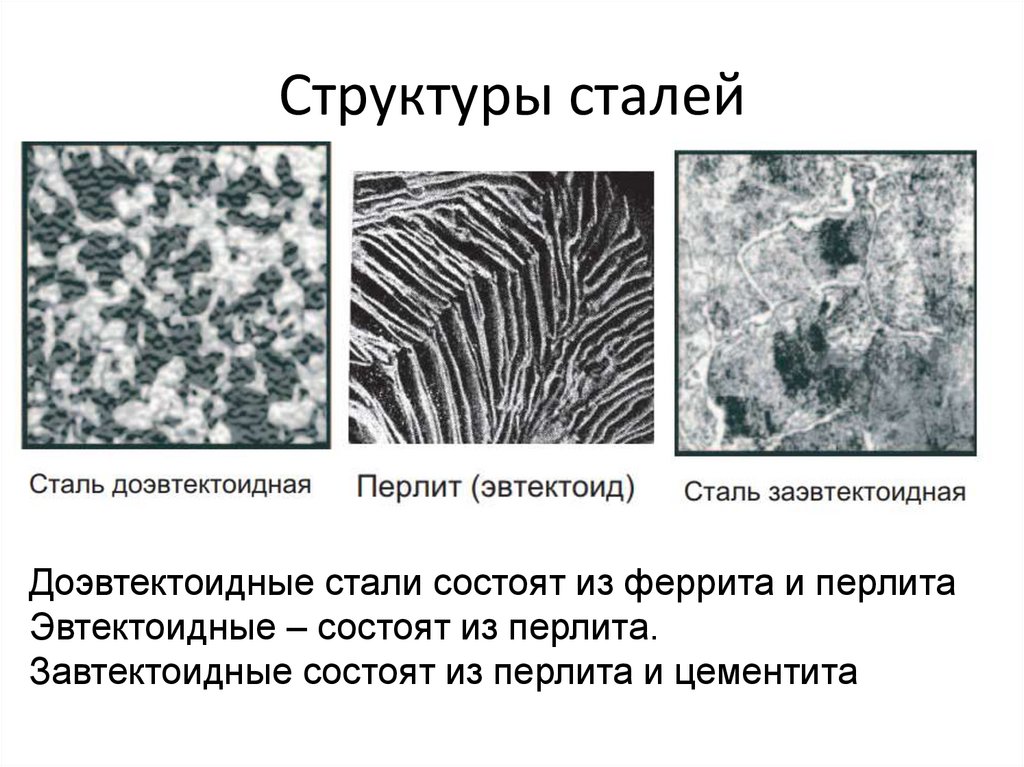
32. Структуры сталей
Доэвтектоидные стали состоят из феррита и перлитаЭвтектоидные – состоят из перлита.
Завтектоидные состоят из перлита и цементита
33.
34.
Цементит, феррит, аустенит – этооднофазные структуры.
• Линия АВСD – линия ликвидуса системы.
Феррит : высокотемпературный – левее
линии АHN; низкотемпературный - левее
линии GPQ.
Аустенит – область ограничена л.NJESG.
Цементит – вертикальная линия DFKL.
• Линия AHJECF – линия солидуса.
35.
В двухфазных областях диаграммы состоянияв равновесии находятся:
• жидкий раствор и кристаллы феррита (ABH)
• кристаллы феррита и аустенита (HIN и GSP);
• жидкий раствор и кристаллы аустенита
(JBCE);
• жидкий раствор и цементит (CDF);
• кристаллы аустенита и цементита (SECFK);
• кристаллы феррита и цементита (QPSKL).
36.
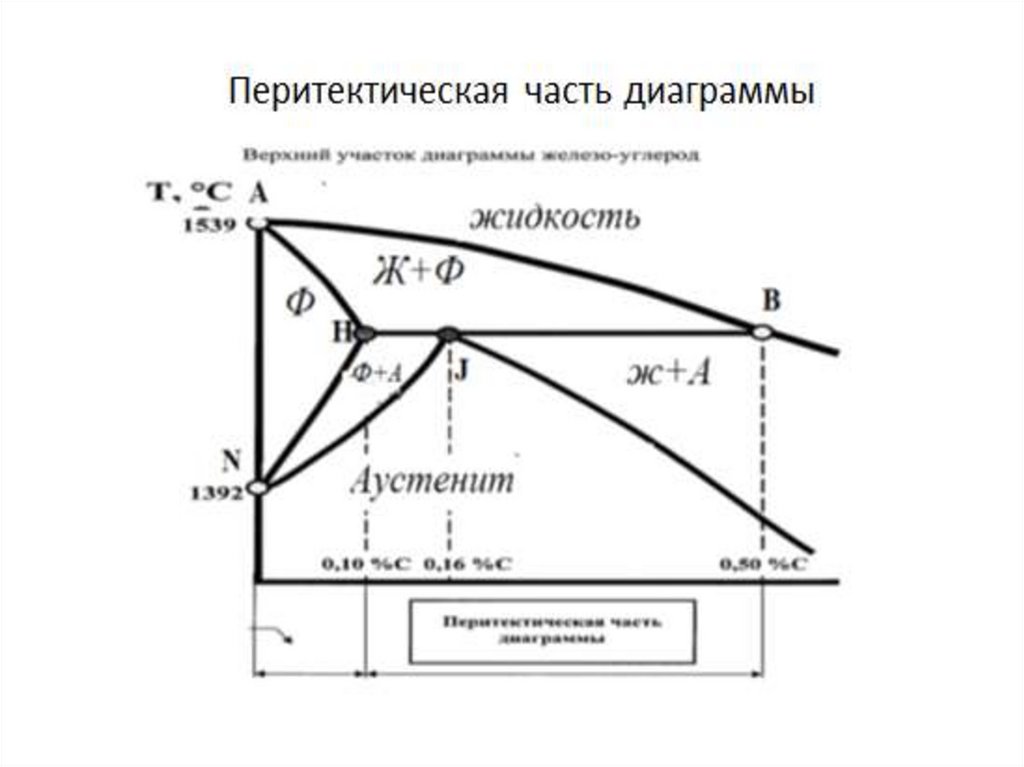
Трехфазным равновесным состояниям сплавовотвечают горизонтальные линии на ДС:
• при 1499 °С (л.HJB) в сплавах от 0,1 до 0,51 %С
происходит перитектическое превращение
ЖB + ФH → АJ
• при 1147 °С (л.ЕСF) в сплавах от 2,14 до 6,67 %С
происходит эвтектическое превращение
ЖB→АЕ + Ц - ледебурит
• при 727 °С (л.РSК) в сплавах с концентрацией углерода
более 0,02 %С происходит эвтектоидное превращение
(распад аустенита на механическую смесь)
АS→ ФР + Ц - перлит
37.
3.1.3 Новые методы производства и обработки стали.Электроннолучевая
плавка
металлов.
Для
получения особо чистых металлов и сплавов используют
электроннолучевую
плавку.
Плавка
основана
на
использовании
кинетической
энергии
свободных
электронов, получивших ускорение в электрическом поле
высокого напряжения. На металл направляется поток
электронов, в результате чего он нагревается и плавится.
Электроннолучевая плавка имеет ряд преимуществ:
электронные лучи позволяют получить высокую плотность
энергии нагрева, регулировать скорость плавки в больших
пределах, исключить загрязнение расплава материалом
тигля и применять шихту в любом виде. Перегрев
расплавленного металла в сочетании с малыми
скоростями плавки и глубоким вакуумом создают
эффективные условия для очистки металла от различных
примесей.
38.
Электрошлаковый переплав. Очень перспективнымспособом
получения
высококачественного
металла
является электрошлаковый переплав. Капли металла,
образующиеся при переплаве заготовки, проходят через
слой жидкого металла и рафинируются. При обработке
металла шлаком и направленной кристаллизации слитка
снизу вверх содержание серы в заготовке снижается на 30
– 50%, а содержание неметаллических включений – в дватри раза.
39.
Вакуумированиестали.
Для
получения
высококачественной
стали,
широко
применяется
вакуумная плавка. В слитке содержатся газы и некоторое
количество неметаллических включений. Их можно
значительно
уменьшить,
если
воспользоваться
вакуумированием стали при ее выплавке и разливке. При
этом способе жидкий металл подвергается выдержке в
закрытой камере, из которой удаляют воздух и другие газы.
Вакуумирование стали производится в ковше перед
заливкой по изложницам. Лучшие результаты получаются
тогда, когда сталь после вакуумирования в ковше
разливают по изложницам так же в вакууме. Выплавка
металла в вакууме осуществляется в закрытых
индукционных печах.
40.
Рафированиестали
в
ковше
жидкими
синтетическими шлаками. Сущность этого метода
состоит в том, что очистка стали от серы, кислорода и
неметаллических
включений
производится
при
интенсивном
перемешивании
стали
в
ковше
с
предварительно слитым в него шлаком, приготовленном в
специальной шлакоплавильной печи. Сталь после
обработки жидкими шлаками обладает высокими
механическими свойствами. За счет сокращения периода
рафинирования в дуговых печах, производительность
которых может быть увеличена на 10 – 15%. Мартеновская
печь, обработанная синтетическими шлаками, по качеству
близка к качеству стали, выплавляемой в электрических
печах.































 chemistry
chemistry








